非水电解质二次电池用正极活性物质以及非水电解质二次电池用正极的制作方法
本发明涉及非水电解质二次电池用正极活性物质以及非水电解质二次电池用正极。
背景技术:
面向锂离子电池的高能量密度化、高输出化,除了提高活性物质的容量的方案、增加每单位体积的活性物质的填充量的方案以外,还有提高电池的充电电压的方案。然而,在提高电池的充电电压的情况下,存在电解液易分解的问题,尤其在高温下保存或者在高温下反复进行充放电循环时,产生放电容量降低的问题。
考虑到这样的情况,提出了对正极活性物质表面进行改良的方案。例如,专利文献1中提出了表面涂布有AlF3、ZnF2等的锂二次电池用正极活性物质的方案。
另外,专利文献2中提出了将正极活性物质颗粒的表面用镧系元素氧化物覆盖以提高活性物质的化学稳定性的方案。
现有技术文献
专利文献
专利文献1:日本特表2008-536285号公报
专利文献2:日本特开2009-4316号公报
技术实现要素:
发明要解决的问题
然而,上述专利文献1、2中公开的技术中存在如下课题,在使用粒径小的正极活性物质的情况下,不能充分地提高电池的特性。
用于解决问题的方案
为了解决上述课题,本发明的非水电解质二次电池用正极活性物质的特征在于,其是具备含锂过渡金属氧化物的非水电解质二次电池用正极活性物质,前述含锂过渡金属氧化物的表面附着有选自锆、钛、铝、镁、以及稀土元素中的至少一种元素以及氟,前述含锂过渡金属氧化物包含钴,前述含锂过渡金属氧化物的平均粒径为10μm以下。
本发明的非水电解质二次电池用正极包含前述非水电解质二次电池用正极活性物质、导电剂、以及粘结剂。
发明的效果
本发明的非水电解质二次电池用正极活性物质以及正极即使在充电状态下被暴晒于高温下,也能够抑制自正极活性物质的钴的溶出。
附图说明
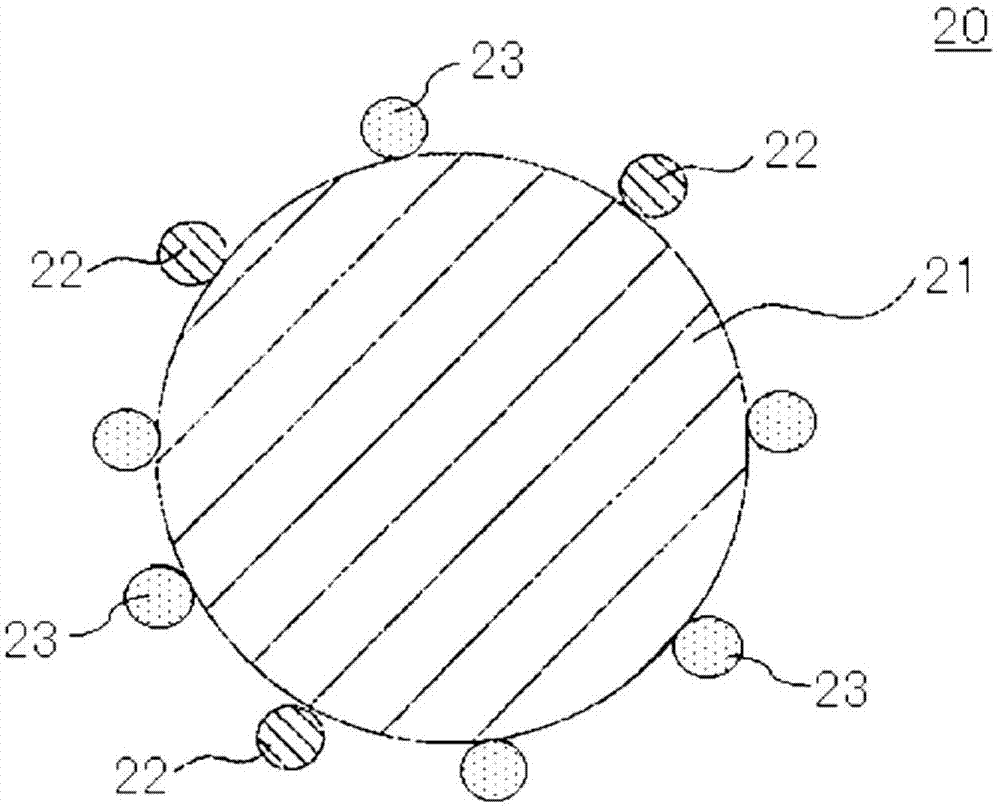
图1是示出作为本发明的实施方式的一个例子的钴酸锂的表面状态的说明图。
图2是示出实验1~8的结果的图表。
具体实施方式
下面,对本发明的实施方式的一个例子详细地说明。实施方式的说明中参照的附图是示意性地记载的,附图中描绘的构成要素的尺寸比率等有时与实物不同。具体的尺寸比率等应参照下面的说明来进行判断。
作为本发明的实施方式的一个例子的非水电解质二次电池具备包含正极活性物质的正极、包含负极活性物质的负极、包含非水溶剂的非水电解质、以及分隔件。作为非水电解质二次电池的一个例子,可以举出正极和负极隔着分隔件卷绕而成的电极体以及非水电解质容纳于外壳体的结构。
[正极]
正极优选由正极集电体以及形成于正极集电体上的正极活性物质层构成。作为正极集电体,例如可以使用具有导电性的薄膜体,尤其是铝等的在正极的电位范围内稳定的金属箔、合金箔,具有铝等的金属表层的薄膜。除了正极活性物质以外,正极活性物质层优选包含导电剂和粘结剂。
如图1所示的那样,正极活性物质20具备:含锂·钴过渡金属氧化物颗粒21;附着于含锂·钴过渡金属氧化物颗粒21的一部分表面的,包含选自锆、钛、铝、镁、以及稀土元素中的至少一种元素的材料22(以下,有时记载为材料22),以及含氟的材料23(以下,有时记载为材料23)。
含锂·钴过渡金属氧化物颗粒21的平均粒径优选为10μm以下,进一步优选为7μm以下。在平均粒径为10μm以下的含锂·钴过渡金属氧化物颗粒21的表面附着包含选自锆、钛、铝、镁、以及稀土元素中的至少一种元素的材料22以及含氟的材料23,从而能够大幅抑制充电状态下钴溶出到电解液中。
含锂·钴过渡金属氧化物颗粒21的平均粒径优选为2μm以上,进一步优选为4μm以上。平均粒径小于2μm时,含锂·钴过渡金属氧化物颗粒21的总表面积变大,存在上述附着物对于含锂·钴过渡金属氧化物颗粒21的总表面积进行覆盖的覆盖率降低的倾向。
含锂·钴过渡金属氧化物颗粒21的平均粒径表示:在用激光衍射散射法测得的粒度分布中,体积累计值达到50%的粒径(体积平均粒径;Dv50)。Dv50例如可以使用HORIBA制造的“LA-750”进行测定。
作为含锂·钴过渡金属氧化物,优选相对于含锂·钴过渡金属氧化物中的过渡金属总量包含80摩尔%以上的钴的物质。作为例子,可以举出钴酸锂、Ni-Co-Mn、Ni-Co-Al等含锂过渡金属氧化物。其中,优选钴酸锂。含锂·钴过渡金属氧化物可以固溶有Al、Mg、Ti、Zr等物质,或者也可以在晶界包含这些物质。
材料22优选为平均粒径100nm以下的颗粒。进一步优选为50nm以下的颗粒。平均粒径大于100nm时,即使使含锂·钴过渡金属氧化物颗粒21附着等量的材料22,也导致附着部位偏向局部,因此有时不能充分地发挥上述效果。材料22的平均粒径的下限优选为0.1nm以上,特别优选为1nm以上。平均粒径小于0.1nm时,导致材料22过量地覆盖正极活性物质表面。
材料22优选为选自氢氧化物、羟基氧化物、以及碳酸化合物中的至少一种,所述氢氧化物、羟基氧化物、以及碳酸化合物包含选自锆、钛、铝、镁、以及稀土元素中的至少一种元素。另外,材料22也可以含有氟。
材料22的附着量相对于含锂过渡金属氧化物的总质量以锆、钛、铝、镁、以及稀土元素换算计,优选为0.005质量%以上且0.5质量%以下,更优选为0.05质量%以上且0.3质量%以下。这是因为,小于0.05质量%时,不能充分地发挥钴溶出的抑制效果,大于0.5质量%时,有时表面的附着物过多从而电阻过度增加,放电性降低。
材料23的平均粒径优选为500nm以下。进一步优选为300nm以下。这是因为,过大时,存在被电子传导性低的氟化合物过度覆盖从而放电性能降低的风险。材料23的平均粒径的下限优选为50nm以上,特别优选为100nm以上。小于100nm时,有时不能充分地发挥包含氟元素的材料23以及材料22的金属元素带来的钴溶出的抑制效果。
材料23也可以仅由氟元素构成,优选为包含碱金属和氟的化合物,更优选为选自氟化锂、氟化钠、氟化钾中的至少一种。材料23也可以任意包含锆、钛、铝、镁、以及稀土元素。
材料23的平均粒径优选大于材料22的平均粒径。
材料23的附着量相对于含锂过渡金属氧化物的总质量以氟元素换算计,优选为0.005质量%以上且1.0质量%以下,尤其更优选为0.01质量%以上且0.5质量%以下。
附着于含锂·钴过渡金属氧化物颗粒21的材料22和材料23所包含的、选自锆、钛、铝、镁、以及稀土元素中的至少一种元素的总量与氟元素的总量以摩尔比计,优选为1:2~1:4。处于上述范围时,容易发挥材料22的金属元素与材料23的氟元素的相互作用,能够抑制来自晶格缺陷的钴溶出。
上述包含选自锆、钛、铝、镁、以及稀土元素中的至少一种元素的材料22以及含氟的材料23的大小是用扫描型电子显微镜(SEM)观察时的值。
作为上述稀土元素,可以使用选自钪、钇、镧、铈、镨、钕、钐、铕、钆、铽、镝、钬、铒、铥、镱、镥中的至少一种。尤其,优选使用钕、钐、铒、镧。
作为在含锂·钴过渡金属氧化物颗粒21的表面附着选自锆、钛、铝、镁、以及稀土元素中的至少一种元素以及氟的方法,例如可以通过如下的方法来得到:在正极活性物质上附着包含稀土元素、锆、镁、钛、铝的氢氧化物、羟基氧化物或碳酸化合物之后,用含氟的水溶液进行喷雾。作为含氟的水溶液的溶质,例如可以适宜地使用NH4F、NaF、KF等。
正极活性物质20可以单独地使用1种,也可以混合使用多种。正极活性物质20也可以与不含Co的正极活性物质一起混合使用。正极活性物质20相对于正极活性物质的总量的比率优选为20质量%以上且100质量%以下。认为,正极活性物质20的比率为20质量%以上时,可充分地体现向上述电解液中的钴溶出的抑制效果。
[负极]
负极优选具备负极集电体以及形成于负极集电体上的负极活性物质层。作为负极集电体,例如可以使用具有导电性的薄膜体,尤其是铜等的在负极的电位范围内稳定的金属箔、合金箔,具有铜等的金属表层的薄膜。除了负极活性物质以外,负极合剂层优选包含粘结剂。作为粘结剂,与正极的情况同样地可以使用聚四氟乙烯等,但优选使用丁苯橡胶(SBR)、聚酰亚胺等。粘结剂也可以与羧甲基纤维素等增稠剂组合使用。
作为负极活性物质,可以举出可吸藏释放锂的碳材料、或者可与锂形成合金的金属或包含该金属的合金化合物。作为碳材料,可以使用天然石墨、难石墨化性碳、人造石墨等石墨类;焦炭类等,作为合金化合物,可以举出包含至少1种可与锂形成合金的金属的合金化合物。尤其,作为可与锂形成合金的元素,优选为硅、锡,还可以使用它们与氧结合的氧化硅、氧化锡等。另外,还可以使用将上述碳材料与硅、锡的化合物混合了的混合物。除上述以外,虽然能量密度降低,但作为负极材料也可以使用钛酸锂等相对于金属锂的充放电的电位高于碳材料等的负极活性物质。
[非水电解质]
作为非水电解质的电解质盐,例如可以使用LiClO4、LiBF4、LiPF6、LiAlCl4、LiSbF6、LiSCN、LiCF3SO3、LiCF3CO2、LiAsF6、LiB10Cl10、低级脂肪族羧酸锂、LiCl、LiBr、LiI、氯硼烷锂、硼酸盐类、酰亚胺盐类等。其中,从离子传导性和电化学稳定性的观点出发,优选使用LiPF6。电解质盐可以单独使用1种,也可以组合使用2种以上。优选相对于非水电解质1L以0.8~1.5mol的比率包含这些电解质盐。
作为非水电解质的溶剂,例如可以使用环状碳酸酯、链状碳酸酯、环状羧酸酯等。作为环状碳酸酯,可以举出碳酸亚丙酯(PC)、碳酸亚乙酯(EC)、氟代碳酸亚乙酯(FEC)等。作为链状碳酸酯,可以举出碳酸二乙酯(DEC)、碳酸甲乙酯(EMC)、碳酸二甲酯(DMC)等。作为环状羧酸酯,可以举出γ-丁内酯(GBL)、γ-戊内酯(GVL)等。作为链状羧酸酯,可以举出丙酸甲酯(MP)、氟代丙酸甲酯(FMP)。非水溶剂可以单独使用1种,也可以组合使用2种以上。
[分隔件]
作为分隔件,可以使用具有离子透过性和绝缘性的多孔片材。作为多孔片材的具体例子,可以举出微多孔膜、织布、无纺布等。作为分隔件的材质,优选聚乙烯、聚丙烯等聚烯烃。
<实施例>
(实验1)
[正极的作成]
准备相对于钴酸锂(平均粒径:7μm)固溶有各1.5摩尔%的Mg和Al的钴酸锂颗粒500g。将该钴酸锂颗粒投入到1.5升的纯水中,一边将其搅拌一边添加100ml的纯水中溶解有1.13g的硝酸铒五水合物(Er(NO3)3·5H2O)的水溶液。此时,以该溶液的pH为9的方式(以pH维持9的方式)适宜地加入10质量%的氢氧化钠水溶液,使钴酸锂颗粒的表面附着氢氧化铒。然后,将其吸引过滤而滤取处理物,将该处理物在120℃下进行干燥,得到氢氧化铒分散且附着于表面的钴酸锂颗粒。
接着,一边搅拌得到的正极活性物质,一边用25g的纯水中溶解有0.28g的氟化铵(NH4F)的水溶液进行喷雾。其后,在400℃下、在空气中进行6小时的热处理。
用扫描型电子显微镜(SEM)对得到的正极活性物质进行观察,结果确认了在钴酸锂的一部分表面附着有含铒的颗粒以及含氟的化合物(氟化锂)。含铒的颗粒的平均粒径为100nm以下。含氟的化合物的大小为200nm以下。利用ICP测定铒的附着量,结果相对于钴酸锂为0.085质量%。通过离子色谱法测定氟的量,结果相对于钴酸锂为0.029质量%,铒与F的摩尔比为1:3。
将得到的正极活性物质、乙炔黑粉末、以及聚偏氟乙烯以质量比计为95:2.5:2.5的比率的方式在N-甲基-2-吡咯烷酮(NMP)溶液中进行混炼,制备正极合剂浆料。接着,将该正极合剂浆料均匀地涂布于由铝箔制成的正极集电体的两面,干燥之后,利用压延辊进行压延,由此制作正极集电体的两面形成有正极合剂层的正极。需要说明的是,该正极的活性物质的填充密度为3.2g/cm3。
[负极的制作]
将负极活性物质的人造石墨、羧甲基纤维素钠、以及丁苯橡胶以98:1:1的质量比在水溶液中进行混合,制备负极合剂浆料。接着,将该负极合剂浆料均匀地涂布于由铜箔制成的负极集电体的两面,进行干燥,利用压延辊进行压延,由此得到负极集电体的两面形成有负极合剂层的负极。需要说明的是,该负极的活性物质的填充密度为1.65g/cm3。
[非水电解质的制备]
相对于以3:5:2的体积比混合了碳酸亚乙酯(EC)、碳酸甲乙酯(MEC)、以及碳酸二乙酯(DEC)的混合溶剂,将六氟磷酸锂(LiPF6)以成为1.0摩尔/升的浓度的方式进行溶解,制备非水电解质(非水电解液)。
[电池的制作]
在上述正负极上分别安装引线端子,在这些两极间配置分隔件,卷绕成螺旋状之后,拔出卷芯,从而制作螺旋状的电极体,进而将该电极体压扁,得到扁平型的电极体。接着,将该扁平型的电极体和上述非水电解液插入铝层压材料制的外壳体内,密封而制作电池A1。电池A1的设计容量(充电至4.40V,放电至2.75V时的放电容量)为750mAh。
(实验2)
作为正极活性物质,使用钴酸锂(平均粒径:10μm),除此以外,与上述实验1同样地制作电池A2。
(实验3)
作为正极活性物质,使用钴酸锂(平均粒径:16μm),除此以外,与上述实验1同样地制作电池B1。
(实验4)
作为正极活性物质,使用钴酸锂(平均粒径:23μm),除此以外,与上述实验1同样地制作电池B2。
(实验5)
作为正极活性物质,使用钴酸锂(平均粒径:28μm),除此以外,与上述实验1同样地制作电池B3。
(实验6)
作为正极活性物质,使用表面分散且附着有氢氧化铒的钴酸锂颗粒(即,表面虽然分散且附着有氢氧化铒但未附着氟的钴酸锂颗粒),除此以外,与上述实验1同样地制作电池C1。
(实验7)
作为正极活性物质,使用钴酸锂(平均粒径:10μm),除此以外,与上述实验6同样地制作电池C2。
(实验8)
作为正极活性物质,使用钴酸锂(平均粒径:16μm),除此以外,与上述实验6同样地制作电池D1。
(实验9)
作为正极活性物质,使用钴酸锂(平均粒径:23μm),除此以外,与上述实验6同样地制作电池D2。
(实验10)
作为正极活性物质,使用钴酸锂(平均粒径:28μm),除此以外,与上述实验6同样地制作电池D3。
(实验例11)
替代硝酸铒五水合物,使用硝酸钐六水合物(Sm(NO3)3·6H2O)1.14g,除此以外,与上述实验2同样地制作电池E1。钐、氟的附着量分别为0.085质量%、0.029质量%,钐与氟的摩尔比为1:3。
(实验例12)
替代硝酸铒五水合物,使用硝酸钕六水合物(Nd(NO3)3·6H2O)1.12g,除此以外,与上述实验2同样地制作电池F1。钕、氟的附着量分别为0.074质量%、0.029质量%,钕与氟的摩尔比为1:3。
(实验例13)
替代硝酸铒五水合物,使用硝酸镧六水合物(La(NO3)3·6H2O)1.11g,除此以外,与上述实验2同样地制作电池G1。镧、氟的附着量分别为0.071质量%、0.029质量%,镧与氟的摩尔比为1:3。
(实验例14)
替代硝酸铒五水合物,使用硝酸锆五水合物(Zr(NO3)4·5H2O)1.10g,除此以外,与上述实验2同样地制作电池H1。锆、氟的附着量分别为0.046质量%、0.039质量%,锆与氟的摩尔比为1:3。
(实验例15)
替代硝酸铒五水合物,使用硝酸镁六水合物(Mg(NO3)2·6H2O)0.65g,除此以外,与上述实验2同样地制作电池I1。镁、氟的附着量分别为0.012质量%、0.019质量%,镁与氟的摩尔比为1:3。
(实验例16)
替代硝酸铒五水合物,使用硝酸铝九水合物(Al(NO3)3·9H2O)0.96g,除此以外,与上述实验2同样地制作电池J1。铝、氟的附着量分别为0.014质量%、0.029质量%,铝与氟的摩尔比为1:3。
(实验例17)
作为正极活性物质,使用表面分散且附着有氢氧化钐的钴酸锂颗粒(即,表面虽然分散且附着有氢氧化钐但未附着氟的钴酸锂颗粒),除此以外,与上述实验11同样地制作电池K1。
(实验例18)
作为正极活性物质,使用表面分散且附着有氢氧化钕的钴酸锂颗粒(即,表面虽然分散且附着有氢氧化钕但未附着氟的钴酸锂颗粒),除此以外,与上述实验12同样地制作电池L1。
(实验例19)
作为正极活性物质,使用表面分散且附着有氢氧化镧的钴酸锂颗粒(即,表面虽然分散且附着有氢氧化镧但未附着氟的钴酸锂颗粒),除此以外,与上述实验13同样地制作电池M1。
(实验例20)
作为正极活性物质,使用表面分散且附着有氢氧化锆的钴酸锂颗粒(即,表面虽然分散且附着有氢氧化锆但未附着氟的钴酸锂颗粒),除此以外,与上述实验14同样地制作电池N1。
(实验例21)
作为正极活性物质,使用表面分散且附着有氢氧化镁的钴酸锂颗粒(即,表面虽然分散且附着有氢氧化镁但未附着氟的钴酸锂颗粒),除此以外,与上述实验15同样地制作电池O1。
(实验例22)
作为正极活性物质,使用表面分散且附着有氢氧化铝的钴酸锂颗粒(即,表面虽然分散且附着有氢氧化铝但未附着氟的钴酸锂颗粒),除此以外,与上述实验16同样地制作电池P1。
[实验1]
关于上述各电池,调查在下述条件下、60℃下连续充电65小时后的钴的溶出量抑制率,将各电池的结果示于表1。另外,将电池A1~A2、B1~B3、C1~C2、以及D1~D3的结果示于图2。
[充电条件]
在60℃的环境下,以1.0It(750mA)的电流进行恒流充电至电池电压成为4.40V,进而以4.40V的电压进行恒压充电。充电将恒流充电和恒压充电总共进行65小时。
[钴溶出量的测定]
将充电后的上述各电池拆开,从取出的负极板切出纵2cm、横2cm的负极片。将负极片拿进株式会社岛津制作所制造的EDX-7000,进行荧光X射线分析,并进行钴元素的定量。
另外,将平均粒径为7μm、10μm、16μm、23μm、以及28μm的钴酸锂(未附着稀土元素、氟的钴酸锂)分别用作正极活性物质,除此以外,与上述实验1同样地制作电池R1、R2、R3、R4、以及R5,与上述同样地在60℃下连续充电65小时后,取出负极片,进行钴元素的定量。
[钴溶出抑制率的计算]
基于以下式(1),算出电池A1~A2、B1~B3、C1~C2、D1~D3、以及E1~P1的钴溶出抑制率。式(1)中,将各电池中定量的钴元素量设为S,将电池R1~R5中与各电池的钴酸锂的平均粒径相同的电池中定量的钴元素量设为T。例如,对于电池A1的情况,将电池A1中定量的钴元素量设为S,将电池R1中定量的钴元素量设为T,从而算出电池A1的钴溶出抑制率。
钴溶出抑制率(%)=100-(S/T)×100…(1)
表1
对于使用平均粒径为10μm以下的钴酸锂的情况,对钴酸锂上附着有铒和氟的电池A1~A2以及钴酸锂上仅附着有铒的B1~B2进行比较时,可知,电池A1~A2中,尤其大幅地抑制了钴的溶出。认为这是基于以下所示的理由。
认为,钴酸锂在充电状态下发生钴的溶出,尤其钴酸锂的平均粒径变成10μm以下时,有颗粒表面存在原子空位、晶界等晶格缺陷的概率变高的倾向,以这些晶格缺陷为起点,钴容易溶出。此处认为,使铒和氟附着于平均粒径为10μm以下的钴酸锂,从而抑制了钴的溶出。
认为对于仅将铒附着于平均粒径为10μm以下的钴酸锂的情况,不能充分地抑制平均粒径为10μm以下的钴酸锂的钴的溶出。
对于使用平均粒径大于10μm的钴酸锂的情况,对钴酸锂上附着有铒和氟的电池B1~B3以及钴酸锂上仅附着有铒的D1~D3进行比较时,没有发现在钴溶出抑制率上存在大的差异。认为这是基于以下所示的理由。
认为,钴酸锂在充电状态下发生钴的溶出,而钴酸锂的平均粒径大于10μm时,与平均粒径为10μm以下的情况进行比较,钴的溶出量没有那么多。因此认为,在使铒和氟附着于钴酸锂的情况下以及在仅使铒附着于钴酸锂的情况下,抑制钴的溶出的效果没有改变。
上述中,举出附着有铒和氟的钴酸锂作为例子进行了说明,但在使用附着有选自锆、钛、铝、镁、以及钐、钕、镧等稀土元素中的至少1种元素和氟的钴酸锂的情况下,出于与上述同样的理由,认为能够抑制钴的溶出。
认为,上述实施例中,正极活性物质使用了钴酸锂,但使用含钴的含锂过渡金属氧化物也能够抑制钴的溶出。
附图标记说明
20:正极活性物质
21:含锂·钴过渡金属氧化物颗粒
22:包含选自锆、钛、铝、镁、以及稀土元素中的至少一种元素的材料
23:含氟的材料
- 还没有人留言评论。精彩留言会获得点赞!