金属掺杂的高电压用正极活性材料的制作方法
相关申请的交叉引用
本申请基于并要求分别于2016年12月21日和2017年12月18日提交的韩国专利申请第10-2016-0175204号和第10-2017-0174513号的优先权,通过援引将其公开内容完整并入本文。
本发明涉及一种金属掺杂的高电压用正极活性材料及其制备方法。
背景技术:
随着技术发展和对移动设备需求的增加,对作为能源的二次电池的需求已迅速增加,并且在这些二次电池中,具有高能量密度和工作电位、长寿命和低自放电率的锂二次电池已经得到商业化和广泛使用。
此外,随着对环境问题的日益关注,已经对电动车辆和混合动力电动车辆进行了许多研究,其可以用于代替作为空气污染的主要原因之一的使用化石燃料的车辆(例如,汽油车辆、柴油车辆等)。尽管镍氢金属二次电池已主要用作电动车辆和混合动力电动车辆的动力源,但是已经积极研究了具有高能量密度和放电电压的锂二次电池的应用,并且其中的一些现已可商购获得。
作为锂二次电池的正极材料,使用了licoo2、三元材料(nmc/nca)、limno4、lifepo4等。licoo2由于具有优异的物理性能(例如高压延密度等)和优异的电化学特性(例如高循环特性)而至今为止被频繁使用。然而,由于licoo2具有低至约150mah/g的充电/放电电流容量,并且其结构在4.3v以上的高电压下不稳定,因此其具有寿命特性迅速降低的问题和与电解质的反应引起着火的问题。
特别是,当为了开发高容量二次电池而向licoo2施加高电压时,licoo2的li使用增加,这可能增加表面不稳定和结构不稳定的可能性。为了解决这些问题,已通过用其他元素取代部分钴来代替licoo2,或者通过形成单独的涂层来开发正极材料。
然而,在具有上述取代或涂层的正极材料中也难以提高licoo2的结构稳定性。特别是,在大于4.5v的高电压下,难以保持结构稳定性。实际上,难以将licoo2应用于高容量二次电池。
此外,对于在licoo2表面上形成有涂层的正极材料,涂层在充电/放电循环期间妨碍li离子的移动或降低licoo2的容量,因此,存在二次电池的性能可能劣化的问题。
因此,对在大于4.5v的高电压下能够确保结构稳定性且性能不劣化的锂钴氧化物类正极活性材料的需求不断增加。
技术实现要素:
[技术问题]
因此,本发明提供一种在大于4.5v的高电压下能够确保结构稳定性且性能不劣化的正极活性材料及其制备方法。
此外,本发明提供一种包含所述正极活性材料的正极,和一种锂二次电池,其包括所述正极以在大于4.5v的高电压下表现出优异的性能和寿命特性。
[技术方案]
因此,本发明提供一种正极活性材料,其包含由下式1表示的层状结构的锂钴氧化物;和
金属元素(m),相对于100重量份的所述锂钴氧化物,所述金属元素(m)以0.2重量份至1重量份的量掺杂到所述锂钴氧化物中,其中,所述正极活性材料在满充电时的高于4.5v的正极电位(基于li电位)下保持晶体结构:
[式1]
li1+xco1-xo2
其中,x满足0≤x≤0.2;和
m是选自由al、ti、mg、mn、zr、ba、ca、ta、mo、nb和氧化数为+2或+3的金属组成的组的一种以上。
此外,本发明提供一种锂二次电池,其包括:含有所述正极活性材料的正极;负极;和电解质。
此外,本发明提供一种所述正极活性材料的制备方法,所述方法包括将钴酸盐、锂前体和掺杂前体干混的工序;和在900℃以上的温度下烧结所述混合物的工序。
以下,将描述本发明具体实施方式的正极活性材料及其制备方法。
根据本发明的一个实施方式,提供了一种正极活性材料,其包含由下式1表示的层状结构的锂钴氧化物;和
金属元素(m),相对于100重量份的所述锂钴氧化物,所述金属元素(m)以0.2重量份至1重量份的量掺杂到所述锂钴氧化物中,其中,所述正极活性材料在满充电时的高于4.5v的正极电位(基于li电位)下保持晶体结构:
[式1]
li1+xco1-xo2
其中,x满足0≤x≤0.2;和
m是选自由al、ti、mg、mn、zr、ba、ca、ta、mo、nb和氧化数为+2或+3的金属组成的组的一种以上。
本发明的发明人已进行了持续的深入研究,如以下更详细描述的,发现当具有层状结构的式1的锂钴氧化物掺杂有预定量以上的一种以上的金属元素时,在大于4.5v的高电压下晶体结构的结构稳定性可以提高,以保持稳定的晶体结构,从而实现高电压特性,由此完成了本发明。
如本文所用,将金属元素“掺杂”到锂钴氧化物中意味着该金属元素不与锂钴氧化物及其元素形成化学键,而是至少部分金属元素m掺入锂钴氧化物的晶格结构中,从而具有物理/晶体学连接。在这方面,掺入锂钴氧化物的晶格结构中的至少部分金属元素m可以例如掺入锂钴氧化物的晶格结构的空隙空间中以具有物理/晶体学连接而不与锂钴氧化物形成化学键。这样,由于金属元素m具有物理/晶体学连接而不与锂钴氧化物形成化学键,金属元素m可以主要分布在靠近锂钴氧化物表面的区域中。
因此,“掺杂”可以清楚地区别于金属元素m与锂钴氧化物形成化学键的状态,例如,区别于锂钴氧化物中的部分钴被金属元素m取代、然后该金属元素m化学键合到氧化物的复合状态。在复合状态下,金属元素m可以通过化学键或复合体的形成均匀地分布在锂钴氧化物的整个区域。
这样,一个实施方式的正极活性材料具有基于掺杂有一种以上金属元素的式1的锂钴氧化物的结构,因此,将预定量以上的掺杂剂掺入且置于锂钴氧化物的晶格中,从而提高晶体结构和颗粒表面的稳定性。
特别地,一个实施方式的正极活性材料可以包括预定量以上的掺杂剂,例如0.2重量份以上,或0.2重量份至1.0重量份,或0.3重量份至0.9重量份,从而即使在4.3v以上或大于4.5v的高电压下也能稳定锂钴氧化物的晶体结构。因此,确认了该正极活性材料可以优选用作在高电压下表现出优异的容量和寿命特性的活性材料。
相反,当掺杂剂的掺杂量小于0.2重量份时,直到4.45v,正极活性材料在容量和结构稳定性方面都优异。然而,在高于4.5v的电压下,存在结构发生坍塌或寿命迅速劣化的问题。此外,当掺杂剂的掺杂量为大于1.0重量份的过大量时,或者当金属元素通过化学键与锂钴氧化物形成复合体(例如,将部分钴换成金属元素m的复合体)而不是掺杂时,或者当形成包含金属元素的涂层时,在高电压下活性材料的结构稳定性可能劣化,替换的元素或涂层可能在充电/放电循环期间妨碍li离子的移动,或者基于式1的活性材料的容量特性可能由于钴含量的相对减少而劣化。
同时,如图6所示,可以通过例如由tof-sims(飞行时间二次离子质谱)分析上述活性材料的结果来确认通过掺杂将至少部分金属元素m掺入了锂钴氧化物的晶格中。确认了金属元素m主要分布在靠近锂钴氧化物表面的区域中,表明至少部分金属元素m掺杂到了锂钴氧化物中,而未通过化学键与锂钴氧化物形成复合体。
另外,在一个具体实施方式中,正极活性材料可以在大于4.5v且4.8v以下的充电范围内保持晶体结构,具体地,正极活性材料可以在大于4.5v且4.6v以下的充电范围内保持晶体结构的稳定性,更具体地,正极活性材料可以在大于4.5v且4.55v以下的充电范围内确保晶体结构的稳定性。
上述掺杂剂金属元素m可以选自由al、ti、mg、mn、zr、ba、ca、ta、mo、nb和氧化数为+2或+3的金属组成的金属元素组,且没有特别限制。然而,考虑到降低与电解质的表面副反应或在高电压下的相稳定性,金属元素m可以是al或mg。在某些情况下,全部al和mg都可以用作掺杂剂。
同时,在另一具体实施方式中,一个实施方式的正极活性材料在高电压下充电时可以保持晶体结构稳定性,并且这种稳定性可以通过xrd分析来确认。例如,在正极活性材料的xrd分析结果的2θ标度上,4.55v下的(003)面的峰强度可以是4.50v下的(003)面的峰强度的30%以上。更具体地,在xrd图的2θ标度上,4.55v下的(003)面的峰强度可以是4.50v下的(003)面的峰强度的40%以上,或者40%至90%。
换句话说,可以通过测量(003)面(表示锂钴氧化物中锂离子入口的晶面)的峰强度来确认锂钴氧化物是否保持晶体结构。当充电至4.55v时,先前的锂钴氧化物表现出晶体结构的坍塌,因此与4.5v的峰强度相比,测量到显著低的峰强度。因此,可以看出,当锂钴氧化物没有金属掺杂或少量掺杂时,在大于4.5v的电压下可能发生晶体结构的坍塌。
然而,由于一个实施方式的正极活性材料包括特定含量和种类的掺杂剂,因此4.55v下的(003)面的峰强度可以是4.5v下的(003)面的峰强度的30%以上,表明在高电压下结构稳定性的改善。
在又一个实施方式中,在满充电时在4.5v的正极电位(基于li电位)下,金属元素(m)的掺杂含量(b)为0.3重量份的正极活性材料可以表现出比金属元素(m)的掺杂含量为0.1重量份的正极活性材料低的容量保持率。
这样,即使金属元素的掺杂含量相对较高,但在满充电时在4.5v的电位下,由于高含量的掺杂剂,容量保持率可能降低。因此,为了实现高容量保持率,一个实施方式的正极活性材料需要具有高含量的掺杂金属以及至少高于4.5v的充电电压。
例如,当掺杂的金属元素是mg时,mg含量为0.3重量份的正极活性材料在30个循环以上的充电/放电循环后可以表现出比mg掺杂含量为0.1重量份的正极活性材料低的容量保持率。
即,当锂钴正极活性材料掺杂有mg并且mg的含量为0.3重量份时,正极活性材料在小于30个循环的充电/放电循环后表现出比mg含量为0.1重量份的正极活性材料更高的容量保持率,但是在充电/放电循环大于30次循环后,其表现出比mg含量为0.1重量份的正极活性材料更低的容量保持率。
因此,在充电电压为4.5v下,即使使用大量的掺杂剂,但随着充电/放电循环次数的增加,容量保持率可能降低并且寿命特性可能劣化。
相反,在满充电时的4.55v的正极电位(基于li电位)下,金属元素(m)的掺杂含量(b)为0.3重量份的正极活性材料可以表现出比金属元素(m)的掺杂含量为0.1重量份的正极活性材料高的容量保持率。
这样,为了实现在大于4.5v的高充电电压下的高容量保持率,一个实施方式的正极活性材料需要包含预定量以上的掺杂剂。与充电电压为4.5v的情况不同,尽管掺杂金属是mg,但是掺杂含量为0.3重量份的正极活性材料在30个以上的充电/放电循环后可以表现出比掺杂含量为0.1重量份的正极活性材料高的容量保持率。
此外,在充电电压为4.55v下,掺杂金属含量为0.3重量份的正极活性材料与掺杂金属含量为0.1重量份的正极活性材料之间的容量保持率差异随着充电/放电循环次数的增加而逐渐增加。
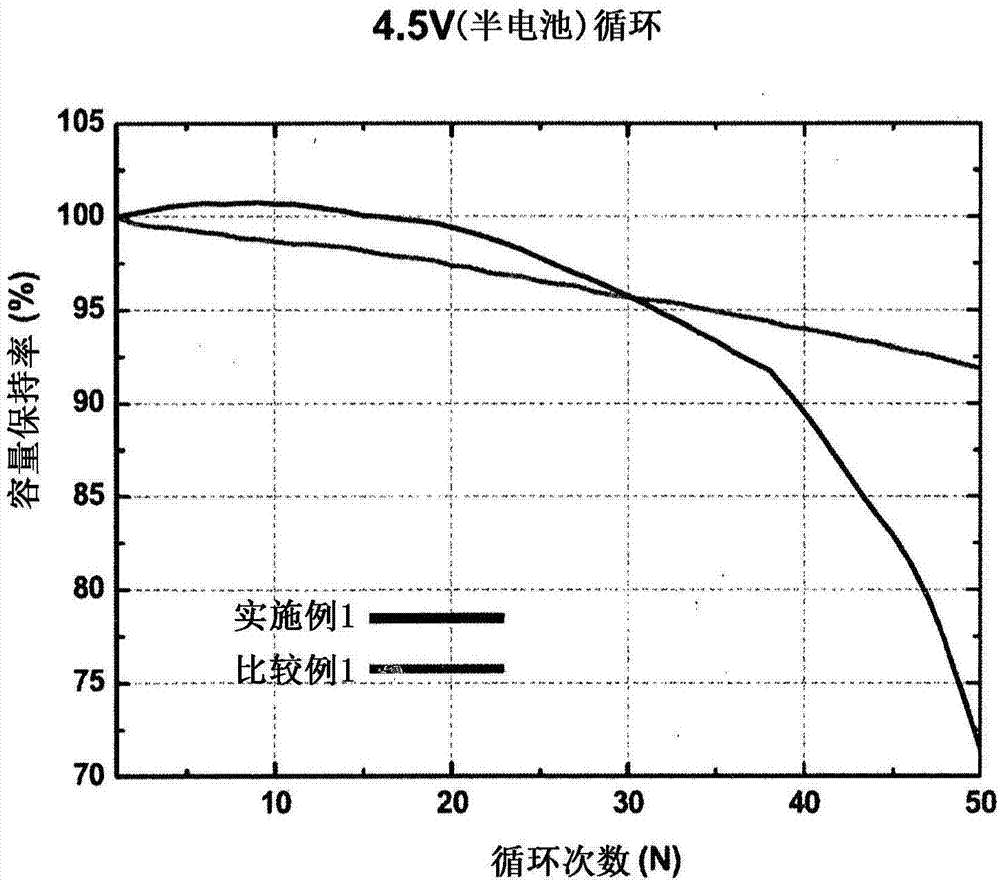
例如,当使用掺杂金属含量为0.3重量份的正极活性材料时,在满充电时的4.55v的正极电位(基于li电位)下,其在50个循环的充电/放电循环后的容量保持率可以是初始容量的85%以上,与在相同循环后通常表现出小于75%的容量保持率的掺杂金属含量为0.1重量份的正极活性材料相比,显示出高的寿命特性。
在一个具体实施方式中,上述一个实施方式的正极活性材料可以进一步包含在锂钴氧化物颗粒上形成的涂层,并且该涂层可以包含选自由al2o3、mgo、zro、li2zro3和tio2组成的组的一种以上金属氧化物。该涂层的形成可以进一步提高锂钴氧化物颗粒的结构稳定性。
通常,当在高电压下使用锂钴氧化物作为正极活性材料时,从锂钴氧化物颗粒释放出大量的锂离子,并且表面上的li离子浓度变低,从而容易释放co。随着co的释放增加,可逆容量降低,并且co在负极表面上析出的可能性增加,这可能增加负极电阻。因此,当在锂钴氧化物颗粒上进一步形成金属氧化物涂层时,涂层中包含的金属元素可以优先于钴与hf反应,以保护正极活性材料颗粒。结果,可以有效地防止高电压下二次电池的循环特性劣化。
基于式1的锂钴氧化物的含量,涂层中包含的金属元素的含量可以控制在300ppmw至1,200ppmw。当涂层中包含的金属元素的含量小于300ppmw时,难以确保正极活性材料的结构稳定性。当该含量大于1,200ppmw时,电池的容量和输出特性不理想地劣化。
同时,根据本发明的另一实施方式,提供了一种制备上述一个实施方式的正极活性材料的方法。该制备方法可以包括将钴酸盐、锂前体和掺杂前体干混的工序;以及在900℃以上的温度下烧结所述混合物的工序。
本发明的发明人的实验结果表明,掺杂有至少部分金属元素m的一个实施方式的活性材料可以通过将前体彼此干混合并在高温下烧结该混合物来制备。与该方法不同,当采用诸如共沉淀等其他湿法时,活性材料通过金属元素m与式1之间的化学键以复合体形式获得,因此很可能无法制备一个实施方式的正极活性材料。
在上述另一实施方式的制备方法中,烧结温度可以是例如900℃至1,200℃,具体地,1,000℃至1,100℃,并且烧结时间可以是4小时至20小时,具体地,5小时至15小时。
当烧结温度低于900℃时,可能无法适当地形成锂钴氧化物的结构,而当烧结温度高于1200℃时,锂钴氧化物过度烧结,从而导致容量或寿命特性劣化,这是不希望的。此外,当烧结时间短于4小时时,可能会发生掺杂不充分的问题,当烧结时间为12小时以上时,锂钴氧化物的物理和化学性质可能改变,从而导致性能劣化,这是不希望的。
在烧结工序之后,该方法可以进一步包括在掺杂有金属元素m的锂钴氧化物的表面上形成涂层的工序。如上所述,该涂层可以包括选自由al2o3、mgo、zro、li2zro3和tio2组成的组的一种以上金属氧化物。
在一个实施方式中,为了形成涂层,可以将包含计划包含在涂层中的金属元素的盐与经掺杂的锂钴氧化物混合,然后可以烧结该混合物。即,其上形成有涂层的正极活性材料可以通过将包含金属元素的盐涂布到经掺杂的锂钴氧化物的颗粒表面上然后进行烧结来制备。
同时,在上述另一实施方式的制备方法中使用的钴氧化物的种类不受特别限制,但钴酸盐可以是例如选自由co3o4、coco3、co(no3)2和co(oh)2组成的组的一种以上,特别是co3o4或co(oh)2。
锂前体可以是选自由li2co3、lioh、lino3、ch3cooli和li2(coo)2组成的组的一种以上,特别是lioh或li2co3。
掺杂前体可以是选自以下组的一种以上:选自由al、ti、mg、mn、zr、ba、ca、ta、mo、nb和氧化数为+2或+3的金属组成的组的一种以上金属,其金属氧化物,及其金属盐;特别是al和/或mg。
同时,根据本发明的又一个实施方式,提供了一种包含上述一个实施方式的正极活性材料的二次电池用正极。
正极可以通过例如将包含由正极活性材料颗粒组成的正极活性材料、导电材料和粘合剂的正极合剂涂布到正极集电体上来制造,并且根据需要,填料可以进一步加入到正极合剂中。
通常将正极集电体制造为具有3μm至500μm的厚度。正极集电体没有特别限制,只要其具有高导电性而不引起相应电池的化学变化即可。正极集电体可以是例如选自不锈钢、铝、镍、钛和表面用碳、镍、钛或银处理过的铝或不锈钢的任何一种。特别地,可以使用铝。集电体可以通过在表面上形成微细的粗糙来增加正极活性材料的粘附。例如,集电体可以是各种形式,例如膜、片、箔、网、多孔材料、泡沫材料、无纺布材料等。
正极活性材料可以由正极活性材料颗粒和以下组分组成:层状结构化合物(例如锂镍氧化物(linio2)),或取代有一种以上金属的化合物;锂锰氧化物,例如式li1+xmn2-xo4(其中,x为0至0.33)、limno3、limn2o3、limno2等;锂铜氧化物(li2cuo2);钒氧化物,例如liv3o8、liv3o4、v2o5、cu2v2o7等;由式lini1-xmxo2(其中,m是co、mn、al、cu、fe、mg、b或ga,并且x是0.01至0.3)表示的ni位型锂镍氧化物;由式limn2-xmxo2(其中,m是co、ni、fe、cr、zn或ta,并且x是0.01至1)或li2mn3mo8(其中,m是fe、co、ni、cu或zn)表示的锂锰复合氧化物;limn2o4,其中式中的一些li被碱土金属取代;二硫化物;fe2(moo4)3等,但不限于此。
基于包含正极活性材料的合剂的总重量,导电材料的添加量通常为0.1重量%至30重量%。导电材料没有特别限制,只要其具有导电性而不引起相应电池的化学变化即可。导电材料的实例可以包括:石墨,例如天然或人造石墨;炭黑,例如炭黑、乙炔黑、科琴黑、槽黑、炉黑、灯黑、热裂法炭黑等;导电纤维,例如碳纤维、金属纤维等;金属粉末,例如氟化碳、铝、镍粉等;导电晶须,例如氧化锌、钛酸钾等;导电金属氧化物,例如氧化钛等;聚亚苯基衍生物等。
正极中包含的粘合剂是有助于活性材料和导电剂之间的粘合以及对集电体的粘合的组分,并且基于包含正极活性材料的合剂的总重量,粘合剂的添加量通常可以为0.1重量%至30重量%。粘合剂的实例可以包括聚偏二氟乙烯、聚乙烯醇、羧甲基纤维素(cmc)、淀粉、羟丙基纤维素、再生纤维素、聚乙烯吡咯烷酮、四氟乙烯、聚乙烯、聚丙烯、乙烯-丙烯-二烯三元共聚物(epdm)、磺化epdm、苯乙烯-丁二烯橡胶、氟橡胶、各种共聚物等。
根据又一实施方式,提供了一种包含上述正极、负极和电解质的锂二次电池。锂二次电池的种类没有特别限制,但锂二次电池可以包括例如具有高能量密度、放电电压、输出稳定性等优点的锂离子电池或锂离子聚合物电池。
通常,锂二次电池由正极、负极、隔膜和含有锂盐的非水性电解质组成。
以下,将描述锂二次电池的其他组分。
负极可以通过将负极活性材料涂布到负极集电体上然后进行干燥来制造。根据需要,可选地可以进一步包括上述组分。
通常将负极集电体制成具有3μm至500μm的厚度。负极集电体没有特别限制,只要其具有导电性而不引起相应电池的化学变化即可。例如,可以使用铜、不锈钢、铝、镍、钛、煅烧碳或表面用碳、镍、钛、银等处理过的铜或不锈钢以及铝镉合金等。与正极集电体相同,负极集电体可以在其表面上具有微细的粗糙以增强负极活性材料的粘附,并且可以以各种形式使用,例如膜、片、箔、网、多孔材料、泡沫材料、无纺布材料等。
负极活性材料可以包括例如:碳,例如非石墨化碳、石墨化碳等;金属复合氧化物,例如lixfe2o3(0≤x≤1)、lixwo2(0≤x≤1)、snxme1-xme’yoz(me:mn、fe、pb、ge;me’:al、b、p、si、元素周期表i、ii或iii族元素、卤素;0<x≤1;1≤y≤3;1≤z≤8)等;锂金属;锂合金;硅类合金;锡类合金;金属氧化物,例如sno、sno2、pbo、pbo2、pb2o3、pb3o4、sb2o3、sb2o4、sb2o5、geo、geo2、bi2o3、bi2o4和bi2o5等;导电聚合物,例如聚乙炔等;li-co-ni类材料。
隔膜介于正极和负极之间,并且使用具有高离子渗透性和机械强度的绝缘薄膜。隔膜通常具有0.01μm至10μm的孔径和5μm至300μm的厚度。作为隔膜,例如,使用由烯烃聚合物(例如具有耐化学性和疏水性的聚丙烯)或者玻璃纤维或聚乙烯形成的片或无纺布。当采用诸如聚合物等固体电解质作为电解质时,固体电解质也可以同时充当隔膜和电解质。
含锂盐的非水性电解质由非水性电解质和锂盐组成。非水性电解质可以包括非水性有机溶剂、有机固体电解质或无机固体电解质,但不限于此。
非水性有机溶剂可以是例如非质子有机溶剂,例如n-甲基-2-吡咯烷酮、碳酸亚丙酯、碳酸亚乙酯、碳酸亚丁酯、碳酸二甲酯、碳酸二乙酯、γ-丁内酯、1,2-二甲氧基乙烷、四羟基法兰克(franc)、2-甲基四氢呋喃、二甲基亚砜、1,3-二氧戊环、甲酰胺、二甲基甲酰胺、二氧戊环、乙腈、硝基甲烷、甲酸甲酯、乙酸甲酯、磷酸三酯、三甲氧基甲烷、二氧戊环衍生物、环丁砜、甲基环丁砜、1,3-二甲基-2-咪唑烷酮、碳酸亚丙酯衍生物、四氢呋喃衍生物、乙醚、丙酸甲酯、丙酸乙酯等。
有机固体电解质可以包括例如聚乙烯衍生物、聚氧化乙烯衍生物、聚氧化丙烯衍生物、磷酸酯聚合物、聚搅拌赖氨酸(polyagitationlysine)、聚酯硫醚、聚乙烯醇、聚偏二氟乙烯、含离子解离基团的聚合物等。
无机固体电解质可以包括例如li类氮化物、卤化物或硫酸盐,例如li3n、lii、li5ni2、li3n-lii-lioh、lisio4、lisio4-lii-lioh、li2sis3、li4sio4、li4sio4-lii-lioh、li3po4-li2s-sis2等。
锂盐是易溶于非水性电解质的物质,可以包括例如licl、libr、lii、liclo4、libf4、lib10cl10、lipf6、licf3so3、licf3co2、liasf6、lisbf6、lialcl4、ch3so3li、cf3so3li、(cf3so2)2nli、氯硼烷锂、低级脂肪族羧酸锂、四苯基硼酸锂、酰亚胺等。
为了改善充电/放电特性和阻燃性,可以在非水性电解质中加入例如吡啶、亚磷酸三乙酯、三乙醇胺、环醚、乙二胺、正甘醇二甲醚、六磷酸三酰胺、硝基苯衍生物、硫、醌亚胺染料、n-取代的噁唑烷酮、n,n-取代的咪唑烷、乙二醇二烷基醚、铵盐、吡咯、2-甲氧基乙醇、三氯化铝等。可选地,可以进一步添加例如四氯化碳或三氟乙烯等含卤素的溶剂以提供阻燃性,或者可以进一步添加二氧化碳气体以提高高温保持特性,并且可以进一步添加fec(碳酸氟代乙烯酯)、prs(丙烯磺酸内酯)等。
根据本发明的又一实施方式,提供了一种包含二次电池的电池组,以及包含该电池组的设备。上述电池组和设备在本领域是已知的,因此,在本发明中将省略其具体描述。
该设备可以是例如笔记本电脑、上网本、平板电脑、移动电话、mp3、可穿戴电子产品、电动工具、电动车辆(ev)、混合动力电动车辆(hev)、插电式混合动力电动车辆(phev)、电动自行车、电动滑板车、电动高尔夫球车或电力存储系统等,但不限于此。
[有益效果]
如上所述,本发明的正极活性材料具有在层状结构的锂钴氧化物中掺杂有一种以上金属元素的结构,因此,将预定量以上的掺杂剂掺入且置于锂钴氧化物的晶格中,从而在大于4.5v的高电压下防止晶体结构的坍塌并确保结构稳定性。
与三元体系不同,锂钴氧化物的容量仅通过增加电压来增加。然而,当使用本发明的正极活性材料时,可以解决高电压下的稳定性问题,从而实现高容量和高循环特性。
附图说明
图1是显示在上限电压为4.5v下充电时,包含掺杂有1,000ppm或3,000ppmmg的锂钴氧化物的硬币型(coin-type)半电池的容量保持率的图;
图2是显示在上限电压为4.55v下充电时,包含掺杂有1,000ppm或3,000ppmmg的锂钴氧化物的硬币型半电池的容量保持率的图;
图3是显示在上限电压为4.5v下充电时,包含掺杂有1,000ppm或3,000ppmal的锂钴氧化物的硬币型半电池的容量保持率的图;
图4是显示在上限电压为4.55v下充电时,包含掺杂有1,000ppm或3,000ppmal的锂钴氧化物的硬币型半电池的容量保持率的图;
图5显示了实施例1的正极活性材料的tof-sims(飞行时间二次离子质谱)分析结果;和
图6是显示包含实施例1或比较例1的正极活性材料的硬币型半电池的峰强度的xrd图,其是在将上限电压从4.5v以0.01v的间隔增加至4.54v时测得的。
具体实施方式
以下将参考附图描述本发明的实施方式。然而,提供这些实施方式仅是为了更好地理解,但本发明的范围不限于此。
正极活性材料的制备
<实施例1>
将0.294g的mgo、80.27g的co3o4和36.94g的li2co3彼此干混,使得基于正极活性材料的总重量,mg的含量为3,000ppm。然后,将混合物在1050℃的炉内烧结10小时,以制备mg掺杂的锂钴氧化物。
<实施例2>
将0.147g的al2o3、80.27g的co3o4和36.94g的li2co3彼此干混,使得基于正极活性材料的总重量,al的含量为3,000ppm。然后,将混合物在1050℃的炉内烧结10小时,以制备al掺杂的锂钴氧化物。
<实施例3>
将0.245g的mgo、80.27g的co3o4和36.94g的li2co3彼此干混,使得基于正极活性材料的总重量,mg的含量为5,000ppm。然后,将混合物在1050℃的炉内烧结10小时,以制备al掺杂的锂钴氧化物。
<实施例4>
将0.343g的mgo、80.27g的co3o4和36.94g的li2co3彼此干混,使得基于正极活性材料的总重量,mg的含量为7,000ppm。然后,将混合物在1050℃的炉内烧结10小时,以制备al掺杂的锂钴氧化物。
<实施例5>
将0.441g的mgo、80.27g的co3o4和36.94g的li2co3彼此干混,使得基于正极活性材料的总重量,mg的含量为9,000ppm。然后,将混合物在1050℃的炉内烧结10小时,以制备al掺杂的锂钴氧化物。
<实施例6>
为了在实施例1中制备的mg掺杂的锂钴氧化物上形成涂层,将500ppm的al2o3与锂钴氧化物颗粒干混以涂覆锂钴氧化物颗粒,然后在700℃的炉内烧结5小时,以制备其上形成有涂层的正极活性材料。
<比较例1>
以与实施例1相同的方式制备mg掺杂的锂钴氧化物,不同之处在于,基于正极活性材料的总重量,mg的含量为1,000ppm。
<比较例2>
以与实施例2相同的方式制备al掺杂的锂钴氧化物,不同之处在于,基于正极活性材料的总重量,al的含量为1,000ppm。
<比较例3>
以与实施例1相同的方式制备mg掺杂的锂钴氧化物,不同之处在于,基于正极活性材料的总重量,mg的含量为10,000ppm。
二次电池的制造
将实施例1至6和比较例1至3中制备的各个金属掺杂的正极活性材料、pvdf粘合剂和天然石墨导电材料以96:2:2的重量比(正极活性材料:粘合剂:导电材料)在nmp中充分混合,然后涂布到厚度为20μm的al箔上,并在130℃下干燥,从而制造各个正极。作为负极,使用锂箔,使用在ec:dmc:dec=1:2:1的溶剂中含有1mlipf6的电解液来制造各个硬币型半电池。
<实验例1>容量保持率的分析
将上面制造的各个硬币型半电池在25℃下以0.5c充电至上限电压4.5v或4.55v,然后以1.0c放电至下限电压3v。这个过程视为1次循环,并且测量了50次循环后的容量保持率。结果示于下表1和图1至4中。表2显示了分别以4.5v和4.55v充电时的初始容量。
【表1】
【表2】
参考表1、图1至4和表2,当如实施例1或2中那样掺杂3,000ppm的mg或al时,在4.5v下进行50次充电/放电循环后,容量保持率低于掺杂有1000ppm的mg或al的比较例1或2的容量保持率。图1显示,当使用实施例1的正极活性材料时,直至约30次循环,容量保持率都高于比较例1的容量保持率,但超过30次循环后,实施例1的容量保持率迅速降低。
然而,以4.55v进行50次充电/放电循环后,具有更高掺杂含量的实施例1和2表现出明显更高的容量保持率。
al掺杂含量为3,000ppm的实施例2在4.5v下表现出比在4.55v下低的容量保持率。然而,与al掺杂含量为1,000ppm的比较例1相比,在4.5v下其容量保持率降低,而在4.55v下其容量保持率增加。
同时,与实施例相比,mg掺杂含量为10,000ppm的比较例2表现出低的容量保持率。
这是因为正极活性材料在充电/放电期间经历可逆相变,并且随着充电电位的增加,相变的可逆性降低,从而导致容量的降低。然而,当为了制备具有高容量的高电位锂钴氧化物而在锂钴氧化物中掺杂特定范围内的金属时,可以使不可逆相变最小化,从而防止容量保持率的下降。然而,当掺杂金属的含量如比较例1和2中那样太小时,难以获得上述效果,并且因此以4.55v进行充电/放电时容量保持率迅速下降。
因此,当锂钴氧化物掺杂有特定含量范围内的mg或al时,可以使高电位下的相变最小化,从而表现出高的容量保持率。
此外,随着掺杂元素含量的增加,在高于4.5v的电压下初始效率降低,因此预期在制造电池单元时容易平衡正极和负极。还预期正极活性材料的剩余量减少,这将有助于降低电池单元的生产成本。因此,预期可以设计适合于电池单元的操作电压条件的材料,可以实现电池单元所需的性能,并且可以大幅降低生产成本。
同时,在4.55v下,随着mg掺杂量的增加,寿命略有改善,这推测是归因于结构稳定化。然而,在4.55v下,随着mg掺杂量的增加,初始效率降低。预期当mg的掺杂量增加到10,000ppm以上时,可以进一步促进正极活性材料的电阻增加而不是结构稳定性,从而可能劣化容量,并且可能降低寿命稳定性。
同时,与不具有涂层的实施例1相比,以4.55v进行50次充电/放电循环后,实施例6的具有涂层的经掺杂的锂钴氧化物表现出高的容量保持率。
因此,可以看出,实施例的正极活性材料在高于4.5v的电位下表现出改善的寿命特性。
<实验例2>tof-sims(飞行时间二次离子质谱)分析
图5显示了通过tof-sims(飞行时间二次离子质谱)分析实施例2中得到的活性材料的结果。
参考图5,确认了掺杂的金属元素al分布在锂钴氧化物上,特别是,掺杂的金属元素al主要分布在靠近锂钴氧化物表面的区域中。这些分析结果表明,金属元素al掺杂到了锂钴氧化物中以形成物理/晶体学连接,而未通过化学键与锂钴氧化物形成复合体。
<实验例3>xrd分析
为了检查实施例1和比较例1的锂钴氧化物的晶体结构变化,制造了包含其的硬币型半电池,并且在将上限电压从4.5v以0.01v的间隔增加至4.55v的同时测量了峰强度。如此测量的xrd图(2θ-标度)示于图6中。
参考图6,实施例1的正极活性材料在4.40v至4.55v在23至24度的范围内显示出(003)面的峰,并且在4.55v下在24至25度的范围内显示出峰。当正极活性材料的充电电位为4.54v以上时,晶体结构向另一相进行相变,并且当充电电位为4.55v时,在24至25度范围内观察到指示相变后的晶体结构的新峰。然而,在一定程度上持续观察到(003)面的峰,表明相变可逆地发生。因此,即使在充电/放电期间,也可以在一定程度上保持容量保持率。
具体而言,图6显示了在各个电压下相变前/后的峰。4.55v下的(003)面的峰强度是4.50v下的(003)面的峰强度的30%以上。金属掺杂的锂钴氧化物使相变最小化,以表现出高的容量保持率,从而表现出显著改善的寿命特性。
然而,比较例1的正极活性材料在4.55v下表现出显著低的(003)面的峰强度,指示相变后的晶体结构的峰高于指示相变前的晶体结构的峰,这表明相变的可逆性显著降低。因此,可以看出,当掺杂金属的含量低时,寿命特性可能大幅劣化。
对于本发明所属领域的技术人员显而易见的是,在不脱离本发明的范围的情况下,可以对其进行各种修改和改变。
- 还没有人留言评论。精彩留言会获得点赞!