锂离子二次电池用负极活性物质的制造方法与流程
本发明涉及一种在用作锂离子二次电池用负极活性物质时,显示出充放电循环劣化得到极度抑制的、高电容且优异的充放电特性的二次电池用负极活性物质的制造方法。
背景技术:
近年来,伴随着电子设备、通讯设备等的急速发展及小型化技术的急速发达,各种可携式设备不断普及。而且,作为这些可携式设备的电源,就经济性及设备的小型化、轻量化的观点而言,强烈要求开发出高电容及寿命特性优异的二次电池。
作为此种小型、轻量的高电容的二次电池,目前正进行摇椅(rockingchair)型的锂离子电池的开发并使其实用化而普遍使用,所述摇椅(rockingchair)型的锂离子电池是将自层间释放锂离子的锂插层(intercalation)化合物用于正极物质,且将可在充放电时在结晶面间的层间吸藏释放(插入(intercalate))锂离子的石墨等所代表的碳质材料用于负极物质。
使用锂化合物作为负极的非水电解质二次电池具有高电压及高能量密度,其中,锂金属因丰富的电池电容而作为负极活性物质,在初期成为大量的研究对象。然而,在使用锂金属作为负极的情形时,在充电时在负极锂表面析出大量的树枝状锂,故有时充放电效率降低,另外,有时树枝状锂成长而引起与正极的短路,或者因锂自身的不稳定性、即高的反应性而对热或冲击敏感,故在商用化方面留有课题。
因此,作为代替所述锂金属的负极活性物质,逐渐使用吸藏、释放锂的碳系负极。
碳系负极解决了锂金属所具有的各种问题点,对锂离子电池的普及作出了大的贡献。然而,随着各种可携带用设备逐渐小型化、轻量化及高性能化,锂离子二次电池的高电容化作为重要的问题而浮现。
使用碳系负极的锂离子二次电池本质上具有低的电池电容。例如即便在作为所使用的碳而结晶性最高的石墨的情形时,理论电容在为lic6的组成时也仅为372mah/g。这与锂金属的理论电容为3860mah/g相比,仅不过为10%左右。因此,正在活跃地尝试进行以下研究:不论金属负极所具有的现有的问题点如何,也要再次将锂那样的金属导入至负极中并提高电池的电容。
作为具有代表性者,正在研究将以si、sn、a1那样的可与锂形成合金的金属作为主成分的材料用作负极活性物质。然而,si、sn那样的可与锂形成合金的物质存在以下问题点:在与锂的合金化反应时,伴随着体积膨胀而金属材料粒子微粉化,因此金属材料粒子间的接触减少而在电极内产生电性孤立的活性物质,或金属材料粒子自电极脱离,产生内部电阻的增加、电容的降低,或结果使循环特性降低,另外使由比表面积(specificsurfacearea)扩大所致的电解质分解反应加剧等。
为了解决因使用所述金属材料所致的问题点,也正进行以下研究:将体积膨胀率与金属相比而相对较低的两种以上的金属氧化物用作负极活性物质的材料。
例如在专利文献1中公开有:使用将氧化钛被覆于具有硅浓度倾斜的硅氧化物而成的材料作为锂离子二次电池的负极活性物质,获得高电容且具有经改良的循环特性的电地,在详细的说明中,虽具有使经氧化钛被覆的氧化硅在还原性环境下进行热处理的表述,但未记载针对充放电循环特性的效果,且实施例中是在惰性环境下进行热处理。
另外,在专利文献2中提出有将氧化钛被覆于分散有硅纳米粒子的硅氧化物粒子的表面而成的材料作为二次电池用负极材料。
进而,另外在非专利文献1中公开有:在锂离子电池的负极材料中使用将锐钛矿(anatase)型氧化钛被覆于硅氧化物而成的材料。
然而,使用将氧化钛被覆于硅氧化物系化合物所得的材料的任一种公知技术均是虽然最初的电容及循环特性确认到了一定程度的改良,但因反复进行充放电而能够可逆地利用的电容逐渐减小,无法获得可耐受实用化的循环特性。
进而,为了获得负极材料,制造方法为生产性差、结果需要高成本的技术。
现有技术文献
专利文献
专利文献1:us9,088,045b2
专利文献2:日本专利特开2011-96455号公报
非专利文献
非专利文献1:《材料化学期刊(j.mater.chem.)》,(2012)227999-8004
技术实现要素:
发明所要解决的问题
关于锂离子二次电池负极活性物质,依然要求解决现有的负极材料所具有的所述问题点,开发出一种显示出充放电循环劣化得到极度抑制的、高电容且优异的充放电特性的负极活性物质、及生产性优异的其制造方法。
本发明的课题为提供一种应对所述要求的以高生产性制造二次电池用负极活性物质的方法。
解决问题的技术手段
本发明人等人对所述课题进行了研究,结果发现了一种以高生产性制造负极活性物质的方法,所述负极活性物质在用作锂离子二次电池用的负极活性物质时,所得的二次电池具有充放电循环劣化得到极度抑制的、高电容且优异的充放电特性。
本发明的第一方案为一种锂离子二次电池用负极活性物质的制造方法,所述锂离子二次电池用负极活性物质包含硅-钛氧化物复合物,所述锂离子二次电池用负极活性物质的制造方法的特征在于:所述硅-钛氧化物复合物是通过将氧化钛被覆于硅氧化物而获得,
所述硅氧化物是对倍半硅氧烷聚合物(以下称为psq)在非氧化性环境下进行热处理而获得,且由通式sioxcyhz(0.5<x<1.8、0≤y<5、0≤z<0.4)表示,所述psq是使至少一种硅化合物进行水解及缩聚反应而获得,且具有下述式(1)的结构,
在对所述硅氧化物被覆氧化钛后,在还原性气体环境下进行热处理。
[化1]
(式中,r1及r4s别独立地为选自氢原子、碳数1~45的经取代或未经取代的烷基的群组、经取代或未经取代的芳基的群组及经取代或未经取代的芳烷基的群组中的基团;其中,在碳数1~45的烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-、亚环烷基或亚环烯基取代;在经取代或未经取代的芳烷基中的亚烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-或亚环烷基取代;
r2、r3、r5及r6分别独立地为选自氢原子、碳数1~45的经取代或未经取代的烷基的群组、经取代或未经取代的芳基的群组及经取代或未经取代的芳烷基的群组中的基团;其中,在碳数1~45的烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-、亚环烷基、亚环烯基或-sir12-取代;在经取代或未经取代的芳烷基中的亚烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-、亚环烷基、亚环烯基或-sir12-取代;
n表示1以上的整数。)
本发明的第二方案为本发明的第一方案所记载的锂离子二次电池用负极活性物质的制造方法,其特征在于:所述非氧化性环境下的热处理是在100℃~2000℃的温度范围内进行。
本发明的第三方案为本发明的第一方案或第二方案所记载的锂离子二次电池用负极活性物质的制造方法,其特征在于:所述还原性气体环境下的热处理是在200℃~850℃的温度范围内进行。
本发明的第四方案为本发明的第一方案至第三方案中任一方案所记载的锂离子二次电池用负极活性物质的制造方法,其特征在于:所述还原性气体环境为氢气环境、或包含2体积%以上的氢气的氢气与惰性气体的混合气体环境。
本发明的第五方案为本发明的第一方案至第四方案中任一方案所记载的锂离子二次电池用负极活性物质的制造方法,其特征在于:所述psq为具有选自下述式(2)、式(3)及式(4)中的一个以上的结构的衍生物或混合物。
[化2]
[化3]
[化4]
(式中,r1及r4分别独立地为选自氢原子、碳数1~45的经取代或未经取代的烷基的群组、经取代或未经取代的芳基的群组及经取代或未经取代的芳烷基的群组中的基团;其中,在碳数1~45的烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-、亚环烷基或亚环烯基取代;在经取代或未经取代的芳烷基中的亚烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-或亚环烷基取代;
r2、r3、r5及r6分别独立地为选自氢原子、碳数1~45的经取代或未经取代的烷基的群组、经取代或未经取代的芳基的群组及经取代或未经取代的芳烷基的群组中的基团;其中,在碳数1~45的烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-、亚环烷基、亚环烯基或-sir12-取代;在经取代或未经取代的芳烷基中的亚烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-、亚环烷基、亚环烯基或-sir12-取代;
n表示1以上的整数)
本发明的第六方案为本发明的第一方案至第四方案中任一方案所记载的锂离子二次电池用负极活性物质的制造方法,其特征在于:所述硅化合物的至少一种为下述式(5)所表示的硅化合物。
r10si(r7)(r8)(r9)(5)
(式中,r7、r8及r9分别独立地为氢、卤素、羟基或碳数1~4的烷氧基,r10为选自碳数1~45的经取代或未经取代的烷基的群组、经取代或未经取代的芳基的群组及经取代或未经取代的芳烷基的群组中的基团;其中,在碳数1~45的烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-、亚环烷基或亚环烯基取代;在经取代或未经取代的芳烷基中的亚烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-或亚环烷基取代)
本发明的第七方案为本发明的第一方案至第四方案中任一方案所记载的锂离子二次电池用负极活性物质的制造方法,其特征在于:所述硅化合物的至少一种为下述式(6)所表示的硅化合物。
hsi(r)3(6)
(式中,r为分别相同或不同的选自卤素、氢、碳数1~10的经取代或未经取代的烷氧基、碳数6~20的经取代或未经取代的芳氧基及碳数7~30的经取代或未经取代的芳基烷氧基中的基团;其中,在碳数1~10的经取代或未经取代的烷氧基、碳数6~20的经取代或未经取代的芳氧基及碳数7~30的经取代或未经取代的芳基烷氧基中,任意的氢可经卤素取代)
本发明的第八方案为一种锂离子二次电池用负极的制造方法,其特征在于:使用利用所述本发明的第一方案至第七方案中任一方案所记载的锂离子二次电池用负极活性物质的制造方法而制造的锂离子二次电池用负极活性物质。
本发明的第九方案为一种锂离子二次电池的制造方法,其特征在于:使用利用所述本发明的第八方案所记载的锂离子二次电池用负极的制造方法而制造的锂离子二次电池用负极。
发明的效果
根据本发明,可通过将氧化钛在还原性气体环境下进行热处理而被覆于硅氧化物而以低成本提供负极活性物质,所述硅氧化物是对使硅化合物进行水解及缩聚反应所得的psq在非氧化性环境下进行热处理而获得,且由通式sioxcyhz(0.5<x<1.8、0≤y<5、0≤z<0.4)表示。
另外,将使用利用本发明的制造方法所得的锂离子二次电池用负极活性物质而获得的锂离子二次电池用负极用作负极的锂离子二次电池具有充放电循环劣化得到极度抑制的、高电容且优异的充放电特性。
附图说明
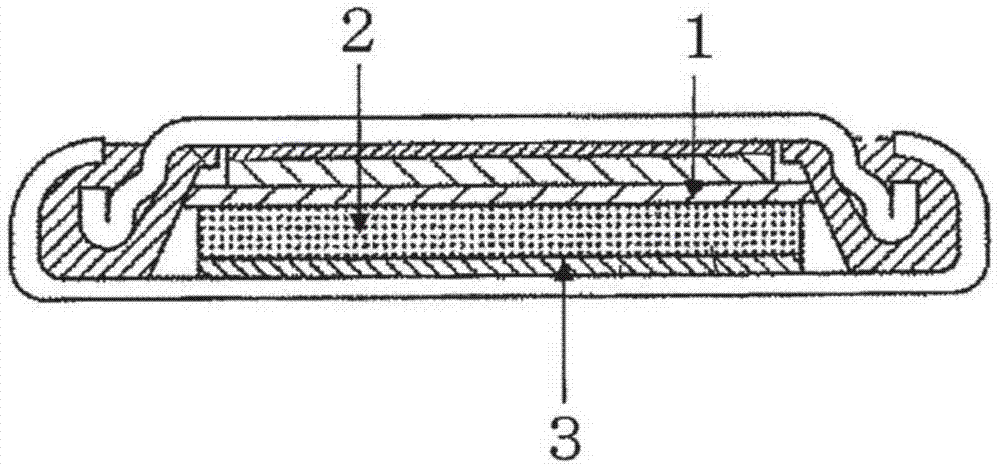
图1为表示硬币型的锂离子二次电池的构成例的图。
图2为实施例4中制造的硅-钛氧化物复合物(1)的显微镜(sem)照片。
具体实施方式
以下,对本发明加以更详细的说明。
<倍半硅氧烷聚合物(psq)的制造>
本发明中使用的psq是使至少一种硅化合物进行水解及缩聚反应而获得。
可用作硅化合物者如下述所例示。
例如为下述式(5)所表示的硅化合物。
r10si(r7)(r8)(r9)(5)
(式中,r7、r8及r9分别独立地为氢、卤素、羟基或碳数1~4的烷氧基,式r10为选自碳数1~45的经取代或未经取代的烷基的群组、经取代或未经取代的芳基的群组及经取代或未经取代的芳烷基的群组中的基团;其中,在碳数1~45的烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-、亚环烷基或亚环烯基取代;在经取代或未经取代的芳烷基中的亚烷基中,任意的氢可经卤素取代,任意的-ch2-在基团中的碳数不超过45的范围内可经-o-、-ch=ch-或亚环烷基取代)
本发明中,所述r7、r8及r9的例子具体而言包含氢、氟、氯、溴、羟基、甲氧基、乙氧基、正丙氧基、异丙氧基等。
作为所述r10,碳数1~45的未经取代的烷基的例子中包含甲基、乙基、丙基、1-甲基乙基、丁基、2-甲基丙基、1,1-二甲基乙基、戊基、己基、1,1,2-三甲基丙基、庚基、辛基、2,4,4-三甲基戊基、壬基、癸基、十一基、十二基、十四基、十六基、十八基、二十基、二十二基、三十基等。
作为所述r10,碳数1~45的氟化烷基的例子中包含3,3,3-三氟丙基、3,3,4,4,5,5,6,6,6-十九氟己基、十三氟-1,1,2,2-四氢辛基、十七氟-1,1,2,2-四氢癸基、全氟-1h,1h,2h,2h-十二基、全氟-1h,1h,2h,2h-十四基等。
作为所述r10,碳数2~45的烷氧基烷基的例子中包含3-甲氧基丙基、甲氧基乙氧基十一基、3-七氟异丙氧基丙基等。
作为所述r10,一个-ch2-经亚环烷基取代的碳数1~45的烷基的例子中包含环己基甲基、金刚烷乙基、环戊基、环己基、2-双环庚基、环辛基等。环己基为甲基的-ch2-经亚环己基取代的例子。环己基甲基为乙基的β位的-ch2-经亚环己基取代的例子。
作为所述r10,碳数2~45的烯基的例子中包含乙烯基、2-丙烯基、3-丁烯基、5-己烯基、7-辛烯基、10-十一烯基、21-二十二烯基等。碳数2~45的烯氧基烷基的例子为烯丙氧基十一基。一个-ch2-经亚环烯基取代的碳数1~45的烷基的例子中包含2-(3-环己烯基)乙基、5-(双环庚烯基)乙基、2-环戊烯基、3-环己烯基、5-降冰片烯-2-基、4-环辛烯基等。
在所述r10为经取代或未经取代的芳基的情形时的例子中包含任意的氢可经卤素或碳数1~10的烷基取代的苯基及未经取代的萘基等。卤素的优选的例子为氟原子、氯原子及溴。在碳数1~10的烷基中,任意的氢可经氟取代,任意的-ch2-可经-o-、-ch=ch-或亚苯基取代。即、在r10为经取代或未经取代的芳基的情形时的优选的例子中包含未经取代的苯基、未经取代的萘基、烷基苯基、烷氧基苯基、烯基苯基、具有在碳数1~10的烷基中任意的-ch2-经亚苯基取代的基团作为取代基的苯基、在这些基团中任意的氢经卤素取代的基团等。
卤化苯基的例子中包含五氟苯基、4-氯苯基、4-溴苯基等。烷基苯基的例子中包含4-甲基苯基、4-乙基苯基、4-丙基苯基、4-丁基苯基、4-戊基苯基、4-庚基苯基、4-辛基苯基、4-壬基苯基、4-癸基苯基、2,4-二甲基苯基、2,4,6-三甲基苯基、2,4,6-三乙基苯基、4-(1-甲基乙基)苯基、4-(1,1-二甲基乙基)苯基、4-(2-乙基己基)苯基、2,4,6-三(1-甲基乙基)苯基等。烷氧基苯基的例子中包含(4-甲氧基)苯基、(4-乙氧基)苯基、(4-丙氧基)苯基、(4-丁氧基)苯基、(4-戊氧基)苯基、(4-庚氧基)苯基、(4-癸氧基)苯基、(4-十八烷氧基)苯基、4-(1-甲基乙氧基)苯基、4-(2-甲基丙氧基)苯基、4-(1,1-二甲基乙氧基)苯基等。烯基苯基的例子中包含4-乙烯基苯基、4-(1-甲基乙烯基)苯基、4-(3-丁烯基)苯基等。
另外,作为本发明中使用的硅化合物,下述式(6)所表示的硅化合物也适宜。
hsi(r)3(6)
式(6)中,r的优选的例子中包含分别相同或不同的选自卤素、氢、碳数1~10的经取代或未经取代的烷氧基及碳数6~20的经取代或未经取代的芳氧基中的基团。其中,在碳数1~10的经取代或未经取代的烷氧基及碳数6~20的经取代或未经取代的芳氧基中,任意的氢可经卤素取代。式(6)所述r的具体例可选择与式(5)中的r10的例子相同的基团(关于碳数,依据所述本发明的第七方案)。
式(6)所表示的硅化合物具体而言可列举下述化合物等。
例如可列举:三氯硅烷、三氟硅烷、三溴硅烷、二氯硅烷等三卤化硅烷或二卤化硅烷,三正丁氧基硅烷、三叔丁氧基硅烷、三正丙氧基硅烷、三异丙氧基硅烷、二正丁氧基乙氧基硅烷、三乙氧基硅烷、三甲氧基硅烷、二乙氧基硅烷等三烷氧基硅烷或二烷氧基硅烷,进而三芳氧基硅烷、二芳氧基硅烷、二芳氧基乙氧基硅烷等芳氧基硅烷或芳氧基烷氧基硅烷。
这些化合物中,就反应及获取的容易性及制造成本的观点而言,优选为三卤化硅烷或三烷氧基硅烷,特别优选为三卤化硅烷。
这些式(5)及式(6)所表示的硅化合物可单独使用,也可混合使用两种以上。另外,此并不妨碍包含其他硅化合物。
另外,本发明中使用的式(5)及式(6)所表示的硅化合物的水解性及缩聚反应性高,不仅容易获得psq,而且容易控制在非氧化性环境下进行热处理时所得的硅氧化物的组成与结构。
继而,本发明中使用的psq是使所述硅化合物进行水解及缩聚反应而获得。
水解可利用公知的方法、例如在醇或二甲基甲酰胺(dimethylformamide,dmf)等溶剂中、在盐酸等无机酸或乙酸等有机酸及水的存在下、在常温或加热下实施。因此,在水解后的反应液中,除了本发明的硅化合物的水解物以外,也可含有溶剂、酸及水以及来源于这些物质的物质。
另外,在水解后的反应液中,本发明中使用的硅化合物可不完全水解,也可局部残留。
此时,除了水解反应以外,也局部进行水解物的缩聚反应。
此处,缩聚反应进行的程度可通过水解温度、水解时间、酸性度和/或溶剂等来控制,例如可如后述那样根据目标硅氧化物而适当设定。
考虑到其生产性及制造成本,本发明包括在一个反应器中、在同一条件下同时进行水解与缩聚反应的方法。
关于反应条件,在搅拌下、在酸性水溶液中添加本发明的式(1)所表示的硅化合物,使其在-20℃~50℃、优选为0℃~40℃、特别优选为10℃~30℃的温度下反应0.5小时~20小时、优选为1小时~10小时、特别优选为1小时~5小时。
反应时的酸性度可进行适当调整。用于酸性度调整的酸可使用有机酸、无机酸的任一种。
具体而言,有机酸可例示甲酸、乙酸、丙酸、草酸、柠檬酸等,无机酸可例示盐酸、硫酸、硝酸、磷酸等,就可容易地控制而进行水解反应及其后的重缩合反応且获取或ph值调整、及反应后的处理也容易的方面而言,优选为盐酸。
另外,在使用三卤化硅烷等卤化硅烷作为本发明中使用的硅化合物的情形时,在水的存在下会形成酸性水溶液,故无需另外特别添加酸,为本发明的优选方案之一。
水解反应及缩聚反应结束后,通过过滤分离或离心分离等将液体部分加以分离去除,视情形而进行水洗净或有机溶剂洗净后,加以干燥,获得具有下述式(1)的结构的psq。
[化5]
(式中,关于r1及r4、另外关于r2、r3、r5及r6以及关于n,分别如上文所述)
另外,本发明中使用的psq除使所述硅化合物进行水解反应及缩聚反应而获得者以外,也可使用具有选自下述式(2)、式(3)及式(4)中的一个以上的结构的衍生物或混合物。
[化6]
[化7]
[化8]
(式中,关于r1及r4、另外关于r2、r3、r5及r6以及关于n,分别如上文所述)
所述式(2)至式(4)的倍半硅氧烷聚合物可利用公知的方法而获得。
例如,式(3)的例子可列举国际公开第2003/024870号及国际公开第2004/081084号的各公报中所记载的倍半硅氧烷聚合物化合物。
<硅氧化物的制造>
本发明中使用的硅氧化物是对利用所述方法所得的本发明的psq在非氧化性环境下进行热处理而获得。
若通过元素分析对如此而获得的硅氧化物的组成进行测定,则为通式sioxcyhz(0.5<x<1.8、0≤y<5、0≤z<0.4)所表示的硅氧化物。
若x在0.5<x<1.8、优选为1.0<x<1.8、更优选为1.2<x<1.7的范围内,则容易制造硅氧化物,可获得充分的电池电容。若y在0≤y<5、优选为0≤y<4的范围内,则可获得充分的导电性与高电池电容。若z为0≤z<0.4、优选为0≤z<0.35的范围内,则所得的二次电池具有优异的充放电电容及电容维持率提高的良好的循环特性。另外,更优选为y与z不同时为0的值且处于所述范围内。
进而,本发明中使用的硅氧化物进而优选为如下的硅氧化物:其为使用由上文所述的式(6)所表示的硅化合物所得的氢化倍半硅氧烷聚合物而获得的硅氧化物,且具有在利用红外光谱法(ir)所测定的光谱中,处于820cm-1~920cm-1间的来源于si-h键的峰值1的强度(i1)与处于1000cm-1~1200cm-1间的来源于si-o-si键的峰值2的强度(i2)之比(i1/i2)在0.01~0.35的范围内的特征。
若所述峰值1的强度(i1)与峰值2的强度(i2)之比(i1/i2)在0.01~0.35、优选为0.01~0.30、更优选为0.03~0.20的范围内,则可通过适量的si-h键的存在而在制成电池的情形时表现出充放电循环劣化得到极度抑制的、高电容且优异的充放电特性。
本发明中使用的硅氧化物是对上文所述的本发明的psq在非氧化性环境下进行热处理而获得。
热处理必须在非氧化性环境下进行。
非氧化性环境包括:惰性气体环境、通过高真空而除去了氧的环境(只要为以不阻碍目标硅氧化物的生成的程度除去了氧的环境即可)、还原性环境及并用了这些环境的环境。惰性气体可列举氮气、氩气、氦气等。这些惰性气体只要为通常所使用的高纯度规格的气体,则可无问题地使用。另外,也可为不使用惰性气体而通过高真空除去了氧的环境。还原性环境包括包含氢等还原性气体的环境。
本发明的在非氧化性环境下进行热处理的温度为100℃~2000℃、优选为200℃~1500℃。进而优选为650℃~1200℃。
热处理时间并无特别限定,通常为30分钟~10小时,优选为1小时~8小时。
如此而获得的本发明中使用的硅氧化物中,作为粒径为次微米(submicron)的球状粒子的一次粒子进一步凝聚而形成粒径为几微米的二次凝聚体。
因一次粒子小,在作为锂离子二次电池的负极材料而用于电池的情形时,作为二次电池反复进行充放电时所产生的膨胀收缩时的应力得到松弛,在抑制循环劣化而循环特性提高的方面有效果。另外,通过具有复杂的二次凝聚结构,与粘合剂的粘合性变得良好,表现出更优异的循环特性。
硅氧化物系负极活性物质如上所述,粒径越小越可松弛膨胀收缩时的应力,但若为粒径为纳米尺寸、或在粒子内部含有纳米气孔结构等而比表面积以必要以上的程度变大的粒子,则与电解液的接触面积也增大,负极粒子表面上的被膜形成反应量增加而导致循环特性的劣化。关于此方面,可认为本发明的硅氧化物具有次微米尺寸的适度的粒径、及3m2/g~8m2/g的适度的比表面积,故即便在被覆氧化钛后,由与电解液的与电解液的被膜形成反应所致的电容降低的影响也小,可获得优异的循环特性。
另外,本发明中使用的硅氧化物具有粒度分布非常狭窄的特征。所述狭窄的粒度分布不仅在被覆氧化钛时及制造负极时的操作性良好,而且可提高电极密度。
进而,另外作为本发明中使用的硅氧化物而使用本申请人之前所申请的发明(申请号:wo2014-002602)的专利说明书中记载的、通式sioxcy(0.5<x<1.8、1<y<5)所表示的硅氧化物也为本发明的优选方案之一。
若通过元素分析对所述硅氧化物进行测定,则为至少含有硅(si)、碳(c)及氧(o)者而与之前的一般硅氧化物不同,另外,在通过x射线小角散射法对2θ<10°以下的低角度区域中所显现者进行测定所得的光谱中,在
若散射q处于
进而,在利用拉曼分光法对所述硅氧化物的由热处理引起的碳材料的结构变化进行测定所得的光谱中,在1590cm-1(g带/石墨结构)与1325cm-1(d带/非晶性碳)处观察到散射,确认到结晶性碳与非晶性碳的峰值强度比(id/ig比)处于2.0~5.0范围内的、作为碳的石墨质碳材料的形成,为在硅氧化物中具有石墨碳固体者。
若峰值强度比(id/ig比)处于2.0~5.0的范围内,则结晶性碳变多而石墨质碳材料生长,可在导电性不表现出各向异性的情况下获得所期望的纳米畴结构,可获得良好的导电性。
根据以上情况而推测,所述硅氧化物包含被覆于碳的直径为1nm~3nm左右的纳米畴结构。若o/si比在0.5~1.8的范围内,则容易制造作为硅氧化物系复合材料而可获得纳米畴结构的非晶质硅氧化物成分,可获得充分的电池电容。若c/si比在1~5的范围内,则石墨适度生长,导电性与电池电容的平衡性良好,可获得充分的导电性与高电池电容。
<硅-钛氧化物复合物前体的制造(对硅氧化物被覆氧化钛)>
通过本发明而制造的硅-钛氧化物复合物可通过将氧化钛被覆于利用所述方法所得的本发明中使用的硅氧化物而获得。
进行被覆的方法可使用各种方法。
例如可列举在使氧化钛粒子悬浮于溶剂中而成的悬浮液中添加硅氧化物,其后进行过滤、干燥、热处理的方法,优选为使本发明的硅氧化物悬浮于烷氧基钛溶液中后,使其进行缩合反应,从而使氧化钛的被膜被覆于硅氧化物表面,之后进行过滤、干燥、热处理的方法。
被覆氧化钛时所使用的烷氧基钛可列举:四烷氧基钛、芳氧基三烷氧基钛、二芳基二烷氧基钛等。优选为四烷氧基钛,具体而言可列举:四辛氧基钛、四正-丁氧基钛、四异-丙氧基钛、四(2-乙基己氧基)钛等。
悬浮液中的硅氧化物与烷氧基钛的缩合反应可利用公知的方法、例如在醇或dmf等溶剂中、视需要在盐酸等无机酸或乙酸等有机酸及水的存在下、在常温或加热下实施。
关于反应条件,在搅拌下使其在-20℃~50℃、优选为0℃~40℃、特别优选为10℃~30℃的温度下反应0.5小时~20小时、优选为1小时~10小时、特别优选为1小时~5小时。
另外,作为所述硅氧化物与烷氧基钛的使用比例,在最终的硅-钛氧化物复合物中,以成为氧化钛为0.1重量%~10重量%、优选为0.2重量%~8重量%的被覆量范围的方式使用。
缩合反应结束后,通过减压干燥、或过滤分离或离心分离等将液体部分加以分离去除,视情形而进行溶剂洗净后,加以干燥,获得硅-钛氧化物复合物前体。
<硅-钛氧化物复合物的制造>
通过本发明而制造的硅-钛氧化物复合物是对利用所述方法所得的本发明中使用的硅-钛氧化物复合物前体在还原性气体环境下进行热处理而获得。
热处理必须在还原性气体环境下进行。
作为还原性气体,除氢气以外也可列举一氧化碳、氨气、硫化氢等,但就操作容易性的方面而言,优选为氢气。这些还原性气体可单独使用,另外也可混合使用两种以上。
进而也可使用氮气或氩气等惰性气体与还原性气体的混合气体。作为混合比例,只要还原性气体为与惰性气体的混合气体全体的2体积%以上即可。
表现出充放电循环劣化得到极度抑制的、高电容且优异的充放电特性的热处理温度为200℃~850℃,优选为250℃~850℃,更优选为250℃~800℃。
热处理时间并无特别限定,通常为30分钟~10小时,优选为1小时~8小时。
如此获得通过本发明而制造的硅-钛氧化物复合物,如上文所述那样,作为氧化钛的被覆量,在最终的硅-钛氧化物复合物中,为氧化钛为0.1重量%~10重量%、优选为0.2重量%~8重量%的被覆量范围。
作为所被覆的氧化钛的作用,认为有以下三种。一种为对活性物质赋予导电性。氧化钛自身为绝缘体,但通过插入锂而在传导带注入电子,从而导体化,可在充电时使活性物质表面的电子传导性提高。另一种为促进活性物质-电解液界面中的锂的交接。关于硅氧化物的充电反应,伴随着硅-氧键的开裂而在进行反应时需要大的能量,但可经由能以相对较低的能量进行锂脱插的氧化钛来降低电解液-活性物质界面的活性障壁。最后一种为形状稳定化效果。氧化钛能够不引起结构变化地使锂脱插,因此通过配置于表面可使形状稳定化,可抑制由活性物质的脱落或新生面显现所致的电解液的分解反应。
另外,氧原子的一部分自通过在还原性气体环境下进行热处理而被覆的氧化钛表层脱离,由此可在氧化钛骨架中产生变形而生成价数低的钛。此种存在价数低的钛原子的氧化钛层与价数一定的氧化钛层相比,在插入锂时的电子传导性提高效果更强,可进一步降低电解液-活性物质介面的活性障壁,因此可使充放电反应顺利地进行。认为由此充放电效率进一步提高,且循环劣化得到抑制。
本发明中使用的硅氧化物其自身具有高的充放电循环稳定性,但认为通过被覆有在还原性气体环境下进行了热处理的氧化钛,除了以上那样的作用外也可获得更高的充放电循环稳定性。
<包含硅-钛氧化物复合物的负极活性物质>
本发明提供一种包含所述通过本发明所制造的硅-钛氧化物复合物而成的锂离子二次电池用负极活性物质。
为了实现电池的高电容化而必须将大量的电流进行充放电,故要求电极的电阻低的材料。
因此,使碳系物质与所述硅-钛氧化物复合物复合也为本发明的一方案。
为了使碳系物质复合,可列举:利用机械融合(mechanofusion)等机械融合处理法或化学气相沉积(chemicalvapordeposition,cvd)等蒸镀法使碳系物质与所述硅-钛氧化物复合物复合化的方法;或通过使用球磨机或振动磨机等的机械混合法等使碳系物质在所述硅-钛氧化物复合物内分散的方法。
再者,在使碳系物质与所述硅氧化物复合化的方法中,也可在所述硅-钛氧化物复合物中混合碳系物质前体并进行热处理,由此使碳系物质前体转化而成的碳系物质与所述硅-钛氧化物复合物复合化。
本发明中使用的碳系物质可优选地列举:石墨、碳黑、石墨烯(graphene)、富勒烯、碳纳米管、碳纳米泡沫(carbonnanofoam)、沥青系碳纤维(pitchcarbonfiber)、聚丙烯腈系碳纤维及非晶形碳等碳系物质。
另外,本发明中使用的碳系物质前体可列举:可通过热处理而转化成碳系物质的含有碳的有机化合物或聚合物。
例如可列举:甲烷、乙烯、丙烯或乙炔等烃气体类,蔗糖、葡萄糖、纤维素等糖类,乙二醇、二乙二醇、聚乙二醇、丙二醇等二醇类,酚树脂、环氧树脂、聚氯乙烯、聚乙烯醇、聚吡咯,进而石油沥青、煤焦油沥青、乙炔黑。
再者,关于所述硅-钛氧化物复合物与碳系物质的复合比例,相对于所述硅-钛氧化物复合物与碳系物质的合计量,碳系物质优选为10重量%~95重量%的范围。
<负极>
另外,本发明提供一种含有上文所述的锂离子二次电池用负极活性物质的负极的制造方法,所述锂离子二次电池用负极活性物质包含通过本发明而制造的硅-钛氧化物复合物。
例如,可将包含含有通过本发明所制造的所述硅-钛氧化物复合物或使所述碳系物质复合的硅-钛氧化物复合物而形成的负极活性物质及粘合剂的负极混合材料成形为一定的形状,也可利用将所述负极混合材料涂布于铜箔等集电体上的方法来制造。负极的成形方法并无特别限定,可使用公知的方法。
更详细而言,将含有通过本发明所制造的硅-钛氧化物复合物或使所述碳系物质复合的硅-钛氧化物复合物的负极活性物质如通常那样与粘合剂以及视需要的导电材料等混合而制备负极材料组合物,将其直接涂布于以铜、镍、不锈钢等为主体的棒状体、板状体、箔状体、网状体等集电体上,或将负极材料组合物另行浇注(casting)于支撑体上,将自所述支撑体剥离的负极活性物质膜层压于集电体上而获得负极极板。另外,本发明的负极不限定于所述列举的形态,也可为所列举的形态以外的形态。
粘合剂只要为二次电池中通常所使用者,则均可使用,除了羧甲基纤维素、聚丙烯酸、海藻酸、葡甘露聚糖、直链淀粉、蔗糖及其衍生物或聚合物、进而除了各自的碱金属盐以外,可例示聚酰亚胺树脂或聚酰亚胺酰胺树脂。这些粘合剂可单独使用,也可为混合物,进而也可另加成、混合提高与集电体的粘合性、改善分散性、提高粘合剂自身的导电性等赋予其他功能的成分,例如苯乙烯-丁二烯-橡胶系聚合物或苯乙烯-异戊二烯-橡胶系聚合物。
<锂离子二次电池>
进而,另外本发明提供一种使用含有上文所述的锂离子二次电池用负极活性物质的负极的锂离子二次电池的制造方法,所述锂离子二次电池用负极活性物质包含通过本发明所制造的硅-钛氧化物复合物而成。
例如,可利用如下方法来制造锂离子二次电池。
首先,将能可逆地吸藏及释放li的正极活性物质、导电助剂、粘合剂及溶剂混合,准备正极活性物质组合物。将所述正极活性物质组合物与负极同样地如通常所进行那样,直接涂布于金属集电体上及加以干燥,准备正极板。
也可将所述正极活性物质组合物另行浇注于支撑体上后,将自所述支撑体剥离所得的膜层压于金属集电体上而制造正极。正极的成形方法并无特别限定,可使用公知的方法。
所述正极活性物质只要为含锂的复合金属氧化物、且在所述二次电池的领域中通常所使用者,则均可使用,例如可列举linimconmn1-m-no2、limn2o4等。具体的复合氧化物可列举limn2o4、licoo2、linio2、lifeo2。另外,也可使用作为可进行锂的氧化还原的化合物的v2o5、tis及mos等。
导电助剂是使用碳黑、石墨微粒子等,粘合剂可使用偏二氟乙烯/六氟丙烯共聚合物、聚偏二氟乙烯(pvdf)、聚丙烯腈、聚甲基丙烯酸甲酯、聚四氟乙烯及其混合物、苯乙烯-丁二烯-橡胶系聚合物,溶剂是使用n-甲基吡咯烷酮、丙酮、水等。
此时,正极活性物质、导电助剂、粘合剂及溶剂的含量是设为锂离子二次电池中通常可使用的量。
介于正极与负极之间的隔离片(separator)只要为锂离子二次电池中通常所使用者,则均可使用。尤其优选为对电解质的离子迁移的阻抗低、或电解液含浸能力优异者。具体而言为选自玻璃纤维、聚酯、聚乙烯、聚丙烯、聚四氟乙烯(ptfe)、其化合物中的材质,也可为不织布或织布的形态。
更具体而言,在锂离子二次电池的情形时,使用包含聚乙烯、聚丙烯那样的材料的可卷取的隔离片,在锂离子聚合物电池的情形时,使用有机电解液含浸能力优异的隔离片,所述隔离片的成形方法并无特别限定,可使用公知的方法。例如可利用下述方法制造。
即,可将高分子树脂、填充剂及溶剂混合而准备隔离片组合物后,将所述隔离片组合物直接涂布于电极上部及加以干燥而形成隔离膜,或将所述隔离片组合物浇注于支撑体上及加以干燥后,将自所述支撑体剥离的隔离膜层压于电极上部而形成。
所述高分子树脂并无特别限定,只要为用于电极板的粘合剂的物质,则均可使用。例如可使用偏二氟乙烯/六氟丙烯共聚合物、聚偏二氟乙烯、聚丙烯腈、聚甲基丙烯酸甲酯及其混合物等。
关于电解液,可在碳酸亚丙酯、碳酸亚乙酯、碳酸亚二乙酯、碳酸乙基甲酯、碳酸甲基丙酯、碳酸亚丁酯、苯甲腈、乙腈、四氢呋喃、2-甲基四氢呋喃、γ-丁内酯、二氧杂环戊烷、4-甲基二氧杂环戊烷、n,n-二甲基甲酰胺、二甲基乙酰胺、二甲基亚砜、二噁烷、1,2-二甲氧基乙烷、环丁砜、二氯乙烷、氯苯、硝基苯、碳酸二甲酯、碳酸甲基异丙酯、碳酸乙基丙酯、碳酸二丙酯、碳酸二丁酯、二乙二醇或二乙醚等溶剂或这些溶剂的混合溶剂中,溶解包含lipf6、libf4、lisb6、liasf6、liclo4、licf3so3、li(cf3so2)2n、lic4fgso3、lisbf6、lialo4、lialcl4、lin(cpf2p+1so2)(cqf2q+1so2)(其中,p及q为自然数)、licl、lii那样的锂盐的电解质中的一种或将这些的两种以上混合而成的物质而使用。
另外,也可使用除此以外的各种非水系电解质或固体电解质。例如可使用添加有锂离子的各种离子液体、将离子液体与微粉末混合的拟固体电解质、锂离子导电性固体电解质等。
进而,另外为了提高充放电循环特性,在所述电解液中适当含有在负极活性物质表面促进稳定的被膜形成的化合物也为本发明的一方案。例如有效的是碳酸亚乙烯酯(vc)、氟苯、环状氟化碳酸酯[碳酸亚氟乙酯(fec)、碳酸亚三氟丙酯(tfpc)等]、或链状氟化碳酸酯[碳酸三氟二甲酯(tfdmc)、碳酸三氟二乙酯(tfdec)、碳酸三氟乙基甲酯(tfemc)等]等氟化碳酸酯。特别优选为碳酸亚氟乙酯(fec)。
若添加fec,则初次充电时,fec在负极上被还原分解而形成lif或li2co3等分解产物。这些分解生成成分在负极活性物质表面聚合而稳定化并形成优良的被膜。所述被膜即便在严酷的充放电环境下也稳定地存在,认为也发挥促进锂离子的迁移并且抑止电解液的分解反应的作用。
再者,所述环状氟化碳酸酯及链状氟化碳酸酯也可如碳酸亚乙酯等那样用作溶剂。
在如所述那样的正极极板与负极极板之间配置隔离片而形成电池结构体。若将所述电池结构体缠绕(winding)、或弯折而放入至圆筒形电池盒或方型电池盒中后,注入电解液,则锂离子二次电池完成。
另外,若将所述电池结构体层叠成叠片电池(bi-cell)结构后,使其含浸至有机电解液中,将所得的物品放入至袋(pouch)中加以密封,则锂离子聚合物电池完成。
[实施例]
以下示出各实施例、比较例及参考例对本发明加以更具体的说明,但本发明不限定于这些实施例。
在本实施例中,对各实施例、比较例及参考例中制备的硅氧化物及硅-钛氧化物复合物进行各种分析、评价。
在各实施例、比较例及参考例中的“元素分析”中使用的测定装置及测定方法以及“电池特性的评价”如下。
(元素分析)
关于元素组成分析是利用拉塞福背向散射分析(rutherfordbackscattering,rbs)/氢前向散射分析(hydrogenforwardscattering,hfs)法来进行,即,使试样粉末凝固成颗粒状后,对试样照射经加速至2.3mev的he离子,分析背向散射粒子的能量光谱、及经前向散射的氢原子的能量光谱,由此获得含氢的准确度高的组成值。硅、氧、钛的含量是利用rbs光谱分析来测量,氢含量是通过使用rbs与hfs的光谱的分析来测量。另外,氧化钛含量是假设将所有钛二氧化钛化并将钛含量设为(tio2/ti=79.87/47.87=1.67)1.67倍而进行换算。
测定装置是利用美国国家静电公司(nationalelectrostaticscorporation)制造的派勒特(pelletron)3sdh,在入射离子:2.3mevhe、rbs/hfs同时测定时入射角:75deg.、散射角:160deg.、试样电流:4na、射束径:2mmφ的条件下进行测定。
(氧化钛被覆层的分析)
氧化钛被覆层的分析是使用x射线光电子光谱分析装置phiquanterasxm[爱科发真空(ulvac-phi)]在经x射线源单色化的a1kα、输出15kv/25w、射束径100μmφ下进行,并根据ti2p、o1s的峰值位置与峰值形状确定结合状态。
(电池特性的评价)
使用含有通过本发明制造的硅-钛氧化物复合物的负极活性物质的锂离子二次电池等的充放电特性是如以下那样测定。
使用长野(nagano)股份有限公司制造的bts2005w,相对于硅-钛氧化物复合物1g重量而以100ma的电流对li电极进行恒定电流充电直至达到0.001v,继而一面维持0.001v的电压,一面实施恒定电压充电直至相对于活性物质1g而电流成为20ma以下的电流值。
对于充电完成的单元,经过约30分钟的休止期间后,相对于活性物质1g而以100ma的电流进行恒定电流放电直至电压达到1.5v。
另外,充电电容是根据直至恒定电压充电结束的累计电流值而计算,放电电容是根据直至电池电压到达1.5v的累计电流值来计算。在各充放电的切换时,通过开路而休止30分钟。
关于充放电循环特性,也在同样的条件下进行。
再者,充放电效率是设定为放电电容相对于初次(充放电的第1循环)的充电电容的比率,电容维持率是设为充放电第100循环的放电电容相对于初次的放电电容的比率。
<倍半硅氧烷聚合物(psq)的制造>
(合成例1)
在1000ml的四口烧瓶中加入360ml甲苯(和光纯药工业)、42.2g四丁基氢氧化铵(东京化成工业)(37%tbah在meoh中)、16.2g纯水,在冰浴中进行搅拌、冷却。在500ml的滴液漏斗中添加360ml二乙醚(和光纯药工业)、118.8g苯基三甲氧基硅烷(东京化成工业),花5分钟进行滴加。在滴加后撤去冰浴,在室温下搅拌70小时。70小时后,利用加压过滤机进行过滤。
将所获得的粉体移至烧杯中,利用甲苯进行洗净,再次进行加压过滤。在过滤后利用减压干燥器进行120℃、6小时减压干燥而获得48.8g的作为psq的八苯基倍半硅氧烷。
(合成例2)
(phsio3/2)n的合成
在500m1的四口烧瓶中加入99.1g苯基三甲氧基硅烷(东京化成)、16g甲醇(和光纯药工业)。一面在室温下搅拌,一面利用滴液漏斗花30分钟缓缓滴加36g1n的hcl。在滴加结束后在60℃下进行2小时加热搅拌。在2小时后进行冷却,滴加200g甲苯(和光纯药工业)。
其后,将反应液转移至500ml的分液漏斗中。通过饱和的食盐水进行水洗后,通过饱和的碳酸氢钠水进行水洗,进而通过饱和的食盐水进行2次水洗,最后利用纯水进行2次水洗。在水洗后,利用硫酸镁(和光纯药工业)进行脱水。将所述溶液移至可分离式烧瓶中,将溶剂蒸馏去除并进行减压加热而获得56.1g的作为psq的(phsio3/2)n(其中,n为1以上的整数)。
(合成例3)
(mesio3/2)4n(phsio3/2)n的合成
在3l的四口可分离式烧瓶中添加1.3l由纯水将2mg的乙酸稀释而成的乙酸水溶液,一面对119g苯基三甲氧基硅烷(东京化成)、326g甲基三甲氧基硅烷(东京化成)的混合液进行搅拌,一面花30分钟缓缓进行滴加。进而搅拌2小时后,将50g的0.4wt%氨水投入至烧瓶内以进行缩聚。静置15小时后,使用薄膜过滤器(membranefilter)(孔径0.45μm,亲水性)将反应物过滤,回收固体。将所得的固体在80℃下减压干燥10小时,获得244g的作为psq的(mesio3/2)4n(phsio3/2)n(其中,n为1以上的整数)。
(合成例4)
在300m1的三口烧瓶中添加96g纯水后,利用氮气对烧瓶内进行置换。继而一面将烧瓶冰浴冷却,一面在搅拌下在20℃下滴加16.0g(118mmol)的三氯硅烷。滴加结束后,一面搅拌一面在20℃下进行2小时的水解反应及缩合反应。
经过反应时间后,使用薄膜过滤器(孔径0.45μm,亲水性)将反应物过滤,回收固体。将所得的固体在80℃下减压干燥10小时,获得6.03g的作为psq的氢倍半硅氧烷聚合物。
(合成例5)
在31的可分离式烧瓶中添加12.2g(120mmol)的36重量%浓度的盐酸及1.19kg的纯水,在搅拌下在25℃下滴加167g(1.37mol)的三甲氧基硅烷(东京化成)。滴加结束后,一面搅拌一面在25℃下进行2小时的水解反应及缩合反应。
经过反应时间后,利用薄膜过滤器(孔径0.45μm,亲水性)将反应物过滤,回收固体。将所得的固体在80℃下减压干燥10小时,获得76.0g的作为psq的氢倍半硅氧烷聚合物。
[实施例1]
<硅氧化物的制造>
在ssa-s级的氧化铝制舟皿中,载置15.0g的合成例1中所得的八苯基倍半硅氧烷后,将所述舟皿设置于真空净化式管炉ktf43n1-vps(光洋热系统(koyothermosystem)公司制造)中,作为热处理条件,在氩气环境下(高纯度氩气99.999%)一面以250ml/min的流量供给氩气,一面以4℃/min的比例升温,在1200℃下煅烧1小时,由此获得硅氧化物。
继而,使用氧化锆制球磨机将所得的硅氧化物在大气中粉碎约3小时,进而使用32μm的不锈钢制筛进行分级,由此获得最大粒径为32μm的粉粒状的硅氧化物。
将所得的硅氧化物的元素分析结果示于表1中。
<硅-钛氧化物复合物前体的制造(对硅氧化物被覆氧化钛)>
在添加有95ml的乙醇(和光纯药:特级试剂)的300m1茄型烧瓶中投入18.9g的与上述同样地获得的硅氧化物,利用超声波洗净器进行3分钟分散处理,并利用磁力搅拌器进行5分钟分散处理。分散处理后,一面进行搅拌一面滴加3.64g的四异丙氧基钛(阿法艾莎(alfaaesar)95%试剂),在室温下继续搅拌1.5小时。1.5小时后停止搅拌并使用蒸发器对溶剂进行浓缩。在溶剂挥发以后连同烧瓶一起移至减压干燥器,在60℃下加热减压干燥1小时,回收硅-钛氧化物复合物前体粉末。
<硅-钛氧化物复合物的制造>
将回收的硅-钛氧化物复合物前体粉末与所述硅氧化物的调整同样地设置于真空净化式管炉ktf43n1-vps中,作为热处理条件,在氩-氢混合气体(氢气浓度:10体积%)环境下,一面以250ml/min的流量供给氩-氢混合气体,一面以4℃/min的比例升温,在400℃下煅烧1小时。继而,进行利用研钵的破碎与利用不锈钢制筛的分级,获得19.3g的最大粒径为32μm的粉粒状的硅-钛氧化物复合物。
将硅-钛氧化物复合物的被覆氧化钛含量分析结果示于表1中。
<负极的制作>
在20g的羧甲基纤维素的2重量%水溶液中,添加3.2g的所述硅-钛氧化物复合物(1)及0.4g的乙炔黑,在烧瓶内使用搅拌子(stirringbar)混合15分钟后,以固体成分浓度成为15重量%的方式添加蒸馏水,进而搅拌15分钟而制作浆料状组合物。将所述浆料状组合物移至普莱密克斯(primix)公司制造的薄膜旋转型高速混合机(菲尔密克司(filmix)40-40型)中,以转速20m/s进行30秒钟搅拌分散。对于分散处理后的浆料,利用刮刀法将浆料以200μm的厚度涂敷于铜箔辊上。
在涂敷后进行30分钟风干,然后利用80℃的热板进行90分钟干燥。干燥后,利用2t小型精密辊压机(塞克金属(thank-metal)公司制造)压制负极片。压制后,利用φ14.50mm的电极冲压头hsng-ep冲压电极,利用玻璃管烘箱gto-200(sibata)在80℃下进行12小时以上减压干燥,制作负极。
<锂离子二次电池的制作及评价>
制作图1所示的结构的2032型硬币电池。使用金属锂作为正极3,使用微多孔性的聚丙烯制膜作为隔离片2,使用所述负极体作为负极1,关于电解液,使用在以1mol/l的比例溶解有lipf6的碳酸亚乙酯与碳酸二乙酯1:1(体积比)混合溶剂中添加5重量%的碳酸亚氟乙酯(fec)所得的溶液。
继而,实施对锂离子二次电池的电池特性的评价。将结果示于表1及表2中。
[实施例2]
在硅氧化物的制造中,代替八苯基倍半硅氧烷而使用合成例2中所得的(phsio3/2)n,将氩气环境下的煅烧温度设为1000℃,且在硅-钛氧化物复合物的制造中,将氩-氢混合气体下的煅烧温度设为600℃,除此以外,与实施例1同样地进行而获得硅-钛氧化物复合物。
将硅氧化物的元素分析结果及使用硅-钛氧化物复合物作为负极材料的电池特性的评价结果示于表1及表2中。
[实施例3]
在硅氧化物的制造中,代替八苯基倍半硅氧烷而使用合成例3中所得的(mesio3/2)4n(phsio3/2)n(其中,n为1以上的整数),将氩气环境下的煅烧时间设为5小时,且在硅-钛氧化物复合物的制造中,将氩-氢混合气体中的氢浓度设为4体积%,将所述混合气体下的煅烧温度设为200℃,除此以外,与实施例1同样地进行而获得硅-钛氧化物复合物。
将硅氧化物的元素分析结果及使用硅-钛氧化物复合物作为负极材料的电池特性的评价结果示于表1及表2中。
[实施例4]
<硅氧化物的制造>
在硅氧化物的制造中,作为psq而使用20.0g的合成例4中合成的氢倍半硅氧烷聚合物,将氩气环境下的煅烧温度设为900℃,除此以外,以与实施例1相同的方式获得18.9g的硅氧化物。将所得的硅氧化物的元素分析结果示于表1中。
<氧化钛被覆处理>
除使用通过所述方法制造的硅氧化物以外,以与实施例1相同的方式获得硅-钛氧化物复合物。所述硅-钛氧化物复合物如图2所示的扫描式电子显微镜(scanningelectronmicroscope,sem)照片所表明,作为粒径为次微米(submicron)的球状粒子的一次粒子进一步凝聚而形成粒径为几微米的二次凝聚体。
<负极的制作>
在30g的褐藻酸钠的1.5重量%水溶液中,添加3.2g的所述硅-钛氧化物复合物及0.4g的乙炔黑,在烧瓶内使用搅拌子混合15分钟后,以固体成分浓度成为13重量%的方式添加蒸馏水,进而搅拌15分钟而制作浆料状组合物。将所述浆料状组合物移至普莱密克斯(primix)公司制造的薄膜旋转型高速混合机(菲尔密克司(filmix)40-40型)中,以转速20m/s进行30秒钟搅拌分散。对于分散处理后的浆料,利用刮刀法将浆料以200μm的厚度涂敷于铜箔辊上。
涂敷后,利用80℃的热板进行90分钟干燥。干燥后,利用2t小型精密辊压机(塞克金属(thank-metal)公司制造)压制负极片。压制后,利用φ14.50mm的电极冲压头hsng-ep冲压电极,利用玻璃管烘箱gto-200(sibata)在80℃下进行16小时减压干燥,制作负极。
(锂离子二次电池的制作及评价)
除了使用所述负极体来作为负极1以外,与实施例1同样地制作锂离子二次电池,并实施电池特性的评价。
将结果示于表2中。
[实施例5]
在硅氧化物的制造中,作为psq而使用合成例5中合成的氢倍半硅氧烷聚合物,将氩气环境下的煅烧温度设为1000℃,除此以外,与实施例4同样地进行而获得硅氧化物。继而,虽与实施例4为相同的顺序,但将四异丙氧基钛的滴加量减少至一半来进行氧化钛被覆处理,将氩-氢混合气体中的氢浓度设为4体积%,除此以外,与实施例4同样地进行而获得硅-钛氧化物复合物。
对于所述硅-钛氧化物复合物,与实施例1同样地制作负极体,并对锂离子二次电池的电池特性进行评价。
将结果示于表2中。
[比较例1]
代替psq而使用如下的一氧化硅粉末:通过使用32μm的不锈钢制筛将市售的一氧化硅(奥德里奇(aldrich)公司制造的小于325目(under325mesh))进行分级而最大粒径为32μm,并将煅烧温度设为900℃,除此以外,与实施例4同样地进行而获得硅氧化物。
除使用所述硅氧化物以外,以与实施例4相同的方式获得硅-钛氧化物复合物。
对于所述硅-钛氧化物复合物,与实施例4同样地制作负极体,并对锂离子二次电池的电池特性进行评价。
[比较例2]
在比较例1中,代替氩-氢混合气体而使用未混合氢的仅氩的气体来进行热处理,除此以外,与比较例1同样地进行而获得硅-钛氧化物复合物。
对于所述硅-钛氧化物复合物,与实施例4同样地制作负极体,并对锂离子二次电池的电池特性进行评价。
[参考例1]
在实施例1中,将制造硅-钛氧化物复合物时的热处理温度设为200℃,另外代替氩-氢混合气体而使用未混合氢的仅氩的气体来进行热处理,除此以外,与实施例1同样地进行而获得硅-钛氧化物复合物。
对于所述硅-钛氧化物复合物,与实施例1同样地制作负极体,并对锂离子二次电池的电池特性进行评价。
本发明的实施例1~实施例5、比较例1~比较例2及参考例1的硅氧化物的元素分析结果及采用使用各负极活性物质所制作的负极的电池特性的评价结果如表1及表2所示。
[表1]
[表2]
根据所述结果,关于对由本发明中使用的psq所制造的硅氧化物在还原性气体环境下进行氧化钛被覆处理而成者,均是初期电容与第100次的放电电容均具有较现有的碳系负极活性物质更高的电容,而且电容降低少,具有高的电容维持率、即充放电循环劣化得到极度抑制的良好的循环特性,可作出以下评价:通过本发明的方法制造的负极活性物质、负极及锂离子二次电池可耐实用。
产业上的可利用性
通过使用由本发明的方法所得的锂离子二次电池用负极活性物质形成负极而用于锂离子二次电池,可获得具有优异的电容且具有优异的充放电特性及循环特性的锂离子二次电池,例如本发明为在电池的领域、特别是二次电池的领域中有用的技术。
符号的说明
1:负极
2:隔离片
3:锂对极
- 还没有人留言评论。精彩留言会获得点赞!