包含层状钠和金属的氧化物的电极材料,包含其的电极及其在电化学中的用途的制作方法
包含层状钠和金属的氧化物的电极材料,包含其的电极及其在电化学中的用途
1.相关申请
2.本申请根据适用法律要求在2018年10月2日提交的美国临时专利申请62/740185的优先权,其内容通过引用整体并出于所有目的并入本文。
技术领域
3.本申请涉及电化学活性材料及其在电化学应用中的用途的领域。更具体地,本申请总体上涉及包含层状钠金属氧化物作为电化学活性材料的电极材料,包含它们的电极,它们的制造方法及它们在电化学电池中的用途。
4.发明背景
5.式limo2(m=过渡金属)的层状锂金属氧化物如具有层状结构的氧化物像锂钴氧化物(licoo2)和锂镍氧化物(linio2)是商业上用于锂离子电池组(lib)中的正极材料。层状limo2可以根据其堆叠几何形状进行分类。不同类型的堆的不同之处在于,氧化层的堆叠顺序会改变(mo2)片的排列以及锂离子所占据位置的几何形状。锂离子的氧环境可以是例如八面体的(o)、棱形的(p)或四面体的(t)。层状limo2的特征还可以在于在单元电池中发现的mo2片的数量。层状limo2的结构会显著影响材料的电化学性能,例如其容量、循环性以及充放电速率。层状p2和o3型结构是例如在电化学电池中使用所关注的。
6.当前使用的包含层状氧化物作为电化学活性材料的电极材料的主要缺点之一是它们的高生产成本。例如,锂价格的上涨可能会给libs市场份额的增长带来问题。实际上,锂已用于常规lib的几个组件中,例如在正极和负极以及电解质中。因此,供应问题和锂的成本对于影响其扩展到某些商业可再生能源应用的主要因素至关重要。
7.因此,需要开发新的电极材料。例如,电极材料包含p2和/或o3型层状氧化物作为电化学活性材料,排除了常规层状氧化物材料的一个或多个缺点。
技术实现要素:
8.根据一个方面,本技术涉及包含电化学活性材料的电极材料,所述电化学活性材料包括式na
x
mo2的层状钠金属氧化物,其中0.5≤x≤1.0,m选自co,mn,fe,ni,ti,cr,v,cu,sb及其组合。
9.在一个实施方案中,电化学活性材料包括选自以下的层状钠金属氧化物:
10.‑
式na
x
mo2的p2型层状钠金属氧化物,其中x是使得0.5≤x≤0.8的数,m选自co,mn,fe,ni,ti,cr,v,cu及其组合;和
11.‑
式na
x
mo2的o3型层状钠金属氧化物,其中x是使得0.8≤x≤1.0的数,m选自co,mn,fe,ni,ti,cr,v,cu,sb及其组合。
12.在另一个实施方案中,电化学活性材料包括式na
x
m'1‑
y
m
y
o2的层状钠金属氧化物,其中x和m如本文所定义,y为使得0≤y≤1.0的数,m'不同于m且选自co,mn,fe,ni,ti,cr,v,cu,sb及其组合。
13.在另一个实施方案中,电化学活性材料包括式na
x
m'1‑
y
mn
y
o2的层状钠金属氧化物,其中x如本文所定义,其中y为使得0≤y≤1.0的数,m'选自co,fe,ni,ti,cr,v,cu,sb及其组合。
14.在另一个实施方案中,电极材料还包含选自炭黑,乙炔黑,石墨,石墨烯,碳纤维,碳纳米纤维,碳纳米管及其组合的电子导电材料。
15.在另一个实施方案中,电极材料还包含选自聚醚型聚合物粘合剂,氟化聚合物和水溶性粘合剂的粘合剂。
16.根据另一方面,本技术涉及电极,其包含在集电体上的本文所定义的电极材料。在一实施方案中,电极是正极。
17.根据另一方面,本技术涉及包含负极、正极和电解质的电化学电池,其中正极如本文所定义。在一实施方案中,负极包括金属锂。或者,负极包括金属钠。
18.在另一实施方案中,电解质是包含在溶剂中的盐的液体电解质。替代地,电解质是凝胶电解质,其包含在溶剂和任选的溶剂化聚合物中的盐。根据另一替代方案,电解质是包含在溶剂化聚合物中的盐的固体聚合物电解质。在一个实施方案中,盐是锂盐。或者,盐是钠盐。
19.根据另一方面,本技术涉及电池组,其包含至少一个如本文所定义的电化学电池。在一个实施方案中,电池组选自锂离子电池组和钠离子电池组。
附图说明
20.图1是使用固态法获得的式na
0.5
coo2的p2型层状钠钴氧化物粉末的x射线衍射图。
21.图2是使用固态法获得的式nani
0.4
co
0.2
mn
0.4
o2的混合o3型混合层状钠过渡金属氧化物粉末的x射线衍射图。
22.图3显示了电池1的充电和放电曲线,充电和放电在0.1c下进行,并在25℃的温度下相对于li/li
+
记录。
23.图4显示了电池1在不同循环速率下的充电和放电曲线,充电和放电分别在0.1c,0.2c,0.5c,1c,2c和4c下进行,并在25℃的温度下相对于li/li
+
记录。
24.图5显示了表示容量(mah/g)与循环数的关系的图,即电池1的老化曲线。长循环或循环稳定性实验在1c的恒定充电/放电电流下进行,结果在25℃的温度下相对于li/li
+
记录。
25.图6显示了电池2的充电和放电曲线。充电和放电在0.3c在2.0
‑
4.4v相对于li/li
+
在50℃的温度下进行。
26.图7显示了电池2的充电和放电曲线。充电和放电在0.3c在2.0
‑
4.4v相对于li/li
+
在80℃的温度下进行。
27.图8显示了电池3的充电和放电曲线。充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃的温度下进行。
28.图9显示了电池3在不同循环速率下的充电和放电曲线,充电和放电在0.1c,0.2c,0.5c,1c,2c和4c下进行并在25℃的温度下相对于li/li
+
记录。
29.图10显示了表示电池3的容量(mah/g)与循环数的关系的图。长循环实验在2c的恒定充电/放电电流下进行,并在25℃的温度下相对于li/li
+
记录。
30.图11显示了电池4的初始充电和放电曲线。充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃的温度下进行。
31.图12显示了电池5的两个充电和放电曲线,分别是第一个循环和第五个循环。充电和放电在0.3c在2.0
‑
4.0v相对于li/li
+
在80℃的温度下进行。
32.图13显示了电池6的充电和放电曲线,充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃温度下进行。
33.图14显示了电池7的充电和放电曲线,充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃温度下进行。
34.图15显示了电池8的充电和放电曲线,充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃温度下进行。
35.图16显示了电池9的充电和放电曲线,充电和放电在0.1c在2.0
‑
4.5v相对于li/li
+
在25℃温度下进行。
36.图17显示了电池10的充电和放电曲线,充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃温度下进行。
37.图18显示了电池11的充电和放电曲线,充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃温度下进行。
38.图19显示了表示电池11的容量(mah/g)与循环数的关系的图。长循环实验在0.1c的恒定充电/放电电流下进行,结果在25℃的温度下相对于li/li
+
记录。
39.发明详述
40.给出以下详细描述和实施例仅出于说明性目的,不应解释为进一步限制本发明的范围。
41.本文中使用的所有技术和科学术语和表达具有与本领域技术人员有关本技术的通常理解的定义相同的定义。然而,下面提供了一些使用的术语和表达的定义。
42.当在本文中使用术语“大约”或其等同术语“约”时,其表示在附近或周围。例如,当相对于数值使用术语“大约”或“约”时,其相对于标称值上下变化10%。该术语还可以考虑例如测量设备的实验误差或四舍五入。
43.当在本申请中提及值的范围时,除非另外指出,否则该范围的下限和上限始终包括在定义中。
44.本技术涉及钠和至少一种金属元素的层状氧化物作为电化学活性材料的用途。钠和至少一种金属元素的层状氧化物具有p2型或o3型堆。
45.在一个实例中,金属元素是金属,例如过渡金属,后过渡金属,准金属,碱金属,碱土金属或其组合。例如,金属选自co,mn,fe,ni,ti,cr,v,cu,sb及其至少两种的组合。
46.在一个实例中,电化学活性材料包括式na
x
mo2的层状钠金属氧化物,其中x为使得0.5≤x≤1.0的数,m选自co,mn,fe,ni,ti,cr,v,cu,sb及其组合。
47.在另一个实例中,电化学活性材料包括式na
x
mo2的p2型层状钠金属氧化物,其中x为使得0.5≤x≤0.8的数,m选自co,mn,fe,ni,ti,cr,v,cu及其组合。
48.在另一个实例中,电化学活性材料包括式na
x
mo2的o3型层状钠金属氧化物,其中x为使得0.8≤x≤1.0的数,m选自co,mn,fe,ni,ti,cr,v,cu,sb及其组合。
49.在另一个实例中,电化学活性材料是式na
x
coo2的层状钠钴氧化物,其中x如本文所
定义。例如,层状钠钴氧化物具有p2型堆。层状钠钴氧化物的实例具有式na
0.5
coo2。
50.在另一个实例中,电化学活性材料是式na
x
mno2的层状钠锰氧化物,其中x如本文所定义。
51.电化学活性材料的另一个实例包括式na
x
m'1‑
y
m
y
o2的混合层状氧化物,其中x和m如本文所定义,y为使得0≤y≤1.0的数,m'选自co,mn,fe,ni,ti,cr,v,cu,sb及其组合,其中m和m'不同。
52.例如,电化学活性材料包括式na
x
m'1‑
y
mn
y
o2的钠、锰和金属的混合层状氧化物,其中x和y如本文所定义,m'选自co,fe,ni,ti,cr,v,cu,sb及其组合。例如,电化学活性材料选自式na
x
(nico)1‑
y
mn
y
o2,na
x
co1‑
y
mn
y
o2,na
x
ni1‑
y
mn
y
o2和na
x
(coti)1‑
y
mn1‑
y
o2的混合层状氧化物,其中x和y如所定义。电化学活性材料的非限制性实例包括na
0.5
coo2,na
0.67
coo2,na
0.67
co
0.67
mn
0.33
o2,na
0.67
ni
0.33
mn
0.67
o2,na
0.67
co
0.6
mn
0.4
o2,na
0.67
co
0.55
mn
0.45
o2,na
0.67
co
0.5
mn
0.5
o2,na
0.67
co
0.50
mn
0.33
ti
0.17
o2,na
0.6
mno2,nani
0.4
co
0.2
mn
0.4
o2和nani
0.33
fe
0.33
mn
0.33
o2。
53.电化学活性材料可任选地掺杂有其他元素或以较小量包含的杂质,例如以调节或优化其电化学性能。在某些情况下,电化学活性材料可以通过用其他离子部分取代金属(m)而掺杂。例如,电化学活性材料可以掺杂有过渡金属(例如fe,co,ni,mn,ti,cr,cu,v)和/或过渡金属以外的金属(例如mg,al,sb)。
54.本文所述的电化学活性材料优选基本上不含锂。例如,电化学活性材料包含小于2重量%,小于1重量%,小于0.5重量%,小于0.1重量%,小于0.05重量%或小于0.01重量%的锂。因此,本电化学活性材料与相应的p2型或o3型锂金属氧化物结构相比可以潜在地降低生产成本。电化学活性材料还可以保持与相应的p2型或o3型锂金属氧化物结构相同的结构,并具有相似的电化学性能。
55.本技术还涉及包含如本文定义的电化学活性材料的电极材料。在一个实例中,本文所述的电极材料可以进一步包含电子导电材料。电子导电材料的非限制性实例包括炭黑,ketjen
tm
碳,super p
tm
碳,乙炔黑,shawinigan碳,denka
tm
碳黑,石墨,石墨烯,碳纤维(例如气相生长碳纤维(vgcfs)),碳纳米纤维,碳纳米管或其至少两种的组合。根据一个实例,电子导电材料是ketjen
tm
碳。根据一种替代方案,电子导电材料是super p
tm
碳。根据另一替代方案,电子导电材料是vgcf。
56.本文所述的电极材料还可以进一步包含粘合剂。例如,粘合剂根据其与电化学电池的各种元件的相容性选择。可以考虑任何已知的相容性粘合剂。例如,粘合剂选自聚醚型聚合物粘合剂,氟化聚合物和水溶性粘合剂(水溶性)。根据一个实例,粘合剂是氟化聚合物,例如聚偏二氟乙烯(pvdf)或聚四氟乙烯(ptfe)。根据另一个实例,粘合剂是水溶性粘合剂,例如丁苯橡胶(sbr),丙烯腈
‑
丁二烯橡胶(nbr),氢化nbr(hnbr),表氯醇橡胶(chr)或丙烯酸酯橡胶(acm),任选地包含增稠剂如羧甲基纤维素(cmc),或聚合物如聚(丙烯酸)(paa),聚(甲基丙烯酸)(pmma)或它们的组合。根据一个实例,粘合剂是聚醚型聚合物粘合剂。例如,聚醚型聚合物粘合剂是线性、支化和/或交联的且基于聚环氧乙烷(peo)、聚环氧丙烷(ppo)或两者的组合(例如eo/po共聚物),任选地包含可交联的单元。在一个感兴趣的变型中,粘合剂是pvdf或本文定义的聚醚型聚合物。
57.本文所述的电极材料可进一步任选地包含另外的组分或添加剂,例如无机颗粒,
玻璃或陶瓷颗粒,离子导体,盐(例如锂盐)和其他类似的添加剂。
58.本技术还涉及电极,其包含在集电体(例如铝,铜)上的本文所限定的电极材料。替代地,电极可以是自支撑的。在关注的一个变型中,电极是正极。
59.本技术还涉及包含负极、正极和电解质的电化学电池,其中正极如本文所定义。
60.在一个实例中,负极或反电极的电化学活性材料可以选自所有已知的相容性材料。例如,可以根据其与本文限定的电化学活性材料的电化学相容性选择负极的电化学活性材料。例如,负极的电化学活性材料可以包括碱金属膜,例如金属锂膜,金属钠膜或包含这些中的至少一种的合金膜。
61.还根据其与电化学电池的各种元件的相容性选择电解质。可以考虑任何类型的相容性电解质。根据一个实例,电解质是包含在溶剂中的盐的液体电解质。根据一个替代方案,电解质是凝胶电解质,其包含在溶剂和任选的溶剂化聚合物中的盐。根据另一替代方案,电解质是包含在溶剂化聚合物中的盐的固体聚合物电解质。
62.该盐优选是离子盐如锂盐或钠盐。锂盐的非限制性实例包括六氟磷酸锂(lipf6),双(三氟甲磺酰基)酰亚胺锂(litfsi),双(氟磺酰基)酰亚胺锂(lifsi),2
‑
三氟甲基
‑
4,5
‑
二氰基咪唑锂(litdi),4,5
‑
二氰基
‑
1,2,3
‑
三唑锂(lidcta),双(五氟乙基磺酰基)酰亚胺锂(libeti),四氟硼酸锂(libf4),双(草酸根合)硼酸锂(libob),硝酸锂(lino3),氯化锂(licl),溴化锂(libr),氟化锂(lif),高氯酸锂(liclo4),六氟砷酸锂(liasf6),三氟甲磺酸锂(liso3cf3)(litf),氟代烷基磷酸锂li[pf3(cf2cf3)3](lifap),四(三氟乙酰氧基)硼酸锂li[b(ococf3)4](litfab),双(1,2
‑
苯二醇基(2
‑
)
‑
o,o')硼酸锂[b(c6o2)2](libbb)和它们的组合。根据关注的第一变型,锂盐是lipf6。根据关注的第二变型,锂盐是lifsi。根据关注的第三变型,锂盐是litfsi。钠盐的非限制性实例包括上述盐,其中锂离子被钠离子替代。
[0063]
如果存在于电解质中,则溶剂可以是极性非质子非水性溶剂。溶剂的非限制性实例包括环状碳酸酯如碳酸亚乙酯(ec),碳酸亚丙酯(pc),碳酸亚丁酯(bc)和碳酸亚乙烯酯(vc);无环碳酸酯如碳酸二甲酯(dmc),碳酸二乙酯(dec),碳酸乙基甲基酯(emc)和碳酸二丙酯(dpc);内酯如γ
‑
丁内酯(γ
‑
bl)和γ
‑
戊内酯(γ
‑
vl);无环醚如1,2
‑
二甲氧基乙烷(dme),1,2
‑
二乙氧基乙烷(dee),乙氧基甲氧基乙烷(eme),三甲氧基甲烷和乙基单甘醇二甲醚;环醚如四氢呋喃,2
‑
甲基四氢呋喃,1,3
‑
二氧戊环和二氧戊环衍生物;以及其他溶剂如二甲亚砜,甲酰胺,乙酰胺,二甲基甲酰胺,乙腈,丙腈,硝基甲烷,磷酸三酯,环丁砜,甲基环丁砜,碳酸亚丙酯衍生物及其混合物。
[0064]
电解质的实例包括溶解在非水溶剂混合物如碳酸亚乙酯和碳酸二乙酯的混合物(ec/dec)(按体积计[3:7])或碳酸亚乙酯和碳酸二甲酯的混合物(ec/dmc)(按体积计[4:6])中的六氟磷酸锂(lipf6)。
[0065]
当电解质是凝胶电解质或聚合物凝胶电解质时,凝胶聚合物电解质可包括例如聚合物前体和盐(例如,如上所定义的盐)、溶剂以及聚合和/或交联引发剂(如有必要)。凝胶电解质的非限制性实例包括但不限于在pct专利申请wo2009/111860(zaghib等人)和wo2004/068610(zaghib等人)的中描述的凝胶电解质。
[0066]
电解质也可以是包含在溶剂化聚合物中的盐的固体聚合物电解质(spe)。可以考虑任何类型的已知相容性spe。例如,根据其与电化学电池的各种元件的相容性选择spe。例如,根据其与锂和/或钠的相容性选择spe。spe通常可以包含盐以及一种或多种固体极性聚
合物,其任选是交联的。可以使用聚醚型聚合物,例如基于聚环氧乙烷(peo)的那些,但是也已知几种其他相容性聚合物用于制备spe,并且也可以考虑使用。根据一个实例,该聚合物可以进一步交联。这样的聚合物的实例包括支化聚合物,例如星形聚合物或梳状聚合物,例如pct专利申请wo2003/063287(zaghib等人)中描述的那些。
[0067]
如上所定义的凝胶电解质或液体电解质也可以浸渍隔膜如聚合物隔膜。隔膜的非限制性实例包括聚乙烯(pe),聚丙烯(pp),纤维素,聚四氟乙烯(ptfe),聚偏二氟乙烯(pvdf)和聚丙烯
‑
聚乙烯
‑
聚丙烯(pp/pe/pp)膜。例如,隔膜是celgard
tm
型的商业聚合物隔膜。
[0068]
电解质还可任选包含其他组分或添加剂,例如离子导体,无机颗粒,玻璃或陶瓷颗粒,例如纳米陶瓷(例如al2o3,tio2,sio2和其他类似的化合物)和其他类似的添加剂。
[0069]
本技术通常还涉及电池组,其包括至少一个如本文所定义的电化学电池。例如,所述电池组选自锂电池组,锂离子电池组,钠电池组和钠离子电池组。根据感兴趣的一个变型,电池组是锂电池组或锂离子电池组。
实施例
[0070]
下列实施例仅用于说明目的,不应解释为进一步限制本发明的范围。通过参考附图将更好地理解这些实施例。
[0071]
实施例1:电化学活性材料的合成
[0072]
使用固态反应技术制备了式na
0.5
coo2,na
0.67
coo2,na
0.67
co
0.67
mn
0.33
o2,na
0.67
ni
0.33
mn
0.67
o2,na
0.67
co
0.6
mn
0.4
o2,na
0.67
co
0.55
mn
0.45
o2,na
0.67
co
0.5
mn
0.5
o2,na
0.67
co
0.50
mn
0.33
ti
0.17
o2,na
0.6
mno2,nani
0.4
co
0.2
mn
0.4
o2和nani
0.33
fe
0.33
mn
0.33
o2的层状氧化物。称量各个前体(na2co3和金属氧化物如mn2o3,co2o3,nio,fe2o3和tio2)以获得所需的化学计量。通过研磨和混合前体粉末来制备样品。然后将研磨的和混合的前体粉末放入烘箱中,在空气或氧气气氛下在700℃
‑
1000℃下加热5
‑
24小时。
[0073]
实施例2:电化学活性材料的表征
[0074]
a)粉末x射线衍射(xrd)
[0075]
通过对实施例1中制备的p2型和o3型层状钠金属氧化物结构进行x射线衍射研究了电化学活性材料的原子和分子结构。图1显示了p2型层状na
0.5
coo2粉末的x射线衍射图,图2显示了o3型层状nani
0.4
co
0.2
mn
0.4
o2粉末的x射线衍射图。
[0076]
实施例3:电化学性能
[0077]
将所有电池组装在具有表1中指示的组件和负极(包括铝集电体上的金属锂膜)的2032型纽扣电池外壳中。包含液体电解质的电池用celgard
tm
隔膜组装,该隔膜用lipf6在ec/dec混合物([3:7]体积)或ec/dmc混合物([4:6]体积)中的1m溶液浸渍。将包含固体聚合物电解质的电池与包含lifsi或litfsi的spe组装在一起。
[0078]
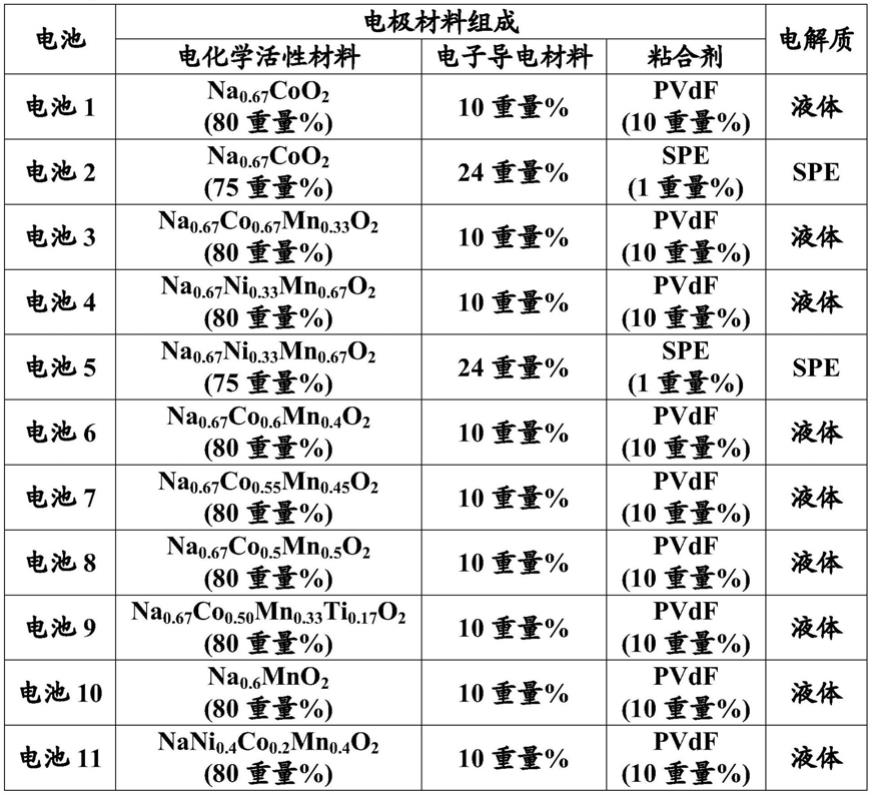
表1.电池配置
[0079][0080]
a)p2型na
0.67
coo2的电化学行为
[0081]
该实施例说明了在实施例1中制备的p2型层状na
0.67
coo2材料的电化学行为。
[0082]
图3显示了电池1的充电和放电曲线。充电和放电在0.1c下进行,并在25℃的温度下相对于li/li
+
记录。电池1的容量为约104mah/g。
[0083]
图4显示了电池1在不同循环速率下的充电和放电曲线。充电和放电在0.1c,0.2c,0.5c,1c,2c和4c下进行,并在25℃的温度下相对于li/li
+
记录。在4c的循环速率下,电池1的容量为约92mah/g,随着循环速率从0.5c增加到4c,有效显示了87%的容量保持率。
[0084]
图5显示了表示电池1的容量(mah/g)与循环数的关系的图。长循环实验在1c的恒定充电/放电电流下进行。结果在25℃的温度下相对于li/li
+
记录。图5显示了200个循环后的容量保持率为约97%。
[0085]
粘合剂选择和循环温度的影响如图6和7所示。
[0086]
图6显示了电池2的充电和放电曲线。充电和放电是在0.3c在2.0
‑
4.4v相对于li/li
+
在50℃的温度下进行的。电池2的容量为约107mah/g。
[0087]
图7显示了电池2的充电和放电曲线。充电和放电是在0.3c在2.0
‑
4.4v相对于li/li
+
在80℃的温度下进行的。电池2的容量为约107mah/g。
[0088]
b)p2型na
0.67
co
0.67
mn
0.33
o2的电化学行为
[0089]
该实施例说明了在实施例1中制备的p2型层状na
0.67
co
0.67
mn
0.33
o2材料的电化学行
为。
[0090]
图8显示了电池3的充电和放电曲线。充电和放电是在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃的温度下进行的。电池3的容量为约150mah/g。
[0091]
图9显示了电池3在不同循环速率下的充电和放电曲线。充电和放电在0.1c,0.2c,0.5c,1c,2c和4c下进行,并在25℃的温度下相对于li/li
+
记录。在4c的循环速率下,电池3的容量为约121mah/g,随着循环速率从0.1c升高至4c,有效显示了80%的容量保持率。
[0092]
图10显示了表示电池3的容量(mah/g)与循环数的关系的图。长循环实验是在2c的恒定充电/放电电流下进行的。结果在25℃的温度下相对于li/li
+
记录。图10显示了100个循环后的容量保持率为约93.4%。
[0093]
c)p2型na
0.67
ni
0.33
mn
0.67
o2的电化学行为
[0094]
该实施例说明了在实施例1中制备的p2型层状na
0.67
ni
0.33
mn
0.67
o2材料的电化学行为。
[0095]
图11显示了电池4的初始充电和放电曲线。充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃的温度下进行。电池4的容量为约182mah/g。
[0096]
图12显示了电池5的两个充电和放电曲线,即第一循环和第五循环。充电和放电在0.3c在2.0
‑
4.0v相对于li/li
+
在80℃的温度下进行。电池5的容量为约120mah/g。
[0097]
d)p2型na
0.67
co
0.6
mn
0.4
o2的电化学行为
[0098]
该实施例说明了在实施例1中制备的p2型层状na
0.67
co
0.6
mn
0.4
o2材料的电化学行为。
[0099]
图13显示了电池6的充电和放电曲线。充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃的温度下进行。电池6的容量为约142mah/g。
[0100]
e)p2型na
0.67
co
0.55
mn
0.45
o2的电化学行为
[0101]
该实施例说明了如实施例1中制备的p2型层状na
0.67
co
0.55
mn
0.45
o2材料的电化学行为。
[0102]
图14显示了电池7的充电和放电曲线。充电和放电在0.1c在2.0
‑
4.4相对于li/li
+
在25℃的温度下进行。电池7的容量为约110mah/g。
[0103]
f)p2型na
0.67
co
0.5
mn
0.5
o2的电化学行为
[0104]
该实施例说明了在实施例1中制备的p2型层状na
0.67
co
0.5
mn
0.5
o2材料的电化学行为。
[0105]
图15显示了电池8的充电和放电曲线。充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃的温度下进行。电池8的容量为约114mah/g。
[0106]
g)p2型na
0.67
co
0.50
mn
0.33
ti
0.17
o2的电化学行为
[0107]
该实施例说明了如实施例1中制备的p2型层状na
0.67
co
0.50
mn
0.33
ti
0.17
o2材料的电化学行为。
[0108]
图16显示了电池9的充电和放电曲线。充电和放电在0.1c在2.0
‑
4.5v相对于li/li
+
在25℃的温度下进行。电池9的容量为约137mah/g。
[0109]
h)p2型na
0.60
mno2的电化学行为
[0110]
该实施例说明了在实施例1中制备的p2型层状na
0.60
mno2材料的电化学行为。
[0111]
图17显示了电池10的充电和放电曲线。充电和放电在0.1c在2.0
‑
4.4v相对于li/
li
+
在25℃的温度下进行。电池10的容量为约73mah/g。
[0112]
i)o3型nani
0.4
co
0.2
mn
0.4
o2的电化学行为
[0113]
该实施例说明了在实施例1中制备的o3型层状nani
0.4
co
0.2
mn
0.4
o2材料的电化学行为。
[0114]
图18显示了电池11的充电和放电曲线。充电和放电在0.1c在2.0
‑
4.4v相对于li/li
+
在25℃的温度下进行。电池11的容量为约118mah/g。
[0115]
图19显示了表示电池11的容量(mah/g)与循环数的关系的图。长循环实验是在0.1c的恒定充电/放电电流下进行的。结果在25℃的温度下相对于li/li
+
记录。图19显示了50个循环后的良好容量保持率。
[0116]
在不脱离本发明范围的情况下,可以对上述任何实施例进行多种修改。为了所有目的,本申请中引用的参考文献、专利或科学文献文件通过引用整体并入本文。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1