一种LiAl5O8纳米线的制备方法、复合固态电解质、锂金属电池
一种lial5o8纳米线的制备方法、复合固态电解质、锂金属电池
技术领域
1.本发明涉及电池材料技术领域,尤其涉及一种lial5o8纳米线的制备方法、复合固态电解质、锂金属电池。
背景技术:
2.便携式电子器件、电动汽车和储能电网的快速发展推动了高能量密度的二次电池的开发。锂金属电池,因锂金属(li)负极具有高理论比容量(3860mah
·
g
‑1),低密度(0.59g
·
cm
‑3)和低还原电位(相对于标准氢电位为
‑
3.04v)等优点,使其成为一种极具应用前景的高比能量密度二次电池
1.。然而,在实际应用中,液态有机电解液中不稳定的电解质膜(sei膜)和生长不受控制的枝晶,严重限制了锂金属电池的发展。首先,锂金属在沉积和溶解过程中存在严重的体积变化,很难形成稳定的sei膜。因此,电解液与锂金属反复反应,导致库仑效率低,容量迅速下降。其次,在充放电过程中由于锂的不均匀沉积形成锂枝晶,导致“死锂”的形成和极化的增加,甚至会穿透电池隔膜接触阴极,造成电池内部短路,从而引起热失控甚至爆炸
2.。因此,必须消除这些障碍才能实现锂金属电池的安全、高库伦效率和长循环寿命。
3.近年来,研究人员为解决上述问题做了大量工作,如优化电解液的组成
[3
‑
6]
、构建界面保护层
[7
‑
10]
和构筑三维复合锂金属负极
[11
‑
14]
。此外,固态电解质的快速发展为锂金属电池的安全问题提供了一个重要的解决途径,因为固态电解质具有较高的剪切模量和硬度,有望抵抗锂枝晶的侵入
[15]
。固态电解质类型包括氧化物、硫化物、薄膜和聚合物
[16]
。氧化物固态电解质如li
3.3
la3zr2o
12
(llzo)和 li
3.3
la
0.56
tio3(llto),因其离子电导率高、机械强度高、电化学稳定性好而得到广泛研究。但同时也面临着高能耗、非均相、对空气中水分和二氧化碳不稳定等问题。因此,开发成本低、合成简单、储存方便的新型固态电解质是非常必要的。此外,当与锂金属直接接触时,固态电解质通常会还原为更稳定的化合物。例如,根据第一性原理密度泛函理论(dft)计算,llzo的还原极限为0.05v(或0.07v),llzo可能的还原产物有zr、la2o3、li8zro6、zr3o和li2o
[18,19]
。之前的大部分研究工作采用了涂层等策略
[20,21]
,以避免固态电解质在界面上发生副反应,使其适用于固态锂金属电池。然而,利用副产物直接改善固态电解质与锂金属界面相容性的例子很少。
[0004]
lial5o8一直被用作具有光学特性的荧光粉
[22]
,并曾经在锂金属负极和石榴石型固态电解质之间的氧化铝涂层中被检测到
[23]
。最近,根据dft计算提出 lial5o8是一种具有高锂离子(li
+
)迁移率的潜在锂离子导体。计算结果表明,在低电极电位下锂间隙是主要的扩散载体,而在高电极电位下锂空位是主要的扩散载体。通过计算预测,lial5o8涂层的稳定电压范围为0.08~4.08v vs li/li
+
。当电压低于0.8v时,lial5o8会被还原为铝(al),在较低的电压下会进一步形成li
x
al
y
合金。大量研究证明al可以诱导li
+
均匀地沉积在li金属负极上,从而抑制li枝晶的生长
[25
‑
27]
。然而如果没有有效的调控,这些严重的副作用会破坏lial5o8固态电解质与电极的界面接触。事实上,lial5o8的上述副反应在实验中仍未得到证实,因为传统固相烧结方法难以制备该材料
[28]
。因此,开发一种大规模制备lial5o8的新方
法,然后仔细调节lial5o8固态电解质与锂金属负极的界面以显著降低副反应是非常重要的。
[0005]
参考文献:
[0006]
[1]j.m.tarascon,m.armand,nature 2001,414,359.
[0007]
[2]x.b.cheng,r.zhang,c.z.zhao,q.zhang,chem.rev.2017,117, 10403.
[0008]
[3]z.zeng,v.murugesan,k.s.han,x.jiang,y.cao,l.xiao,x.ai,h.yang, j.
‑
g.zhang,m.l.sushko,j.liu,nat.energy 2018,3,674.
[0009]
[4]x.q.zhang,x.chen,x.b.cheng,b.q.li,x.shen,c.yan,j.q.huang, q.zhang,angew.chem.
‑
int.edit.2018,57,5301.
[0010]
[5]s.lee,k.park,b.koo,c.park,m.jang,h.lee,h.lee,adv.funct. mater.2020,30,2003132.
[0011]
[6]q.k.zhang,s.liu,z.h.lin,k.wang,m.chen,k.xu,w.s.li,nano energy 2020,74,11.
[0012]
[7]a.c.kozen,c.
‑
f.lin,a.j.pearse,m.a.schroeder,x.han,l.hu,s.
‑
b. lee,g.w.rubloff,m.noked,acs nano 2015,9,5884.
[0013]
[8]e.k.jong,j.ahn,s.yoon,k.y.cho,adv.funct.mater.2019,29, 1905078.
[0014]
[9]p.b.zhai,l.x.liu,x.k.gu,t.s.wang,y.j.gong,adv.energy mater.2020,32,2001257.
[0015]
[10]h.chen,a.pei,d.c.lin,j.xie,a.k.yang,j.w.xu,k.x.lin,j.y. wang,h.s.wang,f.f.shi,d.boyle,y.cui,adv.energy mater.2019,9, 1900858.
[0016]
[11]y.liu,d.lin,z.liang,j.zhao,k.yan,y.cui,nat.commun.2016,7, 10992.
[0017]
[12]y.zhang,w.luo,c.w.wang,y.j.li,c.j.chen,j.w.song,j.q.dai, e.m.hitz,s.m.xu,c.p.yang,y.b.wang,l.b.hu,proc.natl.acad.sci.u.s. a.2017,114,3584.
[0018]
[13]d.c.lin,y.y.liu,z.liang,h.w.lee,j.sun,h.t.wang,k.yan,j. xie,y.cui,nat.nanotechnol.2016,11,626.
[0019]
[14]y.g.zhou,x.zhang,y.ding,j.bae,x.l.guo,y.zhao,g.h.yu,adv. mater.2020,32,2003920.
[0020]
[15]a.manthiram,x.w.yu,s.f.wang,nat.rev.mater.2017,2,16.
[0021]
[16]r.s.chen,q.h.li,x.q.yu,l.q.chen,h.li,chem.rev.2020,120, 6820.
[0022]
[17]z.gao,h.sun,l.fu,f.ye,y.zhang,w.luo,y.huang,adv.mater. 2018,30,1705702.
[0023]
[18]y.z.zhu,x.f.he,y.f.mo,j.mater.chem.a 2016,4,3253.
[0024]
[19]l.j.miara,w.d.richards,y.e.wang,g.ceder,chem.mater.2015,27, 4040.
[0025]
[20]y.l.liu,q.sun,y.zhao,b.q.wang,p.kaghazchi,k.r.adair,r.y.li, c.zhang,j.r.liu,l.y.kuo,y.f.hu,t.k.sham,l.zhang,r.yang,s.g.lu,x. p.song,x.l.sun,acs appl.mater.interfaces 2018,10,31240.
[0026]
[21]l.z.sang,k.l.bassett,f.c.castro,m.j.young,l.chen,r.t.haasch, j.w.elam,v.p.dravid,r.g.nuzzo,a.a.gewirth,chem.mater.2018,30,8747.
[0027]
[22]v.singh,t.k.gundu rao,j.solid state chem.2008,181,1387.
[0028]
[23]x.han,y.gong,k.fu,x.he,g.t.hitz,j.dai,a.pearse,b.liu,h. wang,g.rubloff,y.mo,v.thangadurai,e.d.wachsman,l.hu,nature mater. 2017,16,572.
[0029]
[24]s.mo,b.zhang,k.zhang,s.li,f.pan,pccp 2019,21,13758.
[0030]
[25]z.lu,w.li,y.long,j.liang,q.liang,s.wu,y.tao,z.weng,w.lv, q.
‑
h.yang,adv.funct.mater.2020,30,1907343.
[0031]
[26]h.zhong,y.wu,f.ding,l.sang,y.mai,electrochim.acta 2019,304, 255.
[0032]
[27]k.k.fu,y.h.gong,b.y.liu,y.z.zhu,s.m.xu,y.g.yao,w.luo, c.w.wang,s.d.lacey,j.q.dai,y.n.chen,y.f.mo,e.wachsman,l.b.hu, sci.adv.2017,3,11.
[0033]
[28]r.ribeiro,g.g.silva,n.d.s.mohallem,electrochim.acta 2001,46, 1679.
技术实现要素:
[0034]
本发明旨在至少解决现有技术中存在的技术问题之一。为此,本发明提出一种lial5o8纳米线的制备方法,能够成功制得lial5o8纳米线,且操作简单、通用性强。
[0035]
本发明还提供一种复合固态电解质和锂金属电池。
[0036]
具体地,本发明采取的技术方案为:
[0037]
本发明的第一方面是提供一种lial5o8纳米线的制备方法,包括如下步骤:
[0038]
对al(eto)3纳米线进行预煅烧,然后在保护气氛下,将预煅烧后的al(eto)3纳米线浸泡于锂离子溶液中;
[0039]
浸泡结束后进行固液分离,得到补充锂的al(eto)3纳米线;
[0040]
煅烧所述补充锂的al(eto)3纳米线,得到lial5o8纳米线。
[0041]
所述锂离子溶液包括乙醇锂(etoli)溶液、磷酸锂(li3po4)溶液、高氯酸锂(liclo4)溶液、碳酸锂(li2co3)溶液、甲醇锂(ch3oli)溶液中的至少一种。
[0042]
所述锂离子溶液中的锂离子浓度为0.1~0.5m。
[0043]
所述al(eto)3纳米线与锂离子溶液的质量比为1:500~700,优选1:625。
[0044]
所述浸泡时间为2~20min,优选5min。
[0045]
所述lial5o8纳米线的制备方法中,所述预煅烧的温度为300~500℃,优选 400℃;所述预煅烧的时间为5~15min。al(eto)3纳米线直接浸泡在溶液中会断裂和溶解,通过预煅烧后再浸泡于锂离子溶液,可避免断裂和溶解,对维持纳米线形貌具有关键作用。
[0046]
所述煅烧(煅烧所述补充锂的al(eto)3纳米线)的温度为800~1500℃,优选1000~1200℃;所述煅烧时间为1~4h。
[0047]
更具体地,所述煅烧过程可按照如下程序进行:先以0.5~1.5℃
·
min
‑1的升温速率从室温加热到500~600℃,再以4~6℃
·
min
‑1的速率升温到800~1500℃,保温1~4h后自然冷却。
[0048]
所述al(eto)3纳米线可为纳米线膜。当所述al(eto)3纳米线为纳米线膜时,制得的lial5o8纳米线也保持纳米线膜的形貌。
[0049]
所述al(eto)3纳米线膜由al(eto)3纳米线凝胶形成。
[0050]
更具体地,所述al(eto)3纳米线膜的制备方法为,对al(eto)3纳米线凝胶进行抽滤
以形成膜。
[0051]
所述al(eto)3纳米线凝胶由室温去合金法制备得到。更具体地,所述al(eto)3纳米线凝胶的制备方法包括如下步骤:将铝和锂混合,煅烧得到li
‑
al合金;将所述li
‑
al合金浸泡于乙醇中,加热反应得到al(eto)3纳米线凝胶。
[0052]
所述铝和锂的摩尔比为1:1~1.5。
[0053]
制备所述al(eto)3纳米线凝胶的方法中,所述煅烧温度为600~1000℃,优选750~850℃;所述煅烧时间为20~60min。
[0054]
所述li
‑
al合金浸泡于乙醇中后的加热反应的温度为50~80℃,优选55~ 65℃;所述加热反应的时间20~40h。
[0055]
本发明的第二方面是提供一种复合固态电解质,所述复合固态电解质含有上述lial5o8纳米线。
[0056]
所述复合固态电解质含有所述lial5o8纳米线和导电凝胶聚合物,所述导电凝胶聚合物包覆所述lial5o8纳米线。
[0057]
所述复合固态电解质还含有锂盐,所述锂盐分散在所述lial5o8纳米线和导电凝胶聚合物中。
[0058]
所述导电凝胶聚合物包括聚丙烯腈、聚氧乙烯、聚氧丙烯、聚偏氟乙烯、偏二氟乙烯
‑
六氟丙烯共聚物(pvdf
‑
hfp)、聚甲基丙烯酸酯、聚丙烯腈中的至少一种,优选偏二氟乙烯
‑
六氟丙烯共聚物。
[0059]
所述锂盐包括六氟磷酸锂(lipf6)、磷酸锂(li3po4)、高氯酸锂(liclo4)、碳酸锂(li2co3)、乙醇锂(etoli)、甲醇锂(ch3oli)中的至少一种。
[0060]
本发明的第三方面是提供一种复合固态电解质的制备方法,包括如下步骤:将所述lial5o8纳米线浸泡于导电凝胶聚合物溶液中,干燥后得到导电凝胶聚合物包覆所述lial5o8纳米线的膜a;使所述膜a吸收锂盐溶液,得到复合固态电解质。
[0061]
所述导电凝胶聚合物的质量浓度为5%~15%。
[0062]
所述锂盐溶液的浓度为0.5~1.5m。
[0063]
本发明还提供一种锂金属电池,所述锂金属电池含有上述复合固态电解质。
[0064]
本发明具有如下有益效果:
[0065]
(1)本发明以al(eto)3纳米线为原料,通过简单的浸泡、煅烧即可成功制得lial5o8纳米线,所得lial5o8纳米线纯度高,而且保持al(eto)3纳米线的纳米线形貌;同时本发明制备lial5o8纳米线的方法成本低、操作简单、通用性强。
[0066]
(2)本发明的复合固态电解质具有导电凝胶聚合物包覆lial5o8纳米线的结构,将其应用于以锂金属作为电极的锂金属电池时,不仅避免了锂金属电极与电解质过度反应造成的界面破坏,而且在复合固态电解质与锂金属电极的界面上产生了有益的al层。al层对锂金属具有良好的润湿性,可以在al位点上形成均匀的li核。此外,复合固态电解质中lial5o8具有纳米线形貌,致密的lial5o8纳米线具有大量的离子传导通道,可以分散li
+
流,实现均匀分布。基于这两个优点,本发明的复合固态电解质可以引导li
+
以层片状而不是以枝晶状的形式沉积。因此,使用本发明的复合固态电解质能够显著改善锂金属电池的长循环稳定性和倍率性能。
附图说明
[0067]
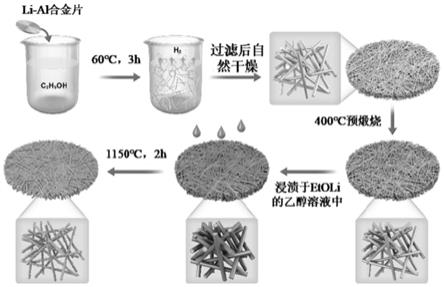
图1为lial5o8纳米线膜的制备流程图;
[0068]
图2为lial5o8纳米线膜的xrd图谱;
[0069]
图3为lial5o8纳米线膜的sem图像;
[0070]
图4为由lph
‑
gpe和aph
‑
gpe组装成的cu/li电池中的li沉积在cu箔上的形貌;
[0071]
图5为由lph
‑
gpe和aph
‑
gpe组装成的lfp/li电池中的sei膜形貌;
[0072]
图6为由lph
‑
gpe和aph
‑
gpe组装成的lfp/li电池的长期循环性能图。
具体实施方式
[0073]
以下结合具体的实施例进一步说明本发明的技术方案。
[0074]
原材料:铝粉(99.5%)、li颗粒(99.9%)、乙醇(>99.8%,分子生物学)、pvdf
‑
hfp(mw=40万)均购自阿拉丁。丙酮(hplc)购自广州化学试剂厂。液态电解液[由lipf6溶于体积比为1:1:1的碳酸亚乙酯(ec),碳酸二乙酯(dec) and乙基碳酸甲酯(emc)而得,lipf6浓度为1m)购自苏州乾民化学试剂公司。
[0075]
实施例1
[0076]
以下提供一种lial5o8纳米线膜的制备方法,其制备流程如图1所示,具体的制备方法包括如下步骤:
[0077]
(1)制备al(eto)3纳米线凝胶:al(eto)3纳米线凝胶的制备可参考d.lei, j.benson,a.magasinski,g.berdichevsky,g.yushin,science 2017,355,267。具体地,将含有铝粉(0.3g)和li块(0.085g)(1:1原子比)的石墨坩埚置于马弗炉在后,在800℃下加热30min,自然冷却后得到一块li
‑
al合金片。在充满氩气的手套箱中对所述li
‑
al合金片进行抛光,抛光后的li
‑
al合金片(0.1105g) 与乙醇(20ml)在60℃下反应30h,得到al(eto)3纳米线凝胶。
[0078]
(2)制备lial5o8纳米线膜:对al(eto)3纳米线凝胶进行抽滤,在滤纸上留下一层al(eto)3纳米线膜,然后自然干燥。将所述al(eto)3纳米线膜置于马弗炉中,以1℃
·
min
‑1的加热速率升温到400℃预煅烧10min。然后将50mgal(eto)3纳米线膜浸泡在20ml 0.15m etoli的乙醇溶液中,以向膜中补充 li源,浸泡时间为5min。浸泡结束后,将纳米线膜从etoli溶液中取出,然后置于马弗炉中,以1℃
·
min
‑1的升温速率从室温加热到600℃,再以5℃
·
min
‑1的速率升温到1150℃,保温2h后自然冷却,得到lial5o8纳米线膜。本步骤中,在马弗炉中的预煅烧和煅烧步骤是在空气中进行的,其他操作都是在充满氩气的手套箱中完成的。
[0079]
所述lial5o8纳米线膜的xrd图谱和sem图像分别如图2和3所示。 xrd图谱中除了lial5o8的特征衍射峰外没有杂质峰,说明成功制得高纯度、无杂质的lial5o8。从sem图像可以看出所述lial5o8具有纳米线形貌。
[0080]
对比例1
[0081]
本对比例与实施例1的不同之处在于:将al(eto)3纳米线凝胶抽滤成膜后,用乙醇(10ml)洗涤纳米线膜三次,去除所有的etoli(制备al(eto)3纳米线凝胶过程中形成的etoli),然后直接加热至1200℃,得到的是α
‑
al2o3纳米线膜。
[0082]
具体地,对al(eto)3纳米线凝胶进行抽滤,在滤纸上留下一层al(eto)3纳米线膜,
接着用乙醇(10ml)洗涤纳米线膜三次,去除所有的etoli,然后自然干燥。将所述al(eto)3纳米线膜置于马弗炉中,以1℃
·
min
‑1的升温速率从室温加热到600℃,再以5℃
·
min
‑1的速率升温到1200℃,保温2h后自然冷却,得到α
‑
al2o3纳米线膜。
[0083]
(1)制备复合固态电解质
[0084]
将pvdf
‑
hfp(0.96g)溶于乙醇(0.48g)和丙酮(8.64g)中,50℃下搅拌2h,制备pvdf
‑
hfp溶液。将40mg实施例1的lial5o8纳米线膜浸渍于9.3gpvdf
‑
hfp溶液中,浸渍时间为3min。浸渍结束后将lial5o8纳米线膜取出,经自然干燥,得到lph膜。将lph膜裁剪成直径为14mm(厚约100μm) 的圆片,在5g电解液(1m lipf
6 in ec:dmc:emc=1:1:1vol%)中浸泡12h,使lph膜充分吸收电解液。浸泡结束后,沥去多余电解液,得到复合固态电解质,标记为lph
‑
gpe,lph
‑
gpe吸收有27μl的电解液。
[0085]
采用相同的方法将对比例1的α
‑
al2o3纳米线膜在pvdf
‑
hfp溶液中浸渍,制得吸收有27μl电解液的对比样aph
‑
gpe。
[0086]
(2)组装电池
[0087]
将lph
‑
gpe和aph
‑
gpe组装成cu/li电池或lfp/li电池,具体如下:
[0088]
将lfp(70wt.%)、乙炔黑(20wt.%)、聚偏二氟乙烯(10wt.%)溶解于 n
‑
甲基
‑2‑
吡咯烷酮(nmp)中形成浆料。将浆料刮涂在铝箔上,80℃烘干12h,裁剪成直径10mm的lfp极片。将lfp极片、lph
‑
gpe和li负极在手套箱中组装成2032型扣式电池,标记为lfp/lph
‑
gpe/li电池。另外将cu箔、 lph
‑
gpe和li负极在手套箱中组装成cu/lph
‑
gpe/li电池。
[0089]
采用相同的方法将lfp极片、aph
‑
gpe和li负极组装为lfp/aph
‑
gpe/li 电池,将cu箔、aph
‑
gpe和li负极在手套箱中组装成cu/aph
‑
gpe/li电池。
[0090]
在cu/lph
‑
gpe/li电池和cu/aph
‑
gpe/li电池中,分别以0.5ma
·
cm
‑2的电流密度使li沉积在cu箔表面,li沉积在cu箔上的形貌如图4所示。从图4可以看出,使用lph
‑
gpe时,li沿二维方向沉积,形成层状li金属,避免了穿透电解质造成短路的风险。这是因为lial5o8纳米线在对锂时会还原生成al层。al均匀分布在lial5o8纳米线的边缘,这不仅促进形成均匀的成核位点,而且均匀化li
+
流,从而使li
+
沉积成片状而不是枝晶状。而使用aph
‑
gpe时,li沉积层会形成尖锐的li枝晶,这将大大增加电极与电解液的副反应。
[0091]
在lfp/lph
‑
gpe/li电池和lfp/aph
‑
gpe/li电池中,分别以1c(1c=170 ma
·
g
‑1)的电流密度充放电50次后,lfp/lph
‑
gpe/li电池在li负极上均匀分布上光滑的、致密的sei膜;而lfp/aph
‑
gpe/li电池中,由于锂枝晶导致 sei膜较厚而且出现严重的裂纹,如图5所示。
[0092]
在2.5~3.8v的电压窗口内对lfp/lph
‑
gpe/li电池和lfp/aph
‑
gpe/li 电池以1c(1c=170ma
·
g
‑1)的电流密度进行恒流充放电。如图6所示, lfp/lph
‑
gpe/li电池和lfp/aph
‑
gpe/li电池的初始比容量分别为139.6 mah
·
g
‑1和140.4mah
·
g
‑1。在经过150圈循环后,lfp/lph
‑
gpe/li电池的比容量为144mah
·
g
‑1,没有发生衰减,而lfp/lph
‑
gpe/li电池的比容量衰减为133.9mah
·
g
‑1,说明lph
‑
gpe能够提高电池的长期循环性,这是因为在 lfp/lph
‑
gpe/li电池中,无枝晶的锂负极和高质量的sei膜为li
+
在锂金属与固态电解质的界面上快速均匀的迁移提供了良好的环境。
[0093]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,
均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1