一种四氧化三钴贵金属复合材料及其制备方法和应用、直接肼燃料电池
1.本发明涉及催化剂技术领域,尤其涉及一种四氧化三钴贵金属复合材料及其制备方法和应用、直接肼燃料电池。
背景技术:
2.随着环境污染和能源危机的日益加剧,发展可再生清洁能源刻不容缓。燃料电池是一种把燃料储存的化学能转化为电能的装置,同时因为其转化效率高、产物对环境友好以及操作简单等优势而备受关注。近几年来,由于燃料电池的技术获得创新突破,再加上环保问题与能源不足等多重压力相继到来,各国政府与汽车、电力和能源等产业渐渐重视燃料电池技术的发展。质子交换膜燃料电池(pemfc)被认为是移动式和便携式电源领域最有前景的技术之一。虽然pemfc技术已日趋成熟,但其商品化还面临一个十分棘手的问题,即氢的生产和储运。
3.针对上述问题,以直接肼燃料电池(dhzfc)为代表的液体燃料电池进入人们视野。由于肼的含氢量高达12.5%,能量密度为5.428wh/g,理论能量转换效率为100%,因此,直接肼燃料电池具有较高的理论电压和能量密度,且所述直接肼燃料电池的反应产物仅为氮气和水,无温室气体排放,并且能够以固体腙的形式存在,便于存储和运输,发展前景良好。直接肼燃料电池的半电池反应和总反应如下所示:
4.阳极:n2h4+4oh-=n2+4h2o+4e-;
5.阴极:o2+2h2o+4e-=4oh-;
6.总反应:n2h4+o2=n2+2h2o。
7.在军事上,肼燃料电池作为体积能量密度高、无噪音及携带轻便的电池电源装置,已引起了人们越来越大的兴趣。但是在实际应用过程中,dhzfc的输出能量却小于理论值。这主要是因为阳极反应的发生产生了较大的超电势,降低了直接肼燃料电池的发电性能。而使用合适的催化剂可以降低反应超电势。其中,铂基催化剂对水合肼氧化反应催化活性的较高,但是成本较高和稳定性较差等因素限制了其进一步发展。因此,开发非贵金属催化剂是解决该问题的关键,其中所述非贵金属化合物如过渡金属催化剂、硫化物和磷化物等在碱性环境中都是良好的hzor电催化剂。其中,过渡金属催化剂因较大的比表面积和孔隙度、良好的稳定性和较短的传输粒子通道等优势,使其作为电极材料时可以提高燃料电池的性能和循环稳定性而受到广泛关注。过渡金属催化剂一般可以分为两类:单一金属氧化物或氢氧化物、多金属氧化物或氢氧化物。单一金属催化剂中由于co、mn或fe等元素的氧化物或氢氧化物具有较高的电子电导率和优异的化学稳定性而被研究的较多。其中,氢氧化钴会催化水合肼发生非电化学氧化反应,但催化活性很低。
技术实现要素:
8.本发明的目的在于提供一种四氧化三钴负载贵金属复合材料及其制备方法和应
用、直接肼燃料电池。所述四氧化三钴负载贵金属复合材料的催化活性高,应用范围广。
9.为了实现上述发明目的,本发明提供以下技术方案:
10.本发明提供了一种四氧化三钴贵金属复合材料,包括四氧化三钴纳米片和负载在所述四氧化三钴纳米片上的贵金属单原子。
11.优选的,所述贵金属单原子为钌原子、铱原子、铂原子和铑原子中的一种或几种。
12.优选的,所述贵金属单原子在所述四氧化三钴纳米片上的负载量为1~10wt%。
13.本发明还提供了上述技术方案所述的四氧化三钴贵金属复合材料的制备方法,包括以下步骤:
14.将四氧化三钴纳米片、可溶性贵金属盐和碱液混合后,进行氧化还原反应,得到所述四氧化三钴贵金属复合材料。
15.优选的,所述可溶性贵金属盐为rucl3、pt(no3)2、ircl3和rhcl3中的一种或几种。
16.优选的,所述四氧化三钴纳米片和可溶性贵金属盐的质量比为(10~50):1;
17.所述可溶性贵金属盐的质量以所述可溶性贵金属盐中的贵金属元素的质量计。
18.优选的,所述氧化还原反应的ph值为10~14;
19.所述氧化还原反应的温度为20~95℃,保温时间为2~24h。
20.本发明还提供了上述技术方案所述的四氧化三钴贵金属复合材料或上述技术方案所述的制备方法制备得到的四氧化三钴贵金属复合材料作为催化剂在水合肼电氧化反应中的应用。
21.优选的,所述四氧化三钴复合材料作为催化剂在直接肼燃料电池中的应用。
22.本发明提供了一种直接肼燃料电池,包括阳极、电解液和阴极,所述阳极包括集流体和所述集流体表面的nafion高分子膜;所述nafion高分子膜中包括催化剂;
23.所述催化剂为上述技术方案所述的四氧化三钴贵金属复合材料或上述技术方案所述的制备方法制备得到的四氧化三钴贵金属复合材料。
24.本发明提供了一种四氧化三钴贵金属复合材料,包括四氧化三钴纳米片和负载在所述四氧化三钴纳米片上的贵金属单原子。
25.本发明所述四氧化三钴贵金属复合材料中的四氧化三钴中的含氧基团与肼上氢的反应以及二价钴、三价钴与肼之间的电子转移都可以促进肼发生脱氢反应。同时,所述四氧化三钴纳米片上的贵金属单原子大大增加了四氧化三钴贵金属复合材料的活性比表面积,并且贵金属与钴元素之间存在的电子转移也进一步促进了其催化本征活性,从而具备优异的水合肼氧化性能和直接肼燃料电池性能;同时,本发明所述的四氧化三钴贵金属复合材料的上述结构既在三维层面上抑制了贵金属催化位点的聚集,提高了贵金属的利用率,又能够利用四氧化三钴载体和催化位点间的强电荷作用,提高了催化剂的活性和选择性,从而促进水合肼氧化反应,更进一步的提高直接肼燃料电池的发电能力。
26.本发明还提供了上述技术方案所述的四氧化三钴贵金属复合材料的制备方法,包括以下步骤:将四氧化三钴纳米片、可溶性贵金属盐和碱液混合后,进行氧化还原反应,得到所述四氧化三钴贵金属复合材料。在本发明所述的制备方法中,所述可溶性贵金属盐在碱性溶液中可以发生水解反应生成羟基化贵金属,所述羟基化贵金属与四氧化三钴表面的含氧官能团发生脱水反应,从而使贵金属以单原子形式锚定在载体四氧化三钴的表面,阻止了催化位点的聚集,提高了贵金属的利用率,并且四氧化三钴载体与催化位点间的强电
荷相互作用,提高了催化剂的活性和选择,进一步提升了水合肼氧化反应性能和直接肼燃料电池的发电性能与稳定性。同时,所述制备方法简单、成本低廉、重复性好以及环境友好。
附图说明
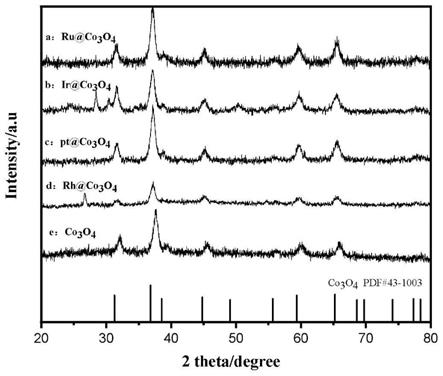
27.图1为实施例1所述四氧化三钴纳米片和实施例1~4所述四氧化三钴负载贵金属复合材料的xrd图;
28.图2为实施例1~4所述四氧化三钴负载贵金属复合材料的sem图;
29.图3为实施例1所述四氧化三钴负载贵金属复合材料的能谱图;
30.图4为实施例3所述四氧化三钴负载贵金属复合材料的能谱图;
31.图5为实施例2所述四氧化三钴负载贵金属复合材料的能谱图;
32.图6为实施例4所述四氧化三钴负载贵金属复合材料的能谱图;
33.图7为实施例1~4所述四氧化三钴负载贵金属复合材料的球差校正透射电镜(actem)图;
34.图8为测试例2所述的线性扫描伏安法(lsv)曲线;
35.图9为实施例5和对比例3~4所述的直接肼燃料电池的j-v曲线。
具体实施方式
36.本发明提供了本发明提供了一种四氧化三钴贵金属复合材料,包括四氧化三钴纳米片和负载在所述四氧化三钴纳米片上的贵金属单原子。
37.在本发明中,所述四氧化三钴纳米片优选为六边形纳米片。
38.在本发明中,所述贵金属单原子优选为钌原子、铱原子、铂原子和铑原子中的一种或几种;当所述贵金属单原子为上述具体选择中的两种以上时,本发明对上述具体物质的配比没有任何特殊的限定,按任意配比进行混合即可。当所述贵金属单原子为钌原子、铱原子、铂原子和铑原子时,所述ru、ir、pt和rh的质量比更优选为5:9:6:5。
39.在本发明中,所述贵金属单原子在所述四氧化三钴纳米片上的负载量优选为1~10wt%,更优选为1~8wt%,最优选为2~3wt%。
40.在本发明中,所述贵金属单原子和四氧化三钴以离子键的结合方式均匀的分散在所述四氧化三钴纳米片的表面。
41.在本发明中,所述四氧化三钴呈现纳米片的结构,其表面平整光滑,排布整齐,更容易锚定贵金属,使其均匀分散。
42.在本发明中,所述四氧化三钴贵金属复合材料优选为六边形纳米片,所述四氧化三钴贵金属复合材料的边长优选为50~60nm,更优选为56~58nm;所述四氧化三钴贵金属复合材料的厚度优选为40~50nm,更优选为45~46nm。
43.本发明还提供了上述技术方案所述的四氧化三钴贵金属复合材料的制备方法,包括以下步骤:
44.将四氧化三钴纳米片、可溶性贵金属盐和碱液混合后,进行氧化还原反应,得到所述四氧化三钴贵金属复合材料。
45.在本发明中,若无特殊说明,所有制备原料均为本领域技术人员熟知的市售产品。
46.在本发明中,所述四氧化三钴纳米片优选通过制备得到。在本发明中,所述四氧化
三钴纳米片的制备方法优选包括以下步骤:
47.将氢氧化钠溶液、钴盐溶液和氨水混合,进行沉淀反应,得到氢氧化钴;
48.将所述氢氧化钴进行煅烧,得到四氧化三钴纳米片。
49.本发明将氢氧化钠溶液、钴盐溶液和氨水混合,进行沉淀反应,得到氢氧化钴。
50.在本发明中,所述氢氧化钠溶液的浓度优选为4~10mol/l,更优选为5~9mol/l,最优选为5~7mol/l。
51.在本发明中,所述钴盐溶液的浓度优选为0.5~2.0mol/l,更优选为0.8~1.6mol/l,最优选为1.0~1.3mol/l。本发明对所述钴盐溶液中的钴盐的种类没有任何特殊的限定,采用本领域技术人员熟知的可溶性钴盐即可。在本发明的具体实施例中,所述钴盐具体为硝酸钴。
52.在本发明中,所述氨水的浓度优选为0.1~1.5mol/l,更优选为0.2~1.2mol/l,最优选为0.4~0.8mol/l。
53.在本发明中,所述氢氧化钠溶液、钴盐溶液和氨水的体积比优选为(1~6):(1~6):(1~3),更优选为(1~3):(1~3):(1~2),最优选为3:3:1。
54.在本发明中,所述混合的顺序优选为先将氨水加入到氢氧化钠溶液中,再与所述钴盐溶液混合。
55.在本发明中,所述沉淀反应的ph值优选为10~12,更优选为10.5~11.5,最优选为10.8~11.2;所述沉淀反应的温度优选为10~80℃,更优选为20~60℃,最优选为25~40℃;时间优选为1~5h,更优选为1~3h,最优选为1~2h。
56.所述沉淀反应完成后,本发明还优选包括依次进行的洗涤、过滤和干燥,本发明对所述洗涤、过滤和干燥的过程没有任何特殊的限定,采用本领域技术人员熟知的过程进行即可。
57.在本发明中,上述制备方法可以使氢氧化钴的结晶度良好。
58.得到氢氧化钴后,本发明将所述氢氧化钴进行煅烧,得到四氧化三钴纳米片。
59.在本发明中,所述煅烧优选在氧化气氛或保护气氛中进行;所述氧化气氛优选为空气气氛;所述保护气氛优选为氮气或氩气。在本发明中,所述煅烧的温度优选为150~650℃,更优选为200~600℃,最优选为300~400℃;保温时间优选为2~12h,更优选为4~10h,最优选为6~8h;升温至所述煅烧的温度的升温速率优选为1~20℃/min,更优选为2~10℃/min,最优选为2~5℃/min。
60.在本发明中,所述可溶性贵金属盐优选为rucl3、pt(no3)2、ircl3和rhcl3中的一种或几种;当所述可溶性贵金属盐为上述具体选择中的两种以上时,本发明对上述具体物质的配比没有任何特殊的限定,按任意配比进行混合即可。
61.在本发明中,所述四氧化三钴纳米片和可溶性贵金属盐的质量比优选为(10~50):1,更优选为(20~40):1,最优选为(25~35):1;所述可溶性贵金属盐的质量以所述可溶性贵金属盐中的贵金属元素的质量计。
62.在本发明中,所述四氧化三钴纳米片与碱液的质量比优选为1:(1~200),更优选为1:(50~150),最优选为1:(80~120)。
63.在本发明中,所述碱液的浓度优选为0.01~1.0mol/l,更优选为0.02~0.7mol/l,最优选为0.3~0.5mol/l。在本发明中,所述碱液中的碱性物质优选为六次甲基四胺、氢氧
化钠、氢氧化钾和氢氧化铵中的一种或几种;当所述碱性物质为上述具体选择中的两种以上时,本发明对上述具体物质的配比没有任何特殊的限定,按任意配比进行混合即可。
64.在本发明中,所述氧化还原反应的ph值优选为10~14,更优选为10~12。所述氧化还原反应的温度优选为20~95℃,更优选为30~80℃,最优选为40~60℃;保温时间优选为2~24h,更优选为10~20h,最优选为13~15h。
65.在本发明中,所述氧化还原反应过程中,所述贵金属盐发生水解反应生成贵金属氢氧化物,且所述贵金属氢氧化物在与四氧化三钴以共价键和离子键的方式结合的过程中会发生一定程度的脱水反应,进而使贵金属能够以单原子形式负载在所述四氧化三钴载体表面。
66.所述氧化还原反应完成后,本发明还优选包括依次进行的固液分离、洗涤和干燥;所述固液分离的方式优选为离心,本发明对所述离心的过程没有任何特殊的限定,采用本领域技术人员熟知的过程进行即可。在本发明中,所述洗涤优选为依次采用去离子水和无水乙醇洗涤3次。在本发明中,所述干燥优选为真空冷冻干燥;所述真空冷却干燥后,还优选包括恢复至室温。
67.本发明还提供了上述技术方案所述的四氧化三钴贵金属复合材料或上述技术方案所述的制备方法制备得到的四氧化三钴贵金属复合材料作为催化剂在直接肼燃料电池中的应用。
68.本发明提供了一种直接肼燃料电池,包括阳极、电解液和阴极,所述阳极包括集流体和所述集流体表面的nafion高分子膜;所述nafion高分子膜中包括催化剂;
69.所述催化剂为上述技术方案所述的四氧化三钴贵金属复合材料或上述技术方案所述的制备方法制备得到的四氧化三钴贵金属复合材料。
70.在本发明中,所述阳极包括集流体和所述集流体中的催化剂;所述催化剂为上述技术方案所述的四氧化三钴贵金属复合材料或上述技术方案所述的制备方法制备得到的四氧化三钴贵金属复合材料。在本发明中,所述集流体优选为泡沫镍。在本发明中,所述催化剂在集流体上的负载量优选为2~5mg/cm2。
71.在本发明中,所述阳极的制备过程优选包括以下步骤:
72.本发明将催化剂、nafion溶液和乙醇混合,得到催化剂浆料。
73.将催化剂、nafion溶液和异丙醇混合,得到催化剂浆料;
74.将所述催化剂浆料喷涂在集流体的表面,得到所述阳极。
75.在本发明中,所述nafion溶液的质量浓度优选为5%;所述nafion溶液优选为5%。
76.在本发明中,所述催化剂、nafion溶液和异丙醇的质量比优选为(9~6):(5~2):(5~2),更优选为(8~7):(5~2):(5~2),最优选为7:3:3。
77.本发明对所述混合的顺序没有任何特殊的限定,采用本领域技术人员熟知的顺序进行混合,并能够保证所述催化剂和nafion溶液溶解在异乙醇中即可。
78.在本发明中,所述混合优选在超声的条件下进行,所述超声的时间优选为2~3h,更优选为2.2~2.6h,最优选为2.3~2.5h;本发明对所述超声的频率没有任何特殊的限定,采用本领域技术人员熟知的频率进行并使所述催化剂和nafion溶液溶解在异乙醇中即可。
79.得到催化剂浆料后,本发明将所述催化剂浆料喷涂在集流体的表面,得到所述阳极。
80.在本发明中,所述集流体优选置于加热台上,并将量所述加热台的温度调整为80~120℃,更优选为90~100℃。
81.本发明对所述喷涂的过程没有任何特殊的限定,采用本领域技术人员熟知的过程进行即可。
82.在本发明中,所述喷涂的涂覆量优选为1~5g/l,更优选为1~3g/l,最优选为2g/l。
83.所述喷涂完成后,本发明还优选包括干燥,所述干燥优选为自然晾干。
84.本发明将所述催化剂浆料直接喷涂在集流体上,使催化活性物质直接与作为集流体的导电基底相连,制作时无需添加粘合剂,具有优良的导电性质,这样的结构避免了常规的粉体材料与集流体接触不良、电子传输效果差和比表面积小的问题,进而改善了包含该材料的电极和直接肼燃料电池的整体电化学性能。
85.在本发明中,所述阴极优选为商业二氧化锰阴极,所述商业二氧化锰的购买于常州优特科新能源科技有限公司。
86.在本发明中,所述电解液优选包括氢氧化钾和水合肼的混合溶液;所述电解液中的氢氧化钾和水合肼的摩尔浓度之比优选为(1~5):1,更优选为2:1。所述电解液中的氢氧化钾的浓度优选为1~6mol/l,更优选为2~5mol/l,最优选为4mol/l;所述电解液中的水合肼的浓度优选为0.5~5mol/l,更优选为0.6~3mol/l,最优选为2mol/l。
87.在本发明中,所述直接肼燃料电池还优选包括极板、第一防水透气层、第一密封垫、带有燃料进出口的夹板、第二密封垫、第三密封垫和带有氧气出口的极板。在本发明中,所述极板、第一防水透气层、阳极、第一密封垫、带有燃料进出口的夹板、第二密封垫、阴极(含防水透气层)、第三密封垫和带有氧气出口的极板依次设置。本发明对所述防水透气层的材料没有任何特殊的限定,采用本领域技术人员熟知的材料即可。
88.本发明对所述直接肼燃料电池的制备过程没有任何特殊的限定,采用本领域技术人员熟知的过程进行即可。
89.在本发明中,所述电解液通入带有燃料进出口的夹板中,氧气通入带有氧气进出口的夹板中,在所述阳极和阴极进行外电路连接并形成电池工作回路。在本发明中,所述电解液的通入温度优选为60~120℃,更优选为80~110℃,最优选为90℃;所述电解液的通入速率优选为50~150ml/min,更优选为80~120ml/min,最优选为90ml/min。在本发明中,所述电解液的通入优选通过循环蠕动泵实现,所述循环蠕动泵的转速优选为30~80r/min,更优选为40~60r/min,最优选为50r/min。在本发明中,所述氧气的通入速率优选为200~800ml/min,更优选为300~600ml/min,最优选为400ml/min。
90.下面结合实施例对本发明提供的一种四氧化三钴负载贵金属复合材料及其制备方法和应用、直接肼燃料电池进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
91.实施例1
92.将5ml浓度为0.5mol/l的氨水加入到15ml浓度为6mol/l的氢氧化钠溶液中,与15ml浓度为1mol/l的co(no3)2溶液混合,得到ph值为12的混合体系,进行沉淀反应,所述沉淀反应的温度为25℃,时间为2h,然后依次进行洗涤、过滤和干燥,得到氢氧化钴;
93.将2g氢氧化钴置于瓷舟内,空气气氛中以5℃/min的升温速率升至400℃后保温
6h,自然冷却至室温,得到四氧化三钴纳米片;
94.将0.1g所述四氧化三钴纳米片、5mg rucl3和100ml 0.01mol/l的氢氧化钾溶液混合,室温搅拌12h后,离心,依次用去离子水和无水乙醇洗涤3次后,真空冷冻干燥,恢复室温,得到四氧化三钴负载贵金属复合材料(记为ru@co3o4,ru的负载量为2.0wt%)。
95.实施例2
96.参考实施例1,区别在于,将5mg rucl3替换为5mg pt(no3)2,得到四氧化三钴负载贵金属复合材料(记为pt@co3o4,pt的负载量为1.8wt%)。
97.实施例3
98.参考实施例1,区别在于,将5mg rucl3替换为5mg ircl3,得到四氧化三钴负载贵金属复合材料(记为ir@co3o4,ir的负载量为1.9wt%)。
99.实施例4
100.参考实施例1,区别在于,将5mg rucl3替换为5mg rhcl3,得到四氧化三钴负载贵金属复合材料(记为rh@co3o4,rh的负载量为1.9wt%)。
101.测试例1
102.将实施例1所述四氧化三钴纳米片和实施例1~4所述四氧化三钴负载贵金属复合材料进行xrd测试,测试结果如图1所示,由图1可知,实施例1~4所述四氧化三钴负载贵金属复合材料均未显示出贵金属单原子峰,原因可能在于金属负载量低,图中31.2
°
、36.8
°
、38.5
°
、44.8
°
、55.6
°
、59.3
°
和65.2
°
出现衍射峰,分别对应载体氧化钴(co3o4)的(220),(311),(222),(400),(422),(511)和(440)晶面;
103.将实施例1~4所述四氧化三钴负载贵金属复合材料进行sem测试,测试结果如图2所示,由图2可知,实施例1~4所述所述四氧化三钴负载贵金属复合材料均为六边形片状结构;ru@co3o4纳米片的边长为58nm、厚度为45.4nm;ir@co3o4纳米片的边长为56.9nm、厚度为45.3nm;pt@co3o4纳米片的边长为57.3nm、厚度为44.9nm和rh@co3o4纳米片的边长为56.4nm、厚度为45.1nm。
104.将实施例1所述四氧化三钴负载贵金属复合材料进行能谱测试,测试结果如图3所示,由图3可知,实施例1所述四氧化三钴负载贵金属复合材料中含有ru金属;
105.将实施例2所述四氧化三钴负载贵金属复合材料进行能谱测试,测试结果如图5所示,由图5可知,实施例2所述四氧化三钴负载贵金属复合材料中含有pt金属;
106.将实施例3所述四氧化三钴负载贵金属复合材料进行能谱测试,测试结果如图4所示,由图4可知,实施例3所述四氧化三钴负载贵金属复合材料中含有ir金属;
107.将实施例4所述四氧化三钴负载贵金属复合材料进行能谱测试,测试结果如图6所示,由图6可知,实施例4所述四氧化三钴负载贵金属复合材料中含有rh金属。
108.将实施例1~4所述四氧化三钴负载贵金属复合材料进行actem测试,测试结果如图7所示,由图7可知,所述四氧化三钴负载贵金属复合材料中的贵金属均是以单原子形式分散于载体中。
109.对比例1
110.四氧化三钴:所述四氧化三钴为实施例1制备得到的四氧化三钴纳米片。
111.对比例2
112.pt/c:所述pt/c中pt的质量百分含量为40%。
113.测试例2
114.将5mg实施例1~4制备得到的四氧化三钴负载贵金属复合材料或对比例1所述的四氧化三钴或对比例2所述的pt/c、2mg卡博导电炭黑、10μl质量浓度为5%的nafion溶液和990μl无水乙醇混合,超声1h,得到催化剂浆料(记为催化剂“ink”);
115.将100μl所述催化剂浆料均匀滴涂在面积为1平方厘米的亲水碳纸上,所述亲水碳纸在使用前依次在无水乙醇和去离子水中超声清洗5min以去除亲水碳纸表面的氧化物或其他污染物后,在红外灯下晾干,得到工作电极;
116.将所述工作电极、碳棒(对电极)和hg/hgo电极(参比电极)构成三电极体系(所述三电极体系采用的电解质溶液为50ml的氢氧化钾(1mol/l)和水合肼(0.5mol/l)的混合溶液),hg/hgo电极与可逆氢电极(rhe)的关系为e
rhe
=e
hg/hgo
+0.0591
×
14+0.098(25℃),进行水合肼氧化反应测试;进行测试前,将三期通入电解质溶液中至少20min以消除所述电解质溶液中的溶解氧,然后利用电化学工作站或测试仪进行过电化学测试,并得到线性扫描伏安法(lsv)曲线;
117.得到的所述线性扫描伏安法(lsv)曲线如图8所示,由图8可知,ru@co3o4、ir@co3o4、pt@co3o4和rh@co3o4的起始电位分别为-0.151v、-0.139v、-0.132v和-0.105v;在10ma处的过电势分别为20.5mv、53mv、59mv和71mv,相比于对比例1的四氧化三钴(起始电位-0.062v,在10ma处的过电势138mv)和对比例2的pt/c(起始电位-0.046v,在10ma处的过电势110mv)表现出更优异的水合肼氧化活性;原因在于贵金属单原子提供了更多的活性位点,提高了贵金属的利用率以及载体四氧化三钴与表面单原子良好的电子转移。
118.实施例5
119.将80mg实施例1~4制备得到的四氧化三钴负载贵金属复合材料、800μl质量浓度为5%的nafion溶液和50ml异乙醇混合,超声2h,得到催化剂浆料;
120.将所述催化剂浆料转移到喷枪中,调节加热台温度至100℃,喷涂到面积为16cm2的泡沫镍上,所述泡沫镍使用前依次经浓度为0.5mol/l的稀盐酸、无水乙醇和去离子水清洗以去除泡沫镍表面的氧化物,进而防止其在碱性介质中形成ni(oh)2,喷涂结束后,自然晾干,得到阳极;
121.在100ml浓度为4mol/l的氢氧化钾溶液中加入50ml浓度为2mol/l的水合肼溶液,得到肼燃料(电解液);
122.以所述阳极为直接肼燃料电池的阳极,以商业二氧化锰阴极(来源常州优特科新能源科技有限公司)为阴极,按照极板、第一防水透气层、阳极、第一密封垫、带有燃料进出口的夹板、第二密封垫、阴极(含防水透气层)、第三密封垫和带有氧气出口的极板依次设置的顺序组装成直接肼燃料电池。
123.对比例3
124.参考实施例5,区别在于将实施例1~4制备得到的四氧化三钴负载贵金属复合材料替换为对比例1所述的四氧化三钴。
125.对比例4
126.参考实施例5,区别在于将实施例1~4制备得到的四氧化三钴负载贵金属复合材料替换为对比例2所述的pt/c。
127.测试例3
128.将90℃的所述肼燃料通过转速为50r/min的蠕动泵通入实施例5和对比例3~4所述直接肼燃料电池的阳极极板,所述肼燃料的流量为90ml/min;将氧气以400ml/min的流量通入所述直接肼燃料电池的阴极极板,接通外电路负载或测试仪实现所述直接肼燃料电池的发电;
129.其中,图9为实施例5和对比例3~4所述的直接肼燃料电池的j-v曲线,由图9可知,ru@co3o4、ir@co3o4、pt@co3o4和rh@co3o4作为催化剂制备得到的直接肼燃料电池的功率密度分别为302mw/cm2、256mw/cm2、215mw/cm2和171mw/cm2,相比于四氧化三钴(功率密度为157mw/cm2)和pt/c(功率密度为73mw/cm2)作为催化剂制备得到的直接肼燃料电池的电池功率密度有明显提高。
130.以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1