一种碳点调控的金属氧化物-碳复合材料及其制备方法和应用
1.本发明涉及金属氧化物/碳复合材料领域,更具体地,涉及一种金属氧化物与碳点均匀嵌布并具有类石榴籽排布结构的微米级复合材料及其制备方法与应用。
背景技术:
2.随着全球变暖与能源消耗的问题日益严重,当今世界对于风能、太阳能灯等可再生清洁能源的依赖逐渐加重,但是清洁能源的间歇性与不稳定性使得其在并入电网过程中亟需高能量/功率密度和低成本的电能存储设备。由于其便携、节能、环保等优点,碱金属离子电池(锂离子电池、钠离子电池或钾离子电池)成为了下一代能源技术的主要候选之一。其中高电压、高能量密度的锂离子电池目前在电动汽车和便携式电子设备市场具有显著优势,开发高性能的锂离子电池电池负极材料对于提高碱金属电池的能量密度至关重要。
3.目前,随着人类社会的飞速发展,化石能源消耗急剧增加,亟需开发新型的可再生清洁能源来应对这一问题,如核能、风能、太阳能、潮汐能等。然而由于可再生能源的间歇性和波动性,先进的储能系统成为了发展的关键。碱金属离子电池(锂离子电池、钠离子电池或钾离子电池)具有便携性、节能性、环保性等优点,是新一代能源技术的候选产品。其中,高电压、高能量密度的锂离子电池主导了电动汽车和便携式电子设备的市场。由于在自然界的远高于锂资源的丰度,钠离子电池和钾离子电池在近年来也逐步受到关注。由于其丰富的资源与较低廉的价格也逐步受到关注。随着新能源技术的进步、智能电网和5g技术的拓宽,人们急需开发具有更高使用寿命,更高能量密度,更快充电速度和更安全的电极材料。
4.由于高比容量特性,金属氧化物材料一直受到广泛关注。然而,金属氧化物负极仍存在着一些问题需要解决:(1)在碱金属离子电池的嵌入脱出的过程中存在严重的体积膨胀问题,同时,在电池循环过程中颗粒之间容易团聚,最终使得电极材料粉化脱落致使电池容量迅速衰减,电池循环寿命缩短;(2)导电性较差,在一定程度上阻碍了电池倍率性能的提升。
5.针对上述问题,目前的改性方法主要包括以下两种:(1)减小颗粒尺寸:颗粒尺寸的减小可以使得活性材料颗粒之间的空隙得以充分利用,有效缩小单位体积的电极材料的变化率;(2)与碳材料复合并构筑特殊的多孔结构:碳材料具有较高的化学稳定性,能够作为框架提升材料的结构稳定性,并作为体积膨胀的应力缓冲,同时碳材料具有高导电性,能够提升金属离子的电荷传输速率,进一步提升电池的倍率性能;并且碳材料具有极强的结构可塑性,能够构成中空或多孔结构,利用其中空或多孔的内部空间缓冲活性材料的体积改变,可以进一步提高材料的结构稳定性,且促进电解液的完全浸润。
6.但是目前针对金属氧化物与碳材料复合的研究仍然存在以下问题:1)实验原料复杂;2)实验合成步骤繁琐;3)实验合成条件苛刻,进而导致碱金属离子电池的成本上升,不具备大规模产业化的生产价值。
技术实现要素:
7.基于此,为了解决现有技术中存在的上述技术问题,本发明的目的之一在于提供一种碳点调控的金属氧化物-碳复合材料,金属氧化物
‑ꢀ
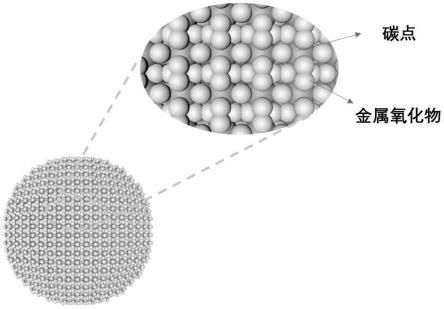
碳复合材料由碳点颗粒和金属氧化物颗粒组成,所述碳点颗粒和金属氧化物颗粒相互均匀嵌布形成类石榴籽排布结构,碳点颗粒之间通过官能团的作用交联,而金属氧化物颗粒均匀嵌布在碳点颗粒之间,这一独特的交联骨架形成网络结构,有效缓解金属氧化物的体积膨胀问题。
8.为了实现上述目的,本发明的技术方案如下:
9.一种碳点调控的金属氧化物-碳复合材料,其特征在于,由碳点颗粒与金属氧化物颗粒组成,所述金属氧化物颗粒和所述碳点颗粒之间相互均匀嵌布成类石榴籽排布结构;所述金属氧化物为第三周期至第五周期金属元素的氧化物中的一种。
10.在一些实施方式中,所述金属氧化物为铜、钴、铁、锡、锑、铋的氧化物中的一种。
11.本发明的目的之二在于提供上述任一实施方式的碳点调控的金属氧化物-碳复合材料的制备方法,该方法以碳点作为形貌诱导剂,可一步反应形成上述排布结构的碳点调控的金属氧化物-碳复合材料,简化了金属氧化物的形貌调控过程,同时将碳点作为碳源,无需额外掺杂碳源,促进复合材料的导电性和循环稳定性。具体如下:
12.一种碳点调控的金属氧化物-碳复合材料的制备方法,包括以下步骤:
13.将可溶性金属盐和碳点分散在有机溶剂中,然后在密封条件下加热进行反应,得到金属氧化物-碳复合材料;所述可溶性金属盐为第三周期至第五周期的金属元素的可溶性金属盐。
14.在一些实施方式中,反应温度为80~200℃,反应时间为0.5~30h。
15.在一些实施方式中,所述有机溶剂为醇类溶剂。具体地,包括乙醇、丙醇、丁醇、异丙醇、异丁醇、戊醇、异戊醇等醇类溶剂。
16.在一些实施方式中,所述可溶性金属盐为金属盐的氯化盐和/或硝酸盐。具体地,包括但不限于硝酸铜、硝酸钴、硝酸铁、氯化铁、氯化锡、氯化锑、氯化铋、硝酸铋、硝酸锑、氯化亚铁、硝酸亚铁、氯化钴、氯化铜、氯化亚铜、硝酸亚铜等。
17.在一些实施方式中,碳点的用量为10~500mg每毫摩尔金属离子,即每毫摩尔金属离子添加10~500mg碳点。
18.反应完成后,还包括洗涤、干燥的步骤,具体为:反应完成后,将水热反应后得到的产物,用去离子水和乙醇分别反复洗涤至少3次,然后在60~100℃下干燥6~12h。
19.本发明的目的之三在于提供上述任一实施方式的碳点调控的金属氧化物-碳复合材料或上述任一实施方式的碳点调控的金属氧化物-碳复合材料的制备方法制成的金属氧化物-碳复合材料作为电极材料的应用。
20.本发明的目的之四在于提供一种电极极片,所述电极极片包括上述任一实施方式的碳点调控的金属氧化物-碳复合材料或上述任一实施方式的碳点调控的金属氧化物-碳复合材料的制备方法制成的金属氧化物-碳复合材料。
21.本发明的目的之五在于提供一种电化学储能装置,所述电化学储能装置包括上述的电极极片。具体地,所述电化学储能装置包括锂离子电池、钠离子电池、钾离子电池。
22.相较于现有技术,本发明的有益效果如下:
23.本发明提供的金属氧化物-碳复合材料,由碳点颗粒和金属氧化物颗粒组成,所述
碳点颗粒和金属氧化物颗粒之间相互均匀嵌布成类石榴籽排布结构(如图1所示),碳点颗粒之间基于官能团的作用相互连接,而金属氧化物颗粒均匀嵌布在碳点颗粒之间,这一独特的交联骨架形成网络结构,可有效缓解金属氧化物的体积膨胀问题,提高复合材料的循环稳定性,而且碳点还可提高复合材料的导电性能,该复合材料作为负极材料应用,表现出优异的循环稳定性和极高的比容量。
24.本发明利用碳点作为形貌诱导剂,通过一步水热法制备了具有类石榴籽排布结构且金属氧化物与碳点相互均匀嵌布的微米级复合材料。本发明中,通过碳点吸附金属离子到碳点表面,然后在水热反应过程中,金属离子在溶剂中水解并受热后进一步分解形成金属氧化物晶核,随着水热反应继续进行,在碳点官能团的作用下,碳点颗粒之间相互连接形成网络结构,而被吸附在碳点表面的金属氧化物颗粒嵌布在碳点颗粒表面和形成的网络之间,由内而外形成类石榴籽排布结构的微米级颗粒。该法制备简单,对金属氧化物具有普遍适用性,一方面大大简化了金属氧化物-碳复合材料的制备流程,另一方面形成的复合材料中金属氧化物和碳点颗粒具有独特的排布结构,这一独特的交联骨架能有效缓解金属氧化物的体积膨胀问题,将该种金属氧化物
‑ꢀ
碳点复合材料作为电极材料应用,其表现出持久的循环稳定性和极高的电池比容量。
附图说明
25.图1为本发明的金属氧化物-碳复合材料的结构示意图;
26.图2为实施例1中sno2/cds复合材料的形貌表征图,其中(a) 图为sno2/cds复合材料的sem图;(b)图为sno2/cds复合材料的 hrtem图;(c1)、(c2)、(c3)和(c4)图为sno2/cds复合材料的 hrtem及其对应的元素分布图;
27.图3为实施例2中cu2o/cds复合材料的形貌表征图,其中(a) cu2o/cds复合材料的sem图;(b)图为cu2o/cds复合材料的hrtem 图;图(c1)、(c2)、(c3)和(c4)为cu2o/cds复合材料的hrtem 及其对应的元素分布图;
28.图4为实施例3中fe2o3/cds复合材料的形貌表征图,其中(a) 图为fe2o3/cds复合材料的sem图;(b)图为fe2o3/cds复合材料的 hrtem图;(c1)、(c2)(c3)和(c4)图为fe2o3/cds复合材料的 hrtem及其对应的元素分布图;
29.图5为实施例4中制成的sno2和sno2/cds复合材料的sem图,其中,(a)图为sno2材料的sem图;(b)、(c)和(d)图分别为加入125mg、250mg和300mg的碳点时制成的sno2/cds复合材料的 sem图;
30.图6为实施例5中sno2/cds-300和sno2/cds-500在0.1ag-1
电流密度下的循环性能图;
31.图7为实施例5中sno2/cds-300和sno2/cds-500在4ag-1
大电流密度的循环性能图;
32.图8为实施例5中sno2/cds-300和sno2/cds-500的倍率性能图;
33.图9为对比例sno2在0.1ag-1
电流密度下的循环性能图;
34.图10为对比例sno2在4ag-1
大电流密度的循环性能图。
具体实施方式
35.在下面的描述中阐述了很多具体细节以便于充分理解本发明。但是本发明能够以
很多不同于在此描述的其它方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似改进,因此本发明不受下面公开的具体实施的限制。
36.除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。
37.碳点的制备:将8g氢氧化钠与40ml乙醛(40%水溶液)磁力搅拌2h以混合均匀,随后在常温常压下静置72h;接着加入1m的盐酸调节至中性,用去离子水离心洗涤3遍,真空干燥得到粒径为3~5nm 的橙黄色碳点。
38.将上述制得的碳点应用于下述实施例中。
39.另外,如无特别说明,本发明具体实施方式中的试剂、原料等均为市购。
40.实施例1
41.sno2/cds复合材料的制备
42.将1.753g sncl4·
5h2o与300mg碳点加入60ml乙醇中,搅拌均匀后,超声10分钟后,将得到的混合溶液转移至反应釜中,在180℃下水热反应16h,得到的产物用去离子水和乙醇离心洗涤3遍,80℃下真空干燥10h,得到的棕色粉末状固体即为sno2/cds复合材料。经检测, sno2/cds复合材料的形貌如图2所示。
43.实施例2
44.cu2o/cds复合材料的制备
45.将0.483g cu(no3)2·
3h2o与100mg碳点加入50ml乙醇中,搅拌均匀后,超声10分钟后,将得到的混合溶液转移至反应釜中,在180℃下水热反应12h,得到的产物用去离子水和乙醇离心洗涤3遍,80℃下真空干燥10h,得到的红褐色粉末状固体即为cu2o/cds复合材料。经检测,cu2o/cds复合材料的形貌如图3所示。
46.实施例3
47.fe2o3/cds复合材料的制备
48.将1.6325g fecl3·
6h2o与500mg碳点加入50ml乙醇中,搅拌均匀后,超声10分钟后,将得到的混合溶液转移至反应釜中,在180℃下水热反应12h,得到的产物用去离子水和乙醇离心洗涤3遍,80℃下真空干燥10h,得到的棕褐色粉末状固体即为fe2o3/cds复合材料。经检测,fe2o3/cds复合材料的形貌如图4所示。
49.从图2、3和4可以看出,金属氧化物/碳点复合材料(m
x
oy/cds, m为金属元素)呈现出表面粗糙的微米级球状结构。在水热过程中, m
x
oy/cds复合材料的生长主要分为三个阶段:第一,在分散阶段,碳点表面官能团吸附多个金属离子到碳点表面;第二,随着水热反应的开始,二氧化锡在碳点表面多点成核形成multi-m
x
oy@cds(碳点表面具有多个m
x
oy的颗粒);第三,在碳点的作用下,多个multi-m
x
oy@cds 之间相互交联形成微米级石榴籽状均匀负载的m
x
oy/cds复合材料。其中,通过元素分布图显示出在m
x
oy/cds复合材料中元素c、m、o均匀分布在整个球体。进一步来说,其中的金属氧化物几乎呈连续一相,而碳点则以石榴籽的形式均匀地嵌布在金属氧化物-碳复合材料中。所制备的sno2/cds、fe2o3/cds和cu2o/cds复合材料都具有这种结构特征。
50.本发明通过一步反应制备了具有石榴籽排布结构的sno2/cds、 cu2o/cds和fe2o3/cds微米级复合材料,进一步说明了该法对于金属氧化物合成的普遍适用性。
51.实施例4
52.一、sno2材料的制备
53.将1.753g sncl4·
5h2o加入60ml乙醇中,搅拌均匀后,超声10分钟后,将得到的溶液转移至反应釜中,在180℃下水热反应16h,得到的产物用去离子水和乙醇离心洗涤3遍,80℃下真空干燥10h,得到的棕色粉末状固体即为sno2材料。经检测,sno2材料的形貌如图5中(a) 图所示,为无定型的纳米小颗粒。
54.二、sno2/cds-x复合材料的制备
55.本实施例中碳点与前驱体的具体制备方法和步骤与实施例1中 sno2/cds复合材料相同,区别在于:为对比不同碳点含量对形貌的影响规律,本实施例中,sno2/cds复合材料的制备过程中所加入碳点含量不同。具体为:将125mg、250mg和300mg碳点分别与1.753gsncl4·
5h2o加入60ml乙醇中,搅拌均匀后,超声10分钟后,将得到的混合溶液转移至反应釜中,在180℃下水热反应16h,得到的产物用去离子水和乙醇离心洗涤3遍,80℃下真空干燥10h,得到的棕色粉末状固体即为sno2/cds-x(x代表碳点加入量)复合材料。经检测, sno2/cds-x复合材料的形貌如图5中(b)、(c)、(d)图所示。其中, (b)、(c)和(d)图分别为加入sno2/cds-125、sno2/cds-250和 sno2/cds-300的sem图。可以看出,随着碳点的增多,由二氧化锡小颗粒逐渐生长为表面粗糙的微米级球状颗粒。
56.实施例5
57.一、sno2/cds复合材料的制备
58.本实施例中碳点与前驱体的具体制备方法和步骤与实施例1中 sno2/cds复合材料相同。本实施例中,sno2/cds复合材料的制备过程中所加入碳点含量不同。具体为:将300mg和500mg碳点分别与 1.753g sncl4·
5h2o加入60ml乙醇中,搅拌均匀后,超声10分钟后,将得到的混合溶液转移至反应釜中,在180℃下水热反应16h,得到的产物用去离子水和乙醇离心洗涤3遍,80℃下真空干燥10h,得到的棕色粉末状固体即为sno2/cds-x(x代表碳点加入量)复合材料;即制得的产物分别为sno2/cds-300和sno2/cds-500。
59.二、sno2/cds复合材料电池性能测试
60.将上述实施例5制备的sno2/cds-300和sno2/cds-500复合材料用作锂离子二次电池活性物质,制成负极极片。具体方式为:将制备的sno2/cds-x复合材料与superp(导电剂)、羧甲基纤维素钠(cmc,粘结剂)按照70:15:15的质量比混合,加入适量去离子水调制成浆料,随后采用涂布法涂在集流体铜箔上,待去离子水挥发后于80℃下真空干燥12h。将含有活性材料的铜箔裁成直径为14mm的圆片,并在 10mpa压力下进行压片处理,然后转移至惰性气体手套箱中。
61.在ar气氛手套箱中,以金属锂为对电极,以lipf6/ec:dmc:dec =1:1:1作为电解液,以celgard2400膜为隔膜,组装成cr2016型扣式电池。随后进行电化学性能测试,测试结果如图6、图7和图8所示。
62.具体来说,在电流密度为100ma g-1
时,sno2/cds-300的容量在 150次循环后可以保持在982.9mah g-1
;当电流密度增加到4a g-1
后,300次循环后仍可获得782.2mah g-1
的容量;在电流密度为100 ma g-1
时。sno2/cds-500的容量在150次循环后可以保持在678.9mah g-1
;当电流密度增加到4a g-1
时,300次循环后仍可获得549.9 mah g-1
的容量。
63.它们的倍率性能显示在图8中。在0.1、0.5、1.0、2.0以及5ag-1
的电流密度下,可逆
比容量分别为1041.0、748.4、667.8、以604.9mahg-1
。不同电流密度充放电结束后,当电流密度回到0.1a g-1
时,可逆比容量恢复至823.5mah g-1
。
64.对比例1
65.一、sno2材料的制备
66.本实施例中sno2材料的制备具体制备方法和步骤与实施例4中 sno2材料相同。
67.二、sno2材料电池性能测试
68.将上述制备的sno2材料用作锂离子二次电池活性物质,制成负极极片,具体方式和步骤与实施例5中sno2/cds复合材料制备负极极片的方式相同。测试其电化学性能,具体如下:
69.在ar气氛手套箱中,以金属锂为对电极,以lipf6/ec:dmc:dec =1:1:1作为电解液,以celgard 2400膜为隔膜,组装成cr2016型扣式电池。随后进行电化学性能测试,测试结果如图9和图10所示。其中循环性能如图9和图10所示,具体来说,在电流密度为100ma g-1
时, sno2的容量在150次循环后容量下降至318.8mah g-1
;当电流密度增加到4ag-1
时,300次循环后容量下降至157.7mah g-1
的容量。
70.本发明提供的金属氧化物-碳复合材料,作为负极材料,可表现出优异的电化学性能。综上,本发明利用碳点作为形貌诱导剂,通过一步水热法制备了具有石榴籽排布结构且金属氧化物与碳点均匀嵌布的微米级复合材料。该法简化了制备金属氧化物/碳点复合材料的步骤,所形成的sno2/cds复合材料能够有效提升sno2材料的电化学性能。
71.需要说明的是,本发明的方法,同样适用于制备其他的具有石榴籽二级结构且金属氧化物与碳点均匀嵌布的微米级复合材料,制备方法与上述实施例中的基本相同,不排除为了得到最优结构的复合材料进行适当的反应条件包括温度、反应时间的调整。
72.以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
73.以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1