正极和蓄电池的制作方法
本发明涉及一种蓄电池的正极活性物质。另外,涉及一种由该正极活性物质构成的蓄电池。
背景技术:
1、索尼株式会社于1991年投产的锂离子蓄电池具有高能量密度,因此被广泛应用于笔记本电脑、手机等中,最近作为电动车用电池而备受瞩目。然而,虽然汽油车在油箱加满的情况下可以行驶1000km以上,但是目前市面上贩卖的日产聆风电动车的单次充电行驶距离为商品目录值400km,作为私家车购买时行驶距离不足。因此,希望开发出一种单次充电能够行驶1000km、即具有2倍以上的能量密度的创新电池。
2、锂离子随着充放电而嵌入/脱嵌的层状金属氧化物用作锂离子蓄电池的正极活性物质,但在最近的研究中发表了,获得了大幅度超过构成晶体的金属离子的氧化还原量的容量的实验结果。该大幅度得到的容量被称为正极过剩容量,以现有的钴/镍/锰3元系层状金属氧化物160mah/g的2倍以上为目标进行了很多研究。过剩容量的原因被认为是构成晶体的氧原子从通常的负2价变成过氧化状态的负1价。但是,过氧化状态的氧的键合力弱,会从晶体中脱离,结构被破坏而无法作为蓄电池进行充分的充放电循环。另外,过量地被晶体收入的锂离子在晶体中的占有位置也不明确显现。
3、在两极使用嵌入型的碳的双碳电池中,如图2所示将多孔体结构的正负极活性物质的细孔以示意图的方式描绘成筒状。两极的表面被与电解液的反应所形成的sei(固体电解质界面)或“筛膜”覆盖,所述筛膜可使锂离子这样的电荷载体离子通过而不使碳酸亚乙酯这样的溶剂通过,细孔内成为没有溶剂的状态。通过充电,向负极活性物质注入电子,向正极活性物质注入空穴(電子欠損),以保持活性物质的电荷和电中性的方式,在负极活性物质细孔中对正离子进行储存/蓄电,在正极活性物质细孔中对负离子进行储存/蓄电。反应式为下式。
4、正极反应:
5、负极反应:
6、总电池反应:
7、充电后,电解液中几乎没有正离子和负离子,以电解液中存在的正离子和负离子的量来限制电池的充放电量。电解液中存在的正离子和负离子是通过将电解质盐溶解于溶剂中而得到的,因此显然不能超过在固体活性物质中对正离子进行储存/蓄电的现有的锂离子电池。
8、将锂金属作为负极、将现有负极的石墨作为正极来实现放电的方法被公知且实用化,其是为了碳极的sei形成处理等而预先嵌入锂离子的被称为“预掺杂”的方法。该反应具有可逆性,在负极发生锂金属析出反应,在正极发生锂离子嵌入/脱嵌反应。反应式为下式。
9、正极反应:
10、负极反应:
11、总电池反应:
12、将预掺杂的碳作为正负两极来构成电池时,高电位的碳极成为正极,低电位的碳极成为负极。图3以示意图示出了其反应机理。反应式为下式。
13、正极反应:
14、负极反应:
15、总电池反应:
16、参考作为现有技术文献的专利文献1和专利文献2,若使用锂离子能够通过但溶剂和负离子不能通过的筛膜,则负极能够嵌入/蓄电至碳数n=2即lic2,正极能够充电至不再嵌入锂离子的状态,且能够在此期间进行放电。现有的石墨的理论容量为372mah,根据非专利文献1、非专利文献2和非专利文献3,通过使用筛膜,对于软碳/硬碳这样的多孔体结构碳而言,每单位重量的容量约为石墨的3倍、为1000mah,每单位体积的容量约为石墨的2倍、为700mah,可以实现目标的现有的2倍的高容量正极。但是,由于两极同为脱嵌入反应,正负极的电位差即蓄电池电压只有现有的锂离子蓄电池的一半左右,不能提高能量密度。
17、参照非专利文献4,绘制了图4。充电时,锂离子从正极钴酸锂向负极集电体pt移动到固体电解质latspo内,从pt起至700nm左右会形成锂离子非常多的分布区域,再向前2μm左右会形成锂离子少量存在的分布区域。虽然在图中不连续地绘制,但浓度是连续变化的,浓度梯度呈指数函数。高浓度地分布的700nm的区域的锂离子随着充放电而增减,因此被命名为“原位形成负极”。
18、充放电并非锂金属的析出电位,而是锂离子在固体电解质中嵌入和脱嵌,因此是基于非专利文献1和2的计算化学所证实的“悬臂论(片持ち論)”的锂离子的储存/蓄电。图5的左图为初充电时的锂离子嵌入,晶体中产生变形,存在固体电解质内形成的纳米尺寸的空隙/间隙/裂纹的状态图。根据发表者的说明,在充放电后的基于透射型显微镜的观察中确认了空隙的存在,但由于测量分辨率不足,无法测定在该空隙中存在锂离子这一点。通过在该空隙中嵌入/脱嵌,发生了锂离子的充放电。非专利文献1、2和3所述的计算化学所证实的“悬臂论”定性地成立于具有电子导电性的物质中形成的任何形状的空隙,而不限于碳纳米管。图5的右图为放大了空隙的图,锂离子沿着空隙的壁以一定间隔排列。不是被夹在空隙的中央,也不会多个聚集成簇。通过初充电时的锂离子的嵌入,晶体中产生变形而形成空隙,进而还由于晶体变形而表现出电子导电性。非专利文献1和2中的碳纳米管调换为“空隙”和表现出电子电导的固体电解质。反应式为下式。充放电也为相同反应式。
19、负极充电(形成)反应:
20、正极负极是由哪一个电位高来决定的,若为可逆反应,则根据对方而可以为正极也可以为负极。若对电极为金属锂,则“原位负极”也会变为“原位正极”。
21、现有技术文献
22、专利文献
23、专利文献1:日本专利第5062989号公报
24、专利文献2:日本专利第5134254号公报
25、非专利文献
26、非专利文献1:第50届电池讨论会演讲摘要集演讲编号3a21佐野茂、楠美智子、立花明知
27、非专利文献2:第51届电池讨论会演讲摘要集演讲编号2b14佐野茂、楠美智子、立花明知
28、非专利文献3:(株)情报机构主页讲师专栏佐野茂
29、非专利文献4:electrochmistry communications 20(2012)113-116
技术实现思路
1、发明要解决的问题
2、锂离子二次电池的蓄电能量为蓄电量与电压的乘积,如背景技术中所说明的那样,能够通过以往的理论/技术实现将蓄电量增加至现有的3元系层状金属氧化物的160mah/g的2~3倍,但不存在可以用相同的材料得到与现有的锂离子电池相同的电压3.6v的理论/技术。
3、用于解决问题的方案
4、为了实现高容量和高电压,就蓄电方法而言,需要新的电池理论,本发明提供了该理论和方案。
5、把正极分割成n个要素。n个分割是虚拟的分割,因此不需要特定的场所,不需要均等,可以是任意的,n的数目是任意的,也可以是无限的。n个部分各自的电特性如下所示。
6、n个部分的充放电(闭路)电位=平衡电位±{n个部分的(电子阻力+离子移动阻力)}*{n个部分的电流}±n个部分的电荷转移过电压±n个部分活性物质非均一性的soc调整电压±n个部分的反应面离子浓度校正电压
7、分割的n个部分并联连接,因此n个部分的充放电(闭路)电位相对于负极在1~n个部分均相同。n个部分的电子阻力、n个部分的离子移动阻力、n个部分的电荷转移过电压、n个部分的活性物质非均一性的soc调整电压、n个部分的反应面离子浓度校正电压在n个部分均不同,但由于n个部分的电流以n个部分的充放电(闭路)电位相等的方式变化,因此各个部分的各构成要素不显现于外部电压。
8、切断电流时,电流变为“0”,因此n个部分的电子阻力和n个部分的离子移动阻力乘以n个部分的电流后的值立即变为“0”,电流的对数函数的电荷转移过电压也在几秒后变为“0”,n个部分的正极电位用下式表示。
9、n个部分的正极电位=平衡电位±n个部分活性物质非均一性的soc调整电压±n个部分反应面离子浓度校正电压
10、n个部分的正极电位、平衡电位、n个部分活性物质非均一性的soc调整电压、n个部分反应面离子浓度校正电压并不相同,为n个部分各自的固有值,但其各个部分并联连接,因此正极电位以负极为基准成为达到最大电位差的电位。也就是说,即使电极内存在不同的平衡电位、即热力学内部能量不同的部分,正极电位相对于负极也只显现最高电位。关于该电位的研究/建议为新的理论,在构成本发明方面是非常重要的。
11、即使存在电位不同的成分,为了显示电极电位,也需要发生电荷转移反应、即需要与电解质接触。即使存在不同的成分,也会出现与电解液接触的表面处的电化学反应的电极电位、即电池电压。若与电解液接触的第m个电位在n个部分中最高,则不管其他部位的电位如何,正极的电位都是第m个电位。
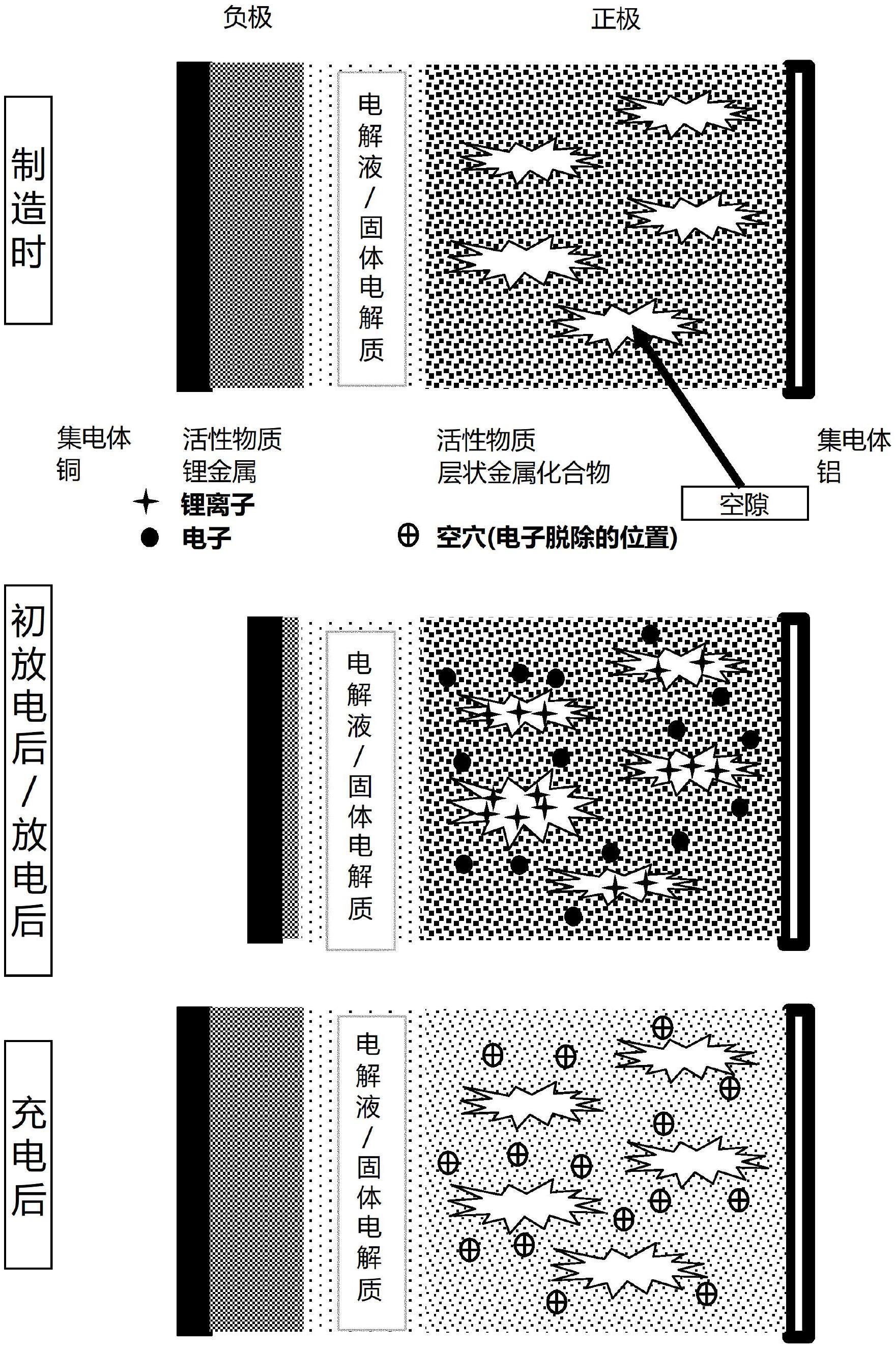
12、如图1所示,在放电状态下制造的具有氧化还原电位的层状化合物内存在空隙,初放电、即注入电子时,层状化合物内的锂离子等电荷载体离子因静电力被储存/蓄电于空隙内。与注入的电子相平衡,通过“悬臂论”被储存/蓄电于沿空隙的壁间隔几nm的位置。电解液或固体电解质中的电荷载体离子通过氧化还原反应嵌入层状化合物内,以补充在层状化合物内减少的电荷载体离子。只要是通过嵌入而发生具有氧化还原电位即电极反应电位的反应即可,例如以现有的锂离子电池中使用的钴酸锂为示例时,为下式那样的反应式。
13、
14、空隙中的储存反应为下式的反应式。
15、
16、x的值由空隙的大小决定,根据非专利文献1、2的计算化学中的结果,直径4nm以上是好的,但由于沿着壁排列,因此如果过大,则中央部成为多余的空间,因此体积效率变差。即便x=1,也为现有的正极材料的2倍,且正极电位为钴酸锂的氧化还原电位,因此能量密度至少为2倍以上,能够满足作为电动车用电池的要求基准。初放电后的每次放电都为相同的反应。
17、充电时,如图1的下图所示,存在于层状化合物内的电荷载体离子通过氧化还原反应从层状化合物向电解液或固体电解质内脱嵌。只要是通过脱嵌而发生具有氧化还原电位即电极反应电位的反应即可,例如以现有的锂离子电池中使用的钴酸锂为示例时,为下式那样的反应式。
18、
19、在进行上述反应式的充电反应的同时,在层状化合物的空隙周边注入空穴,空隙内的电荷载体离子被静电斥力挤出,电荷载体离子嵌入层状化合物中,以补充层状化合物内的电荷载体离子的减少。空隙中的储存反应为下式的反应式。
20、
21、发明的效果
22、根据本发明,通过在现有的钴酸锂、镍/钴/锰酸锂、镍锰酸锂、磷酸铁锂等层状化合物中设置空隙,如图1所示,在空隙内可以储存例如锂离子等电荷载体离子,该空隙内的电荷载体离子经由该层状化合物与电解液或固体电解质接触而进行电荷转移反应,电极反应电位达到该层状化合物的氧化还原电位,因此可以增大能量密度。通过进行空隙的最优化,可以对现有的层状金属氧化物的2倍以上的电荷进行蓄电。
23、根据本发明,通过在面向电解液或固体电解质的具有空隙的多孔体结构的表面覆盖现有的层状化合物,如图6所示,可以以通过嵌入/脱嵌而具有氧化还原电位的层状化合物的电位将电荷载体离子导入多孔体结构中。电荷载体离子可以储存于硬碳/软碳那样的具有电子电槽性的多孔体结构的空隙中,因此可以对远多于现有的钴酸锂等层状金属氧化物的电荷进行蓄电。需要说明的是,根据非专利文献1和2的稳定化能的计算结果推定的空隙内的电荷载体离子的电位非常低,但由于经由层状化合物,因此成为层状化合物所具有的氧化还原反应电位。
- 还没有人留言评论。精彩留言会获得点赞!