基于高亮度电子束的精确放射治疗方法及系统与流程
本发明涉及一种基于高亮度电子束的精确放射治疗方法,同时也涉及相应的精确放射治疗系统,属于肿瘤放射治疗
技术领域:
。
背景技术:
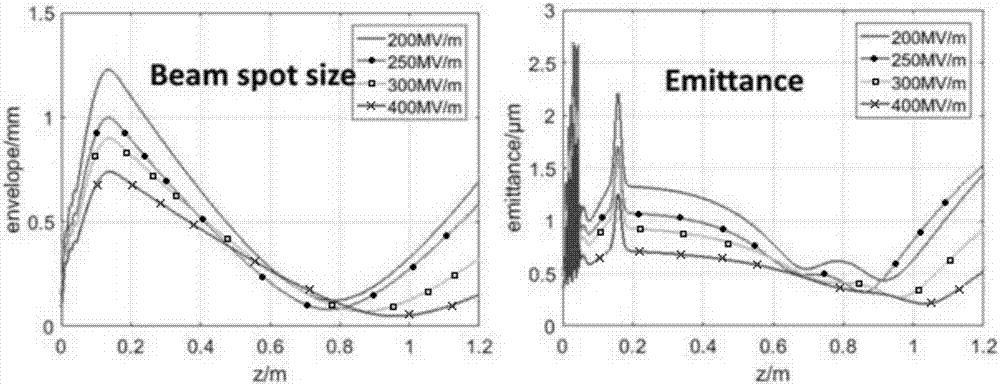
:肿瘤放射治疗是利用放射线杀死癌细胞的一种肿瘤治疗方法。目前,放射治疗作为肿瘤治疗的三大手段之一,大约有65%~75%的患者需要接受放射治疗。其中,基于加速器产生的x射线、电子束和重离子束在肿瘤治疗中最为有效。各类放射线都通过在肿瘤部位沉积能量将癌细胞杀死,但不同种类射线的能量沉积方式有所不同,在治疗的过程中对人体正常组织的影响差异很大。x射线的穿透能力强,可以用来治疗体内肿瘤。但是x射线在治疗肿瘤的同时,会对肿瘤周围的正常组织有所伤害。质子束或重离子束治疗肿瘤也需要穿透皮肤和正常组织到达病灶,由于质子束或重离子束在到达病灶之前要在正常组织处损失大部分的能量,使患者的正常组织也连带受到伤害,在治疗结束后恢复困难。此外,质子或重离子加速器的价格十分昂贵,造价往往高达数十亿元人民币。传统的电子束广泛应用于治疗皮肤和浅表层的肿瘤,但由于电子的穿透能力小,不能直接进入到皮肤以下深层的病灶部位。在现有技术中,以美国intraop公司生产的mobetron移动式电子线术中放射治疗系统为代表的小型电子加速器广泛应用在手术过程中的治疗。该电子线术中放射治疗系统的显著特点是在外科手术切除肿瘤之后(伤口直径通常在5厘米左右),使用电子束在肿瘤病灶原来位置附近进行照射,消灭残余的肿瘤细胞或组织。这种术中放射治疗方式是肿瘤外科手术的一种有益补充。然而,对于不能进行手术切除的肿瘤,这种术中放射治疗方式将不再适用。技术实现要素:本发明所要解决的首要技术问题在于提供一种基于高亮度电子束的精确放射治疗方法。本发明所要解决的另一技术问题在于提供一种基于高亮度电子束的精确放射治疗系统。为了实现上述目的,本发明采用了下述的技术方案:根据本发明实施例的第一方面,首先提供一种基于高亮度电子束的精确放射治疗方法,包括如下步骤:生成高亮度电子束,所述高亮度电子束通过预设的电子束管道引入患者体内的肿瘤病灶部位,对所述肿瘤进行消融。其中较优地,所述高亮度电子束的归一化发射度不大于10毫米毫弧度,优选不大于1毫米毫弧度。这里的发射度为衡量电子束流方向的单位。其中较优地,所述高亮度电子束的能量范围为1~100mev。其中较优地,所述电子束管道通过介入治疗方式插入患者体内,前端靠近所述肿瘤或插入所述肿瘤内部。其中较优地,所述高亮度电子束由电子枪产生,所述电子枪的阴极为光阴极、热阴极和场致发射阴极中的任意一种。其中较优地,所述高亮度电子束通过加速管进行加速;所述加速管的电子束出口设置有栅栏结构,用于对所述高亮度电子束进行部分截取。其中较优地,被加速的高亮度电子束经磁铁聚焦后进入所述电子束管道,或者,进入所述电子束管道内部的电子束在磁铁引导下进行方向调整。其中较优地,所述电子束管道对高亮度电子束进行真空低损传输。其中较优地,所述高亮度电子束用于在术中治疗或介入治疗中消融患者浅表和深部的肿瘤。根据本发明实施例的第二方面,提供一种基于高亮度电子束的精确放射治疗系统,包括:电子枪,用于生成高亮度电子束;加速器,用于对所述高亮度电子束进行加速,以及电子束管道,用于对所述高亮度电子束进行真空低损传输,并引入患者体内的肿瘤病灶部位对所述肿瘤进行消融。其中较优地,所述电子枪的阴极为光阴极、热阴极和场致发射阴极中的任意一种。其中较优地,所述加速器具有加速管,所述加速管的电子束出口设置有用于对所述高亮度电子束进行部分截取的栅栏结构。其中较优地,所述加速管为s波段加速管或者x波段加速管。其中较优地,所述精确放射治疗系统还包括用于对高亮度电子束进行聚焦的磁铁,被加速的高亮度电子束经磁铁聚焦后进入所述电子束管道。其中较优地,所述精确放射治疗系统还包括用于对高亮度电子束进行方向引导的磁铁,进入所述电子束管道内部的高亮度电子束在磁铁引导下进行方向调整。其中较优地,所述电子束管道为无磁性的金属管;所述电子束管道的直径为毫米级,长度在1~100厘米之间。其中较优地,所述电子束管道使用钛窗或铍窗作为高亮度电子束的出射窗口。与现有技术相比较,本发明所提供的精确放射治疗方法及系统,通过细长的电子束管道将经过加速和聚焦的高亮度电子束直接传输到肿瘤处进行消融。经过单次或多次照射,可以达到相当于外科切除的治疗效果。使用上述精确放射治疗方法对肿瘤进行精确消融,消融次数少,单次剂量高,损毁直接;并且,在整个传输路径上电子不与正常组织发生相互作用,能量损失非常小,同时电子直接与肿瘤直接相互作用,射线利用率高。另外,在该精确放射治疗系统中,用于传输高亮度电子束的电子束管道很细,经皮穿刺对组织的损伤非常小。附图说明图1是不同粒子射线(x,e和p)的剂量沉积曲线;其中,纵轴刻度是线性变化的剂量刻度;图2示意性地描述了高亮度电子束到达肿瘤处的过程;图3是从图2所示过程产生的模拟高亮度电子束的参数图。具体实施方式下面结合附图和具体实施例对本发明的技术内容做进一步的详细说明。图1是不同粒子射线(x,e和p)的剂量沉积曲线图。在本发明的一个实施例中,假设在患者体内13厘米处具有肿瘤,在x射线和质子束从皮肤表层到达该位置的过程中,将在正常组织中沉积大量的辐射剂量;对于能量级别为4mev的电子束,吸收剂量曲线在穿入体内1~2厘米后迅速跌落至0,因此不能到达肿瘤位置。基于上述情况,发明人大胆地提出一种设想并进行了实验验证,具体说明如下:被加速器加速后的高亮度电子束,通过细长如针的电子束管道(直径应该小于2毫米)直接送到体内13厘米处的肿瘤位置进行消融,从而实现对肿瘤或癌变组织进行放射治疗。在具体进行放射治疗时,电子束管道的前端可以设置在肿瘤附近对肿瘤进行消融,也可以穿入肿瘤内部从内到外进行消融。由于治疗次数少,单次剂量高,损毁直接,发明人将这一新技术命名为“电子消融刀”(eknife)。使用该“电子消融刀”(eknife)治疗技术,可以达到与使用电子束治疗皮肤或浅层肿瘤一样的消融效果。本发明首先提供一种基于高亮度电子束的精确放射治疗方法,包括如下的步骤:高亮度电子束被加速后通过细长的电子束管道,被送达患者体内病灶位置进行肿瘤消融。这里的高亮度电子束的归一化发射度应该不大于10毫米毫弧度(mm·mrad),优选为1~10毫米毫弧度之间,进一步优选为不大于1毫米毫弧度甚至不大于1um·mrad,总之越小越好;相应地,高亮度电子束的能量范围为1~100mev。这里的发射度为衡量电子束流方向的单位,其含义可以参阅程国均在《四川大学学报(自然科学版)》1979年第4期发表的论文《粒子束发射度和亮度的物理概念》。在本发明的不同实施例中,该发射度的取值越小越好。需要说明的是,现有mobetron移动式电子线术中放射治疗系统因其阴极部分的设计限制,无法提供满足上述指标要求的高亮度电子束。该系统所产生的电子束与本发明所提供的高亮度电子束之间就像手电光和激光之间的差别。只有满足上述指标要求的高亮度电子束才可以在小尺寸空间内长距离的传播。在本发明的一个实施例中,该电子束管道可以通过常规手术方式或者介入治疗方式插入患者体内,电子束管道的前端靠近肿瘤或插入肿瘤内部。上述精确放射治疗方法利用加速器产生高亮度电子束,并通过一根细长针管状的电子束管道(使用方式类似现有的穿刺针)将电子束直接传输到肿瘤处,直接将高能电子沉积到肿瘤处,通过单次或多次照射,可以达到相当于外科切除的治疗效果,从而在术中消融患者浅表和深部的肿瘤或通过介入治疗方式进入患者体内消融浅表和深部的肿瘤。在上述精确放射治疗方法中,使用加速器可以产生一种类似激光的具有高方向性的高亮度电子束,然后由高亮度电子束通过穿透皮肤和正常组织的细长电子束管道到达患者体内病灶位置进行肿瘤消融。下面对高亮度电子束的产生、加速及传输过程进行介绍。高亮度电子束的传输原理如图2所示,具体来说,从阴极发射的高亮度电子束被加速器加速到合适的能量级别(例如为4mev)后,可以穿过直径约几毫米、长度约几十厘米的针状细管(本发明中称为电子束管道)到达肿瘤处。基于加速器技术的最新发展以及物理原理上的深入理解,通过与外科诊断方法的比较,发明人认为用极小的创伤(类似于广泛用于门诊的穿刺活检诊断)将电子束从外界直接通过直径为毫米级(例如,直径小于1毫米)、长度为10~40厘米的电子束管道传输至病灶是可行的。这是一种不需要外科手术的新型放射治疗方式。其中,该电子束管道的长度可以长达几十厘米,优选为直线形式,这样控制起来最为简单。当然,采用磁铁等工具可以使该高亮度电子束在控制下转变方向,因此该电子束管道并不局限于直线形式。在过去的二十年里,充分发展的加速器技术可以产生亮度很高的电子束并将其传输很长的距离。在本发明所提供的精确放射治疗方法中,可以直接将高亮度电子束传输到肿瘤部位进行放射治疗。根据已有的加速器技术,此方法在实际应用中切实可行,并且将成为电子束在肿瘤治疗上的一次飞跃。具体地说,本发明通过将高亮度电子束送到肿瘤病灶处,利用高亮度电子束(例如归一化发射度不大于1毫米毫弧度,能量范围为1~100mev)直接消融身体浅表和深部的肿瘤。与现有的各种肿瘤消融技术相比,本发明具有如下技术特点:加速器产生高亮度的电子束后,通过一根细长针管状的电子束管道(类似穿刺针)将电子束直接传输肿瘤处,从而直接将电子携带的能量沉积到肿瘤处,通过单次或多次照射,可以达到类似于外科切除的治疗效果。其中,用于传输电子束的电子束管道很细,直径至多只有几个毫米,经皮穿刺对正常组织的损伤非常小。并且,在整个传输路径上电子不与正常组织发生相互作用,能量损失非常小,同时电子直接与肿瘤发生相互作用,射线利用率高。现有的mobetron移动式电子线术中放射治疗系统等必须由医生对人体开展外科手术,将需要电子束照射的部位暴露在外面,然后才能利用电子束照射病灶。如果不进行外科手术,上述设备无法将高亮度电子束打入到人体深层的病灶。本发明所提供的精确放射治疗方法可以实现肿瘤治疗的“精确制导”,并使剂量在时间和空间上得到精确控制,不伤害任何正常组织,可以将电子束在放射治疗上的应用扩展到一些不可外科手术的肿瘤放射治疗中,并可以极大地缩短治疗时间(基本上一次的治疗就可以代替现有技术的多次放射治疗)和病人的恢复期。此外,该精确放射治疗方法极大地减少了对传统的放射治疗设备机头的机械控制要求,还具有背景辐射极小等优点,在技术上是一次革命性的提高。在本发明中,同时提供了一种用于实现上述精确放射治疗方法的精确放射治疗系统。具体实现方案的示例如下:1.高亮度电子束的产生在本发明中,高亮度电子束是指归一化发射度不大于10毫米毫弧度,能量范围为1~100mev的电子束。它是本发明所提供的精确放射治疗方法及系统成败的关键,因为只有亮度足够高的电子束才能在直径不大于2毫米的电子束管道内无损传输,顺利到达患者病灶位置。高亮度电子束的产生包括电子束发射和电子束加速两个过程,每一个过程对于最终电子束的引出都至关重要。(1)高亮度电子束的发射电子枪有很高的加速梯度,能够有效地拟制空间电荷效应,是加速器领域产生高亮度电子束的常用设备。按照发射方式的不同,电子枪的阴极可分为光阴极、热阴极和场致发射阴极三种。光阴极用激光在阴极上打出电子,具有峰值流强高,发射度低的优势。现在此技术非常成熟,但目前还没有在医学上的应用。世界上,包括中国在内,已经成功研制了几十个此类电子枪,并成功运行使用在各类科学装置中。热阴极将阴极加热发射电子,其平均流强高,发射度较低,现在已经在国际上广泛使用。场致发射阴极依靠阴极表面的强电场将阴极的电子拉出,电子束发射度较低,平均流强较高,然而这种阴极对材料要求苛刻。总之,现有技术已经可以完全满足我们的需求,现阶段的实验证明,具有三种阴极中任意一种的电子枪均可用于产生符合本发明要求的高亮度电子束。在不久的将来,更加深入研究三种阴极的电子枪,综合考虑电子束发射度、阴极寿命以及设备成本等因素,可以找出电子发射的最佳方案。(2)高亮度电子束的加速由于现有的电子枪可以产生能量范围在1~10mev的电子束,基本可以满足医学上的要求。具体参数可以根据实际需求进行优化,不过通常所需的加速器件都有成熟的供应商供应。我们在此仅讨论两种技术已经很成熟的方案(s波段方案和x波段方案):s波段加速管已经在市场上广为应用。发明人在研制过程中,基于商用的s波段加速管进行了修改,并改进了原来的运行模式,通过在s波段加速管的电子束出口添加栅栏结构,对电子束进行部分截取,可以得到符合要求的高亮度电子束。另一方面,国际上很多大型电子加速装置的注入器都能产生高亮度电子束,例如同步辐射、自由电子激光等。相关技术已经非常成熟,x波段方案将基于这些已有的高亮度电子束产生方法。在本发明的研制过程中,发明人设计了能量范围在2~10mev的多腔电子枪,并具有小于1毫米毫弧度的发射度。图3所示是在实验室中,在z=0,加速场为200mv~400mv的情况下,x波段(11.424ghz)加速器产生的模拟高亮度电子束的束斑及发射度参数图,其具体数值可以参见表1。图中显示出光阴极射频枪发射的携带200pc电荷的调整良好的电子束可以在小型真空管(即电子束管道)中行进较长的距离,例如为10~40厘米。该加速器具有x波段加速管,x波段加速管的电子束出口设置有用于对高亮度电子束进行部分截取的栅栏结构。另外,在小型真空管(即电子束管道)的末端,可以连接少量电子束散射的薄而低原子序数的材料(例如钛或铍)。通过在电子束管道的前端设置钛窗或铍窗作为出射窗口,可以将高亮度电子束更好地从电子束管道引出。ec[mv/m]εx[μm]σx[mm]b0[t]射束能量[mev]2000.420.120.364.72500.320.080.475.83000.260.070.557.04000.200.049.340表1x波段加速器设计产生的电子束参数2.电子束的传输由于紧凑型加速器的横向尺寸较小,使得外加聚焦磁铁变得非常容易,从而可以很好地将发射度小于1毫米毫弧度的电子束聚焦并传输超过50厘米的距离而无丢失。电子束被加速管(s波段加速管或者x波段加速管)加速到足够的能量后,其计量将高达10~100gy/min,最后被真空低损地传输至患者病灶。电子束管道用于对高亮度电子束进行真空低损传输。它使用钛窗或铍窗作为高亮度电子束的出射窗口。电子束管道的直径为毫米级,长度可以在1~100厘米之间。电子束管道要求有足够的刚性且无磁性,真空对接部分需要可重复拆卸。这些技术可以参考已有的高能物理和医疗器械技术实现,在此不予赘述。电子束从电子束管道真空低损甚至无损传输到外界,现有的钛窗技术和铍窗技术等基本满足要求。此外,在高亮度电子束的传输过程中,有时还需要使用对高亮度电子束进行聚焦或方向引导的磁铁。例如,被加速的高亮度电子束经聚焦磁铁聚焦后进入电子束管道,或者,进入电子束管道内部的电子束在磁铁的引导下进行方向调整。3.高亮度电子束的消融能力在上述实施例中,采用x波段(11.424ghz)加速器,由射频枪产生携带200pc电荷的高亮度电子束,可以进入一个细长的真空管中(长度在10~40厘米之间),在真空管的末端连接一个低原子序数的具有极低电子散射的铍管或钛管(也称为钛窗或铍窗),用于向肿瘤处引出高亮度电子束。一般情况下,对于一个可以产生200pc的4mev、重复频率为100hz的紧凑型加速器,每秒可以产生80j的能量。假设所有能量沉积到1立方厘米的体积中,产生的剂量约为80gy/s,这肯定可以杀死几乎任意的癌变组织,也就是说一个患病部位理论上在一秒之内就可以达到处方剂量,完成肿瘤治疗。4.辐射防护本发明中,只需要使用紧凑型加速器就能实现所要求的技术效果,这使得辐射防护变得非常容易。根据估算,3厘米厚的铅板足以屏蔽电子产生的辐射,从而不再需要非常昂贵的治疗室。通过对整个仪器进行蒙特卡洛模拟,系统分析剂量的分布并在实验上验证,可以采用局部屏蔽的方法对本精确放射治疗系统进行辐射防护,从而尽可能减少屏蔽材料的重量,最终可以使整个精确放射治疗系统的重量控制在20公斤以内。此外,整个精确放射治疗系统无需要在隔离室中运行,在不需要额外屏蔽的同时,能保证医护人员免受辐射的威胁。在本精确放射治疗系统的一个实施例中,电子枪、加速管以及电子束引出设备等都可以采用现有成熟的紧凑设计,以减轻整机的重量,提高仪器的稳定性和可操作性。该精确放射治疗系统的紧凑设计使电子束的产生、传输以及仪器辐射的防护变得非常简单。需要说明的是,本发明所提供的精确放射治疗方法及系统(即“电子消融刀”)不同于现有的术中放射治疗,也不同于常规加速器电子束外照射。它和其他肿瘤消融方法的比较参见表2。表2电子消融刀与其他肿瘤消融方法的比较其中,术中放射治疗是指在手术创口区照射残存肿瘤细胞或组织,通常作为手术后的补充照射使用。常规加速器的电子束外照射是使电子束穿过正常组织到达肿瘤,路径中会对正常组织造成损伤,同时照射深度有限。手术切除损伤大,护理麻烦。氩氦刀针较粗,损伤大,给患者带来痛苦也大,同时受血管、肠管等影响,多针插入,患者难以承受。射频针也较粗,热效应损伤大,温度控制困难,容易复发,同时需要避开血管、肠管。激光消融的创口大,损伤范围有限,患者痛苦大。与它们不同的是,本发明所提供的“电子消融刀”治疗技术,通过细长的电子束管道将经过加速和聚焦的高亮度电子束直接传输到肿瘤处进行消融。它可以直接将电子沉积到肿瘤处,直接消融身体浅表和深部的肿瘤。经过单次或多次照射,可以达到类似外科切除的治疗效果。使用该“电子消融刀”治疗技术对肿瘤进行精确消融,消融次数少,单次剂量高,损毁直接;并且,在整个传输路径上电子不与正常组织发生相互作用,能量损失非常小,同时电子直接与肿瘤直接相互作用,射线利用率高。在本发明所提供的精确放射治疗系统中,用于传输高亮度电子束的管道很细,只有几个毫米,经皮穿刺对组织的损伤非常小。除了上述优点外,本发明还具有占用空间较小、不需要带有防护的机房、不产生伽马射线等优点。以上对本发明所提供的基于高亮度电子束的精确放射治疗方法及系统进行了详细的说明。对本领域的一般技术人员而言,在不背离本发明实质精神的前提下对它所做的任何显而易见的改动,都将构成对本发明专利权的侵犯,将承担相应的法律责任。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1