一种鞘氨醇激酶1抑制剂在制备用于预防和/或治疗脑出血后继发性脑损伤的药物中的应用的制作方法
本发明涉及一种鞘氨醇激酶1抑制剂在制备用于预防和/或治疗脑出血后继发性脑损伤的药物中的应用,属于医药技术领域。
背景技术:
脑出血,是一种突然发病的血液循环障碍疾病,临床上表现为一过性或永久性功能障碍,是脑卒中重要类型。中国人群脑出血致死患者约占脑血管病致死患者的61.7%,其高发病率和死亡率已成为国人首要致死疾病。目前认为脑出血后继发性脑损伤是主要损伤机制,包括红细胞降解产物的神经毒性、凝血酶、炎症、水肿、血脑屏障破坏等,上述因素导致发生凋亡、坏死、自噬等细胞死亡而造成不可逆神经损伤。因此保护神经细胞免受死亡是改善继发性脑损伤进而保护脑出血的重要途径。
尽管脑出血病理生理研究已有巨大进步,但有效治疗手段尚局限于手术清除血肿、脱水、降颅压、神经保护。从疗效上看,无论是手术治疗还是药物干预,脑出血的病死率仍然居高,复发率、并发症、后遗症仍很多。为了解决以上存在的问题,人们一直在寻求一种理想的技术解决方案。
鉴于此,本发明提供一种鞘氨醇激酶1抑制剂在制备治疗脑出血后继发性脑损伤药物中的应用,以解决上述问题。目前,鞘氨醇激酶1抑制剂在脑出血后继发性脑损伤中的作用尚未见报道。
技术实现要素:
本发明的目的在于克服现有技术的不足,提供一种鞘氨醇激酶1抑制剂在制备用于预防和/或治疗脑出血后继发性脑损伤的药物中的应用。
为实现上述目的,本发明采取的技术方案为:一种鞘氨醇激酶1抑制剂在制备用于预防和/或治疗脑出血后继发性脑损伤药物中的应用,所述鞘氨醇激酶1抑制剂为5c,所述鞘氨醇激酶1抑制剂5c的结构式为:
鞘氨醇激酶1(sphingosinekinase1,sphk1),是促进神经鞘磷脂代谢为1-磷酸鞘氨醇(1-phosphatesphingosine,s1p)的关键酶。已知s1p具有细胞内外双重作用,可通过激活细胞外的s1p的多种受体(s1pr1-s1pr5)调节多种生理活动包括细胞迁移、增殖、分化、血管再生及神经发育的功能,也可作为第二信使调节细胞内钙离子水平的稳定、促进细胞增殖、抑制细胞凋亡。
有研究均表明抑制鞘氨醇激酶1(sphk1)表达可抑制1-磷酸鞘氨醇(s1p)活性,从而调节神经递质的释放、抑制炎症反应、抑制神经元凋亡等,进而使得sphk1在多种神经系统疾病中发挥保护作用。因此,通过使用鞘氨醇激酶1的抑制剂减少s1p的生成,有望成为脑出血的一种有效治疗手段。
作为本发明所述的应用的优选实施方式,所述的鞘氨醇激酶1抑制剂用于改善脑出血后的神经功能损伤。
作为本发明所述的应用的优选实施方式,所述的鞘氨醇激酶1抑制剂用于改善脑出血后的运动功能损伤。
作为本发明所述的应用的优选实施方式,所述的鞘氨醇激酶1抑制剂用于抑制脑出血后的炎症因子表达。
作为本发明所述的应用的优选实施方式,所述脑出血后的炎症因子包括il-1β、tnfα和il-6。
作为本发明所述的应用的优选实施方式,所述的鞘氨醇激酶1抑制剂用于减少脑出血后活化小胶质细胞的数量。
所述鞘氨醇激酶1抑制剂用于抑制因脑出血继发性脑损伤后小胶质细胞活化诱导的炎症反应。
作为本发明所述的应用的优选实施方式,所述的鞘氨醇激酶1抑制剂用于减少脑出血后神经元死亡的数量。
作为本发明所述的应用的优选实施方式,所述的鞘氨醇激酶1抑制剂用于抑制脑出血后神经元铁死亡。
另外,本发明的另一目的是提供一种药物组合物,所述药物组合物包括鞘氨醇激酶1抑制剂和药学上可接受的载体,所述鞘氨醇激酶1抑制剂的结构式为:
本发明的另一目的是提供所述的药物组合物在制备用于预防和/或治疗脑出血后继发性脑损伤药物中的应用。
与现有技术相比,本发明的有益效果为:本发明提供的一种鞘氨醇激酶1抑制剂在制备用于预防和/或治疗脑出血后继发性脑损伤的药物中的应用,将现有的鞘氨醇激酶1抑制剂5c应用于制备预防和/或治疗脑出血后继发性脑损伤的药物方面,不仅为制备预防和/或治疗脑出血后继发性脑损伤的药物提供了一种新来源,同时也发掘出了鞘氨醇激酶1抑制剂5c的新的药用价值。
附图说明
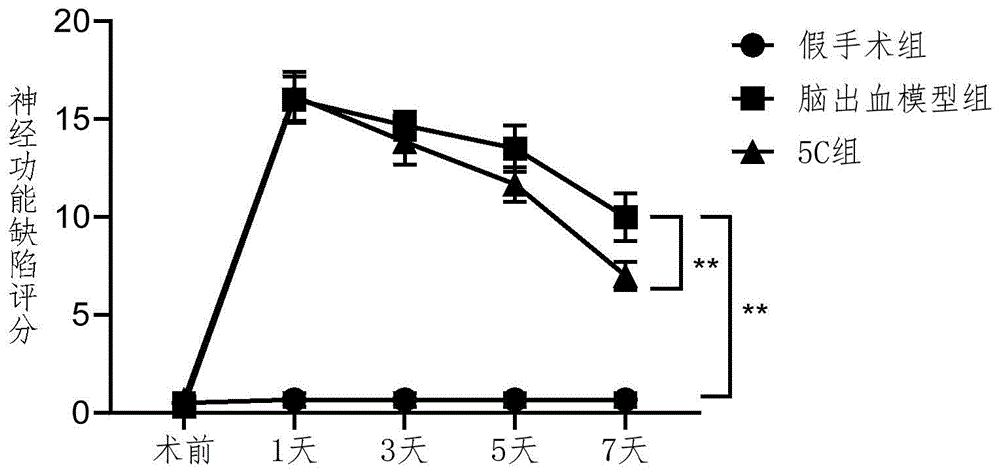
图1为本发明所述的鞘氨醇激酶1抑制剂5c改善脑出血后的神经功能损伤的结果图。
图2为本发明所述的鞘氨醇激酶1抑制剂5c改善脑出血后的运动功能损伤的结果图。
图3为本发明所述的鞘氨醇激酶1抑制剂5c抑制脑出血后的炎症因子(il-1β、tnfα和il-6)表达的结果图。
图4为本发明所述的鞘氨醇激酶1抑制剂5c减少脑出血后活化小胶质细胞的数量的结果图。
图5为本发明所述的鞘氨醇激酶1抑制剂5c减少脑出血后神经元死亡的数量的结果图。
图6为本发明所述的鞘氨醇激酶1抑制剂5c抑制脑出血后神经元铁死亡结果图。
具体实施方式
为更好地说明本发明的目的、技术方案和优点,下面将结合具体实施例对本发明作进一步说明。
实施例1
本实施例为鞘氨醇激酶1抑制剂5c对脑出血后继发性脑损伤的保护作用的研究试验
1.试剂及动物
1.1试剂:鞘氨醇激酶1抑制剂5c(caymanchemical,美国),由恒顺成生物有限公司代购,cas编号120005-55-2,pubchem识别号11305122,纯度>98%,其分子量为435.65,分子式为c26h45no4,保存条件:-20度、避光,分子结构式为:
il-6、il-1β和tnfα的elisa检测试剂盒(南京建成生物工程公司,批号分别为e20160628、20171134b、20170945b);iba-1多克隆抗体(批号66827-1-ig)购于proteintech公司;tf多克隆抗体(批号ab47981)购于abcam公司;gpx4酶活性检测试剂盒和dcfh-da荧光探针均购自碧云天生物技术有限公司;脑立体定位仪、高速颅骨磨钻(瑞沃德生命科技有限公司,深圳),冰冻切片机(thermonx50,美国);酶标仪(biotek/elx808,美国);荧光显微镜(leicadm4b,德国);旷场实验平台(欣软科技,上海);垂直电泳-转膜系统(bio-rad公司;美国);凝胶成像仪(上海天能科技有限公司,中国);荧光显微镜(leicadm4b,德国);sts-3脱色摇床(上海琪特分析仪器有限公司,中国);雪科制冰机(常熟市雪科电器有限公司,中国);高速离心机(eppendorf公司,德国)。
1.2实验动物:c57bl/6:spf级,雄性,36只,体重:18.5~22.6g,长沙斯莱克实验动物有限责任公司,生产许可证号:scxk(湘)2016-0002。动物饲养于桂林医学院附院医院spf级实验动物中心,实验动物室温度20~26℃(日温差≤4℃),湿度40%~70%,照明12h:12h明暗交替。
2.实验内容
2.1动物分组:假手术组、脑出血模型组、鞘氨醇激酶1抑制剂5c组,小鼠脑出血造模后,根据组别随机分配。
2.2上述各分组的剂量设计如下表1所示。
表1
2.3试验方法:脑出血模型采用自体血注射法。
手术操作如下:雄性c57bl/6小鼠通过10%水合氯醛(40mg/kg)腹腔注射麻醉,麻醉后将小鼠置于脑立体定位仪上固定,根据小鼠脑图谱定位右侧脑基底节进针点,具体位置为前颅起,前后:-0.0mm,左右:+1.0mm,深度:-3.0mm。钻孔至硬脑膜,将小鼠尾部脱毛后,用酒精摩擦使尾部血管膨胀,同时按住尾部根部使血液不能回流使尾动脉血充盈,用消毒后的手术刀片将尾动脉割破,使血液滴落一张蜡纸上后用微量进样针抽取约20μl的动脉血后以2μl/min的速度匀速注血,待注射10μl后留针5min后将针向上拔出约0.5mm后继续将余下的动脉血注射完毕后,留针10min后退针。骨蜡封闭骨空并缝合头皮。对照组采用相同的方法从右侧基底节脑注入等量生理盐水,其余处理相同。
2.4观察指标
2.4.1一般状态观察:观察时间和频率:给药后每天固定时间观察1次;观察结果:给药期受试动物整体状态,包括但不限于给药局部反应。
2.4.2神经功能损伤评分:评分时间:于给药前对造模动物进行神经功能损伤行为学评分;评分方法:采用28分评分法。
具体如下:身体对称性(0-4分),步态(0-4分),45度攀爬实验(0-4分),转圈实验(0-4分),前肢对称性(0-4分),强迫转圈(0-4分),触须反应(0-4分)。0分为正常,4分为严重障碍。综合以上分数为该实验最终得分,以综合得分在5-15分作为纳入标准。
2.4.3运动功能评价:通过旷场实验评价各组小鼠运动功能情况,旷场设备由开口的方形盒子构成(长×宽×高为:45cm×45cm×45cm)。将小鼠面朝一个特定的方向放入旷场箱中央,让其自由探索10min,并通过软件进行运动轨迹的自动追踪和小鼠的运动路程、运动速度等参数的分析,最后通过对应软件统计小鼠的运动量。
2.4.4脑出血后炎症因子表达:脑出血造模7天后,通过elisa检测各组损伤周边脑组织炎症因子表达水平。
具体如下:损伤周边脑组织100mg,按50mg:1ml加入冷生理盐水,冰浴下匀浆5min,于4℃下2000r/min离心15min,分离出上清,取1ml均分2份,置于-80℃冰箱待测。炎症因子il-1β、tnfα和il-6用elisa试剂盒检测,具体操作按说明书进行,结果以10-5g/g湿重脑组织表示。
2.4.5脑出血后小胶质细胞活化:脑出血造模7天后,通过免疫组化检测各组炎症相关的i型小胶质细胞活化。
具体如下:将小鼠麻醉,用预冷的生理盐水灌流后,再用4%的多聚甲醛固定,30%的蔗糖溶液脱水;当样本彻底脱水后即开始切片,厚度为20μm,用pbs洗脑片,每次5min,共3次,驴血清室温封闭脑片2h,加入相应iba-1一抗4℃过夜;然后再用pbs清洗,每次5min,共3次,加入相应的二抗后室温孵育2h;再用pbs清洗,每次5min共3次,最后封闭液封片,在荧光显微镜下观察。
2.4.6脑出血后血肿周边区神经元铁死亡:脑出血造模7天后,各组按2.4.5方法取脑,冰冻切片后脑组织通过nissl染色检测损伤周边区神经元损伤程度。各组按2.4.4方法取脑,通过elisa法检测gpx4酶活性、ros水平,通过westernblot检测转铁蛋白表达水平。
3.统计分析
试验数据以mean±sem表示,两组之间采用studentt检验,三组之间采用one-wayanova检验(m-w法)对组间差异进行比较。统计学分析结果p<0.05认为有显著性差异,p<0.01认为有极显著性差异。
4.试验结果
4.1神经功能损伤评分:结果如图1所示,由图1可知,脑出血7天后,脑出血模型组神经功能损伤评分显著性高于假手术组(**p<0.01);而鞘氨醇激酶1抑制剂5c组与脑出血模型组比较,神经功能损伤评分显著降低(**p<0.01),由此说明,本发明所述的鞘氨醇激酶1抑制剂5c能有效改善脑出血后的神经功能损伤。
4.2运动功能评价:结果如图2所示,由图2可知,脑出血7天后,与假手术组,脑出血模型组运动功能显著损伤(**p<0.01);鞘氨醇激酶1抑制剂5c组与脑出血模型组比较,显著改善运动功能(**p<0.01),由此说明,本发明所述的鞘氨醇激酶1抑制剂用于改善脑出血后的运动功能损伤。
4.3炎症因子表达水平:结果如图3所示,由图3可知,脑出血7天后,脑出血模型组炎症因子il-1β、tnfα和il-6均显著性高于假手术组(**p<0.01);鞘氨醇激酶1抑制剂5c组与脑出血模型组比较,炎症因子表达水平显著下降(*p<0.05),由此说明,本发明所述的鞘氨醇激酶1抑制剂用于抑制脑出血后的炎症因子表达。
4.4小胶质细胞激活情况:结果如图4所示,由图4可知,脑出血7天后,脑出血模型组中处于活化状态的小胶质细胞数量显著增加(**p<0.01);鞘氨醇激酶1抑制剂5c组与脑出血模型组比较,活化状态的小胶质细胞数量显著下降(*p<0.05),由此说明,本发明所述的鞘氨醇激酶1抑制剂用于减少脑出血后活化小胶质细胞的数量。
4.5神经元损伤情况:结果如图5所示,由图5可知,脑出血7天后,脑出血模型组中神经元的数量显著减少;鞘氨醇激酶1抑制剂5c组与脑出血模型组比较,神经元数量显著升高,由此说明,本发明所述的鞘氨醇激酶1抑制剂用于减少脑出血后神经元死亡的数量。
4.6神经元铁死亡水平:结果如图6所示,由图6可知,脑出血7天后,脑出血模型组中铁死亡相关指标gpx4酶活性显著下降(**p<0.01)、ros水平显著升高(**p<0.01)而转铁蛋白水平显著升高(**p<0.01);鞘氨醇激酶1抑制剂5c组与脑出血模型组比较,铁死亡相关指标gpx4酶活性显著升高(**p<0.01)、ros水平显著下降(**p<0.01)而转铁蛋白水平显著下降(**p<0.01),由此说明,本发明所述的鞘氨醇激酶1抑制剂用于抑制脑出血后神经元铁死亡。
5.结果
本试验采用自体血注射脑出血模型,模拟临床上脑实质脑出血,研究鞘氨醇激酶1抑制剂5c(2mg/kg)对脑出血后继发性脑损伤的保护作用及机制,本试验发现鞘氨醇激酶1抑制剂5c显著抑制炎症因子表达、抑制小胶质细胞活动及减少神经元铁死亡,最终改善脑出血后继发性脑损伤。
综上表明,本发明提供的一种鞘氨醇激酶1抑制剂在制备用于预防和/或治疗脑出血后继发性脑损伤的药物中的应用,将现有的鞘氨醇激酶1抑制剂5c应用于制备预防和/或治疗脑出血后继发性脑损伤的药物方面,所述的鞘氨醇激酶1抑制剂用于改善脑出血后的神经功能损伤、用于改善脑出血后的运动功能损伤、用于抑制脑出血后的炎症因子(il-1β、tnfα和il-6)表达、用于减少脑出血后活化小胶质细胞的数量、用于减少脑出血后神经元死亡的数量以及用于抑制脑出血后神经元铁死亡,从而为制备预防和/或治疗脑出血后继发性脑损伤的药物提供了一种新来源,同时也发掘出了鞘氨醇激酶1抑制剂5c的新的药用价值。
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
- 还没有人留言评论。精彩留言会获得点赞!