一种近红外光响应抗菌涂层及制备方法
1.本发明属于生物医用材料,尤其涉及一种新型的近红外光响应的抗菌涂层和制备方法。
背景技术:
2.目前,院内感染已经被认为是医院发病率和死亡率的重要原因,特别是可植入性医疗设备(如留置针和留置管)的细菌感染,不仅增加了患者的发病率和死亡率,还可能会导致严重的公共卫生健康问题。为了防止与植入性医疗设备相关的感染,在生物医学材料表面建造抗菌涂层已被认为是减少细菌粘附,从而抵抗生物膜形成的一种简单而有效的方法,许多杀菌剂已被用于制造抗菌涂层,如季铵盐、抗菌肽、银、酶等。但季铵类化合物在长期使用后具有诱导细菌耐药性的风险,导致抗菌效果下降。抗菌肽具有高效的抗菌能力,但其诸多缺点如合成困难,应用复杂和成本高昂等问题,限制其在医学材料上的应用。金属离子如银离子等表现出高效的杀菌性能,且具有广谱抗菌性,但是其对某些哺乳动物细胞具有严重的毒副作用,使其在生物体内的应受到限制。
3.一些具有细胞毒性的气体分子(如:活性氧,一氧化氮,一氧化碳,硫化氢等)具有广谱抗菌性,可以有效杀灭耐药菌,且不易诱发细菌耐药性。一氧化碳(co)气体曾被认为对人体具有毒副作用,但是近期的研究证明它们可参与多种生理和病理过程,具有多重生物学功能。已证实,co气体可以靶向细菌呼吸链进而增强活性氧(ros)的产生、对细菌膜结构的破坏以及干扰细菌dna合成等过程。co释放分子(corms)已被整合应用至各种纳米材料,使其具备智能响应性co诊疗功效。但传统的corms可控性较差,很难实现精准的时空控释效果,进而使其诊疗效果不佳且伴有一定的潜在毒性,使其在临床应用中受到阻碍。相比较而言,羰基铁作为一种热敏性co供体,在光热辐射条件下,fe-co配位键会发生断裂,进而释放co分子,可以通过对温度的精确调控,实现安全可控的抗菌疗效。但是羰基铁的水溶性较低,稳定性较差且不具有目标选择性,使其抗菌效果受到限制。
技术实现要素:
4.发明目的:本发明的第一目的是提供一种具有光热治疗与co协同抗菌的近红外光响应抗菌涂层;本发明的第二目的在于提供上述抗菌涂层的制备方法。
5.技术方案:本发明的一种近红外光响应抗菌涂层,该涂层为pda@msn@feco,包括负载于基底上用于光热响应的多巴胺层、负载于多巴胺层上的介孔二氧化硅以及负载于介孔二氧化硅孔道内的用于释放一氧化碳的羰基铁。
6.进一步的,所述介孔二氧化硅的平均粒径为100~500 nm,内部孔道的孔径范围为2~5 nm;所述羰基铁的负载量为10~20 wt%,负载量具体是指羰基铁占msn@feco总质量的质量百分比。
7.进一步的,所述羰基铁为fe(co)5或fe3(co)
12
。
8.进一步的,所述基底选自钛合金、镁合金、留置针、留置管、聚氨酯、无纺布和硅片
中的任一种。
9.本发明还保护一种近红外光响应抗菌涂层的制备方法,包括以下步骤:(1)将乙醇和去离子水混合,再加入氨水溶液和烷氧基硅烷进行反应,离心洗涤后再分散至去离子水中得到sio2分散液;将阳离子表面活性剂和醇胺加入到去离子水中,80~100℃的温度下搅拌至溶解,加入上述sio2水溶液搅拌后,再逐滴加入烷氧基硅烷,磁力搅拌,离心洗涤,得白色粉末产物,经过萃取、真空干燥得到msn;(2)将msn分散至有机溶剂,在液氮中冷冻、脱气,再加入羰基铁,在避光、n2保护条件下磁力搅拌,离心、洗涤、干燥后得到msn@feco;(3)将基底材料置于含有多巴胺的tris-hcl缓冲液中,磁力搅拌一段时间,用去离子水清洗,干燥后得到表面沉积聚多巴胺的基底材料;(4)将msn@feco分散至含有多巴胺的tris-hcl缓冲液中,加入表面沉积多巴胺的基底材料,磁力搅拌,用去离子水清洗,干燥处理后得到表面沉积pda@msn@feco的基底材料。
10.进一步的,所述步骤(1)中,氨水溶液与烷氧基硅烷的体积比为5~7:1~3;其中,烷氧基硅烷为三甲氧基硅烷、三乙氧基硅烷、四乙氧基硅烷中的一种或两种以上混合。
11.进一步的,所述步骤(1)中,阳离子表面活性剂与醇胺的质量比为80~100:1;其中,阳离子表面活性剂为十六烷基三甲基氯化铵、十二烷基三甲基氯化铵或二者的混合;所述的醇胺为二乙醇胺、三乙醇胺或二者的混合。
12.进一步的,所述步骤(2)中,msn与羰基铁质量比为2~5:1;有机溶剂为二氯甲烷、三氯甲烷或二者的混合。
13.进一步的,所述步骤(3)中,多巴胺的浓度为2~4 mg/ml,磁力搅拌时间为10~24 h,干燥温度为40~60℃,干燥时间为24~48 h。
14.进一步的,所述步骤(4)中,msn@feco的浓度为1~5 mg/ml,磁力搅拌时间为20~30 h,干燥温度为40~60℃,干燥时间为24~48 h。
15.本发明的制备原理为:通过制备介孔二氧化硅纳米粒子(msn),利用负压脱气的方法使羰基铁进入msn孔道,负载热敏性co供体(羰基铁),合成msn@feco纳米材料;利用pda优越的粘合性能,将msn@feco紧密涂敷至基底材料表面,制备一种抗菌涂层pda@msn@feco,在近红外光(nir)照射下,触发pda的光热活性,使体系温度升高,赋予其光热治疗灭菌性能;同时在光热辐射条件下,羰基铁中的fe-co配位键会发生断裂,释放co分子,展现出co的灭菌疗效,最终达到光热治疗与co协同抗菌的目的。
16.本发明将pda的强黏附性和nir光热响应性与纳米材料的低黏附性和羰基铁的热敏性有机结合,多巴胺的邻苯二酚基团和氨基官能团在聚多巴胺的黏附过程中起到主要作用,这种特殊结构可以使聚多巴胺分子与有机或无机表面建立共价或非共价的相互作用,强有力地与材料表面黏附,同时聚多巴胺作为一种优异的光热转换材料,可以吸收nir光源能量,使体系温度升高,而光热效应本身也具有杀菌效果,最终可以实现co和光热治疗协同抗菌疗效。
17.有益效果:与现有技术相比,本发明的显著优点为:本发明制备了一种负载热敏性co供体的msn材料,利用pda涂层的强黏附性,将msn@feco负载至基底层,同时利用pda的光热响应性能,在近红外光照下触发羰基铁释放co分子,展现出良好的光热治疗与co协同抗
菌疗效,本发明可以将光热治疗与co抗菌疗法相统一,实现nir诱导的安全有效且精准可控的抗菌疗效,该抗菌涂层的制备方法简单易行且成本较低,适用于生物医疗领域。
附图说明
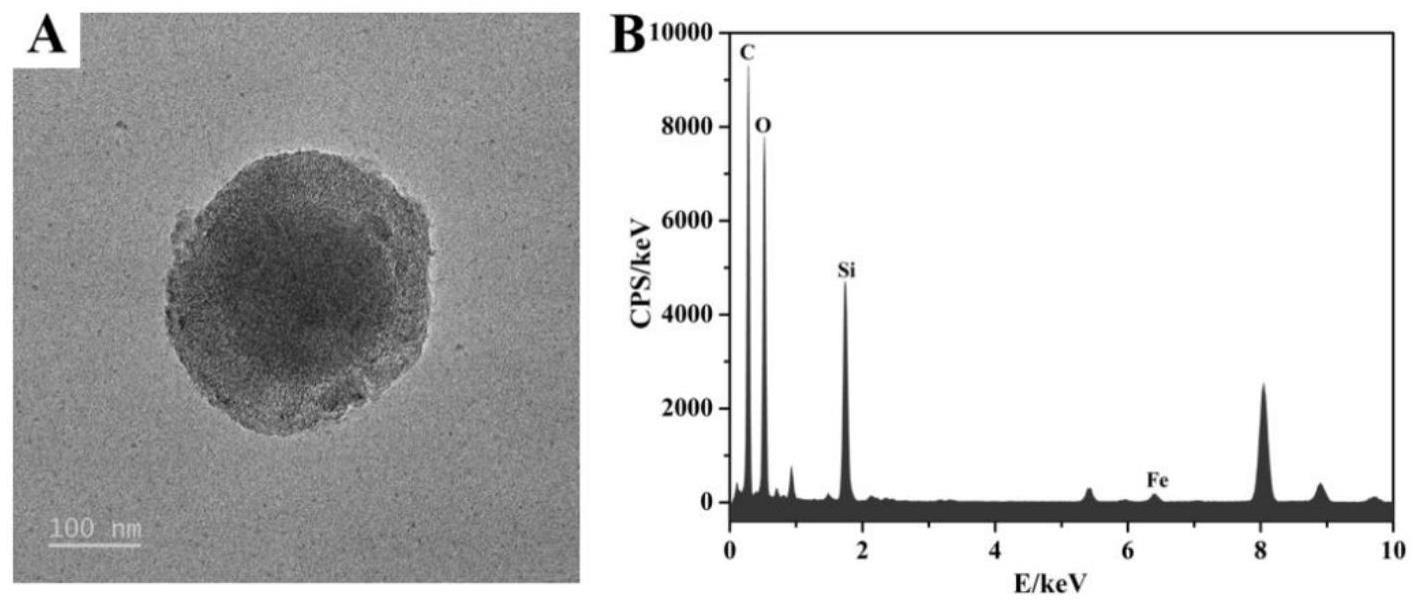
18.图1为msn@feco的透射电子显微镜图和元素能谱图;图2为pda@msn@feco涂层的表征图;图3为留置管、pda以及pda@msn@feco涂层在808 nm红外光照射下的温度变化曲线;图4为pda@msn@feco涂层在808 nm红外光照射下的co释放动力学;图5为留置管、pda以及pda@msn@feco涂层在光照/黑暗条件下金黄色葡萄球菌分布照片;图6为金黄色葡萄球菌的相对细菌存活率柱状图;图7为留置管、pda以及pda@msn@feco涂层在光照/黑暗条件下大肠杆菌分布照片;图8为大肠杆菌的相对细菌存活率柱状图。
具体实施方式
19.下面结合附图和实施例对本发明的技术方案作进一步详细说明。
20.实施例1(1)取150 ml乙醇和3 ml的去离子水混合,常温下搅拌10 min后,加入17 ml浓度为 33%的氨水溶液,搅拌5 min后再加入3 ml的四乙氧基硅烷反应6h,离心水洗,再分散至去离子水中得到sio2分散液;将2 g十六烷基三甲基氯化铵、0.02 g 三乙醇胺与20 ml的去离子水混合,80℃搅拌溶解,加入10 ml上述所得sio2水溶液,搅拌1 h后,逐滴加入0.3 ml的四乙氧基硅烷,搅拌1 h,离心、无水乙醇清洗,用1wt%的nacl甲醇溶液中萃取3 h,重复该过程4次,真空干燥得到msn纳米粒子。
21.(2)将10 mg msn溶于5 ml的三氯甲烷中,液氮下冷冻、脱气后,加入5 mg fe3(co)
12
,避光、n2保护下搅拌24 h,离心,三氯甲烷洗涤,室温干燥12 h得到msn@feco纳米材料。
22.(3)取留置管置于2 mg/ml的多巴胺tris-hcl缓冲液中,磁力搅拌20 h,用去离子水清洗,然后50℃干燥处理36 h,得到表面沉积聚多巴胺层的留置管;将浓度为1 mg/ml 的msn@feco加入20 ml tris-hcl缓冲液配制的盐酸多巴胺溶液,搅拌1 h,将负载聚多巴胺层的留置管置于其中,搅拌24 h,用无水乙醇充分清洗,再用去离子水超声洗涤,放入真空干燥箱50℃干燥24 h,得到负载msn@feco和聚多巴胺涂层的留置管。
23.msn@feco材料的表征参见图1,a表示msn@feco的透射电子显微镜图,b表示msn@feco的元素能谱图;由图可知,msn@feco的透射电子显微镜结果可知其尺寸约为280 nm,同时该纳米粒子壳层结构中有蠕虫状无序的孔道结构,证明其具有介孔结构,孔径约为3nm;此外msn@feco的元素能谱图显示fe元素的存在,证明羰基铁的成功负载。
24.实施例2(1)取120 ml乙醇和3 ml的去离子水混合,常温下搅拌10 min后,加入20 ml浓度
为20%的氨水溶液,搅拌5 min后再加入8 ml的三甲氧基硅烷反应6h,离心水洗,再分散至去离子水中得到sio2分散液;将1.6 g十二烷基三甲基氯化铵、0.02 g二乙醇胺与20 ml的去离子水混合,100℃搅拌溶解,加入10 ml上述所得sio2水溶液,搅拌1 h后,逐滴加入0.3 ml的三甲氧基硅烷,搅拌1 h,离心、无水乙醇清洗,用1wt%的nacl甲醇溶液中萃取3 h,重复该过程4次,真空干燥得到msn纳米粒子。
25.(2)将10 mg msn溶于5 ml的二氯甲烷中,液氮下冷冻、脱气后,加入2 mg fe3(co)
12
,避光、n2保护下搅拌24 h,离心,三氯甲烷洗涤,室温干燥12 h得到msn@feco纳米材料。
26.(3)取留置针置于4 mg/ml的多巴胺tris-hcl缓冲液中,磁力搅拌20 h,用去离子水清洗,然后60℃干燥处理24 h,得到表面沉积聚多巴胺层的留置针;将浓度为3 mg/ml 的msn@feco加入20 ml tris-hcl缓冲液配制的盐酸多巴胺溶液,搅拌1 h,将负载聚多巴胺层的留置管置于其中,搅拌30 h,用无水乙醇充分清洗,再用去离子水超声洗涤,放入真空干燥箱60℃干燥24 h,得到负载msn@feco和聚多巴胺涂层的留置针。
27.实施例3(1)取150 ml乙醇和3 ml的去离子水混合,常温下搅拌10 min后,加入15 ml浓度为15%的氨水溶液,搅拌5 min后再加入5 ml的三乙氧基硅烷反应6 h,离心水洗,再分散至去离子水中得到sio2分散液;将1.8 g十六烷基三甲基氯化铵、0.02 g 三乙醇胺与20 ml的去离子水混合,90℃搅拌溶解,加入10 ml上述所得sio2水溶液,搅拌1 h后,逐滴加入0.3 ml的四乙氧基硅烷,搅拌1 h,离心、无水乙醇清洗,用1 wt%的nacl甲醇溶液中萃取3 h,重复该过程4次,真空干燥得到msn纳米粒子。
28.(2)将10 mg msn溶于5 ml的三氯甲烷中,液氮下冷冻、脱气后,加入3.5 mg fe3(co)5,避光、n2保护下搅拌24 h,离心,三氯甲烷洗涤,室温干燥12 h得到msn@feco纳米材料。
29.(3)取留置管置于3 mg/ml的多巴胺tris-hcl缓冲液中,磁力搅拌20h,用去离子水清洗,然后40℃干燥处理48 h,得到表面沉积聚多巴胺层的留置管;将浓度为5 mg/ml 的msn@feco加入20 ml tris-hcl缓冲液配制的盐酸多巴胺溶液,搅拌1 h,将负载聚多巴胺层的留置管置于其中,搅拌24 h,用无水乙醇充分清洗,再用去离子水超声洗涤,放入真空干燥箱40℃干燥48 h,得到负载msn@feco和聚多巴胺涂层的留置管。
30.对比例1留置管在去离子水和无水乙醇中超声清洗15 min,然后真空干燥24 h。
31.对比例2留置管在去离子水和无水乙醇中超声清洗15 min,然后真空干燥24 h。将留置管置于20 ml tris-hcl缓冲液配制的盐酸多巴胺溶液(2 mg/ml),搅拌24 h,去离子水和无水乙醇清洗,放入真空干燥箱干燥24 h,得到负载聚多巴胺涂层的留置管。
32.pda@msn@feco涂层的表征参见图2,a表示留置管表面的扫描电子显微镜图,b表示pda@msn@feco表面沉积留置管的扫描电子显微镜图,c、d和e表示pda@msn@feco的元素能谱面扫描图;f表示pda@msn@feco的元素能谱图;由图可知,a和b的对比表明pda@msn@feco黏附留置管的表面粗糙度增加,且其表面有明显的纳米粒子聚集,证明msn@feco的成功黏附,且充分洗涤后不影响其表
面黏附量,证明pda@msn@feco涂层具有强稳定性;元素能谱图显示n,si,fe元素的存在,进一步证明pda@msn@feco涂层的成功负载。
33.实施例4pda@msn@feco涂层的光热效果及co释放检测利用808 nm近红外光照射pda@msn@feco涂层验证其光热效果及co释放性能。如图3所示,留置管(对比例1)的温度随光照时间增加没有明显变化,光照10 min后,其温度小于32℃。相比较而言,表面黏附了pda涂层的留置管(对比例2)以及表面黏附了pda@msn@feco涂层的留置管(实施例1)的温度随光照时间增加逐渐升高,光照10 min后,其温度达到50℃左右。该实验结果进一步证明pda具有光热性能,可以吸收近红外光能量转化为热能。
34.以血红蛋白作为co捕获剂,间接检测pda@msn@feco涂层在808 nm近红外光照射下的co释放动力学。如图4所示,对于表面黏附了pda@msn@feco涂层的留置管(实施例1),血红蛋白的吸收峰位置随近红外光照射时间增加逐渐蓝移(430 nm
ꢀ→ꢀ
405 nm),即血红蛋白逐渐向羧基血红蛋白转化,证明该过程中有co气体产生。
35.实施例5pda@msn@feco涂层抑菌效果实验以大肠杆菌和金黄色葡萄球菌菌液的稀释液作为实验菌液,根据gb/t21510贴膜法测定,对实施例1以及对比例1-2制得的材料进行抑菌试验,通过菌落计数法计算抗菌率,数据如图6-8所示,实验结果表明本发明实施例1所得涂层材料在近红外光照射下对金黄色葡萄球菌和大肠杆菌均具有高效的杀灭活性,其抗菌效率可达到98%以上。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1