关节腔注射用雷公藤甲素包合物温变凝胶及其制备方法与流程
1.本发明属于药物制备技术领域,具体涉及一种关节腔注射用雷公藤甲素包合物温变凝胶及其制备方法。
背景技术:
2.类风湿关节炎(rheumatoid arthritis,ra)是一种以多发性关节炎症为主要临床表现的慢性自身免疫性疾病,在我国的患病率较高(0.32%-0.36%),致残率亦较高(60%-70%),且预后较差,严重危害人类生命健康。目前ra的病因尚不明确,一般认为与免疫系统异常、遗传、感染等多种因素有关。ra患者基本病理特点包括滑膜炎与血管生成,一方面滑膜血管增生,并分泌大量细胞因子,引起滑膜组织增厚,破坏软骨和骨结构完整,并侵犯骨关节周围软组织,从而导致关节畸形,另一方面血管生成增多,侵犯人体各器官,如肺心、眼、脾和皮下组织等,随着病程延长,会引起相关脏器功能障碍。主要表现为关节疼痛、肿胀、僵硬、畸形和功能不全等致残率高,不仅影响患者生活质量,还加重家庭负担。
3.临床使用的关节腔注射制剂多是以溶液形式给药,给药后药物迅速渗透到体循环,即从关节腔内快速清除,导致药物在关节腔内作用时间缩短、药效持续时间缩短,需频繁给药,而且渗漏会引起全身吸收,副作用增大。以微球、纳米粒等剂型为主的关节腔注射用缓解制剂普遍存在载药量和包封率较小,制备工艺复杂,无法达到临床使用剂量和工业化生产要求等问题。
4.雷公藤是治疗关节肿痛的传统中药,具有活血化瘀、去湿止痛的作用,含有80种以上有效成分,其中雷公藤甲素(tp)是最主要的免疫抑制与抗炎成分。雷公藤多苷片是临床常用的ra治疗药,雷公藤甲素相比于雷公藤多苷,生化稳定性更好,药物活性更强,相关效价高达100倍以上。但由于tp水溶性差,体内消除快,毒副作用大,极大限制了其在临床的应用。其毒副作用大小与用药量有关,通常用药量越大,毒副作用也就越明显。常见的毒副作用包括胃肠道刺激、生殖系统毒性、皮肤黏膜反应、肝毒病、心律失常、急性中毒等。因此鉴于ra疾病的复杂性、关节腔用注射制剂及tp治疗的缺点,急需一种既能够增加疗效又减轻毒性的新型治疗方案。
技术实现要素:
5.本发明旨在至少在一定程度上解决相关技术中的技术问题之一。为此,本发明的主要目的在于提供一种关节腔注射用雷公藤甲素包合物温变凝胶,旨在解决现有雷公藤甲素在制剂中载药量低、以及传统关节腔给药滞留时间短,需频繁给药的问题。
6.本发明的目的是通过以下技术方案实现的:
7.一种关节腔注射用雷公藤甲素包合物温变凝胶,其包括雷公藤甲素包合物和温变凝胶材料,所述雷公藤甲素包合物的质量与温变凝胶材料的体积比为0.2-0.5g/ml。
8.在某些具体实施例中,所述雷公藤甲素包合物包括包合材料、雷公藤甲素、ph调节剂和冻干保护剂,其中所述包合材料与雷公藤甲素的摩尔比为1:1,所述冻干保护剂的质量
与包合材料、雷公藤甲素和ph调节剂组成的混合物的体积比为15-20mg/ml。
9.在某些具体实施例中,所述包合材料为羟丙基-β-环糊精和磺丁基环糊精中的一种或者其混合物。
10.在某些具体实施例中,所述温敏凝胶材料为泊洛沙姆和透明质酸钠中的一种或者其混合物。
11.进一步,所述泊洛沙姆的质量浓度为18.5-22.5%。
12.进一步,所述透明质酸钠的质量浓度为0.01-0.05%。
13.在某些具体实施例中,所述冻干保护剂为甘露醇和甘氨酸中的一种或者其混合物。
14.本技术的目的在于还提供了一种前述关节腔注射用雷公藤甲素包合物温变凝胶的制备方法,包括如下步骤:
15.1)按配方要求,在搅拌的条件下,将雷公藤甲素溶液加入温度为35-45℃的羟丙基-β-环糊精蒸馏水溶液中,反应2-5h,静置,ph调节剂调节ph至7-8,过滤,过滤所得滤液加入冻干保护剂后进行冷冻干燥,得到雷公藤甲素包合物;
16.2)在3-5℃下将温敏凝胶材料溶胀后,加入步骤1)制备所得的雷公藤甲素包合物,静置过夜,得到雷公藤甲素包合物温变凝胶。
17.进一步:步骤1)中所述冷冻干燥的升温程序为:c1:-40℃,85min;c2:-25℃,60min;c3:-20℃,30min;c4:-15℃,60min;c5:-15℃,30min;c6:-10℃,450min;c7:-10℃,30min;c8:0℃,60min;c9:0℃,30min;c10:15℃,450min,c11:-121℃,程序结束。
18.与现有技术相比,本发明至少具有以下优点:
19.1)本发明所提供的关节腔注射用雷公藤甲素包合物温变凝胶,通过将雷公藤甲素制成包合物,有效增加了雷公藤甲素在凝胶中的载药量;将该雷公藤甲素包合物与温变凝胶材料配合使用,使得该药物在低温或常温下是自由流动的液体,置于体温下(30-35℃)则迅速发生相转变,在用药部位形成半固体状凝胶,有效减少药物突释并延缓药物释放,大大减少了药物突释带来的副作用。
20.2)本发明所提供的关节腔注射用雷公藤甲素包合物温变凝胶的制备方法,工艺简单,符合工业生产要求,便于推广实施。
附图说明
21.为了更清楚地说明本发明具体实施方式,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍。
22.图1为雷公藤甲素微球的体外累积释放曲线;
23.图2为雷公藤甲素纳米粒的体外累积释放曲线;
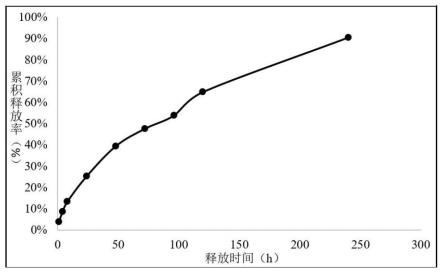
24.图3为本发明所提供的关节腔注射用雷公藤甲素包合物温变凝胶的体外累积释放曲线。
具体实施方式
25.下面结合附图和实施例对本发明作进一步详述,以下实施例只是描述性的,不是限定性的,不能以此限定本发明的保护范围。
26.当以范围、优选范围、或者优选的数值上限以及下限的形式表述某个量、浓度或其它值或参数的时候,应当理解相当于具体揭示了通过将任意一对范围上限或优选数值与任意范围下限或优选数值结合起来的任何范围,而不考虑该范围是否具体揭示。除非另外指出,本文所列出的数值范围值在包括范围的端点,和该范围之内的所有整数和分数。
27.除非另外说明,本文中所有的百分比、份数、比值等均是按重量计。
28.本文的材料、方法和实施例均是示例性的,并且除非特别说明,不应理解为限制性的。
29.下述实施例中,本技术中的羟丙基-β-环糊精选自西安德立生物化工公司;磺丁基环糊精、雷公藤甲素和甘露醇购自上海源叶生物;泊洛沙姆为泊洛沙姆407和188,均购自德国basf公司,其质量浓度为18.5-22.5%;透明质酸钠购自山东众山生物科技有限公司,其质量浓度为0.01-0.05%;甘氨酸购自瑞芬思生物;
30.下述实施例中,其中载药量、包封率和体外释放采用设安捷伦超高效液相色谱仪,安捷伦三重四级杆质谱进行测试,黏度通过赛默飞智能流变仪粘度计进行测试。
31.实施例1
32.本技术所提供的关节腔注射雷公藤甲素包合物温变凝胶通过如下制备方法获得:
33.1)按配方要求,在搅拌的条件下,将摩尔比为1:1雷公藤甲素溶液加入温度为35℃的羟丙基-β-环糊精蒸馏水溶液中,反应5h,静置,ph调节剂调节ph至7.2,用0.45μm微孔滤膜过滤,过滤所得滤液加入冻干保护剂(甘露醇、甘氨酸,其加入的质量与包合材料、雷公藤甲素和ph调节剂组成的混合物的体积比为15mg/ml)后进行冷冻干燥,该冷冻干燥的升温程序为:c1:-40℃,85min;c2:-25℃,60min;c3:-20℃,30min;c4:-15℃,60min;c5:-15℃,30min;c6:-10℃,450min;c7:-10℃,30min;c8:0℃,60min;c9:0℃,30min;c10:15℃,450min,c11:-121℃,程序结束,即得到雷公藤甲素包合物;
34.2)在5℃下将温敏凝胶材料(质量浓度为18.5%的泊洛沙姆407)溶胀后,加入步骤1)制备所得的雷公藤甲素包合物(雷公藤甲素包合物的加入质量与温变凝胶材料的体积比为0.5g/ml),室温下静置过夜,得到雷公藤甲素包合物温变凝胶。
35.实施例2
36.本技术所提供的关节腔注射雷公藤甲素包合物温变凝胶通过如下制备方法获得:
37.1)按配方要求,在搅拌的条件下,将摩尔比为1:1雷公藤甲素溶液加入温度为40℃的羟丙基-β-环糊精(磺丁基环糊精)蒸馏水溶液中,反应3h,静置,ph调节剂调节ph至7.4,用0.45μm微孔滤膜过滤,过滤所得滤液加入冻干保护剂(甘露醇,甘露醇的加入质量与包合材料、雷公藤甲素和ph调节剂组成的混合物的体积比为20mg)后进行冷冻干燥,该冷冻干燥的升温程序为:c1:-40℃,85min;c2:-25℃,60min;c3:-20℃,30min;c4:-15℃,60min;c5:-15℃,30min;c6:-10℃,450min;c7:-10℃,30min;c8:0℃,60min;c9:0℃,30min;c10:15℃,450min,c11:-121℃,程序结束,即得到雷公藤甲素包合物;
38.2)在4℃下将温敏凝胶材料(质量浓度为0.03%的透明质酸)溶胀后,加入步骤1)制备所得的雷公藤甲素包合物(雷公藤甲素包合物的加入质量与温变凝胶材料的体积比为0.2g/ml),室温下静置过夜,得到雷公藤甲素包合物温变凝胶。
39.实施例3
40.本技术所提供的关节腔注射雷公藤甲素包合物温变凝胶通过如下制备方法获得:
41.1)按配方要求,在搅拌的条件下,将摩尔比为1:1雷公藤甲素溶液加入温度为45℃的磺丁基环糊精蒸馏水溶液中,反应2h,静置,ph调节剂调节ph至7.6,用0.45μm微孔滤膜过滤,过滤所得滤液加入冻干保护剂(甘氨酸,甘氨酸加入的质量与包合材料、雷公藤甲素和ph调节剂组成的混合物的体积比为15mg/ml)后进行冷冻干燥,该冷冻干燥的升温程序为:c1:-40℃,85min;c2:-25℃,60min;c3:-20℃,30min;c4:-15℃,60min;c5:-15℃,30min;c6:-10℃,450min;c7:-10℃,30min;c8:0℃,60min;c9:0℃,30min;c10:15℃,450min,c11:-121℃,程序结束,即得到雷公藤甲素包合物;
42.2)在3℃下将温敏凝胶材料(质量浓度为20.5%的泊洛沙姆188)溶胀后,加入步骤1)制备所得的雷公藤甲素包合物(雷公藤甲素包合物的加入质量与温变凝胶材料的体积比为0.3g/ml),室温下静置过夜,得到雷公藤甲素包合物温变凝胶。
43.性能测试:
44.本技术以实施例2为例对本技术制备所得的关节腔注射用雷公藤甲素包合物温变凝胶进行性能测试:
45.1)载药量测试
46.为了比较雷公藤甲素在微球、纳米粒和包合物中的载药量,本技术首先建立了雷公藤甲素的含量测定方法(hplc-ms方法),然后对比了雷公藤甲素在微球、纳米粒和包合物三种新制剂中的载药量。其中,雷公藤甲素在微球、纳米粒中的载药量测定方法为:精密称取适量雷公藤甲素微球或纳米粒于10ml的容量瓶中,加入少量二氯甲烷:甲醇(9:1),使其完全溶解,超声破坏、反复涡旋,待微球或纳米粒内的药物完全溶解,定容至刻度,离心,取上清液0.45μm滤头过滤后进样,采用前述测定方法测定雷公藤甲素实际含量,按下式计算载药量。雷公藤甲素在包合物中的载药量测定方法为:精密称取包合物适量置10ml容量瓶,加入甲醇,超声振荡20min,代雷公藤甲素完全溶解后稀释定容。按下式计算载药量。
47.载药量(%)=制剂中雷公藤甲素的量/制剂总重量
×
100%
48.结果显示,雷公藤甲素在微球中的载药量测得为1.82
±
0.16%;在纳米粒中的载药量测得为1.53
±
0.27%;在包合物中的载药量测得为11.38
±
0.21%。包合物的载药量分别是微球和纳米粒的6.25倍和7.43倍。
49.2)体外释药时间
50.根据建立的雷公藤甲素的含量测定方法(hplc-ms方法),分别采用体外透析袋法和凝胶溶蚀法,然后对比了雷公藤甲素在微球、纳米粒和包合物三种新制剂中的体外释药行为。
51.雷公藤甲素在微球、纳米粒中的体外释药行为测定方法为:称取雷公藤甲素微球或纳米粒约20mg,加入2ml生理盐水,超声使其分散混匀,置预先处理后的透析袋内,紧密封口,悬于10ml释放介质中(pbs,ph=7.40,含1%吐温-80为增溶剂)。释放介质安放于37℃恒温水浴中,磁力搅拌,转速75rpm。分别于1h,4h,8h,1d,2d,3d,4d,5d,10d取释放介质0.5ml(取后补充等量新鲜释放介质),离心取上清液,用0.45μm滤头过滤后,取滤液,测定其中雷公藤甲素的实际含量,并按以下公式计算累积释放量(%)。以q作为纵坐标,释放时间(t)为横坐标绘制体外释放曲线。
52.53.ci:第i个时间点所取样品浓度,v:释放介质总体积,c1:第1次取样时的浓度,v1:第1次取样体积,w:微球或纳米粒中药物的总量。
54.雷公藤甲素在包合物温敏凝胶中的体外释药行为测定方法为:取3ml凝胶样品置具塞试管(w0)中,迅速称重(w1),37℃保存0.5小时,待其完全形成凝胶后加入磷酸盐pbs7.4缓冲液0.5ml,保持凝胶表面不破损,37℃
±
0.5℃恒温水浴振荡(60rpm),分别于1h,4h,8h,1d,2d,3d,4d,5d,10d倾倒出上层溶液,立即擦干试管外壁,称重(w
t
),同时补充0.5ml缓冲液,恒温振荡。将溶蚀液置65℃烘箱内烘干,1mlpbs7.4复溶,0.45μm微孔滤膜过滤,测定其中雷公藤甲素的实际含量,按下式计算药物累积释放百分率q
释放
(%)。
55.q
释放
(%)=(c1×v1
+
……
+ci×vi
)/w
×
100%
56.ci:第i个时间点所取样品浓度,vi:释放介质总体积,c1:第1次取样时的浓度,v1:第1次取样体积,w:包合物温敏凝胶中药物的总量。
57.结果如图1、图2和图3所示,从图中可以看出微球和纳米粒突释现象明显,体外释放曲线表明微球和纳米粒前24h的累积释放量达32.61%和37.93%,包合物温敏凝胶前24h的累积释放量为25.25%,实验结束时(10d),微球和纳米粒的累积释放量仅为62.14%和60.59%,即后续9天的释放量较少,从给药剂量上来考虑较难满足临床用量要求,而包合物温敏凝胶的释放量可达90.46%,包合物凝胶中药物的释放规律呈现突释较小、释放速度比较均匀、释放完全等特点。
58.3)凝胶特性研究
59.包合物温敏凝胶除了在载药量和体外累积释放行为与微球和纳米粒有不同之外,还具有如下特性,比如相转变温度、黏度等,采用旋转流变仪进行测试;将不同处方浓度的雷公藤甲素包合物温敏凝胶装入样品池中,升温范围从15℃-45℃,测试中注意观察凝胶的状态。旋转流变仪测得当泊洛沙姆浓度为p407:p188=19.5%/5%相转变温度约为30-31℃,其在相转变温度之前的粘度为0.05~0.5pa
·
s,相转变温度后的粘度为90-105pa
·
s。提示该凝胶方便注射使用,且当凝胶进入人体后可迅速由液态转变为半固体凝胶,进而使得其可以更好的在关节腔滞留,保证其安全使用效果。这一结果与肉眼观察(精密温度计记录温度)结果一致。黏度测试结果显示,低于相转变温度时黏度较小,呈现出典型的牛顿流体特征,当到达相转变温度时,黏度突然增大,高于相转变温度时,黏度可进一步增大,但增长幅度低于相转变温度时。
60.以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围,其均应涵盖在本发明的权利要求和说明书的范围当中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1