用于治疗精神分裂症的包含2‑((1‑(2‑(4‑氟苯基)‑2‑氧代乙基)哌啶‑4‑基)甲基)异吲哚啉‑1‑酮的组合物的制作方法
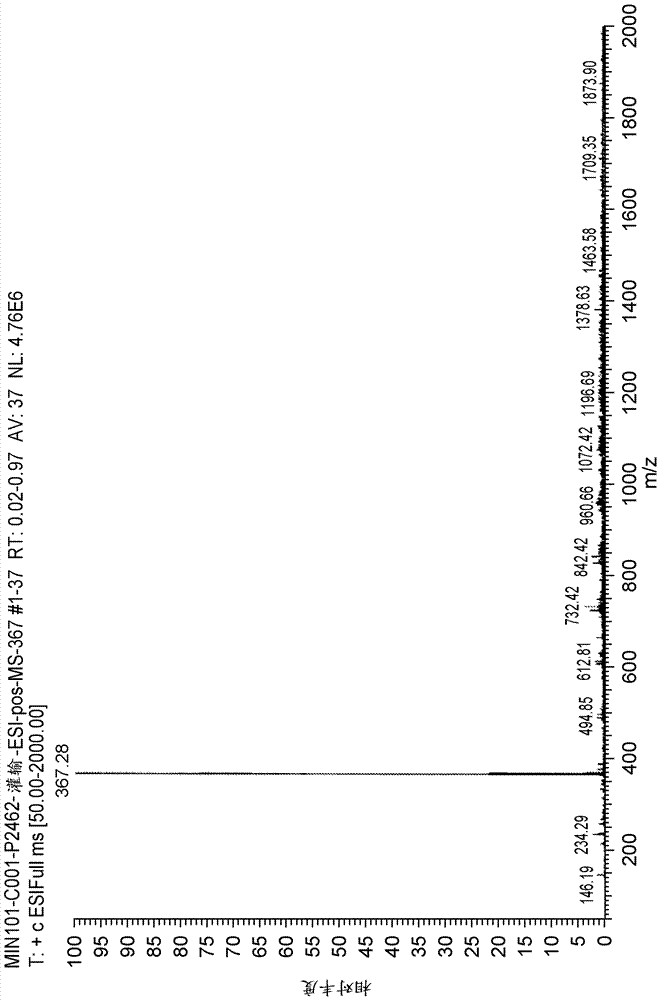
交叉引用本申请要求保护2014年12月2日提交的美国临时申请序列号62/086,691和2015年10月29日提交的美国临时申请序列号62/248,071的益处,每个申请通过引用以其整体并入本文中。在一些实施方案中,本发明涉及用于治疗患者中的精神分裂症的组合物和方法。发明背景根据世界卫生组织(who,2006),精神分裂症是复杂的、挑战性和异质性精神病症,影响到的世界人口高达0.7%。患有精神分裂症的患者存在一系列症状,包括:阳性症状,例如妄想、幻觉、思维障碍和激动;阴性症状,例如心情平缓和日常生活中缺乏乐趣;认知症状,例如理解信息和作出决定的能力下降、难以专注和工作记忆功能降低;和睡眠障碍。精神分裂症的病因尚未完全理解。精神分裂症的病理生理学的一个主要解释性假说是多巴胺(da)假说,其提议da传送的极度活跃对紊乱的表达症状负责。这一假说是基于观察到有效治疗精神分裂症的药物具有阻断dad2受体的共同特征。然而,这些所谓的典型抗精神病药与锥体束外症状(eps)的很高发生率相关。此外,阴性症状和认知损害被认为对典型的抗精神病药相对没有响应。大多数当前批准的用于精神分裂症的疗法主要表现在控制阳性症状中的功效。2012年美国和五大欧盟市场估计有420万人患有精神分裂症。其中估计48%的患者主要经历阴性症状,而80%患有认知损害。此外,约50%的精神分裂症患者经历睡眠障碍,这可能进一步加剧阳性和阴性症状二者。在过去十年中引入所谓的非典型抗精神病药代表了治疗精神分裂症的重大进展。尽管这些非典型抗精神病药在化学结构和受体结合特征上差异很大,但它们具有血清素(5-羟色胺)2型受体(5-ht2a)的有效拮抗作用的特征。与典型的抗精神病药相比,高5-ht2a:d2亲和力比率被认为大大降低了诱导eps的倾向。然而,尽管非典型抗精神病药具有耐受性的优点,但许多患者仍不顺从治疗。尽管非典型抗精神病药的eps风险明显较低,但一些非典型抗精神病药所需的高剂量可能导致eps发生率增加,并需要伴随药剂,例如抗帕金森药物。除eps以外,抗精神病药引起广泛的副作用,包括镇静、抗胆碱能作用、催乳素升高、直立性低血压、体重增加、葡萄糖代谢改变和qtc延长。这些副作用可以影响患者对其治疗方案的顺从性。应当指出,对治疗方案的不顺从性是疾病复发的主要原因。虽然非典型抗精神病药在症状减轻和副作用特征方面提供优于典型抗精神病药的优点,但这些差异通常是适度的。某些患者群体对所有目前可获得的抗精神病药来说仍是难治的。仍在继续寻求解决这些问题的新试剂。本公开提供组合物、方法和试剂盒以解决用于治疗精神分裂症的长期和未满足的需求,其对于所有受试者,特别是那些没有被目前可用的疗法有效治疗的人来说是有效的。本公开的组合物、方法和试剂盒导致更大的患者顺从性。概述本发明提供新型多晶型的化合物(i),(也称为min-101、cyr-101和mt-210),其在精神病的动物模型中显示出有效性(也参见美国专利号7,166,617,其内容以其整体并入本文)。化合物(i)是属于新化学种类的抗精神病药,环状酰氨基衍生物。化学名称是2-((1-(2-(4-氟苯基)-2-氧代乙基)哌啶-4-基)甲基)异吲哚啉-1-酮单盐酸盐二水合物。本文所用的新型多晶型的化合物(i):,2-((1-(2-(4-氟苯基)-2-氧代乙基)哌啶-4-基)甲基)异吲哚啉-1-酮单盐酸盐二水合物也称为形式(a)的化合物(i)∙hcl∙2h2o。在一个实施方案中,形式(a)的化合物(i)∙hcl·2h2o通过xrpd表征。在一个实施方案中,形式(a)的化合物(i)∙hcl∙2h2o通过ir表征。在一个实施方案中,形式(a)的化合物(i)∙hcl·2h2o通过1hnmr表征。在一个实施方案中,形式(a)的化合物(i)∙hcl·2h2o通过13cnmr表征。本公开提供制备形式(a)的化合物(i)∙hcl·2h2o的方法。本公开提供包含形式(a)的化合物(i)∙hcl·2h2o和药学上可接受的稀释剂、赋形剂或载体的药物组合物。本公开提供治疗神经精神疾病或紊乱的方法,包括向有需要的受试者施用治疗有效量的形式(a)的化合物(i)∙hcl∙2h2o或其药物组合物。本公开提供治疗精神分裂症的方法,其包括向有需要的受试者施用治疗有效量的形式(a)的化合物(i)∙hcl∙2h2o或其药物组合物。本公开涉及本发明的药物制剂在制造用于治疗精神分裂症的药物中的用途。本公开提供一种包含药物组合物和使用说明书的试剂盒,所述药物组合物包含形式(a)的化合物(i)∙hcl∙2h2o。除非另有限定,本文使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常理解的相同含义。在说明书中,单数形式也包括复数,除非上下文另有明确规定。尽管与本文所述的那些类似或等同的方法和材料可以用于本公开的实践或试验,但在下文描述合适的方法和材料。本文提及的所有出版物、专利申请、专利和其它参考文献通过引用并入。本文引用的参考文献不被认为是所要求保护的发明的现有技术。在冲突的情况下,将以本说明书(包括定义)为准。此外,材料、方法和实施例仅是说明性,而非限制性。从下面的详述和权利要求中,本公开的其它特征和优点将是显而易见的。附图简述当结合附图阅读时,将更好地理解本发明的上述概述以及以下详述。图1是说明min-101的血浆浓度-时间曲线的曲线图。图2是说明bfb-520的血浆浓度-时间曲线的曲线图。图3是说明bfb-999的血浆浓度-时间曲线的曲线图。图4是通过周期说明min-101、bfb-520和bfb-999的血浆浓度的曲线图。图5是说明bfb-520、bfb-999和cyr-101浓度的qtcf变化的一系列曲线图。图6是说明使用psg和v-watch监视睡眠的方案的图。图7是说明第1部分研究设计的图。图8是说明第2部分研究设计的图。图9是说明研究周期方案的图。图10是说明精神分裂症患者的iib阶段的全球研究设计的图。图11是形式(a)的化合物(i)∙hcl∙2h2o的x射线粉末衍射。图12是形式(a)的化合物(i)∙hcl∙2h2o的ir光谱。图13是形式(a)的化合物(i)∙hcl∙2h2o的1h-nmr光谱。图14是形式(a)的化合物(i)∙hcl∙2h2o的13c-nmr光谱。图15是批次c001和v039ss(来自mtpc的次级参考标准)之间的ir光谱比较。图16是批次c001(来自pcas)的1h-nmr光谱。图17是批次c001(来自pcas)的13c-nmr光谱。图18是通过maldi-tof(来自mtpc)的形式(a)的化合物(i)∙hcl∙2h2o的质谱。图19是通过esi电离批次c001(来自pcas)的形式(a)的化合物(i)∙hcl∙2h2o的质谱。发明详述本公开提供用于治疗神经精神疾病或病症的组合物、方法和试剂盒。优选地,神经精神疾病或病症是精神分裂症。本公开的组合物和试剂盒包括药物组合物。本公开的组合物包含化合物(i)∙hcl∙2h2o的稳定多晶型,其优选为化合物(i)∙hcl·2h2o的形式(a)。化合物(i)的形式a本公开至少部分地涉及化合物(i)∙hcl∙2h2o的稳定多晶型。在一个实施方案中,化合物(i)∙hcl·2h2o的多晶型是形式(a)。在一个实施方案中,形式(a)的化合物(i)∙hcl∙2h2o具有基本上类似于图11所示的x射线粉末衍射图。在一个实施方案中,形式(a)的化合物(i)∙hcl∙2h2o具有在约7.6和14.3°2θ下使用cukα辐射的x射线粉末衍射峰。在一个实施方案中,形式(a)具有在约7.6、14.3和14.7°2θ下使用cukα辐射的x射线粉末衍射峰。在一个实施方案中,形式(a)具有在约7.6、14.3和27.5°2θ下使用cukα辐射的x射线粉末衍射峰。在一个实施方案中,形式(a)具有在约7.6、14.3、14.7和27.5°2θ下使用cukα辐射的x射线粉末衍射峰。在一个实施方案中,形式(a)具有在约7.6、14.3、14.7、18.6和27.5°2θ下使用cukα辐射的x射线粉末衍射峰。在一个实施方案中,形式(a)具有在约7.6、14.3、14.7、14.9、18.6、27.5和30.1°2θ下使用cukα辐射的x射线粉末衍射峰。在一个实施方案中,形式(a)具有在约7.6、11.2、14.3、14.7、14.9、18.6、22.0、25.9、27.5和30.1°2θ下使用cukα辐射的x射线粉末衍射峰。在一个实施方案中,形式(a)的化合物(i)∙hcl·2h2o具有与图12所示基本类似的ir吸收光谱。在一个实施方案中,形式(a)具有在2916cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在1684cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在1665cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在1594cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在1235cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在1684和1665cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在2916、1684和1665cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在2916、1684和1665cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在2916、1594和1235cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在2916、1684、1665和1235cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)具有在2916、1684、1665、1594和1235cm-1下主波吸收数的ir吸收光谱。在一个实施方案中,形式(a)的化合物(i)∙hcl∙2h2o具有基本上类似于图13所示的1hnmr光谱。在一个实施方案中,形式(a)的化合物(i)∙hcl∙2h2o具有基本上类似于图14所示的13cnmr光谱。在一个实施方案中,形式(a)具有在d6-二甲基亚砜中在164.7、166.7、167.6和190.1δ下的13cnmr光谱峰。在一个实施方案中,形式(a)具有在d6-二甲基亚砜中在60.6、167.7、166.7、167.6和190.1δ下的13cnmr光谱峰。在一个实施方案中,形式(a)具有在d6-二甲基亚砜中在50.2、60.6、167.7、166.7、167.6和190.1δ下的13cnmr光谱峰。在一个实施方案中,形式(a)具有在d6-二甲基亚砜中在46.5、50.2、60.6、167.7、166.7、167.6和190.1δ下的13cnmr光谱峰。本申请还至少部分涉及制备化合物(i)∙hcl∙2h2o的多晶型的方法。在一个实施方案中,本公开涉及制备形式(a)的化合物(i)∙hcl∙2h2o的方法。在一个实施方案中,形式(a)的化合物(i)∙hcl∙2h2o通过以下方法制备,所述方法包括:(1)使化合物(i)的游离碱与盐酸在丙酮中反应;和(2)将粗制化合物(i)在丙酮和水中加热,然后冷却,在减压下过滤和干燥。本公开还至少部分涉及制备化合物(i)∙hcl∙2h2o的高纯度形式的多晶型的方法。在一个实施方案中,化合物(i)∙hcl∙2h2o的高纯度形式的多晶型是形式(a)。在一个实施方案中,形式(a)具有至少90%的纯度。在一个实施方案中,形式(a)具有至少92%的纯度。在一个实施方案中,形式(a)具有至少94%的纯度。在一个实施方案中,形式(a)具有至少95%的纯度。在一个实施方案中,形式(a)具有至少96%的纯度。在一个实施方案中,形式(a)具有至少97%的纯度。在一个实施方案中,形式(a)具有至少98%的纯度。在一个实施方案中,形式(a)具有至少99%的纯度。在一个实施方案中,形式(a)具有至少99.5%的纯度。在一个实施方案中,形式(a)具有至少99.6%的纯度。在一个实施方案中,形式(a)具有至少99.7%的纯度。在一个实施方案中,形式(a)具有至少99.8%的纯度。本公开还至少部分涉及制备具有最少量杂质的化合物(i)∙hcl∙2h2o的多晶型形式的方法。在一个实施方案中,具有最少量杂质的化合物(i)∙hcl∙2h2o的多晶型形式是形式(a)。在一个实施方案中,具有最少量杂质的化合物(i)∙hcl∙2h2o的多晶型形式是形式(a),其中杂质为(ⅴ),,(vi),,或(vii),。在一个实施方案中,形式(a)含有小于3%的杂质(v)、(vi)和(vii)的组合。在一个实施方案中,形式(a)含有小于2.5%的杂质(v)、(vi)和(vii)的组合。在一个实施方案中,形式(a)含有小于2%的杂质(v)、(vi)和(vii)的组合。在一个实施方案中,形式(a)含有小于1.5%的杂质(v)、(vi)和(vii)的组合。在一个实施方案中,形式(a)含有小于1%的杂质(v)、(vi)和(vii)的组合。在一个实施方案中,形式(a)含有小于0.5%的杂质(v)、(vi)和(vii)的组合。在另一个实施方案中,形式(a)含有小于0.5%的杂质(v)。在另一个实施方案中,形式(a)含有小于0.2%的杂质(v)。在另一个实施方案中,形式(a)含有小于0.1%的杂质(v)。在另一个实施方案中,形式(a)含有小于1%的杂质(vi)。在另一个实施方案中,形式(a)含有小于0.5%的杂质(vi)。在另一个实施方案中,形式(a)含有小于0.2%的杂质(vi)。在另一个实施方案中,形式(a)含有小于0.1%的杂质(vi)。在另一个实施方案中,形式(a)含有小于1%的杂质(vii)。在另一个实施方案中,形式(a)含有小于0.5%的杂质(vii)。在另一个实施方案中,形式(a)含有小于0.2%的杂质(vii)。在另一个实施方案中,形式(a)含有小于0.1%的杂质(vii)。本公开还涉及包含化合物(i)∙hcl∙2h2o的多晶型和一种或多种药学上可接受的稀释剂、赋形剂或载体的药物组合物。在一个实施方案中,药物组合物包含形式(a)的化合物(i)∙hcl∙2h2o和一种或多种药学上可接受的稀释剂、赋形剂或载体。本公开还涉及治疗神经精神疾病或紊乱的方法,包括向有需要的受试者施用治疗有效量的化合物(i)∙hcl∙2h2o的多晶型或其药物组合物。在一个实施方案中,本公开还涉及治疗神经精神疾病或紊乱的方法,包括向有需要的受试者施用治疗有效量的形式(a)的化合物(i)∙hcl·2h2o或其药物组合物。在一个实施方案中,神经精神疾病是精神分裂症。术语“多晶型”与“结晶多晶型”、“晶体多晶型”、“晶体形式”和“多晶型形式”同义。各个术语是指化合物(i)∙hcl∙2h2o以特定晶体填充布置结晶的晶体结构,即形式(a),其具有与化合物(i)∙hcl∙2h2o相同的元素组成。由多晶型表现的物理性质的差异影响药物参数,例如储存稳定性、可压缩性和密度(在制剂和产品制造中重要)和溶解速率(生物利用性中的重要因素)。稳定性的差异也可以由化学反应性的变化(例如差异氧化,使得当由一种多晶型组成时,相对于当由另一种多晶型或非晶形式组成时,剂型更快速地变色)或机械性能(例如,当动力学有利的多晶型或非晶形式转化为热力学更稳定的多晶型或非晶形式时,片剂在储存时粉碎)或二者(例如,一种多晶型或非晶形式的片剂在高湿度下更易于粉碎)产生。此外,晶体的物理性质在加工中可能是重要的,例如,多晶型或非晶形式更可能形成溶剂化物,或可能难以过滤和洗涤掉杂质(例如,颗粒形状和尺寸分布可能在多晶型和非晶形式之间是不同的)。分子的多晶型可以通过本领域已知的多种方法获得。这些方法包括但不限于熔融重结晶、熔融冷却、溶剂重结晶、去溶剂化、快速蒸发、快速冷却、缓慢冷却、蒸气扩散和升华。用于表征多晶型的技术包括但不限于差示扫描量热法(dsc)、x射线粉末衍射(xrpd)、单晶x射线衍射、振动光谱(例如ir和拉曼光谱)、tga、dta、dvs、固态nmr、热台光学显微镜、扫描电子显微镜(sem)、电子晶体学和定量分析、粒度分析(psa)、表面积分析、溶解度研究和溶解研究。如本文所用,术语“非晶形式”是指物质的非结晶固态形式。如本文所用,化合物是“稳定的”,其中在恒定的湿度条件(例如10%,20%,30%,40%,50%,60%,70%,75%,80%,85%,90%和95%相对湿度)、曝光和温度(例如高于0℃,例如20℃,25℃,30℃,35℃,40℃,45℃,50℃,55℃,60℃,65℃和70℃)下在一定时间(例如一周、两周、三周和四周)中没有观察到显著量的分解产物。不认为化合物在出现分解杂质或现有杂质的面积百分数(例如,如由hplc表征的auc)开始增长的一定条件下是稳定的。作为时间的函数的分解增长量对于确定化合物的稳定性是重要的。如本文所用,术语“混合”是指结合、共混、搅拌、摇动、旋转或搅动。术语“搅拌”是指混合、摇动、搅动或旋转。术语“搅动”是指混合、摇动、搅拌或旋转。除非另有明确说明,否则术语“大约”和“约”是同义的。在一个实施方案中,“大约”和“约”是指所述量、值或持续时间±20%,±15%,±10%,±8%,±6%,±5%,±4%,±2%,±1%或±0.5%。在另一个实施方案中,“大约”和“约”是指列出的量、值或持续时间±10%,±8%,±6%,±5%,±4%或±2%。在另一个实施方案中,“大约”和“约”是指列出的量、值或持续时间±5%。当叙述xrpd峰使用术语“大约”和“约”时,这些术语是指所述的x射线粉末衍射峰±0.5°2θ,±0.4°2θ,±0.3°2θ,±0.2°2θ,或±0.1°2θ。在另一个实施方案中,术语“大约”和“约”是指列出的x射线粉末衍射峰±0.2°2θ。在另一个实施方案中,术语“大约”和“约”是指列出的x射线粉末衍射峰±0.1°2θ。当叙述温度或温度范围使用术语“大约”和“约”时,这些术语是指所述温度或温度范围±5℃,±2℃或±1℃。在另一个实施方案中,术语“大约”和“约”是指所述的温度或温度范围±2℃。化合物(i)本公开提供化合物(i)的药物制剂:,或其药学上可接受的盐。在一个实施方案中,本公开的制剂提供化合物(i)及其两种活性代谢物(bfb-520和bfb-999)在与改进的治疗响应和较少的不良反应(例如延长qt间隔)相关的水平下的最大血浆浓度(cmax)和曲线下面积(auc)。在一个实施方案中,本公开的制剂提高bfb-999的最大血浆浓度(cmax)和曲线下面积(auc),同时降低bfb-520的最大血浆浓度(cmax)和曲线下面积(auc)。在一个实施方案中,本公开的制剂提供低于50ng/ml、低于45ng/ml、低于40ng/ml、低于35ng/ml、低于30ng/ml、低于25ng/ml、低于20ng/ml、低于15ng/ml或低于10ng/ml的化合物(i)的最大血浆浓度(cmax)。在一个实施方案中,本公开的制剂提供低于400hr*ng/ml、低于350hr*ng/ml、低于300hr*ng/ml、低于250hr*ng/ml、低于200hr*ng/ml、低于150hr*ng/ml或低于100hr*ng/ml的化合物(i)的auc。在一个实施方案中,本公开的制剂提供低于5.0ng/ml、低于4.5ng/ml、低于4.0ng/ml、低于3.5ng/ml、低于3.0ng/ml、低于2.5ng/ml、低于2.0ng/ml、低于1.5ng/ml或低于1.0ng/ml的bfb-520的最大血浆浓度(cmax)。在一个实施方案中,本公开的制剂提供低于40hr*ng/ml、低于35hr*ng/ml、低于30hr*ng/ml、低于25hr*ng/ml、低于20hr*ng/ml、低于15hr*ng/ml或低于10hr*ng/ml的bfb-520的auc。在一个实施方案中,bfb-520与超治疗水平的qt间隔延长有关。在一个实施方案中,为了避免qt延长,化合物(i)和bfb-520的最大血浆浓度(cmax)应当分别不超过80ng/ml和12ng/ml。在一个实施方案中,本公开的制剂提供低于10ng/ml、低于9.0ng/ml、低于8.0ng/ml、低于7.0ng/ml、低于6.0ng/ml,5.0ng/ml、低于4.5ng/ml、低于4.0ng/ml、低于3.5ng/ml、低于3.0ng/ml、低于2.5ng/ml、低于2.0ng/ml、低于1.5ng/ml或低于1.0ng/ml的bfb-520的cmax。在一个实施方案中,本公开的制剂提供低于5.0ng/ml、低于4.5ng/ml、低于4.0ng/ml、低于3.5ng/ml、低于3.0ng/ml、低于2.5ng/ml、低于2.0ng/ml、低于1.5ng/ml或低于1.0ng/ml的bfb-999的cmax。在一个实施方案中,本公开的制剂提供低于40hr*ng/ml、低于35hr*ng/ml、低于30hr*ng/ml、低于25hr*ng/ml、低于20hr*ng/ml、低于15hr*ng/ml或低于10hr*ng/ml的bfb-999的auc。在一个实施方案中,本公开的制剂包含约1-100mg化合物(i)、约1-75mg化合物(i)、约2-75mg化合物(i)、约5-75mg化合物(i)、约10-75mg化合物(i)、约15-75mg化合物(i)、约15-70mg化合物(i)、约15-65mg化合物(i)。在一个实施方案中,本公开的制剂包含约16mg化合物(i)、约32mg化合物(i)、约40mg化合物(i)或约64mg化合物(i)。在一个实施方案中,本公开的制剂适合于慢性施用(例如一周,两周,三周,四周,两个月,四个月,六个月,八个月,十个月,一年,两年,三年,四年和五年)。在一个实施方案中,本公开的制剂每天施用一次。在一个实施方案中,将本公开的制剂在快速条件下施用于受试者。在一个实施方案中,本公开的制剂在受试者进餐后至少4小时,在受试者进餐后至少6小时,在受试者进餐后至少8小时,在受试者进餐后至少10小时,在受试者进餐后至少12小时施用于受试者。在一个实施方案中,本公开的制剂在进食条件下施用于受试者。在一个实施方案中,本公开的制剂在受试者进餐后4小时内,在受试者进餐后3小时内,在受试者进餐后2小时内,在受试者进餐后1小时内或在受试者进餐后0.5小时内施用于受试者。“进餐”是指任何量的食品,包括碳水化合物、蛋白质、氨基酸等的任何来源。在一个实施方案中,本公开的制剂适合于口服施用、静脉内施用、肌内施用或皮下施用。在一个实施方案中,本公开的制剂适合于口服施用。在一个实施方案中,本公开的制剂是片剂或胶囊的形式。在一个实施方案中,片剂制剂包含化合物(i)、释放调节剂、填料、助流剂和润滑剂。在一个实施方案中,释放调节剂是羟丙甲纤维素(例如羟丙甲纤维素k100lvcr、羟丙甲纤维素k4mcr、羟丙甲纤维素e50或其组合)。在一个实施方案中,填料是微晶纤维素、乳糖或其组合。在一个实施方案中,助流剂是无水硅胶。在一个实施方案中,润滑剂是硬脂酸镁、kolliwaxhco、硬脂酰富马酸钠,或其组合。在另一个实施方案中,片剂制剂还可以包含粘合剂,例如羟丙基纤维素。在另一个实施方案中,片剂制剂还可以包含崩解剂,例如交聚维酮。在另一个实施方案中,片剂制剂还可包含抗粘附剂,例如滑石粉。在另一个实施方案中,片剂制剂还可以包含ph调节剂,例如有机或无机酸或有机或无机碱。在另一个实施方案中,片剂制剂还可以包含甜味剂,例如糖(例如甘露醇)。在一个实施方案中,通过改变制剂中释放调节剂的量来控制片剂制剂的释放曲线。在一个实施方案中,化合物(i)从片剂制剂的释放速率通过增加释放调节剂的量而降低。在一个实施方案中,本公开的制剂是立即释放形式。在一个实施方案中,本公开的制剂是调节释放形式。在一个实施方案中,调节释放制剂是缓慢(释放速率为16-24小时)、中速(释放速率为10-12小时)或快速(释放速率为5-7小时)释放形式。在一个实施方案中,本公开的制剂是受控释放形式。在一个实施方案中,本公开的制剂是持续释放形式(例如,释放发生至少4小时、6小时、8小时、10小时、12小时、18小时或24小时)。在一个实施方案中,本公开的制剂是缓慢持续释放形式的形式。本公开还涉及用于治疗神经精神疾病和紊乱,特别是精神分裂症的方法,包括向有需要的受试者施用治疗有效量的本发明的制剂。在一个实施方案中,提供治疗或减少神经精神疾病和紊乱,特别是精神分裂症的至少一种症状的方法,包括向有需要的受试者施用治疗有效量的本发明的制剂。在一个实施方案中,提供治疗或减少精神分裂症的至少一种症状的方法,包括向有需要的受试者施用治疗有效量的本发明的制剂。在一个实施方案中,提供治疗或减少精神分裂症的至少一种症状的方法,包括向有需要的受试者施用本发明的制剂,其中化合物(i)的量在约1-100mg、约1-75mg、约2-75mg、约5-75mg、约10-75mg、约15-75、约15-70mg或约15-65mg范围内。在一个实施方案中,提供治疗或减少精神分裂症的至少一种症状的方法,包括向有需要的受试者施用本发明的制剂,其中化合物(i)的量为约16mg、约32mg、约40mg,或约64mg。在一个实施方案中,施用本公开的制剂用于治疗或减少与精神分裂症、认知功能、睡眠结构和连续性以及社会功能的阴性和/或阳性症状相关的精神分裂症的至少一种症状。在另一个实施方案中,施用本公开的制剂用于改进抑郁症状。在一个实施方案中,提供治疗或减少与抑郁相关的至少一种病症或紊乱的方法,包括向有需要的受试者施用本发明的制剂。在另一个实施方案中,提供一种改进睡眠的方法,例如睡眠结构和连续性,包括向有需要的受试者施用本发明的制剂。在一个实施方案中,提供治疗或减轻患有神经精神疾病和紊乱,特别是精神分裂症的受试者的睡眠障碍的至少一个方面的方法,包括向受试者施用本发明的制剂。在一个实施方案中,治疗睡眠障碍的至少一个方面。在另一个实施方案中,睡眠障碍的至少一个方面得到改进。在一方面,睡眠的至少一个方面的破坏与精神分裂症有关。可以治疗睡眠的各个方面,包括但不限于入睡潜伏期、持续睡眠前的潜伏期、整个睡眠周期时间内的慢波睡眠分布,或睡眠周期时间的一个或多个部分、整体睡眠连续性和睡眠结构。认知损害是思考、集中、制定想法、理性和记忆的能力下降。在一个实施方案中,提供治疗或减少认知损害或改进认知的方法,包括向有需要的受试者施用本发明的制剂。在一个实施方案中,提供治疗精神分裂症而不引起认知损害的方法。在一个实施方案中,提供在用另一种活性药物成分例如抗抑郁化合物停止治疗后,在受试者中治疗精神分裂症并恢复、增强和改进认知的方法。在一个实施方案中,提供一种与认知损害活性药物成分(例如,认知损害抗抑郁化合物)组合治疗精神分裂症而不引起或增加认知损害的方法,或用于改进、增强或恢复受试者中的认知的方法。在另一个实施方案中,存在于患有精神分裂症的受试者中的认知损害通过向受试者施用本发明的制剂来治疗或减少。如基于本文的公开将理解的,睡眠参数的修改可以改进认知。作为非限制性实施例,慢波睡眠(sws)的改进和/或增加改进了认知。在一方面,一般认知得到改进。另一方面,认知的一个或多个方面得到改进,包括记忆巩固、执行功能、言语记忆和言语流畅性等其它方面。在一个实施例中,在受试者中认知被改进到在受试者中恢复正常认知的点。在另一个实施方案中,在受试者中超出受试者中的正常认知点改进认知,使得受试者的认知水平增强。在一个实施方案中,在患有精神分裂症的受试者中改进认知。活性成分是化合物(i)(也称为cyr-101和mt-210)。美国专利号7,166,617(通过引用以其整体并入本文)公开了包括化合物(i),2-{1-[2-(4-氟苯基)-2-氧代乙基]哌啶-4-基甲基}-2,3-二氢异吲哚-1-酮单盐酸盐二水合物的环酰胺衍生物。发现美国专利号7,166,617中公开的衍生物对σ配体结合位点具有高亲和力,和对σ1和/或σ2具有低抑制常数ki。还发现这些化合物具有与常规已知化合物的那些完全不同的选择性结合特征,并且可用于治疗可通过σ配体的神经控制功能治疗性和/或预防性治疗的疾病。本文所述的化合物(i)的制剂表示基于最佳功效、安全性、耐受性和药代动力学特征开发神经精神疗法的定制制剂的重要里程碑。本文所述的制剂能够在治疗阴性症状、认知损害和睡眠障碍中靶向未满足需要的重要领域,同时提供非常有利的安全性特征。本公开的制剂能够在一天的过程中维持化合物(i)的血浆水平,同时降低bfb-520水平和提高与睡眠改进相关的bfb-999水平,由于其对5-ht2a和组胺能h1受体的亲和力。本公开的制剂显示较低水平的bfb-520,其与超治疗水平的qt间隔延长相关。qt间隔表示心室去极化和随后复极化的持续时间,并且从qrs波群的开始到t波的结束测量。心脏复极化的延迟产生有利于心律失常发展的电生理环境,最明显的是尖端扭转型室速(tdp),但也可能是其它室性快速性心律失常。tdp是ecg上作为等电位基线周围的qrs波群的矢量的连续扭转出现的多形性室性快速性心律失常。tdp的特征是在心律失常之前的室上搏动中qt间隔的显著延长。tdp可以退化为心室颤动,导致猝死。根据关于非抗心律失常药物的qt/qtc间隔延长和心律失常潜力的临床评估的ich-e14,如果在用研究药物治疗期间qt/qtc间隔明显延长,特别是如果从多于一个ecg获得测量值,应考虑受试者从临床试验中停止。本公开提供降低qt/qtc延长的风险的最佳制剂,并且实现一天一次的投配方案以促进患者顺从性。定义在其它实施方案中,如本文其它地方更详细阐述的,化合物(i)和/或形式a的化合物(i)的剂量和投配方案可以基于待治疗的受试者的健康和状况以及治疗的期望结果来优化。本文所用的术语“受体”是指可与一种或多种信号分子特异性相互作用的分子。例如,5-ht1a受体是5-ht受体的亚型,其结合神经递质血清素(“5-羟色胺”)。术语“受试者”是指任何动物,包括哺乳动物,例如但不限于人、小鼠、大鼠、其它啮齿动物、兔、狗、猫、猪、牛、绵羊、马或灵长类动物。术语“治疗(treating)”(以及相应的术语“治疗(treat)”和“治疗(treatment)”)包括对受试者的姑息性、恢复性和防止性(“预防性”)治疗。术语“姑息性治疗”是指在不治愈病症的情况下缓解或降低受试者的病症的作用或强度的治疗。术语“防止性治疗”(以及相应的术语“预防性治疗”)是指防止受试者的病症发生的治疗。术语“恢复性治疗”(“治疗性”)是指停止受试者的病症的进展,减少其病理表现或完全消除病症的治疗。可以用治疗有效量的化合物、盐或组合物进行治疗,所述化合物、盐或组合物引起个体如研究者、医生、兽医或临床医生正在寻求的组织、系统或受试者的生物或药物响应。术语“治疗”将理解为不仅包括经治疗个体经历的所有症状的完全缓解,还包括一种或多种现有症状的缓解,以及通过先发性施用式i化合物到易于或可能发展任何症状的个体,例如具有慢性或复发性神经精神疾病或紊乱的个体防止症状的发生。本文所用的术语“调节释放”可以理解为药物从片剂逸出以某种方式改变。通常这是为了减缓药物的释放,使得不必太频繁地服用药物,从而改进顺从性。调节释放的其它益处是药物释放受到控制,且血液水平中的峰和谷较小,从而降低了峰值作用的机会,并增加了较长时间段的治疗有效性的可能性。自调节释放(mr)剂型的药物释放模式从常规(立即释放)剂量制剂的模式故意改变,以实现所需的治疗目标或更好的患者顺应性。mr药物产品的类型可以包括延迟释放(例如肠溶包衣)、延长释放(er)和口腔崩解片(odt)。术语调节释放制剂可用于描述改变药物物质释放时间和/或速率的制剂。调节释放剂型是其中选择时间进程和/或位置的药物释放特征以实现不由常规剂型例如溶液、软膏或立即溶解剂型提供的治疗或方便目的的制剂。认可几种类型的调节释放口服药物产品,包括:延长释放制剂是指允许是立即释放(常规)剂型的剂量频率的至少二分之一的制剂。延长释放剂型的实例包括受控释放、持续释放和长效药物产品。延迟释放制剂是指不在施用后立即释放药物的一个或多个离散部分的制剂。初始部分可以在施用后立即释放。肠溶包衣的剂型是常见的延迟释放产品(例如肠溶包衣阿司匹林和其它nsaid产品)。术语“本公开的多种化合物”或“本公开的化合物”是指本文所述的化合物(i)、形式a的化合物(i)或其药学上可接受的盐。本文关于化合物或组合物使用的术语“药学上可接受的”是指可以增加或增强化合物在受试者中的溶解度或可用性的化合物或组合物的形式,以促进或提高化合物或组合物的生物利用度。术语“药学上可接受的盐”描述一种或多种本文组合物的盐形式,其提供以增加化合物例如在患者的胃肠道的胃液中的溶解度,以便促进化合物和/或组合物的溶解和生物利用度。在一个实施方案中,药学上可接受的盐包括衍生自药学上可接受的无机或有机碱和酸的那些。合适的盐包括衍生自碱金属(例如钾和钠)、碱土金属(例如钙、镁和铵盐)以及制药领域中众所周知的许多其它酸的那些。钠和钾盐特别优选为本公开所涵盖的羧酸和含游离酸磷酸盐的组合物的中和盐。术语“盐”应当指与本公开所涵盖的化合物的用途一致的任何盐。在化合物用于药物适应症,包括治疗抑郁症的情况下,术语“盐”应当指与作为药物试剂的化合物的用途一致的药学上可接受的盐。如本文所用,术语药学上可接受的盐是指保留母体化合物的所需生物活性并表现出最小的(如果有的话)不期望的毒理作用的盐。这些盐的非限制性实例是(a)与无机酸(例如盐酸、氢溴酸、硫酸、磷酸、硝酸等)形成的酸加成盐,以及与有机酸(例如乙酸、草酸、酒石酸、琥珀酸、苹果酸、抗坏血酸、苯甲酸、单宁酸、双羟萘酸、海藻酸、聚谷氨酸、萘磺酸、萘二磺酸和聚半乳糖醛酸)形成的盐;(b)与多价金属阳离子(例如锌、钙、铋、钡、镁、铝、铜、钴、镍、镉、钠、钾等)或与由n,n-二苯甲基乙二胺、铵或乙二胺形成的有机阳离子形成的碱加成盐;或(c)(a)和(b)的组合;例如,单宁酸锌盐等。在一个实施方案中,组合物包含本发明的化合物的碱加成盐。可用作制备本质上呈酸性的本发明的化合物的药学上可接受的碱盐的试剂的化学碱是与这些化合物形成无毒碱盐的化学碱。这种无毒碱盐包括但不限于衍生自这种药理学上可接受的阳离子例如碱金属阳离子(如钾和钠)和碱土金属阳离子(如钙和镁)、铵或水溶性的胺加成盐如n-甲基葡糖胺(葡甲胺)和低级烷醇铵和药学上可接受的有机胺的其它碱盐等的那些。“组合物”或“药学上可接受的组合物”是含有本发明的化合物或其盐、溶剂合物、酯或氨基酸缀合物的制剂。在一个实施方案中,药物组合物是大量或单位剂型。单位剂型是任何各种形式,包括例如胶囊、iv袋、片剂、气雾剂吸入器上的单个泵或小瓶。单位剂量组合物中的活性成分(例如,本发明的化合物或其盐的制剂)的量是有效量并且根据所涉及的具体治疗而改变。本领域技术人员将理解,有时需要根据患者的年龄和状况对剂量进行常规改变。剂量也将取决于施用途径。考虑各种途径,包括口服、眼睛、眼科、肺、直肠、胃肠外、经皮、皮下、静脉内、肌肉内、腹膜内、鼻内等。局部或经皮施用本发明的化合物的剂型包括粉末、喷雾剂、软膏、糊剂、霜剂、洗剂、凝胶剂、溶液剂、贴剂和吸入剂。在另一个实施方案中,活性化合物在无菌条件下与药学上可接受的载体以及所需的任何防腐剂、缓冲剂或推进剂混合。在某些实施方案中,本发明的药物制剂或组合物可以另外含有药物组合物中常规发现的在其技术确定的使用水平下的其它辅助成分。因此,例如,组合物可以含有用于物理配制本发明的组合物的各种剂型的其它物质,例如染料、调味剂、防腐剂、抗氧化剂、遮光剂、增稠剂和稳定剂。然而,这些材料在加入时不应当不适当地干扰本发明的组合物的组分的生物活性。制剂可以消毒,并且如果需要,与辅助剂例如润滑剂、防腐剂、稳定剂、润湿剂、乳化剂、用于影响渗透压的盐、缓冲剂、着色剂、调味剂和/或芳族物质等(不与制剂的寡核苷酸有害相互作用)混合。在某些实施方案中,本发明的药物组合物包含一种或多种赋形剂。在某些这样的实施方案中,赋形剂选自水、盐溶液、醇、聚乙二醇、明胶、乳糖、淀粉酶、硬脂酸镁、滑石、硅酸、粘性石蜡、羟甲基纤维素和聚乙烯吡咯烷酮。在某些实施方案中,使用已知技术制备本发明的药物组合物,包括但不限于混合、溶解、制粒、制糖衣丸、研磨、乳化、包封、包埋或压片过程。化合物的改性可以影响活性物质的溶解度、生物利用度和代谢速率,从而提供对活性物质递送的控制。此外,改性可影响化合物的所需活性,在一些情况下相对于母体化合物增加活性。这可以通过制备衍生物并根据本文包括的方法或本领域技术人员已知的其它方法试验其抗抑郁活性来容易地评估。本文包括的组合物可以口服施用。在其它实施方案中,组合物可以胃肠外、通过吸入喷雾、局部地、直肠、经鼻、经口、阴道或经由植入的储器施用。本文所用的术语“胃肠外”包括皮下、经皮、静脉内、肌内、关节内、滑膜内、胸骨内、鞘内、肝内、病灶内和颅内注射或灌输技术。本领域技术人员将理解,鉴于本文包括的实施方案,可以基于所选择的施用途径,向上或向下调节活性成分或成分(例如,式i的化合物)的施用方式和剂量。此外,应当理解,可以期望优化任何选择剂型的活性成分的剂量,并且可以通过使用本文所述或本领域已知的方法来评估抗精神病药化合物的有效性来实现。本文包括的药物组合物可以任何口服可接受的剂型口服施用,包括但不限于胶囊、片剂、水悬浮液或溶液。在口服使用的片剂的情况下,通常使用的载体包括乳糖和玉米淀粉。在一个实施方案中,还加入润滑剂,例如硬脂酸镁。对于胶囊形式的口服施用,有用的稀释剂包括乳糖和/或干玉米淀粉,作为两个非限制性实例。当水性悬浮液需要用于口服使用时,活性成分与乳化剂和悬浮剂组合。如果需要,还可以加入某些甜味剂、调味剂或着色剂。在一个实施方案中,本发明的制剂可以与一种或多种其它药物联合施用。这样的其它药物可以本领域已知的形式和剂量施用或共同施用。术语“共同施用”或“联合疗法”用于描述其中使用至少两种化合物同时治疗文中所述的精神分裂症或另一种神经精神疾病或病症的疗法。在一个实施方案中,有效量的至少两种化合物用于同时治疗精神分裂症或另一种神经精神疾病或病症。在另一个实施方案中,至少两种化合物(其组合包含有效量)同时用于治疗文中所述的精神分裂症或另一种神经精神疾病或病症。在一个实施方案中,用至少两种化合物治疗的结果可以是分开使用各种化合物获得的治疗结果的相加,直接相加或加到小于分开用两种化合物获得的结果的程度。在一个实施方案中,用至少两种化合物治疗的结果可以在不同程度上协同作用。在一个实施方案中,用至少两种化合物治疗的结果可以小于分开使用各种化合物获得的治疗结果。一方面,用本文包括的组合物的治疗结果使得对于一种化合物,治疗结果小于分开用化合物获得的结果,而关于组合物中的其它化合物的治疗结果与分开获得的治疗结果大致相同。虽然术语共同施用包括同时向患者施用两种活性化合物,但不必同时向患者施用该化合物,尽管有效量的单种化合物将在患者中同时存在。在一个实施方案中,本文所述的化合物可与一种或多种非典型抗精神病药共同施用。非典型抗精神病药的实例包括但不限于氟奋乃静、利培酮、奥氮平、氯氮平、喹硫平、齐拉西酮、阿立哌唑、舍吲哚、佐替平和哌罗匹隆。可用于本文所包括的联合疗法的抗抑郁药的实例包括但不限于氟西汀、西酞普兰、依他普仑、文拉法辛、度洛西汀、安非他酮。化合物(i)的合成用于制备有机分子和官能团转化和控制(包括使用保护基团)的标准合成方法和程序可以从相关科学文献或本领域的标准参考教科书中获得。虽然不限于任何一个或多个来源,但有机合成的公认参考教科书包括:smith,m.b.march,j.march'sadvancedorganicchemistry:reactions,mechanisms,andstructure,第5版;johnwiley&sons:newyork,2001;和greene,t.w.;wuts,p.g.m.protectivegroupsinorganicsynthesis,3rd;johnwiley&sons:newyork,1999。美国专利号7,166,617中描述了制备化合物(i)的方法,其全部内容通过引用并入本文。形式(a)的化合物(i)∙hcl∙2h2o的药物组合物本公开还提供包含形式(a)的化合物(i)∙hcl∙2h2o和一种或多种药学上可接受的稀释剂、赋形剂或载体的药物组合物。“药物组合物”是适合施用于受试者的形式的含有形式(a)的化合物(i)∙hcl∙2h2o的制剂。在一个实施方案中,药物组合物是大量或单位剂型。单位剂型是任何各种形式,包括例如胶囊、iv袋、片剂、气雾剂吸入器上的单个泵或小瓶。单位剂量组合物中活性成分(例如,形式(a)的化合物(i)∙hcl∙2h2o的制剂)的量是有效量并且根据所涉及的具体治疗而改变。本领域技术人员将了解,有时需要根据患者的年龄和状况对剂量进行常规改变。剂量也将取决于施用途径。考虑各种途径,包括口服、肺、直肠、胃肠外、经皮、皮下、静脉内、肌内、腹膜内、吸入、口腔、舌下、胸膜内、鞘内、鼻内等。用于局部或经皮施用形式(a)的化合物(i)∙hcl∙2h2o的剂型包括粉末、喷雾剂、软膏、糊剂、霜剂、洗剂、凝胶剂、溶液剂、贴剂和吸入剂。在一个实施方案中,形式(a)的化合物(i)∙hcl∙2h2o在无菌条件下与药学上可接受的载体以及所需的任何防腐剂、缓冲剂或推进剂混合。如本文所用,短语“药学上可接受的”是指在合理的医学判断范围内适合与人类和动物的组织接触使用的那些化合物、材料、组合物、载体和/或剂型,而没有过多的毒性、刺激、过敏响应或其它问题或并发症,与合理的益处/风险比相称。“药学上可接受的赋形剂”是指可用于制备药物组合物的赋形剂,所述药物组合物通常是安全的,无毒的,既不是生物学的,也不是在其它方面不理想的,且包括兽医用途以及人类药物用途可接受的赋形剂。在说明书和权利要求书中使用的“药学上可接受的赋形剂”包括一种和多于一种这样的赋形剂二者。本公开的药物组合物配制成与其预期施用途径相容。施用途径的实例包括胃肠外,例如静脉内、皮内、皮下、口服(例如吸入)、经皮(局部)和经粘膜施用。用于胃肠外、皮内或皮下施用的溶液或悬浮液可包括以下组分:无菌稀释剂,例如注射用水、盐水溶液、固定油、聚乙二醇、甘油、丙二醇或其它合成溶剂;抗菌剂如苯甲醇或对羟基苯甲酸甲酯;抗氧化剂如抗坏血酸或亚硫酸氢钠;螯合剂如乙二胺四乙酸;缓冲剂如乙酸盐、柠檬酸盐或磷酸盐,以及用于调节渗透压的试剂如氯化钠或葡萄糖。ph可以用酸或碱调节,如盐酸或氢氧化钠。胃肠外制剂可以包封在由玻璃或塑料制成的安瓿、一次性注射器或多剂量小瓶中。本文所用的术语“治疗有效量”是指治疗、改善或防止所鉴定的疾病或病症或显示可检测的治疗或抑制作用的药物试剂的量。该作用可以通过本领域已知的任何测定方法检测。受试者的精确有效量将取决于受试者的体重、大小和健康;条件的性质和程度;以及选择用于施用的治疗剂或治疗剂的组合。对于给定情况的治疗有效量可以通过在临床医生的技能和判断范围内的常规实验来确定。在一方面,待治疗的疾病或紊乱是神经精神疾病或紊乱。在另一方面,待治疗的疾病或病症是精神分裂症。对于任何化合物,可以在细胞培养测定或动物模型(通常是大鼠、小鼠、兔、狗或猪)中最初估计治疗有效量。动物模型也可用于确定合适的浓度范围和施用途径。然后可以使用这样的信息来确定在人中施用的有用剂量和途径。治疗/预防功效和毒性可以通过细胞培养物或实验动物中的标准药物程序来确定,例如ed50(在50%的群体中治疗有效的剂量)和ld50(对群体的50%致死的剂量)。毒性和治疗效果之间的剂量比是治疗指数,可以表示为ld50/ed50的比率。显示出大的治疗指数的药物组合物是优选的。剂量可以在该范围内变化,这取决于所用的剂型、患者的敏感性和施用途径。调节剂量和施用以提供足够水平的活性成分或维持期望的效果。可以考虑的因素包括疾病状态的严重性、受试者的一般健康、受试者的年龄、体重和性别、饮食、施用时间和频率、药物组合、反应敏感性和对疗法的耐受性/响应。长效药物组合物可以每3至4天、每周或每两周施用一次,这取决于具体制剂的半衰期和清除率。包含形式(a)的化合物(i)∙hcl∙2h2o的药物组合物可以通常已知的方式制备,例如通过常规混合、溶解、制粒、制糖衣丸、研磨、乳化、包封、包埋或冻干过程。药物组合物可以常规方式配制,使用一种或多种药学上可接受的载体,其包含促进活性成分加工成可药学上使用的制剂的赋形剂和/或助剂。当然,合适的制剂取决于所选择的施用途径。适用于可注射用途的药物组合物包括无菌水溶液(其中为水溶性)或分散体和用于临时制备无菌可注射溶液或分散体的无菌粉末。对于静脉内施用,合适的载体包括生理盐水、抑菌水、cremophoreltm(basf,parsippany,n.j.)或磷酸盐缓冲盐水(pbs)。在所有情况下,组合物必须是无菌的,并且应当在一定程度上是易于注射的流体。在制造和储存的条件下必须是稳定的,并且必须防止例如细菌和真菌等微生物的污染作用。载体可以是含有例如水、乙醇、多元醇(例如,甘油、丙二醇和液体聚乙二醇等)的溶剂或分散介质及其合适的混合物。例如通过使用涂层例如卵磷脂,通过在分散体的情况下维持所需的粒度和通过使用表面活性剂,可以维持合适的流动性。防止微生物的作用可以通过各种抗细菌和抗真菌剂,例如对羟基苯甲酸酯、氯丁醇、苯酚、抗坏血酸、硫柳汞等来实现。在许多情况下,优选在组合物中包括等渗剂,例如糖、多元醇如甘露醇、山梨糖醇、氯化钠。可以通过在组合物中包含延迟吸收的试剂例如单硬脂酸铝和明胶来实现可注射组合物的延长吸收。无菌可注射溶液可以通过在具有上文列举的一种成分或成分的组合(根据需要)的合适溶剂中结合所需量的形式(a)的化合物(i)∙hcl∙2h2o,然后过滤灭菌来制备。通常,分散体通过将形式(a)的化合物(i)∙hcl·2h2o结合在含有碱性分散介质和上文列举的那些的所需的其它成分的无菌媒介中来制备。在制备无菌可注射溶液的无菌粉末的情况下,制备方法是真空干燥和冷冻干燥,得到形式(a)的化合物(i)∙hcl·2h2o的粉末加上来自其先前无菌过滤溶液的任何另外的所需成分。口服组合物通常包括惰性稀释剂或可食用的药学上可接受的载体。它们可以封闭在明胶胶囊中或压制成片剂。为了口服治疗施用的目的,形式(a)的化合物(i)∙hcl∙2h2o可与赋形剂结合且以片剂、锭剂或胶囊的形式使用。口服组合物也可以使用流体载体制备,用作漱口剂,其中流体载体中形式(a)的化合物(i)∙hcl∙2h2o口服施用且漱口(swished)并祛痰或吞咽。作为组合物的一部分,可以包括药学上相容的结合剂和/或佐剂材料。片剂、丸剂、胶囊、锭剂等可以含有以下成分中的任一种或类似性质的化合物:粘合剂如微晶纤维素、黄蓍胶或明胶;赋形剂如淀粉或乳糖、崩解剂如藻酸,primogel或玉米淀粉;润滑剂如硬脂酸镁或sterotes;助流剂例如胶体二氧化硅;甜味剂如蔗糖或糖精;或调味剂如薄荷、水杨酸甲酯或橙子调味剂。对于通过吸入施用,形式(a)的化合物(i)∙hcl∙2h2o以气雾剂喷雾的形式从加压容器或分配器(含有合适的推进剂,例如气体如二氧化碳)或雾化器递送。全身施用也可以是经粘膜或经皮的方式。对于经粘膜或经皮施用,在制剂中使用适合渗透屏障的渗透剂。这种渗透剂在本领域中通常是已知的,并且包括例如经粘膜施用的洗涤剂、胆汁盐和夫西地酸衍生物。经粘膜施用可以通过使用鼻喷雾剂或栓剂来实现。对于经皮施用,形式(a)的化合物(i)∙hcl∙2h2o配制成本领域通常已知的软膏、油膏、凝胶或霜剂。形式(a)的化合物(i)∙hcl∙2h2o可以用药学上可接受的载体制备,其可以保护化合物免于从身体快速消除,例如受控释放的制剂,包括植入物和微胶囊递送系统。可以使用可生物分解的生物相容性聚合物,例如乙烯乙酸乙烯酯、聚酐、聚乙醇酸、胶原、聚原酸酯和聚乳酸。制备这些制剂的方法对于本领域技术人员是显而易见的。这些材料也可以从alzacorporation和novapharmaceuticals,inc.商购获得。脂质体悬浮液(包括靶向到针对病毒抗原的单克隆抗体的感染细胞的脂质体)也可以用作药学上可接受的载体。这些可以根据本领域技术人员已知的方法制备,例如如美国专利号4,522,811描述(其内容以其整体并入本文)。特别有利的是以剂量单位形式配制口服或胃肠外组合物以便于施用和剂量的均匀性。本文使用的剂量单位形式是指适用于待治疗的受试者的单位剂量的物理离散单位;每单位含有经计算的预定量活性成分,以产生与所需药物载体相关联的所需治疗效果。本公开的剂量单位形式的规格由形式(a)的化合物(i)∙hcl∙2h2o的独特特征和待实现的具体治疗效果决定并且直接取决于此。在治疗应用中,根据本申请使用的药物组合物的剂量根据接受者患者的试剂、年龄、体重和临床状况和实施疗法的临床医师或从业者的经验和判断以及影响选择剂量的其它因素等而变化。剂量范围可以为每天约0.01mg/kg至每天约5000mg/kg。在一方面,剂量范围可以为每天约1mg/kg至每天约1000mg/kg。在一方面,剂量范围将为约0.1mg/天至约50g/天;约0.1mg/天至约25g/天;约0.1mg/天至约10g/天;约0.1mg至约3g/天;或约0.1mg至约1g/天,以单次、分次或连续剂量施用(可以针对患者体重(kg)、体表面积(m2)和年龄(岁)调节剂量)。在其它方面,剂量范围可以为单次剂量施用的每天约16mg的化合物(i)至每天约64mg的化合物(i)。另一方面,剂量范围可以为单次剂量施用的每天约30mg的化合物(i)至约50mg的化合物(i)。在一方面,药物组合物中化合物(i)的剂量为单次剂量施用的30mg/天、31mg/天、32mg/天、33mg/天、34mg/天、35mg/天、36mg/天、37mg/天、38mg/天、39mg/天、40mg/天、41mg/天、42mg/天、43mg/天、44mg/天、45mg/天、46mg/天、47mg/天、48mg/天、49mg/天和50mg/天。在一个实施方案中,药物组合物中化合物(i)的剂量为单次剂量施用的40mg/天。有效量的药物试剂提供如临床医生或其它合格观察者所指出的客观可辨识的改进。如本文所用,术语“剂量有效方式”是指形式(a)的化合物(i)∙hcl∙2h2o的量,以在受试者中产生所需的效果。药物组合物可以与施用说明书一起包括在容器、包装或分配器中。本公开的药物组合物口服、经鼻、经皮、肺、吸入、口腔、舌下、腹膜内、皮下、肌肉内、静脉内、直肠、胸膜内、鞘内和胃肠外施用。在一个实施方案中,形式(a)的化合物(i)∙hcl∙2h2o口服施用。本领域技术人员将认识到某些施用途径的优点。利用形式(a)的化合物(i)∙hcl∙2h2o的剂量方案根据各种因素来选择,所述因素包括:患者的类型、物种、年龄、体重、性别和医学状况;待治疗的病症的严重性;施用途径;患者的肾功能和肝功能;和所采用的特定化合物或其盐。普通技术的医生或兽医可以容易地确定和规定预防、反击或阻止病症进展所需的有效量的药物。制备和施用本申请的公开的化合物的技术可以发现于remington:thescienceandpracticeofpharmacy,第19版,mackpublishingco.,easton,pa(1995)。在一个实施方案中,形式(a)的化合物(i)∙hcl∙2h2o在药物制剂中与药学上可接受的载体或稀释剂组合使用。合适的药学上可接受的载体包括惰性固体填料或稀释剂和无菌水性或有机溶液。形式(a)的化合物(i)∙hcl∙2h2o将以足以在本文所述的范围内提供所需剂量的量存在于该药物组合物中。除非另有说明,否则本文使用的所有百分比和比率均为重量比。治疗方法本公开还提供通过向需要这种治疗的受试者施用治疗有效量的形式(a)的化合物(i)∙hcl∙2h2o或其药物组合物来治疗有需要的受试者的神经精神疾病或紊乱的方法。神经精神疾病或紊乱可以是精神分裂症。术语“受试者”是指任何动物,包括哺乳动物,例如但不限于人、小鼠、大鼠、其它啮齿动物、兔、狗、猫、猪、牛、绵羊、马或灵长类动物。受试者可以或可以不被诊断为精神分裂症。受试者可以存在精神分裂症的一种或多种体征或症状。在某些实施方案中,本公开的受试者可以在用包含形式(a)的化合物(i)的药物组合物治疗之前、与用包含形式(a)的化合物(i)的药物组合物治疗组合或在用包含形式(a)的化合物(i)的药物组合物治疗之后用一种或多种典型的或非典型的抗精神病疗法治疗精神分裂症。在某些实施方案中,本公开的受试者可以在用包含形式(a)的化合物(i)的药物组合物治疗之前用一种或多种典型或非典型的抗精神病疗法治疗精神分裂症,且一种或多种典型或非典型的抗精神病疗法对治疗受试者的精神分裂症的体征或症状可能对无效。从不同实施例,本公开的其它特征和优点是显而易见的。所提供的实施例说明在实践本公开中有用的不同组分和方法。这些实施例不限制本公开的要求保护的组合物、方法和试剂盒。基于本公开,本领域技术人员可以识别和采用对实施本公开有用的其它组分和方法。实施例实施例1观察到qtc间隔提高,并且似乎与暴露于化合物(i)及其代谢物bfb-520有关。在cyp2d6代谢较差和显示bfb-520的高血浆水平的患者中,qt延长特别明显。进一步分析qt/qtc与化合物(i)和bfb-520浓度之间的关系。确定为了避免qt延长,化合物(i)和bfb-520的cmax应当分别不超过80ng/ml和12ng/ml。为了进一步评估大于30和60ms的自基线的qt/qtc变化的发生率以及大于450、480和500ms的qtc值的发生率,进行以下研究。本研究的第1部分设计成表征和比较作为mr制剂施用时化合物(i)的药代动力学(pk)特征,和以6路、受试者内、交叉设计单剂量施用后的食品效应。本研究的第2部分设计成评估多剂量的选择的mr制剂对安全性、耐受性和心血管参数的影响。化合物(i)对睡眠参数的影响也将进行评估。在cyr-101c01研究中,化合物(i)对慢波睡眠(sws)分布具有影响:化合物(i)在前三分之一夜间显著增加sws,并在后三分之一夜间减少sws。结果还表明,化合物(i)可以具有睡眠促进作用,因为它改进睡眠起始参数(入睡潜伏期,持续睡眠前的潜伏期)。在当前研究中,睡眠将用作生物标志物,可有助于限定在下一个患者研究中评估的最小活性剂量。睡眠参数将通过vwatch方法分析。研究的第1部分中使用的制剂选自具有积极治疗的设计空间,作为2个主要组成变量的化合物(i)和hpmc(一种受控释放剂)。在设计空间的释放速率轴上,mr制剂将描述为缓慢(释放速率为16-19小时)、中速(释放速率为10-12小时)或快速(释放速率为5-7小时)。方案1中显示2维组成制剂设计空间,其中f1至f4表示边界制剂(boundaryformulations)。本研究的第2部分设计成在较大的未处理(native)受试者群组中,与安慰剂相比,在低剂量和高剂量水平下评估来自第1部分的所选制剂的多剂量施用。药理学特征(非临床研究):在体外受体结合研究中,化合物(i)证明了独特的结合特征。化合物(i)仅与5-ht2a、α1-肾上腺素和σ2受体(ki=7.53,14.43,8.19nmol/l,分别地)以高亲和力结合。对da受体的亲和力相当弱(ic50>1000nmol/l)。两种主要代谢物bfb-520和bfb-999分别显示出与化合物(i)类似的特征,对σ2受体的亲和力较低,低于和等于化合物(i)对5-ht2a受体的亲和力。在体内功能试验中,化合物(i)充当σ2和5-ht2a受体的拮抗剂。口服施用后,化合物(i)稍微提高伏隔和纹状体中的多巴胺周转,并以高剂量水平增加前额叶皮质中da代谢物如dopac和hva的输出。在抗精神病活动的动物模型中的有效剂量水平下,化合物(i)不影响单胺水平,而其它抗精神病药显著增加da周转和dopac和hva的输出,反映其有效的d2拮抗作用。化合物(i)在雄性wistar大鼠中在几种设计成评估在人体中产生药物抗精神病活性的潜力的行为范例中进行试验。化合物(i)以与其它抗精神病药类似的方式抑制甲基苯丙胺、阿朴吗啡和苯环利定诱导的兴奋性运动。同样,bfb-520和bfb-999也抑制甲基苯丙胺诱导的兴奋性运动,ed50高于化合物(i)的ed50。此外,化合物(i)在重复施用后显著改善pcp诱导的社会互动损伤,而其它非典型抗精神病药不能改善该损伤,并改进由mk-801引起的自发交替行为的损伤。安全性药理学:在一系列安全性药理学研究中,在引起一般活动和行为的各种变化的1至30mg/kg化合物(i)的口服剂量范围下,在大鼠中检查化合物(i)对一般活动和行为、cns、呼吸功能、胃肠系统和水和电解质排泄的影响。在投配后0.25至4小时观察到这些临床体征,并在投配后6小时消失。化合物(i)抑制cns功能,降低电击诱导惊厥阈值。化合物(i)的高剂量(>10mg/kg)影响呼吸功能,抑制胃排空,损害胃肠膜,减少尿量,且增加尿钾排泄。在体外和体内研究中检查化合物(i)对心血管系统的作用。在使用豚鼠乳头肌的体外电生理研究中,1μm或更多的化合物(i)延长动作电位持续时间(apd),且程度与利培酮和氟哌啶醇相同。同样地,0.1μm或更多的bfb-520和1μm或更多的bfb-999延长离体豚鼠乳头肌中的apd,且程度与化合物(i)相同或更大。在使用表达克隆心脏离子通道的培养细胞的体外电生理研究中,化合物(i)抑制ikr电流,ic50为0.325μm,与利培酮的ic50(0.319μm)相当。对于bfb-520,它阻止ikr电流,0.181μm的ic50低于母体化合物的ic50,但高于氟哌啶醇(0.026μm)、硫利达嗪(0.145μm)或齐拉西酮(0.134μm)的ic50。药代动力学特征:化合物(i)的药代动力学(pk)研究特别是在大鼠和猴中进行。在单次口服施用后,化合物(i)被快速吸收。雄性大鼠的血浆放射性在0.63至2.75小时之间出峰,雄性猴在3至3.5小时出峰。大鼠和猴的口服吸收率分别为90.3至94.7%和70.0至99.9%。大鼠和猴的自血浆的放射性的消除半衰期分别为45.13至51.52小时和174.74至184.78小时。大鼠和猴的未变化的化合物(i)的消除半衰期分别为1.68至2.06小时和1.68至2.57小时。大鼠和猴的化合物(i)的绝对口服生物利用度分别为52.4至64.5%和90%或更高。在经14天向雄性大鼠重复施用1mg/kg/天期间,血浆放射性随着剂量数增加而增加,在第七次施用后达到稳定状态。还在大鼠中评估食品和性别的影响。当化合物(i)以1mg/kg口服施用到未禁食大鼠时,血浆放射性在禁食雄性大鼠中具有延迟约1小时的tmax和降低cmax至该值的约72%,尽管auc在两组类似。此外,雌性大鼠的总放射性的药代动力学参数与雄性大鼠的那些相当。当将14c-化合物(i)口服施用于哺乳期大鼠时,认为化合物(i)和/或其代谢物快速转移到奶中并缓慢消除。还在针对毒代动力学的大鼠和猴的单次和重复剂量毒性研究以及用于血浆暴露证据的遗传毒性和胚胎发育研究中研究化合物(i)的吸收。在单次和重复施用后,化合物(i)及其主要代谢物bfb-520和bfb-999的暴露水平在大鼠和猴中均以剂量依赖性方式增加,仅在大鼠中具有性别差异。在猴中单次施用bfb-520后,bfb-520、化合物(i)和bfb-999的暴露水平随大于比例1的剂量增量增加。bfb-520在投配后4小时内达到其最大浓度,且化合物(i)和bfb-999的tmax与bfb-520的tmax相当。最后,口服施用(10mg/kg)后用雄性大鼠研究化合物(i)的脑转移。血浆和脑浓度的cmax分别为3164.62ng/ml和4946.62ng/g。kp值(脑/血浆浓度比)为1.38ml/g。在口服施用14c化合物(i)后,在雄性和雌性大鼠和雄性猴的血浆和尿液中检测到几种代谢物(即bfb-999、bfb-520和bfb-885)。雌性大鼠的代谢率比雄性大鼠慢,但雄性和雌性大鼠之间的代谢特征类似。即使化合物(i)显示为通过细胞色素p450cyp1a2、cyp2c19、cyp2d6和cyp3a4在bfb-520和bfb-999中代谢,使用人肝微粒体的进一步研究表明,化合物(i)主要通过除了cyp同种型以外的酶促反应代谢。对于bfb-520,它被cyp2d6和cyp3a4代谢。没有观察到对人p450同种型(cyp1a2、2a2、2b6、2c8/9、2c19、2e1和3a4)的显著抑制作用,而显示对cyp2d6的抑制作用较弱。化合物(i)对体外代谢的药物-药物相互作用的研究对于以下伴随药物测定的ic50值大于50μm:酮康唑、氟伏沙明、帕罗西汀和劳拉西泮。在单次口服或静脉内施用后,大鼠和猴中放射性消除的主要途径是通过粪便。在单次口服施用到胆管插管大鼠后48小时内胆汁排泄量为44.2%。大鼠和猴的放射性尿排泄率约为35%。在单次口服施用后168小时内,大鼠的给与的放射性的总回收率为101.1%(包括残骸),而猴为92.6%。经14天反复施用到大鼠后,尿液和粪便中给与的放射性总回收率为96.6%,而最后施用后168小时内残骸中的总回收率为0.7%。14c-化合物(i)处理的大鼠的十二指肠内施用胆汁样品后,肠肝循环率确定为约27%。在一个实施方案中,组合物可以使用一种或多种药学上可接受的载体以常规方式配制,并且也可以受控释放制剂施用。实施例2研究的第1部分是12个健康cyp2d6em男性受试者的开放标签、非随机、单剂量、6周期交叉设计。对于第1部分,受试者将以非随机方式接受以下方案:方案a:mr制剂原型1:32mg化合物(i)在禁食状态中缓慢释放施用方案b:mr制剂原型2在禁食状态中施用方案c:mr制剂原型3在禁食状态中施用或制剂原型1或2在进食状态中施用方案d:mr制剂原型4在禁食状态中施用或制剂原型1、2或3在进食状态中施用方案e:mr制剂原型5在禁食状态中施用或制剂原型1、2、3或4在进食状态中施用方案f:mr制剂原型1、2、3、4或5在进食状态中施用。第1部分中的制剂选择是在对从先前方案收集的所有数据进行全面审查后进行的,并且在对第2部分的所有数据进行全面审查之后,对第2部分的可选回访的制剂、剂量和要求进行选择。该研究的第2部分是在24个健康的cyp2d6em男性和女性受试者中的双盲、随机、安慰剂对照、6序列、3周期交叉设计。对于第2部分,在3个研究期间,受试者以随机方式接受以下方案:方案g:安慰剂qd历时7天方案h:高剂量mr制剂原型qd历时7天方案i:低剂量mr制剂原型qd历时7天基于设计空间的上述概念,本研究第1部分中使用的imp制剂选自具有活性处理化合物(i)和羟丙甲纤维素(hpmc)作为释放控制剂、作为两个主要组成变量的设计空间(释放由hpmc粘度控制,基于2hpmc聚合物的比率)。2维组成制剂设计空间如表1所示,其中f1至f4代表边界制剂。该研究的第2部分设计用于在较大的未处理受试者群组中,与安慰剂相比,在低和高剂量水平下评估来自第1部分的所选制剂的多剂量施用。表1:设计空间的赋形剂定量组成范围组分16mg缓慢制剂1%w/w64mg缓慢制剂2%w/w16mg快速制剂3%w/w64mg快速制剂4%w/w化合物(i)*6.4025.606.4025.60羟丙甲纤维素k100lvcr12.006.0036.0030.00羟丙甲纤维素k4mcr24.0024.00−−微晶纤维素ph102**36.1022.9036.1022.90乳糖fastflo31620.0020.0020.0020.00无水硅胶aerosil200pharma0.500.500.500.50硬脂酸镁1.001.001.001.00总计100.00100.00100.00100.00*应用的盐修正系数为1.2。**微晶纤维素ph102的量将相应地调节以维持相同的片剂重量。因此,在组成细节下,我们提出了16-64mg化合物(i)的剂量范围和mr片剂中羟丙甲纤维素k100lvcr和羟丙甲纤维素k4mcr水平范围的极值,应理解为这些范围内的任何临时制剂可以在临床研究期间作为imp制造和投配。制剂的所有其它组分保持恒定,例外之处在于微晶纤维素ph102,其可以根据药物物质的效力和纯度以及羟丙甲纤维素k100lvcr和羟丙甲纤维素k4mcr的重量进行调节以保持片剂重量。所选制剂的最终组成记录在临床试验制造商生产的批次记录中。化合物(i)原型mr片剂(制剂1、2、3和4)的组成化合物(i)原型mr片剂制剂1、2、3和4的组分和定量组成的完整说明在表2中给出。与2.1.p.1节中描述的制剂设计空间方法一致,该制剂表示16-64mg化合物(i)的剂量范围和可用于本研究中的羟丙甲纤维素k100lvcr和羟丙甲纤维素k4mcr的浓度范围的极值。表2:化合物(i)原型mr片剂(制剂1、2、3和4)的组成组分16mg缓慢制剂1mg/片剂64mg缓慢制剂2mg/片剂16mg快速制剂3mg/片剂64mg快速制剂4mg/片剂功能参考标准化合物(i)119.2076.8019.2076.80活性ds章节或合适的其它羟丙甲纤维素k100lvcr36.0018.00108.0090.00释放调节剂usp,ph.eur.,jp羟丙甲纤维素k4mcr72.0072.00−−释放调节剂usp,ph.eur.,jp微晶纤维素ph1022108.3068.70108.3068.70填料ph.eur.,nf,jp乳糖fastflo31660.0060.0060.0060.00填料nf/usp,ph.eur.,jp无水硅胶aerosil200pharma1.501.501.501.50助流剂usp,ph.eur.,jp硬脂酸镁3.003.003.003.00润滑剂ph.eur.,nf,jp总重量300.00300.00300.00300.001应用的盐修正系数为1.22微晶纤维素ph102的量将相应调节以维持相同的片剂重量。表3显示了化合物(i)原型mr片剂制剂1、2、3和4的分批配方。这些制剂表示化合物(i)的剂量范围和可以用于研究的羟丙甲纤维素k100lvcr和羟丙甲纤维素k4mcr的浓度的极值。无硅胶体、乳糖fastactlo316和硬脂酸镁的组成比率保持不变。微晶纤维素ph102的组成比率可以基于药物的效力和纯度以及羟丙甲纤维素k100lvcr和羟丙甲纤维素k4mcr的重量进行调节以维持片剂重量为300mg。表3:化合物(i)原型mr片剂的“设计空间”批次配方组分16mg缓慢制剂1%w/w64mg缓慢制剂2%w/w16mg快速制剂3%w/w64mg快速制剂4%w/w化合物(i)16.4025.606.4025.60羟丙甲纤维素k100lvcr12.006.0036.0030.00羟丙甲纤维素k4mcr24.0024.00−−微晶纤维素ph102236.1022.9036.1022.90乳糖fastflo31620.0020.0020.0020.00无水硅胶aerosil200pharma0.500.500.500.50硬脂酸镁1.001.001.001.00总计100.00100.00100.00100.001应用的盐修正系数为1.22微晶纤维素ph102的量将相应调节以维持相同的片剂重量。方案2:化合物(i)原型mr片剂的制造化合物(i)和各种赋形剂的量通过使用适当校正的天平称重来控制,以证实实现了正确的制剂组成。第二操作员验证重量。共混物均匀性由方案2中详述的预限定的混合条件控制。已经开发这些参数以确保所有可能的制剂共混物的均匀性在所提出的设计空间内。这些加工指令的执行将在批量制造记录中进行控制和记录。为了确保整个设计空间的内容物均匀性一致,制造和试验方案1中描述的设计空间中的点的开发批次。通过测定评估最终片剂的内容物的均匀性。片剂硬度通过使用片剂压缩硬度试验在整个批次中施加一致压力进行定期试验(破坏性)来控制。片剂手动压制;每个片剂使用适当校准的天平分开称重,且第二操作者验证重量。制剂中使用的所有赋形剂符合以下所述的ph.eur.、usp/nf或jp要求的当前专著。所有赋形剂均从批准的供应商处购买。将接受制造商分析证书,且在quotientclinicalltd收到的所有赋形剂将根据quotientclinicalltd接收要求进行适当的鉴定试验。表4.化合物(i)原型mr片剂的规格溶解试验溶解试验是根据usp专著<711>装置2进行的药典方法。溶解介质是450ml0.01m盐酸,用双强度的禁食状态模拟肠液(第2版)转变ph,给出总体积900ml搅拌并在75rpm下搅拌。通过使用intersilods-3v(4.6mm×150mm)5μm柱的反相等度hplc方法或在248nm下进行uv检测的适当验证的替代方法来分析样品的化合物(i)含量。流动相由乙腈:水:三氟乙酸组成。化合物(i)原型mr片剂的hplc测定、特性和内容物均匀性方法的描述用于测定化合物(i)原型mr片剂的活性成分含量的方法是使用intersilods-3v(4.6mm×150mm)5μm柱的反相等度hplc方法或在248nm下进行uv检测的适当验证的替代方法。流动相由乙腈:水:三氟乙酸组成。相关物质试验的描述用于化合物(i)原型mr片剂的相关物质的方法是使用intersilods-3v(4.6mm×150mm)5μm柱的反相梯度hplc方法或在248nm下进行uv检测的适当验证的替代方法。流动相a由0.1%tfa水溶液组成,流动相b为0.1%tfa乙腈溶液组成。化合物(i)c02:一天一次制剂在健康的cyp2d6强代谢剂男性和女性受试者中单剂量和多剂量调节释放原型制剂施用后,两部分研究设计成评估化合物(i)及其主要代谢物的药代动力学特征,和评估化合物(i)及其主要代谢物的药代动力学特征和心血管参数之间的关系。第1部分和第2部分的研究设计分别在图7和8中显示,且图9显示投配的周期方案。表5.选择pk参数的概要-周期1(32mg缓慢释放,禁食)另外,化合物(i)、bfb-520和bfb-999的血浆浓度-时间曲线在图1-3中显示。化合物(i)、bfb-520和bfb-999的cmax在图4中显示。化合物(i)、bfb-520和bfb-999对qtcf的影响在图5中显示。禁食条件下的mr制剂:■短迟滞时间表示生物利用度快■暴露可变性一般较低■至第24小时,大多数低至无法量化的值■pk通常与化合物(i)和bfb-999成比例,而对bfb-520较不成比例■bfb-520和bfb-999的反转在通常抑制水平的bfb-520和较高bfb-999与bfb-520比率下发生■mr制剂结果表明,在小肠中较短时间有助于抑制bfb-520水平■化合物(i)和2种代谢物在3-8小时范围中的半衰期,对于40mg缓慢释放较长,最可能是由于触发(flip-flop)(终端阶段期间平衡的吸收和消除)■模拟结果表明在10-14天内的稳态,且对于所有3种分析物均无积累。食品效应:■阳性的食品效应明显-更高的暴露■mr制剂表现与ir制剂类似,具有快速释放和吸收,主要在到达结肠前●这解释了bfb-520水平的进一步提高■由于快速吸收化合物(i)cmax增加约2倍,bfb-520cmax增加约3倍,且bfb-999cmax增加约0.5倍■半衰期显著缩短:进食与禁食比率是●化合物(i)的0.5●bfb-520为0.8●bfb-999为0.6■因此,积累是不可预料的■auc增加最小(与cmax相比):1.3至1.8倍,bfb-520具有最高增加精神分裂症患者中的化合物(i)c03iib阶段进行iib阶段、多中心、随机、双盲、平行组、安慰剂对照研究,以评估化合物(i)在精神分裂症阴性症状患者中的功效、耐受性和安全性,接着进行24周、开放标签延长。研究设计在图10中显示。研究目标:基本目标:为了评估化合物(i)与安慰剂相比在改进精神分裂症的阴性症状中的功效,如通过在阳性和阴性综合症量表(panss)中的自基线变化测量,其中五边形模型在12周治疗中具有阴性子量表得分。主次要目标:■为了评估化合物(i)与安慰剂相比在改进精神分裂症的其它症状中的功效,如通过panss总分,以及五边形模型的子分数和双盲治疗12周的3因素分析中的自基线变化测量。■为了评估化合物(i)与安慰剂相比在改进精神分裂症的阴性症状中的功效,如通过双盲治疗12周中的简要阴性症状量表(bnss)总分数中的自基线变化测量。■为了评估化合物(i)相对于安慰剂对认知功能的影响,如在双盲治疗12周中通过精神分裂症认知的简要评估(bacs)成套测验(battery)测量。■为了评估化合物(i)在开放标签延长阶段的24周期间的功效持续性以及安全性和耐受性。其它目标:■为了评估化合物(i)相对于安慰剂对抑郁症状的影响,如在双盲治疗12周中通过精神分裂症的卡尔加里抑郁量表(cdss)测量。■为了评估化合物(i)相对于安慰剂对社会功能的影响,在双盲治疗12周中通过个人和社会表现(psp)。■为了评估化合物(i)相对于安慰剂对睡眠结构和连续性的影响,如在双盲治疗12周中在v-watch方法的帮助下测量。主要包含标准:■男性或女性患者,18至60岁,包括在内。■患者满足“精神障碍诊断与统计手册”第五版(dsm-v)中限定的精神分裂症诊断标准■根据患者的治疗精神病医生,患者在过去三个月的阳性症状方面是稳定的■根据患者的治疗精神病医生,患者在过去三个月中呈现阴性症状■患者的panss阴性子分数至少为20。■患者关于以下的panss项目得分<4:p4兴奋,多动p7敌视p6多疑g8不配合g14差的脉冲控制■上个月期间精神药物没有变化■患者必须是p450cyp2d6的强代谢剂,如在施用第一药物剂量之前通过基因分型试验确定的。主要排除标准:当前两级障碍、恐慌障碍、强迫性精神障碍或精神发育不全证据。患者的病症是由于物质的直接生理作用(例如滥用药物或药剂)或一般的医疗条件引起。自杀或企图自杀或对自己或他人有危险的重大风险。除了那些被允许的以外,不能中断精神药物的患者。筛选访问的6个月内接受氯氮平的患者。在最后注射后4周内,可以在研究中加入接受储存抗精神病药治疗的患者。具有显著的其它主要或不稳定的神经系统、神经外科(例如头部创伤)、代谢、肝、肾、血液学、肺、心血管、代谢、胃肠道或泌尿障碍的病史的患者。具有临床明显的心电图(ecg)异常的患者,可能是研究中的安全问题,包括使用fridericia公式(qtcf)修正心率的qt间隔值(男性>430ms,女性>450ms)。主要功效评估:-阳性和阴性症状量表(panss)-简要的阴性症状量表(bnss):半结构化访谈,设计成测量精神分裂症和分裂情感障碍中阴性症状严重度的当前水平(kirkpatrick等)○快感缺乏○苦恼○孤僻○无意志力○感情迟钝○失语症-精神分裂症认知的简要评估(bacs)-个人和社会表现(psp):评估社会功能;临床医师评分-社会有用的活动,-个人和社会关系,-自我护理-令人不安和攻击性行为-睡眠结构和连续性睡眠评估:30%至80%的精神分裂症患者报告睡眠和昼夜节律紊乱。-失眠报告的患者•较低生活品质•更严重的症状•对治疗较差的依附性/顺从性睡眠障碍也与精神病增强有关睡眠对记忆巩固很重要,因此睡眠结构紊乱或昼夜节律失调也可能导致精神分裂症中观察到的认知损害。-化合物(i)在以前的2a阶段研究中显示对睡眠结构的影响,可能与阴性症状和认知观察到的改进有关,因此本研究将进一步研究它们。•在进行睡眠记录(psg)的患者的亚组(20)中,在基线和第14天评估睡眠。化合物(i)对以下具有影响:-慢波睡眠(sws)分布:其从夜晚结束至夜晚开始转变sws:化合物(i)在前三分之一夜间显著增加sws,而在后三分之一夜间减少sws。-睡眠启动参数(入睡潜伏期,持续睡眠前的潜伏期)。•如通过psqi测量的主观睡眠品质得到改进,且用化合物(i)的这种改进大于用安慰剂的改进,尽管在统计学上不明显。v-watch:睡眠生物标志物和陪伴诊断工具vwatch方法概述-1(图6):与依靠脑波测量的标准多导睡眠图(psg)相比,v-watch方法使用生理测量来评估睡眠。生理系统及其规定取决于生理状态(醒或睡)睡眠过程影响整个身体,而不仅仅影响大脑•睡眠期间皮质波中观察到的变化只是睡眠阶段之间转变的反映,而不是评估这些转变的唯一方法•这些转变也可以从其它生理系统检测可以使用心率特征(水平、规律性、可变性和突然变化)和身体运动活动来区分醒与睡,和区分主要睡眠阶段。实施例3.化合物(i)的各种片剂制剂表6-1.16mg和64mgmin-101mr片剂制剂的组成表6-2.16mg和64mgmin-101mr片剂制剂的组成表7.16mg和64mgmin-101mr片剂制剂的组成表8.16mg和64mgmin-101mr片剂制剂的组成表9.64mgmin-101mr片剂制剂的组成表10.16mg和64mgmin-101mr片剂制剂的组成表11.16mg和64mgmin-101mr片剂制剂的组成表12.16mg和64mgmin-101mr片剂制剂的组成表13.16mg和64mgmin-101mr片剂制剂的组成表14.64mgmin-101mr片剂制剂的分析研究(实验9的64mg缓慢)表15.64mgmin-101mr片剂制剂的组成表16.16mg和64mgmin-101mr片剂制剂的组成表17.16mg和64mgmin-101mr片剂制剂的组成表18.16mg和64mgmin-101mr片剂制剂的组成表19.16mg和64mgmin-101mr片剂制剂的组成表20.参考min-101sr片剂的批次配方表21.16mg和64mgmin-101mr片剂制剂的组成(制造过程开发)实施例4:形式(a)的化合物(i)∙hcl·2h2o的制备2-((1-(2-(4-氟苯基)-2-氧代乙基)哌啶-4-基)甲基)异吲哚啉-1-酮(即化合物(i)的游离碱)溶解于丙酮中,并通过无定形火山玻璃即perlite®过滤,以除去任何外来物质。向该溶液中加入2mol/l盐酸水溶液,即2nhcl。将混合物在搅拌几个小时的同时冷却,并将化合物(i)的盐酸盐的粗晶体过滤并在减压下干燥。然后将粗晶体通过在丙酮和去离子水中加热粗材料并搅拌数小时来纯化。然后通过过滤除去外来物质,然后向滤液中加入另外的丙酮。将混合物冷却并在减压下过滤和干燥晶体,提供形式(a)的化合物(i)∙hcl·2h2o。实施例5:形式(a)的化合物(i)∙hcl·2h2o的x射线粉末衍射使用rigaku、rint2500进行x射线衍射。形式(a)的化合物(i)∙hcl∙2h2o的x射线粉末衍射在图11中显示。实施例6:形式(a)的化合物(i)∙hcl∙2h2o的ir吸收光谱使用perkin-elmer,paragon1000进行红外(ir)吸收光谱测定。形式(a)的化合物(i)∙hcl∙2h2o的ir光谱通过如图12所示的氯化钾盘法测量。吸收的主要波数及其指定如下:表22.形式(a)的化合物(i)∙hcl∙2h2oir光谱的指定波数(cm-1)分配2916c-h伸缩振动1684,1665c=o伸缩振动1594苯环1235c-f伸缩振动实施例7:形式(a)的化合物(i)∙hcl∙2h2o的核磁共振光谱在d6-二甲基亚砜中测量的形式(a)的化合物(i)∙hcl∙2h2o的1h-nmr光谱和13c-nmr光谱分别示于图13和图14中。通过引用结合在此引用的每个专利文献和科学文章的全部公开内容通过引用并入本文用于所有目的。等同方式在不脱离本申请的精神或基本特征的情况下,本申请的公开内容可以其它具体形式体现。因此,前述实施方案在所有方面都被认为是说明性的,而不是限制本文描述的申请的公开内容。因此,通过所附权利要求而不是前面的描述来指示本申请的公开范围,并且在权利要求的等同物的含义和范围内的所有改变旨在被包含在其中。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1