一种细胞球精准定位生物打印装置及方法与流程
本发明涉及组织工程中的生物打印领域,具体涉及一种细胞球精准定位生物打印装置及方法。
背景技术:
现有的细胞片形成方法主要有温敏培养皿、细胞包埋法、胶原凝胶法、磁力组织工程法、表面粗糙颗粒单分子层法和聚合电解质等。各自的特性与技术缺陷说明如下:
温敏培养皿法:在皿底壁涂抹温度敏感性聚N-异丙基酰胺,当温度低于32℃时,细胞构建亲水性表面而获得单层细胞膜片,此法培养过程操作复杂,特殊设备价格昂贵,要获得完整细胞片并不容易。即使获得了完整细胞片,所获得的细胞片的力学性能差,不利于移植操作。
细胞包埋法:将细胞与富血小板血浆、纤维蛋白胶、胶原、明胶等天然生物材料混合,用物理刮取法获得具有一定韧性厚的细胞片,这种方法的培养时间长,一般需10天至2周。另外,在生物材料内培养的细胞片不利于上皮细胞通过气-液培养获得复层上皮细胞,也难以获得成熟屏障细胞片的极性结构。
酶消化法:用胶原蛋白作为细胞培养支架,用胶原蛋白酶消化分离得到细胞片,但酶消化过程对细胞会有损伤,使得细胞活性降低。另外,酶消化法不易控制,难以获得较大成片的细胞片。
磁力组织工程法:将精氨酸、甘氨酸、天冬氨酸结合磁性阳离子脂质体添加至由亲水性、中性的共价水凝胶层组成的培养板或培养皿表面。在培养板(皿)下面放置一块磁铁,细胞培养后,移去培养板(皿)底的磁铁,此时的细胞片含有磁性纳米粒子,可将磁铁棒伸入培养孔收获细胞片。此法细胞培养过程复杂,部分磁性物质会残留细胞片中,使得细胞活性降低。
表面粗糙颗粒单分子层法:将细胞移植到聚苯乙烯-丙烯酰胺单分子层上培养,轻轻吹打后细胞收缩分离得到细胞片,不需酶处理,但单分子层粗糙表面制作复杂,需要用到价格昂贵的特殊设备。
聚合电解质法:在聚合电解质精氨酸-甘氨酸-天冬氨酸-聚L-赖氨酸-聚乙二醇薄膜上培养细胞,待细胞增殖生长后,在电化学控制下解除细胞片黏附,这种方法操作复杂,同时需要用到特殊的材料和设备。
三维打印技术又称为增材制造,根据零件或者物体的三维模型数据,快速准确地制造零件或者物体实体模型。而随着生物制造概念的提出,用组织工程方法进行组织器官的修复和重建是当前科学研究的热点之一,其基本原理是将细胞在体外培养扩增后,附着于预先设计的生物支架,构成细胞-支架复合体。生物支架主要使用快速成型技术制备,但目前使用快速成型技术制备生物支架出现很多难题,其中最大的难题是:难以将细胞或聚集的细胞精确定位于支架中,而细胞打印技术的出现可很好地解决这一问题。三维生物打印技术在医学领域发挥越来越重要的作用,以计算机三维设计模型为基础,通过控制软件对细胞或者材料控制重组得到具有生物活性的人工组织器官、医疗辅具等医学产品。
圣地亚哥的Invetech和Organovo两家公司合作研制出一款生物打印机(NoveGen MMX BioprinterTM),该技术特点是可利用计算机编程控制特制的生物”喷墨”打印机逐层打印,将特定细胞或细胞/基质作为堆积对象进行堆积成形,精确定位,并可最终用来制造三维器官。目前此项技术尚处于研究起始阶段,被制造的三维结构层与层之间的连接不可靠,难于成形具有三维高度要求的多层细胞三维结构,且成形结构的机械强度不高。
申请号为201510164921.6的中国发明专利文献公开一种三维生物打印装置和生物打印方法,三维生物打印装置,包括打印平台、喷头、喷头电控制器、两个带光源的CCD 光学系统、等离子除菌机构、运动控制系统、气压控制机构、湿度调节器、温度控制单元、储液罐、可盛装培养液的敞口容器、安装架、外壳,该专利在一定程度上解决了现有技术存在的问题,但是其结构不适用于高活性、多种类细胞球的多层细胞片结构的制造。
技术实现要素:
本发明的目的是解决现有技术的缺陷,提供一种细胞球精准定位生物打印装置,采用的技术方案如下:
一种细胞球精准定位生物打印装置,包括显微成像系统、中央控制处理系统和显示系统、吸取打印平台、三维控制系统、加注系统,三维控制系统由控制方位角的旋转控制装置、控制高度的高度调整装置和控制径向距离的径向距离调整装置组成,加注系统固定于三维控制系统的径向距离调整装置上,所述中央控制处理系统连接了吸取打印平台、加注系统、三维控制系统、显微成像系统和显示系统,所述显微成像系统在工作时对准加注系统在吸取打印平台上面的投影位置,所述吸取打印平台包括二维位移平台、琼脂糖固定装置和培养皿固定装置,所述培养皿固定装置用于固定培养皿,所述琼脂糖固定装置用于固定琼脂糖,所述琼脂糖中培养有细胞球,此细胞球即为打印过程中所使用的生物墨水。
本发明对细胞球进行打印,而不是细胞悬液,打印过程都能在显微成像系统下观察细胞球,极大的提高了细胞存活率,以及打印后材料的紧密连接性,并且适用于多种生物细胞的打印。
琼脂糖和培养皿同时固定在二维位移平台上,通过二维位移平台精确控制琼脂糖和培养皿的位置。三维控制系统用于调整加注系统的位置,加注系统在细胞打印过程中只通过高度调整装置在较小的范围内调整高度,不做水平方向运动,始终位于显微镜工作范围内。
作为优选,所述三维控制系统包括旋转控制装置、高度调整装置和径向距离调整装置,所述三维控制系统采用圆柱坐标系,所述旋转控制装置用于调整喷头的相对方位角,所述的高度调整装置用于调整喷头的高度,所述径向距离控制装置用于调整喷头的径向距离。
在打印过程中,由于加注系统只在有限范围内做高度方向的运动,因此加注系统始终在显微镜的观察范围内,也即细胞球始终在显微镜有效景深内,采集卡能够全程对细胞球成像并实时监控细胞球状态,一旦打印过程出现差错,控制处理系统会进行智能纠错。
打印所使用的生物墨水为培养于琼脂糖上的细胞球,打印所使用的细胞球,在打印前或者打印中都培养于琼脂糖中,以便保持细胞活性。
作为优选,所述加注系统包括喷头、加注器、加注器控制器、以及加注器固定装置,所述喷头与加注器连接,所述加注器与加注器控制器连接,所述加注器固定装置固定于三维控制系统的径向距离调整装置上。
作为优选,所述显微成像系统包括阵列LED照明装置、显微镜和图像采集卡。
显微镜可以选择具有长工作距离以及大景深的显微镜。
作为优选,所述加注器包括气压控制结构,所述气压控制结构包括空气压缩机和气压调节阀,由加注器控制器控制。
作为优选,所述喷头和备用喷头采用透光性良好的透明材料制造,以便使得细胞球无论是在打印过程前位于琼脂糖上、打印过程中位于喷头内还是打印过程后位于培养皿中都能通过显微镜成像并被中央控制处理系统实时监测,以此来保证整个打印过程的顺利进行以及高质量的打印效果。
采用上述生物打印装置进行生物打印的方法,包括以下步骤:
培育细胞球;
制备培养基;
固定琼脂糖及培养皿;
输入打印图形信息和作为生物墨水的打印源细胞信息;
根据打印源细胞信息,中央控制处理系统自动选择最优喷头规格,中央处理控制系统通过三维控制系统控制加注器在喷头更换平台上选择合适规格的喷头,再通过三维控制系统控制喷头到达工作位置;
初始化装置:粗调显微成像系统的位置以及角度,使得显微镜的工作位置为喷头在吸取打印平台上的投影位置;
粗调二维位移平台,使得在显微成像系统中可以观测到喷头对准第一个细胞球;
精调显微成像系统的位置以及角度及吸取打印平台的位置,使得在显微成像系统中可以同时清晰的观测到细胞球以及喷头,并且它们在同一个水平位置上;
打印开始,打印过程分为依次进行的细胞球吸取过程、状态切换过程和细胞球挤出过程:
细胞球吸取过程:高度调整装置在等待高度时,中央控制处理系统通过加注器控制器使得加注器挤出喷头内部空气,使喷头内形成负压;中央控制处理系统控制高度调整装置向下运动,连带加注器还有喷头移至吸取高度,此时中央控制处理系统通过加注器控制器控制加注器释放喷头内压力,使得喷头将对准的细胞球连同培养液一同吸取;中央控制处理系统控制高度调整装置向上运动,使得加注器和喷头移至等待高度;
状态切换过程:细胞球吸取完成之后,中央控制处理系统控制吸取打印平台上的二维位移平台移至挤出坐标位置,该过程中加注器和喷头始终在等待位置等待;
细胞球挤出过程:当二维位移平台运动至挤出坐标位置后,中央控制处理系统通过加注器控制器控制加注器将喷头内的细胞球以及培养液一同挤出至打印坐标。
整个打印过程由细胞球吸取过程、状态切换过程和细胞球打印过程组成。每完成一次细胞球吸取以及细胞球挤出后,中央控制处理系统根据打印完成状态以及细胞球形态决定是否进入下一个过程,并读取下一个吸取细胞球的坐标和打印坐标,由于琼脂糖上的细胞器是均匀规律排布的,每一个细胞球的坐标都是已知的,而打印坐标由控制处理系统全部计算出。
整个过程中,由于加注器以及喷头始终在吸取位置、等待位置和挤出位置上工作,水平方向上没有发生位置变化,因此吸取以及打印的细胞球始终在显微成像系统的工作范围内,细胞球无论是在打印过程前位于琼脂糖上、打印过程中位于喷头内还是打印过程后位于培养皿中都能通过显微镜成像并被中央控制处理系统实时监测,以此来保证整个打印过程的顺利进行以及高质量的打印效果。并由控制处理系统判断该次细胞球打印过程是否顺利,只有该次细胞球打印过程顺利完成才会进入下一个细胞球的打印过程,否则会放弃该细胞球,以此来保证细胞球在整个打印过程中始终有较高活性,保证整个打印过程的高质量完成。
作为优选,本发明的打印过程均在无菌环境下完成。
作为优选,本发明采用以下方法培育作为生物墨水的细胞球:向高压灭菌过的多孔橡胶模具中加入热的1%-3% G-10琼脂糖溶液,待其冷却后折叠橡胶模具取出琼脂糖并存放在培养皿中, 将密度为1×106~10×106的指定细胞加入到琼脂糖中,并在培养皿周围加入适量的培养基,置于37℃和5% CO2的培养箱中培养3-4天即可获得装有指定细胞球的琼脂糖。
作为优选,培养基采用高糖DMEM和10%的胎牛血清,另外培养上皮细胞系时再加入1%双抗、1%非必需氨基酸和10 ng/mL上皮生长因子。
将培养有指定细胞球的琼脂糖以及准备好用于打印的培养皿分别安放在吸取打印平台上的琼脂糖固定装置和培养皿固定装置上。以此将载有打印细胞源的琼脂糖和用于打印的培养皿准确的固定在吸取打印平台的预设坐标上,中央控制处理系统通过控制吸取打印平台上的二维位移平台便可实现对琼脂糖或者说打印源细胞球位置的精确控制。
作为优选,培育细胞球时的参数如下:
培养时间:3天—5天;
培养温度:37℃;
培养基的基本成分包括:HG DMEM,10%FBS、NEAA非必需氨基酸、Human EGF生长因子、P/S双抗加入ROCK抑制剂:0.1uM—1uM;培养基也可以参照不同的细胞给予相应的体细胞培养液以及干细胞培养液。
作为优选,打印过程中的参数控制如下:
两个细胞球的间距:0.3mm—1.5mm;
包裹细胞球的液滴的体积:3uL—8uL;
细胞球贴壁的时间:12小时—18小时;
细胞球展开至融合成片的时间:5天—8天。
实验发现,将细胞球的间距、包裹细胞球的液滴的体积、细胞球贴壁时间和展开至融合成片的时间控制在上述范围内,细胞球打印形成细胞片效果最佳。
与现有的细胞打印方法相比较而言,本发明将一般的细胞悬液打印改为细胞球打印,细胞球相对于细胞而言具有更好的增殖能力、抗凋亡能力、抗衰老和细胞干性(例如β3-tubulin、Nestin等表达的上调)。与传统平面培养的细胞相比,三维培养的体细胞球(例如角膜上皮细胞、基质细胞、内皮细胞球等)具有较高的干性潜力,有利于分化为特有细胞。同时由细胞球打印出来的生物结构相对于直接由细胞悬液打印出来的生物结构而言,更有利于保持细胞的特有表型与结构(例如角膜内皮细胞球和视网膜上皮细胞球贴壁后更有利于六边形细胞结构的形成与细胞间的紧密连接)。另外细胞球比散细胞更有利于组织损伤的修复。
打印初期根据不同的打印要求以及细胞种类的不同,将细胞成球至不同直径,再由此设定两个打印坐标之间的距离以及喷头规格,可以满足不同生长要求的打印过程,同时由于实际完成吸取以及挤出的加注器和喷头始终在显微镜工作的景深范围内,细胞球始终处于监控中,保证打印质量。
本发明的3D细胞球打印可以形成的根据需要的不同面积与体积的细胞片,细胞片的厚度可根据需要打印形成单层细胞薄片或多层细胞片,而打印的细胞种类可根据需要形成单种细胞片、不同种多细胞单片或不同种多细胞多层细胞片。也可以根据组织结构,打印形成有曲率、球面、以及符合需要移植的缺损组织形态及大小的细胞片。
本发明的3D细胞球打印形成的细胞片不需特殊的支架材料,也不需磁力等特殊材料和设备,与有支架材料的组织构建方法相比,本发明构成的细胞片仅含有细胞,提高了其生物相容性,避免了由于支架材料引入引起的炎症反应,及生物材料降解后的细胞排列顺序紊乱和组织纤维化的副作用,也避免了胶原改性可能带入有害物质(如交联剂)。
本发明的3D细胞球打印可以可通过机器参数设定,快速打印细胞片的二维或三维基本结构,通过细胞培养获得生物活性良好的细胞片。细胞片形成与细胞生长速度相关,本发明的3D细胞球打印使用的是细胞球,与单散细胞打印比较,细胞活性、增殖潜能与干细胞特征都更好,对促进细胞快速增殖、迁移有很好的效果,同时由于细胞球展开后可以形成完整、连续的高密度及有极性的细胞片,对细胞间形成紧密连接有很大帮助,不干扰细胞正常生理过程,移植时可直接粘附于受伤组织。
本发明的3D细胞球打印使用的是细胞球,与单散细胞打印比较,由于细胞活性高,细胞功能的建立更完善,特别有利于构建需要建立屏障功能的细胞片。
(1)建立打印的计算机实体模型,对其进行切片分层,得到每层的形状信息;
(2)根据打印要求培养细胞成球至指定直径,同时准备培养及打印过程中所需的培养液;
(3)根据每层的形状信息,以及打印细胞球的直径和细胞球种类选择喷头和打印间距,并计算出每个细胞球的打印坐标;
(4)中央控制处理系统通过三维控制系统控制加注器,在喷头更换平台上选取最优规格喷头并移动至工作位置;
(5)打印装置初始化,此时培养细胞球的琼脂糖上,第一个细胞球对准喷头,并记录此时的吸取坐标;
(6)步骤(3)中的每个细胞球的打印坐标输入控制处理系统中,通过控制处理系统控制协调装置的运行及工作;
(7)控制二维位移平台移动至吸取坐标,通过高度调整装置调整加注系统的高度,使其移动到吸取高度,控制加注系统的气压控制结构,使得加注系统的喷头吸取对应的细胞球;
(8)细胞球吸取完成后,通过控制处理系统控制二维位移平台移动至打印坐标,并通过高度调整装置调整加注系统的高度,使其移动到打印高度,同时通过控制气压控制结构使得喷头打印对应细胞球;
(9)重复步骤(7)和(8),直至打印完成。
附图说明
图1是本发明的打印装置的结构示意图;
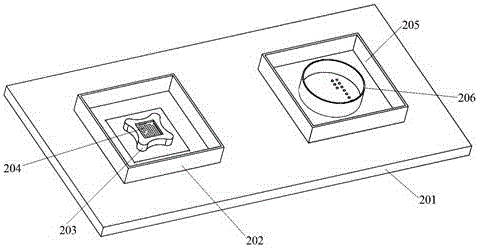
图2是本发明的吸取打印平台的结构示意图;
图3是本发明的加注系统的结构示意图;
图4是本发明的显微成像系统的结构示意图;
图5是人角膜上皮细胞系融合生长及成球示意图;
图6是人角膜上皮细胞系成球第5天的效果示意图;
图7是人角膜上皮细胞系细胞球打印后展开后第五天的示意图;
图8是人角膜上皮细胞系细胞球打印后展开后第七天的示意图。
具体实施方式
下面结合附图和实施例对本发明做进一步详细说明。
实施例:
如图1一种细胞球精准定位生物打印装置包括:固定底板1、吸取及打印平台2、方位角控制装置3、高度调整装置4、径向距离调整装置5、加注系统6、喷头更换平台7、显微成像系统8、中央控制处理系统9和显示系统10,方位角控制装置3、高度调整装置4和径向距离调整装置5构成三维控制系统,加注系统6固定于三维控制系统的径向距离调整装置上,所述控制处理系统9连接了吸取打印平台2、加注系统6、三维控制系统的方位角控制装置3、高度调整装置4和径向距离调整装置5、显微成像系统8和显示系统10,所述显微成像系统8在工作时对准加注系统6在吸取打印平台2上面的投影位置,所述吸取打印平台2包括二维位移平台201、琼脂糖固定装置202和培养皿固定装置205,所述培养皿固定装置用于固定培养皿206,所述琼脂糖固定装置202用于固定琼脂糖203,所述琼脂糖203中培养有作为生物墨水的细胞球204,打印所使用的生物墨水为培养于琼脂糖203上的细胞球204。
所述加注系统包括喷头601、加注器602、加注器控制器603、以及加注器固定装置604,所述喷头601与加注器602连接,所述加注器602与加注器控制器603连接,所述加注器固定装置604固定于三维控制系统的径向距离调整装置5上。
所述显微成像系统包括阵列LED照明装置801、显微镜802和图像采集卡803。
显微镜802选择具有长工作距离以及大景深的显微镜。
所述加注器602包括气压控制结构,所述气压控制结构包括空气压缩机和气压调节阀,由加注器控制器控制。
所述喷头601为中央控制处理系统9根据输入的打印源细胞信息自动选择并通过三维控制系统的方位角控制装置3、高度调整装置4和径向距离调整装置5控制加注系统6在喷头更换平台7选取,所有喷头均采用透光性良好的透明材料制造,以便使得细胞球204无论是在打印过程前位于琼脂糖203上、打印过程中位于喷头601内还是打印过程后位于培养皿206中都能通过显微镜成像并被中央控制处理系统实时监测,以此来保证整个打印过程的顺利进行以及高质量的打印效果。
所述三维控制系统包括方位角控制装置3和径向距离调整装置4与高度调整装置5,所述三维控制系统采用圆柱坐标系,所述方位角控制装置3用于调整喷头601位置的相对方位角,所述的高度调整装置5用于调整喷头601的高度,所述径向距离调整装置4用于调整喷头601的径向距离。采用上述生物打印装置进行生物打印的方法,包括以下步骤:
培育细胞球204;
制备培养基;
固定琼脂糖203及培养皿206;
输入打印图形信息和作为生物墨水的打印源细胞信息;
根据打印源细胞信息,中央控制处理系统9自动选择最优喷头规格,中央处理控制系统9通过三维控制系统的方位角控制装置3、高度调整装置4和径向距离调整装置5控制加注器6在喷头更换平台7上选择合适规格的喷头,再通过三维控制系统控制喷头601到达工作位置;初始化装置:粗调显微成像系统8的位置以及角度,使得显微镜802的工作位置为喷头601在吸取打印平台2上的投影位置;
粗调二维位移平台2,使得在显微成像系统6中可以观测到喷头601对准第一个细胞球204;
精调显微成像系统8的位置以及角度及吸取打印平台2的位置,使得在显微成像系统8中可以同时清晰的观测到细胞球204以及喷头601,并且它们在同一个水平位置上;
打印开始,打印过程分为依次进行的细胞球吸取过程、状态切换过程和细胞球挤出过程:
细胞球吸取过程:高度调整装置4在等待高度时,中央控制处理系统9通过加注器控制器603使得加注器602挤出喷头601内部的空气,使喷头601内形成负压;中央控制处理系统9控制高度调整装置4向下运动,使得加注器602和喷头601移至吸取高度,此时中央控制处理系统9通过加注器控制器603控制加注器602释放喷头601内压力,使得喷头601将对准的细胞球204连同培养液一同吸取;中央控制处理系统9控制高度调整装置4向上运动,使得加注器602和喷头601移至等待高度;
状态切换过程:细胞球204吸取完成之后,中央控制处理系统9控制二维位移平台201移至挤出坐标位置,该过程中加注器602和喷头601始终在等待位置等待;
细胞球挤出过程:当二维位移平台201运动至挤出坐标位置后,中央控制处理系统9通过加注器控制器603控制加注器602将喷头601内的细胞球204以及培养液一同挤出至打印坐标。
整个打印过程由细胞球吸取过程、状态切换过程和细胞球打印过程。每完成一次细胞球吸取以及细胞球挤出后,中央控制处理系统9读取下一个吸取细胞球204的坐标和打印坐标,由于琼脂糖203上的细胞器是均匀规律排布的,每一个细胞球204的坐标都是已知的,而打印坐标由控制处理系统全部计算出。
本实施例的打印过程均在无菌环境下完成。
本实施例采用以下方法培育作为生物墨水的细胞球:向高压灭菌过的多孔橡胶模具中加入热的1%-3% G-10琼脂糖溶液,待其冷却后折叠橡胶模具取出琼脂糖并存放在培养皿中, 将密度为1×106~10×106的指定细胞加入到琼脂糖中,并在培养皿周围加入适量的培养基,置于37℃和5% CO2的培养箱中培养3-4天即可获得装有指定细胞球的琼脂糖。
本实施例中,培养基采用高糖DMEM和10%的胎牛血清,另外培养上皮细胞系时再加入1%双抗、1%非必需氨基酸和10 ng/mL上皮生长因子。培养基也可以参照不同的细胞给予相应的体细胞培养液以及干细胞培养液。
将培养有指定细胞球的琼脂糖以及准备好用于打印的培养皿分别安放在吸取打印平台上的琼脂糖固定装置和培养皿固定装置上。以此将载有打印细胞源的琼脂糖和用于打印的培养皿准确的固定在吸取打印平台的预设坐标上,中央控制处理系统通过吸取打印平台上的二维位移平台便可实现对琼脂糖或者说打印源细胞球位置的精确控制。本实施例中,培育细胞球时的参数如下:
培养时间:3天—5天;
培养温度:37℃;
培养基的成分包括:HG DMEM,10%FBS、NEAA非必需氨基酸、Human EGF生长因子、P/S双抗加入ROCK抑制剂:0.1uM—1uM;培养基也可以参照不同的细胞给予相应的体细胞培养液以及干细胞培养液。
本实施例中,打印过程中的参数控制如下:
两个细胞球的间距:0.3mm—1.5mm;
包裹细胞球的液滴的体积:3uL—8uL。
- 还没有人留言评论。精彩留言会获得点赞!