一种路德维希肠杆菌及其在诱导镁离子成矿中的应用的制作方法
本发明涉及微生物领域,具体地说,涉及一种路德维希肠杆菌及其在诱导镁离子成矿中的应用。
背景技术:
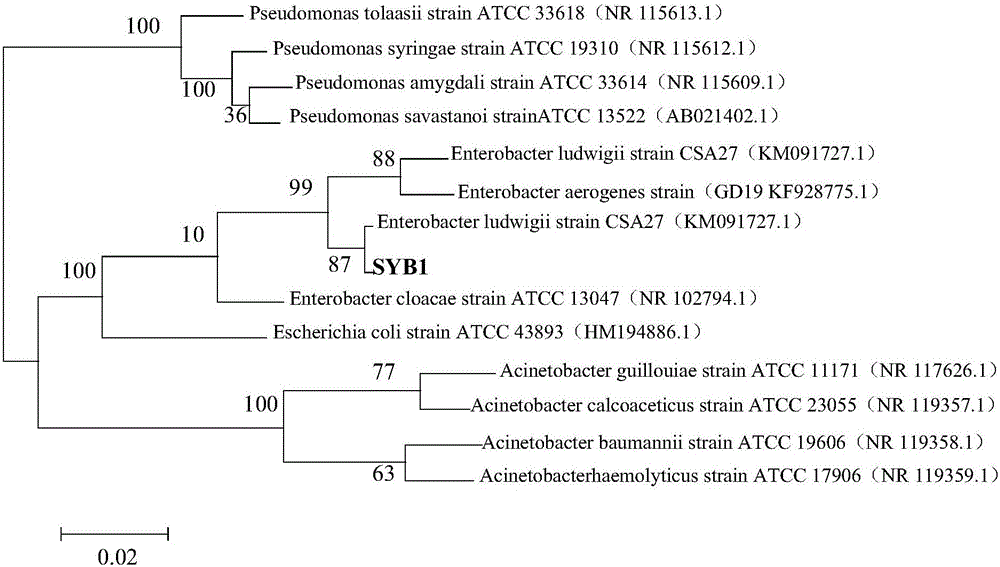
:菱镁矿,又称菱镁石或碱菱镁苦土,是镁的碳酸盐矿物,主要化学成分为碳酸镁(MgCO3)。菱镁矿经加工后主要用作工业高温炉窖及设备耐高温、抗侵蚀等方面的耐火材料。此外,还应用在建材、化工、农牧业、造纸、航天航空、汽车及环保等行业。而且菱镁石是生产碱性耐火材料的基本原料,是我国耐火原料的三大支柱之一。目前,全国镁质材料行业已开发生产了镁质材料、镁质定形和不定形耐火材料、溶剂、镁质化工材料、金属镁及镁合金等七大系列几百种产品。全国现有各类镁质原料生产企业600多家,拥有资产总额200亿元以上,从业人员20多万人,生产能力1500多万吨,其中出口200多万吨,出口创汇6亿多美元,产品远销世界50多个国家和地区。我国现已探明的菱镁矿储量达31.18×108t,占世界探明储量的31%左右,居世界之首。但经过几十年的开采,商品级的菱镁矿已越来越少。现在企业通常都利用浮选、轻烧、热选、重选、化学等方法对不纯的菱镁矿进行纯化以满足市场需求。但是这些方法有的条件苛刻,有的操作较为复杂,成本高。所以现在急需一种操作简便,成本低廉的方法生产高质量的菱镁石以解决菱镁矿短缺的问题。球碳镁石又称杜平石(Mg5(CO3)4(OH)2·5H2O),是一种花状矿物,常与三水菱镁矿伴(共)生,但目前对球碳镁石的报道很少。很多文章中指出,球碳镁石易在微生物诱导的条件下形成,而且一般都会和含镁碳酸盐矿物共生,所以球碳镁石对微生物诱导条件下含镁碳酸盐矿物,尤其是菱镁矿的的形成,有重大的研究意义。肠杆菌在自然界分布非常广泛,生理特性丰富多样,是土壤和植物微生态优势种群之一。肠杆菌属的菌株一般都有强大的沉降金属离子的能力。路德维希肠杆菌(Enterobacterludwigii)是肠杆菌中具强大应用潜力的菌种之一,其已在环境污染治理等行业取得了较好的研究成果,例如路德维希肠杆菌对Cd2+具有很好的成矿效果。因此,有针对性的筛选路德维希肠杆菌菌株,制备菌剂,通过人工接种有效诱导Mg2+成矿是一项十分必要的工作和切实可行的途径。技术实现要素:本发明所要解决的技术问题是如何利用肠杆菌菌株诱导镁离子成矿,为含镁废水的处理及三水菱镁矿的生成提供一种新方法。本发明的技术方案之一,是提供一种路德维希肠杆菌菌株,所述菌株的分类命名为EnterobacterludwigiiSYB1,已于2016年6月27日在中国微生物菌种保藏管理委员会普通微生物中心保藏,保藏编号为CGMCCNo.12709。本发明的技术方案之二,是提供上述路德维希肠杆菌菌株在诱导镁离子成矿中的应用。优选地,上述路德维希肠杆菌菌株在诱导镁离子成矿中的应用包括如下步骤:向含有Mg2+的液相体系中加入上述保藏编号为CGMCCNo.12709的路德维希肠杆菌。优选地,上述含有Mg2+的液相体系中Mg2+的浓度为0.03~0.12mol/L。优选地,上述含有Mg2+的液相体系中还包括Ca2+,且Mg/Ca(摩尔浓度比)等于12。优选地,上述Ca2+的浓度为0.01mol/L。本发明的有益效果:(1)控制溶液中的Mg/Ca比,利用本发明所述路德维希肠杆菌菌株可以制备高质量的菱镁矿,且操作简单,价格低廉,对环境友好;(2)本发明所述路德维希肠杆菌菌株对Mg2+和Ca2+具有明显的沉降效果,用于硬水软化领域,前景广阔。保藏说明:菌种名称:路德维希肠杆菌;拉丁名:Enterobacterludwigii;菌株编号:SYB1;保藏机构:中国微生物菌种保藏管理委员会普通微生物中心;保藏机构简称:CGMCC;地址:北京市朝阳区北辰西路1号院3号;保藏日期:2016年06月27日;保藏中心登记入册编号:CGMCCNo.12709。附图说明图1为路德维希肠杆菌EnterobacterludwigiiSYB1在高分辨率透射电镜下的形态图;图2为路德维希肠杆菌EnterobacterludwigiiSYB1的系统发育树图;图3为含不同Mg/Ca比的培养基中路德维希肠杆菌EnterobacterludwigiiSYB1的生长曲线图;图4为含不同Mg/Ca比的培养基中路德维希肠杆菌EnterobacterludwigiiSYB1的pH值变化曲线图;图5为对照组矿物沉淀的X射线衍射分析图;图6为实验组矿物沉淀的X射线衍射分析图;图7为对照组在含钙镁培养基戊中形成的表面形貌为圆球状的矿物沉淀的扫描电镜图和能谱分析图;图8为对照组在含钙镁培养基戊中形成的表面形貌为菱面体的矿物沉淀的扫描电镜图和能谱分析图;图9为实验组在含钙镁培养基甲中矿物沉淀的扫描电镜图;图10为实验组在含钙镁培养基甲中矿物沉淀的能谱分析;图11为实验组在含钙镁培养基乙中矿物沉淀的扫描电镜图;图12为实验组在含钙镁培养基乙中矿物沉淀的能谱分析;图13为实验组在含钙镁培养基丙中矿物沉淀的扫描电镜图;图14为实验组在含钙镁培养基丙中矿物沉淀的能谱分析;图15为实验组在含钙镁培养基丁中矿物沉淀的扫描电镜图;图16为实验组在含钙镁培养基丁中矿物沉淀的能谱分析;图17为实验组在含钙镁培养基戊中矿物沉淀的扫描电镜图;图18为实验组在含钙镁培养基戊中矿物沉淀的能谱分析;图19为对照组含不同Mg/Ca比的培养基中,Mg2+的变化趋势图;图20为实验组含不同Mg/Ca比的培养基中,Mg2+的变化趋势图;图21为对照组含不同Mg/Ca比的培养基中,Ca2+的变化趋势图;图22为实验组含不同Mg/Ca比的培养基中,Ca2+的变化趋势图。具体实施方式下面结合附图和具体实施例对本发明的具体实施方式作进一步的说明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。下述实施例中所用的培养基如下:富集培养基:溶质及其浓度为K2HPO40.5g/L,NH4Cl1.0g/L,CaCl20.1g/L,MgSO4·7H2O2.0g/L,酵母浸粉1.0g/L,Na2SO40.5g/L,Fe(NH4)2(SO4)20.5g/L,抗坏血酸0.5g/L,L-Cys0.5g/L,60%的乳酸钠溶液6mL/L;溶剂为蒸馏水;pH6.0~8.0;其中Fe(NH4)2(SO4)2、抗坏血酸和L-Cys需先用蒸馏水配制成母液,再用0.22μm滤膜过滤除菌,然后用于制备富集培养基;60%的乳酸钠溶液为国药集团化学试剂有限公司产品,产品目录号为30168018。固体纯化培养基:将牛肉膏5g,胰蛋白胨10g,NaCl5g溶于1L蒸馏水,调节pH至7.5,然后加入琼脂20g。液体纯化培养基:将牛肉膏5g,胰蛋白胨10g和NaCl5g溶于1L蒸馏水,调节pH至7.5。2mol/LNa2CO3水溶液:取10.6g的Na2CO3,溶解于50mL无菌蒸馏水中,然后用孔径为0.22微米的滤膜过滤。1.07mol/LNaHCO3水溶液:取9.0g的NaHCO3,溶解于100mL无菌蒸馏水中,然后用孔径为0.22微米的滤膜过滤。含钙镁培养基甲:将牛肉膏5g,胰蛋白胨10g和NaCl5g溶于蒸馏水,然后加入1.47g的CaCl2·2H2O和0ml2mol/L的MgSO4·7H2O溶液定容至1L,121℃高温灭菌30min。冷却后加入2mol/LNa2CO35mL和1.07mol/LNaHCO33mL,调节pH至7.5。含钙镁培养基甲中,Mg/Ca比为0(摩尔浓度比),Ca2+的浓度为0.01mol/L,Mg2+的浓度为0mol/L。应当说明的是,本文中提到的Mg/Ca均指Mg2+/Ca2+的摩尔浓度比。含钙镁培养基乙:将牛肉膏5g,胰蛋白胨10g和NaCl5g溶于蒸馏水,然后加入1.47g的CaCl2·2H2O和15ml2mol/L的MgSO4·7H2O溶液定容至1L,121℃高温灭菌30min。冷却后加入2mol/LNa2CO35mL和1.07mol/LNaHCO33mL,调节pH至7.5。含钙镁培养基乙中,Mg/Ca比为3(摩尔浓度比),Ca2+的浓度为0.01mol/L,Mg2+的浓度为0.03mol/L。含钙镁培养基丙:将牛肉膏5g,胰蛋白胨10g和NaCl5g溶于蒸馏水,然后加入1.47g的CaCl2·2H2O和30ml2mol/L的MgSO4·7H2O溶液定容至1L,121℃高温灭菌30min。冷却后加入2mol/LNa2CO35mL和1.07mol/LNaHCO33mL,调节pH至7.5。含钙镁培养基丙中,Mg/Ca比为6(摩尔浓度比),Ca2+的浓度为0.01mol/L,Mg2+的浓度为0.06mol/L。含钙镁培养基丁:将牛肉膏5g,胰蛋白胨10g和NaCl5g溶于蒸馏水,然后加入1.47g的CaCl2·2H2O和45ml2mol/L的MgSO4·7H2O溶液定容至1L,121℃高温灭菌30min。冷却后加入2mol/LNa2CO35mL和1.07mol/LNaHCO33mL,调节pH至7.5。含钙镁培养基丁中,Mg/Ca比为9(摩尔浓度比),Ca2+的浓度为0.01mol/L,Mg2+的浓度为0.09mol/L。含钙镁培养基戊:将牛肉膏5g,胰蛋白胨10g和NaCl5g溶于蒸馏水,然后加入1.47g的CaCl2·2H2O和60ml2mol/L的MgSO4·7H2O溶液定容至1L,121℃高温灭菌30min。冷却后加入2mol/LNa2CO35mL和1.07mol/LNaHCO33mL,调节pH至7.5。含钙镁培养基戊中,Mg/Ca比为12(摩尔浓度比),Ca2+的浓度为0.01mol/,Mg2+的浓度为0.12mol/L。X射线衍射分析使用转靶X射线衍射仪,日本理学电器公司产品,产品型号为D/Max-RC;扫描电镜分析使用日本日立公司产品,产品型号为HitachiS-4800;能谱分析使用美国伊达克斯有限公司产品,产品型号为GENESIS能谱仪;高分辨率透射电镜分析使用日本电子株式会社公司产品,产品型号为JEM-2100。实施例1路德维希肠杆菌EnterobacterludwigiiSYB1CGMCCNo.12709的分离、鉴定和保藏一、硫酸盐还原菌SYB1的分离1、在100mL无菌蒸馏水中加入10g岩石粉末样品(采自中国济南长清馒头山的白云岩),搅拌均匀,静止放置10分钟,然后取20mL上清液加入200mL富集培养基中,并用无菌液体石蜡封闭瓶内液面,置于37℃恒温培养箱中静置培养、观察。培养至第7天,富集培养基颜色变黑,可见硫酸盐还原菌富集成功(富集培养基中的Fe(NH4)2(SO4)2中的亚铁离子能与富集培养基中的S2-反应生成黑色的硫化亚铁)。2、完成步骤1后,取上清液接种至含0.5g/LFe(NH4)2(SO4)2的固体纯化培养基上,37℃厌氧培养箱中培养、观察。培养至第7天,产生黑色单菌落。挑取单菌落,反复纯化3次以上。将筛选到的一株硫酸盐还原菌菌株命名为硫酸盐还原菌SYB1。二、硫酸盐还原菌SYB1的鉴定1、形态学鉴定将硫酸盐还原菌SYB1接种到固体纯化培养基上,3天后观察单菌落的形态。结果表明,硫酸盐还原菌SYB1菌落圆形,直径3.0~5.0mm,表面光滑有光泽,质地粘,不透明。硫酸盐还原菌SYB1经染色后,鉴定为革兰氏阳性菌。通过高分辨率透射电镜分析硫酸盐还原菌SYB1,实验结果见图1。结果表明,硫酸盐还原菌SYB1的大小约1.0μm×0.5μm,细菌为短杆状,有夹膜和鞭毛。2、16SrDNA序列同源性分析硫酸盐还原菌SYB1的16SrDNA如序列表中的序列1所示。通过ClustalX软件将序列表中的序列1与GenBank中的序列进行比对,采用邻接法(N-J法)构建系统发育树。系统发育树的实验结果见图2。硫酸盐还原菌SYB1与路德维希肠杆菌(Enterobacterludwigii)同源性达到99%。综合上述各个鉴定结果,硫酸盐还原菌SYB1为路德维希肠杆菌(Enterobacterludwigii)。三、硫酸盐还原菌SYB1的保藏EnterobacterludwigiiSYB1已于2016年06月27日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称CGMCC,地址为:北京市朝阳区北辰西路1号院3号),保藏编号为CGMCCNo.12709。硫酸盐还原菌SYB1的全称为路德维希肠杆菌(Enterobacterludwigii)CGMCCNo.12709,简称为路德维希肠杆菌SYB1或SYB1。实施例2制备路德维希肠杆菌SYB1菌剂将路德维希肠杆菌SYB1在固体纯化培养基上活化,然后挑取单菌落接种于装有100mL液体纯化培养基的250mL锥形瓶中,37℃、130r/min的恒温摇床上培养1天,得到OD600值约为1.80的路德维希肠杆菌SYB1菌剂甲。路德维希肠杆菌SYB1菌剂甲在下文简称为SYB1菌剂甲。实施例3路德维希肠杆菌SYB1的特性本实施例研究不同Mg/Ca比下路德维希肠杆菌SYB1的生长曲线和pH变化曲线。分别采用各个培养基(含钙镁培养基甲、含钙镁培养基乙、含钙镁培养基丙、含钙镁培养基丁和含钙镁培养基戊)进行如下操作:取6个250mL的锥形瓶,每个锥形瓶装入150mL培养基,将6个锥形瓶分为实验组和对照组,每组3个锥形瓶;向实验组的锥形瓶中接种SYB1菌剂甲1.5mL,向对照组的锥形瓶中接种等体积无菌超纯水;接种完毕后,将锥形瓶置于恒温振荡培养箱,37℃、130r/min培养。接种完毕时取样4mL,然后每3小时取样4mL,测量菌浓度和pH值。进行三次试验,结果取平均值。实验组中SYB1的生长曲线见图3。SYB1在各个培养基中的生长过程均包括延滞期(图3的0~3h)、对数期(图3的3~50h)和稳定期(图3的50~79h)三个阶段:(1)延滞期,此时细菌正在适应培养基内的生长条件,从图中可看出是0~3h,即为硫酸盐还原菌SYB1生长的延滞期。(2)对数期,代表着活跃的细胞分裂状态,从图中可以看出是3~50h,即在这段时间内硫酸盐还原菌SYB1在迅速生长。(3)稳定期,此时由于培养基内的营养物质被消耗以及有毒代谢产物的逐渐积累,细菌的生长速率逐渐减慢,但总生物量基本维持不变。从图中可看出是50~79h。在此期间内,硫酸盐还原菌SYB1生长速率与衰亡分解速率相当,细菌处于稳定期。实施例4微生物诱导矿化培养1、分别采用培养基(钙镁培养基甲、钙镁培养基乙、钙镁培养基丙、钙镁培养基丁和钙镁培养基戊)进行如下操作:取30个250mL的锥形瓶,每个锥形瓶装入150mL的培养基,并按照不同镁钙比分成5大组,每一大组有6瓶。2、完成步骤1后,将每一个镁钙比下的6个锥形瓶分为实验组和对照组,每组3个锥形瓶。向实验组的每个锥形瓶中接种实施例2制备的SYB1菌剂甲1.5mL(接种比例1:100),向对照组的每个锥形瓶中接种1.5mL的无菌超纯水。接种完毕后,将所有锥形瓶置于恒温振荡培养箱,37℃、130r/min培养14天。实施例5对实施例4中对照组和实验组中获得的矿物沉淀进行分析。一、X射线衍射(X-raydiffraction,XRD)分析取实施例4步骤2中培养14天的各培养基底部沉淀,置于1.5mL离心管,静置5min,弃上清液,然后每个离心管中各加入1mL的蒸馏水进行洗涤,静置5分钟,弃上清,洗涤三次,以除去各种盐离子,沉淀自然干燥后进行XRD分析。XRD扫描角度为10~90°,步长为0.02,扫描速度8°/min。实验结果见图5和图6(图5为对照组,图6为实验组,其中Mg/Ca=0、Mg/Ca=3、Mg/Ca=6、Mg/Ca=9和Mg/Ca=12分别代表含钙镁培养基甲、含钙镁培养基乙、含钙镁培养基丙、含钙镁培养基丁和含钙镁培养基戊中的镁钙摩尔比)和表1。结果表明,路德维希肠杆菌EnterobacterludwigiiSYB1与产生球碳镁石和三水菱镁矿矿物沉淀有密切联系。培养了14天的实验组中,Mg/Ca比为0时图中为方解石对应的衍射峰,所以Mg/Ca比为0时,含钙镁培养基甲中生成的矿物是方解石;Mg/Ca比为3时图中为单水方解石对应的衍射峰,所以Mg/Ca比为3时,含钙镁培养基乙中生成的矿物为单水方解石;Mg/Ca为6和9时图中有单水方解石对应的衍射峰,也有球碳镁石对应的衍射峰,所以当Mg/Ca比为6和9时,含钙镁培养基丙和丁中均生成了单水方解石和球碳镁石,此时Mg2+浓度为0.06~0.09mol/L,Ca2+浓度为0.01mol/L;当Mg/Ca比为12时图中为三水菱镁矿的衍射峰,所以生成的矿物是三水菱镁矿,此时Mg2+浓度为0.12mol/L,Ca2+浓度为0.01mol/L。在对照组中,所有Mg/Ca比下生成矿物的衍射峰均与方解石对应,所以对照组中生成的矿物均为方解石。对照组和实验组中生成矿物的种类有很大差异,说明在微生物的作用下,培养基中所生成碳酸盐矿物的种类发生了明显的变化。表1.XRD分析矿物沉淀二、矿物沉淀的扫描电镜和能谱分析取实施例4步骤2中培养14天的各培养基底部沉淀,置于1.5mL离心管,静置5min,弃上清液,然后每个离心管中各加入1mL的蒸馏水进行洗涤,静置5分钟,弃上清,洗涤三次,以除去各种盐离子,然后向沉淀中加入100μL的无水乙醇进行悬浮。取部分样品置于载物台上,自然干燥后喷金,置于扫描电镜下观察,然后进行能谱分析。实验结果如下:图7为对照组在含钙镁培养基戊中形成的表面形貌为圆球状的矿物沉淀和能谱分析图,图8为对照组在含钙镁培养基戊中形成的表面形貌为菱面体的矿物沉淀和能谱分析图。结果表明,对照组在含钙镁培养基戊中形成的矿物沉淀形貌主要是圆球状、菱面体,且表面粗糙。能谱分析表明,圆球状矿物主要含有C、O和Ca三种元素,菱面体矿物主要含有C、O、Ca和少量的Mg元素,另外,这两种矿物中均含有Na元素和Al元素,其中Na可能来源于培养液中的NaCl,Al元素可能来源于载物台。由于对照组中生成矿物均为方解石,所以在此不一一列举。图5为实验组在含钙镁培养基甲中形成的矿物沉淀的扫描电镜图和能谱分析图。扫描电镜结果图9表明含钙镁培养基甲中形成的矿物沉淀的表面形貌为菱面体,表面比较粗糙且含有大量的孔隙,矿物由许多纳米级颗粒状矿物组成。结果表明,在含钙镁培养基甲中EnterobacterludwigiiSYB1可以影响所形成矿物的形貌。对图9中的矿物进行能谱分析,结果图10表明该矿物主要含有C、O和Ca这三种元素,说明形成的矿物为CaCO3,此外矿物还含有少量的Na元素和Al元素,推测钠元素可能来源于培养液中的氯化钠,Al元素可能来源于载物台。图6为实验组在含钙镁培养基乙中形成的矿物沉淀的扫描电镜图和能谱分析图。扫描电镜结果图11表明,实验组在含钙镁培养基乙中形成的矿物沉淀的表面形貌发生了巨大变化,呈不规则球状,且球状矿物表面也有少量花状矿物。球状矿物直径约14μm,由许多小的菱面体矿物聚集形成,且矿物上附着大量的菌体。对图11中的矿物进行能谱分析,结果图12表明该矿物主要含C、O、Ca这3种元素,说明形成的矿物为CaCO3,此外矿物还含有少量的Al元素和Mg元素,Mg元素可能是溶液中高浓度的Mg2+附着在矿物上形成,Al元素可能来源于载物台。图7和图8分别为实验组在含钙镁培养基丙、含钙镁培养基丁中形成的矿物沉淀的扫描电镜图和能谱分析图。扫描电镜结果图13和图15表明,两种培养基中所形成的矿物沉淀的表面形貌均为花状。花状矿物直径约为10μm。分别对图13和图15的矿物进行能谱分析,结果图14和图16表明,花状矿物均含有C、O和Mg三种元素,说明形成的矿物为碳酸镁盐类,但含钙镁培养基丙中所形成矿物中含少量的Ca元素,说明可能形成了少量CaCO3。结合XRD图,说明含钙镁培养基丙、丁中形成的矿物均为球碳镁石。此外,两种培养基所形成的矿物中还有Al元素和Pt元素,其中Al元素可能来自载物台,Pt元素的存在可能是实验时对矿物喷金所致。图9为实验组在含钙镁培养基戊中形成的矿物沉淀的扫描电镜图和能谱分析图。扫描电镜结果图17表明,实验组在含钙镁培养基戊中形成了大量杆状矿物,矿物表面光滑且形状规则。杆状矿物长度在10μm-80μm。对图17中杆状矿物进行能谱分析,结果表明,杆状矿物主要含C、O和Mg三种元素,结合XRD图,说明形成的杆状矿物为三水菱镁矿。此外,杆状矿物还含有少量Al元素和Pt元素,其中Al元素可能来自载物台,Pt元素的存在可能是实验时对矿物喷金所致。图19为对照组在含不同Mg/Ca比的培养基中Mg2+的变化趋势图,图20为实验组在含不同Mg/Ca比的培养基中Mg2+的变化趋势图。对比图19和图20可以说明,路德维希肠杆菌EnterobacterludwigiiSYB1对溶液中的Mg2+有明显的沉降作用。图21为对照组在含不同Mg/Ca比的培养基中Ca2+的变化趋势图,图22为实验组在含不同Mg/Ca比的培养基中Ca2+的变化趋势图。对比图21和图22可以说明,路德维希肠杆菌EnterobacterludwigiiSYB1对溶液中的Ca2+有明显的沉降作用。具体数值见表2-表5所示。表2对照组含不同Mg/Ca比培养基中Mg2+变化情况表3实验组含不同Mg/Ca比培养基中Mg2+变化情况时间(天)Mg/Ca=3Mg/Ca=6Mg/Ca=9Mg/Ca=12186.4194.4302.4410.4380189.6295.3397.5476.3185.4284.6381.4542177.3195.63287.3649139.1156.1256.1742138.65176.3237.65834.3128.69138.38213.6931121.3120.3200.31032.7108.9118.6186.2112595109.5180.3由表2和表3可以看出,在Mg/Ca比为3、6、9和12的培养基中,对照组中Mg2+分别减少了43.2、92.67、93.4和105.2mg。实验组中Mg2+分别减少了61.4、99.4、192.9和230.1mg。说明路德维希肠杆菌SYB1对溶液中的Mg2+有很好的沉降效果。表4对照组含不同Mg/Ca比培养基中Ca2+变化情况时间(天)Mg/Ca=0Mg/Ca=3Mg/Ca=6Mg/Ca=9Mg/Ca=120270260251190.471702233.63190.89160.91143.82124.554160.91150.37124.559288.1826133.63121.66106.367851.821295.2990.3884.5855.4236.471488.748.05672.0849.2324.711683.5377.6671.7647.0822.081880.4271.3265.8935.4117.92表5实验组含不同Mg/Ca比培养基中Ca2+变化情况时间(天)Mg/Ca=0Mg/Ca=3Mg/Ca=6Mg/Ca=9Mg/Ca=120270260.73251.82220.65188.182160.01150.82142.73120.53115.464124.545120.75115.467851.82697.27392.8388.1827433.641233.6428.6422.0818.657.061422.0819.3213.7510.16.321618.8216.5912.947.065.421817.9215.7812.945.420.51由表4和表5可以看出,在Mg/Ca比为0、3、6、9和12的培养基中,对照组中Ca2+分别减少189.58、188.68、185.11、155.06和152.08mg。实验组中Ca2+分别减少了252.08、244.95、215.23、和187.67mg。说明路德维希肠杆菌SYB1可加快并加大溶液中的Ca2+的沉降。应当指出的是,上述说明并非是对本发明的限制,本发明也并不仅限于上述举例,本
技术领域:
的技术人员在本发明的实质范围内所做出的变化、改型、添加或替换,也应属于本发明的保护范围。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1