分子标志物在骨关节炎中的应用的制作方法
本发明属于生物医药领域,涉及分子标志物在骨关节炎中的应用,具体的该分子标志物为FGGY。
背景技术:
骨关节炎是一种慢性关节疾病。它以关节软骨的变性、软骨组织的破坏以及关节周围骨质的增生为特征。骨关节炎的发生率随着年龄的增长而增高,它是一种常见的老年性的关节疾病,也是老年人疼痛和致残的主要病因。全世界范围内的研究显示60-65%的60岁以上老人患有症状性骨关节炎,并且80%的此类患者活动受限。
随着中国经济的快速发展、营养水平的提高以及医疗水平的改善,居民的平均寿命得到延长且逐渐步入老龄化社会;因此对于慢性病的预防和控制变得更加重要。骨关节炎作为一种慢性病,给社会带来了诸如残疾、活动障碍和疼痛的社会问题,更增加了医疗和护理的负担。
虽然目前研究认为骨关节炎的发病与年龄、性别有关,且与遗传因素和环境因素等密切相关,但骨关节炎的发病机制仍不明确。骨关节炎发病通常累及膝关节,早期症状较轻,容易延误诊断,临床上大多数骨关节炎患者至医院就诊时已经处于中晚期,晚期患者往往只能通过关节置换手术治疗,给患者和家属带来了巨大的精神和经济负担。因此,骨关节炎的早期诊断、治疗效果监测和预后评估对于骨关节炎的防治具有重要作用。目前,骨关节炎的诊断仍然依赖于临床症状和X线影像学诊断,K-L分级仍为判断骨关节炎严重程度、预后和指导骨关节炎治疗的主要依据。理论上,分子标志物的发现是疾病诊断、疗效检测和预后评估最敏感、最有效的指标。因此,寻找新的骨关节炎分子标志物和药物靶点是骨关节炎早期防治中亟待解决的关键问题。
分子靶向治疗是指在细胞分子水平上,调控疾病相关基因、干预疾病异常的信号通路或阻断能量通路,寻找可干预的分子靶点对骨关节炎的靶向治疗具有重要的意义。
技术实现要素:
为了弥补现有技术的不足,本发明的目的在于提供一种用于骨关节炎诊断和治疗的分子标志物。
为了实现上述目的,本发明采用如下技术方案:
本发明提供了FGGY基因的应用,用于制备诊断骨关节炎的产品。
进一步,所述产品通过测定样本中FGGY的表达水平来诊断骨关节炎。
进一步,FGGY在骨关节炎中表达上调。
进一步,所述产品包括通过通过测序技术、核酸杂交技术、核酸扩增技术或免疫测定的方法检测FGGY基因和/或其表达产物的变化。
进一步,所述核酸扩增技术选自聚合酶链式反应、逆转录聚合酶链式反应、转录介导的扩增、连接酶链式反应、链置换扩增和基于核酸序列的扩增。
本发明提供了一种诊断骨关节炎的产品,所述产品能够通过检测样本中FGGY基因基因和/或其表达产物的变化来诊断骨关节炎。
进一步,所述产品包括芯片、试剂盒或制剂。
进一步,所述产品包括芯片、试剂盒或制剂。其中,所述芯片包括基因芯片、蛋白质芯片;所述基因芯片包括固相载体以及固定在固相载体的寡核苷酸探针,所述寡核苷酸探针包括用于检测FGGY基因转录水平的针对FGGY基因的寡核苷酸探针;所述蛋白质芯片包括固相载体以及固定在固相载体的FGGY蛋白的特异性抗体或配体;所述试剂盒包括基因检测试剂盒和蛋白免疫检测试剂盒;所述基因检测试剂盒包括用于检测FGGY基因转录水平的试剂;所述蛋白免疫检测试剂盒包括FGGY蛋白的特异性抗体或配体。
本发明所述的基因芯片或基因检测试剂盒可用于检测包括FGGY基因在内的多个基因(例如,与骨关节炎相关的多个基因)的表达水平。所述蛋白芯片或蛋白免疫检测试剂盒可用于检测包括FGGY蛋白在内的多个蛋白质(例如与骨关节炎相关的多个蛋白质)的表达水平。将骨关节炎的多个标志物同时进行检测,可大大提高骨关节炎诊断的准确率。
本发明提供了FGGY基因在制备治疗骨关节炎的药物组合物中的应用。
进一步,所述药物组合物包括FGGY基因和/或其表达产物的下调剂。所述下调剂包括抑制FGGY基因表达的物质、抑制FGGY基因表达产物稳定性的物质、和/或抑制FGGY基因表达产物活性的物质。
优选的,所述下调剂为针对FGGY基因的siRNA、或针对FGGY蛋白的抗体。
进一步,所述药物组合物还包括抗骨关节的其他药物,药物之间的联用,有利于疾病的有效的治疗。
本发明的优点和有益效果:
本发明首次发现了分子标志物FGGY与骨关节炎发生发展相关,通过检测受试者FGGY的变化,可用于骨关节炎的诊断。
本发明为骨关节炎的机制研究提供了理论依据,为骨关节炎的临床诊断和治疗提供了一种辅助手段。
附图说明
图1为利用高通量测序检测基因在骨关节炎组织中的差异表达情况图;
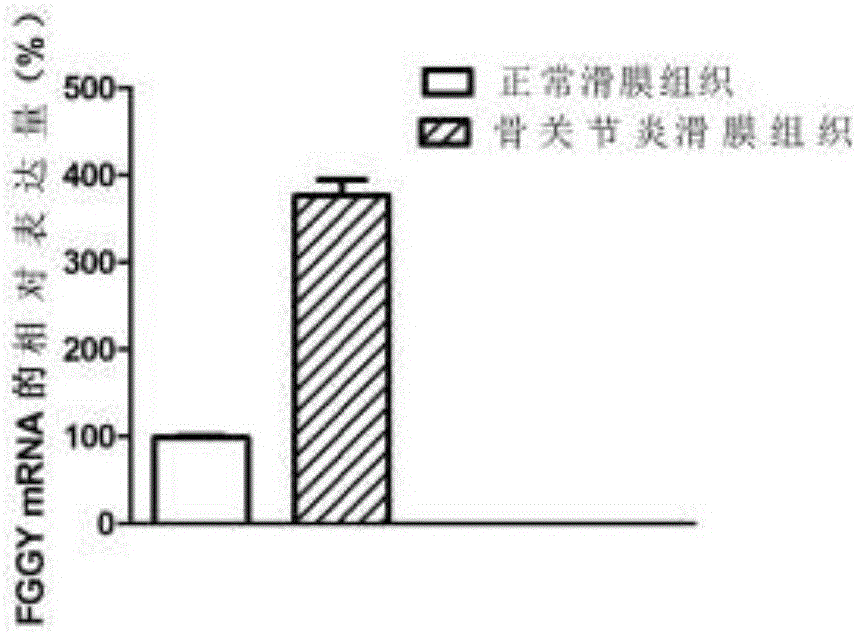
图2为利用QPCR检测FGGY基因在骨关节炎患者中的表达情况图。
具体的实施方式
本发明经过广泛而深入的研究,通过大量筛选,首次发现了在骨关节炎中FGGY呈现特异性低表达。
FGGY
FGGY基因编码的蛋白可以磷酸化核酮糖、核糖醇、L-阿拉伯糖醇等碳水化合物,有研究发现在一些人群中,该基因的多态性与散发型肌萎缩侧索硬化有关。
可用于本发明的FGGY多核苷酸或蛋白(多肽)序列包括各种来源和物种的FGGY,并且包括野生型、突变型的FGGY,或其活性片段。在本发明的一些实施方案中,所述FGGY来源于人类,一种代表性的人FGGY的编码序列或氨基酸序列分别如SEQ ID NO.1和SEQ ID NO.2所示。
本发明的多核苷酸可以是DNA形式或RNA形式。DNA形式包括cDNA、基因组DNA或人工合成的DNA。DNA可以是单链的或是双链的。DNA可以是编码链或非编码链。
本发明的多肽可以是重组多肽、天然多肽、合成多肽,优选重组多肽。本发明的多肽还可包括或不包括起始的甲硫氨酸残基。
编码FGGY的成熟多肽的多核苷酸包括:只编码成熟多肽的编码序列;成熟多肽的编码序列和各种附加编码序列;成熟多肽的编码序列(和任选的附加编码序列)以及非编码序列。术语“编码多肽的多核苷酸”可以是包括编码此多肽的多核苷酸,也可以是还包括附加编码和/或非编码序列的多核苷酸。
本发明还涉及上述多核苷酸的变异体,其编码与本发明有相同的氨基酸序列的多肽或多肽的片段、类似物和衍生物。此多核苷酸的变异体可以是天然发生的等位变异体或非天然发生的变异体。这些核苷酸变异体包括取代变异体、缺失变异体和插入变异体。如本领域所知的,等位变异体是一个多核苷酸的替换形式,它可能是一个或多个核苷酸的取代、缺失或插入,但不会从实质上改变其编码多肽的功能。
本发明还涉及与上述的序列杂交的核酸片段,包括正义和反义的核酸片段。如本文所用,“核酸片段”的长度至少含15个核苷酸,较好是至少30个核苷酸,更好是至少50个核苷酸,最好是至少100个核苷酸以上。核酸片段可用于核酸的扩增技术(如PCR)以确定和/或分离编码FGGY蛋白的多核苷酸。
本发明的人FGGY核苷酸全长序列或其片段通常可以用PCR扩增法、重组法或人工合成的方法获得。对于PCR扩增法,可根据已公开的有关核苷酸序列,尤其是开放阅读框序列来设计引物,并用市售的cDNA库或按本领域技术人员已知的常规方法所制备的cDNA库作为模板,扩增而得有关序列。当序列较长时,常常需要进行两次或多次PCR扩增,然后再将各次扩增出的片段按正确次序拼接在一起。一旦获得了有关的序列,就可以用重组法来大批量地获得有关序列。这通常是将其克隆入载体,再转入细胞,然后通过常规方法从增殖后的宿主细胞中分离得到有关序列。
宿主细胞和载体
本发明所述携带基因的载体是本领域已知的各种载体,如市售的载体、包括质粒、粘粒、噬菌体、病毒等。宿主细胞可以是原核细胞,如细菌细胞;或是低等真核细胞,如酵母细胞;或是高等真核细胞,如哺乳动物细胞。代表性例子有:大肠杆菌,链霉菌属的细菌细胞;真菌细胞如酵母;植物细胞;果蝇S2或Sf9的昆虫细胞;CHO、COS、或293细胞的动物细胞等。
用重组DNA转化宿主细胞可用本领域技术人员熟知的常规技术进行。当宿主为原核生物如大肠杆菌时,能吸收DNA的感受态细胞可在指数生长期后收获,用CaCl2法处理,所用的步骤在本领域众所周知。另一种方法是使用MgCl2。如果需要,转化也可用电穿孔的方法进行。当宿主是真核生物,可选用如下的DNA转染方法:磷酸钙共沉淀法,常规机械方法如显微注射、电穿孔、脂质体包装等。
在上面的方法中的重组多肽可在细胞内、或在细胞膜上表达、或分泌到细胞外。如果需要,可利用其物理的、化学的和其它特性通过各种分离方法分离和纯化重组的蛋白。这些方法是本领域技术人员所熟知的。这些方法的例子包括但并不限于:常规的复性处理、用蛋白沉淀剂处理(盐析方法)、离心、渗透破菌、超处理、超离心、分子筛层析(凝胶过滤)、吸附层析、离子交换层析、高效液相层析(HPLC)和其它各种液相层析技术及这些方法的结合。
分子标志物
本发明中术语“分子标志物”是其在组织或细胞中的表达水平与正常或健康细胞或组织的表达水平相比发生改变的任何基因或蛋白。
本文包含用于检测分子标志物表达的现有技术中任何可用方法。本发明分子标志物的表达可在核酸水平上被检测(如,RNA转录物)或蛋白质水平。通过“检测表达”旨在确定RNA转录物或其分子标志物基因的表达产物的数量或存在。因此,“检测表达”包含一分子标志物被确定不能被表达、不能被检测表达,表达在低水平、表达在正常水平或过表达的实例。为了确定低表达,被检查的所述身体样本能够与相应的来自健康人的身体样本比较。那就是说,所述表达的“正常”水平是分子标志物的表达水平,例如在来自人类主体或未被骨关节炎折磨的病患的宫颈组织样本中的分子标志物表达水平。这个样本可以以标准化形式呈现。在一些实施例中,分子标志物过表达的确定需不比较身体样本和相应来自健康人的身体样本。
检测方法
本发明所述核酸扩增技术选自聚合酶链式反应(PCR)、逆转录聚合酶链式反应(RT-PCR)、转录介导的扩增(TMA)、连接酶链式反应(LCR)、链置换扩增(SDA)和基于核酸序列的扩增(NASBA)。其中,PCR需要在扩增前将RNA逆转录成DNA(RT-PCR),TMA和NASBA直接扩增RNA。
通常,PCR使用变性、引物对与相反链的退火以及引物延伸的多个循环,以指数方式增加靶核酸序列的拷贝数;RT-PCR则将逆转录酶(RT)用于从mRNA制备互补的DNA(cDNA),然后将cDNA通过PCR扩增以产生DNA的多个拷贝;TMA在基本上恒定的温度、离子强度和pH的条件下自身催化地合成靶核酸序列的多个拷贝,其中靶序列的多个RNA拷贝自身催化地生成另外的拷贝,TMA任选地包括使用阻断,部分、终止部分和其他修饰部分,以改善TMA过程的灵敏度和准确度;LCR使用与靶核酸的相邻区域杂交的两组互补DNA寡核苷酸。DNA寡核苷酸在热变性、杂交和连接的重复多个循环中通过DNA连接酶共价连接,以产生可检测的双链连接寡核苷酸产物;SDA使用以下步骤的多个循环:引物序列对与靶序列的相反链进行退火,在存在dNTPαS下进行引物延伸以产生双链半硫代磷酸化的(hemiphosphorothioated)引物延伸产物,半修饰的限制性内切酶识别位点进行的核酸内切酶介导的切刻,以及从切口3'端进行的聚合酶介导引的物延伸以置换现有链并产生供下一轮引物退火、切刻和链置换的链,从而引起产物的几何扩增。
探针
“探针”是指能够用于测量特定基因的表达情况的分子。示例性探针包括PCR引物以及基因特异性DNA寡核苷酸探针,例如固定于微阵列基底上的微阵列探针、定量核酸酶保护检验探针、与分子条形码连接的探针、以及固定于珠上的探针。
本发明中术语“探针”指能与另一分子的特定序列或亚序列或其它部分结合的分子。除非另有指出,“探针”通常指能通过互补碱基配对与另一多核苷酸(往往称为“靶多核苷酸”)结合的多核苷酸探针。根据杂交条件的严谨性,探针能和与该探针缺乏完全序列互补性的靶多核苷酸结合。探针可作直接或间接的标记,其范围包括引物。杂交方式,包括,但不限于:溶液相、固相、混合相或原位杂交测定法。
作为探针,可以使用荧光标记、放射标记、生物素标记等对癌检测用多核苷酸进行了标记的标记探针。多核苷酸的标记方法本身是公知的。可通过如下方法检查试样中是否存在受试核酸:固定受试核酸或者其扩增物,与标记探针进行杂交,洗涤,以及然后测定与固相结合的标记。备选地,还可固定癌检测用多核苷酸,使受试核酸与其杂交,然后应用标记探针等检测结合于固相上的受试核酸。在这种情况下,结合于固相上的癌检测用多核苷酸也称为探针。使用多核苷酸探针测定受试核酸的方法在本领域也是公知的。可以如下进行该方法:在缓冲液中使多核苷酸探针与受试核酸在Tm或者其附近(优选在±4℃以内)接触用于杂交,洗涤,然后测定杂交的标记探针或者与固相探针结合的模板核酸。
在作为探针使用的多核苷酸的大小优选为18个或更多个核苷酸、更优选为20个或更多个核苷酸,以及编码区域的全长或更少。作为引物使用时,该多核苷酸大小优选为18个或更多个核苷酸,以及50个或更少核苷酸。这些探针具有与靶点基因的特定的碱基序列互补的碱基序列。这里,所谓“互补”,只要是杂交即可,可以不是完全互补。这些多核苷酸通常相对于该特定的碱基序列具有80%以上、优选90%以上、更优选95%以上、特别优选100%的同源性。这些探针可以是DNA,也可以是RNA,另外,可以为在其一部分或全部中核苷酸通过PN、LNA、ENA、GNA、TNA等人工核酸置换得到的多核苷酸。
芯片
术语“芯片”也称为“阵列”,指包含连接的核酸或肽探针的固体支持物。阵列通常包含按照不同的已知位置连接至基底表面的多种不同的核酸或肽探针。这些阵列,也称为“微阵列”,通常可以利用机械合成方法或光引导合成方法来产生这些阵列,所述光引导合成方法合并了光刻方法和固相合成方法的组合。阵列可以包含平坦的表面,或者可以是珠子、凝胶、聚合物表面、诸如光纤的纤维、玻璃或任何其它合适的基底上的核酸或肽。可以以一定的方式来包装阵列,从而允许进行全功能装置的诊断或其它方式的操纵。
抗体
在本发明中,术语“抗体”是指选择性结合目标抗原的天然或合成抗体。该术语包括多克隆和单克隆抗体。除了完整的免疫球蛋白分子外,那些免疫球蛋白分子的片段或聚合物以及选择性结合目标抗原的免疫球蛋白分子的人类或人源化形式也包括在术语“抗体”的范围内,只要它们展现出期望的生物学活性即可。“单克隆抗体”指从一群基本上同质的抗体获得的抗体,即构成群体的各个抗体相同和/或结合相同表位,除了生产单克隆抗体的过程中可能产生的可能变体外,此类变体一般以极小量存在。此类单克隆抗体典型的包括包含结合靶物的多肽序列的抗体,其中靶物结合多肽序列是通过包括从众多多肽序列中选择单一靶物结合多肽序列在内的过程得到的。
单克隆抗体还包括“嵌合”抗体,其中重链和/或轻链的一部分与衍生自特定物种或属于特定抗体类别或亚类的抗体中的相应序列相同或同源,而链的剩余部分与衍生自另一物种或属于另一抗体类别或亚类的抗体中的相应序列相同或同源,以及此类抗体的片段,只要它们展现出期望的生物学活性即可。
多克隆抗体包含对产生人抗体的动物(例如,小鼠)免疫FGGY蛋白质而得的抗体。当制备了嵌合抗体或人源化抗体之后,可以将可变区(例如,FR)和/或恒定区中的氨基酸用其他氨基酸替换等。
药物组合物
本发明的药物组合物包括FGGY基因和/或其表达产物的下调剂,当在治疗上进行施用(给药)时,可抑制FGGY基因和/或蛋白的表达或活性,从而抑制骨关节炎。在本发明的具体实施方案中,所述下调剂包括抑制FGGY基因表达的物质、抑制FGGY基因表达产物稳定性的物质、和/或抑制FGGY基因表达产物活性的物质。
通常可将这些配置于无毒的、惰性的和药学上可接受的水性载体介质中,其中pH通常约为5-8,较佳的pH约为6-8,尽管pH值可随被配置物质的性质以及待治疗的病症而有所变化。配置好的药物组合物可以通过常规途径给药,其中包括但并不限于口服给药、非胃肠道给药、通过吸入喷雾给药、局部给药、直肠给药、鼻给药、颊给药、或通过植入的贮药装置给药。本发明中术语非胃肠道包括皮下、皮内、静脉内、肌内、关节内、动脉内、滑膜内、胸骨内、鞠内、损伤部位内、和颅内注射或输注技术。只要能达到目标组织即可。
本发明中的药物组合物,含有安全有效量的本发明FGGY蛋白或其下调剂以及药学上可接受的载体或赋形剂。这类载体包括(但不限于):盐水、缓冲液、葡萄糖、水、甘油、乙醇及其组合。药物制剂应与给药方式相匹配。本发明的药物组合物可以被制成针剂形式,例如用生理盐水或含有葡萄糖和其他辅剂的水溶液通过常规方法进行制备。诸如片剂和胶囊之类药物组合物,可以通过常规方法进行制备。药物组合物如针剂、溶液、片剂和胶囊宜在无菌条件下制备。活性成分的给药量是治疗的有效量。
本发明的药物组合物可以用于下调内源性的FGGY蛋白过多,通过降低FGGY蛋白的表达或减弱FGGY蛋白的功能,从而治疗因FGGY蛋白增加导致的骨关节炎。
本发明的药物还可与其他治疗骨关节炎的药物联用,其他治疗性化合物可以与主要的活性成分同时给药,甚至在同一组合物中同时给药。还可以以单独的组合物或与主要的活性成分不同的剂量形式单独给予其它治疗性化合物。主要成分的部分剂量可以与其它治疗性化合物同时给药,而其它剂量可以单独给药。在治疗过程中,可以根据症状的严重程度、复发的频率和治疗方案的生理应答,调整本发明药物组合物的剂量。
本发明中术语“治疗”是指以治愈、改善、稳定或预防疾病、病理状态或病症为目的对患者进行的医学管理。该术语包括积极疗法,即专门以改善疾病、病理状态或病症为目的的治疗,并且还包括病因治疗,即以除去相关疾病、病理状态或病症的病因为目的的治疗。此外,该术语还包括姑息治疗,即设计用于缓解症状而非治愈疾病、病理状态或病症的治疗;预防性治疗,即以最大程度降低或者部分或完全抑制相关疾病、病理状态或病症的发展为目的的治疗;以及支持性治疗,即用于补充另一种以改善相关疾病、病理状态或病症为目的的特定疗法的治疗。
本发明中术语“样本”包括任何细胞、组织或体液取样,其中包括但不限于,组织或细胞样本的来源可以来自新鲜、冷冻和/或保存的器官或组织样本的固体组织,或者活组织检查或者抽吸物,血液或任何血液成分;体液如脑脊髓液、羊水、腹腔液或间质液。组织样本可以是初级或体外培养的细胞或细胞株。可选地,组织或细胞样本从疾病组织/器官获取。组织样本可能包含所述组织自然混合的化合物,诸如防腐剂、抗凝血剂、缓冲剂、固定剂、营养剂、抗生素、或类似化合物。
下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,例如Sambrook等人,分子克隆:实验室手册(New York:Cold Spring HarborLaboratory Press,1989)中所述的条件,或按照制造厂商所建议的条件。
实施例1筛选与骨关节炎相关的基因标志物
1、样品收集
各收集6例周围正常滑膜组织和骨关节炎滑膜组织,均经病理学诊断证实,所有患者术前未接受任何形式的治疗。手术切下的样本于液氮中冻存,患者均知情同意,上述所有标本的取得均通过组织伦理委员会的同意。
2、RNA样品的制备
取出冻存于液氮中的组织样本,把组织样本放入已预冷的研钵中进行研磨,按照试剂盒中的说明书提取分离RNA。具体如下:
1)将1ml TRIzol在超净台里加入至玻璃匀浆瓶中(提前将匀浆瓶用烘箱180℃烘4个小时),将匀浆瓶按到仪器上,称取50-100mg的组织放入玻璃匀浆瓶内,将转速调至1500转左右,开始在冰水浴中进行匀浆,每研磨30s,停止30s,反复3-4次。样品体积不应超过TRIzol体积10%。
2)将加入TRIzol的样品在室温(15-30℃)放置10min,使核酸蛋白复合物完全分离。
3)1ml TRIzol加入200μl氯仿,剧烈振荡2min,每隔1min晃动一次,5-6次后,再静止7min。
4)4℃,12000rpm,离心15min。样品分为三层:底层为黄色有机相,上层为无色水相和一个中间层。RNA主要在水相中,水相体积约为所用TRIzol的60%。
5)重复步骤3)和4)。
6)把上层水相转移到新的EP管中(尽量不要吸取到中间层以免污染)。加入500μl异丙醇,室温放置10min。
7)4℃,12000rpm,离心15min,离心后在管底出现白色沉淀。用移液器小心移去上清。
8)加入1ml 75%冷乙醇,震荡洗涤沉淀。4℃,7500rpm,离心5min,小心弃掉上清。
9)重复步骤8)。
10)将EP管倒扣于滤纸上吸去多余的水分,并用10μl枪头小心吸取管内的液体(枪头不要接触RNA),将EP管室温放置5min。
11)加入40μl无RNase的水(DEPC水),将提取的RNA稀释5倍后,用Nanodrop检测OD值与浓度,在管上做好标记;置于-80℃冰箱保存。
3、高通量转录组测序
3.1 RNA-seq读段定位
首先将低质量的读段去除得到清洁读段,然后利用TopHat v1.3.1将清洁片段与UCSC H.sapiens参考基因组(hg19)进行匹配,H.sapiens UCSC hg19版的预先构建的索引从TopHat主页下载,并作为参考基因组,利用TopHat与基因组匹配时,允许每个读段(默认到20)有多个匹配位点,最多2次错配。TopHat根据外显子区域和GT-AG剪切信号建立可能的剪切位点库,根据这些剪切位点库将没有定位到基因组的读段定位到基因组上。我们使用TopHat方法的系统默认参数。
3.2转录丰度评估
匹配上的读段文件通过Cufflinks v1.0.3处理,Cufflinks v1.0.3将RNA-seq片段数目进行标准化计算转录本的相对丰度。FPKM值指的是每一百万测序片段中匹配到特定基因1kb长的外显子区域的片段数目。通过贝叶斯推理方法计算FPKM估计值的置信区间。Cufflinks使用的参考的GTF注释文件从Ensembl数据库下载(Homo_sapiens.GRCh37.63.gtf)。
3.3差异表达基因的检测
将下载的Ensembl GTF文件和通过TopHat匹配的原始文件传输到Cuffdiff,Cuffdiff使用原始的匹配文件重新估算GTF文件中列出的转录本的表达丰度,检测差异表达。在Cuffidff输出中只有q值<0.01,测试显示成功的比较才被认为是差异表达。
4、结果
RNA-seq结果显示,FGGY基因在骨关节炎患者中的表达量显著高于正常人的表达量。
实施例2 QPCR测序验证FGGY基因的差异表达
1、对FGGY基因差异表达进行大样本QPCR验证。按照实施例1中的样本收集方式选择正常滑膜组织和骨关节炎滑膜组织各80例。
2、RNA提取步骤如实施例1所述。
3、逆转录:(采用FastQuant cDNA第一链合成试剂盒(货号:KR106)进行mRNA反转录)
首先去除基因组DNA反应,在试管中加入5×gDNA Buffer 2.0μl,TotalRNA 1μg,加Rnase Free ddH2O使总体积至10μl,水浴锅中42℃加热3min,再将10×Fast RT Buffer 2.0μl,RT Enzyme Mix 1.0μl,FQ-RT Primer Mix 2.0μl,RNase Free ddH2O 5.0μl,混合后加入上述试管中一起混合共20μl,水浴锅中42℃加热15min,95℃加热3min,合成的cDNA需要长期保存时,请于-20℃或更低温度保存。
3)聚合酶链式反应
用SuperReal PreMix Plus(SYBR Green)(货号:FP205),进行扩增,实验操作按产品说明书进行。
1)引物设计
根据Genebank中FGGY基因和GAPDH基因的编码序列设计QPCR扩增引物,由博迈德生物公司合成。具体引物序列如下:
FGGY基因:
正向引物为5’-GGACATATTCAGCAGAGA-3’(SEQ ID NO.3);
反向引物为5’-AGCACTTGGTTTCCTATT-3’(SEQ ID NO.4)。
管家基因GAPDH的引物序列为:
正向引物:5’-GGAGCGAGATCCCTCCAAAAT-3’(SEQ ID NO.5)
反向引物:5’-GGCTGTTGTCATACTTCTCATGG-3’(SEQ ID NO.6)
2)按照表1配制20μl PCR反应体系:
表1 PCR反应体系
3)PCR反应条件::95°15min,(95℃10s,55℃30s,72℃32s)×40个循环,95℃15s,60℃60s,95℃15s。以SYBR Green作为荧光标记物,在Light Cycler荧光定量PCR仪上进行PCR反应,通过融解曲线分析和电泳确定目的条带,ΔΔCT法进行相对定量,每个样进行3次重复实验。
5、统计学方法
以GAPDH为内参,计算骨关节炎滑膜组织与正常滑膜组织荧光定量RT-PCR的实验结果,采用SPSS18.0统计软件来进行统计分析,两者之间的差异采用t检验,以P<0.05具有统计学差异。
6、结果
如图2所示,与对照组相比,FGGY基因在骨关节炎组织中表达显著上调,差异具有统计学意义(P<0.05),同RNA-sep结果一致。
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
SEQUENCE LISTING
<110> 天津市天津医院
<120> 分子标志物在骨关节炎中的应用
<160> 6
<170> PatentIn version 3.5
<210> 1
<211> 1728
<212> DNA
<213> 人源
<400> 1
atgtctggtg gagaacagaa accagagagg tactatgtgg gtgtggacgt tggaacaggc 60
agtgtccgtg cagctctggt ggaccagagt ggggtcctgt tggcttttgc agaccagcca 120
attaagaatt gggagcccca gttcaaccac catgagcagt cctccgagga catctgggct 180
gcgtgctgtg ttgtcacaaa gaaagttgta caagggattg atttaaacca aattcgagga 240
cttgggtttg atgccacgtg ttctctggtt gttttggata agcagtttca cccattacca 300
gtcaaccagg aaggggattc ccatcgaaac gtcatcatgt ggctggacca tcgagcagtc 360
agtcaagtta acaggatcaa tgagaccaag cacagtgtcc tccagtacgt cgggggggtg 420
atgtctgtgg aaatgcaggc cccgaaactt ctgtggctga aagagaactt gagagagatt 480
tgctgggata aggcgggaca tttctttgat ctcccggact tcttatcgtg gaaggcaaca 540
ggtgtcacag cacggtctct ctgctccctg gtgtgtaagt ggacatattc agcagagaaa 600
ggctgggacg acagtttctg gaaaatgatt ggtttggaag actttgttgc agataattac 660
agcaaaatag gaaaccaagt gctacctcct ggagcttctc ttggaaatgg gctcacacca 720
gaggcagcaa gagaccttgg ccttctccct gggattgcgg tcgcagcttc actcattgat 780
gcccatgcag gaggactagg agtgattggg gcagatgtga gagggcacgg cctcatctgt 840
gaggggcagc cagtgacgtc acggctggct gtcatctgtg gaacgtcttc ttgtcacatg 900
gggatcagca aagacccgat ttttgtacca ggcgtctggg ggccttattt ctcagccatg 960
gtacctgggt tctggctgaa tgaaggtggt cagagcgtta ctggaaaatt gatagaccac 1020
atggtacaag gccatgctgc ttttccagaa ctacaagtaa aggccacagc cagatgccag 1080
agtatatatg catatttgaa cagtcacctg gatctgatta agaaggctca gcctgtgggt 1140
ttccttactg ttgatttaca tgtttggcca gatttccatg gcaaccggtc tcccttagca 1200
gatctgacac taaagggcat gagaaccact ggatatctgt atattccggc tttggcagcg 1260
ttgcactctc ccagttctct actctcccct caggtcaccg gattgaaact gtctcaggac 1320
cttgatgatc ttgccattct ctacctggcc acagttcaag ccattgcttt ggggactcgc 1380
ttcattatag aagccatgga ggcagcaggg cactcaatca gtactctttt cctatgtgga 1440
ggcctcagca agaatcccct ttttgtgcaa atgcatgcgg acattactgg catgcctgtg 1500
gtcctgtcgc aagaggtgga gtccgttctt gtgggtgctg ctgttctggg tgcctgtgcc 1560
tcaggggatt tcgcttctgt acaggaagca atggcaaaaa tgagcaaagt tgggaaagtt 1620
gtgttcccga gactacagga taaaaaatac tatgataaga aataccaagt attcctgaag 1680
ctggttgaac accagaagga gtatttggcg atcatgaatg atgactga 1728
<210> 2
<211> 575
<212> PRT
<213> 人源
<400> 2
Met Ser Gly Gly Glu Gln Lys Pro Glu Arg Tyr Tyr Val Gly Val Asp
1 5 10 15
Val Gly Thr Gly Ser Val Arg Ala Ala Leu Val Asp Gln Ser Gly Val
20 25 30
Leu Leu Ala Phe Ala Asp Gln Pro Ile Lys Asn Trp Glu Pro Gln Phe
35 40 45
Asn His His Glu Gln Ser Ser Glu Asp Ile Trp Ala Ala Cys Cys Val
50 55 60
Val Thr Lys Lys Val Val Gln Gly Ile Asp Leu Asn Gln Ile Arg Gly
65 70 75 80
Leu Gly Phe Asp Ala Thr Cys Ser Leu Val Val Leu Asp Lys Gln Phe
85 90 95
His Pro Leu Pro Val Asn Gln Glu Gly Asp Ser His Arg Asn Val Ile
100 105 110
Met Trp Leu Asp His Arg Ala Val Ser Gln Val Asn Arg Ile Asn Glu
115 120 125
Thr Lys His Ser Val Leu Gln Tyr Val Gly Gly Val Met Ser Val Glu
130 135 140
Met Gln Ala Pro Lys Leu Leu Trp Leu Lys Glu Asn Leu Arg Glu Ile
145 150 155 160
Cys Trp Asp Lys Ala Gly His Phe Phe Asp Leu Pro Asp Phe Leu Ser
165 170 175
Trp Lys Ala Thr Gly Val Thr Ala Arg Ser Leu Cys Ser Leu Val Cys
180 185 190
Lys Trp Thr Tyr Ser Ala Glu Lys Gly Trp Asp Asp Ser Phe Trp Lys
195 200 205
Met Ile Gly Leu Glu Asp Phe Val Ala Asp Asn Tyr Ser Lys Ile Gly
210 215 220
Asn Gln Val Leu Pro Pro Gly Ala Ser Leu Gly Asn Gly Leu Thr Pro
225 230 235 240
Glu Ala Ala Arg Asp Leu Gly Leu Leu Pro Gly Ile Ala Val Ala Ala
245 250 255
Ser Leu Ile Asp Ala His Ala Gly Gly Leu Gly Val Ile Gly Ala Asp
260 265 270
Val Arg Gly His Gly Leu Ile Cys Glu Gly Gln Pro Val Thr Ser Arg
275 280 285
Leu Ala Val Ile Cys Gly Thr Ser Ser Cys His Met Gly Ile Ser Lys
290 295 300
Asp Pro Ile Phe Val Pro Gly Val Trp Gly Pro Tyr Phe Ser Ala Met
305 310 315 320
Val Pro Gly Phe Trp Leu Asn Glu Gly Gly Gln Ser Val Thr Gly Lys
325 330 335
Leu Ile Asp His Met Val Gln Gly His Ala Ala Phe Pro Glu Leu Gln
340 345 350
Val Lys Ala Thr Ala Arg Cys Gln Ser Ile Tyr Ala Tyr Leu Asn Ser
355 360 365
His Leu Asp Leu Ile Lys Lys Ala Gln Pro Val Gly Phe Leu Thr Val
370 375 380
Asp Leu His Val Trp Pro Asp Phe His Gly Asn Arg Ser Pro Leu Ala
385 390 395 400
Asp Leu Thr Leu Lys Gly Met Arg Thr Thr Gly Tyr Leu Tyr Ile Pro
405 410 415
Ala Leu Ala Ala Leu His Ser Pro Ser Ser Leu Leu Ser Pro Gln Val
420 425 430
Thr Gly Leu Lys Leu Ser Gln Asp Leu Asp Asp Leu Ala Ile Leu Tyr
435 440 445
Leu Ala Thr Val Gln Ala Ile Ala Leu Gly Thr Arg Phe Ile Ile Glu
450 455 460
Ala Met Glu Ala Ala Gly His Ser Ile Ser Thr Leu Phe Leu Cys Gly
465 470 475 480
Gly Leu Ser Lys Asn Pro Leu Phe Val Gln Met His Ala Asp Ile Thr
485 490 495
Gly Met Pro Val Val Leu Ser Gln Glu Val Glu Ser Val Leu Val Gly
500 505 510
Ala Ala Val Leu Gly Ala Cys Ala Ser Gly Asp Phe Ala Ser Val Gln
515 520 525
Glu Ala Met Ala Lys Met Ser Lys Val Gly Lys Val Val Phe Pro Arg
530 535 540
Leu Gln Asp Lys Lys Tyr Tyr Asp Lys Lys Tyr Gln Val Phe Leu Lys
545 550 555 560
Leu Val Glu His Gln Lys Glu Tyr Leu Ala Ile Met Asn Asp Asp
565 570 575
<210> 3
<211> 18
<212> DNA
<213> 人工序列
<400> 3
ggacatattc agcagaga 18
<210> 4
<211> 18
<212> DNA
<213> 人工序列
<400> 4
agcacttggt ttcctatt 18
<210> 5
<211> 21
<212> DNA
<213> 人工序列
<400> 5
ggagcgagat ccctccaaaa t 21
<210> 6
<211> 23
<212> DNA
<213> 人工序列
<400> 6
ggctgttgtc atacttctca tgg 23
- 还没有人留言评论。精彩留言会获得点赞!