SKIL作为诊断冠心病的分子标志物的制作方法
本发明涉及冠心病诊断领域,更具体地,本发明涉及以检测skil异常为手段的冠心病诊断方法。
背景技术:
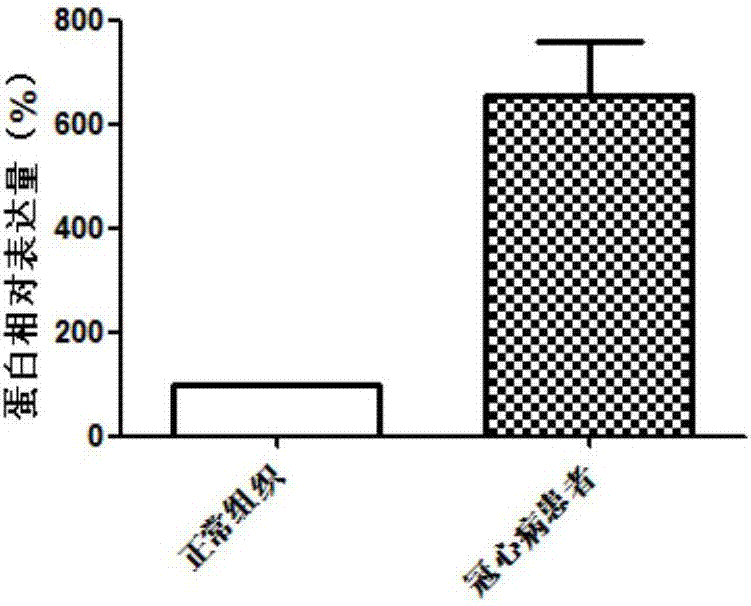
:随着经济和社会的发展,心血管疾病尤其是冠状动脉粥样硬化性心脏病(冠心病;coronaryarterydisease;cad)的发病率正在逐年上升。对于发达国家,还有大多数的发展中国家来讲,cad已经成为成年人发病和死亡的主要原因。近年来,对于cad的流行趋势以及越来越严峻的不良预后的现状,各国卫生组织均给予了高度的关注。在中国,由于改革开放,物质生活条件的提高,人均寿命逐渐延长,相应的,心血管疾病尤其是冠心病的发病率逐年升高,有人预计,到本世纪的20年代,冠心病有可能会成为威胁人类健康的首位疾病。近年来对冠心病的诊断方法和治疗措施有了重大的突破,尤其是近年来抗血小板药物、抗凝药物、溶栓药物的更新换代,以及经皮冠状动脉介入治疗(pci)措施的日益普及,使大多数的冠心病患者的临床结局发生了巨大改善。但是,目前冠心病的病因学研究以及对其发病机制的研究尚待提高和突破。技术实现要素:本发明的目的之一在于提供一种通过检测skil基因或蛋白表达差异来诊断冠心病的方法。为了实现上述目的,本发明采用了如下技术方案:本发明提供了检测skil基因或skil蛋白的产品在制备冠心病诊断工具中的用途。进一步,所述检测skil基因或skil蛋白的产品包括检测skil基因或skil蛋白的表达水平的产品。所述产品包括能够结合skil基因的核酸或者能够结合skil蛋白的物质(例如抗体)。所述核酸能够检测skil基因的表达水平;所述物质能够检测skil蛋白的表达水平。本发明的检测skil基因的产品可基于使用核酸分子的已知方法来发挥其功能:如pcr、如southern杂交、northern杂交、点杂交、荧光原位杂交(fish)、dna微阵列、aso法、高通量测序平台等。使用该产品可以定性地、定量地、或半定量地实施分析。包含在上述产品中的核酸可以通过化学合成来获得,或通过从生物材料制备含有期望核酸的基因,然后使用设计用于扩增期望核酸的引物扩增它来获得。进一步,所述pcr方法为已知方法,例如,arms(amplificationrefractorymutationsystem,扩增不应突变系统)法、rt-pcr(逆转录酶-pcr)法、嵌套pcr法等等。扩增的核酸可以通过使用点印迹杂交法、表面等离子共振法(spr法)、pcr-rflp法、原位rt-pcr法、pcr-sso(序列特异性寡核苷酸)法、pcr-ssp法、ampflp(可扩增片段长度多态性)法、mvr-pcr法、和pcr-sscp(单链构象多态性)法来检测。上面所述的核酸包括扩增skil基因的引物,产品中包括的引物可以通过通过化学合成来制备,通过使用本领域技术人员知道的方法参考已知信息来适当地设计,并通过化学合成来制备。在本发明的具体实施方案中,所述核酸为qpcr实验中使用的扩增引物,所述引物的序列如seqidno.1(正向序列)和seqidno.2(反向序列)所示。上面所述的核酸还可包括探针,所述探针可以通过化学合成来制备,通过使用本领域技术人员知道的方法参考已知信息来恰当设计,并通过化学合成来制备,或者可以通过从生物材料制备含有期望核酸序列的基因,并使用设计用于扩增期望核酸序列的引物扩增它来制备。本发明的检测skil蛋白的产品可基于使用抗体的已知方法来发挥其功能:例如,可以包括elisa、放射免疫测定法、免疫组织化学法、western印迹等。本发明的检测skil蛋白的产品包括特异性结合skil蛋白的抗体或其片段。可以使用任何结构、尺寸、免疫球蛋白类别、起源等的抗体或其片段,只要它结合靶蛋白质即可。本发明的检测产品中包括的抗体或其片段可以是单克隆的或多克隆的。抗体片段指保留抗体对抗原的结合活性的抗体一部分(部分片段)或含有抗体一部分的肽。抗体片段可以包括f(ab′)2、fab′、fab、单链fv(scfv)、二硫化物键合的fv(dsfv)或其聚合物、二聚化v区(双抗体)、或含有cdr的肽。本发明的检测skil蛋白的产品可以包括编码抗体或编码抗体片段的氨基酸序列的分离的核酸,包含该核酸的载体,和携带该载体的细胞。抗体可以通过本领域技术人员公知的方法来获得。例如,制备保留整个或部分靶蛋白质的多肽或整合编码它们的多核苷酸的哺乳动物细胞表达载体作为抗原。使用抗原免疫动物后,从经过免疫的动物获得免疫细胞并融合骨髓瘤细胞以获得杂交瘤。然后从杂交瘤培养物收集抗体。最后可以通过使用被用作抗原的skil蛋白或其部分对获得的抗体实施抗原特异性纯化来获得针对skil蛋白的单克隆抗体。可以如下制备多克隆抗体:用与上文相同的抗原免疫动物,从经过免疫的动物收集血液样品,从血液中分离出血清,然后使用上述抗原对血清实施抗原特异性纯化。可以通过用酶处理获得的抗体或通过使用获得的抗体的序列信息来获得抗体片段。标记物与抗体或其片段的结合可以通过本领域普遍知道的方法来实施。例如,可以如下荧光标记蛋白质或肽:用磷酸盐缓冲液清洗蛋白质或肽,添加用dmso、缓冲剂、等准备的染料,然后混合溶液,再于室温放置10分钟。另外,标记可使用商品化的标记试剂盒,诸如生物素标记试剂盒,如生物素标记试剂盒-nh2、生物素标记试剂盒-sh(dojindolaboratories);碱性磷酸酶标记试剂盒诸如碱性磷酸酶标记试剂盒-nh2、碱性磷酸酶标记试剂盒-sh(dojindolaboratories);过氧化物酶标记试剂盒诸如过氧化物酶标记试剂盒-nh2、过氧化物酶标记试剂盒-nh2(dojindolaboratories);藻胆蛋白标记试剂盒诸如藻胆蛋白标记试剂盒-nh2、藻胆蛋白标记试剂盒-sh、b-藻红蛋白标记试剂盒-nh2,b-藻红蛋白标记试剂盒-sh、r-藻红蛋白标记试剂盒-nh2、r-藻红蛋白标记试剂盒sh(dojindolaboratories);荧光标记试剂盒诸如荧光素标记试剂盒-nh2、hilytefluor(tm)555标记试剂盒-nh2、hilytefluor(tm)647标记试剂盒-nh2(dojindolaboratories);及dylight547和dylight647(technochemicalcorp.)、zenon(tm)、alexafluor(tm)抗体标记试剂盒、qdot(tm)抗体标记试剂盒(invitrogencorporation)和ez-标记物蛋白质标记试剂盒(funakoshicorporation)。为了正确标记,可以使用适宜的仪器来检测经过标记的抗体或其片段。进一步,所述检测skil基因或skil蛋白的产品可以是检测skil基因或skil蛋白的试剂、也可以是包含所述试剂的试剂盒、芯片、试纸等,也可以是使用所述试剂的高通量测序平台。利用前面所述的检测产品检测受试者样本中的skil基因或skil蛋白的表达水平,与正常人相比,受试者样本中的skil基因或skil蛋白的表达水平升高,则诊断该受试者为冠心病患者。作为依照本发明的检测产品的样本,可以使用例如自活检受试者获得的组织样品或流体。样本不受特别限制,只要它适于本发明的测定;例如,它可以包括组织、血液、血浆、血清、淋巴液、尿液、浆膜腔液、脊髓液、滑液、房水、泪液、唾液、或其级分或经过处理的材料。在本发明的具体实施方案中,所述样本来自受试者的血液。本发明还提供了一种诊断冠心病的工具,所述工具能够检测受试者样本中skil基因或skil蛋白的表达水平。所述工具包括能够结合skil基因的核酸或者能够结合skil蛋白的物质(例如抗体)。所述核酸能够检测skil基因的表达水平;所述物质能够检测skil蛋白的表达水平。进一步,所述核酸和所述物质的性质同前面所述。进一步,所述诊断冠心病的工具包括但不限于芯片、试剂盒、试纸、或高通量测序平台;高通量测序平台是一种特殊的诊断冠心病的工具,随着高通量测序技术的发展,对一个人的基因表达谱的构建将成为十分便捷的工作。通过对比疾病患者和正常人群的基因表达谱,容易分析出哪个基因的异常与疾病相关。因此,在高通量测序中获知skil基因的异常与冠心病相关也属于skil基因的用途,同样在本发明的保护范围之内。本发明的检测产品、诊断工具中使用的抗skil抗体或其片段所识别的氨基酸的数目没有特别限制,只要抗体能够结合skil即可。当抗体作为治疗药物时,优选的是它能够识别尽可能多的氨基酸,只要它能抑制skil功能。抗体或其片段识别的氨基酸的数目是至少一个,更优选至少三个。抗体的免疫球蛋白类别不受限制,可以是igg、igm、iga、ige、igd或igy。本发明的检测产品、诊断工具中使用的抗skil抗体的其他性质同前面所述。进一步,所述受试者样本可以使用例如自活检受试者获得的组织样品或流体。样本不受特别限制,只要它适于本发明的测定;例如,它可以包括组织、血液、血浆、血清、淋巴液、尿液、浆膜腔液、脊髓液、滑液、房水、泪液、唾液、或其级分或经过处理的材料。在本发明的具体实施方案中,所述样本来自受试者的血液。本发明还提供了一种诊断冠心病的方法,所述方法包括如下步骤:(1)获取冠心病受试者的样品;(2)检测受试者样品中skil基因或蛋白的表达水平;(3)将测得的skil基因或蛋白的表达水平与受试者的患病与否关联起来。(4)与对照相比,skil基因或蛋白的表达水平升高,则该受试者被诊断为冠心病。在本发明的上下文中,“诊断冠心病”既包括判断受试者是否已经患有冠心病、也包括判断受试者是否存在患有冠心病的风险。本发明的优点和有益效果:本发明的发现了一种诊断冠心病的分子标志物,使用该分子标志物可以在冠心病发生的早期即可作为判断,提供了患者的生存率。附图说明图1显示利用qpcr检测skil基因在冠心病患者与正常人中的表达情况;图2显示利用westernblot检测skil蛋白在冠心病患者与正常人中的表达情况。具体的实施方式下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。实施例1skil基因的差异表达1、研究对象:收集冠心病患者6例,正常人6例。冠心病组的纳入标准:按照世界卫生组织制定的缺血性心脏病的诊断标准,选择经冠状动脉造影证实有一支或多支血管狭窄程度≥50%的冠心病患者。对照组的入选标准为:1)在流行病学调查时筛选年龄、性别、民族均与cad组相匹配,经过问卷调查、体格检查、心脏超声检查及心电图检查及相关实验室检查没有冠心病的临床表现及主要危险因素的体检者;2)住院行健康体检并行冠状动脉造影检查排除冠心病并年龄、性别、民族与cad组匹配者;符合以上任何一条者入选为对照组。两组在纳入研究前签署知情同意书。剔除标准:cad组-临床资料不全者及同时合并以下疾病之一者予以剔除。(如:先天性心脏病者、主动脉夹层、多脏器功能衰竭、风湿性心脏病以及具有精神障碍不能配合者)。对照组:有精神障碍者或经多普勒检查证实有颈动脉斑块或狭窄者,予以剔除。2、血液中总rna的提取使用百泰克血液rna提取试剂盒进行血液总rna的提取(1)取全血250μl(或0.25g)至rnase-free过滤柱中,13000rpm离心2分钟,收集下液,加入0.75ml裂解液rls。(2)将匀浆样品剧烈震荡混匀,在15-30℃条件下孵育5分钟以使核蛋白体完全分解。(3)可选步骤:4℃的条件下12,000rpm离心10分钟,小心取上清转入一个新的无rna酶的离心管中。(4)每1mlrls加0.2ml氯仿。盖紧样品管盖,剧烈振荡15秒并将其在室温下孵育3分钟。(5)于4℃12,000rpm离心10分钟,样品会分成三层:下层有机相,中间层和上层无色的水相,rna存在于水相中。水相层的容量大约为所加rls体积的60%,把水相转移到新管中,进行下一步操作。(6)加入1倍体积70%乙醇,颠倒混匀(此时可能会出现沉淀),得到的溶液和可能沉淀一起转入吸附柱ra中(吸附柱套在收集管内)。(7)10,000rpm离心45秒,弃掉废液,将吸附柱重新套回收集管。(8)加500μl去蛋白液re,12,000rpm离心45秒,弃掉废液。(9)加入700μl漂洗液rw,12,000rpm离心60秒,弃掉废液。(10)加入500μl漂洗液rw,12,000rpm离心60秒,弃掉废液。(11)将吸附柱ra放回空收集管中,12,000rpm离心2分钟,尽量除去漂洗液,以免漂洗液中残留乙醇抑制下游反应。(12)取出吸附柱ra,放入一个无rna酶的离心管中,根据预期rna产量在吸附膜的中间部位加50-80μl无rna酶的水,室温放置2分钟,12,000rpm离心1分钟,收集洗脱液。3、rna样品的质量分析(nanodrop1000分光光度计)nanodrop1000分光光度计检测rna样品,rna-seq测序的样品要求:od260/od280为1.8-2.2。4、rna样品的完整性分析(agilenttechnologies2100bioanalyzer)agilenttechnologies2100bioanalyzer检测rna样品,观察28srrna和18srrna主带明显、无降解、rna完整性指数合格、浓度达到要求的符合rna-seq测序cdna文库构建的要求,可以用于文库构建及测序。5、高通量转录组测序(1)rna-seq读段定位首先将低质量的读段去除得到清洁读段,然后利用tophatv1.3.1将清洁片段与ucsch.sapiens参考基因组(hg19)进行匹配,h.sapiensucschg19版的预先构建的索引从tophat主页下载,并作为参考基因组,利用tophat与基因组匹配时,允许每个读段(默认到20)有多个匹配位点,最多2次错配。tophat根据外显子区域和gt-ag剪切信号建立可能的剪切位点库,根据这些剪切位点库将没有定位到基因组的读段定位到基因组上。我们使用tophat方法的系统默认参数。(2)转录丰度评估匹配上的读段文件通过cufflinksv1.0.3处理,cufflinksv1.0.3将rna-seq片段数目进行标准化计算转录本的相对丰度。fpkm值指的是每一百万测序片段中匹配到特定基因1kb长的外显子区域的片段数目。通过贝叶斯推理方法计算fpkm估计值的置信区间。cufflinks使用的参考的gtf注释文件从ensembl数据库下载(homo_sapiens.grch37.63.gtf)。(3)差异表达基因的检测将下载的ensemblgtf文件和通过tophat匹配的原始文件传输到cuffdiff,cuffdiff使用原始的匹配文件重新估算gtf文件中列出的转录本的表达丰度,检测差异表达。在cuffidff输出中只有q值<0.01,测试显示成功的比较才被认为是差异表达。6、结果rna-seq结果显示,与正常人相比,冠心病人血液中存在596个差异表达基因。实施例2qpcr实验验证冠心病患者和正常人中差异表达的基因1、研究对象:筛选标准同实施例1,冠心病患者和正常人各45例。2、血液中总rna的提取步骤同实施例1。3、逆转录用逆转录缓冲液对lμg总rna进行逆转录合成cdna。采用25μl反应体系,每个样品取1μg总rna作为模板rna,在pcr管中分别加入以下组分:depc水,5×逆转录缓冲液,10mmol/ldntp,0.1mmol/ldtt,30μmmol/loligodt,200u/μlm-mlv,模板rna。42℃孵育1h,72℃10min,短暂离心。4、qpcr(1)引物设计根据genbank中skil基因和gapdh基因的编码序列设计qpcr扩增引物,由上海生工生物工程技术服务有限公司合成。具体引物序列如下:skil基因:正向引物为5’-ttcatctccgcttcttgt-3’(seqidno.1);反向引物为5’-tgttcttcagtgagttcct-3’(seqidno.2),gapdh基因:正向引物为5’-gaaggtgaaggtcggagt-3’(seqidno.3);反向引物为5’-catgggtggaatcatattggaa-3’(seqidno.4)。(2)按照表1配制pcr反应体系:其中,sybrgreen聚合酶链式反应体系购自invitrogen公司。表1pcr反应体系试剂体积正向引物1μl反向引物1μlsybrgreen聚合酶链式反应体系12.5μl模板2μl去离子水补足25μl(3)pcr反应条件:95℃5min,(95℃15s,60℃40s)*42个循环。以sybrgreen作为荧光标记物,在lightcycler荧光定量pcr仪上进行pcr反应,通过融解曲线分析和电泳确定目的条带,δδct法进行相对定量。5、统计学方法结果数据都是以平均值±标准差的方式来表示,采用spss13.0统计软件来进行统计分析的,两者之间的差异采用t检验,认为当p<0.05时具有统计学意义。6、结果结果如图1所示,与正常人相比,冠心病患者血液中skil基因的mrna水平显著增加,差异具有统计学意义(p<0.05)。实施例3skil蛋白差异表达检测1、研究对象同实施例2。2、单核细胞分离无菌采集静脉血10ml,注入盛肝素的无菌小瓶中,加盖后立即轻轻摇匀。用无菌吸管加入等体积的hbss(nacl8.0g,na2hpo40.132g,kh2po40.06g,kcl0.4g,酚红1ml,nahco30.35g,d-葡萄糖1.0g,溶于1000ml双蒸水),以降低红细胞的凝聚。吸取8ml淋巴细胞分层液置50ml离心管中,将稀释血液沿管壁缓慢加入,保持界面清楚,勿使两者相混,在20℃2000r/min离心30min,小心吸取分层液与血浆交接部位混浊的灰白色层,即淋巴细胞层,加入另一支离心管中,用5倍体积的hbss洗涤2次,依次以2000r/min、1500r/min在室温下离心10min,以便去除大部分混杂的血小板,用10ml双蒸水与细胞团块混合1min,使残余红细胞裂解,然后迅速加入等量1.8%nacl溶液,2000r/min离心,去上清,经细胞计数后用hbss溶液调整细胞至1×106个/ml备用。3、单核细胞总蛋白质提取将上述实验所得细胞悬液(浓度为1×106个/ml)室温1000r/min离心10min,弃上清后加入100μl裂解缓冲液,4℃震荡1h,用超声波仪破碎细胞,每次10s,共10次,于4℃12000r/min离心1h;取上清用brandford法定量蛋白,分装成2.5μg/μl,-80℃冰箱保存备用。4、westernblot检测将提取的蛋白进行sds-page电泳,之后进行转膜、封闭、一抗孵育、二抗孵育、显色。5、统计学处理将蛋白条带的灰度值使用imagej软件进行分析,以β-actin为内参,将目的白条带的灰度值进行归一化处理。结果数据都是以平均值±标准差的方式来表示,采用spss13.0统计软件来进行统计分析的,两者之间的差异采用t检验,认为当p<0.05时具有统计学意义。6、结果结果如图2所示,与正常人相比,冠心病患者血液中skil蛋白含量高,差异具有统计学意义(p<0.05)。上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。sequencelisting<110>程琦<120>skil作为诊断冠心病的分子标志物<160>4<170>patentinversion3.5<210>1<211>18<212>dna<213>人工序列<400>1ttcatctccgcttcttgt18<210>2<211>19<212>dna<213>人工序列<400>2tgttcttcagtgagttcct19<210>3<211>18<212>dna<213>人工序列<400>3gaaggtgaaggtcggagt18<210>4<211>22<212>dna<213>人工序列<400>4catgggtggaatcatattggaa22当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1