一种检测肿瘤标志物的方法与流程
本发明涉及一种基于纳米金粒子和核酸结构的相互作用的新型纳米探针,以及在此基础上建立的肿瘤标志物的快速荧光检测方法。
背景技术:
dna在自然界中主要以双螺旋形式存在,然而,随着体外快速筛选技术的建立,人们可以获得数量众多的新的核酸结构如核酸适体、dna酶、rna酶。核酸适体是一类对于配体具有高亲和力的dna或rna,而dna酶/rna酶则是如蛋白酶一类具有酶催化活性的结构。这些体外筛选技术作为分子工具在生物技术领域中变得越来越重要。例如,他们在生物传感器的设计中起着重要作用,而且应用于生物学、环境、安全等领域的检测,包括蛋白质(凝血酶、生长因子、hiv相关多肽等)、有机小分子(camp、atp、cocaine等)和金属离子(k+、hg2+、pb2+等)、其他新的令人兴奋的应用包括基于核酸适体的蛋白质芯片,并在蛋白质组学中用于高通量成像、以及基于dna酶和rna酶的分子尺度的逻辑门dna分子计算机。
我们尤其对发展基于核酸结构的分子传感器保有浓厚的兴趣,因为核酸结构具有几种优势,首先,任何靶物质在理论上都可以通过selex技术寻找到特异性的核酸结构,因此以核酸结构为识别元件的生物传感方法可以作为一个生物检测的平台,实现对众多靶物质的检测。其次,核酸结构通常都具有非常高的亲和力,而高亲和力使得我们可以很方便地检测到极微量的靶分子,并将反应信号直接传输到检测元件进行读取,同时又不受其他非靶物质的干扰,实现对靶分子的特异性检测。另外,dna(包括部分rna)在化学性质上非常稳定,适于固定在固相表面,这使得发展耐用和可重复使用的固相传感器成为可能。
核酸结构在遇到相应的配体进行结合时通常会伴有明显的结构变化。这种结构的差异形成了基于核酸结构传感器的理论基础。一个典型的基于核酸结构的传感器包括一个双标记的寡核苷酸序列(电子传递或能量传递的受体和供体),因此,配体结合导致的结构变化直接可以影响到受体和配体之间的距离,从而可以高灵敏度的检测到电信号或光信号的产生。
本方法在上述基础上,提出利用纳米金颗粒对荧光的猝灭来检测核酸结构的构象变化。纳米金颗粒在生物学中的应用非常广泛,最早可以追溯到二十世纪七十年代免疫金在生物成像中的应用。近几年研究发现,纳米金是一种非常高效的荧光猝灭体系。1996年,mirkin和alivisatos所在工作组分别报道了纳米金-dna复合物的重要应用,并将其发展为基于纳米结构的新型检测平台。rothberg等人报道了一种更为简便的、利用未经过修饰的金胶来检测靶dna的比色法,其基本原理是纳米金颗粒可以和单链dna,通过静电作用发生瞬时的吸附结合,从而可以在高离子强度条件下有效地稳定纳米金,而且吸附在纳米金颗粒表面的dna由于拉近了荧光素与纳米金的距离,使得荧光素被有效猝灭,而双链dna则不具有这种作用。在此基础上,我们将这种新的理论应用在pcr领域,发展了一种高选择性的基于纳米金增强的nanoparticlepcr方法。
技术实现要素:
本发明提出进一步将纳米金用于核酸结构的荧光探针的方法。首先将与靶作用的特异性dna(aptamer等)与其互补的荧光标记cdna杂交形成dsdna作为双链探针,当加入靶分子后,特异性dna与靶进行高效结合,导致dsdna解离,荧光标记cdna释放到溶液中呈单链状态,当其吸附到纳米金表面时,纳米金可以非常高效地猝灭cdna的荧光。而双链探针本身以及其它刚性dna结构由于不能吸附到纳米金表面,从而荧光没有明显降低。利用这种方法,可以建立一种生物检测的通用模式实现对靶分子的快速、灵敏检测。、
本发明采用的技术方案是:
一种检测肿瘤标志物的方法,所述方法包括以下步骤:
(1)将肿瘤标志物的特异性核酸适体与其互补序列cdna反应,制成双链探针,所述互补序列的5’端标记有荧光基团;所述荧光基团优选fam
(2)向双链探针中加入待测肿瘤标志物靶分子,充分反应,作为实验组;
向双链探针中加水,作为空白组;向双链探针中加入与步骤(1)的核酸适体不匹配的肿瘤标志物作为对照组;记录三组的荧光光谱强度
取实验组、空白组、对照组加入纳米金,记录三组加入纳米金后的荧光光谱强度;
(3)实验组中,待测肿瘤标志物靶分子与核酸适体特异性结合,释放出互补序列,互补序列标记有荧光基团,以单链状态存在,吸附到纳米金表面,纳米金猝灭互补序列的荧光;实验组加入纳米金后的荧光强度显著下降;且荧光强度的下降值与待测肿瘤标志物靶分子的浓度呈比例关系;
空白组和对照组中,水或不匹配的肿瘤标志物无法与核酸适体特异性结合,双链探针无法吸附到纳米金表面,双链探针上的荧光无法被纳米金猝灭;空白组和对照组加入纳米金的荧光强度无显著变化;
所述步骤(1)中,所述肿瘤标志物包括前列腺特异性抗原(psa)、癌胚抗原(cea)、甲胎蛋白(afp)或上皮细胞粘附分子(epcam)
所述步骤(1)中,前列腺特异性抗原(psa)、癌胚抗原(cea)、甲胎蛋白(afp)或上皮细胞粘附分子(epcam)各自的核酸适体和其互补序列cdna的序列如下表1所示。
表1序列表
互补序列的5’端标记有荧光基团;所述荧光基团优选fam
所述步骤(1)中,将肿瘤标志物的特异性核酸适体与其互补序列cdna反应,制成双链探针,优选按以下步骤操作:取2μl浓度为100μm的特异性核酸适体溶液与2μl浓度为100μm的互补序列cdna溶液,加入18μl的缓冲溶液后进行充分杂交形成双链探针。一般在室温下反应,反应时间通常为10~30分钟;所述缓冲溶液为25mmtris,ph8.2,0.3mnacl。
所述步骤(2)中,向双链探针中加入待测肿瘤标志物靶分子,充分反应,优选按以下步骤操作:向双链探针溶液中加入2μl浓度为0.01-1mm的待测肿瘤标志物靶分子溶液,室温下充分反应。反应时间通常为30~60分钟。
进一步,所述步骤(2)中,取实验组、空白组、对照组加入纳米金,优选按以下方法操作:分别取2μl的实验组、空白组、对照组溶液,加入10-100μl的纳米金溶液,用缓冲溶液补足总体积0.2ml后,记录三组的荧光光谱。所述纳米金溶液的浓度优选1~5nm更优选3.5nm。
本发明的基本原理是:利用纳米金对不同结构dna的吸附作用不同,以及纳米金高效猝灭荧光的性质来实现对靶物质的检测。首先设计任意靶的特异性dna-荧光标记cdna双链作为捕获探针,加入靶后释放出的荧光标记cdna以单链形式存在,靶与特异性dna形成二级结构。由于单链dna可以通过表面氨基吸附到纳米金颗粒表面,因此cdna的荧光被纳米金猝灭。而双链dna和其它刚性的二级结构均不能吸附到纳米金表面,因此双链的荧光没有明显降低。这种双链探针,改变了目前所使用的单链探针依赖于探针本身结构变化提供信号的检测模式,建立了一种通用的工作模式,即通过释放出的cdna单链与纳米金的相互作用来进行检测,从而扩大了其应用范围。利用这种方法可以很方便地实现对靶分子的快速、灵敏、选择性检测。
本发明利用上述原理能够实现对前列腺特异性抗原(psa)、癌胚抗原(cea)、甲胎蛋白(afp)、上皮细胞粘附分子(epcam)等的快速检测。
附图说明
图1本发明检测反应原理图。
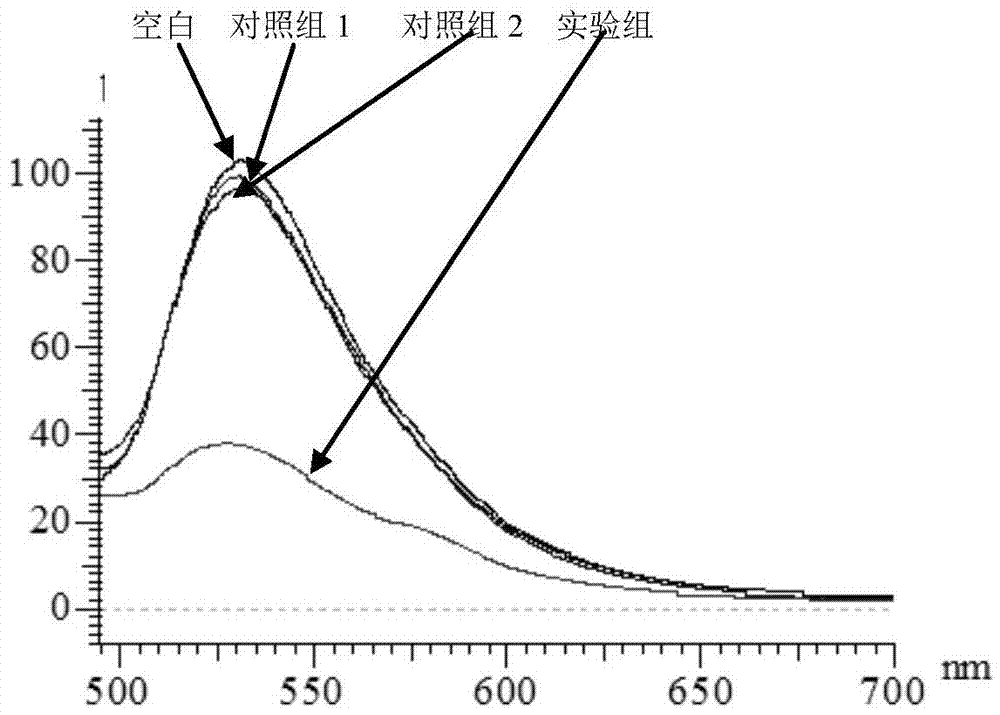
图2实施例1的实验组、空白组、对照组1、对照组2加入纳米金后的的荧光光谱图。
具体实施方式
荧光光谱在hitachif4500fluorescenespectrophotometer上进行,激发波长480nm,发射波长490-900nm,用200μl石英比色皿,取200μl样品进行测量。
本发明中所用纳米金颗粒为实验室自制,参考文献“grabar,k.c.;freeman,r.g.;hommer,m.b.;natan,m.j.anal.chem.1995,67,735-743.”进行。具体步骤如下,将100ml0.01%的氯金酸溶液加热到沸腾后,在剧烈搅拌下快速加入3.5ml的柠檬酸三钠溶液(10mg/ml)并继续加热15-30min,溶液变成酒红色。停止加热继续搅拌30min后,静置过夜。然后用0.22μm滤膜进行过滤,并放置在冰箱4℃保存。根据本方法得到粒径为13nm左右,浓度为3.5nm的纳米金溶液。
本发明实施例中所用的各种dna序列购自上海生物工程技术有限公司,如表1所示。
表1序列表
互补序列cdna的5’端标记有荧光基团fam
实施例1纳米金-dna相互作用原理对前列腺特异性抗原(psa)的检测
步骤:分别取2μl浓度为100μm的psa-aptamer溶液与2μl浓度为100μm的cdna溶液,加入18μl的缓冲溶液(25mmtris,ph8.2,0.3mnacl)后进行充分杂交形成双链探针(室温下反应30分钟)。然后向杂交液中加入2μl浓度为1mm的psa水溶液,室温下进行充分反应。同时以不加psa,加入2μl水的一组作为空白、以及加入2μl1mm的afp(n1)、cea(n2)的两组分别作为对照组1和对照组2。然后分别取2μl的上述反应溶液加入100μl3.5nm的纳米金溶液,用缓冲溶液(25mmtris,ph8.2,0.3mnacl)补足总体积0.2ml后,记录实验组和对照组的荧光光谱。
结果:如图1所示,在含有psa的一组溶液中,psa与双链探针中的psa-aptamer结合,释放出fam-cdna单链,吸附到纳米金表面从而荧光被猝灭70%以上。而没有加psa的一组,以及n1、n2组,双链探针的结构没有发生变化,因此加入纳米金后荧光降低幅度较小(小于30%,可能是由于杂交效率而导致溶液中部分fam-cdna以单链形式存在)。利用此法最低可以检测到fmol数量级的psa。
实施例2纳米金-dna相互作用原理对癌胚抗原(cea)的检测
步骤:分别取2μl浓度为100μm的cea-aptamer溶液与2μl浓度为100μm的cdna溶液,加入18μl的缓冲溶液(25mmtris,ph8.2,0.3mnacl)后进行充分杂交形成双链探针(室温下反应30分钟)。然后向杂交液中加入2μl浓度为0.1mm的cea水溶液,室温下进行充分反应。同时以不加cea,加入2μl水的一组作为空白、以及加入2μl1mm的psa、afp的两组作为对照。然后分别取2μl的上述反应溶液加入10μl3.5nm的纳米金溶液,用缓冲溶液补足总体积0.2ml后,记录实验组和对照组的荧光光谱。
结果:在含有cea的一组溶液中,cea与双链探针中的cea-aptamer结合,释放出fam-cdna单链,吸附到纳米金表面从而荧光被猝灭70%以上。而没有加cea的一组,以及psa、afp组,双链探针的结构没有发生变化,因此加入纳米金后荧光降低幅度较小(小于30%,可能是由于杂交效率而导致溶液中部分fam-cdna以单链形式存在)。利用此法最低可以检测到fmol数量级的cea。
实施例3纳米金-dna相互作用原理对甲胎蛋白(afp)的检测
步骤:分别取2μl浓度为100μm的afp-aptamer溶液与2μl浓度为100μm的cdna溶液,加入18μl的缓冲溶液(20mmtris-乙酸,ph7.4,140mmnacl,1mmcacl2,1mmmgcl2)后进行充分杂交形成双链探针(室温下反应30分钟)。然后向杂交液中加入2μl浓度为0.05mm的afp的水溶液,室温下进行充分反应。同时以不加afp,加入2μl水的一组作为空白实验。以及加入2μl1mm的bsa的一组作为对照。然后分别取2μl的上述反应溶液加入50μl3.5nm的纳米金溶液,用缓冲溶液补足总体积0.2ml后,记录实验组和对照组的荧光光谱。
结果:在含有afp的一组溶液中,afp与双链探针中的afp-aptamer结合,释放出fam-cdna单链,吸附到纳米金表面从而荧光被猝灭70%以上。而没有加afp的一组,以及bsa组,双链探针的结构没有发生变化,因此加入纳米金后荧光降低幅度较小(小于30%,可能是由于杂交效率而导致溶液中部分fam-cdna以单链形式存在)。利用此法最低可以检测到fmol数量级的afp。
实施例4纳米金-dna相互作用原理对上皮细胞粘附分子(epcam)的检测
步骤:分别取2μl浓度为100μm的epcam-aptamer溶液与2μl浓度为100μm的cdna溶液,加入18μl的缓冲溶液(10mmpb,ph7.0,0.2mnacl)后进行充分杂交形成双链探针(室温下反应30分钟)。然后向杂交液中加入2μl浓度为1mm的epcam的水溶液,室温下进行充分反应。同时以不加epcam,加入2μl水的一组作为空白实验。以及加入2μl1mm的bsa的一组作为对照。然后分别取2μl的上述反应溶液加入100μl3.5nm的纳米金溶液,用缓冲溶液补足总体积0.2ml后,记录实验组和对照组的荧光光谱。
结果:在含有epcam的一组溶液中,epcam与双链探针中的epcam-aptamer结合,释放出fam-cdna单链,吸附到纳米金表面从而荧光被猝灭70%以上。而没有加epcam的一组,以及bsa组,双链探针的结构没有发生变化,因此加入纳米金后荧光降低幅度较小(小于30%,可能是由于杂交效率而导致溶液中部分fam-cdna以单链形式存在)。利用此法最低可以检测到fmol数量级的epcam。
sequencelisting
<110>绍兴康知生物科技有限公司
<120>一种检测肿瘤标志物的方法
<130>
<160>8
<170>patentinversion3.3
<210>1
<211>23
<212>dna
<213>unknown
<220>
<223>人工序列
<400>1
aattaaggctcgccatcaaatag23
<210>2
<211>23
<212>dna
<213>unknown
<220>
<223>人工序列
<400>2
ctatttgatggcgagccttaatt23
<210>3
<211>35
<212>rna
<213>unknown
<220>
<223>人工序列
<400>3
gugcugggcuagggcggcggcgggaaaaccaguac35
<210>4
<211>35
<212>dna
<213>unknown
<220>
<223>人工序列
<400>4
gtactggttttcccgccgccgccctagcccagcac35
<210>5
<211>35
<212>dna
<213>unknown
<220>
<223>人工序列
<400>5
ttttaattcttgtttattggtatatccgcctctga35
<210>6
<211>35
<212>dna
<213>unknown
<220>
<223>人工序列
<400>6
tcagaggcggatataccaataaacaagaattaaaa35
<210>7
<211>48
<212>dna
<213>unknown
<220>
<223>人工序列
<400>7
cactacagaggttgcgtctgtcccacgttgtcatggggggttggcctg48
<210>8
<211>48
<212>dna
<213>unknown
<220>
<223>人工序列
<400>8
caggccaaccccccatgacaacgtgggacagacgcaacctctgtagtg48
- 还没有人留言评论。精彩留言会获得点赞!
- 普适型用于同时检测多种肿瘤标志物的微流控芯片装置的制造方法
- 男性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 女性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 一种检测口腔癌的标志物及其试剂盒的制造方法与工艺
- microRNA 标志物组及其在制备检测胃癌淋巴结转移试剂盒中的应用的制造方法与工艺
- 基于弹性蛋白酶荧光底物检测乳腺癌肿瘤标志物CA153的酶联免疫试剂盒制备方法与制造工艺
- 检测和评价力量训练效果的miRNA标志物或其组合及其应用的制造方法与工艺
- 一种最优超平面的构建方法、动态优化系统和构建装置与制造工艺
- 癌症标志物及癌症的判定方法与制造工艺
- 检测尿液中单羟酚类代谢物的试剂盒及其制备方法与制造工艺