具有皮肤美白活性的肽及其用途的制作方法
本发明涉及包含具有皮肤美白活性的肽作为有效成分的皮肤美白用组合物。
背景技术:
转化生长因子-β1(Transforming growth factor beta 1,TGF-β1)为在多样的种类的细胞中,通过调节生长、分化及凋亡,来进行组织的发达或维持稳态的因子。众所周知,转化生长因子-β1在黑色素细胞中呈现与黑色素生成有关的抑制效果(THE JOURNAL OF BIOLOGICAL CHEMISTRY Vol.272,No.7,Issue of February 14,pp.3967-3972,1997)。
转化生长因子-β1的这种功能通过增加在黑色素生成中作为重要的酶的酪氨酸酶的分解来呈现。并且,还通过促进细胞外调节蛋白激酶(ERK1/2)活性来呈现抑制黑色素形成,上述细胞外调节蛋白激酶(ERK1/2)用于促进作为调节如酪氨酸酶、与酪氨酸酶关联的基因-1、与酪氨酸酶关联的基因-2等参与黑色素生成的酶的表达的转录因子的小眼畸形相关转录因子(MITF,Microphthalmia-associated transcription factor)的分解(Physiol Rev 84:1155-1228,2004;10.1152/physrev.00044.2003.)。
本发明人通过现有研究开发了基于转化生长因子-β1的一部分氨基酸序列的肽,并验证了在黑色素细胞中的美白功效。之后,为了将肽的功能最大化,进行了通过与多种化学合成物相结合的改善研究,并通过功效筛选过程来发掘了相比于现有肽,美白功效得到提高的本发明的原材料。
本说明书全文中,参照了多篇论文及专利文献,并表示了其引用。所引用的论文及专利文献的公开内容全部插入于本说明书作为参照,从而更加明确说明本发明所属的技术领域的水平及本发明的内容。
技术实现要素:
本发明人为了开发具有优秀的皮肤美白活性的肽锐意努力研究。其结果,通过由序列1的氨基酸序列组成的肽抑制黑色素生成,抑制酪氨酸酶的活性,抑制与黑色素形成相关的因子的表达,来阐明对皮肤美白呈现优秀的效果,从而完成了本发明。
因此,本发明的目的在于,提供由记载于序列1的氨基酸序列组成的具有皮肤美白活性的肽。
本发明的再一目的在于,提供包含上述肽的皮肤美白用组合物。
本发明的另一目的在于,提供上述肽的皮肤美白用途。
本发明的还一目的在于,提供利用上述肽的皮肤美白方法。
根据以下发明的详细说明、发明要求保护范围及附图更加明确本发明的其他目的及优点。
本发明人为了开发具有优秀的皮肤美白活性的肽锐意努力研究。其结果,通过由序列1的氨基酸序列组成的肽抑制黑色素生成,抑制酪氨酸酶的活性,抑制与黑色素形成相关的因子的表达,抑制黑色素传递,来阐明对皮肤美白呈现优秀的效果。
以下,对本发明进行更详细地说明。
本发明的一实施方式涉及由序列1的氨基酸序列组成的具有皮肤美白活性的肽。
根据本发明的一实例,上述肽抑制黑色素的生成,抑制酪氨酸酶的活性及表达,并抑制作为参与黑色素形成的因子的小眼畸形相关转录因子、蛋白酶激活受体2的表达,肽抑制作为参与黑色素形成的信号传导物质的环磷腺苷效应元件结合蛋白(CREB)的磷酸化,不仅抑制参与皮肤美白的黑素体的传递,而且促进黑素体的分解。并且,本发明的肽抑制毛发生长。这种结果意味着本发明的肽对皮肤美白具有非常优秀的功效。
在本说明书中所使用的术语“肽”是指通过肽键来由多个氨基酸残基互相结合而成的线性分子。本发明的肽可通过本领域中公知的化学合成方法,尤其,固相合成技术(solid-phase synthesis techniques:Merrifield,J.Amer.Chem.Soc.85:2149-54(1963);Stewart,et al.,So]id Phase Peptide Synthesis,2nd.ed.,Pierce Chem.Co.:Rockford,111(1984))或液相合成技术(美国登录专利第5516891号)来制备而成。
作为本发明的肽,为了选定氨基酸序列的一部分部位,并使其活性增加,可在N-末端和/或C-末端诱导变形。
例如,上述肽的C-末端可变形为羟基(-OH)、氨基(-NH2)、叠氮基(-NHNH2)等,但并不限定于此。并且,上述肽的N-末端可与选自由乙酰基、芴甲氧羰基、甲酰基、棕榈基、肉豆蔻基、硬脂酰基及聚乙二醇(PEG)组成的组中的保护基相结合而成,但并不限定于此。
通过这种N-末端和/或C-末端的变形,来使本发明的肽的半衰期增加,从而在向生物体内给药时,可具有高的半衰期,并起到大大改善肽的稳定性的作用。
在本说明书中所使用的术语“稳定性”不仅是指“体内”稳定性,还指储存稳定性(例如,常温储存稳定性)。上述保护基起到从生物体内的蛋白质切割酶的攻击保护本发明的肽的作用。
本发明的另一实施方式涉及包含由序列1的氨基酸序列组成的肽作为有效成分的皮肤美白用组合物。
上述皮肤美白用组合物包含上述的本发明的肽作为有效成分,因而为了避免本说明书过于复杂,省略两者之间的共同的记载内容。
本发明的皮肤美白用组合物可制备成化妆品组合物。
上述化妆品组合物可制备成本发明所属领域中通常制备的任何剂型,例如,可剂型化为溶液、悬浮液、乳浊液、糊剂、凝胶、乳霜、乳液、粉、肥皂、含有表面活性剂的洁面剂、油、粉状粉底、乳浊液粉底、蜡粉底及喷雾剂等,更详细地,可制备成柔肤化妆水、营养化妆水、营养霜、按摩霜、精华素、眼霜、洁面霜、洗面奶、卸妆水、面膜、喷雾剂或粉的剂型,但并不限定于此。
在本发明的剂型为糊剂、乳霜或凝胶的情况下,可利用动物性油、植物性油、蜡、石蜡、淀粉、胺黄树胶、纤维素衍生物、聚乙二醇、硅、膨润土、二氧化硅、滑石或氧化锌等作为载体成分。
并且,在本发明的剂型为粉或喷雾剂的情况下,可利用乳糖、滑石、二氧化硅、氢氧化铝、硅酸钙和/或聚酰胺粉作为载体成分。
并且,在上述化妆品组合物的剂型为喷雾剂的情况下,还可包含如氟代烃、丙烷、丁烷和/或二甲醚等推进剂。
在上述化妆品组合物的剂型为溶液或乳浊液的情况下,可利用溶剂、增溶剂和/或乳化剂作为载体成分,例如水、乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苯甲醇、苯甲酸苄酯、丙二醇、1,3-丁基乙二醇油、甘油脂肪酸酯、聚乙二醇和/或山梨糖醇的脂肪酸酯,但并不限定于此。
在上述化妆品组合物的剂型为悬浮液的情况下,可利用液体稀释剂,如水、乙醇和/或丙二醇等;悬浮剂,如乙氧基化异硬脂醇、聚氧乙烯山梨醇酯和/或聚氧乙烯山梨糖醇酐酯等;微晶纤维素;甲基氢氧化铝;膨润土;琼脂和/或胺黄树胶等,但并不限定于此。
在上述化妆品组合物的剂型为含有表面活性剂的洁面剂的情况下,可利用脂肪醇硫酸盐、脂肪醇醚硫酸盐、磺基琥珀酸单酯、羟乙基磺酸盐、咪唑啉衍生物、甲基牛磺酸盐、肌氨酸盐、脂肪酸酰胺醚硫酸盐、烷基酰胺甜菜碱、脂肪醇、脂肪酸甘油酯、脂肪酸二乙醇酰胺、植物性油、羊毛脂衍生物或乙氧基化甘油脂肪酸酯等作为载体成分,但并不限定于此。
包含于本发明的化妆品组合物的成分除了作为有效成分的由序列1的氨基酸序列组成的肽及载体成分之外,可包含通常利用于化妆品组合物的多种成分,例如,可包含抗氧化剂、净化剂、增溶剂、维生素、颜料及香料等的通常的助剂。
本发明涉及具有皮肤美白活性的肽及包含其作为有效成分的皮肤美白用组合物,上述肽通过抑制黑色素生成,抑制酪氨酸酶的活性,抑制与黑色素形成相关的因子的表达,抑制黑素体传递,来对皮肤美白呈现优秀的效果。并且,因上述肽的尺寸小,因此皮肤透射度非常优秀,可借助优秀的活性及稳定性有利地适用于化妆品。
附图说明
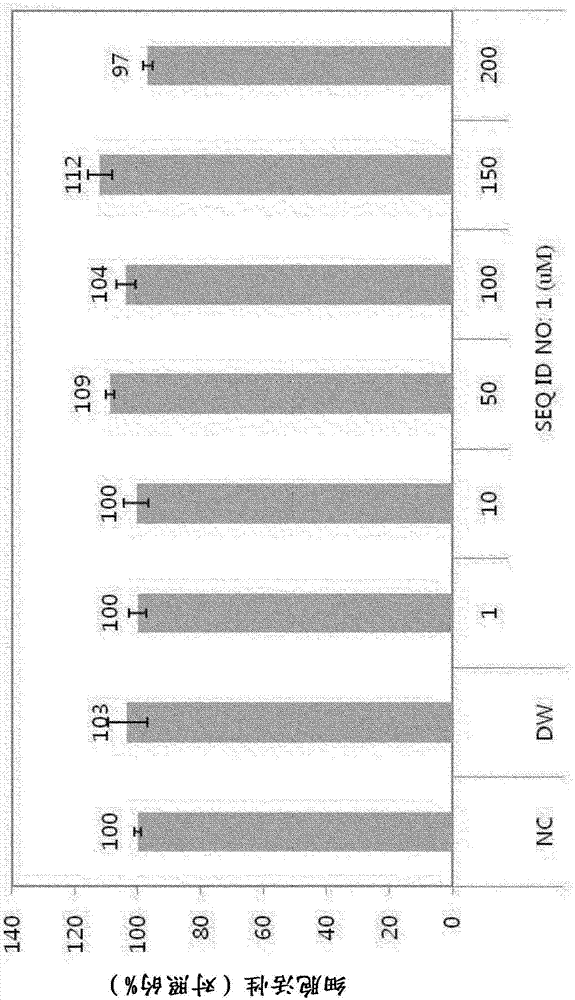
图1为表示对本发明一实施例的肽的细胞毒性进行评价的结果的图表。
图2a为表示在黑素瘤细胞株(B16F10)对本发明一实施例的肽进行处理,并测定黑色素生成量的结果的图表。
图2b为表示在黑素瘤细胞株(B16F10)对本发明一实施例的肽进行处理,并测定黑色素生成量的结果的照片。
图3为表示在黑素瘤细胞株(B16F10)对本发明一实施例的肽进行处理,并通过光学显微镜观察黑色素生成量的结果的照片。
图4为表示在黑素瘤细胞株(B16F10)对本发明一实施例的肽进行处理,并测定酪氨酸酶活性的结果的图表。
图5为表示在黑素瘤细胞株(B16F10)对本发明一实施例的肽进行处理,并利用酪氨酸酶抗体,来确认细胞内酪氨酸酶表达程度的照片。
图6为表示在黑素瘤细胞株(B16F10)对本发明一实施例的肽进行处理,并利用聚合酶链式反应(PCR)确认黑色素形成因子的基因表达变化的照片。
图7为表示在黑素瘤细胞株(B16F10)对本发明一实施例的肽进行处理,并利用对黑色素形成因子的蛋白质具有特异性的抗体,来确认它们的表达变化的照片。
图8为表示在黑素瘤细胞株(B16F10)对本发明一实施例的肽进行处理,并利用特异性的抗体,来确认作为黑色素形成因子信号传导物质的环磷腺苷效应元件结合蛋白的磷酸化程度的照片。
图9为表示在人类角质形成细胞株(HaCat)对本发明一实施例的肽进行处理,并利用聚合酶链式反应确认与角质形成细胞活性及吞噬作用相关的基因表达变化的照片。
图10为表示在人类角质形成细胞株(HaCat)对本发明一实施例的肽进行处理,并确认抑制黑素体向角质形成细胞流入的结果的图表。
图11为表示在人类角质形成细胞株(HaCat)对本发明一实施例的肽进行处理,并通过显微镜确认抑制角质形成细胞的黑素体吞噬作用的结果的照片。
图12为表示为了根据本发明一实施例观察黑素体流入抑制效果,利用荧光-结合生物粒子(bioparticles),来执行角质细胞吞噬作用分析的结果的照片。
图13为表示在人类角质形成细胞株(HaCat)对本发明一实施例的肽进行处理,并确认在角质形成细胞中的黑素体分解能力的的结果的图表。
图14a为表示对本发明一实施例的肽进行脂质体化,来涂敷于C57BL/6小鼠尾巴,并观察生物体内美白功效的结果的照片。
图14b为表示对本发明一实施例的肽进行脂质体化,来涂敷于C57BL/6小鼠尾巴,并观察生物体内美白功效的结果(比较例)的照片。
图14c为表示对本发明一实施例的肽进行脂质体化,来涂敷于C57BL/6小鼠尾巴,并观察生物体内美白功效的结果(实施例)的照片。
图15a至图15f为表示对本发明一实施例的肽进行脂质体化,来去除C57BL/6小鼠背部的毛后,进行涂敷,并观察0、7、10、13、15及17天的毛发生长速度的照片。
具体实施方式
以下,通过实施例更加详细说明本发明。这种实施例只用于更加详细说明本发明,根据本发明的要旨,本发明的范围不局限于这些实施例,这对于本发明所属技术领域的普通技术人员来说是显而易见的。
实施例
合成例1:肽合成
将700mg的氯三苯甲基氯树脂(Chloro trityl chloride resin;CTL resin,Nova biochem Cat No.01-64-0021)放入反应容器中,并加入10ml的二氯甲烷(MC)来搅拌了3分钟。去除溶液,并放入10ml的二甲基甲酰胺(DMF)来搅拌3分钟。然后,重新去除了溶剂。将10ml的二氯甲烷(DCM)溶液放入反应器中,并放入200mmole的Fmoc-Asp(OtBu)-OH(Bachem,Swiss)及400mmole的二异丙基乙胺(DIEA)后,搅拌并均匀溶解,搅拌1小时并进行反应。反应后清洗,将甲醇和二异丙基乙胺(2:1)溶解于二氯甲烷中,反应10分钟,并用过量的二氯甲烷/二甲基甲酰胺(1:1)进行清洗。去除溶液,并放入10ml的二甲基甲酰胺(DMF)来搅拌3分钟后,重新去除了溶剂。将10ml的脱保护溶液(20%的哌啶(Piperidine)/二甲基甲酰胺)放入反应容器中,并在常温条件下搅拌10分钟后,去除了溶液。放入同量的脱保护溶液,并重新维持10分钟反应后,去除溶液,并分别以3分钟为间隔用二甲基甲酰胺清洗2次、用二氯甲烷清洗1次、用二甲基甲酰胺清洗1次,从而制备了Asp-CTL树脂(Resin)。在新的反应器中放入10ml的二甲基甲酰胺溶液,并加入200mmole的Fmoc-Gly-OH(Bachem,Swiss)、200mmole的羟基苯并三唑(HoBt)及200mmole的苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐(Bop)后,搅拌来均匀溶解。在反应器中,经过2次以分馏的方式放入400mmole的N,N-二异丙基乙胺(DIEA)后,搅拌至少5分钟至所有固体溶解为止。将溶解的氨基酸混合溶液放入具有脱保护的树脂的反应容器中,在常温条件下搅拌1小时并进行反应。去除反应液,并用二甲基甲酰胺溶液每次搅拌5分钟,并搅拌3次后去除。取少量的反应树脂,并利用茚三酮测试(Nihydrin test)检查了反应程度。使用脱保护溶液,以与上述方法相同的方法进行2次脱保护反应,来制备了Gly-Asp-CTL树脂。使用二甲基甲酰胺和二氯甲烷充分清洗,并重新执行一次茚三酮测试,然后以与上述方法相同的方法执行了以下氨基酸附着实验。根据选定的氨基酸序列,按Fmoc-Arg(Pbf)-OH、Fmoc-Gly-OH、Fmoc-Gly-OH、Fmoc-Tyr(tBu)-OH、Fmoc-Gln(Trt)-OH、Fmoc-Thr(tBu)-OH、Fmoc-Asp(OtBu)-OH、Fmoc-Leu-OH,Fmoc-Ser(tBu)-OH、Fmoc-Trp-OH及Fmoc-Ile-OH的顺序进行连锁反应。利用脱保护溶液使Fmoc-保护基以10分钟为间隔反应2次后,清洗干净并去除。利用二甲基甲酰胺、二氯甲烷及甲醇,分别将与激活的丙戊酸(valproic acid)相结合后制备的肽基树脂清洗3次,使氮气慢慢流入来干燥后,在五氧化二磷(Phosphorus pentoxide,P2O5)条件下,减压成真空状态,来完全干燥后,放入30ml的泄漏溶液(81.5%的三氟乙酸(Trifluroacetic acid)、5%的蒸馏水、5%的苯甲硫醚(Thioanisole)、5%的苯酚(Phenol)、2.5%的1,2-乙二硫醇(EDT)及1%的三异丙基硅烷(TIS)),然后,在常温条件下微动一下,并维持2小时反应。通过过滤对树脂进行过滤,并利用少量的溶液清洗三氟乙酸(TFA)树脂后,与母液进行混合。利用减压蒸馏至剩有总容积的一半左右的容积,并加入50ml的凉的醚诱导沉淀后,进行离心分离来收集沉淀,并利用更凉的醚清洗2次。去除母液,并在氮条件下充分干燥,来合成了0.8g的纯化前丙戊酸基-Ile-Trp-Ser-Leu-Asp-Thr-Gln-Tyr-Gly-Gly-Arg-Gly-Asp-COOH肽1(序列1)(收率:89.0%)。当利用分子量测定仪测定时,可得到的分子量为1593.7(理论值:1593.7)。
表1
实施例1:细胞毒性实验
在37℃的培养器中将接种于48-孔培养用平板的黑色素形成细胞(B16F10细胞系(cell line))培养24小时后,去除各板的培养基,并更换为无血清培养基后,按浓度(1μM、10μM、50μM、100μM、150μM、200μM)对本肽进行了处理。然后,培养72小时后,放入噻唑蓝(MTT)试剂,并反应4小时后,利用二甲基亚砜(DMSO)溶解所生成的甲腊,并在560nm条件下测定了吸光度。
为了确认是否具有与由序列1的氨基酸序列组成的肽的黑色素细胞有关的细胞毒性,进行噻唑蓝实验,其结果确认了从1μM至200μM处理组未呈现细胞毒性(图1)。
实施例2:黑色素生成量的测定
在37℃的培养器中将接种于6-孔培养用平板的黑色素形成细胞(B16F10细胞系)培养24小时后,去除各板的培养基,并更换为新的培养基(2%血清培养基)后,按浓度(50μM、100μM、200μM)对α-促黑素细胞激素(α-MSH)(200ng/ml)、熊果苷(200、500μM)及本肽进行了处理。然后,培养72小时后去除培养液,并摘除细胞,然后移到1.5ml的管来在13000rpm下,进行3分钟的离心分离,从而去除上清液,并回收细胞颗粒来观察了黑色素。针对于细胞颗粒,每次放入150μl的2M的NaOH,在60℃条件下将细胞内黑色素溶解30分钟。然后,每次放入100μl的通过溶解于96-孔平板的各孔来取得的上清液,来在490nm下测定吸光度,并将其结果呈现于图2a及图2b。
如在图2a及图2b可确认,确认了由序列1的氨基酸序列组成的肽的浓度依赖性的抑制黑色素生成的效果(**P≤0.01)。
实施例3:黑色素生成量的肉眼观察
在37℃的培养器中将接种于6-孔培养用平板的黑色素形成细胞(B16F10细胞系)培养24小时后,去除各板的培养基,并更换为新的培养基(10%血清培养基)后,按浓度(50μM、100μM、200μM)对α-促黑素细胞激素(200ng/ml)、熊果苷(500μM)及本肽进行了处理。在图3表示通过光学显微镜观察培养72小时后,形成的黑色素的结果。
如在图3可确认,以细胞形态确认了由序列1的氨基酸序列组成的肽的浓度依赖性的抑制黑色素生成的效果。
实施例4:细胞内酪氨酸酶活性测定
在6-孔培养用平板中将黑色素形成细胞(B16F10细胞系)培养24小时后,并对α-促黑素细胞激素(200ng/ml)、不同浓度的肽(50μM、100μM、200μM)或作为阳性对照组的熊果苷(200μM、500μM)进行了处理来培养了72小时。然后,将6-孔培养用平板放置于冰块上,并利用凉的磷酸盐缓冲液(PBS)进行清洗后,放入300μl的含有1%的Triton X-100的0.1M的磷酸钠缓冲液(pH6.8,裂解缓冲液(lysis buffer),并在管收集1.5mL的细胞,来反复5次在-270℃温度下进行急速冷冻后解冻的反应,从而破坏了细胞膜。然后,在13000rpm下,进行20分钟的离心分离后,将上清液收集于另一1.5mL管,并对试样蛋白质进行定量。稀释成试样的蛋白质浓度相同,来按每个样品3孔的方式接种于96-孔培养用平板,并添加20μl的10mM的左旋多巴(L-dopa),来在37℃温度下,培养1小时后,在475nm条件下测定吸光度,并将其结果呈现于图4。
如在图4可确认,确认了由序列1的氨基酸序列组成的肽的浓度依赖性的抑制黑色素生成的效果(**P≤0.01)。
实施例5:酪氨酸酶表达量测定
在37℃的培养器中将接种于6-孔培养用平板的黑色素形成细胞(B16F10细胞系)培养24小时后,去除各板的培养基,并更换为新的培养基(10%血清培养基)后,按浓度(50μM、100μM)对α-促黑素细胞激素(200ng/ml)及本肽进行了处理。然后,培养48小时后利用附着酪氨酸酶抗体(美国圣克鲁斯生物技术(Santa cruz biotechnology)公司)及异硫氰酸荧光素(FITC)的二次免疫球蛋白(IgG)抗体(美国圣克鲁斯生物技术公司)来对细胞内表达蛋白质进行染色,并通过荧光显微镜以肉眼观察表达程度,来将其结果呈现于图5。
如在图5可确认,确认了由序列1的氨基酸序列组成的肽的浓度依赖性的抑制酪氨酸酶表达的效果。
实施例6:黑色素形成因子的基因表达变化观察
在6-孔培养用平板中将黑色素形成细胞(B16F10细胞系)培养24小时后,按浓度(100μM、200μM)对α-促黑素细胞激素(200ng/ml)、熊果苷(500μM)及本肽进行了处理。提取培养24小时的细胞的核糖核酸(RNA)后,制作了互补脱氧核糖核酸(cDNA)。然后,利用与作为参与黑色素形成的因子的小眼畸形相关转录因子及酪氨酸酶有关的各个具有特异性的以下表2的引物,来进行聚合酶链式反应而对各个基因的表达变化进行观察,并将其结果呈现于图6。
表2
如图6可确认,确认了由序列1的氨基酸序列组成的肽的高小眼畸形相关转录因子、酪氨酸酶基因的表达抑制效果。
实施例7:观察黑色素形成因子的蛋白质表达变化
在6-孔培养用平板中将黑色素形成细胞(B16F10细胞系)培养24小时后,按浓度(50μM、200μM)对α-促黑素细胞激素(200ng/ml)及本肽进行了处理。然后,培养72小时后,溶解细胞,来通过利用特异性抗体的蛋白质印迹法,对作为参与黑色素形成的核心因子的小眼畸形相关转录因子(美国圣克鲁斯生物技术公司)及酪氨酸酶(美国圣克鲁斯生物技术公司)的表达进行观察,将其结果呈现于图7。
如图7可确认,确认了由序列1的氨基酸序列组成的肽的浓度依赖性的抑制小眼畸形相关转录因子及酪氨酸酶蛋白质的表达的效果。
实施例8:观察黑色素形成信号传导物质
在6-孔培养用平板中将黑色素形成细胞(B16F10细胞系)培养24小时后,按浓度(50μM、100μM)对α-促黑素细胞激素(200ng/ml)及本肽进行了处理。然后,培养10分钟后,溶解细胞,来通过利用特异性抗体(美国圣克鲁斯生物技术公司)的蛋白质印迹法,对作为参与黑色素形成的信号传导物质的环磷腺苷效应元件结合蛋白的磷酸化程度进行观察,将其结果呈现于图8。
如图8可确认,确认了由序列1的氨基酸序列组成的肽的环磷腺苷效应元件结合蛋白的磷酸化抑制效果。
通过上述结果,可确认如下:由本发明的序列1的氨基酸序列组成的肽,通过抑制利用α-促黑素细胞激素激活的MC1R信号传导途径,来呈现抑制黑色素生成的效果。
实施例9:观察与角质形成细胞活性及吞噬作用相关的基因表达变化
在6-孔培养用平板中将人类角质形成细胞株(HaCaT)培养24小时后,按浓度(100μM、200μM)对作为诱导活性的物质的胰蛋白酶((Trypsin)4单位(Unit))大豆胰蛋白酶抑制剂(Soybean trypsin inhibitor)10Unit)及本肽进行了处理。然后,提取培养16小时的细胞的核糖核酸后,制作了互补脱氧核糖核酸。
利用对作为借助胰蛋白酶作用激活的角质形成细胞的表面受体中之一的蛋白酶激活受体2具有特异性的引物对(参照以下表3),来进行聚合酶链式反应,从而对各个基因的表达变化进行观察,将其结果呈现于图9。
表3
如在图9可确认,通过作为丝氨酸蛋白酶的胰蛋白酶处理,来根据角质细胞的蛋白酶激活受体2的激活诱导基因表达,通过对由序列1的氨基酸序列组成的肽进行处理,来观察了浓度依赖性的蛋白酶激活受体2的基因表达减少。
实施例10:确认抑制黑素体向角质形成细胞流入(使用分离的黑素体)
在6-孔培养用平板中将人类角质形成细胞株(HaCaT)培养24小时,并在无血清培养培养基中对从小鼠黑素瘤细胞株(B16F10)中分离的黑素体进行3小时的预处理,并对不同浓度的肽(10μM、50μM、100μM、200μM)或作为阳性对照组的熊果苷(200μM)进行处理并培养了48小时。然后,通过利用磷酸盐缓冲液进行清洗,来去除未流入的黑素体,并在收集角质形成细胞且进行沉淀后取得的颗粒添加1M的NaOH,在80℃的烘箱中溶解颗粒后,在490nm条件下,测定了OD值。为了观察由序列1的氨基酸序列组成的肽的不同浓度抑制黑素体的流入的效果,利用从黑素瘤中分离的黑素体,来执行角质细胞吞噬作用分析,并将其结果呈现于图10。
如在图10可确认,通过测定吸光度,来确认向角质细胞内流入的黑素体的量,其结果,可确认由序列1的氨基酸序列组成的肽的浓度依赖性的抑制吞噬作用的效果。
实施例11:确认抑制黑素体向角质形成细胞流入(使用分离的黑素体)
在6-孔培养用平板中将人类角质形成细胞株(HaCaT)培养24小时,并在无血清培养培养基中对从小鼠黑素瘤细胞株(B16F10)中分离的黑素体进行3小时的预处理,并对不同浓度的肽(10μM、50μM、100μM、200μM)或作为阳性对照组的熊果苷(200μM)进行处理并培养了48小时。然后,通过利用磷酸盐缓冲液进行清洗,来去除未流入的黑素体,并进行韦塔纳-麦森二氏染剂(fontana-masson stain)染色,来通过显微镜观察了抑制角质形成细胞的黑素体吞噬作用。为了观察由序列1的氨基酸序列组成的肽的不同浓度抑制黑素体的流入的效果,利用从黑素瘤中分离的黑素体,来执行角质细胞吞噬作用分析,并将其结果呈现于图11。
如在图11可确认,通过光学显微镜图像分析,确认向角质细胞内流入的黑素体的量,其结果,可确认由序列1的氨基酸序列组成的肽的浓度依赖性的抑制吞噬作用的效果。
实施例12:确认向角质形成细胞的黑素体流入抑制(使用生物粒子)
在24-孔培养用平板中将人类角质形成细胞株(HaCaT)培养24小时,并在胎牛血清培养培养基中对不同浓度的肽(100μM、200μM)或作为阳性对照组的熊果苷(200μM)进行处理,来培养24小时。之后,使用Vybrant.吞噬作用测定试剂盒(Phagocytosis Assay Kit)(V-6694),通过荧光显微镜观察了人类角质形成细胞株的吞噬作用的抑制。为了观察由序列1的氨基酸序列组成的肽的不同浓度黑素体流入的抑制效果,利用荧光-结合生物粒子(bioparticles)来执行吞噬作用分析,并将其结果呈现于图12。
如在图12可确认,通过荧光显微镜图像分析,确认向角质细胞内流入的生物粒子的量,其结果,可确认由序列1的氨基酸序列组成的肽的浓度依赖性的抑制吞噬作用的效果。
实施例13:在角质形成细胞中的黑素体分解能力的观察
在6-孔培养用平板中将人类角质形成细胞株培养24小时,并在无血清培养培养基中对从小鼠黑素瘤细胞株(B16F10)中分离的黑素体进行48小时的预处理,之后,并利用磷酸盐缓冲液进行清洗来去除未流入的黑素体,并对不同浓度的肽(100μM、200μM)或作为阳性对照组的熊果苷(200μM)及转化生长因子-β(TGFβ-1)进行处理并培养了72小时。为了测定对利用角质形成细胞进行吞噬作用的黑素体的分解,在收集角质形成细胞来进行沉淀后取得的颗粒添加1M的NaOH,并在80℃的烘箱溶解颗粒后,在490nm条件下测定OD值,将其结果呈现于图13。
如在图13可确认,对与角质细胞流入的黑素体有关的由序列1的氨基酸序列组成的肽的分解促进功效进行观察,其结果,确认了浓度依赖性效果。
实施例14:生物体内美白功效的观察(体内(in vivo))
在8周龄的C57BL/6小鼠的尾部以一天一次的方式涂敷脂质体化肽(5000ppm)及作为阳性对照组的熊果苷,来进行了约8周的实验。实验结束后通过牺牲小鼠来摘出尾部皮肤组织,并利用石蜡包埋尾部皮肤组织来制作石蜡块。然后制备成石蜡切片来进行韦塔纳-麦森二氏染剂(fontana-masson stain),以形态学的方式进行观察,将其结果呈现于图14a至图14c。
如在图14a可确认,进行8周的涂敷实验,可观察到如下结果:与对照组相比,包含由序列1的氨基酸序列组成的肽的脂质体处理组的尾部的颜色变亮。
并且,如在图14b及图14c的通过F&M染色的黑色素分布确认结果中可确认,与分布于对照组表皮的基底层的黑色素相比,由序列1的氨基酸序列组成的肽处理组的分布量少很多。
实施例15:观察生物体内毛发生长抑制(体内)
通过打蜡去除8周龄的C57BL/6小鼠的背部毛后,以一日一次的方式将得到脂质体化的肽涂敷17天,来观察毛发生长速度,并将其结果呈现于图15。
如在图15可确认,在通过打蜡去除背部毛的小鼠上将包含由序列1的氨基酸序列组成的肽的脂质体涂敷17天,其结果可确认与对照组相比,毛发生长速度显著变慢。
以上,详细说明了本发明的特定部分,但可以明确的是,对于本发明所属技术领域的普通技术人员来说,这些具体说明只属于一个实例,本发明的范围不局限于此。因此,本发明的实质性范围由所附的发明要求保护范围和其等同技术方案来定义。
序列表
<110> CAREGEN CO., LTD.
<120> 具有皮肤美白活性的肽及其用途
<130> PP170010
<141> 2017-02-06
<160> 7
<170> SIPOSequenceListing 1.0
<210> 1
<211> 13
<212> PRT
<213> Apigmerin
<400> 1
Ile Trp Ser Leu Asp Thr Gln Tyr Gly Gly Arg Gly Asp
1 5 10
<210> 2
<211> 21
<212> DNA
<213> MITF正向引物
<400> 2
ccagcctggc gatcatgtca t 21
<210> 3
<211> 20
<212> DNA
<213> MITF反向引物
<400> 3
ggtctggaca ggagttgctg 20
<210> 4
<211> 20
<212> DNA
<213> 酪氨酸酶正向引物
<400> 4
ggccagcttt caggcagagg 20
<210> 5
<211> 20
<212> DNA
<213> 酪氨酸酶反向引物
<400> 5
tggtgcttca tgggcaaaat 20
<210> 6
<211> 20
<212> DNA
<213> PAR2正向引物
<400> 6
tgctagcagc ctctctctcc 20
<210> 7
<211> 20
<212> DNA
<213> PAR2反向引物
<400> 7
cttcaagggg aaccagatga 20
- 还没有人留言评论。精彩留言会获得点赞!