酪氨酸酶生物发光探针及其制备方法和应用与流程
本发明公开了一类用于酪氨酸酶检测的生物发光探针及其制备方法和应用。
背景技术:
酪氨酸酶是一种含铜酶,其广泛存在于植物、动物和微生物体中,是黑色素代谢过程中的关键酶之一。酪氨酸酶不仅可以将邻位双羟基化的酚类化合物通过催化氧化作用使其转化为对应的醌,还可以在一些单羟基化的酚类化合物的羟基邻位引入第二个羟基。据报道,酪氨酸酶在黑色素瘤细胞中是过量表达的,所以在临床研究中,它可以作为一种黑色素瘤的生物标记。因此,构建一种可以快速检测酪氨酸酶的方法在生命科学及医学临床研究中具有重要意义。
目前检测酪氨酸酶的方法有很多种,如电化学方法,荧光法等。但是,这些分析方法当中,电化学方法由于需要电流,会对蛋白造成一定的化学损伤从而影响检测的准确性;荧光法由于存在对激发光源的依赖性从而产生如光漂白和自发荧光等不可忽视的缺点,也限制了其进一步的应用。因此开发更加简便、快速、高效灵敏的酪氨酸酶定量检测方法仍是目前研究的一个热点。
生物发光是一种存在于生物体内的特殊类型的化学发光,其本质是生物体内的萤光素酶在氧气、atp和镁离子等存在的前提下,催化其底物萤光素发生生化反应,并以光子的形式释放能量的过程。生物发光成像技术由于其具有非侵袭性、低背景、高灵敏度、可视化以及能够实现实时动态观测等优点而得到广泛关注,逐渐发展,成为一种重要的活体成像手段。
技术实现要素:
本发明的目的在于提供一类可用于酪氨酸酶检测的化合物,所述化合物用作生物发光探针对体内和体外酪氨酸酶的检测具有非常高的灵敏度和选择性。
本发明的另一目的在于提供上述化合物的制备方法。
本发明的又一目的在于提供上述化合物在酪氨酸酶检测中的应用。
本发明目的通过如下技术方案实现:
如下式(i)所示的化合物:
其中,r1、r2、r3相同或不同,彼此独立地选自h、c1-6烷基、c1-6烷氧基、-co-c1-6烷基、-co-nh-c1-6烷基、-cooc1-6烷基、f、cl、br、i、环烷基、杂环基、芳基、杂芳基;
x选自o或nr5;y选自s或nr6;z选自s、se或te;r5、r6相同或不同,彼此独立地选自h或c1-6烷基。
根据本发明的实施方案,r1、r2、r3相同或不同,彼此独立地选自h、c1-3烷基、c1-3烷氧基;例如r1、r2、r3彼此独立地选自下列基团:h,-ch3、-och3。
根据本发明的实施方案,x选自o或nh。
根据本发明的实施方案,y、z选自s。
作为实例,所述式(i)化合物选自如下化合物:
本发明还提供上述式(i)化合物的制备方法,包括如下步骤:
其中,r1、r2、r3、x、y、z如上面所定义;
(a)将式(ii)化合物与d-半胱氨酸盐酸盐、或硒基-d-半胱氨酸盐酸盐或碲基-d-半胱氨酸盐酸盐反应,得到式(i)化合物。
根据本发明,步骤(a)中,所述反应在溶剂环境下进行;所述溶剂为醇类溶剂、卤代烷烃类溶剂和水构成的混合溶剂;优选为甲醇、二氯甲烷和水构成的混合溶剂。
根据本发明,所述反应在催化剂的存在下进行,所述催化剂选自碱金属的碳酸盐或碳酸氢盐,例如为碳酸钾。
根据本发明,式(ii)化合物与d-半胱氨酸盐酸盐或硒基-d-半胱氨酸盐酸盐或碲基-d-半胱氨酸盐酸盐的摩尔比为1:(1~2),例如为1:1。
根据本发明,所述制备方法可以采用如下步骤:将化合物(ii)溶解于溶剂中(例如为甲醇和二氯甲烷的混合溶剂),再加入用甲醇和去离子水溶解的d-半胱氨酸盐酸盐或硒基-d-半胱氨酸盐酸盐或碲基-d-半胱氨酸盐酸盐和碳酸钾溶液,反应得到式(i)化合物。
根据本发明,所述制备方法还包括式(ii)化合物的制备,式(ii)化合物可以由如下方法制备,包括:
其中,r1、r2、r3、x、y如上面所定义;l选自离去基团,例如为cl、br、i;
(b)将化合物(a)和化合物(b)进行反应,得到式(ii)化合物。
根据本发明,步骤(b)中,所述反应在溶剂中进行,所述溶剂可为腈类溶剂,例如乙腈。
根据本发明,所述反应在催化剂的存在下进行,所述催化剂选自碱金属的碳酸盐或碳酸氢盐,例如为碳酸钾。
根据本发明,反应温度优选为60-100℃,例如85℃。
根据本发明,化合物(a)与化合物(b)的摩尔比为(1~3):1,例如为3:1。
本发明所述式(i)化合物的合成步骤简单,反应时间短,提纯方便,工艺简单。
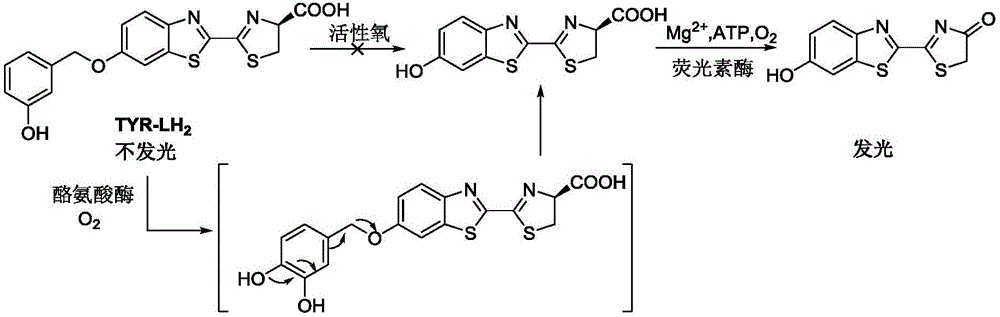
本发明通过对萤光素类物质进行化学修饰,引入具有与酪氨酸酶反应特异性的基团,得到了一类可用于酪氨酸酶检测的生物发光探针。在萤光素/氨基萤光素类物质中,当其6’位为羟基/氨基时,其可以在萤光素酶、atp和mg2+的存在下发生生物发光。本发明化合物以这些可以发光的萤光素/氨基萤光素类物质为母体,将能够识别酪氨酸酶的基团链接到萤光素/氨基萤光素的6’位羟基/氨基上。本发明化合物作为底物并不能被荧光素酶识别,不具有发光能力。而当本发明化合物遇到酪氨酸酶后,化合物中的识别基团与酪氨酸酶发生反应,从而释放出萤光素/氨基萤光素类物质,在atp、mg2+和萤光素酶的作用下发生生物发光(具体实例参见图1)。该类探针对酪氨酸酶有很好的选择性和灵敏度,可用作酪氨酸酶的生物发光探针。
本发明还提供式(i)化合物用作酪氨酸酶生物发光探针的用途。
本发明还提供一种检测酪氨酸酶的方法,包括将式(i)化合物施用于需要检测的样品。
根据本发明,所述检测可以在缓冲溶液中进行。
根据本发明,所述缓冲溶液选自hepes缓冲溶液,tris-hcl缓冲溶液,或pbs缓冲溶液等。
根据本发明,所述检测在atp、萤光素酶和镁离子的存在下进行。
根据本发明,所述检测在含有氧气的环境下进行。
本发明式(i)化合物对酪氨酸酶的检测具有专一性,而对其他活性氧物种、氨基酸及其他生物体内酶则无响应。
根据本发明,所述检测可用于体外或体内酪氨酸酶的检测。
本发明所述式(i)化合物可用于细胞内酪氨酸酶成像,用于区分黑色素瘤细胞和其他细胞中酪氨酸酶含量的变化。例如所述式(i)化合物可用于小鼠体内酪氨酸酶成像。
本发明还提供式(i)化合物在制备用于检测酪氨酸酶的试剂中的应用。
术语定义和说明:
除非另有定义,否则本文所有科技术语具有的涵义与权利要求主题所属领域技术人员通常理解的涵义相同。应理解,上述简述和下文的详述为示例性且仅用于解释,而不对本申请主题作任何限制。在本申请中,除非另有说明,所用术语“包括”以及其它形式,例如“包含”、“含”和“含有”并非限制性。
术语“烷基”指具有1-6个,优选1-3个碳原子的直链或支链烷基,所述烷基例如为甲基、乙基、丙基、异丙基、丁基、异丁基、叔丁基、仲丁基、戊基、新戊基。
术语“芳基”应理解为优选表示具有6~20个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环,优选“c6-14芳基”。术语“c6-14芳基”应理解为优选表示具有6、7、8、9、10、11、12、13或14个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环(“c6-14芳基”),特别是具有6个碳原子的环(“c6芳基”),例如苯基;或联苯基,或者是具有9个碳原子的环(“c9芳基”),例如茚满基或茚基,或者是具有10个碳原子的环(“c10芳基”),例如四氢化萘基、二氢萘基或萘基,或者是具有13个碳原子的环(“c13芳基”),例如芴基,或者是具有14个碳原子的环(“c14芳基”),例如蒽基。
术语“杂芳基”应理解为含有5-20个环原子、5-14个环原子,或5-12个环原子,或5-10个环原子,或5-6个环原子的单环、双环和三环体系,其中至少一个环体系是芳香族的,且至少一个环体系包含一个或多个杂原子(例如n、o、s、se等),其中每一个环体系包含5-7个原子组成的环,且有一个或多个连接点与分子其余部分相连。所述杂芳基基团任选地被一个或多个本发明所描述的取代基所取代。在一些实施方案中,5-10个原子组成的杂芳基包含1,2,3或4个独立选自o、s、se和n的杂原子。在另一些实施方案中,5-6个原子组成的杂芳基包含1,2,3或4个独立选自o、s、se和n的杂原子。
杂芳基基团的单环实例包括,但并不限于,噻吩基、呋喃基、吡咯基、噁唑基、噻唑基、咪唑基、吡唑基、异噁唑基、异噻唑基、噁二唑基、三唑基、噻二唑基、噻-4h-吡唑基等以及它们的苯并衍生物,例如苯并呋喃基、苯并噻吩基、苯并噁唑基、苯并异噁唑基、苯并咪唑基、苯并三唑基、吲唑基、吲哚基、异吲哚基等;或吡啶基、哒嗪基、嘧啶基、吡嗪基、三嗪基等,以及它们的苯并衍生物,例如喹啉基、喹唑啉基、异喹啉基等;或吖辛因基、吲嗪基、嘌呤基等以及它们的苯并衍生物;或噌啉基、酞嗪基、喹唑啉基、喹喔啉基、萘啶基、蝶啶基、咔唑基、吖啶基、吩嗪基、吩噻嗪基、吩噁嗪基等。
术语“杂环基”意指单环,双环或三环体系,其中环上一个或多个原子独立任选地被杂原子所取代,环可以是完全饱和的或包含一个或多个不饱和度,但不是芳香族类,有一个或多个连接点连接到其他分子上去。一个或多个环上的氢原子可以独立地未被取代或被一个或多个本发明所描述的取代基所取代。其中一些实施例是,“杂环基”是3-7个原子组成的单环、或7-10个原子组成的的双环,其包含1-5个,优选1-3个选自n、o、s和se的杂原子。特别地,所述杂环基可以包括但不限于:4元环,如氮杂环丁烷基、氧杂环丁烷基;5元环,如四氢呋喃基、二氧杂环戊烯基、吡咯烷基、咪唑烷基、吡唑烷基、吡咯啉基;或6元环,如四氢吡喃基、哌啶基、吗啉基、二噻烷基、硫代吗啉基、哌嗪基或三噻烷基;或7元环,如二氮杂环庚烷基。任选地,所述杂环基可以是苯并稠合的。所述杂环基可以是双环的,例如但不限于5,5元环,如六氢环戊并[c]吡咯-2(1h)-基环,或者5,6元双环,如六氢吡咯并[1,2-a]吡嗪-2(1h)-基环。含氮原子的环可以是部分不饱和的,即它可以包含一个或多个双键,例如但不限于2,5-二氢-1h-吡咯基、4h-[1,3,4]噻二嗪基、4,5-二氢噁唑基或4h-[1,4]噻嗪基,或者,它可以是苯并稠合的,例如但不限于二氢异喹啉基、1,3-苯并噁唑基、1,3-苯并二氧杂环戊烯基。
除非另有说明,杂环基、杂芳基包括其所有可能的异构形式,例如其位置异构体。因此,对于一些说明性的非限制性实例,吡啶基或亚吡啶基包括吡啶-2-基、亚吡啶-2-基、吡啶-3-基、亚吡啶-3-基、吡啶-4-基和亚吡啶-4-基;噻吩基或亚噻吩基包括噻吩-2-基、亚噻吩-2-基、噻吩-3-基和亚噻吩-3-基。
本文所用的有关术语“受试者”、“患者”或“个体”是指患有疾病、病症或病况等的个体,包括哺乳动物和非哺乳动物。哺乳动物的实施例包括但不限于哺乳动物纲的任何成员:人,非人的灵长类动物(例如黑猩猩和其它猿类和猴);家畜,例如牛、马、绵羊、山羊、猪;家养动物,例如兔、狗和猫;实验室动物,包括啮齿类动物,例如大鼠、小鼠和豚鼠等。非人哺乳动物的实施例包括但不限于鸟类和鱼类等。在本文提供的一个有关方法和组合物的实施方式中,所述哺乳动物为人。
本文所用的术语“治疗”和其它类似的同义词包括缓解、减轻或改善疾病或病症症状,预防其它症状,改善或预防导致症状的潜在代谢原因,抑制疾病或病症,例如阻止疾病或病症的发展,缓解疾病或病症,使疾病或病症好转,缓解由疾病或病症导致的症状,或者中止疾病或病症的症状,此外,该术语包含预防的目的。该术语还包括获得治疗效果和/或预防效果。所述治疗效果是指治愈或改善所治疗的潜在疾病。此外,对与潜在疾病相关的一种或多种生理症状的治愈或改善也是治疗效果,例如尽管患者可能仍然受到潜在疾病的影响,但观察到患者情况改善。就预防效果而言,可向具有患特定疾病风险的患者施用所述组合物,或者即便尚未做出疾病诊断,但向出现该疾病的一个或多个生理症状的患者施用所述组合物。
本文所使用术语“有效量”、“治疗有效量”或“药学有效量”是指服用后足以在某种程度上缓解所治疗的疾病或病症的一个或多个症状的至少一种药剂或化合物的量。其结果可以为迹象、症状或病因的消减和/或缓解,或生物系统的任何其它所需变化。例如,用于治疗的“有效量”是在临床上提供显著的病症缓解效果所需的包含本文公开化合物的组合物的量。可使用诸如剂量递增试验的技术测定适合于任意个体病例中的有效量。
本文所用术语“服用”、“施用”、“给药”、“给予”等是指能够将化合物或组合物递送到进行生物作用的所需位点的方法。这些方法包括但不限于口服途径、经十二指肠途径、胃肠外注射(包括静脉内、皮下、腹膜内、肌内、动脉内注射或输注)、外用和经直肠给药。本领域技术人员熟知可用于本文所述化合物和方法的施用技术。在优选的实施方式中,本文讨论的化合物和组合物通过口服施用。
附图说明
图1为实施例2制备的tyr-lh2对酪氨酸酶进行检测的反应机理图;
图2为实施例2制备的tyr-lh2在pbs缓冲溶液中,随酪氨酸酶浓度变化而变化的生物发光强度图;
图3为实施例2制备的tyr-lh2对不同类型细胞内酪氨酸酶检测成像的生物发光图。
具体实施方式
本发明通过下述实施例进行详细说明。但本领域技术人员了解,下述实施例不是对本发明保护范围的限制。任何在本发明基础上做出的改进和变化,都在本发明的保护范围之内。
实施例1
制备化合物(1)
在氩气保护下,将3-溴甲基苯酚(8.52mmol,1.6g),2-氰基-6-羟基苯并噻唑(2.84mmol,500mg),碳酸钾(5.67mmol,783mg)溶解于15ml乙腈中,于85℃反应5h。反应完成后,反应液过滤,用二氯甲烷萃取有机相,有机相旋干,粗产物用展开剂乙酸乙酯/石油醚过硅胶色谱柱,得到淡黄色固体化合物(1)(750mg,93%)。1hnmr(300mhz,dmso),δ:9.45(d,j=14.7hz,1h),8.16(d,j=9.1hz,1h),7.95(s,1h),7.39(d,j=9.1hz,1h),7.18(m,1h),6.87(t,j=10.6hz,2h),6.72(t,j=8.9hz,1h),5.14(m,2h).maldi-tof:m/zfound283.0539,calcd.283.0539for[m+h]+。
实施例2
制备化合物(2):tyr-lh2
在氩气保护下,将实施例1制备的化合物(1)(1.06mmol,300mg)溶解于5ml甲醇和二氯甲烷的混合溶剂(v/v=1:1)中,加入用5ml甲醇和去离子水的混合溶剂(v/v=1:1)溶解的d-半胱氨酸盐酸盐(1.06mmol,160mg)和碳酸钾(1.32mmol,183mg)溶液。常温下反应20min。反应结束后,将有机溶剂旋干,加入等体积水,用1m的盐酸溶液调整ph至2-3左右。得到的粗产物黄色固体。粗产物用甲醇重结晶后得到微黄色产物(268mg,65%)。1hnmr(300mhz,dmso),δ:8.06(d,j=9.0hz,1h),7.83(d,j=2.4hz,1h),7.37–7.23(m,1h),7.17(m,2h),7.06(d,j=8.0hz,1h),6.87(t,j=9.5hz,2h),6.72(t,j=7.9hz,1h),5.40(t,j=9.0hz,1h),5.16(d,j=13.5hz,2h),3.85–3.56(m,2h).maldi-tof:m/zfound387.0472,calcd.387.0472for[m+h]+。
实施例3
将实施例2中得到的化合物tyr-lh2针对不同浓度酪氨酸酶进行检测:用pbs缓冲溶液(含有10mm的mgso4)分别将tyr-lh2配制成浓度为60μm的溶液,将酪氨酸酶配制成浓度为15u/ml、30u/ml、60u/ml、150u/ml、300u/ml、450u/ml、600u/ml的溶液。然后将50ultyr-lh2溶液和50μl上述不同浓度的酪氨酸酶溶液分别加入到黑色96孔板的各个孔中,将板子放在37℃恒温摇床中,孵育3h,然后在各个孔中加入50μl含有2mmatp的萤光素酶溶液(60μg/ml)。将该96-孔板用活体成像仪测试生物发光强度。最后测得不同酪氨酸酶浓度(0、5u/ml、10u/ml、20u/ml、50u/ml、100u/ml、150u/ml、200u/ml)下tyr-lh2的生物发光光谱(见附图2),由图2中可以看出,随着酪氨酸酶浓度增加,溶液生物发光强度增强。
实施例4
将实施例2中得到的tyr-lh2用于不同类型的细胞成像:本实验分为三组,一组为酪氨酸酶过量表达的黑色素瘤细胞,作为实验组直接加入不同浓度的探针溶液(tyr-lh2溶液);第二组、第三组作为对照组用酪氨酸酶少量表达的细胞类型,同样加入不同浓度的探针溶液(tyr-lh2溶液)。三组细胞与探针溶液孵化1h后,用活体成像仪测试生物发光强度(见附图3)。由图3中可以明显看出黑色素瘤细胞与其他细胞中酪氨酸酶的含量有很明显的差异。
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!