含金属配位吡啶衍生物配体的共聚物核酸载体及制备方法和应用与流程
本发明属于基因治疗及新材料领域,具体涉及一种含金属配位吡啶衍生物配体的共聚物核酸载体的制备方法和应用。
背景技术
基因治疗通过将治疗功能核酸分子递送至患者特定细胞,实现治疗疾病的目的,为人类当前许多无法治愈的重大疾病,如,癌症、遗传性疾病(如,血友病)、感染性疾病(如,艾滋病和类风湿病等)和心血管疾病等的治愈带来了希望。成功实现基因治疗的关键是,如何构筑安全、高效的核酸递送系统,把治疗基因送达治疗部位并高效转染。目前,临床上主要采用病毒载体,虽然病毒载体展现出非常可观的转染效率,但其潜在的免疫原性限制了临床应用。相反,非病毒载体如,阳离子聚合物是最主要的一类非病毒基因载体,由于免疫原性弱,核酸装载能力强且易于结构改性等优点近年来得到较快速发展,然而,阳离子聚合物包裹核酸是带负电的核酸和过量的聚阳离子形成带有过剩正电荷的纳米核酸复合物粒子,如此带有过剩正电荷的纳米粒与带负电荷的血清蛋白或细胞膜组件,由于静电相互作用在体内循环中易聚集形成大颗粒而被网状内皮系统(res)迅速清除。此外,核酸复合物过量的正电荷还与持续的细胞毒性,炎症和细胞凋亡等存在正相关性。因此,基于上述有关聚阳离子基核酸复合物纳米粒的不良特性,从临床应用的角度,开发低电荷密度或非带电载体对于推动非病毒载体的临床应用具有重要意义。
技术实现要素:
本发明的目的是针对目前聚阳离子核酸载体存在的正电荷密度高,体内应用存在细胞毒性较大的问题,提供一种低电荷密度、多功能的含金属配位吡啶衍生物配体的共聚物核酸载体制备方法和应用。
本发明首先合成不同组成、结构的含吡啶衍生物配体的功能单体,利用可控自由基聚合方法(如,raft方法)合成出结构精细的含金属配位吡啶衍生物配体的共聚物非病毒核酸载体材料,最终展现出很高的转染效率,有望用于临床治疗。
本发明的技术方案:
一种含金属配位吡啶衍生物配体的共聚物核酸载体材料,由配位金属、配位单元、刺激响应单元构成的金属配体功能单体和其它具有亲水性功能单体以及疏水性的功能单体共聚,并金属配位而成,其中金属配体功能单体、亲水性功能单体以及疏水性的功能单体的共聚摩尔比为:1:(0.5‐8):(0.5‐10)。
所述配位金属为锌、钙、镁、铁、铝、铜、铕或钆;所述配位单元为含吡啶环类基团或多氮环类基团;所述刺激响应单元为含二硫键单体n,n'‐双(丙烯酰)胱胺(cba)、双(2‐甲基丙烯)乙氧基二硫(dsdma)或双(2‐丙烯)乙氧基二硫(dsda);所述的亲水性功能单体,是指侧基中含羟基、聚乙二醇链段或含糖链段的具有水溶性或强亲水性的甲基丙烯酸酯、丙烯酸酯、甲基丙烯酰胺和丙烯酰胺类单体;所述的疏水性功能单体,选择带有疏水侧基的甲基丙烯酸酯、丙烯酸酯、甲基丙烯酰胺和丙烯酰胺类单体。
一种所述含金属配位吡啶衍生物配体的共聚物核酸载体材料的制备方法,包括如下步骤:
将金属配体功能单体、亲水性功能单体和疏水性功能单体按摩尔比1:(0.5‐8):(0.5‐10)在二甲基甲酰胺中混合均匀,然后按金属配体功能单体比例为1加入摩尔比为0.06-0.08的引发剂偶氮二异丁腈aibn或4,4'‐偶氮双(4‐氰基戊酸)(acva)和摩尔比为0.1-0.4的链转移剂4‐氰基戊酸二硫代苯甲酸(cpadb);将混合物转移到玻璃封管中,用液氮处理3个冻‐融循环,以去除氧气;聚合反应在60‐80℃,持续4‐48小时,然后冰水浴冷却;在10倍体积反应混和液的乙醚:石油醚体积比v/v为1:2的溶液中沉淀三次,产品在真空下干燥,得含吡啶衍生物配体的共聚物;经与金属离子水合硝酸盐配位后得含金属配位吡啶衍生物配体的共聚物核酸载体。
1)将所制备的含金属配体功能单体和亲、疏水性功能单体在兼顾材料亲疏水平衡和配位作用的基础上整合起来,以4-氰基戊酸二硫代苯甲酸cpadb为链转移剂,偶氮二异丁腈aibn或4,4'-偶氮双(4-氰基戊酸)acva为引发剂,通过raft共聚合合成一系列分子量在3000-10000da,不同组成和链结构的两嵌段、多嵌段或无规共聚物。
2)将上述得到的共聚物与等摩尔的含配位金属的化合物室温下混合搅拌0.5‐12h,形成金属离子配体,得到含金属配位吡啶衍生物配体的共聚物核酸载体。
一种所述含金属配位吡啶衍生物配体的共聚物核酸载体的应用,主要用于非病毒基因载体,方法如下:将含金属配位吡啶衍生物配体的共聚物核酸载体与脱氧核糖核酸(dna)或核糖核酸(rna)等体积混合,室温下静置10‐30分钟,制得质量比5‐60:1的dna或rna复合物;制得的复合物用以转染不同类别细胞系。
本发明的优点是:
本发明通过可控聚合方式所制备出的含金属配位吡啶衍生物配体的共聚物核酸载体材料具备很强的dna结合能力和与细胞膜的作用力,所得的dna复合物内吞效率高;复合物进入细胞后,由于刺激响应,金属离子配体单元从共聚物主链上断开,dna得以释放、表达,展现出很高的转染效率,同时,由于共聚物体系中含阳离子数量少,共聚物与核酸复合物所带的正电荷密度低,复合物的细胞毒性低,因此,含金属配位吡啶衍生物配体的共聚物是一类具有很好临床应用潜力的新型低电荷密度非病毒基因载体材料。
附图说明
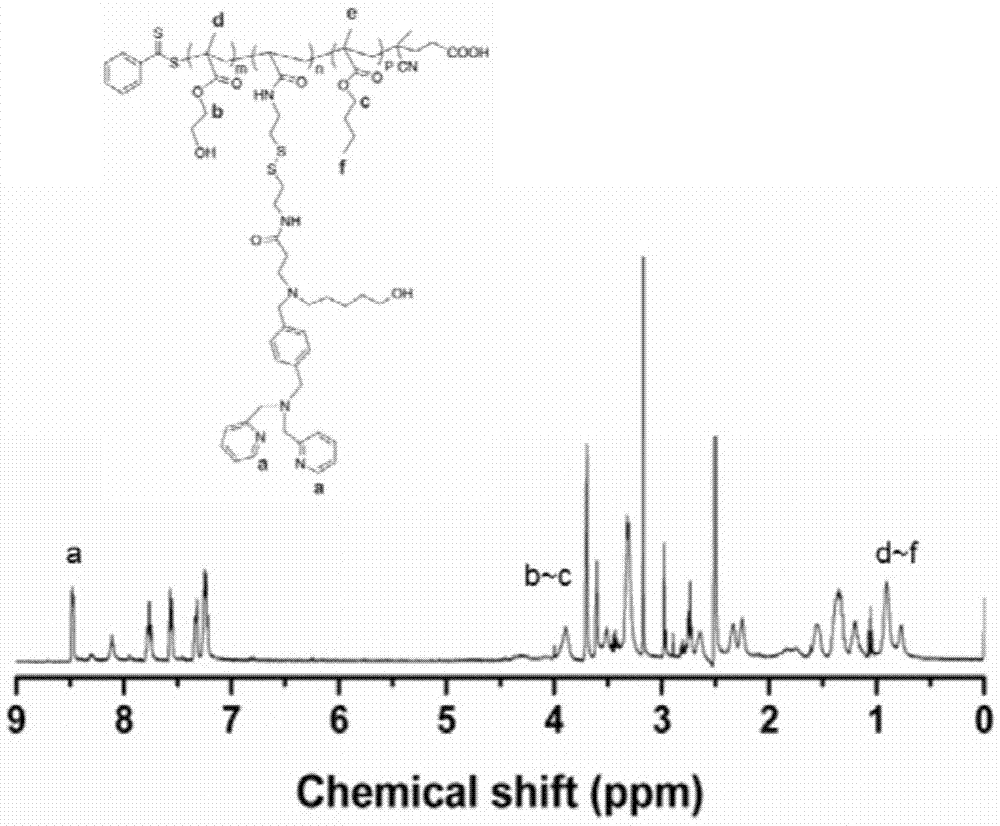
图1为zn‐hdb的400m核磁谱图。
图2为zn‐hdb/dna不同质量比条件下的体外293t细胞绿色荧光转染图。商业化试剂lipo2k以及pei25k按照各自的转染说明书进行转染。
具体实施方式
以下结合具体实施例对本发明方案作进一步说明但这些实施例仅用于说明本发明而不用于限制本发明的范围。有必要指出,本领域技术人员可以对本发明做各种修改或改动,这些等价形式同样落于本申请所附权利要求书所限定的范围。
实施例1:
一种含金属配位吡啶衍生物配体的共聚物核酸载体材料,由配位单元二甲基吡啶胺基团和刺激响应单元含二硫键单体n,n'‐双(丙烯酰)胱胺(cba)组成的含吡啶衍生物配体功能单体,与亲水性单体甲基丙烯酸羟乙酯(hema)和疏水性单体甲基丙烯酸正丁酯通过可控自由基聚合而成,配位金属为锌(zn)离子、锌配位的吡啶衍生物配体的共聚物核酸载体材料结构式示意如下:
以上结构式所示含金属配位吡啶衍生物配体的共聚物核酸载体材料的制备方法,包括如下步骤:
1)金属配体功能单体dpass的制备
将16mmol1,4‐对二氯苄(dx)溶解于20ml二氯甲烷中,加入8mmol二甲基吡啶胺(dpa)和40mmol无水碳酸钾,室温搅拌48h,旋蒸除去溶剂,产物用快速层析柱纯化,得到dxda;然后,取2.4mmoldxda溶于乙醇,加入10mmol5‐氨基‐1‐戊醇(ap)和12mmol无水碳酸钾,60℃反应过夜,产物在蒸馏水中沉淀,以二氯甲烷萃取,有机相用无水硫酸钠干燥,旋蒸除去有机相,得到dxda‐ap;再将0.75mmoldxda‐ap和1.5mmoln,n'‐双(丙烯酰)胱胺(cba)共同溶于甲醇,40℃反应48h,产物用快速层析柱纯化,得到金属配体功能单体dpass。
2)含金属配位吡啶衍生物配体的共聚物zn-hdb的制备
甲基丙烯酸羟乙酯(0.1mmol),dpass(0.1mmol),甲基丙烯酸正丁酯(0.4mmol)在二甲基甲酰胺中混合,然后加入引发剂acva(0.0067mmol)和链转移剂cpadb(0.02mmol)。将混合物转移到玻璃封管中,用液氮处理3个冻-融循环,以去除氧气。在70℃下聚合反应48小时,然后冰水冷却。在乙醚:石油醚(v/v,1:2)溶液中沉淀三次,真空干燥,得共聚物hdb。取等摩尔量的hdb和六水合硝酸锌混合溶于甲醇,40℃下搅拌24h,产物真空干燥得到zn-hdb。
图1为zn-hdb的核磁谱图。
实施例2:
一种含金属配位吡啶衍生物配体的共聚物核酸载体材料,由配位金属,配位单元、刺激响应单元组成的含吡啶衍生物配体功能单体,亲水性单体和疏水性单体构成,所述配位金属为镁(mg),配位单元为二甲基吡啶胺基团,刺激响应单元为含二硫键单体双(2‐丙烯)乙氧基二硫(dsda);亲水单体为甲基丙烯酸羟乙酯;疏水单体为异丙基丙烯酰胺。
一种所述含金属配位吡啶衍生物配体的共聚物载体mg‐hdn的制备方法,包括如下步骤:
1)金属配体的功能单体ddad的制备
将20mmol1,4‐对二氯苄(dx)溶解于20ml二氯甲烷中,加入10mmol二甲基吡啶胺(dpa)和45mmol无水碳酸钾,室温搅拌24h,旋蒸除去溶剂,产物用快速层析柱纯化,得到dxda;然后,取3.0mmoldxda溶于乙醇,加入12mmol5‐氨基‐1‐戊醇(ap)和12mmol无水碳酸钾,65℃反应过夜,产物在蒸馏水中沉淀,以二氯甲烷萃取,有机相用无水硫酸钠干燥,旋蒸除去有机相,得到dxda‐ap;再将0.9mmoldxda‐ap和1.8mmol双(2‐丙烯)乙氧基二硫(dsda)共同溶于甲醇,40℃反应24h,产物用快速层析柱纯化,得到金属配体功能单体ddad;
2)含金属配位吡啶衍生物配体的共聚物mg-hdn的制备
甲基丙烯酸羟乙酯(0.2mmol),ddad(0.1mmol),n-异丙基丙烯酰胺(0.6mmol)在二甲基甲酰胺中混合,然后加入引发剂acva(0.0067mmol)和链转移剂cpadb(0.03mmol)。将混合物转移到玻璃封管中,用液氮处理3个冻-融循环,以去除氧气。聚合在70℃反应48小时,然后用冰水冷却,在乙醚:石油醚(v/v,1:2)溶液中沉淀三次,产品在真空下干燥,得hdn。之后,hdn与mg(no3)2·6h2o进行配位,得mg-hdn,mg(no3)2·6h2o的用量为每一聚合物中ddad残留量。
实施例3:
所制备的含金属配位吡啶衍生物配体的共聚物的应用,用于核酸载体,向细胞中传递脱氧核糖核酸(dna),方法如下:将实施例1制备的含金属配位吡啶衍生物配体的共聚物zn-hdb与dna等体积混合,室温下静置15分钟,制得质量比分别为20、40和60:1的dna复合物;制得的复合物用以转染不同细胞系,方法如下:
细胞转染步骤
1)dna复合物的制备:
所用dna为绿色荧光蛋白质粒pcmv‐gfp和荧光素酶质粒pcmv‐gluc。将实施例1制备的含金属配位吡啶衍生物配体的共聚物zn-hdb与dna分别溶于ph5.2的醋酸盐缓冲液,等体积混合,室温静置15分钟,可得dna复合物纳米粒子。
2)体外细胞转染实验:
将人胚肾细胞系293t以每孔5×104的细胞数种入24孔培养板,培育24小时,加入上述的dna复合物纳米粒子,dna的用量为1μg/孔,继续培育48h;当用绿色荧光蛋白质粒pcmv‐gfp转染时,以倒置荧光显微镜观察转染情况,当用荧光素酶质粒pcmv‐gluc转染时,以bioluxtm荧光素酶检测试剂盒评估转染效率。
图2为实施例1制备的含金属配位吡啶衍生物配体的共聚物zn-hdb和商业化转染试剂lipo2k以及pei25k在293t细胞中的gfp转染图片。图中表明:实施例1制备的含金属配位吡啶衍生物配体的共聚物zn-hdb的转染效率与商业化转染试剂lipo2k和pei25k相当。
3)体外细胞毒性实验:
●将人胚肾细胞系(293t)、人结肠癌细胞(hct116)、人宫颈癌细胞(hela)和鼠结肠癌细胞(ct26)分别以每孔1×104的细胞数种入96孔培养板,培育24小时,加入zn‐hdb/dna复合物纳米粒子,dna的用量为0.25μg/孔,继续培育48h,加入3‐(4,5‐二甲基噻唑‐2)‐2,5‐二苯基四氮唑溴盐(mtt),检测细胞毒性。
本发明制备的含金属配位吡啶衍生物配体的共聚物核酸载体zn‐hdb,在常规细胞系(293t)和多种肿瘤细胞中均具有很高的转染效率,此外,zn‐hdb核酸载体在上述细胞中均表现出优越的低细胞毒性。
实施例4:
所制备的含金属配位吡啶衍生物配体的共聚物的应用,主要用于非病毒基因载体,向细胞中传递核糖核酸(rna),方法如下:将上述实施例2制备的含金属配位吡啶衍生物配体的共聚物mg-hdn与rna等体积混合,室温下静置20分钟,制得质量比分别为10、20、40和60:1的dna复合物;制得的复合物具有很高的细胞转染效率以及低细胞毒性,方法如下:
细胞转染步骤
1)rna复合物的制备:
所用rna为萤火虫荧光素酶沉默基因siluc。将上述实施例2制备的含金属配位吡啶衍生物配体的共聚物mg-hdn与rna分别溶于ph5.2的醋酸盐缓冲液,等体积混合,室温静置15分钟,可得rna复合物纳米粒子。
2)体外细胞转染实验:
将稳定表达萤火虫荧光素酶(firefly‐luciferase)基因的人结肠癌细胞(hct116)、人宫颈癌细胞(hela)分别以每孔1×104的细胞数种入96孔培养板,培育24小时,加入上述的含金属配位吡啶衍生物配体的共聚物mg-hdn/rna复合物纳米粒子,rna的用量为5pmol/孔,继续培育24h,以萤火虫荧光素酶检测试剂盒检测rna干扰效率。
3)体外细胞毒性实验:
将稳定表达萤火虫荧光素酶(firefly‐luciferase)基因的人结肠癌细胞(hct116)、人宫颈癌细胞(hela)分别以每孔1×104的细胞数种入96孔培养板,培育24小时,加入含金属配位吡啶衍生物配体的共聚物mg-hdn/rna复合物纳米粒子,rna的用量为5pmol/孔,继续培育24h,加入3‐(4,5‐二甲基噻唑‐2)‐2,5‐二苯基四氮唑溴盐(mtt),检测细胞毒性。
本发明制备的含金属配位吡啶衍生物配体的共聚物mg-hdn核酸载体,在人结肠癌细胞(hct116)、人宫颈癌细胞(hela)中展现出很高的rna干扰效率,并且细胞毒性很低。
- 还没有人留言评论。精彩留言会获得点赞!