一株吉氏库特菌及其在拆分1-苯基-1,2-乙二醇中的应用的制作方法
本发明属于生物化工领域,特别涉及一株吉氏库特菌及其在拆分1-苯基-1,2-乙二醇中的应用。
背景技术:
手性邻位二醇是有机合成中极为重要的手性合成子,可进一步转化为许多具有生物活性的化合物,因而在医药、农药、化妆品等行业具有非常广阔的应用前景。(r)-1,2-苯基乙二醇是光学活性药物β-肾上腺素阻断剂(r-硝基心定,抗心律失常药)等的重要合成子;(r)-4-氯苯基乙二醇是合成神经保护药物eliprodil(依利罗地)的关键性手性合成子;(s)-苯乙二醇可以作为液晶材料的手性添加剂,用于缩短液晶面板的响应时间。
用于制备手性1,2-苯基乙二醇的生物法主要包括:环氧化物水解酶水解环氧化物,羰基还原酶还原相应的酮和醇脱氢酶或脂肪酶拆分外消旋的对映体。
在上述主要方法中,应用全细胞动力学拆分外消旋的1-苯基-1,2-乙二醇已经被报道。然而普遍存在反应底物的浓度底的缺点。
技术实现要素:
本发明的首要目的在于克服现有技术的缺点与不足,提供一株吉氏库特菌。
本发明的另一目的在于提供所述吉氏库特菌在拆分1-苯基-1,2-乙二醇中的应用。
本发明的目的通过下述技术方案实现:一株吉氏库特菌,名称为吉氏库特菌(kurthiagibsonii)sc0312,保藏号为cctccno:m2017157,该菌株于2017年3月31日保藏于中国武汉武汉大学的中国典型培养物保藏中心(cctcc)。
所述的吉氏库特菌的16srdna序列如下(seqidno.1)所示:
gaaatgcggcagctataatgcaagtcgagcgaatgacgagaagcttgcttctctgatttagcggcggacgggtgagtaacacgtgggcaacctgccctacagatcgggataactcagggaaacctgggctaataccggataatccttcgaatcacatgttttgaagttgaaaggcgcttcggcgtcactgtaggatgggcccgcggtgcattagctagttggtggggtaacggcctaccaaggcaacgatgcatagccgacctgagagggtgatcggccacattgggactgagacacggcccaaactcctacgggaggcagcagtagggaatcttccacaatggacgaaagtctgatggagcaacgccgcgtgagtgatgaaggttttcggatcgtaaaactctgttgtaagggaagaacaagtacgttaggaaatgaacgtaccttgacggtaccttattagaaagccacggctaactacgtgccagcagccgcggtaatacgtaggtggcaagcgttgtccggatttattgggcgtaaagcgcgcgcaggtggtttcttaagtctgatgtgaaagcccacggctcaaccgtggagggtcattggaaactggggaacttgagtgcagaagaggatagtggaattccaagtgtagcggtgaaatgcgtagagatttggaggaacaccagtggcgaaggcgactgtctggtctgtaactgacactgaggcgcgaaagcgtggggagcaaacaggattagataccctggtagtccacgccgtaaaacgatgagtgctaagtgttagggggtttccgccccttagtgctgcagctaacgcattaagcactcccgcctggggagtacgaccgcaaggttgaaactcaaaggaattgacgggggccccgcacaagccggtggagcatgttgtttaattcgaagcacgcgaagaaccttaccaggtcttgacatcccaatgaccgttctagagataggattttccccttcggggacattggtggacaggtggtg。
一种培养所述的吉氏库特菌的方法,具体步骤为:将吉氏库特菌接种于种子培养基中进行培养,再转接到发酵培养基中进行扩增培养。
所述的种子培养基的组成如下:蛋白胨5~10g,酵母粉3~10g,氯化钠5~10g,加蒸馏水至1l,ph6.0~7.0。
所述的发酵培养基的组成如下:蛋白胨5~10g,酵母粉3~10g,氯化钠5~10g,加蒸馏水至1l,ph6.0~7.0。
所述的种子培养基中培养的条件为:在30~37℃条件下培养10~12h;优选为:在转速150~180rpm、30~37℃条件下培养10~12h。
所述的扩增培养的条件为:在30~37℃条件下培养12~16h;优选为:在转速150~180rpm、30~37℃条件下培养12~16h。
所述的吉氏库特菌在催化合成光学手性化合物中的应用。
所述的吉氏库特菌在拆分1-苯基-1,2-乙二醇中的应用,该菌株可用于拆分外消旋的1-苯基-1,2-乙二醇制备对映体(s)-1,2-苯基乙二醇。
所述的吉氏库特菌在拆分1-苯基-1,2-乙二醇中的应用,通过如下步骤实现:
(1)将吉氏库特菌进行扩增培养,然后在4℃条件下离心,得到静息细胞;
(2)将静息细胞悬浮于磷酸盐缓冲液中,然后加入底物1-苯基-1,2-乙二醇进行催化反应,得到(s)-1,2-苯基乙二醇。
步骤(1)中所述的扩增培养优选为通过如下步骤实现:将吉氏库特菌接种于种子培养基中进行培养,然后将其转接到发酵培养基中进行扩增培养。
所述的种子培养基或发酵培养基的组成如下:蛋白胨5~10g,酵母粉3~10g,氯化钠5~10g,加蒸馏水至1l,ph6.0~7.0。
所述的种子培养基中培养的条件为:在30~37℃条件下培养10~12h;优选为:在转速150~180rpm、30~37℃条件下培养10~12h。
所述的扩增培养的条件为:在30~37℃条件下培养12~16h;优选为:在转速150~180rpm、30~37℃条件下培养12~16h。
步骤(2)中所述的反应体系中1-苯基-1,2-乙二醇的终浓度为20~80mm,吉氏库特菌添加量以湿重计为15~30mg/ml。
步骤(2)中所述的磷酸盐缓冲液为ph5.0~8.5的磷酸缓冲液;优选为ph6.0~7.0的磷酸缓冲液(100mm)。
所述的吉氏库特菌在拆分1-苯基-1,2-乙二醇中的应用,还包括在步骤(2)中的反应体系中加入丙酮的步骤。
所述的丙酮的添加量按其在反应体系中终浓度为20~90mm添加;优选为按其在反应体系中终浓度为20~30mm添加。
步骤(2)中所述的催化反应的条件为:在25~45℃条件下催化5~22h;优选为:在转速150~180rpm、25~45℃条件下催化11~22h。
所述的吉氏库特菌在医药、农药、化妆品、液晶材料等领域中的应用。
本发明相对于现有技术具有如下的优点及效果:
(1)本发明提供的吉氏库特菌(kurthiagibsoniisc0312)催化选择性高,产物产率高,转化操作简单,安全,成本低廉,环境友好。
(2)采用本发明的吉氏库特氏菌拆分外消旋的1-苯基-1,2-乙二醇制备s型的1,2-苯基乙二醇,(s)-1,2-苯基乙二醇的得率为44~49%,光学纯度为93~100%。
(3)采用本发明的吉氏库特氏菌菌株催化合成光学纯手性化合物,不仅具有较好的催化效果,所生成的产物光学纯度较高,而且催化剂容易制备、反应条件温和,具有较好的应用开发前景。
附图说明
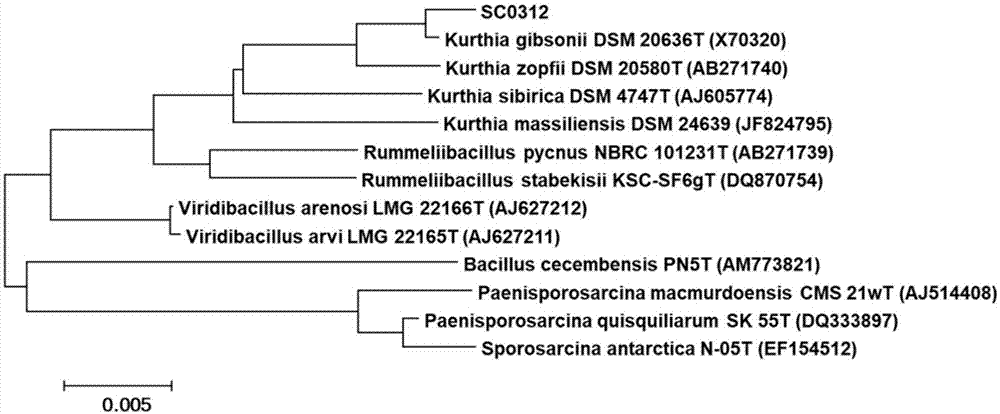
图1是本发明吉氏库特菌(kurthiagibsonii)sc0312的系统发育树图。
图2是本发明实施例2中吉氏库特菌(kurthiagibsonii)sc0312的生长过程中的od值的变化,以及其在12h,16h,20h,24h氧化生成2-羟基苯乙酮的结果图(图中“v”表示单位菌体催化剂催化生成2-羟基苯乙酮的速率)。
具体实施方式
下面结合实施例对本发明作进一步详细的描述,但本发明的实施方式不限于此。以下实施例中除特别说明外,均为本领域内的常规实验方法和操作步骤。
本发明中涉及的种子培养基和发酵培养基组成均如下:蛋白胨5~10g,酵母粉3~10g,氯化钠5~10g,加蒸馏水至1l,ph6.0~7.0。121℃灭菌20min。
实施例1吉氏库特菌(kurthiagibsonii)sc0312的分子生物学水平的鉴定
本发明的吉氏库特菌(kurthiagibsonii)sc0312是从广州本地长期被油浸泡的土壤中筛选而得。其中,菌株系统发育树如图1所示,其16srdna基因序列测定结果如下:
gaaatgcggcagctataatgcaagtcgagcgaatgacgagaagcttgcttctctgatttagcggcggacgggtgagtaacacgtgggcaacctgccctacagatcgggataactcagggaaacctgggctaataccggataatccttcgaatcacatgttttgaagttgaaaggcgcttcggcgtcactgtaggatgggcccgcggtgcattagctagttggtggggtaacggcctaccaaggcaacgatgcatagccgacctgagagggtgatcggccacattgggactgagacacggcccaaactcctacgggaggcagcagtagggaatcttccacaatggacgaaagtctgatggagcaacgccgcgtgagtgatgaaggttttcggatcgtaaaactctgttgtaagggaagaacaagtacgttaggaaatgaacgtaccttgacggtaccttattagaaagccacggctaactacgtgccagcagccgcggtaatacgtaggtggcaagcgttgtccggatttattgggcgtaaagcgcgcgcaggtggtttcttaagtctgatgtgaaagcccacggctcaaccgtggagggtcattggaaactggggaacttgagtgcagaagaggatagtggaattccaagtgtagcggtgaaatgcgtagagatttggaggaacaccagtggcgaaggcgactgtctggtctgtaactgacactgaggcgcgaaagcgtggggagcaaacaggattagataccctggtagtccacgccgtaaaacgatgagtgctaagtgttagggggtttccgccccttagtgctgcagctaacgcattaagcactcccgcctggggagtacgaccgcaaggttgaaactcaaaggaattgacgggggccccgcacaagccggtggagcatgttgtttaattcgaagcacgcgaagaaccttaccaggtcttgacatcccaatgaccgttctagagataggattttccccttcggggacattggtggacaggtggtg。
将16srrna基因序列进行blast结果分析,得到与kurthiagibsonii同源性达到99%。根据分子生物学鉴定结果,将菌株鉴定为吉氏库特菌(kurthiagibsonii,简称k.gibsonii),并命名为吉氏库特菌(kurthiagibsonii)sc0312。该菌株已保存于中国典型培养物保藏中心(cctcc),保藏号为cctccno:m2017157,保藏日期为2017年3月31日,保藏地址为中国武汉武汉大学。
实施例2吉氏库特菌(k.gibsonii)sc0312培养过程曲线及催化活力变化
(1)将保存在甘油管中的菌种按0.1%(v/v)接种于50ml的种子培养基中,180rpm、37℃培养12h后,按0.1%(v/v)的比例接种于100ml的发酵培养基中,180rpm、37℃培养0~32h。监测菌种生长过程中的od(600nm)的变化(每隔4个小时测量一次)。结果如图2所示。
(2)分别将步骤(1)中在发酵培养基中培养了12h,16h,20h,24h的菌在4℃条件下离心,收集菌体得到静息细胞,然后将收获的静息细胞分别重新悬浮于磷酸盐缓冲液(100mm,ph6.5)中,加入外消旋的1-苯基-1,2-乙二醇(底物1-苯基-1,2-乙二醇终浓度为20mm),其中湿菌体终浓度为30mg/ml,催化条件为温度为35℃,摇床培养箱转速为180rpm。催化30min取样,监测其氧化生成2-羟基苯乙酮的活力。催化活力的定义为单位菌体(mg)每分钟生成2-羟基苯乙酮的量(umol)。其中2-羟基苯乙酮为是拆分1-苯基-1,2-乙二醇时产生的一个产物,用它的生成速度来评价活性的大小。结果如图2所示,培养12~16h的菌的催化活力最佳。
(3)催化30min取样,分析(s)-1,2-苯基乙二醇(ped)的得率。使用反相高效液相色谱分析2-羟基苯乙酮的浓度,流动相为乙腈与水(含0.1%(v/v)三氟乙酸)=2:3(体积比),流速为0.5ml/min,色谱柱:watersxbridgec18,4.6mm×250mm,波长245nm。
实施例3吉氏库特菌(k.gibsonii)sc0312制备(s)-ped
(1)将保存在甘油管中的菌种按0.1%(v/v)接种于50ml的种子培养基中,180rpm、37℃培养12h后,按0.1%(v/v)的比例接种于100ml的发酵培养基中,180rpm、37℃培养16h。
(2)4℃下离心收集菌体,再重新悬浮于磷酸盐缓冲液中,加入1-苯基-1,2-乙二醇进行催化反应,其催化体系反应介质为磷酸盐缓冲液(100mm,ph5),底物1-苯基-1,2-乙二醇终浓度为20mm,湿菌体终浓度为30mg/ml,丙酮终浓度30mm。催化条件为温度为45℃,摇床培养箱转速为180rpm。催化11h后取样,分析(s)-1,2-苯基乙二醇(ped)的得率和对映体过量率。
(3)使用反相高效液相色谱分析(s)-ped的浓度,流动相为乙腈:水(含0.1%(v/v)三氟乙酸)=2:3(体积比),流速为0.5ml/min,色谱柱:watersxbridgec18,4.6mm×250mm,波长215nm。使用正相高效液相色谱分析(s)-ped的过量率,流动相为正己烷:异丙醇=9:1(体积比),流速为0.7ml/min,色谱柱为:ob-h,4.6mm×150mm,波长215nm。
催化结束后,(s)-ped的产率为44%,对映体过量率为100%。
实施例4吉氏库特菌(k.gibsonii)sc0312制备(s)-ped
(1)将保存在甘油管中的菌种按0.1%(v/v)接种于50ml的种子培养基中,180rpm、35℃培养10h后,按0.1%(v/v)的比例接种于100ml的发酵培养基中,180rpm、35℃培养14h。
(2)4℃下离心收集菌体,再重新悬浮于磷酸盐缓冲液中,加入1-苯基-1,2-乙二醇进行催化反应,其催化体系反应介质磷酸盐缓冲液(100mm,ph6),底物1-苯基-1,2-乙二醇终浓度为50mm,湿菌体终浓度为30mg/ml,丙酮终浓度20mm。催化条件为温度为25℃,摇床培养箱转速为180rpm。催化22h后取样,分析(s)-1,2-苯基乙二醇的得率和对映体过量率。
(3)使用反相高效液相色谱分析(s)-ped的浓度,流动相为乙腈:水(含0.1%(v/v)三氟乙酸)=2:3(体积比),流速为0.5ml/min,色谱柱:watersxbridgec18,4.6mm×250mm,波长215nm。使用正相高效液相色谱分析(s)-ped的过量率,流动相为正己烷:异丙醇=9:1(体积比),流速为0.7ml/min,色谱柱为:ob-h,4.6mm×150mm,波长215nm。
催化结束后,(s)-ped的产率为47%,对映体过量率为93%。
实施例5不同吉氏库特菌(k.gibsonii)sc0312菌体添加量制备(s)-ped
(1)将保存在甘油管中的菌种按0.1%(v/v)接种于50ml的种子培养基中,160rpm、30℃培养12h后,按0.1%(v/v)的比例接种于100ml的发酵培养基中,160rpm、30℃培养12h。
(2)4℃下离心收集菌体。催化体系反应介质磷酸盐缓冲液(100mm,ph8.5),底物1-苯基-1,2-乙二醇终浓度为20mm,湿菌体终浓度为15mg/ml,丙酮终浓度90mm。催化条件为温度为30℃,摇床培养箱转速为160rpm。催化5h后取样,分析(s)-1,2-苯基乙二醇(ped)的得率和对映体过量率。
(3)使用反相高效液相色谱分析(s)-ped的浓度,流动相为乙腈:水(含0.1%(v/v)三氟乙酸)=2:3(体积比),流速为0.5ml/min,色谱柱:watersxbridgec18,4.6mm×250mm,波长215nm。使用正相高效液相色谱分析(s)-ped的过量率,流动相为正己烷:异丙醇=9:1(体积比),流速为0.7ml/min,色谱柱为:ob-h,4.6mm×150mm,波长215nm。
催化结束后,(s)-ped的产率为49%,对映体过量率为98%。
实施例6吉氏库特菌(k.gibsonii)sc0312在不同底物浓度下制备(s)-ped
(1)将保存在甘油管中的菌种按0.1%(v/v)接种于50ml的种子培养基中,180rpm、35℃培养10h后,按0.1%(v/v)的比例接种于100ml的发酵培养基中,180rpm、35℃培养15h。
(2)4℃下离心收集菌体。催化体系反应介质磷酸盐缓冲液(100mm,ph8),底物1-苯基-1,2-乙二醇终浓度为80mm,湿菌体终浓度为20mg/ml,丙酮终浓度60mm。催化条件为温度为37℃,摇床培养箱转速为180rpm。催化15h后取样,分析(s)-1,2-苯基乙二醇(ped)的得率和对映体过量率。
(3)使用反相高效液相色谱分析(s)-ped的浓度,流动相为乙腈:水(含0.1%(v/v)三氟乙酸)=2:3(体积比),流速为0.5ml/min,色谱柱:watersxbridgec18,4.6mm×250mm,波长215nm。使用正相高效液相色谱分析(s)-ped的过量率,流动相为正己烷:异丙醇=9:1(体积比),流速为0.7ml/min,色谱柱为:ob-h,4.6mm×150mm,波长215nm。
催化结束后,(s)-ped的产率为47%,对映体过量率为94%。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
序列表
<110>华南理工大学
<120>一株吉氏库特菌及其在拆分1-苯基-1,2-乙二醇中的应用
<160>1
<170>siposequencelisting1.0
<210>1
<211>1028
<212>dna
<213>kurthiagibsonii
<220>
<223>吉氏库特菌(kurthiagibsonii)sc0312
<400>1
gaaatgcggcagctataatgcaagtcgagcgaatgacgagaagcttgcttctctgattta60
gcggcggacgggtgagtaacacgtgggcaacctgccctacagatcgggataactcaggga120
aacctgggctaataccggataatccttcgaatcacatgttttgaagttgaaaggcgcttc180
ggcgtcactgtaggatgggcccgcggtgcattagctagttggtggggtaacggcctacca240
aggcaacgatgcatagccgacctgagagggtgatcggccacattgggactgagacacggc300
ccaaactcctacgggaggcagcagtagggaatcttccacaatggacgaaagtctgatgga360
gcaacgccgcgtgagtgatgaaggttttcggatcgtaaaactctgttgtaagggaagaac420
aagtacgttaggaaatgaacgtaccttgacggtaccttattagaaagccacggctaacta480
cgtgccagcagccgcggtaatacgtaggtggcaagcgttgtccggatttattgggcgtaa540
agcgcgcgcaggtggtttcttaagtctgatgtgaaagcccacggctcaaccgtggagggt600
cattggaaactggggaacttgagtgcagaagaggatagtggaattccaagtgtagcggtg660
aaatgcgtagagatttggaggaacaccagtggcgaaggcgactgtctggtctgtaactga720
cactgaggcgcgaaagcgtggggagcaaacaggattagataccctggtagtccacgccgt780
aaaacgatgagtgctaagtgttagggggtttccgccccttagtgctgcagctaacgcatt840
aagcactcccgcctggggagtacgaccgcaaggttgaaactcaaaggaattgacgggggc900
cccgcacaagccggtggagcatgttgtttaattcgaagcacgcgaagaaccttaccaggt960
cttgacatcccaatgaccgttctagagataggattttccccttcggggacattggtggac1020
aggtggtg1028
- 还没有人留言评论。精彩留言会获得点赞!