一种微生物还原二氧化碳产甲烷的方法与流程
本发明涉及co2资源化利用领域,尤其涉及一种促进微生物利用电能将co2转化为甲烷的方法。
背景技术
自工业革命以来,人类的生产活动显著的增加了大气中co2的含量。co2作为主要的温室效应气体之一,其在大气中含量的增长可能导致全球变暖和气候极端事件增加。如何减少大气中co2的含量,甚至将其转化为高附加值的化学品成为一个全球研究的热点。常见的转化方法包含化学转化和生物转化。化学法往往需要高温高压和催化剂,与之相比,生物转化可以在室温常压条件下发生,反应条件温和,有着广阔的应用前景。
利用微生物将co2转化为甲烷已有广泛的研究和报道。专利号为cn102925492a的专利在阴极室中接种污泥富集得到的微生物,利用电流还原co2产甲烷的同时还可以产乙酸。但是其开始产甲烷(-850mv到-950mv,vsag/agcl)的电势偏高,能量消耗较大;在产甲烷的过程中同时生成副产物乙酸,降低了产甲烷的效率,增加了产物分离难度。
对此,我们提供了一种新的生物阴极,能在较低电势下,将co2高效低成本地转化为ch4。利用硝酸-醋酸混合纤维薄膜的高比表面积和多孔性,以及碳纳米管的优良导电性制成工作电极。将其放置在阴极池中,产甲烷八叠球菌能够附着在工作电极上,当在阴极施加电势时,产甲烷菌能够将高效较快地将co2转化为甲烷。
技术实现要素:
本发明的目的就是为了克服上述现有技术存在的缺陷而提供一种微生物还原二氧化碳产甲烷的方法。
本发明的目的可以通过以下技术方案来实现:一种微生物还原二氧化碳产甲烷的方法,其特征在于,包括以下步骤:
1)构建包含阴极池和阳极池的微生物电解池,阴极池中包含电解液,工作电极(阴极),参比电极和产甲烷菌;阳极池包括电解液和铂对电极;阴极池和阳极池之间用n117质子交换膜隔开;
2)阴极池和阳极池中加入产甲烷菌培养基;
3)阴极池中接种3ml产甲烷菌菌液,培养;
4)阴极池加载-0.6v(vsshe)电压;
5)由阴极池顶空收获甲烷。
步骤(1)所述的工作电极由黏附多壁碳纳米管的硝酸—醋酸混合纤维薄膜制成。所述的硝酸—醋酸混合纤维薄膜上黏附着多壁碳纳米管量为0.1~10mg/cm2,多壁碳纳米管长度为0.5~50μm;硝酸—醋酸混合纤维薄膜孔径0.2~2μm。
工作电极的制备方法包括以下步骤:首先,将长度为0.5~50μm多壁碳纳米管用5%双氧水浸泡震荡1h,干燥后溶解在0.5~20%的nafion乙醇溶液中,超声处理1~60min使多壁碳纳米管均匀分散,制成多壁碳纳米管nafion乙醇溶液,然后将其均匀涂在孔径为0.2~2μm硝酸醋酸混合纤维薄膜上,在20~65℃的环境中烘干。使硝酸-醋酸混合纤维薄膜的多壁碳纳米管负载量为0.1~10mg/cm2。将载有多壁碳纳米管的硝酸-醋酸混合纤维薄膜放置在阴极池中,并且与铂丝链接形成工作电极。
将池体、工作电极、参比电极、对电极等组装成电解池。在电解池阴极池和阳极池均通入50ml产甲烷菌常用培养基。
步骤(2)所述的产甲烷菌培养基的配方如下:0.35g/lk2hpo4,0.23g/lkh2po4,0.5g/lnh4cl,0.5g/lmgso4·7h2o,0.25g/lcacl2,2.25g/lnacl,0.85g/lnahco3,0.5g/lna2s·h2o,10ml/l微量元素溶液,1ml/l维生素溶液;电解池顶空为co2:n2=1:4(n/n)的混合气;
所述的微量元素溶液配方如下:1500mg/lfecl2·4h2o,70mg/lzncl2,100mg/lmncl2·4h2o,6mg/lhbo3,190mg/lcocl2·6h2o,2mg/lcucl2·h2o,24mg/lnicl2·6h2o,36mg/lnamo4·2h2o,hcl(25%)10ml/l;
所述的维生素溶液配方如下:2mg/l生物素,2mg/l叶酸,10mg/l维生素b6,5mg/l维生素b1,5mg/l维生素b2,5mg/l烟碱酸,5mg/l泛酸,0.1mg/l维生素b12,5mg/l氨基苯甲酸,5mg/l硫辛酸。
步骤(3)所述的产甲烷菌为包括但不限于巴氏产甲烷菌(methanosarcinabarkeri),布氏产甲烷菌(methanobacteriumbyrantti)以及亨氏产甲烷菌(methanospirllumhungatei)。
步骤(3)所述的产甲烷菌在室温下培养。
在阴极池中接入1.5~5.0%产甲烷菌菌液。为避免生成其他产物,该菌液应由产甲烷菌单菌组成。在阴极施加-0.6v电势(vsshe)启动反应,用气相色谱仪检测顶空气体中甲烷含量。
与现有技术相比,本发明工作电极由负载多壁碳纳米管的硝酸—醋酸混合纤维薄膜组成,该纤维薄膜水平放置在阴极池底部。同时在阴极池接种产甲烷菌,即可在较低负电势下利用微生物将co2还原为甲烷。本发明提供一种无需化学催化剂、清洁高效、低成本的将co2生物还原为甲烷方法,并且无其他副产物,有着广阔的应用前景。
附图说明
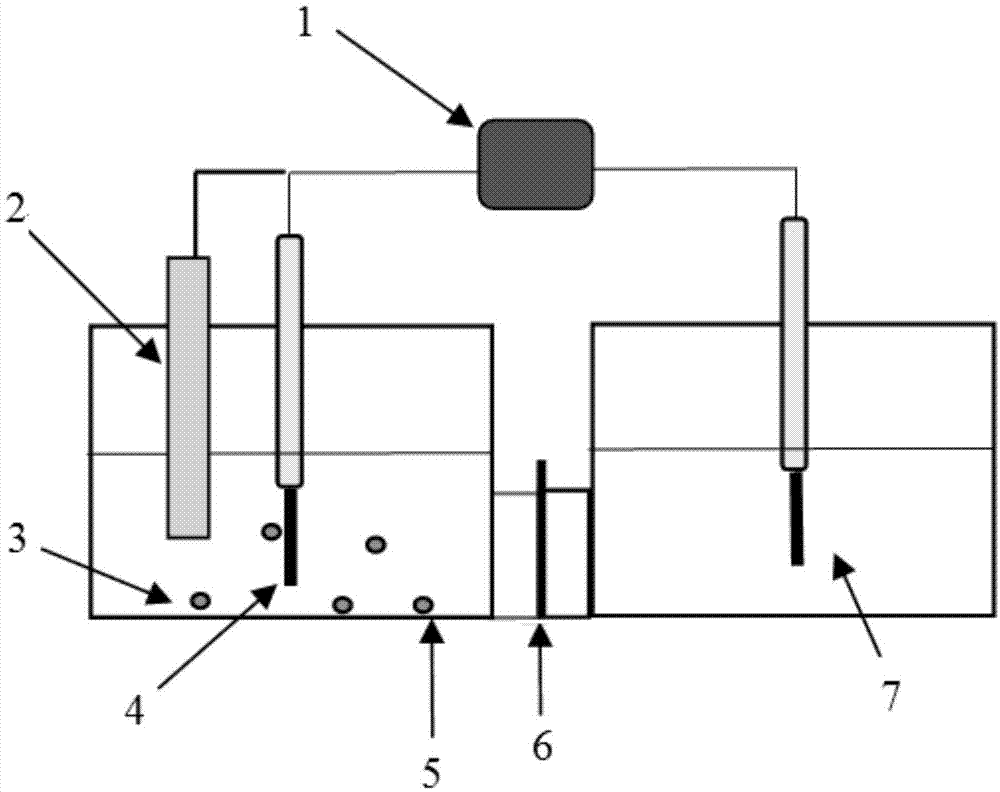
图1为本发明微生物电解池的结构水体
具体实施方式
下面结合附图和具体实施例对本发明进行详细说明。
实施例1:
该实施例分为实验组a以及对照组b,c同时进行:
实验组a如图1所示(实施例二、三同)。微生物电解池包括阴极池和阳极池,其中阴极池内设有参比电极2,阴极4、产甲烷菌3和培养基5,阳极池内设有对电极7,阴极池和阳极池之间设有质子交换膜6,还设有电源1分别连接参比电极2,阴极4和对电极7。在本实施例中产甲烷菌3为巴氏产甲烷菌菌液(methanosarsinabarkeri)。参比电极2为ag/agcl电极,阴极4由黏附多壁碳纳米管的硝酸—醋酸混合纤维薄膜制成。对电极7为铂对电极。
培养基5的配方如下:0.35g/lk2hpo4,0.23g/lkh2po4,0.5g/lnh4cl,0.5g/lmgso4·7h2o,0.25g/lcacl2,2.25g/lnacl,0.85g/lnahco3,0.5g/lna2s·h2o,10ml/l微量元素溶液,1ml/l维生素溶液;电解池顶空为co2:n2=1:4(n/n)的混合气;所述的微量元素溶液配方如下:1500mg/lfecl2·4h2o,70mg/lzncl2,100mg/lmncl2·4h2o,6mg/lhbo3,190mg/lcocl2·6h2o,2mg/lcucl2·h2o,24mg/lnicl2·6h2o,nicl2mg/lnamo4·2h2o,hcl(25%)10ml/l;所述的维生素溶液配方如下:2mg/l生物素,2mg/l叶酸,10mg/l维生素b6,5mg/l维生素b1,5mg/l维生素b2,5mg/l烟碱酸,5mg/l泛酸,0.1mg/l维生素b12,5mg/l氨基苯甲酸,5mg/l硫辛酸。
采用上述装置还原co2为甲烷的方法如下:
在阴极池中接入1.5ml(1.5%)的巴氏产甲烷菌菌液(methanosarsinabarkeri),顶空充满co2和n2混合气(1:4)。工作电极(即阴极4)采用附着多壁碳纳米管的硝酸-醋酸混合纤维薄膜制成。首先,将长度为50μm多壁碳纳米管用5%双氧水浸泡震荡1h,干燥后溶解在15%的nafion乙醇溶液中。超声处理20min使多壁碳纳米管均匀分散,制成多壁碳纳米管nafion乙醇溶液。然后将其均匀涂在孔径为1.5μm硝酸醋酸混合纤维薄膜上,在55℃的环境中烘干。使硝酸-醋酸混合纤维薄膜的多壁碳纳米管负载量为8mg/cm2。工作电极水平放置,将工作电极的电势调整到-0.6v(vsshe)进行反应。
对照组b在阴极池中接入1.5ml(1.5%)的产巴氏产甲烷菌菌液(methanosarsinabarkeri),顶空充满co2和n2混合气(1:4)。工作电极采用传统碳布电极,将工作电极的电势调整到-0.6v(vsshe)进行反应。
对照组c在阴极池中接入1.5ml(1.5%)巴氏产甲烷菌菌液(methanosarsinabarkeri),不放置工作电极,不施加外加电势。顶空充满co2和n2混合气(1:4)。
78小时后三组实验的顶空气体成分使用气相色谱仪测定。结果为,a组为8.453μmol,b组为6.371μmol。c组甲烷产量为3.379μmol。可以看出在相同的条件下,本发明显著地提升了甲烷的产量。具有广泛的应用前景。
实施例2:
该实施例分为实验组a以及对照组b,c同时进行:
实验组a如图1所示。在阴极池中接入5ml(5.0%)的布氏产甲烷菌菌液(methanobacteriumbyrantti),顶空充满co2和n2混合气(1:4)。工作电极采用附着多壁碳纳米管的硝酸-醋酸混合纤维薄膜制成。首先,将长度为10μm多壁碳纳米管用5%双氧水浸泡震荡1h,干燥后溶解在2%的nafion乙醇溶液中。超声处理1h使多壁碳纳米管均匀分散,制成多壁碳纳米管nafion乙醇溶液。然后将其均匀涂在孔径为2μm硝酸醋酸混合纤维薄膜上,在37℃的环境中烘干。使硝酸-醋酸混合纤维薄膜的多壁碳纳米管负载量为4.5mg/cm2。将工作电极的电势调整到-0.6v(vsshe)进行反应。
对照组b在阴极池中接入5ml(5.0%)的产布氏产甲烷菌菌液(methanobacteriumbyrantti),顶空充满co2和n2混合气(1:4)。工作电极采用传统碳布电极,将工作电极的电势调整到-0.6v(vsshe)进行反应。
对照组c在阴极池中接入5ml(5.0%)产布氏产甲烷菌菌液(methanobacteriumbyrantti),不放置工作电极,不施加外加电势。顶空充满co2和n2混合气(1:4)。
78小时后三组实验的顶空气体成分使用气相色谱仪测定。结果为,a组为7.471μmol,b组为5.643μmol。c组甲烷产量为1.808μmol。可以看出在相同的条件下,本发明显著地提升了甲烷的产量。具有广泛的应用前景。
实施例3:
该实施例分为实验组a以及对照组b,c同时进行:
实验组a如图所示。在阴极池中接入3ml(3.0%)的亨氏产甲烷菌菌液(methanospirllumhungatei),顶空充满co2和n2混合气(1:4)。工作电极采用附着多壁碳纳米管的硝酸-醋酸混合纤维薄膜制成。首先,将长度为2μm多壁碳纳米管用5%双氧水浸泡震荡1h,干燥后溶解在20%的nafion乙醇溶液中。超声处理5min使多壁碳纳米管均匀分散,制成多壁碳纳米管nafion乙醇溶液。然后将其均匀涂在孔径为0.44μm硝酸醋酸混合纤维薄膜上,在37℃的环境中烘干。使硝酸-醋酸混合纤维薄膜的多壁碳纳米管负载量为6.8mg/cm2。将工作电极的电势调整到-0.6v(vsshe)进行反应。
对照组b在阴极池中接入3ml(3.0%)的产亨氏产甲烷菌菌液(methanospirllumhungatei),顶空充满co2和n2混合气(1:4)。工作电极采用传统碳布电极,将工作电极的电势调整到-0.6v(vsshe)进行反应。
对照组c在阴极池中接入3ml(3.0%)产亨氏产甲烷菌菌液(methanospirllumhungatei),不放置工作电极,不施加外加电势。顶空充满co2和n2混合气(1:4)。
78小时后三组实验的顶空气体成分使用气相色谱仪测定。结果为,a组为6.845μmol,b组为5.331μmol。c组甲烷产量为1.664μmol。可以看出在相同的条件下,本发明显著地提升了甲烷的产量。具有广泛的应用前景。
- 还没有人留言评论。精彩留言会获得点赞!