一种用于治疗儿童矮小症的重组人血清白蛋白/生长激素融合蛋白的制备纯化方法与流程
本发明涉及生物技术领域,更具体地是一种用于治疗儿童矮小症的重组人血清白蛋白/生长激素融合蛋白及其制备纯化方法和其在制备治疗儿童矮小症药物中的用途。
背景技术:
人血清白蛋白(hsa)是一种可溶性单体蛋白质,构成血液中蛋白总量的一半。白蛋白作为一种基本载体,携带传递脂肪酸、类固醇和激素分子等,其稳定的惰性性质是维持血压的一个重要因素。血清白蛋白是一种球状非糖基化的、分子量为65千道尔顿、具有585个氨基酸的血清蛋白质。这一蛋白(白蛋白前体)再通过高尔基体的转化加工,去除引导多肽,而分泌到细胞外。血清白蛋白有35个半胱氨酸,在血液中,白蛋白是一个有17个二硫键的单体(参见brownjr,“白蛋白的结构、功能和应用”pergamon,纽约,1977)。当没有分泌多肽时,在酵母细胞内的白蛋白产物是错配状态,将失去90%的抗原性(与血浆中自然状态白蛋白相比),并且形成不溶性的白蛋白聚合体,不具有白蛋白的生物活性。现在用于临床的白蛋白均是从人血浆中提取的。利用微生物重组表达白蛋白(rhsa)的生产已在专利ep330451、ep361991和于在林、富岩中国授权专利zl2004010057313.7中公开。
白蛋白是血液中的主要成分,在人体内含量为每升血液含40克,其半衰期寿命为14-20天。在药物制剂组成中,白蛋白也常被用作药物的稳定剂,尤其是生物药和疫苗的制造。综上所述,利用基因工程技术,将人血清白蛋白与治疗性蛋白质基因融合在酵母菌或脊椎动物细胞中表达为重组融合蛋白后,该融合蛋白将具有极大的优势使之可抵御生物体内酶解作用,并可使治疗性蛋白质在体内体外的寿命大大提高,也就是可增加治疗性蛋白质在血清中和储存时的稳定性和较长的半衰期,达到蛋白药物的长效化,大大减少给药频率,在重大疾病临床治疗中获得更好的治疗效果。
人生长激素(humangrowthhormone,hgh)是人脑垂体前叶分泌的一种蛋白质激素.它不仅有促进生长的作用,而且与机体的合成代谢密切相关,是治疗侏儒症、烧伤、创伤、骨折、出血性溃疡的重要药物。由于其体内半衰期仅为0.5~2hr左右,故需要每天、长期注射(数年,5-10年)给药才能发挥疗效,治疗周期长更需要药物长效化。为此,市场急需长效化、特别是适合于儿童的长效药。基因重组的长效重组人血清白蛋白/生长激素融合蛋白是具有与人体内源生长激素同等的作用,刺激骨骺端软骨细胞分化、增殖,刺激软骨基质细胞增长,刺激成骨细胞分化、增殖,引起线形生长加速及骨骼变宽。促进全身蛋白质合成,纠正手术等创伤后的负氮平衡状态,纠正重度感染及肝硬化等所致的低蛋白血症;刺激免疫球蛋白合成,刺激淋巴样组织,巨噬细胞和淋巴细胞的增殖,增强抗感染能力;刺激烧伤创面及手术切口胶原体细胞合成纤维细胞,巨噬细胞分裂增殖,加速伤口愈合,促进心肌蛋白合成,增加心肌收缩力,降低心肌耗氧量,调节脂肪代谢,降低血清胆固醇、低密度脂蛋白的水平;补充生长激素不足或缺乏,调节成人的脂肪代谢、骨代谢、心肾功能。
临床上可用于治疗如下主要适应症。
1、用于因内源性生长激素缺乏所引起的儿童生长缓慢;2、用于重度烧伤治疗;3、用于已明确的下丘脑-垂体疾病所致的生长激素缺乏症和经两种不同的生长激素刺激试验确诊的生长激素显著缺乏。
1985年,每天给药一次的重组人生长激素(rhgh)获得了批准上市销售,取代基于安全考虑而已停用的人垂体源性生长激素,成为一种可以无限获取的人生长激素资源。在随后的20年里,主要是在rhgh生产商的支持下,儿科内分泌科医师率先开展了一系列的临床试验以试图证明rhgh治疗可以改善因某些疾病而非生长激素缺乏(ghd)所致身材矮小患儿的生长速率及最终身高,这些疾病包括特纳综合征(ts)、慢性肾功能不全(cri)、小于胎龄儿(sga)、普-威综合征(pws)或特发性身材矮小(iss)。虽然重组人生长激素达到临床治疗的目的,但是由于给药频次为每天一次,儿童用药时间又至少要1-3年,患者依从度极低,治疗费用又是巨大一般家庭是难于按医嘱要求配合治疗,使得受药人群大大受限。为此,peg化重组人生长激素面世,虽然可以做到每周给药一次,但费用则是普通重组人生长激素的数倍,而且在制剂还含有苯酚作为蛋白质制剂配方组分。为此本发明以此为技术创新,希望获得儿童患者可以每两周给药一次,生产制备费用是peg-化生长激素的1/100,患者依从度将会大大提高,治疗费用会大大降低的创新药物结构。本发明将有利于更多急需要治疗,而在依从度和治疗费用限制用药的人群接受必须的治疗,为此获得意想不到的技术优势和创造性。
技术实现要素:
本发明就是为了解决上述技术问题,所提出的一种用于治疗儿童矮小症的重组人血清白蛋白/生长激素融合蛋白的制备纯化方法。
本发明是按照以下技术方案实现的。
一种用于治疗儿童矮小症的重组人血清白蛋白/生长激素融合蛋白,所述重组人血清白蛋白/生长激素融合蛋白的氨基酸序列为seqidno.1。
进一步的,所述重组人血清白蛋白/生长激素融合蛋白的核酸序列为seqidno.2。
进一步的,所述重组人血清白蛋白/生长激素融合蛋白基因通过重组工程宿主细胞表达;所述重组工程宿主细胞为酵母菌、cho细胞、植物、昆虫、细菌或者动物细胞;重组人血清白蛋白/生长激素融合蛋白基因通过质粒dna载体表达、病毒载体表达、或转基因技术转移到植物和动物体内表达。
进一步的,所述重组人血清白蛋白/生长激素融合蛋白基因选用基因工程技术构建来表达;获得融合蛋白的方法是利用载体质粒,通过转化和转染或感染的方式来表达重组融合蛋白。
进一步的,所述重组人血清白蛋白/生长激素融合蛋白基因选用酵母表达载体来转化毕氏酵母,并使融合蛋白分泌到培养液中。
进一步的,所述重组人血清白蛋白/生长激素融合蛋白基因表达的酵母属宿主为毕氏酵母属巴斯德菌种。
一种上述用于治疗儿童矮小症的重组人血清白蛋白/生长激素融合蛋白的高密度表达方法,包括以下步骤:
a.重组人血清白蛋白/生长激素融合蛋白载体质粒的构建及表达
以人胎肝中提取的总rna为模板,利用反转录多聚酶链聚合反应来合成、扩增hsa基因;经电泳分离纯化hsadna片断,将其克隆至酵母表达表达载体,获得pyz-hsa重组质粒;采用dna全序列合成法来人工合成gh核苷酸序列;用酶切合成的目的基因gh和pyz-hsa重组质粒,并将二者进行连接,获得pyz-hsa/gh重组质粒;
b.毕赤酵母表达工程菌的转化和制备
将pyz-hsa/gh重组质粒经pmei限制性内切酶处理后点转入毕氏酵母x33感受态细胞,转化后的酵母菌接种于含zeocin抗生素的ypd平板培养基上进行培养;
c.重组酵母工程菌的筛选
将数个含有待表达基因的酵母菌落分别在含有zeocin抗生素,具有缓冲能力及甘油的基本培养液中培养;培养一段时候后离心收集菌体,菌体再重悬于不含甘油的同种基本培养液内,含0.5%甲醇;每24小时加入100%甲醇至最终浓度为0.5%,在不同的时间点分别收集培养上清液,筛选表达特异蛋白的重组酵母工程菌株;
d.大规模高密度表达rhsa/gh融合蛋白
使用500l和1000l生物发酵罐系统,取一支工程菌种子库,小规模摇床培养开始,然后扩增到一级种子罐、二级种子罐,进入生产发酵罐;经培养至罐内甘油消耗尽,溶氧随之回至底限再回升时,启动甘油流加;待流加结束,溶氧再回升时,启动甲醇流加,进入诱导和重组蛋白生产阶段,维持72小时甲醇流加;产量不低于3克/l发酵上清液。
一种上述用于治疗儿童矮小症的重组人血清白蛋白/生长激素融合蛋白的纯化方法,将高密度表达获得的重组人血清白蛋白/生长激素融合蛋白进行如下纯化步骤;获得的纯度不低于99%:
a.初纯亲和层析柱:capto-mmc
平衡缓冲液:20~100mmnaac-hac,5~20mm半胱氨酸,2~8%甘氨酸,ph4.0~6.0
洗杂缓冲液:20~100mmmpb,5~20mm半胱氨酸,2~8%甘氨酸,ph6.0~6.5
洗脱缓冲液:20~100mmpb,5~20mm半胱氨酸,2~8%甘氨酸,0.5~2.0mnh4cl或其他高盐溶液,ph6.5~8.5
b.疏水介质层析柱:phenylsepharosetmhighperformance
平衡缓冲液:20~100mmtris-hcl或pb,5~20mm半胱氨酸,2~8%甘氨酸,1~2mnh4cl或(nh4)2so4,ph5.0~9.0
洗脱缓冲液:20~100mmtris-hcl或pb,ph5.0~9.0
c.离子纯化分离层析柱:qsepharosetmfastflow
平衡缓冲液:20~100mmtris-hcl或pb,5~20mm半胱氨酸,2~8%甘氨酸,ph6.0~9.0
洗杂缓冲液:20~100mmpb,180mmnacl,5~20mm半胱氨酸,2~8%甘氨酸,ph6.0~9.0
洗脱缓冲液:20~100mmtris-hcl或pb,200~1000mmnacl或nh4cl,5~20mm半胱氨酸,2~8%甘氨酸,ph6.0~9.0
d.层析柱:sephacryls-200hr
平衡缓冲液:5~50mmpb,2~8%甘氨酸,ph5~8。
进一步的,一种用于治疗儿童矮小症的重组人血清白蛋白/生长激素融合蛋白的纯化方法,将高密度表达获得的重组人血清白蛋白/生长激素融合蛋白进行如下纯化步骤:
a.初纯亲和层析柱:capto-mmc
平衡缓冲液:30mmnaac-hac,10mm半胱氨酸,5%甘氨酸,ph5.5
洗杂缓冲液:20mmpb,10mm半胱氨酸,5%甘氨酸,ph6.5
洗脱缓冲液:20mmpb,10mm半胱氨酸,5%甘氨酸,1.0mnh4cl,ph7.5
b.疏水介质层析柱:phenylsepharosetmhighperformance
平衡缓冲液:20mmpb,10mm半胱氨酸,5%甘氨酸,1.3mnh4cl,ph6.7
洗脱缓冲液:20mmpb,ph6.7
c.离子纯化分离层析柱:qsepharosetmfastflow
平衡缓冲液:20mmpb,10mm半胱氨酸,5%甘氨酸,ph7.2
洗杂缓冲液:20mmpb,180mmnacl,10mm半胱氨酸,5%甘氨酸,ph7.2
洗脱缓冲液:20mmpb,800mmnacl,10mm半胱氨酸,5%甘氨酸,ph7.2
d.层析柱:sephacryls-200hr
平衡缓冲液:20mmpb,5%甘氨酸,ph7.2。以上可否给出相应的
一种上述重组人血清白蛋白/生长激素融合蛋白在制备治疗儿童矮小症药物中的用途。首次达到可2周给药一次的更少给药频次。
本发明获得了如下有益效果。
1.本发明将人的血清白蛋白基因的c-端与人生长激素基因的n-端直接进行分子融合(之间不设有联接肽,no-linker)。通过研究和多次反复试验,构建了长效化重组人血清白蛋白/生长激素融合蛋白表达毕赤酵母工程菌。建立了一个新的重组人血清白蛋白/生长激素融合蛋白特异分离纯化的技术和方法。该融合蛋白可以是分泌型的,其可与特异识别抗人血清白蛋白抗体相结合,也可与特异识别人生长激素的抗体相结合。
2.本发明中的rhsa/gh核苷酸可利用重组克隆技术引入宿主细胞,以使融合蛋白得以表达。工程宿主细胞可以在含常规营养物的培养基中培养,并经过适当修改以利于启动子。以适当的操作方式控制选择转化子或扩增编码rhsa/gh的核苷酸链的培养条件,如温度,ph和选择表达细胞。
本发明的重组人血清白蛋白/生长激素融合蛋白基因(核苷酸序列)表达需要通过重组工程宿主细胞表达。重组工程宿主细胞可以是酵母菌、cho细胞、植物、昆虫、细菌或者动物,可以直接通过质粒dna载体表达、可以通过病毒载体表达、也可以通过转基因技术转移到植物和动物体内表达。
在本发明中提到的重组人血清白蛋白与人生长激素融合蛋白,优选使用基因工程技术构建来表达。获得融合蛋白的优选方法是利用载体质粒,通过转化和转染或感染的方式来表达融合蛋白。特别是优选的利用可转化的酵母表达载体,来转化毕氏酵母,并使融合蛋白分泌到培养液中。优选的用于表达rhsa/gh的酵母属宿主可为毕氏酵母属巴斯德菌种。利用酵母菌表达rhsa/gh的优势在于,酵母菌体系可以产生高质量成熟的融合蛋白,并可以分泌到培养液中而便于纯化。
酵母菌遗传工程的进展使外源基因可以在酵母菌中得到表达并分泌蛋白产品到细胞外。利用酵母菌表达分泌型蛋白的优点为,但不局限于,高表达产量、蛋白质为可溶性的、正确的折迭和易于大规模生产和纯化。
3.本发明提供了利用酵母菌来更有效地及节省费用地生产制造rhsa/gh蛋白。本发明也以实施例的方式提供和公开了表达这种高产无热源重组rhsa/gh蛋白的毕赤酵母工程菌的吨级规模化发酵工艺和融合蛋白分离纯化的方法,该蛋白在毕赤酵母菌在1000l发酵罐中的表达量不低于1g/l,纯化后的纯度可达99%,并且内毒素含量≤0.5eu/mg。
本发明设计了复合式新型弱阳离子交换层析、疏水柱层析、离子交换柱层析和凝胶柱层析顺序组合来去除杂蛋白、糖类、脂类、宿主蛋白等杂质,最终得到高纯度蛋白。
本发明使用毕赤酵母菌表达系统制备重组人血清白蛋白/生长激素融合蛋白,经由这一系统制备的重组蛋白药物完全适合于临床应用,本发明研发的创新药原液中的宿主蛋白残留量也符合2015版中国药典三部的要求。
本发明也完成高剂量蛋白质药物水针剂的25℃快速试验确保新剂型的稳定性不存在问题(25℃长期稳定性考察6个月相当于,该制剂可在规定2-8℃保藏条件下可稳定保藏3年)。
本发明使得在规模化后长效重组人血清白蛋白/生长激素融合蛋白注射液的生产成本将在5元-10元之间。现在市场销售中已经有重组人生长激素产品,生产成本高而销售价格在竞争中日益下滑。可达到2周给药1次的本发明长效人生长激素则是新一代人生长激素药物,其生产成本低,产能大,注射次数少,完全可以逐步取代现有短效和长效人生长激素产品。本发明的技术在市场竞争中具有极大的和明显的优势。
附图说明
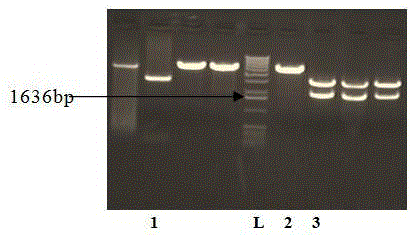
图1是本发明pyz-hsa重组质粒ecorⅰ&xhoⅰ酶切鉴定图;
图2是本发明pyz-hsa/gh重组酵母表达工程菌电转后平板生长情况图;
图3是本发明大规模高密度表达rhsa/gh蛋白sds-page蛋白电泳图;
图4是本发明qff离子交换柱纯化分泌的rhsa/gh蛋白sds-page蛋白电泳图。
图5是本发明精纯后rhsa/gh蛋白的还原和非还原电泳图;
图6是本发明纯化的rhsa/gh蛋白的液相色谱测量纯度图;
图7是本发明纯化的rhsa/gh融合蛋白针对抗人hsa鼠单克隆抗体的蛋白免疫印记图谱;
图8是本发明纯化的rhsa/gh融合蛋白针对抗人gh的单克隆抗体的蛋白免疫印记图谱;
图9是本发明rhsa/gh融合蛋白肽质量指纹图谱测定图;
图10是本发明皮下给药后3种不同结构的生长激素在大鼠中的血药浓度测定图。
具体实施方式
下面结合附图及实施例对本发明作进一步描述。
实施例1:人血清白蛋白(hsa)基因表达及载体质粒的构建
以人胎肝中提取的总rna为模板,利用反转录多聚酶链聚合反应来合成、扩增hsa基因。5微克总rna在反转录酶(购自gibco/brl公司)的作用下,合成相对应的dna链,寡聚核苷酸引物为18个t+ln(n为随机核苷酸)。反应条件为45°c,20分钟,而后升温至55°c,继续保温40分钟。
其寡聚核苷酸引物序列为:5'-gaattcatgaagtgggtaacctttatttcc-3'和5'-gaattcttataagcctaaggcagcttgacttgc-3'
两个ecorⅰ识别位点分别加在hsa基因的两端克隆入一表达载体。pcr反应条件为94°c,4分钟,编码hsa的dna进一步扩增35个循环反应:94°c,30秒;58°c,30秒;72'c,2分30秒。循环反应结束时,再给予72°c,10分钟的延长反应。凝胶电泳显示pcr扩增产物长约1850碱基对。pcr产物利用ta克隆的方法插入pcrii载体(invitrogen公司)。所得质粒命名为pcr-hsa。dna测序结果表明其与发表的人血清白蛋白dna序列相同。用ecorⅰ限制性酶消化pcr产物,经电泳分离纯化hsadna片断,将其克隆至酵母表达载体(pyz载体,购自天津溥瀛生物技术有限公司)。经转化dh5a感受态细胞,在含有抗生素zeocin的低盐lb-琼脂平板上筛选阳性单克隆,其经检定对hsa基因插入的质粒命名为pyz-hsa(见图1,pyz-hsa重组质粒ecorⅰ&xhoⅰ酶切鉴定,目的条带大小约1850bp,与预期目的条带大小一致。测序确认正反向)。
hsa基因dna序列(genebank注册号:ay728024):
atgaagtgggtaacctttatttcccttctttttctctttagctcggcttattccaggggtgtgtttcgtcgagatgcacacaagagtgaggttgctcatcggtttaaagatttgggagaagaaaatttcaaagccttggtgttgattgcctttgctcagtatcttcagcagtgtccatttgaagatcatgtaaaattagtgaatgaagtaactgaatttgcaaaaacatgtgttgctgatgagtcagctgaaaattgtgacaaatcacttcataccctttttggagacaaattatgcacagttgcaactcttcgtgaaacctatggtgaaatggctgactgctgtgcaaaacaagaacctgagagaaatgaatgcttcttgcaacacaaagatgacaacccaaacctcccccgattggtgagaccagaggttgatgtgatgtgcactgcttttcatgacaatgaagagacatttttgaaaaaatacttatatgaaattgccagaagacatccttacttttatgccccggaactccttttctttgctaaaaggtataaagctgcttttacagaatgttgccaagctgctgataaagctgcctgcctgttgccaaagctcgatgaacttcgggatgaagggaaggcttcgtctgccaaacagagactcaagtgtgccagtctccaaaaatttggagaaagagctttcaaagcatgggcagtagctcgcctgagccagagatttcccaaagctgagtttgcagaagtttccaagttagtgacagatcttaccaaagtccacacggaatgctgccatggagatctgcttgaatgtgctgatgacagggcggaccttgccaagtatatctgtgaaaatcaagattcgatctccagtaaactgaaggaatgctgtgaaaaacctctgttggaaaaatcccactgcattgccgaagtggaaaatgatgagatgcctgctgacttgccttcattagctgctgattttgttgaaagtaaggatgtttgcaaaaactatgctgaggcaaaggatgtcttcctgggcatgtttttgtatgaatatgcaagaaggcatcctgattactctgtcgtgctgctgctgagacttgccaagacatatgaaaccactctagagaagtgctgtgccgctgcagatcctcatgaatgctatgccaaagtgttcgatgaatttaaacctcttgtggaagagcctcagaatttaatcaaacaaaattgtgagctttttgagcagcttggagagtacaaattccagaatgcgctattagttcgttacaccaagaaagtaccccaagtgtcaactccaactcttgtagaggtctcaagaaacctaggaaaagtgggcagcaaatgttgtaaacatcctgaagcaaaaagaatgccctgtgcagaagactatctatccgtggtcctgaaccagttatgtgtgttgcatgagaaaacgccagtaagtgacagagtcaccaaatgctgcacagaatccttggtgaacaggcgaccatgcttttcagctctggaagtcgatgaaacatacgttcccaaagagtttaatgctgaaacattcaccttccatgcagatatatgcacactttctgagaaggagagacaaatcaagaaacaaactgcacttgttgagcttgtgaaacacaagcccaaggcaacaaaagagcaactgaaagctgttatggatgatttcgcagcttttgtagagaagtgctgcaaggctgacgataaggagacctgctttgccgaggagggtaaaaaacttgttgctgcaagtcaagctgccttaggcttataa
人血清白蛋白(hsa)成熟肽氨基酸序列(genebank注册号:ay728024):
dahksevahrfkdlgeenfkalvliafaqylqqcpfedhvklvnevtefaktcvadesaencdkslhtlfgdklctvatlretygemadccakqepernecflqhkddnpnlprlvrpevdvmctafhdneetflkkylyeiarrhpyfyapellffakrykaafteccqaadkaacllpkldelrdegkassakqrlkcaslqkfgerafkawavarlsqrfpkaefaevsklvtdltkvhtecchgdllecaddradlakyicenqdsissklkeccekpllekshciaevendempadlpslaadfveskdvcknyaeakdvflgmflyeyarrhpdysvvlllrlaktyettlekccaaadphecyakvfdefkplveepqnlikqncelfeqlgeykfqnallvrytkkvpqvstptlvevsrnlgkvgskcckhpeakrmpcaedylsvvlnqlcvlhektpvsdrvtkccteslvnrrpcfsalevdetyvpkefnaetftfhadictlsekerqikkqtalvelvkhkpkatkeqlkavmddfaafvekcckaddketcfaeegkklvaasqaalgl
实施例2:重组人血清白蛋白/生长激素融合基因(rhsa/gh)表达及载体质粒的构建
采用dna全序列合成法来人工合成gh成熟肽的核苷酸序列(genebank注册号:np_000506)(由北京擎科新业生物技术有限公司合成)。分别在其n端加上bsu36ⅰ酶切位点,在其c端加上xhoⅰ酶切位点,用这两个酶分别酶切合成的目的基因gh和pyz-hsa重组质粒;目的基因gh与pyz-hsa重组质粒的连接:具体步骤:将酶切后的目的基因gh与pyz-hsa重组质粒按一定比例混合,并加入连接buffer和连接酶,22℃连接1小时;连接产物转化dh5α感受态细胞,具体步骤:将连接产物加入dh5α感受态细胞,冰浴30分钟,42℃热激90秒,再冰浴2分钟,加入培养基置于摇床中,150rpm,45分钟,12000rpm离心1分钟,涂板。测序验证,具体步骤:挑取单克隆,扩大培养,小量提取质粒,酶切鉴定,挑选出酶切得到与目的片段大小一致的质粒,并进行测序确认,测序引物为p5和p2,将最终测序确认的质粒命名为pyz-hsa/gh。
p5:5'-aaggagacctgctttgccg-3
p2:5'-caaatggcattctgacatcc-3
rhsa/gh核苷酸dna序列(seqidno.2):
atgaagtgggtaacctttatttcccttctttttctctttagctcggcttattccaggggtgtgtttcgtcgagatgcacacaagagtgaggttgctcatcggtttaaagatttgggagaagaaaatttcaaagccttggtgttgattgcctttgctcagtatcttcagcagtgtccatttgaagatcatgtaaaattagtgaatgaagtaactgaatttgcaaaaacatgtgttgctgatgagtcagctgaaaattgtgacaaatcacttcataccctttttggagacaaattatgcacagttgcaactcttcgtgaaacctatggtgaaatggctgactgctgtgcaaaacaagaacctgagagaaatgaatgcttcttgcaacacaaagatgacaacccaaacctcccccgattggtgagaccagaggttgatgtgatgtgcactgcttttcatgacaatgaagagacatttttgaaaaaatacttatatgaaattgccagaagacatccttacttttatgccccggaactccttttctttgctaaaaggtataaagctgcttttacagaatgttgccaagctgctgataaagctgcctgcctgttgccaaagctcgatgaacttcgggatgaagggaaggcttcgtctgccaaacagagactcaagtgtgccagtctccaaaaatttggagaaagagctttcaaagcatgggcagtagctcgcctgagccagagatttcccaaagctgagtttgcagaagtttccaagttagtgacagatcttaccaaagtccacacggaatgctgccatggagatctgcttgaatgtgctgatgacagggcggaccttgccaagtatatctgtgaaaatcaagattcgatctccagtaaactgaaggaatgctgtgaaaaacctctgttggaaaaatcccactgcattgccgaagtggaaaatgatgagatgcctgctgacttgccttcattagctgctgattttgttgaaagtaaggatgtttgcaaaaactatgctgaggcaaaggatgtcttcctgggcatgtttttgtatgaatatgcaagaaggcatcctgattactctgtcgtgctgctgctgagacttgccaagacatatgaaaccactctagagaagtgctgtgccgctgcagatcctcatgaatgctatgccaaagtgttcgatgaatttaaacctcttgtggaagagcctcagaatttaatcaaacaaaattgtgagctttttgagcagcttggagagtacaaattccagaatgcgctattagttcgttacaccaagaaagtaccccaagtgtcaactccaactcttgtagaggtctcaagaaacctaggaaaagtgggcagcaaatgttgtaaacatcctgaagcaaaaagaatgccctgtgcagaagactatctatccgtggtcctgaaccagttatgtgtgttgcatgagaaaacgccagtaagtgacagagtcaccaaatgctgcacagaatccttggtgaacaggcgaccatgcttttcagctctggaagtcgatgaaacatacgttcccaaagagtttaatgctgaaacattcaccttccatgcagatatatgcacactttctgagaaggagagacaaatcaagaaacaaactgcacttgttgagcttgtgaaacacaagcccaaggcaacaaaagagcaactgaaagctgttatggatgatttcgcagcttttgtagagaagtgctgcaaggctgacgataaggagacctgctttgccgaggagggtaaaaaacttgttgctgcaagtcaagctgccttaggcttattcccaaccattcccttatcccgtctgttcgacaacgctatgctccgcgcccatcgtctgcaccagctggcctttgacacctaccaggagtttgaagaagcctatatcccaaaggaacagaagtattcattcctgcagaacccccagacctccctctgtttctcagagtctattccgacaccctccaacagggaggaaacacaacagaaatccaacctagagctgctccgcatctccctgctgctcatccagtcgtggctggagcccgtgcagtttctcaggagtgtcttcgccaacagcctggtgtacggcgcctctgacagcaacgtctatgacctcctaaaggacctagaggaaggcatccaaacgctgatggggaggctggaagatggcagcccccggactgggcagatcttcaagcagacctacagcaagttcgacacaaactcacacaacgatgacgcactactcaagaactacgggctgctctactgcttcaggaaggacatggacaaggtcgagacattcctgcgcatcgtgcagtgccgctctgtggagggcagctgtggcttctagtga
下划线为人生长激素成熟肽核苷酸序列。
rhsa/gh成熟肽氨基酸序列(seqidno.1):
dahksevahrfkdlgeenfkalvliafaqylqqcpfedhvklvnevtefaktcvadesaencdkslhtlfgdklctvatlretygemadccakqepernecflqhkddnpnlprlvrpevdvmctafhdneetflkkylyeiarrhpyfyapellffakrykaafteccqaadkaacllpkldelrdegkassakqrlkcaslqkfgerafkawavarlsqrfpkaefaevsklvtdltkvhtecchgdllecaddradlakyicenqdsissklkeccekpllekshciaevendempadlpslaadfveskdvcknyaeakdvflgmflyeyarrhpdysvvlllrlaktyettlekccaaadphecyakvfdefkplveepqnlikqncelfeqlgeykfqnallvrytkkvpqvstptlvevsrnlgkvgskcckhpeakrmpcaedylsvvlnqlcvlhektpvsdrvtkccteslvnrrpcfsalevdetyvpkefnaetftfhadictlsekerqikkqtalvelvkhkpkatkeqlkavmddfaafvekcckaddketcfaeegkklvaasqaalglfptiplsrlfdnamlrahrlhqlafdtyqefeeayipkeqkysflqnpqtslcfsesiptpsnreetqqksnlellrisllliqswlepvqflrsvfanslvygasdsnvydllkdleegiqtlmgrledgsprtgqifkqtyskfdtnshnddallknygllycfrkdmdkvetflrivqcrsvegscgf
下划线为人生长激素成熟肽氨基酸序列
实施例3:毕赤酵母表达工程菌的转化和制备
将毕氏酵母菌菌株x33菌落接种于含5mlypd培养液的50ml离心管中,以250转/分的速度于30℃下培养过夜。次日取0.2ml过夜培养物再转接入500mlypd的培养液中,置于2升的三角培养瓶中。在30℃下旋转培养2-3小时,使细胞密度达到od600=1.3-1.5。酵母菌经离心方法收集,再重悬于500ml冰预冷的无菌水中洗涤两次。然后酵母菌悬于20ml冰预冷的1msortbitol溶液洗涤一次。
将实施例2构建的pyz-hsa/gh质粒dna经pmei限制性内切酶处理后,形成线性质粒分子。取5μg线性化后质粒dna与80μl处理后的酵母菌相混合并置于0.2厘米厚的电极杯内,置于电转仪上。电脉冲条件为电压7500v/cm,电极间隔时间为5-10(ms)。电击处理后,立即加入1ml冰预冷的1msorbitol溶液于酵母菌中,然后转入15ml试管中。转化的酵母菌置于30℃培养箱中放置2小时,然后接种涂布在含zeocin抗生素的ypd平板培养基上。经抗性选择而生长出的克隆,再用分子生物学方法鉴定其基因的插入。蛋白质的表达与分泌则以sds-page或用特异抗体做蛋白质免疫印迹检测(见图2)。
实施例4:重组酵母工程菌的筛选
将数个含有待表达基因的酵母菌落分别在含有zeocin抗生素,具有缓冲能力及甘油的基本培养液中培养。以300转/分的速度培养至菌体密度达到od600=2-6。培养物经1500转/分,15分钟条件下离心收集菌体,菌体再重悬于同种基本培养液但不含甘油,改含0.5%甲醇,细胞密度达到od600=1.0,继续培养。酵母菌在甲醇的诱导下,外源蛋白在启动子的作用下开始表达。其后,每24小时加入100%甲醇至最终浓度为0.5%。在不同的时间点分别收集培养上清液。使用sds-page变性聚丙烯酰胺凝胶电泳初步测定重组人血清白蛋白/生长激素融合蛋白的表达,筛选表达目的特异蛋白质的重组酵母工程菌株。
实施例5:大规模高密度表达rhsa/gh融合蛋白
本发明使用1000l(吨级)生物发酵罐系统开展了rhsa/gh融合蛋白的吨级规模化生产和发酵工艺以及公斤级rhsa/gh蛋白的制备工艺和技术建立。重组酵母工程菌按研发的工艺程序制备工程菌种子库。取一支工程菌种子库接种到三角瓶中,从小规模摇床培养开始,然后扩增到一级种子罐、二级种子罐,进入生产发酵罐(1吨体积)。经培养至罐内甘油消耗尽,溶氧随之回至底限再回升时,启动甘油流加。待流加结束,溶氧再回升时,启动甲醇流加,进入诱导和重组蛋白生产阶段,维持72小时甲醇流加。可在不同培养时间点取样测试重组蛋白的表达。对于分泌型蛋白在细胞内及培养液中的含量均用sds-page方法进行分析,表达水平和纯度在每一步中均进行监测。结果显示发酵液中的rhsa/gh蛋白的表达水平在3-10g/l左右(见图3,泳道m:蛋白质标准分子量(由上至下:97.4kd,66.2kd,43.0kd,31.0kd,20.1kd,14.4kd);泳道1:诱导表达52小时的还原rhsa/gh,分子量~88.6kd;泳道2:诱导表达72小时的还原rhsa/gh,分子量~88.6kd;泳道3:诱导表达52小时的非还原rhsa/gh,分子量~88.6kd;泳道4:诱导表达72小时的非还原rhsa/gh,分子量~88.6kd;泳道5:自制mk(分子量由上至下:83kd,66kd))。sds-page分为非还原sds-page和还原sds-page,均是变性条件下的电泳。还原和非还原sds-page的区别是在样品处理时加或不加还原剂(如dtt或2-巯基乙醇等)。
实施例6:分泌的rhsa/gh融合蛋白的纯化与特性
rhsa/gh融合蛋白经酵母工程菌发酵培养直接分泌到上清液。经连续流离心将含有分泌出的血清白蛋白-生长激素融合蛋白上清液与菌体分离后,柱层析纯化首先采用美国ge公司的复合式新型弱阳离子交换层析—capto-mmc层析,因为表达的上清成分复杂,且有一定浓度的盐的存在,capto-mmc层析可以承受较高的流速,高结合载量,并对发酵上清液中的盐浓度要求不高,非常适合发酵液的第一步柱层析收集。
capto-mmc层析可选用20~100mmnaac-hac缓冲液,ph的范围4.0~6.0,洗脱缓冲液可以使用20~100mm的磷酸缓冲液,含有0.5m以上的nh4cl或其他高盐溶液,ph的范围6.5~8.5,也可以使用各种浓度的有机溶剂。也可在缓冲液中加入一定量的甘氨酸或半胱氨酸保持蛋白质的稳定性。
经过大量的筛选和探索性实验,试验流程如下:
初纯亲和层析柱:capto-mmc
平衡缓冲液:30mmnaac-hac,10mm半胱氨酸,5%甘氨酸,ph5.5
洗杂缓冲液:20mmpb,10mm半胱氨酸,5%甘氨酸,ph6.5
洗脱缓冲液:20mmpb,10mm半胱氨酸,5%甘氨酸,1.0mnh4cl,ph7.5。
经由capto-mmc初纯的含有目的蛋白峰组分,为了生产工艺的便捷和有效力,特别探索了可直接进入疏水介质填料分离纯化的工艺步骤。为此在butyl-,phenyl-或octyl基团的疏水填料继续比较和筛选,并分别选用20~100mm的tris-hcl或磷酸缓冲液,ph范围在5.0~9.0,加入1~2m的nh4cl或1~2m的(nh4)2so4的缓冲液为平衡缓冲液,以不含nh4cl或(nh4)2so4的缓冲液为洗脱缓冲液,也可在缓冲液中加入一定量的甘氨酸或半胱氨酸保持蛋白质的稳定性。过程包括将capto-mmc层析柱的洗脱峰用ph5.0~9.0,含有1~2m的nh4cl或1~2m的(nh4)2so4的20~100mm的tris-hcl或磷酸缓冲液稀释数倍,或在capto-mmc层析柱的洗脱峰中直接加入高浓度的nh4cl或(nh4)2so4溶液至浓度为1~2m的nh4cl或1~2m的(nh4)2so4,上样于疏水柱,然后以平衡缓冲液冲洗柱子,再以洗脱缓冲液进行洗脱,收集洗脱峰。通过疏水柱可进一步去除可能存在的多聚体、糖类、脂类、降解蛋白、色素等杂质,进一步提高目的蛋白的纯度。
经过大量的筛选和探索性实验,试验流程如下:
疏水介质层析柱:phenylsepharosetmhighperformance
平衡缓冲液:20mmpb,10mm半胱氨酸,5%甘氨酸,1.3mnh4cl,ph6.7
洗脱缓冲液:20mmpb,ph6.7。
经疏水层析纯化后的样品,也从生产工艺考量,从q或deae等阴离子交换柱进一步直接再纯化。通过与疏水层析不同的分离机制,离子交换层析可使目标蛋白得到进一步的纯化。可以选用ph范围在6.0~9.0之间的20~100mm的tris-hcl或磷酸缓冲液做为平衡缓冲液,也可在缓冲液中加入一定量的甘氨酸或半胱氨酸保持蛋白质的稳定性。可以在平衡缓冲液中加入浓度为200~1000mmnacl或nh4cl做为洗脱缓冲液。经过阴离子交换层析的样品通常可以达到95%以上的纯度。
经过大量的筛选实验,试验流程如下:
离子纯化分离层析柱:qsepharosetmfastflow
平衡缓冲液:20mmpb,10mm半胱氨酸,5%甘氨酸,ph7.2
洗杂缓冲液:20mmpb,180mmnacl,10mm半胱氨酸,5%甘氨酸,ph7.2
洗脱缓冲液:20mmpb,800mmnacl,10mm半胱氨酸,5%甘氨酸,ph7.2
经离子交换层析后收集的洗脱峰,可直接上样于sephacryl、superdex或sephadex等凝胶层析柱,进行脱盐换液。凝胶层析用5~50mm的磷酸缓冲液(pb)为平衡缓冲液,也可在缓冲液中加入一定量的甘氨酸或半胱氨酸保持蛋白质的稳定性。可将阴离子交换层析条件下得到的目的蛋白rhsa-gh的缓冲液体系改为5~10mm的磷酸缓冲液可以直接用于制剂的配制,而无须采用透析或超滤等其他手段,减少处理步骤中可能的污染、蛋白的变性、降解及聚集等损失。
经过大量的筛选实验,试验流程如下:
层析柱:sephacryls-200hr
平衡缓冲液:20mmpb,5%甘氨酸,ph7.2
整个纯化过程中,发酵液经离心后的上清液样品可以直接使用captommc柱收集,收集的目的蛋白可以加入硫酸铵即可直接上疏水柱,疏水柱的洗脱电导较低,而且样品得到了高度浓缩,经过简单的稀释处理或者sephadexg-25脱盐即可满足离子交换层析的要求,经过离子交换层析的样品浓度高,体积小,正好适合凝胶柱层析进行换液处理。整个纯化过程顺序合理,操作简便,易于工业放大生产,最终的产品单一组分可达95%以上,目的蛋白的聚合体、二聚体、目的蛋白的相关蛋白计算为目的蛋白则宿主蛋白残留量则小于0.05%。本发明形成的可大规模化用于生产制备重组人血清白蛋白/生长激素融合蛋白分离纯化生产工艺,最终纯度达到99.95%以上的意想不到的高度纯化效果(见图4和图5,图4中所用mk为自制maker,其分子量由上至下:83kd,66kd)。
实施例7:液相色谱法测定rhsa/gh融合蛋白的纯度测定
使用岛津lc-10avpplus高效液相色谱仪,色谱柱:tosoh公司tsk-gelg2000swxl7.8×300mm柱。以50mmpb-0.1mnacl缓冲液,ph7.0为流动相,流速:0.8ml/min,检测波长:280nm。
经上述程序建立的优化分离纯化工艺,获得了纯度为97.059%的rhsa/gh融合蛋白(见图6),目的蛋白相关蛋白含量(聚合体和目的蛋白降解物)则约3%。
实施例8:重组人血清白蛋白/生长激素融合蛋白酵母菌宿主蛋白残留量检测
采用双抗体夹心酶联免疫法检测。重组人血清白蛋白/生长激素融合蛋白(rhsa/gh)的宿主蛋白残留量,应不高于总蛋白的0.01%。
仪器:酶标仪(例如:bio-rad,model680)
试剂:(1)检测试剂盒immunoenzymetricassaykitforthemeasurementofpichiapastorishostcellproteins(美国cygnus公司),货号:cat#f140,检测波长为450/650nm;
(2)标准品溶液制备:使用试剂盒内提供的标准品溶液,每1ml中含cho细胞蛋白质0ng、1ng、4ng、20ng、75ng和250ng;
(3)供试品溶液:当蛋白含量5mg/ml,时,采用60-80倍稀释(用注射用水稀释);建议采用70倍稀释。
(4)设置回收率测定孔(复孔)。
测定方法(以试剂盒制造商提供的操作说明书为准):
(标准品和待检样品可以以设置复孔的方式进行检测,以提高检测精确度)
(1)样品稀释:将样品用注射用水稀释至1mg/ml。
(2)回收率样品的制备:将各稀释好的样品溶液15μl与15μl250ng/ml标准品充分混匀,备用。
(3)吸取25μl标准品、样品及回收率样品加入96孔板中,每孔再加入100μlanti-p.pastoris:hrp。
(4)封膜盖好96孔板,放进摇床24℃180rpm振摇3小时。
(5)倒出液体,每孔加350μl稀释后的洗液“dilutedwashsolution”(试剂盒中的母液使用注射用水20倍稀释),倒出液体,共洗4次。
(6)加入100μl“tmbsubstrate”,盖好盖,室温静置30分钟。
(7)加入100μl终止液“stopsolution”,设置酶标仪在450/650nm下读数,用excel做出标准曲线并计算样品的宿主蛋白含量和回收率。
以0ng/ml标准品孔作为空白对照调0,然后读取各孔od值。应用计算机分析软件进行读数和数据分析。
(8)以标准品溶液吸光度对应的浓度作标准曲线,并以供试品溶液吸光度在标准曲线上得到相应宿主蛋白含量。按以下公式计算:
式中c为供试品溶液中宿主蛋白质含量,ng/ml;
d为供试品稀释倍数;
t为供试品蛋白质含量,mg/ml。
结果计算及判定:
宿主蛋白百分含量=宿主蛋白浓度/供试品蛋白浓度
回收率=[回收率测定孔浓度-(供试品浓度/2)]/100
使用本发明生产制备的rhsa/gh的3个批次原液9075y20160801、9075y20170501、9075y20180301宿主蛋白检测结果下表:
结果判定:重组人血清白蛋白/生长激素融合蛋白原液中的宿主蛋白残留量应不高于总蛋白的0.01%。
酵母菌的宿主蛋白是酵母菌附件过程中产生的酵母分泌的蛋白、酶和降解的酵母菌生产的市值蛋白。宿主蛋白残留物可以在药物使用皮下注射给药后进入血液,刺激机体产生免疫反应,或者表现为高热、寒战等表征,宿主蛋白残留量越小越好。经本发明生产制备工艺生产的高纯度可注射用重组人血清白蛋白/生长激素融合蛋白产品,经检测结果表明宿主蛋白残留量已经在0.01%以下。即目的蛋白的纯度已经达到99.99%。
实施例9:免疫印记分析重组人血清白蛋白/生长激素融合蛋白
精纯得到的rhsa/gh融合蛋白进行sds-page电泳,经电泳仪将蛋白质转移到醋酸纤维素膜上,再以特异抗体(第一抗体)识别相对应的蛋白质。然后带有辣根过氧化物酶的第二抗体,识别并结合于第一抗体,经过dab显色后在醋酸纤维素膜上上留下印记。
对经酵母菌表达分泌的rhsa/gh融合蛋白以抗人hsa鼠单克隆抗体(sigmacat#:a6684)进行检测,确认含有人血清白蛋白蛋白质序列。同理,以相同的样品电泳胶转印后,以美国abcam公司抗人gh的单克隆抗体anti-ghantibody(cat#:ba14243)所做的蛋白质免疫印迹实验表明,融合蛋白含有与gh相同的抗原性。为此确认表达的rhsa/gh融合蛋白既有人血清白蛋白的抗原性也有人生长激素的抗原性(见图7、8)。
实施例10:重组人血清白蛋白/生长激素融合蛋白质谱分子量测定
1.实验方法
(1)样品前处理方法
完整分子量测定:供试品溶液用原液5mg/ml,进样4µl(上样量20µg)进行分析;系统适应性样品用纯化水稀释至2mg/ml,混匀,进样5µl(上样量10µg)进行分析。
(2)uplc方法参数
流动相a为0.1%fa水溶液,流动相b为0.1%fa乙腈溶液。色谱柱为nano-microunips3-300column,3µm,2.1mmx50mm,[partnr.ups03300]。设置柱温箱温度80℃,样品室温度4℃,流速设置为0.2ml/min。
(3)质谱方法参数
样品经色谱柱脱盐后用ltqorbitrapxl质谱仪(thermoscientific)进行检测扫描质谱分析。分析时长:6min,检测方式:正离子模式,扫描范围:800-3500m/z,质谱分辨率(fullms):7500
(4)数据分析参数
lcms结果在biopharmafinder(version3.0)软件上进行质谱去卷积分析。
2.实验结论
系统适应性样品avastin的理论分子量为:149197.20,测得值为:149198.41,与理论值误差为:8.1ppm,系统适应性结果符合检测要求。在此条件下测得的重组人血清白蛋白/生长激素融合蛋白注射液质谱分析数据经去卷积后的平均分子量为:88542.21da。这与rhsa/gh成熟肽氨基酸序列的理论分子量88583.45da非常接近。
实施例11:重组人血清白蛋白/生长激素融合蛋白肽质量指纹图谱(肽匹配覆盖率)测定
样品在含有dtt的6mguanidinehydrochloride(盐酸胍)溶液中还原变性,加iaa烷基化,缓冲液置换到酶解缓冲液中,加trypsin、glu-c和chymotrypsin酶解后经lcms分析。具体操作过程如下:取248µlsolutionf、4µlsolutionc,加入样品75µg,37℃30min;加入9.6µlsolutiond,室温避光30min,加µlsolutionc;bufferexchange:取一个新的超滤管(20kd),加350µlsolutionh,离心12000rpmx15min,弃掉上下层液体。在超滤管中加入样品,加适量solutionh,离心12000rpmx15min,弃掉下层废液,重复4次;转移样本到离心管,加适量solutionh调整溶液浓度为0.7ug/ul;分为3份,各加glu-c(1:10)、trypsin(1:15)、chymotrypsin(1:20)酶解,37℃18h;加入甲酸使酶失活。酶解产物离心后,在lcms上分析。
样品酶解产物采用uplc进行色谱分离。流动相a为0.1%fa水溶液,流动相b为0.1%fa乙腈溶液。色谱柱为watersacquityuplcpeptidebehc18column,130a,1.7µm,2.1mmx150mm,[partnr.186003556]。设置柱温箱温度60℃,样品室温度4℃,流速设置为0.3ml/min,检测波长215nm,样品上样量15µg。
样品经uplc脱盐及分离后用ltqorbitrapxl质谱仪(thermoscientific)进行检测扫描质谱分析。分析时长:90min,检测方式:正离子模式,扫描范围:300-2000m/z,质谱分辨率(fullms/ms2):30000/7500。
酶解产物的lc-ms/ms结果在biophamafinder(version3.0)上搜索目的蛋白序列,综合trypsin、glu-c、chymotrypsin三种酶解产物的结果后,得到重组人血清白蛋白/生长激素融合蛋白注射液的一级结构覆盖率为:100%(见图9,图9中上图为trypsin酶解产物的结果、中图为glu-c酶解产物的结果、下图为chymotrypsin酶解产物的结果)。
实施例12:rhsa/gh融合蛋白的大鼠体内生物活性测定试验
1.去垂体大鼠体重法
试验当日,取重组peg-人生长激素作为对照品(购自长春金赛公司),对照品和供试品用含0.1%牛血清白蛋白的0.9%氯化钠溶液,制成450µg/kg浓度的溶液。
测定法取同一来源、品系,出生26~28天,体重60~80g,同一性别,健康的大鼠,试验前2~3周手术摘除垂体,手术后于屏障环境饲养使其恢复。取去垂体手术后2~3周、体重变化小于手术前±10%的大鼠,按体重随机等分成4组,每组至少5只,每只编号并记录体重。分别自颈部皮下注射对照品溶液或供试品溶液0.4ml,首日给药1次,第7天处死大鼠,称体重,实验结束后可进行尸检,切开蝶鞍区,肉眼检查有无垂体残留,剔除有垂体残存的大鼠。每只动物给药后体重增加的克数作为反应值。照生物检定统计法(通则1431)中的量反应平行线测定法计算结果及实验误差。
试验数据:
如此计算只有当使用675µg的rhsa/gh给药,才能获得9.0g体重增加,与450µgpeg-rhgh相当。
2.本法系通过比较生长激素标准品(s)与供试品(t)对去垂体大鼠胫骨骨骺板宽度增加的程度,以测定供试品效价的一种方法。
标准品溶液和供试品溶液的制备同体重法。
测定法本法可与去垂体大鼠体重法同步进行。待体重法实验结束后,取下两腿胫骨,置10%甲醛溶液保存,从胫骨近心端顶部中间沿矢状面切开,置10%甲醛溶液中保存,水洗10分钟后,置丙酮溶液中10分钟,水洗3分钟,置2%硝酸银溶液中染色2分钟,水洗后置水中强光照射至变棕黑色,于10%硫代硫酸钠溶液固定30秒钟,置80%乙醇溶液中供测量用。测量时沿刨面切lmm左右薄片,置显微镜下测量胫骨骨骺板宽度,作为反应值。照生物检定统计法(通则1431)中的量反应平行线测定法计算效价及实验误差。
试验数据:
体重结果显示实验结果显示675µg重组人血清白蛋白/生长激素融合蛋白的生物活性与peg-rhgh的450µg相当,由此计算出rhsa/gh的大鼠体内生物比活性值约为4iu/mg(这还是在不考虑人血清白蛋白在大鼠体内必然会是异源体,会产生结合抗体,结合抗体则会降低药物中的gh的作用效力)。但是关键性人生长激素大鼠体内生物活性(药效)测定大鼠骨骺板宽度的增长,则rhsa/gh的生物活性是特别显著优于peg-rhgh。显示本发明的技术获得重组人血清白蛋白/生长激素融合蛋白具有意想不到的增生效果。
根据中国药典二部(2015版)以及市售的重组人生长激素(rhgh)和聚乙二醇化重组人生长激素(peg-rhgh)药品说明书,二者的生物比活性值分别约为3iu/mg和6iu/mg。1mg的peg-rhgh相当于2mg的rhgh;理论上以分子摩尔计算,则4mg的rhsa/gh(88.5kd,其中含有1个gh,分子量约22kd,占1/4)理论上应当相当于1mg的rhgh;8mg的rhsa/gh则理论上应当相当于1mg的peg-rhgh(分子量约60kd,其中含2个gh和19kd的聚乙二醇分子,但蛋白质含量检测技术决定了糖的含量是没有包含在mg重量中)。实际开展的大鼠测定,获得的结果rhsa/gh生物比活性比rhgh要高出5.3倍;比peg-rhgh的生物比活性值要高出10倍则显示通过本发明生产工艺制备的重组人血清白蛋白/生长激素融合蛋白具有意想不到高的大鼠体内生物活性。这个结果的获得是由于融合蛋白在大鼠体内的代谢过程和消除方式完全有别于rhgh和化学修饰的长效化peg-rhgh在体内的代谢过程。这个结果显示出本发明特有的临床应用价值和科学结果。
实施例13:重组人血清白蛋白/生长激素融合蛋白大鼠体内半衰期测定
使用sprague-dawley大鼠(sd,spf级,雌雄各半)。大鼠给药前一天(d-1)对大鼠体重进行了测量,其中雄鼠体重范围约为276-372g,雌鼠体重范围约为221-280g。阳性对照药1为普通注射用重组人生长激素(rhgh)(购自长春金赛公司),规格3mg/ml/支;阳性对照药2为长效peg化重组人生长激素注射液(peg-rhgh)(购自长春金赛公司),规格9mg/ml/支。供试药为本发明的重组人血清白蛋白/生长激素融合蛋白注射液,规格:5mg/0.5ml/支(蛋白质浓度为10mg/ml)。供试药给药大鼠给药时,按融合蛋白中每mg蛋白质中仅有1/4的rhgh含量计算,给药剂量均为200µg/kg。每个给药体积为300µl。给药前1h,药后的2min、0.5h、2h、4h、6h、8h、24h、48h、72h、96h、120h、168h、240h取血。采用异氟烷吸入麻醉后,眼眶静脉丛取血,每只每次采血量约0.2ml。血样采集后转移入含edta的ep管中,充分摇匀,置于碎冰中(碎冰中保存不超过2h),之后在4000rpm低温(约4℃)条件下离心10min,分离血浆,-20℃以下保存待分析。
采用美国r&dsystems公司生产的quantikineelisahumangrowthhormoneimmunoassay试剂盒开展血样的检测。结果显示rhgh的血液半衰期为1.5-2.5h,peg-rhgh的血液半衰期为18-24h,而本发明的重组人血清白蛋白/生长激素(rhsa/gh)的血液半衰期则为58-80h(见图10)。正是因为rhsa/gh在动物体内经由显著和意想不到的长代谢周期,即长血液半衰期,使得在融合蛋白上的gh得到缓慢释放,这个半衰期研究结果也很好地解释了为什么rhsa/gh实测的比理论上的大鼠生物比活性值要远远高于rhgh和peg-rhgh。
这个结果显示了本发明具有意想不到的优于所有现有市售产品或在研中的生长激素药物的长效化药物优势。这个结果也完全支持本发明生产工艺制备的重组人血清白蛋白/生长激素融合蛋白,作为药物可以期待其能达到给药频次为每2周,或每3周,甚至每4周给药一次的临床治疗的特别需求。
序列表
<110>天津林达生物科技有限公司
天津溥瀛生物技术有限公司
<120>一种用于治疗儿童矮小症的重组人血清白蛋白/生长激素融合蛋白的制备纯化方法
<160>2
<170>siposequencelisting1.0
<210>1
<211>776
<212>prt
<213>2ambystomalateralexambystomajeffersonianum
<400>1
aspalahislyssergluvalalahisargphelysaspleuglyglu
151015
gluasnphelysalaleuvalleuilealaphealaglntyrleugln
202530
glncysprophegluasphisvallysleuvalasngluvalthrglu
354045
phealalysthrcysvalalaaspgluseralagluasncysasplys
505560
serleuhisthrleupheglyasplysleucysthrvalalathrleu
65707580
arggluthrtyrglyglumetalaaspcyscysalalysglnglupro
859095
gluargasnglucyspheleuglnhislysaspaspasnproasnleu
100105110
proargleuvalargprogluvalaspvalmetcysthralaphehis
115120125
aspasnglugluthrpheleulyslystyrleutyrgluilealaarg
130135140
arghisprotyrphetyralaprogluleuleuphephealalysarg
145150155160
tyrlysalaalaphethrglucyscysglnalaalaasplysalaala
165170175
cysleuleuprolysleuaspgluleuargaspgluglylysalaser
180185190
seralalysglnargleulyscysalaserleuglnlyspheglyglu
195200205
argalaphelysalatrpalavalalaargleuserglnargphepro
210215220
lysalagluphealagluvalserlysleuvalthraspleuthrlys
225230235240
valhisthrglucyscyshisglyaspleuleuglucysalaaspasp
245250255
argalaaspleualalystyrilecysgluasnglnaspserileser
260265270
serlysleulysglucyscysglulysproleuleuglulysserhis
275280285
cysilealagluvalgluasnaspglumetproalaaspleuproser
290295300
leualaalaaspphevalgluserlysaspvalcyslysasntyrala
305310315320
glualalysaspvalpheleuglymetpheleutyrglutyralaarg
325330335
arghisproasptyrservalvalleuleuleuargleualalysthr
340345350
tyrgluthrthrleuglulyscyscysalaalaalaaspprohisglu
355360365
cystyralalysvalpheaspgluphelysproleuvalgluglupro
370375380
glnasnleuilelysglnasncysgluleuphegluglnleuglyglu
385390395400
tyrlyspheglnasnalaleuleuvalargtyrthrlyslysvalpro
405410415
glnvalserthrprothrleuvalgluvalserargasnleuglylys
420425430
valglyserlyscyscyslyshisproglualalysargmetprocys
435440445
alagluasptyrleuservalvalleuasnglnleucysvalleuhis
450455460
glulysthrprovalseraspargvalthrlyscyscysthrgluser
465470475480
leuvalasnargargprocyspheseralaleugluvalaspgluthr
485490495
tyrvalprolysglupheasnalagluthrphethrphehisalaasp
500505510
ilecysthrleuserglulysgluargglnilelyslysglnthrala
515520525
leuvalgluleuvallyshislysprolysalathrlysgluglnleu
530535540
lysalavalmetaspaspphealaalaphevalglulyscyscyslys
545550555560
alaaspasplysgluthrcysphealaglugluglylyslysleuval
565570575
alaalaserglnalaalaleuglyleupheprothrileproleuser
580585590
argleupheaspasnalametleuargalahisargleuhisglnleu
595600605
alapheaspthrtyrglngluphegluglualatyrileprolysglu
610615620
glnlystyrserpheleuglnasnproglnthrserleucyspheser
625630635640
gluserileprothrproserasnargglugluthrglnglnlysser
645650655
asnleugluleuleuargileserleuleuleuileglnsertrpleu
660665670
gluprovalglnpheleuargservalphealaasnserleuvaltyr
675680685
glyalaseraspserasnvaltyraspleuleulysaspleugluglu
690695700
glyileglnthrleumetglyargleugluaspglyserproargthr
705710715720
glyglnilephelysglnthrtyrserlyspheaspthrasnserhis
725730735
asnaspaspalaleuleulysasntyrglyleuleutyrcysphearg
740745750
lysaspmetasplysvalgluthrpheleuargilevalglncysarg
755760765
servalgluglysercysglyphe
770775
<210>2
<211>2406
<212>dna
<213>2ambystomalateralexambystomajeffersonianum
<400>2
atgaagtgggtaacctttatttcccttctttttctctttagctcggcttattccaggggt60
gtgtttcgtcgagatgcacacaagagtgaggttgctcatcggtttaaagatttgggagaa120
gaaaatttcaaagccttggtgttgattgcctttgctcagtatcttcagcagtgtccattt180
gaagatcatgtaaaattagtgaatgaagtaactgaatttgcaaaaacatgtgttgctgat240
gagtcagctgaaaattgtgacaaatcacttcataccctttttggagacaaattatgcaca300
gttgcaactcttcgtgaaacctatggtgaaatggctgactgctgtgcaaaacaagaacct360
gagagaaatgaatgcttcttgcaacacaaagatgacaacccaaacctcccccgattggtg420
agaccagaggttgatgtgatgtgcactgcttttcatgacaatgaagagacatttttgaaa480
aaatacttatatgaaattgccagaagacatccttacttttatgccccggaactccttttc540
tttgctaaaaggtataaagctgcttttacagaatgttgccaagctgctgataaagctgcc600
tgcctgttgccaaagctcgatgaacttcgggatgaagggaaggcttcgtctgccaaacag660
agactcaagtgtgccagtctccaaaaatttggagaaagagctttcaaagcatgggcagta720
gctcgcctgagccagagatttcccaaagctgagtttgcagaagtttccaagttagtgaca780
gatcttaccaaagtccacacggaatgctgccatggagatctgcttgaatgtgctgatgac840
agggcggaccttgccaagtatatctgtgaaaatcaagattcgatctccagtaaactgaag900
gaatgctgtgaaaaacctctgttggaaaaatcccactgcattgccgaagtggaaaatgat960
gagatgcctgctgacttgccttcattagctgctgattttgttgaaagtaaggatgtttgc1020
aaaaactatgctgaggcaaaggatgtcttcctgggcatgtttttgtatgaatatgcaaga1080
aggcatcctgattactctgtcgtgctgctgctgagacttgccaagacatatgaaaccact1140
ctagagaagtgctgtgccgctgcagatcctcatgaatgctatgccaaagtgttcgatgaa1200
tttaaacctcttgtggaagagcctcagaatttaatcaaacaaaattgtgagctttttgag1260
cagcttggagagtacaaattccagaatgcgctattagttcgttacaccaagaaagtaccc1320
caagtgtcaactccaactcttgtagaggtctcaagaaacctaggaaaagtgggcagcaaa1380
tgttgtaaacatcctgaagcaaaaagaatgccctgtgcagaagactatctatccgtggtc1440
ctgaaccagttatgtgtgttgcatgagaaaacgccagtaagtgacagagtcaccaaatgc1500
tgcacagaatccttggtgaacaggcgaccatgcttttcagctctggaagtcgatgaaaca1560
tacgttcccaaagagtttaatgctgaaacattcaccttccatgcagatatatgcacactt1620
tctgagaaggagagacaaatcaagaaacaaactgcacttgttgagcttgtgaaacacaag1680
cccaaggcaacaaaagagcaactgaaagctgttatggatgatttcgcagcttttgtagag1740
aagtgctgcaaggctgacgataaggagacctgctttgccgaggagggtaaaaaacttgtt1800
gctgcaagtcaagctgccttaggcttattcccaaccattcccttatcccgtctgttcgac1860
aacgctatgctccgcgcccatcgtctgcaccagctggcctttgacacctaccaggagttt1920
gaagaagcctatatcccaaaggaacagaagtattcattcctgcagaacccccagacctcc1980
ctctgtttctcagagtctattccgacaccctccaacagggaggaaacacaacagaaatcc2040
aacctagagctgctccgcatctccctgctgctcatccagtcgtggctggagcccgtgcag2100
tttctcaggagtgtcttcgccaacagcctggtgtacggcgcctctgacagcaacgtctat2160
gacctcctaaaggacctagaggaaggcatccaaacgctgatggggaggctggaagatggc2220
agcccccggactgggcagatcttcaagcagacctacagcaagttcgacacaaactcacac2280
aacgatgacgcactactcaagaactacgggctgctctactgcttcaggaaggacatggac2340
aaggtcgagacattcctgcgcatcgtgcagtgccgctctgtggagggcagctgtggcttc2400
tagtga2406
- 还没有人留言评论。精彩留言会获得点赞!