生化反应液的纯化方法、纯化的生化反应产物及其制备方法与流程
[0001]
本发明属于生化领域,具体涉及一种生化反应液的纯化方法、纯化的生化反应产物及其制备方法,特别地,生化反应液是酶促反应液,其中酶在生化反应中起到催化剂作用。
背景技术:
[0002]
随着社会的发展,绿色合成技术的推广,各种以酶为催化剂的生化反应(例如生化合成反应)越来越多,其后续纯化工艺大多数以离子交换树脂纯化作为工艺纯化的主要手段。离子交换树脂是一类带有活性基团的网状结构高分子化合物,具有交换、选择、吸收和催化等功能,广泛应用在工业高纯水制备、医药卫生、生物工程等领域。
[0003]
根据离子交换树脂所带基团的性质,可分为强酸性阳离子、弱酸性阳离子、强碱性阴离子、弱碱性阴离子、螯合性、两性及氧化还原树脂。在生物医药领域以及生化反应领域进行纯化处理所使用的离子交换树脂大多数是阳离子和/或阴离子树脂。然而,使用离子交换树脂的纯化方法需要耗费大量的水并且使用大量的酸和/或碱。
[0004]
因此需要进行积极改进纯化方法,减少纯水用量,降低酸碱使用量,减少对环境的污染,促进生物医药领域践行绿色化学,环保生产的理念。
技术实现要素:
[0005]
为了解决上述的至少一个问题,本发明提供了一种生化反应液的纯化方法、纯化的生化反应产物及其制备方法。
[0006]
具体而言,本发明提供了:
[0007]
一种生化反应液的纯化方法,包括下列步骤:
[0008]
(s1)提供含有离子以及生化反应产物的生化反应液;
[0009]
(s2)对所述生化反应液进行第一预处理,以除去生化反应液中的离子,从而得到第一预处理液;以及
[0010]
(s3)将所述预处理液通过离子交换树脂,从而得到纯化的生化反应液。
[0011]
其中,步骤(s2)可以包括通过选自离子沉淀法、酸碱沉淀法、离子树脂交换法、纳滤法以及电渗析法中的至少一者进行所述的第一预处理。
[0012]
任选地,离子可以选自硫酸根离子、钾离子、钠离子、氯离子、钙离子和/或磷酸根离子。
[0013]
其中,纯化方法还可以包括(s4)对所述第一预处理液进行第二预处理以进一步除去生化反应液中的一价离子。
[0014]
任选地,第二预处理选自超滤法以及纳滤法中的至少一者。
[0015]
任选地,纳滤的截留分子量为150-300da。
[0016]
其中,生化反应液选自酶催化反应液和发酵反应液中的至少一者。
[0017]
其中,所述方法还可以包括在步骤(s3)之前、同时或之后进行超滤以除去蛋白的
步骤。
[0018]
优选在步骤(s3)之前并且步骤(s2)之后进行超滤以除去预处理液的蛋白。
[0019]
优选地,超滤的截留蛋白为5,00-10,000da。
[0020]
其中,生化反应产物选自氨基酸、肽和蛋白之中的至少一者,优选腺苷蛋氨酸、谷胱甘肽、三磷酸腺苷和/或s-腺苷-l-高半胱氨酸。
[0021]
其中,在生化反应液中,生化反应产物的浓度4~800mm,优选为8~400mm。
[0022]
其中,通过循环反应方式和/或连续方式方式提供所述生化反应液。
[0023]
其中,纯化方法的总收率为20%~70%。
[0024]
其中纯化方法可以产生2000~4000kg/kg生化反应产物的废水,并且和/或者使用了4~30kg/kg生化反应产物的酸。
[0025]
其中,步骤(s2)还包括调节生化反应液的ph值至6~12。
[0026]
任选地,纯化方法还包括在步骤(s3)之前,调节预处理液的ph值至4-6的步骤。
[0027]
一种制备生化反应产物的方法,包括下列步骤:
[0028]
(s11)通过权利要求1-11中任一项所述的方法提供纯化的生化反应液以及
[0029]
(s12)将所述纯化的生化反应液干燥,从而得到生化反应产物。
[0030]
其中,生化反应产物的纯度可以达到90%以上。
[0031]
其中,制备生化反应产物的方法还包括在步骤(s12)之前将纯化的生化反应液浓缩的步骤,优选地,通过纳滤法和/或反渗透法进行所述浓缩步骤。
[0032]
其中,所述干燥选自结晶干燥、冷冻干燥和喷雾干燥中的至少一者。
[0033]
一种纯化的生化反应产物,其是通过任一项所述的方法获得的。
[0034]
根据本发明,生化反应产物的纯度可以为90%以上,甚至达到95%以上。
[0035]
本发明的纯化方法简单易行,是一种通用的可商业化的纯化。此外,本发明的方法还提高了产能、增加了降低了纯水用量和/或减少了酸碱使用量。例如,申请人发现,同样生产1kg生化反应产物,本发明的方法能够提高5~10%的收率,降低10%-40%的废水,节省60%-80%的无机酸或无机碱,例如浓盐酸或者浓硫酸。
[0036]
在一些情况下,本发明的方法还提高了生化反应产物的纯度,例如使得纯度提高至80%-95%。
[0037]
附图简要说明
[0038]
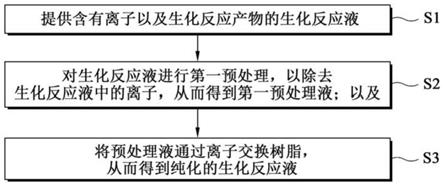
图1示出根据本发明的一个实施方案的纯化方法的流程图;
[0039]
图2示出本发明的另一个实施方案的纯化方法的流程图;
[0040]
图3示出根据本发明的一个实施方案的制备生化反应产物的方法的流程图。
具体实施方案
[0041]
以下通过具体实施方案的描述对本发明作进一步说明,但这并非是对本发明的限制,本领域技术人员根据本发明的基本思想,可以做出各种修改或改进,但是只要不脱离本发明的基本思想,均在本发明的范围之内。
[0042]
如上所述,许多生化反应产物(特别是酶催化反应产物)都用离子交换树脂进行纯化。例如,三磷酸腺苷(atp)用弱碱性阴离子交换树脂即可得到纯化处理。s-腺苷-l-高半胱氨酸以阴离子交换树脂和吸附树脂进行分离纯化,即可得到纯度高达99.5%的产品。但通
过离子交换树脂之前,含有这些产物的待处理溶液中存在大量的阴、阳离子,减少了离子交换树脂对纯化物质的吸附量,降低了离子交换树脂的效果。并且由于每次使用后,都需要用酸或碱对离子交换树脂进行再生处理,更增大了酸碱的使用量。通过数据统计分析,使用离子交换树脂进行产品纯化时,需用大量的纯化水,一般纯化1千克产品大约需要3-6吨纯化水。依此进行工业大生产,用水量和废水量将对水资源和生态环境造成很大的负担,有悖于我国现阶段的绿色环保生产理念。
[0043]
申请人发现,提高离子交换树脂的载样量,能够在生产相同数量的产物的同时,减少离子交换树脂的用量。这不仅大大降低了酸碱和纯水的用量,并且可提高产能。本发明通过在进行离子交换之前除去反应液中的离子,提高了离子交换树脂对纯化物质的吸附量,增强了离子交换树脂的效果。因此,本发明的纯化方法能够提高产能、降低纯水用量和/或减少了酸碱使用量。例如,与不对生化反应液进行预处理的现有方法相比,同样生产1kg生化反应产物,本发明的方法能够提高5~10%的收率,降低10%-40%的废水,节省60%-80%的无机酸或无机碱,例如浓盐酸或者浓硫酸。
[0044]
在一个方面中,如图1所示,本发明提供了一种生化反应液的纯化方法,包括下列步骤的步骤(s1)-(s3)。
[0045]
步骤(s1)包括提供含有离子以及生化反应产物的生化反应液。可以通过固定化酶催化反应、涉及酶的发酵反应等方法得到反应液。生化反应可是循环反应方式和连续反应方式。
[0046]
离子可以选自硫酸根离子、钾离子、钠离子、氯离子、钙离子和/或磷酸根离子。
[0047]
例如,生化反应液可以是在腺苷蛋氨酸合成酶的固定化酶催化下以atp和l-蛋氨酸为原料制备腺苷蛋氨酸得到的反应液;在固定化酶的存在下以谷氨酸、半胱氨酸和甘氨酸等作为原料制备得到的谷胱甘肽反应液等等。
[0048]
在生化反应液中,生化反应产物的浓度可以是8~400mm。生化反应液还可以包含阴离子、阳离子或者其组合。
[0049]
在将含有阴离子和/或阳离子的生化反应液进行离子交换处理之前,可以先对生化反应液进行第一预处理,以除去其中的离子(阴离子和/阳离子)。因此,如图1所示,本发明的纯化方法可以包括步骤(s2)-对所述生化反应液进行第一预处理,以除去生化反应液中的离子,从而得到第一预处理液。
[0050]
优选地,第一预处理可以通过选自纳滤法、离子沉淀法、酸碱沉淀法、离子树脂交换法、电渗析法中的至少一者进行。离子可以为阴离子和/阳离子,并且可以为硫酸根离子、钙离子、磷酸根离子、钠离子、钾离子和氯离子等。
[0051]
换言之,可以通过选自离子沉淀法、酸碱沉淀法、离子树脂交换法、电渗析法中的至少一者除去生化反应液中的离子。
[0052]
如图2所示,纯化方法还可以包括(s4)通过对生化反应液和/或第一预处理液进行第二预处理,以除去生化反应液中的一价离子,包括阳离子和/或阴离子。
[0053]
优选地,所述第二预处理选自超滤法和纳滤法中的至少一者。更优选纳滤法来除去生化反应液中的一价的阴离子和/或阳离子,纳滤的截留分子量可以为150-300da。
[0054]
第一处理和第二处理可以仅仅进行其中的一者,可以同时进行,或者先进行第一预处理然后进行第二预处理或者先进行第二预处理然后进行第一处理。
[0055]
然后,如图1所示,本发明的纯化方法还可以包括步骤(s3)-将预处理液通过离子交换树脂,从而得到纯化的生化反应液。离子交换树脂可以包括各种型号的离子交换树脂,例如阴离子交换树脂、阳离子交换树脂、强酸性阳离子、弱酸性阳离子、强碱性阴离子、弱碱性阴离子、螯合性、两性及氧化还原树脂,优选dk110树脂、hz016树脂。
[0056]
离子交换树脂的用量为产品量(生化反应液)的1%~5%。洗脱液可以为纯水、硫酸溶液、盐酸溶液,丁二磺酸溶液等。
[0057]
还可以在步骤(s3)之前、同时或之后进行超滤以除去蛋白(步骤s5),优选在步骤(s3)之前并且步骤(s2)之后进行超滤以除去预处理液的蛋白。优选地,超滤的截留蛋白为5,000-10,000da。
[0058]
在一个实施方案中,可以依次进行第一预处理以除去离子、超滤除蛋白、纳滤除去一价离子和离子交换树脂纯化的步骤。
[0059]
在一个实施方案中,步骤(s2)还可以包括调节生化反应液的ph值至6~12,优选为9~11。可以用碱性试剂或缓冲液,如氨水、碱金属氢氧化物、碱金属碳酸盐等调节生化反应液的ph值。
[0060]
在一个实施方案中,纯化方法还可以包括在步骤(s3)之前,调节预处理液的ph值至4-6的步骤。
[0061]
可以用盐酸、硫酸、缓冲液等调节预处理液的ph值。缓冲液为选自磷酸盐、草酸盐、醋酸盐、柠檬酸盐和甘氨酸中的一种或多种。
[0062]
在另一个方面中,如图3所示,本发明还提供了一种制备生化反应产物的方法,包括下列步骤:(s11)通过上述的纯化方法提供纯化的生化反应液以及(s12)将所述纯化的生化反应液干燥,从而得到生化反应产物。干燥选自结晶干燥、冷冻干燥和喷雾干燥中的至少一者。
[0063]
如图3所示,制备生化反应产物的方法还可以包括在步骤s12之前将纯化的生化反应液浓缩的步骤s13。可以通过纳滤法和/或反渗透法进行所述浓缩步骤。
[0064]
具体地,本发明的制备生化反应产物的方法可以依次包括下列步骤:
[0065]
(i)步骤s1
→
步骤s2
→
步骤s5
→
步骤s4
→
步骤s3
→
步骤s13
→
步骤s12;
[0066]
(ii)步骤s1
→
步骤s5
→
步骤s4
→
步骤s3
→
步骤s13
→
步骤s12;
[0067]
(iii)步骤s1
→
步骤s2
→
步骤s3
→
步骤s13
→
步骤s12;
[0068]
(iv)步骤s1
→
步骤s4
→
步骤s3
→
步骤s12;
[0069]
(v)步骤s1
→
步骤s2
→
步骤s5
→
步骤s3
→
步骤s13
→
步骤s12;
[0070]
(vi)步骤s1
→
步骤s2
→
步骤s4
→
步骤s3
→
步骤s13
→
步骤s12;
[0071]
(vii)步骤s1
→
步骤s2
→
步骤s3
→
步骤s13
→
步骤s12;或者
[0072]
(viii)步骤s1
→
步骤s2
→
步骤s3
→
步骤s12。
[0073]
在一个实施方案中,本发明的制备生化反应产物的方法可以包括由步骤s2和/或s4到步骤s3。
[0074]
根据本发明,生化反应产物的纯度可以为90%以上,优选95%以上。
[0075]
生化反应产物可以选自氨基酸、肽和蛋白之中的至少一者,优选腺苷蛋氨酸、谷胱甘肽、三磷酸腺苷和/或s-腺苷-l-高半胱氨酸。
[0076]
通过本发明的方法,纯化方法的总收率可以达到40%~60%。
[0077]
纯化方法可以产生2000~4000kg/kg生化反应产物的废水,并且和/或者使用了4~30kg/kg生化反应产物的无机酸或者有机酸。
[0078]
在又一个方面中,本发明还提供了一种纯化的生化反应产物,其是通过上述任意一种方法获得的。
[0079]
以下通过实例子的方式进一步解释或说明本发明内容,但这些实施例不应被理解为对本发明保护范围的限制。
[0080]
例子
[0081]
以下例子中未注明具体条件的,均按常规条件或制造商建议的条件进行。
[0082]
例子中所用材料和设备的描述如下:
[0083]
纯度分析中采用的仪器为高效液相色谱仪(hplc shimadzu lc-20ah,层析柱elite c18 4.6mm x 250mm),依照高效液相色谱法(中国药典2015版四部0512)测定;
[0084]
固定化酶均由基因港(香港)生物科技公司提供;
[0085]
超滤、纳滤、反渗透装置及其膜芯均从杭州道纳膜科技有限公司购入;
[0086]
离子交换树脂均从上海华震科技有限公司购入;
[0087]
所述其他试剂均本领域常规试剂,可从市场购入。
[0088]
制备例1制备腺苷蛋氨酸反应液
[0089]
将腺苷蛋氨酸合成酶的固定化酶装入酶柱,接入管路,设定反应温度45~65℃。将atp、l-蛋氨酸、氯化镁、kcl按照规定的比例(10:50:60:300)配成溶液,用氨水调节酸碱度至6.0~7.0。将配置好的反应原液按一定速率(2bv/h)经过酶柱,维持反应温度(45~65℃),待反应液中腺苷蛋氨酸浓度达到4.0mm以上,接收反应液,作为以下例子中的待处理料液。
[0090]
例1
[0091]
取5.35l制备例1的酶反应料液,含腺苷蛋氨酸15.2g,加入磷酸二氢钠14.0g,用氨水调ph至10,过滤的滤液用盐酸调ph至4~6,得到溶液5.4l。溶液进行超滤,压力0.2-0.6mpa,补水10l,得到透过液14.7l,产生废水0.7l。所得透过液进行纳滤,压力0.6-1.0mpa,补水28l后进行浓缩,得到浓缩液2.5l,产生废水40l。所得浓缩液2.5l经离子交换树脂(dk110),树脂量500g,按1.5-2.5bv/h流速洗脱。上样后,纯水洗脱除杂,以硫酸溶液洗脱,收集产品洗脱液1.32l,产生废水6.88l,其中含浓盐酸109.5g。
[0092]
将收集的洗脱液1.32l加入对甲苯磺酸4g和1m硫酸8ml。搅匀,最后进行冷冻干燥,得冻干产品17.5g。总收率60%,纯度92.3%,总废水量48l。
[0093]
例2
[0094]
取1.75l制备例1得到的酶反应料液,含腺苷蛋氨酸4.75g,加入磷酸二氢钠2.75g,用氨水调ph至10,过滤的滤液用盐酸调ph至4~6,得到溶液1.8l。溶液经离子交换树脂(dk110),树脂量500g,按1.5-2.5bv/h流速洗脱。上样后,纯水洗脱除杂,以硫酸溶液洗脱,收集产品洗脱液0.67l,产生废水5.43l,其中含浓盐酸100.4g。将收集的洗脱液0.67l进行纳滤,压力0.6-1.0mpa,补水10l后浓缩,得浓缩液0.8l,产生废水9.87l。
[0095]
将收集的洗脱液0.8l加入对甲苯磺酸1.1g和1m硫酸5.8ml。搅匀,最后进行冷冻干燥,得冻干品4.51g。总收率49.5%,纯度89.8%,总废水量16.2l。
[0096]
例3
[0097]
取3.6l制备例1得到的酶反应料液,含腺苷蛋氨酸10.2g,将反应液经电渗析,温度控制在10~15℃,压力控制在0.05~0.4mpa,循环1h,得到浓缩液1.2l,产生废水2.4l。浓缩液经离子交换树脂(dk110),树脂量500g,按1.5-2.5bv/h流速洗脱。上样后,纯水洗脱除杂,以硫酸溶液洗脱,收集产品洗脱液0.65l,产生废水6.4l,其中含浓盐酸100.6g。将收集的洗脱液0.65l进行纳滤,压力0.6-1.0mpa,补水25l后浓缩,得浓缩液0.75l,产生废水25.1l。
[0098]
将收集的洗脱液0.8l加入对甲苯磺酸2.3g和1m硫酸10.9ml。搅匀,最后进行冷冻干燥,得冻干品10.1g。总收率51.6%,纯度90.5%,总废水量33.5l。
[0099]
例4
[0100]
取3l制备例1的酶反应料液,含腺苷蛋氨酸8.35g,用盐酸调ph至4~6,得到溶液4.2l。将反应料液进行纳滤,压力0.6-1.0mpa,补水20l后进行浓缩,得到浓缩液1.5l,产生废水22.6l。所得浓缩液1.5l经离子交换树脂(dk110),树脂量500g,按1.5-2.5bv/h流速洗脱。上样后,纯水洗脱除杂,以硫酸溶液洗脱,收集产品洗脱液0.66l,产生废水6.5l,其中含浓盐酸99.6g。
[0101]
将收集的洗脱液0.66l加入对甲苯磺酸1.93g和1m硫酸3.8ml。搅匀,最后进行冷冻干燥,得冻干产品8.6g。总收率53.6%,纯度91.2%,总废水量29.7l。
[0102]
例5(比较例)
[0103]
取1.75l制备例1的酶反应料液,含腺苷蛋氨酸4.8g,用盐酸调ph至4~6,得到溶液2.4l。所得料液2.4l经离子交换树脂(dk110),树脂量500g,按1.5-2.5bv/h流速洗脱。上样后,纯水洗脱除杂,以硫酸溶液洗脱,收集产品洗脱液0.7l,产生废水5.25l,其中含浓盐酸102g。将收集的洗脱液0.7l进行纳滤,压力0.6-1.0mpa,补水7.8l后浓缩,得浓缩液0.65l,产生废水7.55l。
[0104]
将收集的洗脱液0.65l加入对甲苯磺酸0.75g和1m硫酸4.5ml。搅匀,最后进行冷冻干燥,得冻干产品3.3g。总收率36%,纯度90%,总废水量13.2l。
[0105]
例6
[0106]
取2.2l制备例1的酶反应料液,含腺苷蛋氨酸6.0g,用盐酸调ph至4~6,得到溶液3l。溶液进行超滤,压力0.2-0.6mpa,补水4l,得到透过液6.5l,产生废水0.8l。所得透过液进行纳滤,压力0.6-1.0mpa,补水11l后进行浓缩,得到浓缩液1l,产生废水16.2l。所得浓缩液1l经离子交换树脂(dk110),树脂量500g,按1.5-2.5bv/h流速洗脱。上样后,纯水洗脱除杂,以硫酸溶液洗脱,收集产品洗脱液0.68l,产生废水5.7l,其中含浓盐酸99g。将收集的洗脱液0.68l进行纳滤,压力0.6-1.0mpa,补水4l后浓缩,得料液2l,产生废水3.5l。
[0107]
将收集的洗脱液2l加入对甲苯磺酸1.37g和1m硫酸9ml。搅匀,最后进行冷冻干燥,得冻干产品6.06g。总收率52.7%,纯度90.8%,总废水量28.2l。
[0108]
可以看出,与比较例相比,同样生产1kg对甲苯磺酸二硫酸腺苷蛋氨酸产品,本发明的方法将降低4%~23.6%的废水,节省5~7成浓盐酸。
[0109]
制备例2制备谷胱甘肽反应液
[0110]
按照中国专利cn200710020902.1实施例3中所述的制备转化液的方法,将谷氨酸、半胱氨酸和甘氨酸等物质配置成溶液,加入到固定化酶反应罐中,保持规定的ph(8.0)和温度(37℃)进行反应,待谷胱甘肽浓度达到35mm以上时,排出反应液;然后继续配置原料液,加入反应罐中继续循环反应。收集的反应液作为以下例子中的待处理料液。
[0111]
例7
[0112]
取69l制备例2所得的料液,其中含谷胱甘肽746g,加盐酸调ph至3.5~4.5,过滤得滤液73l。滤液进行纳滤,压力0.6-1.0mpa,补水240l后再浓缩,得浓缩液36l,产生废水277l。所得浓缩液36.5l经离子交换树脂(hz016),树脂量18.5kg,按1.0~1.5bv/h流速。上柱后,纯水洗脱除杂,0.2m盐酸洗脱,收集洗脱液238l,产生废水220l,其中含浓盐酸12.6kg。将收集的洗脱液238l进行纳滤,压力0.6~1.0mpa,补水700l后浓缩,得纳滤浓缩液12l,产生废水925l。纳滤浓缩液进行反渗透,得浓缩液3.1l,产生废水9l。浓缩液搅拌下加入4倍体积乙醇结晶,后离心过滤,烘干,得产品470g。总收率63%,纯度96.0%,总废水量1430l。
[0113]
例8
[0114]
取33.5l制备例2所得的料液,其中含谷胱甘肽370g,加盐酸调ph至3.5~4.5,过滤得滤液35.1l。滤液经离子交换树脂(hz016),树脂量18.5kg,按1.0~1.5bv/h流速。上柱后,纯水洗脱除杂,0.2m盐酸洗脱,收集洗脱液235l,产生废水219l,其中含浓盐酸12.45kg。将收集的洗脱液235l进行纳滤,压力0.6~1.0mpa,补水700l后浓缩,得纳滤浓缩液14l,产生废水920l。纳滤浓缩液进行反渗透,得到浓缩液1.35l,产生废水12.5l。浓缩液搅拌下加入4倍体积乙醇结晶,后离心过滤,烘干,得产品206g。总收率55.6%,纯度94.8%,总废水量1150l。
[0115]
对比例7与例8,可以发现同样生产1kg谷胱甘肽产品时,本发明的方法将降低4-5成废水,节省5成浓盐酸。
[0116]
总之,本发明的纯化方法简单易行,是一种通用的可商业化的纯化。此外,本发明的方法还提高了产能、降低了纯水用量和/或减少了酸碱使用量。例如,申请人发现,同样生产1kg生化反应产物,本发明的方法能够提高5~10%的收率,降低10%-40%的废水,节省60%-80%的无机酸或无机碱,例如浓盐酸或者浓硫酸。
[0117]
本发明不受上述具体文字描述的限制,本发明可在权利要求书所概括的范围内做各种修改或改变。这些改变均在本发明要求保护的范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1