罗沙司他新晶型及其制备方法与流程
1.本发明属于药物化学技术领域,具体涉及罗沙司他的新晶型及其制备方法。
背景技术:
2.罗沙司他,英文名roxadustat,商品名为:可博美,分子式为:c
19
h
16
n2o5,分子量为:352.11,cas号为:808118-40-3,结构式为:
[0003][0004]
该药是由fibrogen公司开发的一种治疗肾性贫血的疾病,于2017年11月在国内申请上市,美国和欧洲正在iii期临床中,2018年下半年在美国提交nda申请。
[0005]
原研晶型专利wo2014014835报道了罗沙司他晶型a、晶型b、晶型c、晶型d、无定形、钠盐、l-精氨酸盐、l-赖氨酸盐、乙醇胺盐、二乙醇胺盐、氨丁三醇盐、钾盐、盐酸盐、硫酸盐、甲磺酸盐、双三乙胺盐、半钙盐、半镁盐。
[0006]
该专利说明书中描述,晶型a为无水合物,该晶型虽然稳定性好,但是存在溶解度差的问题。该专利说明书中描述,晶型b为半水合物,晶型b稳定性差,在25℃条件下储存1个月后完全转为晶型a。该专利说明书中描述,晶型c为六氟丙二醇溶剂合物,该晶型在环境条件下为亚稳定的溶剂合物并转化为晶型a。该专利说明书中描述,晶型d为dmso和水的共溶剂合物,该晶型在环境温度下干燥时极易转化为晶型a。该专利说明书中描述的无定形,通过旋蒸或者冷冻干燥制备,在环境条件下放置容易转为晶型a。
[0007]
现有技术wo2013013609公开了罗沙司他的晶型form i、form ii、form iii、form iv、form v、form vi、form vii。其中实施例1公开了该化合物的合成路径,从中间体4到中间体5的转化反应存在基本的技术错误,因而公开的晶型非罗沙司他的晶型。
[0008]
现有技术cn109369525a公开了晶型arz-a、晶型arz-b、晶型arz-c、晶型arz-d、晶型arz-e、晶型arz-f、晶型arz-g、晶型arz-h、晶型arz-j、晶型arz-k。晶型arz-a为一水合物,晶型arz-b为半水合物。其中晶型arz-b通过苯甲醚混合溶剂挥发制备,tg图显示在30-90℃容易脱水,该晶型不稳定。其余公开的晶型大部分为溶剂化物,不适合用于工业化生产。
[0009]
wo2019030711a专利公开了晶型γ、晶型δ、共晶l-脯氨酸、烟酰胺、尿素。其中晶型γ为甲酸-水共溶剂合物,晶型δ同cn109369525a中的晶型arz-a粉末衍射谱图相同,从晶型γ转晶得到,存在甲酸超标的风险。同时该一水合物晶型tga显示在40℃很容易失去水分,dsc显示失去水后变成晶型a,该晶型不稳定。由上述现有技术可见:罗沙司他虽然存在多种晶型,但大部分晶型存在稳定性差、溶解性差或不适宜工业化生产等问题。
[0010]
综上所述,本领域急需一种具有优异的溶解性和稳定性的罗沙司他的新晶型,以适于制剂的工业化制备及满足制剂的各种性能要求。
技术实现要素:
[0011]
本发明的目的就是提供一种既具有优异溶解性又有优异稳定性的罗沙司他的新晶型。
[0012]
本发明提供了一种罗沙司他晶型ⅰ,其特征在于其x射线粉末衍射图谱在下列2θ角处具有特征衍射峰:6.3
±
0.2
°
、12.6
±
0.2
°
、18.9
±
0.2
°
。
[0013]
本发明的一些实施方案中,所述的罗沙司他晶型ⅰ,其使用cu-kα测量的x射线粉末衍射图谱在5个或更多个选自下组的2θ角处具有特征衍射峰:6.3
±
0.2
°
、9.5
±
0.2
°
、12.6
±
0.2
°
、15.8
±
0.2
°
、18.9
±
0.2
°
、20.0
±
0.2
°
、22.2
±
0.2
°
、25.3
±
0.2
°
、25.9
±
0.2
°
、28.5
±
0.2
°
、31.8
±
0.2
°
、35.1
±
0.2
°
。
[0014]
本发明的一些实施方案中,所述的罗沙司他晶型ⅰ,其xrpd图谱如图1所示。
[0015]
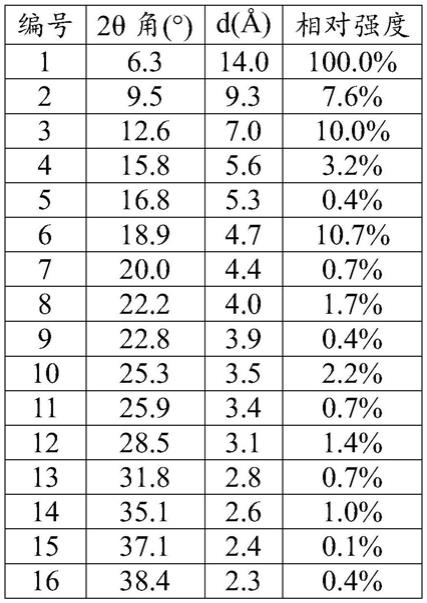
本发明的一些实施方案中,所述的罗沙司他晶型ⅰ的xrpd图谱解析数据如表1所示:
[0016]
表1.本发明的罗沙司他晶型ⅰ使用cu-kα测量的x射线粉末衍射图谱解析数据
[0017][0018]
本发明的一些实施方案中,所述的罗沙司他晶型ⅰ,其差示扫描量热曲线在124.1
±
3℃、151.7
±
3℃、211.6
±
3℃处具有吸热峰。
[0019]
本发明的一些实施方案中,所述的罗沙司他晶型ⅰ,其dsc图谱如图2所示。
[0020]
本发明的一些实施方案中,所述的罗沙司他晶型ⅰ,其热重分析曲线在118
±
3℃处失重为约1.7%,在118~180
±
3℃处失重为约3.1%。
[0021]
本发明的一些实施方案中,所述的罗沙司他晶型ⅰ,其tga图谱如图3所示。
[0022]
本发明提供了一种制备罗沙司他晶型ⅰ的方法,所述方法包括:1)将罗沙司他溶解于第一有机溶剂中;2)使用滤膜过滤后,加入第二有机溶剂;以及3)挥发析晶。
[0023]
在一个实施方式中,该第一有机溶剂是甲醇和苯甲醚的混合溶剂。
[0024]
在一个实施方式中,该第一有机溶剂是甲醇和乙酸乙酯的混合溶剂。
[0025]
在一个实施方式中,该第一有机溶剂是甲醇和丙酮的混合溶剂。
[0026]
在一个实施方式中,该第二有机溶剂是苯甲醚。
[0027]
本发明提供了一种罗沙司他晶型ⅱ,其特征在于其x射线粉末衍射图谱在下列2θ角处具有特征衍射峰:16.3
±
0.2
°
、28.3
±
0.2
°
、33.8
±
0.2
°
。
[0028]
本发明的一些实施方案中,所述的罗沙司他晶型ⅱ,其使用cu-kα测量的x射线粉末衍射图谱在5个或更多个选自下组的2θ角处具有特征衍射峰:16.3
±
0.2
°
、17.2
±
0.2
°
、22.2
±
0.2
°
、23.0
±
0.2
°
、24.8
±
0.2
°
、25.9
±
0.2
°
、28.3
±
0.2
°
、33.0
±
0.2
°
、33.8
±
0.2
°
、37.9
±
0.2
°
。
[0029]
本发明的一些实施方案中,所述的罗沙司他晶型ⅱ,其xrpd图谱如图4所示。
[0030]
本发明的一些实施方案中,所述的罗沙司他晶型ⅱ的xrpd图谱解析数据如表2所示:
[0031]
表2.本发明的罗沙司他晶型ⅱ使用cu-kα测量的x射线粉末衍射图谱解析数据
[0032][0033][0034]
本发明的一些实施方案中,所述的罗沙司他晶型ⅱ,其差示扫描量热曲线在191.1
±
3℃处具有放热峰,在212.1
±
3℃处具有吸热峰。
[0035]
本发明的一些实施方案中,所述的罗沙司他晶型ⅱ,其dsc图谱如图5所示。
[0036]
本发明的一些实施方案中,所述的罗沙司他晶型ⅱ,其热重分析曲线在198
±
3℃处失重为约0.09%。
[0037]
本发明的一些实施方案中,所述的罗沙司他晶型ⅱ,其tga图谱如图6所示。
[0038]
本发明提供了一种制备罗沙司他晶型ⅱ的方法,所述方法包括:将晶型ⅰ加热至175℃,失去溶剂后得晶型ⅱ。
[0039]
本发明提供了一种罗沙司他晶型ⅲ,其特征在于其x射线粉末衍射图谱在下列2θ角处具有特征衍射峰:5.0
±
0.2
°
、24.9
±
0.2
°
、27.4
±
0.2
°
。
[0040]
本发明的一些实施方案中,所述的罗沙司他晶型ⅲ,其使用cu-kα测量的x射线粉末衍射图谱在5个或更多个选自下组的2θ角处具有特征衍射峰:5.0
±
0.2
°
、11.3
±
0.2
°
、16.3
±
0.2
°
、17.4
±
0.2
°
、18.5
±
0.2
°
、19.0
±
0.2
°
、21.0
±
0.2
°
、21.6
±
0.2
°
、22.2
±
0.2
°
、24.9
±
0.2
°
、27.4
±
0.2
°
、32.1
±
0.2
°
。
[0041]
本发明的一些实施方案中,所述的罗沙司他晶型ⅲ,其xrpd图谱如图7所示。
[0042]
本发明的一些实施方案中,所述的罗沙司他晶型ⅲ的xrpd图谱解析数据如表3所示:
[0043]
表3.本发明的罗沙司他晶型ⅲ使用cu-kα测量的x射线粉末衍射图谱解析数据
[0044][0045]
本发明的一些实施方案中,所述的罗沙司他晶型ⅲ,其差示扫描量热曲线在210.7
±
3℃处具有吸热峰。
[0046]
本发明的一些实施方案中,所述的罗沙司他晶型ⅲ,其dsc图谱如图8所示。
[0047]
本发明的一些实施方案中,所述的罗沙司他晶型ⅲ,其热重分析曲线在145
±
3℃处失重为约0.4%。
[0048]
本发明的一些实施方案中,所述的罗沙司他晶型ⅲ,其tga图谱如图9所示。
[0049]
本发明提供了一种制备罗沙司他晶型ⅲ的方法,所述方法包括:将晶型ⅰ或晶型ⅱ加热至200℃,得无水晶型ⅲ。
[0050]
本发明还提供了上述罗沙司他晶型在制备用于治疗贫血的药物中的应用。
附图说明
[0051]
图1显示本发明的罗沙司他晶型ⅰ的x射线粉末衍射图谱。
[0052]
图2显示本发明的罗沙司他晶型ⅰ的差示扫描量热曲线。
[0053]
图3显示本发明的罗沙司他晶型ⅰ的热重分析曲线。
[0054]
图4显示本发明的罗沙司他晶型ⅱ的x射线粉末衍射图谱。
[0055]
图5显示本发明的罗沙司他晶型ⅱ的差示扫描量热曲线。
[0056]
图6显示本发明的罗沙司他晶型ⅱ的热重分析曲线。
[0057]
图7显示本发明的罗沙司他晶型ⅲ的x射线粉末衍射图谱。
[0058]
图8显示本发明的罗沙司他晶型ⅲ的差示扫描量热曲线。
[0059]
图9显示本发明的罗沙司他晶型ⅲ的热重分析曲线。
具体实施方式
[0060]
下面结合附图和实施例对本发明进行进一步的说明。但应理解,这些实施例仅仅是用于更详细具体地说明本发明,而不应理解为用于以任何形式限定本发明。
[0061]
本发明实施例中所使用的试剂和采用的方法均是本领域的常规试剂和常规方法。本领域技术人员应当清楚,在下文中,如未特别说明,温度以摄氏度(℃)表示,操作温度在室温环境下进行,所示室温是指10℃~30℃,优选20℃~25℃;所述熔点的可允许误差在
±
1%;所述的收率为质量百分比。
[0062]
实验方法
[0063]
1.x射线粉末衍射(x-ray powder diffraction,xrpd)
[0064]
晶型的xrpd数据由布鲁克公司(d8 advance)测定,衍射参数如下:
[0065]
x射线:cu,kα,1.54060
[0066]
x射线光管设定:40kv,25ma
[0067]
发散狭缝:自动
[0068]
单色器:无
[0069]
扫描模式:连续
[0070]
扫描范围(
°
2theta):4
°-
40
°
[0071]
扫描速度(秒/步):0.5
[0072]
2.差示扫描量热分析(differential scanning calorimeter,dsc)
[0073]
晶型的dsc数据由ta(dsc 25)型差示扫描量热仪测定,热分析参数如下:
[0074]
温度范围(℃):30-250
[0075]
扫描速率(℃/分钟):10
[0076]
保护气体:氮气
[0077]
3.热重分析(thermogravimetric analysis,tga)
[0078]
晶型的tga数据由ta(tga 550)仪器测定,热分析参数如下:
[0079]
温度范围(℃):30-350℃
[0080]
扫描速率(℃/分钟):10
[0081]
保护气体:氮气
[0082]
技术效果
[0083]
本发明的晶型的含水量低、纯度高、溶解性好、产品稳定性高。
[0084]
实施例
[0085]
以下实施例仅用于说明本发明的具体实施方式,而非任何对本发明的限制。
[0086]
实施例1罗沙司他晶型ⅰ的制备
[0087]
将50mg罗沙司他溶解于2ml苯甲醚和0.5ml甲醇中,过滤膜,滴加20ml苯甲醚,敞口缓慢挥发,得晶体为晶型ⅰ。通过上文所述方法测定该晶型的x射线粉末衍射图谱、差示扫描量热曲线和热重分析曲线。
[0088]
实施例2罗沙司他晶型ⅰ的制备
[0089]
将80mg罗沙司他溶解于2ml乙酸乙酯和0.5ml甲醇中,过滤膜,滴加20ml苯甲醚,敞口缓慢挥发,得晶体为晶型ⅰ。
[0090]
实施例3罗沙司他晶型ⅰ的制备
[0091]
将80mg罗沙司他溶解于2ml丙酮和1ml甲醇中,过滤膜,滴加20ml苯甲醚,敞口缓慢挥发,得晶体为晶型ⅰ。
[0092]
实施例4罗沙司他晶型ⅱ的制备
[0093]
将晶型ⅰ的5mg加热至175℃,失去溶剂后得晶型ⅱ。通过上文所述方法测定该晶型的x射线粉末衍射图谱、差示扫描量热曲线和热重分析曲线。
[0094]
实施例5罗沙司他晶型ⅲ的制备
[0095]
将晶型ⅰ或晶型ⅱ的5mg加热至200℃,得无水晶型ⅲ。通过上文所述方法测定该晶型的x射线粉末衍射图谱、差示扫描量热曲线和热重分析曲线。
[0096]
实施例6稳定性实验
[0097]
取晶型ii和晶型iii以及原研晶型a进行了稳定性试验,实验结果如下:
[0098][0099]
稳定性实验结果显示,晶型ii和晶型iii在有关物质与原研晶型可达到同等效果,同时晶型稳定。
[0100]
实施例7溶解度实验
[0101]
按照药典测溶解性方法,称取供试品细粉,于25℃
±
2℃加入一定量溶剂中,每隔5分钟强力振摇30秒,观察30分钟内的溶解情况,如无目视可见颗粒或液滴时,即视为完全溶解。
[0102][0103]
根据溶解度结果,晶型iii在水中溶解度提高2~3倍,晶型ii在水中溶解度提高8~10倍,具有明显改善该药物溶解性作用,可以达到提高体内生物利用度。
[0104]
应理解,以上实施例只用于对本发明进行进一步说明,而非对本发明保护范围的限制,本领域的技术人员根据本发明的上述内容做出的一些非本质的改进和调整均属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1