用于稳定腔肠素及其类似物和衍生物的组合物和方法与流程
相关申请的交叉引用本申请要求2018年10月3日提交的美国临时专利申请第62/740,622号和2019年2月14日提交的美国临时专利申请第62/805,517号的优先权和权益,所述申请各自通过引用整体且出于所有目的并入本文中。发明领域本文提供用于稳定腔肠素及其类似物和衍生物以及用于改善腔肠素及其类似物和衍生物的溶解性和重构效率的组合物和方法。
背景技术:
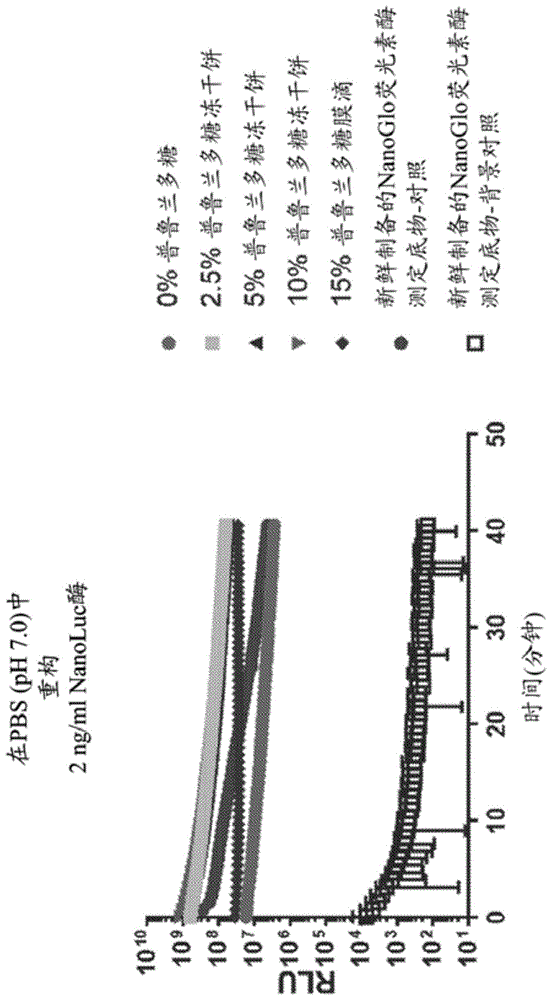
:发光在生物测定中用作报道分子活性的量度。报道分子进而将发光测量值与诸如转录(基因表达)、翻译(蛋白质表达)、蛋白质-蛋白质相互作用等目标生物过程相联系,从而允许定量测量生物过程中发生的变化。报道分子通常是发光酶(例如,萤火虫荧光素酶、海肾荧光素酶、刺虾荧光素酶等),当提供有其发光底物时,其导致光的产生(即发光)。技术实现要素:诸如腔肠素及其类似物和衍生物的发光底物在储存(例如,在有机溶剂中储存、在较高温度下储存、在不恰当的ph下储存等)期间会分解,从而导致在添加到或用于生物测定之前底物的损失。这样的分解可能是发光底物在溶液中以温度依赖性方式随时间的不稳定性的结果。这种分解导致发光底物的浪费以及源自采用分解的发光底物的生物测定的发光测量的灵敏度和再现性降低。这种分解的产物也抑制发光反应。另外,一些腔肠素在不同的测定缓冲液中或直接进入的测试样品中具有低溶解度,或者在不同的测定缓冲液中可能表现出不一致的重构。虽然腔肠素可在稀释到适当的缓冲溶液中之前溶解在有机溶剂中,但是腔肠素化合物的有机溶液可能在储存中遭受不稳定性(热不稳定性和光不稳定性两种)。然而,尽管固体腔肠素和腔肠素类似物和衍生物(例如,呋瑞吗嗪(furimazine))比其有机溶液显著更稳定,但它们表现出极差的重构速度和效率,溶解不一致,并且难以直接用于测定和其他方法中,尤其是当需要非有机溶剂时。这些缺点极大地限制了已开发出腔肠素及其类似物和衍生物的应用的数量和类型。因此,需要用于稳定发光底物、改善发光底物的溶解性和/或增加发光底物的重构效率的新组合物和/或方法。特别地,具有改善的物理特性和/或溶解性的底物对于长期储存(例如,在室温下≥12个月)、对一种或多种测定形式的相容性、稳健性和用户友好性是有益的。本文提供用于稳定和改善诸如腔肠素或其类似物或衍生物的发光底物的溶解性和/或重构效率的组合物和方法。使用hplc、吸光度和质谱分析执行不同固体组合物、制剂和形式内底物的化学完整性和/或重构效率的表征。通过在酶存在下经由相对光单位(rlu)监测生物发光执行在测定相关条件下底物的额外功能表征。本文提供包含选自腔肠素及其类似物或衍生物的化合物和聚合物的组合物。在一些实施方案中,所述化合物选自腔肠素、腔肠素-h、腔肠素-h-h、呋瑞吗嗪、jrw-0238、jrw-1743和jrw-1744。在一些实施方案中,所述化合物为呋瑞吗嗪。在一些实施方案中,所述化合物为jrw-0238。在一些实施方案中,所述化合物为jrw-1743。在一些实施方案中,所述化合物为jrw-1744。在一些实施方案中,所述聚合物为天然存在的生物聚合物。在一些实施方案中,所述天然存在的生物聚合物选自普鲁兰多糖、海藻糖、麦芽糖、纤维素、右旋糖酐及其任意组合。在一些实施方案中,所述天然存在的生物聚合物为普鲁兰多糖。在一些实施方案中,所述聚合物为环状糖聚合物或其衍生物。在一些实施方案中,所述聚合物为羟丙基β-环糊精。在一些实施方案中,所述聚合物为合成聚合物。在一些实施方案中,所述合成聚合物选自聚苯乙烯、聚(甲基)丙烯酸酯及其任意组合。在一些实施方案中,所述合成聚合物为包含至少一种聚(氧丙烯)嵌段和至少一种聚(氧乙烯)嵌段的嵌段共聚物。在一些实施方案中,所述合成聚合物为泊洛沙姆。在一些实施方案中,所述组合物还包含缓冲液、表面活性剂、还原剂、盐、自由基清除剂、螯合剂、蛋白质或其任意组合。在一些实施方案中,所述组合物还包含选自磷酸盐缓冲液、三(羟甲基)甲基甘氨酸(tricine)和2-(n-吗啉代)乙磺酸的缓冲液。在一些实施方案中,所述组合物还包含选自聚山梨酸酯20、聚山梨酸酯40和聚山梨酸酯80的表面活性剂。在一些实施方案中,所述组合物包含选自硫脲和6-氮杂-2-硫代胸腺嘧啶的还原剂。在一些实施方案中,所述组合物还包含选自氯化钠和磷酸钠的盐。在一些实施方案中,所述组合物还包含选自抗坏血酸和抗坏血酸钠的自由基清除剂。在一些实施方案中,所述组合物还包含螯合剂,并且所述螯合剂选自柠檬酸和反-1,2-二氨基环己烷-四乙酸。在一些实施方案中,所述组合物还包含选自牛血清白蛋白、明胶和猪来源的高度纯化的真皮胶原的多肽级分的蛋白质。在一些实施方案中,所述组合物呈冻干粉或饼的形式。在一些实施方案中,所述组合物呈可延展膜的形式。在一些实施方案中,所述组合物为溶液。本文提供包含以下的组合物:选自腔肠素及其类似物或衍生物的化合物;和选自纸或纤维基质、塑料、玻璃或金属的表面。在一些实施方案中,所述化合物选自腔肠素、腔肠素-h、腔肠素-h-h、呋瑞吗嗪、jrw-0238、jrw-1743和jrw-1744。在一些实施方案中,所述化合物为呋瑞吗嗪。在一些实施方案中,所述化合物为jrw-0238。在一些实施方案中,所述化合物为jrw-1743。在一些实施方案中,所述化合物为jrw-1744。在一些实施方案中,所述组合物还包含聚合物。在一些实施方案中,所述聚合物为天然存在的生物聚合物。在一些实施方案中,所述天然存在的生物聚合物选自普鲁兰多糖、海藻糖、麦芽糖、纤维素、右旋糖酐及其任意组合。在一些实施方案中,所述天然存在的生物聚合物为普鲁兰多糖。在一些实施方案中,所述聚合物为环状糖聚合物或其衍生物。在一些实施方案中,所述聚合物为羟丙基β-环糊精。在一些实施方案中,所述聚合物为合成聚合物。在一些实施方案中,所述合成聚合物选自聚苯乙烯、聚(甲基)丙烯酸酯及其任意组合。在一些实施方案中,所述合成聚合物为包含至少一种聚(氧丙烯)嵌段和至少一种聚(氧乙烯)嵌段的嵌段共聚物。在一些实施方案中,所述合成聚合物为泊洛沙姆。在一些实施方案中,所述组合物还包含缓冲液、表面活性剂、还原剂、盐、自由基清除剂、蛋白质或其任意组合。在一些实施方案中,所述组合物还包含选自磷酸盐缓冲液、三(羟甲基)甲基甘氨酸和2-(n-吗啉代)乙磺酸的缓冲液。在一些实施方案中,所述组合物还包含选自聚山梨酸酯20、聚山梨酸酯40和聚山梨酸酯80的表面活性剂。在一些实施方案中,所述组合物包含选自硫脲和6-氮杂-2-硫代胸腺嘧啶的还原剂。在一些实施方案中,所述组合物还包含选自氯化钠和磷酸钠的盐。在一些实施方案中,所述组合物还包含选自抗坏血酸和抗坏血酸钠的自由基清除剂。在一些实施方案中,所述组合物还包含螯合剂,并且所述螯合剂选自柠檬酸和反-1,2-二氨基环己烷-四乙酸。在一些实施方案中,所述组合物还包含选自牛血清白蛋白、明胶和猪来源的高度纯化的真皮胶原的多肽级分的蛋白质。在一些实施方案中,所述表面选自纤维素纸、硝化纤维素纸、尼龙纸、棉纸、聚酯纸、羧甲基纤维素钠、多孔或聚合物膜、高纯度棉纤维、棉/人造丝混纺的高纯度棉和玻璃超细纤维。本文提供稳定选自腔肠素及其类似物或衍生物的化合物的方法,其包括使所述腔肠素化合物或其类似物或衍生物与有效量的所述聚合物和/或所述纸或纤维基质接触以形成组合物。在一些实施方案中,使所述化合物稳定以防止热分解、化学分解、光诱导的分解或其任意组合。本文提供改善选自腔肠素及其类似物或衍生物的化合物的溶解性的方法,其包括使所述腔肠素化合物或其类似物或衍生物与有效量的所述聚合物和/或所述纸或纤维基质接触以形成组合物。在一些实施方案中,与尚未与所述聚合物和/或所述纸或纤维基质接触的化合物相比,所述化合物在水溶液中的溶解性得到改善。本文提供改善选自腔肠素及其类似物或衍生物的化合物的重构速率的方法,其包括使所述腔肠素化合物或其类似物或衍生物与有效量的所述聚合物和/或所述纸或纤维基质接触以形成组合物,其中与尚未与所述聚合物或所述纸或纤维基质接触的化合物相比,所述化合物的重构速率得到改善。在一些实施方案中,所述化合物选自腔肠素、腔肠素-h、腔肠素-h-h、呋瑞吗嗪、jrw-0238、jrw-1743和jrw-1744。在一些实施方案中,所述化合物为呋瑞吗嗪。在一些实施方案中,所述化合物为jrw-0238。在一些实施方案中,所述化合物为jrw-1743。在一些实施方案中,所述化合物为jrw-1744。在一些实施方案中,所述聚合物为天然存在的生物聚合物。在一些实施方案中,所述天然存在的生物聚合物选自普鲁兰多糖、海藻糖、麦芽糖、纤维素、右旋糖酐及其任意组合。在一些实施方案中,所述天然存在的生物聚合物为普鲁兰多糖。在一些实施方案中,所述聚合物为环状糖聚合物或其衍生物。在一些实施方案中,所述聚合物为羟丙基β-环糊精。在一些实施方案中,所述聚合物为合成聚合物。在一些实施方案中,所述合成聚合物选自聚苯乙烯、聚(甲基)丙烯酸酯及其任意组合。在一些实施方案中,所述合成聚合物为包含至少一种聚(氧丙烯)嵌段和至少一种聚(氧乙烯)嵌段的嵌段共聚物。在一些实施方案中,所述合成聚合物为泊洛沙姆。在一些实施方案中,所述组合物还包含缓冲液、表面活性剂、还原剂、盐、自由基清除剂、蛋白质或其任意组合。在一些实施方案中,所述组合物还包含选自磷酸盐缓冲液、三(羟甲基)甲基甘氨酸和2-(n-吗啉代)乙磺酸的缓冲液。在一些实施方案中,所述组合物还包含选自聚山梨酸酯20、聚山梨酸酯40和聚山梨酸酯80的表面活性剂。在一些实施方案中,所述组合物包含选自硫脲和6-氮杂-2-硫代胸腺嘧啶的还原剂。在一些实施方案中,所述组合物还包含选自氯化钠和磷酸钠的盐。在一些实施方案中,所述组合物还包含选自抗坏血酸和抗坏血酸钠的自由基清除剂。在一些实施方案中,所述组合物还包含螯合剂,并且所述螯合剂为柠檬酸。在一些实施方案中,所述组合物还包含选自牛血清白蛋白、明胶和猪来源的高度纯化的真皮胶原的多肽级分的蛋白质。在一些实施方案中,所述纸或纤维基质选自纤维素纸、硝化纤维素纸、尼龙纸、棉纸、聚酯纸、羧甲基纤维素钠、多孔或聚合物膜、高纯度棉纤维、棉/人造丝混纺的高纯度棉和玻璃超细纤维。在一些实施方案中,所述接触步骤包括:将所述化合物溶解在有机溶剂中以形成第一溶液;将所述第一溶液与所述聚合物和/或所述纸或纤维基质混合以形成混合物;和干燥所述混合物。在一些实施方案中,所述混合步骤包括将所述聚合物溶解在第二溶液中和将所述第二溶液与第一溶液混合。在一些实施方案中,所述混合步骤包括将第一溶液施加到纸或纤维基质。在一些实施方案中,所述干燥步骤包括冻干。在一些实施方案中,所述干燥步骤包括空气干燥。在一些实施方案中,所述干燥在环境温度下在惰性气氛中进行。在一些实施方案中,所述干燥包括真空干燥。在一些实施方案中,所述干燥在约30℃至约70℃的温度下进行。在一些实施方案中,将一种或所有溶液脱氧。在一些实施方案中,所述方法包括使所述化合物与所述聚合物接触。在一些实施方案中,所述方法包括使所述聚合物与所述纸或纤维基质接触。在一些实施方案中,所述方法包括使所述聚合物与所述聚合物和所述纸或纤维基质接触。本文提供包含本文公开的组合物中的任一种的试剂盒。在一些实施方案中,所述组合物被容纳在一个或多个容器中。在一些实施方案中,所述组合物被容纳在多个管中。在一些实施方案中,所述组合物呈多个纸斑点的形式,每个斑点具有约2mm至约5mm的直径。附图说明图1a至图1c显示当如实施例1中所述在(a)磷酸盐缓冲盐水(pbs),ph7.0和(b)荧光素酶测定缓冲液中测试根据本公开的组合物的发光输出时的信号动力学。图1(c)显示基于普鲁兰多糖的冻干饼和普鲁兰多糖膜-滴制剂中呋瑞吗嗪底物样品的图像。图2a至图2c显示当如实施例1中所述在pbs,ph7.0中测试根据本公开的组合物的发光输出时在添加纯化的酶之后在不同时间点的rlu值。图3a至图3c显示当如实施例1中所述在荧光素酶测定缓冲液中测试根据本公开的组合物的发光输出时在添加纯化的酶之后在不同时间点的rlu值。图4a至图4c显示当如实施例2中所述在pbs,ph6.8中测试根据本公开的组合物在210-600nm范围内的吸光度时,在水溶液中的吸光度值。图5显示证明如实施例3中所述根据本公开的组合物重构到pbs,ph7.0中的能力的图像。图6a至图6b显示如实施例4中所述在pbs,ph6.8中的普鲁兰多糖在210-600nm范围内的吸光度值。图7a至图7b显示如实施例5中所述含有呋瑞吗嗪的基于0%w/v普鲁兰多糖的冻干饼制剂在重构后(a)0小时和(b)5小时的代表性hplc迹线。图8a至图8b显示如实施例5中所述含有呋瑞吗嗪的基于2.5%w/v普鲁兰多糖的冻干饼制剂在重构后(a)0小时和(b)5小时的代表性hplc迹线。图9a至图9b显示如实施例5中所述含有呋瑞吗嗪的基于15%w/v普鲁兰多糖的冻干饼制剂在重构后(a)0小时和(b)5小时的代表性hplc迹线。图10a至图10b显示如实施例5中所述荧光素酶测定底物在重构后(a)0小时和(b)5小时的代表性hplc迹线。图11a至图11b显示如实施例5所述含有或不含普鲁兰多糖的配制的呋瑞吗嗪样品的hplc迹线分析,显示:(a)254nm处的吸光度随时间的变化和(b)峰面积随时间的变化。图12显示来自如实施例5中所述含有或不含普鲁兰多糖的配制的呋瑞吗嗪样品的hplc迹线的数据,显示氨基吡嗪降解产物随时间的产生。图13a至图13c显示:(a)当如实施例6中所述测试组合物的发光输出时,rlu值的动力学分析;(b)当如实施例6中所述测试组合物的发光输出时,在时间零的rlu值;以及(c)如实施例6中所述制备的由冲孔903蛋白保存卡产生的纸斑点的图像。图14a至图14b显示其中如实施例7中进一步描述配制的呋瑞吗嗪样品干燥到903蛋白保存卡上且(a)在4℃下保持2周或(b)在4℃或25℃下保持3个月的样品的图像。图15a至图15d显示证明如实施例8中所述添加剂对干燥到由冲孔903蛋白保存卡产生的纸斑点的配制的呋瑞吗嗪样品的测定性能的影响的数据。图16显示证明如实施例9中所述制备的由冲孔903蛋白保存卡产生的纸斑点中的配制的呋瑞吗嗪样品的rlu输出的数据。图17a至图17c显示证明如实施例9中所述在由冲孔903蛋白保存卡产生且在(a)4℃、(b)25℃和(c)37℃下储存一天之后测试的纸斑点中的呋瑞吗嗪样品的rlu输出的数据。图18a至图18c显示证明如实施例9中所述在由冲孔903蛋白保存卡产生且在(a)4℃、(b)25℃和(c)37℃下储存三天之后测试的纸斑点中的配制的呋瑞吗嗪样品的rlu输出的数据。图19a至图19d显示如实施例10中所述置于由冲孔903蛋白保存卡产生且用不同的蛋白缓冲液预处理的纸斑点中的配制的呋瑞吗嗪样品的数据以及用纯化的酶测试的活性,显示在(a)60℃和(b)25℃下储存斑点后的rlu输出,以及在(c)60℃和(d)25℃下储存斑点后随时间而变的%活性。图20a至图20d显示如实施例10中所述在25℃或60℃下储存的数天内在由冲孔903蛋白保存卡产生的纸斑点中的配制的呋瑞吗嗪样品的rlu输出以及测试的底物活性的加速的稳定性数据,显示在(a)60℃和(b)25℃下储存斑点后的rlu输出,以及在(c)60℃和(d)25℃下储存斑点后随时间而变的%活性。图21a至图21c显示证明如实施例11中所述在由冲孔903蛋白保存卡产生且使用不同的干燥方法制备的纸斑点中的配制的呋瑞吗嗪样品的rlu输出的数据。图22a至图22d显示证明如实施例11中所述在由冲孔903蛋白保存卡产生且使用不同的干燥方法制备的纸斑点中的配制的呋瑞吗嗪样品随天数而变的rlu输出和%活性的数据。图23a至图23b显示如实施例12中所述在60℃下储存a–0小时和b–48小时后代表性的基于普鲁兰多糖的冻干呋瑞吗嗪样品的hplc迹线。图24a至图24b显示如实施例12中所述市售荧光素酶测定底物样品在储存(在60℃下,图24a,0小时,和图24b,48小时)后的hplc迹线。图25a至图25d显示hplc数据的分析,显示如实施例12中所述配制的呋瑞吗嗪样品作为原始面积(图25a,在25℃下,和图25b,在60℃下)和作为%面积(图25c,在25℃下,和图25d,在60℃下)的热稳定性。图26a至图26f显示在呋瑞吗嗪样品储存之后用纯化的测试的配制的呋瑞吗嗪样品的rlu数据。图26a至图26c显示在重构之前在60℃下储存不同时间且使用50μm底物(a)、10μm底物(b)和0.1μm底物(c)测试的样品的数据;图26d至图26f显示在重构之前在25℃下储存不同时间且使用50μm底物(d)、10μm底物(e)和0.1μm底物(f)测试的样品的数据,如实施例12中所述。图27a至图27f显示当呋瑞吗嗪样品储存之后用纯化的酶测试配制的呋瑞吗嗪样品的活性时在时间零的%底物活性。图27a至图27c显示在重构之前在60℃下储存不同时间且使用50μm底物(a)、10μm底物(b)和0.1μm底物(c)测试的样品的数据;图27d至图27f显示在重构之前在25℃下储存不同时间且使用50μm底物(d)、10μm底物(e)和0.1μm底物(f)测试的样品的数据,如图12中所述。图28a至图28c显示如实施例13中所述当用纯化的酶测试时含有呋瑞吗嗪底物的配制的普鲁兰多糖膜涂覆的96孔微量滴定板的rlu数据。图29显示如实施例13中所述在普鲁兰多糖膜基质内涂覆标准96孔微量滴定板底部的含呋瑞吗嗪的基于普鲁兰多糖的膜形式的代表性实例。图30a至图30c显示在与酶反应或对于同时放置有酶和呋瑞吗嗪制剂的孔用pbs简单重构之后附着到标准96孔微量滴定板的底部的仅含有呋瑞吗嗪或还含有酶的基于普鲁兰多糖的膜的代表性实例的数据;图30a显示原始rlu;图30b显示%活性;且图30c显示10天内的%活性,如实施例13所述。图31a至图31f显示如实施例14中所述与市售呋瑞吗嗪产品相比,对于每种条件在25℃(第一条)或60℃(第二条)下储存之后制备为基于普鲁兰多糖的冻干饼的呋瑞吗嗪的降解产物的归一化吸光度。图32a至图32f显示如实施例14中所述与市售呋瑞吗嗪产品相比,对于每种条件在25℃(第一条)或60℃(第二条)下储存之后制备为基于普鲁兰多糖的冻干饼的呋瑞吗嗪的降解产物的相对面积百分比。图33a至图33b显示如实施例15中所述在室温下储存6个月的含有呋瑞吗嗪的基于普鲁兰多糖的形式的代表性实例的数据。图34a至图34c显示如实施例16中所述在不同类型的纸基质上干燥的呋瑞吗嗪样品的hplc分析的代表性实例。图35a至图35b显示重构后在三种不同固相材料上用报道蛋白lgtrip配制的呋瑞吗嗪样品的生物发光信号的代表性实例。图36a至图36c显示如实施例17中所述的在不同类型的纸基质上作为与抗坏血酸的1:1混合物储存的呋瑞吗嗪样品的hplc分析的代表性实例。图37a至图37c显示如实施例18中所述储存在用30%柠檬酸预处理的纸基质上的呋瑞吗嗪样品的hplc分析的代表性实例。图38a至图38c显示如实施例19中所述在将纸基质用水预处理并在减压下干燥过夜之后储存在所述基质上的呋瑞吗嗪样品的hplc分析的代表性实例。图39a至图39d显示如实施例20中所述在不同的纸基质上作为与柠檬酸的1:1混合物储存的呋瑞吗嗪的hplc分析的代表性实例。图40a至图40c显示由冲孔903蛋白保存卡产生且使用不同干燥方法制备的903纸斑点之中(底部)的配制的呋瑞吗嗪样品的maxrlu(顶部)和%活性,所述干燥方法是如实施例21中所述在存在或不存在蛋白缓冲液的情况下用以1:1摩尔比的呋瑞吗嗪与柠檬酸盐或抗坏血酸盐处理。图41显示证明如实施例22中所述在不同条件下储存且在25℃下储存的数天内取样的由冲孔903蛋白保存卡产生的纸斑点中的配制的呋瑞吗嗪样品的rlu输出和数天内的%活性的数据。图42显示证明如实施例23中所述在从原始孔中移除由冲孔903蛋白保存卡产生的纸斑点之前和之后在纸斑点中的配制的呋瑞吗嗪样品的rlu输出和%信号恢复的数据,确定底物是否从固体基质支撑物上释放。图43a至图43c显示证明如实施例24中所述在由冲孔903蛋白保存卡产生的纸斑点中含有不同糖或聚合物组分以及在存在或不存在抗坏血酸盐的情况下在变化的ph下的各种配制的呋瑞吗嗪溶液的rlu输出和%活性的数据。图44a至图44c显示证明如实施例25中所述在由冲孔903蛋白保存卡产生的纸斑点中在固定ph=7.0下各种配制的呋瑞吗嗪溶液组分的rlu输出和%活性的数据。图45a至图45b显示证明如实施例26中所述在由冲孔903蛋白保存卡产生且在25℃下储存数天内取样的纸斑点中各种配制的呋瑞吗嗪溶液的rlu输出的数据。图46a至图46b显示证明如实施例27中所述在由冲孔903蛋白保存卡产生且在25℃下储存数天内取样的纸斑点中含有prionex、抗坏血酸盐和/或att的各种配制的呋瑞吗嗪溶液的rlu输出的数据。图47a至图47b显示证明如实施例28中所述的已经直接冻干到96孔微量滴定板中的呋瑞吗嗪制剂的rlu输出的数据。图48显示如实施例29中所述其中呋瑞吗嗪制剂置于多层装置的一层中的示例性分层测定形式的组件的预示性图。图49显示证明如实施例30中所述在37℃下含有抗坏血酸钠的底物(promega目录号n113)制剂的rlu输出的数据。图50显示证明如实施例31中所述含有羟丙基-β-环糊精且冻干的底物(promega目录号n113)制剂的rlu输出的数据。图51a至图51b显示证明如实施例32中所述含有具体单独或组合的缓冲液添加剂的底物(promega目录号n113)制剂的rlu输出的数据。图52显示证明如实施例33中所述含有普鲁兰多糖和羟丙基-β-环糊精的混合聚合物的底物(promega目录号n113)制剂的rlu输出的数据。图53显示如实施例34中所述配制的底物的代表性实例的图像。图54a至图54c显示如实施例34中所述用f-127配制的jrw-0238的样品的hplc分析的代表性实例。图55a至图55c显示如实施例35中所述用f-127配制的呋瑞吗嗪的样品的hplc分析的代表性实例。图56显示如实施例36中所述用f-127配制的jrw-0238的溶液样品的代表性图像。图57显示如实施例36中所述用f-127配制的jrw-0238的样品的hplc分析的代表性实例。图58a至图58b显示如实施例37中所述用f-127配制的jrw-0238的样品的代表性图像。图59a至图59b显示如实施例38中所述配制的jrw-0238的样品的代表性图像。图60a至图60b显示如实施例38中所述来自腹膜内注射重构的配制的jrw-0238的小鼠的迹线和图像。图61a至图61b显示如实施例38中所述来自皮下注射重构的配制的jrw-0238的小鼠的迹线和图像。图62a至图62b显示如实施例39中所述在按比例放大和制造后在琥珀色玻璃小瓶内配制的呋瑞吗嗪冻干饼的图像,以及在时间点第“0”天所述底物相对于新鲜制备的活细胞底物的活性。图63显示如实施例39中所述当根据本公开的组合物在25℃和60℃下孵育且在含有0.01%bsa的pbs,ph7.0中测试发光输出时在添加纯化的酶后的各个时间点的rlu值。图64a至图64c.描绘在各种合成/配制步骤期间jrw-1743的图像:(a)左侧的小瓶含有熔融的f-127,而右侧的小瓶含有溶解在etoh中的jrw-1743;(b)jrw-1743,去除etoh后,且将底物/聚合物混合物在2.6ml纯水中重构至最终浓度为8.5mm;(c)冻干后配制的jrw-1743的代表性实例:在干燥f-127基质中的jrw-1743(左)和在纯水中重构后的相同材料(中和右)。图65.在用f-127配制且在纳米纯水中重构后jrw-1743的代表性吸光度迹线。通过吸光度确定溶液中底物的浓度。实验测定jrm-1743在水中的平均浓度为8.5mm。干燥的配制的底物的计算理论浓度为8.7mm。定义虽然可以在本文所述的实施方案的实践或测试中使用类似于或等效于本文中所述的那些方法和材料的任何方法和材料,但本文描述一些优选的方法、组合物、装置和材料。然而,在描述本发明的材料和方法之前,应当理解,本发明不限于本文所述的特定分子、组合物、方法学或方案,因为这些可根据常规实验和优化而变化。还应理解,本说明书中使用的术语仅用于描述特定变型或实施方案的目的,并且并非意图限制本文所述的实施方案的范围。除非另有限定,否则本文中所使用的所有技术和科学术语都具有与本发明所属领域的普通技术人员通常理解的意义相同的意义。然而,如果出现矛盾,则将以本说明书(包括定义)为准。因此,在本文所述的实施方案的上下文中,应用以下定义。如本文所用,术语“刺虾荧光素酶”和“刺虾源性荧光素酶”可互换使用,并且是指从深海虾深海虾(oplophorusgracilirostris)(例如,seqidno:1)分泌的荧光素酶,包括其野生型、变体和突变体。例如,合适的刺虾荧光素酶变体描述于美国专利第8,557,970号和第8,669,103号中,其各自通过引用整体并入本文。示例性刺虾源性荧光素酶包括例如seqidno:2的荧光素酶(在本文中也可互换地称为“nanoluc”、“nluc”、“nluc荧光素酶”和“nluc酶”)。如本文所用,术语“聚合物”是指包括共价键合在链中的两个或更多个重复单元的有机化合物,其中所述链可为直链或支链的。通常,聚合物由一个或多个重复单元组成,所述重复单元通过共价化学键连接在一起以形成线性主链。重复基团可以相同或不同。因此,-a-a-a-a-型结构是聚合物,也称为均聚物,其中a为重复单元。-a-b-a-b-或-a-a-a-b-a-a-a-b-型结构也是聚合物,并且有时也称为共聚物,其中a和b为重复单元。如本文所用,术语“聚合物”明确地包括仅两个重复单元的链,诸如二糖,并且还包括更多重复单元的链,诸如寡糖和多糖。术语“聚合物”还包括非糖基聚合物(和少至两个单体单元的低聚物),诸如合成聚合物。在一些实施方案中,聚合物(例如,多糖)和低聚物(例如,寡糖)限于限定的长度(例如,2、3、4、5、6、7、8、9、10、12、14、16、18、20、25、30、35、40、45、50、60、70、80、90、100、150、200、300、400、500、750、1000或更长或介于其间的范围,例如2-10、5-25、10-50、超过100等)。除非上下文另有明确规定,否则如本文中和所附权利要求中所用,单数形式“一个”、“一种”和“所述”包括复数个指示物。因此,例如,提及“化合物”是指本领域技术人员已知的一种或多种聚合物及其等同物,等等。如本文所用,术语“包括”及其语言变化表示存在一种或多种所列举的特点、要素、方法步骤等,而不排除存在一种或多种额外的特点、要素、方法步骤等。相反地,术语“由……组成”及其语言变化表示存在一种或多种所列举的特点、要素、方法步骤等,并且排除任何一种或多种未列举的特点、要素、方法步骤等,但通常伴随的杂质除外。短语“基本上由……组成”表示一种或多种所列举的特点、要素、方法步骤等,以及不会实质性影响组合物、系统或方法的基本性质的任何一种或多种额外的特点、要素、方法步骤等。使用开放式“包括”语言描述本文的许多实施方案。这样的实施方案涵盖多个封闭的“由……组成”和/或“基本上由……组成”的实施方案,其可以替代地使用这样的语言来要求保护或描述。具体实施方式本文提供包含选自腔肠素及其类似物或衍生物的化合物和聚合物和/或纸或纤维基质或诸如塑料或玻璃的其他表面的组合物。在一些实施方案中,所述组合物稳定所述化合物以防止分解(例如,热分解、化学分解、光诱导的分解等)。在一些实施方案中,与不包含聚合物和/或纸或纤维基质或其他表面的组合物相比,所述组合物稳定所述化合物以防止分解。在一些实施方案中,组合物减少或抑制由化合物形成一种或多种分解产物(例如,与不包含聚合物或纸或纤维基质或其他表面的组合物相比)。在一些实施方案中,组合物增强腔肠素或其类似物或衍生物的重构效率。在一些实施方案中,组合物增强动力学溶解性(例如,与不包含聚合物和/或纸或纤维基质或其他表面的组合物相比)。所述组合物包含选自腔肠素及其类似物或衍生物的化合物。当并入组合物中时,可以保护化合物以防止分解(例如,热分解、化学分解、光诱导的分解等)。在一些实施方案中,所述化合物为腔肠素,其具有以下结构:在一些实施方案中,所述化合物为腔肠素类似物或衍生物。示例性腔肠素类似物包括腔肠素-h(2-脱氧腔肠素或2,8-二苄基-6-(4-羟基苯基)咪唑并[1,2-a]吡嗪-3(7h)-酮)、腔肠素-h-h(二脱氧腔肠素或2,8-二苄基-6-苯基咪唑并[1,2-a]吡嗪-3(7h)-酮)、呋瑞吗嗪(8-苄基-2-(呋喃-2-基甲基)-6-苯基咪唑并[1,2-a]吡嗪-3(7h)-酮)、jrw-0238(8-苄基-2-(呋喃-2-基甲基)-6-(3-羟基苯基)咪唑并[1,2-a]吡嗪-3(7h)-酮)、jrw-1744(6-(3-氨基-2-氟苯基)-8-苄基-2-(呋喃-2-基甲基)咪唑并[1,2-α]吡嗪-3(7h)-酮和jrw-1743(6-(3-氨基-2-氟苯基)-8-(2-氟苄基)-2-(呋喃-2-基甲基)咪唑并[1,2-α]吡嗪-3(7h)-酮),其具有以下结构:额外的示例性腔肠素类似物包括腔肠素-n、腔肠素-f、腔肠素-hcp、腔肠素-cp、腔肠素-c、腔肠素-e、腔肠素-fcp、腔肠素-i、腔肠素-icp、腔肠素-v、2-甲基腔肠素等。在一些实施方案中,化合物可为以下文献中描述的腔肠素类似物:wo2003/040100;美国专利公开案2008/0248511(例如,第[0086]段);美国专利第8,669,103号;wo2012/061529;美国专利公开案2017/0233789;美国专利第9,924,073号;美国专利公开案2018/0030059;美国专利第10,000,500号;美国专利公开案2018/0155350;美国临时专利申请第62/665,346号;美国申请第16/399,410号;美国临时专利申请第62/721,708号;美国申请第16/548,214号;美国专利公开案2014/0227759;美国专利第9,840,730号;美国专利第7,268,229号;美国专利第7,537,912号;美国专利第8,809,529号;美国专利第9,139,836号;美国专利第10,077,244号;美国专利第9,487,520号;美国专利第9,924,073号;美国专利第9,938,564号;美国专利第9,951,373号;美国专利第10,280,447号;美国专利第10,308,975号;美国专利第10,428,075号;其公开内容通过引用整体并入本文。在一些实施方案中,腔肠素类似物包括前底物,例如以下文献中描述的那些:美国专利公开案2008/0248511;美国专利公开案2012/0707849;美国专利公开案2014/0099654;美国专利第9,927,430号;美国专利第10,316,070号,通过引用整体并入本文。在一些实施方案中,化合物为呋瑞吗嗪。在一些实施方案中,化合物为jrw-0238。在一些实施方案中,化合物为jrw-1743。在一些实施方案中,化合物为jrw-1744。腔肠素及其类似物和衍生物可能遭受与它们在诸如如本文所述的生物发光测定和方法的许多测定中使用的缓冲体系中的重构相关的挑战。例如,诸如呋瑞吗嗪的腔肠素或其类似物或衍生物可以缓慢和/或不一致地溶解在非有机缓冲溶液中(例如,由于固体材料的异质微晶性质)。虽然在用缓冲液稀释之前溶解在有机溶剂中可以提供更快和更一致的结果,但是腔肠素化合物在储存期间可能在有机溶液中遭受不稳定性,包括热不稳定性和光不稳定性两种。参见,例如,美国专利第9,676,997号,其通过引用并入本文。在一些实施方案中,将腔肠素或其类似物或衍生物并入本文所述的组合物中提供更可靠和一致的溶解,而没有这样的不稳定性问题。在一些实施方案中,组合物还包含聚合物。如本文进一步描述,在某些实施方案中,聚合物的存在使化合物稳定以防止分解,并且聚合物的存在改善化合物在水或水溶液中的溶解性。在一些实施方案中,通过稳定腔肠素或腔肠素类似物或衍生物(例如,与有机溶剂中的腔肠素或腔肠素类似物相比),改善腔肠素或腔肠素类似物或衍生物的水溶性,和/或改善腔肠素或腔肠素类似物在非有机缓冲液中的重构效率(例如,与不存在聚合物的情况下的腔肠素或腔肠素类似物或衍生物相比)。本文的组合物和系统允许在未配制的和/或有机相的腔肠素或腔肠素类似物不太适合(例如,不是温度或光稳定的)的即时、预包装和/或固相系统、方法和测定中使用腔肠素或腔肠素类似物或衍生物。聚合物可为天然存在的生物聚合物或合成聚合物。在一些实施方案中,聚合物为天然存在的生物聚合物。合适的天然存在的生物聚合物为碳水化合物,包括二糖(例如,海藻糖、麦芽糖和蔗糖)、多糖(例如,普鲁兰多糖、葡聚糖和纤维素)和非硫酸化的糖胺聚糖(例如,透明质酸)。也可使用天然存在的生物聚合物的混合物。聚合物可为天然存在的聚合物的衍生物,诸如官能化的纤维素(例如,羟丙基纤维素、羟丙基甲基纤维素等)。在一些实施方案中,聚合物为普鲁兰多糖,其为包括麦芽三糖重复单元的多糖。麦芽三糖为包括三个经由α-1,4糖苷键连接的葡萄糖单元的三糖。普鲁兰多糖聚合物内的麦芽三糖单元经由α-1,6糖苷键彼此连接。普鲁兰多糖通过真菌金担子菌普鲁兰(aureobasidumpullulans)由淀粉天然产生,并且通常具有约4.5x104至约6x105da的质量范围,并且可从许多供应商(cas号9057-02-7)购得。在一些实施方案中,聚合物为葡聚糖,其是包括葡萄糖重复单元的复杂的支化多糖。直链连接通常由α-1,6糖苷键形成,而分支通常从α-1,3连接开始。天然存在的葡聚糖可具有在约9kda至约2000kda范围内的分子量。葡聚糖可通过包括肠膜明串珠菌(leuconostocmesenteroides)和突变链球菌(streptococcusmutans)的某些细菌由蔗糖合成。由肠膜明串珠菌产生的市售葡聚糖(cas号9004-54-0)可从包括sigmaaldrich的多个供应商购买,并且可具有约1kda至约670kda范围内的多种分子量范围。在一些实施方案中,聚合物为环状糖聚合物,诸如环糊精。典型的环糊精为α-环糊精、β-环糊精和γ-环糊精,它们分别具有六个、七个和八个吡喃葡萄糖单元。所述吡喃葡萄糖单元可为官能化的。示例性环糊精为羟丙基-β-环糊精。在一些实施方案中,所述聚合物为非硫酸化糖胺聚糖。糖胺聚糖为具有重复二糖单元的线性多糖,每个重复单元包括一个氨基糖(n-乙酰基葡糖胺或n-乙酰基半乳糖胺)和糖醛酸(葡萄糖醛酸或艾杜糖醛酸)或半乳糖。示例性的非硫酸化糖胺聚糖为透明质酸,其中重复的二糖包括经由交替的β-(1→4)和β-(1→3)糖苷键连接的n-乙酰基葡糖胺和葡糖醛酸。透明质酸的聚合物的大小可在5kda至20000kda范围内。在一些实施方案中,聚合物为纤维素,其为线性重复β-1,4连接的d-葡萄糖单元的多糖。天然纤维可存在高达10,000个葡萄糖单元,分子量大于1000da。在一些实施方案中,所述聚合物为合成聚合物。合成聚合物可为均聚物、共聚物、嵌段共聚物(例如,二嵌段共聚物、三嵌段共聚物等)。合适聚合物的非限制性实例包括但不限于聚胺、聚醚、聚酰胺、聚酯、聚氨基甲酸酯、聚脲、聚碳酸酯、聚苯乙烯、聚酰亚胺、聚砜、聚氨酯、聚乙炔、聚乙烯、聚乙烯亚胺、聚异氰酸酯、聚丙烯酸酯、聚甲基丙烯酸酯、聚丙烯腈和聚芳酯。具体聚合物的非限制性实例包括聚(己内酯)(pcl)、乙烯乙酸乙烯酯聚合物(eva)、聚(乳酸)(pla)、聚(l-乳酸)(plla)、聚(乙醇酸)(pga)、聚(乳酸-共-乙醇酸)(plga)、聚(l-乳酸-共-乙醇酸)(pllga)、聚(d,l-丙交酯)(pdla)、聚(l-丙交酯)(plla)、聚(d,l-丙交酯-共-己内酯)、聚(d,l-丙交酯-共-己内酯-共-乙交酯)、聚(d,l-丙交酯-共-peo-共-d,l-丙交酯)、聚(d,l-丙交酯-共-ppo-共-d,l-丙交酯)、聚氰基丙烯酸烷基酯、聚氨酯、聚-l-赖氨酸(pll)、甲基丙烯酸羟丙酯(hpma)、聚(乙二醇)、聚l-谷氨酸、聚(羟基酸)、聚酐、聚原酸酯、聚(酯酰胺)、聚酰胺、聚(酯醚)、聚碳酸酯、聚亚烷基(例如,聚乙烯和聚丙烯)、聚亚烷基二醇(例如,聚(乙二醇)(peg)和聚(丙二醇)(ppg))及其共聚物(例如,泊洛沙姆)、聚对苯二甲酸亚烷基酯(例如,聚(对苯二甲酸乙二醇酯)等)、聚乙烯醇(pva)、聚乙烯基醚、聚乙烯基酯(例如,聚(乙酸乙烯酯)等)、聚卤乙烯(例如,聚(氯乙烯)(pvc)等)、聚乙烯吡咯烷酮、聚硅氧烷、聚苯乙烯(ps)、聚氨酯、衍生的纤维素(例如,烷基纤维素、羟烷基纤维素、纤维素醚、纤维素酯、硝化纤维素、羟丙基纤维素、羧甲基纤维素等)、丙烯酸聚合物(“聚丙烯酸”)(例如,聚((甲基)丙烯酸甲酯)(pmma)、聚((甲基)丙烯酸乙酯)、聚((甲基)丙烯酸丁酯)、聚((甲基)丙烯酸异丁酯)、聚((甲基)丙烯酸己酯)、聚((甲基)丙烯酸异癸酯)、聚((甲基)丙烯酸月桂酯)、聚((甲基)丙烯酸苯酯)、聚(丙烯酸甲酯)、聚(丙烯酸异丙酯)、聚(丙烯酸异丁酯)、聚(丙烯酸十八烷基酯)、聚二噁烷酮及其共聚物(例如,聚羟基链烷酸酯、聚富马酸丙烯酯)、聚甲醛、聚(原)酸酯、聚(丁酸)、聚(戊酸)、聚(丙交酯-共-己内酯)、碳酸三甲烯、聚乙烯吡咯烷酮(pvp)、聚(1-乙烯基吡咯烷酮-共-乙酸乙烯酯)(pvp-va)、聚(4-乙烯基吡啶)、聚(4-乙烯基吡啶-共-甲基丙烯酸丁酯)、聚(4-乙烯基吡啶-共-苯乙烯)、聚[4-乙烯基吡啶鎓聚(氟化氢)、丙烯酸甲酯(p(maa-共-mma))共聚物、聚(1-乙烯基吡咯烷酮-共-甲基丙烯酸2-二甲基氨基乙基酯)、聚(1-乙烯基吡咯烷酮-共-苯乙烯)、聚(对甲苯磺酸4-乙烯基吡啶鎓)、羟丙基乙酸琥珀酸酯(hpmc)、羟丙基甲基纤维素乙酸琥珀酸酯(hpmcas)、聚(乙烯-交替-丙烯)(pep)、2-甲基丙烯酰胺基吡喃葡萄糖(mag)、己二酸二甲酯(dma)、聚乙烯基己内酰胺-聚乙酸乙烯酯及其任何的混合物和共聚物。在一些实施方案中,合成聚合物为聚亚烷基二醇。在一些实施方案中,合成聚合物为聚亚烷基二醇共聚物。在一些实施方案中,合成聚合物为包含至少一种聚(氧丙烯)嵌段和至少一种聚(氧乙烯)嵌段的嵌段共聚物,诸如泊洛沙姆。泊洛沙姆为具有由两个聚(氧乙烯)嵌段侧接的中心聚(氧丙烯)嵌段的非离子三嵌段共聚物。泊洛沙姆也以包括和的某些商品名已知。示例性泊洛沙姆包括泊洛沙姆188(f-68)和泊洛沙姆407(f-127)。在一些实施方案中,化合物(即腔肠素或其类似物或衍生物)和聚合物可以约0.001:1至约0.50:1或约0.0025:1至约0.40:1的重量比存在于组合物中。在一些实施方案中,组合物还包含纸或纤维基质或其他材料,并且将组合物置于纸或纤维基质或其他材料之中或之上。在一些实施方案中,所述材料可允许腔肠素(或其类似物或衍生物)在诸如现场测试的多种环境中使用。在一些实施方案中,纸或纤维基质可由诸如100%纯棉绒的高质量棉绒制造。在一些实施方案中,纸或纤维基质可为无灰的。在一些实施方案中,纸或纤维基质可包含至多0.06重量%的灰分。在一些实施方案中,纸或纤维基质可具有约0.1μm至约1mm的厚度。在一些实施方案中,纸或纤维基质可具有约0.02μm至约12μm的孔径范围。纸或纤维基质可具有多种特性,所述特性包括结合亲和力、孔隙率、官能度(例如,具有高度酸性或碱性官能团)等。示例性纸或纤维基质包括但不限于品牌纸(例如,w-903纸、fta纸、fta洗脱纸、ftadmpk纸等)、ahlstrom纸(例如,a-226纸等)、m-tfn纸、fta纸、fp705纸、bodedna收集纸、硝化纤维素纸、尼龙纸、纤维素纸和样品垫(例如,emdmilliporecfsp20300m)、dacron纸、棉纸、聚酯纸(例如,ahlstrom聚酯纤维级6613、ahlstrom处理的聚酯纤维级6613h)、羧甲基纤维素钠、noviplextm血浆制备卡、ahlstrom血浆分离卡、多孔和聚合物膜、高纯度棉纤维(例如ahlstrom级237)、棉/人造丝混纺的高纯度棉(例如ahlstrom级1218)、玻璃超细纤维(例如ahlstrom934-ah、emdmilliporegfdx103000)及其组合。可代替纸或纤维基质使用的其他潜在材料包括由有机或无机材料(例如,金属或陶瓷材料)制成的合成和/或聚合物膜、均质或异质固体、液体或可溶解压片材料。示例性额外材料包括例如乙酸纤维素、纤维素酯、纤维素醚、聚砜、聚醚砜、聚丙烯腈、聚乙烯、聚丙烯、聚偏二氟乙烯、聚乙二醇、聚乙烯醇、淀粉等。可代替纸或纤维基质使用的额外材料包括塑料或玻璃。在一些实施方案中,所述材料可为比色皿、载玻片、板或由塑料或玻璃制成的任何其他合适的表面。在一些实施方案中,材料可为金属表面,其中金属为单一金属或金属合金,例如钢、铜、黄铜、青铜或银。在一些实施方案中,组合物包含(i)腔肠素或腔肠素衍生物或类似物,(ii)合适的聚合物,和(iii)纸或纤维基质或诸如玻璃、塑料或金属的其他表面。除了化合物和聚合物和/或纸或纤维基质或其他表面之外,组合物还可包含额外组分,诸如缓冲液、表面活性剂、还原剂、盐、自由基清除剂、螯合剂、蛋白质或其任意组合。在一些实施方案中,组合物包含缓冲液,诸如磷酸盐缓冲液、硼酸盐缓冲液、乙酸盐缓冲液或柠檬酸盐缓冲液,或其他常用缓冲液,诸如二羟乙基甘氨酸、三(羟甲基)甲基甘氨酸、三(羟甲基)氨基甲烷(tris)、n-[三(羟甲基)甲基]-3-氨基丙磺酸(taps)、3-[n-三(羟甲基)甲基氨基]-2-羟基丙磺酸(tapso)、2-[4-(2-羟乙基)哌嗪-1-基]乙磺酸(hepes)、n-[三(羟甲基)甲基]-2-氨基乙磺酸(tes)、哌嗪-n,n′-双(2-乙磺酸)(pipes)、2-(n-吗啉代)乙磺酸(mes)等。在一些实施方案中,组合物包含磷酸盐缓冲液。在一些实施方案中,组合物包含三(羟甲基)甲基甘氨酸。在一些实施方案中,组合物包含2-(n-吗啉代)乙磺酸。组合物还可包含缓冲液的任意组合。在一些实施方案中,组合物包含洗涤剂或表面活性剂。在一些实施方案中,洗涤剂或表面活性剂以约0.01摩尔%至5摩尔%(例如,0.01%、0.02%、0.05%、0.1%、0.2%、0.5%、1%、2%、5%或其间的任何范围(例如,0.1%至0.5%)存在。示例性表面活性剂包括非离子表面活性剂、阴离子表面活性剂、阳离子表面活性剂和两性离子表面活性剂。非离子洗涤剂的实例包括brij35、tritontm表面活性剂,诸如tritontmx系列(辛基酚乙氧基化物,诸如tritontmx-100、tritontmx-100r、tritontmx-114等)、辛基葡糖苷、聚氧乙烯(9)十二烷基醚、洋地黄皂苷、辛基苯基聚乙二醇(igepalca630)、正辛基-β-d-吡喃葡萄糖苷(betaog)、正十二烷基-β-d-麦芽糖苷、20(聚山梨醇酯20或聚乙二醇(20)山梨糖醇单月桂酸酯)、40(聚山梨醇酯40或聚乙二醇(20)山梨糖醇单棕榈酸酯)、80(聚山梨醇酯80或聚乙二醇(20)山梨糖醇单油酸酯)、聚多卡醇、正十二烷基β-d-麦芽糖苷(ddm)、nonidetp40替代品、np-40壬基苯基聚乙二醇、c12e8(八甘醇正十二烷基单醚)、六甘醇单正十四烷基醚(c14e06)、辛基-β-硫代吡喃葡萄糖苷(辛基硫代葡萄糖苷,otg)、f-68(泊洛沙姆188)、f-127(泊洛沙姆407)、皂苷、emulgen、聚乙二醇三甲基壬基醚和聚氧乙烯10月桂基醚(c12e10)。离子洗涤剂(阴离子或阳离子)的实例包括脱氧胆酸盐、胆酸钠、十二烷基硫酸钠(sds)、n-月桂酰肌氨酸和十六烷基三甲基溴化铵(ctab)。两性离子试剂的实例包括chaps、两性离子3-14和3-[(3-胆酰氨基丙基)二甲基铵]-1-丙磺酸盐。在一些实施方案中,表面活性剂为聚山梨醇酯20。组合物还可包含表面活性剂的任意组合。在一些实施方案中,组合物可包含还原剂,诸如二硫苏糖醇(dtt)、2-巯基乙醇(bme)、半胱胺、(2s)-2-氨基-1,4-二巯基丁烷(dtba)、硫脲、6-氮杂-2-硫代胸腺嘧啶(att)等。在一些实施方案中,还原剂为硫脲。在一些实施方案中,还原剂为att。组合物还可包含还原剂的任意组合。在一些实施方案中,组合物可包含盐,诸如氯化钠、氯化钾、氯化镁、磷酸钠等。在一些实施方案中,所述盐为氯化钠。在一些实施方案中,所述盐为磷酸钠。组合物还可包含盐的任意组合。在一些实施方案中,组合物可包含自由基清除剂,诸如抗坏血酸、抗坏血酸钠等。在一些实施方案中,组合物可包含金属螯合剂,诸如柠檬酸、乙二胺四乙酸、反-1,2-二氨基环己烷-四乙酸等。在一些实施方案中,组合物包含抗坏血酸。在一些实施方案中,组合物包含抗坏血酸钠。在一些实施方案中,组合物包含柠檬酸。在一些实施方案中,组合物包含反-1,2-二氨基环己烷-四乙酸。组合物可包含自由基清除剂和/或螯合剂的任意组合。在一些实施方案中,组合物可包含完整的缓冲液组合物,诸如荧光素酶测定缓冲液(promega目录号n112)、活细胞底物(lcs)稀释缓冲液(promega目录号n206)等。完整的缓冲液组合物可包含本文公开的组分的组合,包括缓冲液本身以及盐、金属螯合剂、还原剂和非离子表面活性剂中的一种或多种。在一些实施方案中,组合物可包含蛋白质。例如,组合物可包含载体蛋白质以防止可在下游测定中添加的发光酶的表面吸附。在一些实施方案中,所述蛋白质可为牛血清白蛋白(bsa)。在一些实施方案中,所述蛋白质可为猪来源的高度纯化的真皮胶原的多肽级分(例如,prionex)。在一些实施方案中,蛋白质可为明胶。组合物还可包含蛋白质的任意组合。在一些实施方案中,组合物可包含溶剂。一些组合物被完全干燥,从而可以去除任何溶剂,而其他组合物可包含溶剂或一定量的残余溶剂。在一些实施方案中,组合物可包括有机溶剂,诸如甲醇、乙醇、异丙醇、乙二醇、丙二醇等,或其任意组合。例如,组合物可包含乙醇和丙二醇的组合。如上所述,组合物可包含上述组分的任意组合。例如,在一些实施方案中,组合物可包含蛋白质、缓冲液和还原剂。在一些实施方案中,组合物可包含蛋白质、缓冲液和金属螯合剂。组合物可呈冻干粉或饼的形式。这种组合物可通过冷冻干燥组合物的组分的混合物来制备,如下文进一步描述。粉状产品可提供在诸如瓶、小瓶、弹扣管、微量滴定板的容器中,纸或纤维基质或其他固体材料支撑物上,芯片实验室中等。粉末产品可容纳在多个弹扣管中,每个管含有预定量的组合物,所述组合物溶解到适量的溶液中并直接用于目标测定。所述组合物也可为硬的但有延展性的材料形式,诸如“滴落”流延体或膜的形式。这样的组合物可通过将含有组合物的组分的溶液施加到表面并例如通过如下方式干燥组合物来制备:空气干燥、在环境温度下干燥、在升高的温度下(例如,在约30℃至约70℃、或约30℃至约40℃,例如在约30℃、约35℃、约40℃、约45℃、约50℃、约55℃、约60℃、约65℃或约70℃的温度下)干燥、在惰性气氛下干燥、或真空干燥。滴落流延体或膜可提供在诸如瓶、小瓶、弹扣管、微量滴定板、微量滴定板的容器中,纸或纤维基质或其他固体材料支撑物上,芯片实验室中等。在一些实施方案中,组合物呈溶液(例如,水溶液)的形式。当组合物为溶液时,组合物可具有约5.5至约8.0,例如约6.5至约7.5的ph。在一些实施方案中,组合物具有约5.5、5.6、5.7、5.8、5.9、6.0、6.1、6.2、6.3、6.4、6.5、6.6、6.7、6.8、6.9、7.0、7.1、7.2、77.3、7.4、7.5、7.6、7.7、7.8、7.9或8.0的ph。组合物还可以其他形式提供,诸如片剂或包含可溶解片剂的胶囊或可滴入诸如缓冲液或生物样品的样品中的胶囊。组合物也可以作为预形成的膜包含在诸如96孔板的孔的表面上,使得组合物可以直接溶解在适量的溶液中,并且直接用于目标测定中。当将组合物提供在纸或纤维基质上时,纸或纤维基质可呈具有斑点的卡的形式,所述斑点可被打孔,使得斑点可被重构并且直接用于目标测定。或者,纸或纤维基质可以预穿孔的斑点(例如,直径为约1-5mm)的形式提供,所述斑点可被重构用于目标测定。具有组合物的纸或纤维基质可例如通过空气干燥、在环境温度下干燥、在升高的温度下(例如,在约30℃至约70℃,或约30℃至约40℃,例如在约30℃、约35℃、约40℃、约45℃、约50℃、约55℃、约60℃、约65℃或约70℃的温度下)干燥、在惰性气氛下干燥或通过真空干燥来干燥。本公开的组合物可以例如腔肠素及其类似物和衍生物的荧光素酶底物已被使用的任何方式使用。例如,它们可用于采用腔肠素或其类似物或衍生物的生物发光方法中,以检测样品中的一种或多种分子,例如酶、酶反应的辅因子、酶底物、酶抑制剂、酶活化剂或·oh自由基,或一种或多种条件,例如氧化还原条件。样品可包含动物(例如,脊椎动物)、植物、真菌、生理流体(例如,血液、血浆、尿液、粘液分泌物)、细胞、细胞裂解物、细胞上清液或细胞的纯化级分(例如,亚细胞级分)。可以检测或量化这种分子的存在、量、光谱分布、发射动力学或比活性。分子可在包括多相溶液(例如,乳液或悬浮液)的溶液中或在固体支撑物(例如,颗粒、毛细管或测定容器)上检测或定量。在某些实施方案中,所述组合物可用于定量目标分子。在一些实施方案中,组合物可用作例如细胞凋亡或药物代谢的特定生物化学活性的探针。在某些实施方案中,所述组合物可用于例如体内检测活细胞或动物中的发光。在一些实施方案中,荧光素酶可在细胞中表达(作为报道基因或其他),并且细胞用组合物处理。腔肠素或其类似物或衍生物将渗透培养物中的细胞,与荧光素酶反应,并发光。在一些实施方案中,组合物可用于更稳健的、基于活细胞荧光素酶的报道基因测定。在再其他实施方案中,含有荧光素酶和本公开的组合物的样品(包括细胞、组织、动物等)可使用各种显微镜和成像技术,例如体内成像测定。在再其他实施方案中,可分泌荧光素酶在细胞中作为活细胞报道系统的一部分表达。本文还提供一种稳定选自腔肠素或其类似物或衍生物的化合物的方法,其包括使所述化合物与有效量的聚合物和/或纸或纤维基质接触以形成组合物。可使化合物稳定以防止热分解、化学分解、光诱导的分解或其任意组合。在一些实施方案中,本文的组合物使化合物(即腔肠素或其类似物或衍生物)稳定以防止在以下温度下分解(例如,与尚未与聚合物和/或纸或纤维基质接触的腔肠素化合物或其类似物或衍生物相比):约-80℃至约80℃、约-75℃至约80℃、约-70℃至约80℃、约-65℃至约80℃、约-60℃至约80℃、约-55℃至约80℃、约-50℃至约80℃、约-45℃至约80℃、约-40℃至约80℃、约-35℃至约80℃、约-30℃至约80℃、约-25℃至约80℃、约-20℃至约80℃、约-15℃至约80℃、约-10℃至约80℃、约-5℃至约80℃、约0℃至约80℃、约-80℃至约75℃、约-80℃至约70℃、约-80℃至约65℃、约-80℃至约60℃、约-80℃至约55℃、约-80℃至约50℃、约-80℃至约45℃、约-80℃至约40℃、约-80℃至约35℃、约-80℃至约30℃、约-80℃至约25℃、约-20℃至约60℃、约-20℃至约55℃、约-20℃至约50℃、约-20℃至约45℃、约-20℃至约40℃、约-20℃至约35℃、约-20℃至约30℃、或约-20℃至约25℃。在一些实施方案中,本文的组合物使化合物(即腔肠素或其类似物或衍生物)稳定以防止在以下温度下分解(例如,与尚未与聚合物和/或纸或纤维接触的腔肠素化合物或其类似物或衍生物相比):约-80℃、-79℃、-78℃、-77℃、-76℃、-75℃、-74℃、-73℃、-72℃、-71℃、-70℃、-69℃、-68℃、-67℃、-66℃、-65℃、-64℃、-63℃、-62℃、-61℃、-60℃、-59℃、-58℃、-57℃、-56℃、-55℃、-54℃、-53℃、-52℃、-51℃、-50℃、-49℃、-48℃、-47℃、-46℃、-45℃、-44℃、-43℃、-42℃、-41℃、-40℃、-39℃、-38℃、-37℃、-36℃、-35℃、-34℃、-33℃、-32℃、-31℃、-30℃、-29℃、-28℃、-27℃、-26℃、-25℃、-24℃、-23℃、-22℃、-21℃、-20℃、-19℃、-18℃、-17℃、-16℃、-15℃、-14℃、-13℃、-12℃、-11℃、-10℃、-9℃、-8℃、-7℃、-6℃、-5℃、-4℃、-3℃、-2℃、-1℃、0℃、1℃、2℃、3℃、4℃、5℃、6℃、7℃、8℃、9℃、10℃、11℃、12℃、13℃、14℃、15℃、16℃、17℃、18℃、19℃、20℃、21℃、22℃、23℃、24℃、25℃、26℃、27℃、28℃、29℃、30℃、31℃、32℃、33℃、34℃、35℃、36℃、37℃、38℃、39℃、40℃、41℃、42℃、43℃、44℃、45℃、46℃、47℃、48℃、49℃、50℃、51℃、52℃、53℃、54℃、55℃、56℃、57℃、58℃、59℃、60℃、61℃、62℃、63℃、64℃、65℃、66℃、67℃、68℃、69℃、70℃、75℃或80℃。所述组合物可使所述化合物稳定以防止在约-80℃、约-20℃、约4℃、约20℃、约25℃或约37℃下分解。在一些实施方案中,本文的组合物使所述化合物(即腔肠素或其类似物或衍生物)稳定以防止在光存在下的分解(例如,与尚未与聚合物和/或纸或纤维基质接触的腔肠素化合物或其类似物或衍生物相比)。与不含聚合物或纸或纤维基质的组合物相比,所述组合物可增加化合物在光存在下的半衰期。与不含聚合物或纸或纤维基质的组合物相比,所述组合物可使化合物在光存在下的半衰期增加约1.1倍、1.2倍、1.3倍、1.4倍、1.5倍、1.6倍、1.7倍、1.8倍、1.9倍、2.0倍、2.1倍、2.2倍、2.3倍、2.4倍、2.5倍、2.6倍、2.7倍、2.8倍、2.9倍、3.0倍、3.1倍、3.2倍、3.3倍、3.4倍、3.5倍、3.6倍、3.7倍、3.8倍、3.9倍、4.0倍、4.1倍、4.2倍、4.3倍、4.4倍、4.5倍、4.6倍、4.7倍、4.8倍、4.9倍或5.0倍或更多倍。在一些实施方案中,与不含聚合物或纸或纤维基质的组合物相比,本文的组合物使化合物(即腔肠素或其类似物或衍生物)稳定至少约1天、2天、3天、4天、5天、6天、7天、8天、9天、10天、11天、12天、13天、14天、15天、16天、17天、18天、19天、20天、21天、22天、23天、24天、25天、26天、27天、28天、29天、30天、35天、40天、45天、50天、55天、60天、65天、70天、75天、80天、85天、90天、100天、110天、120天、130天、140天、150天、160天、170天、180天、190天、200天、210天、220天、230天、240天、250天、260天、270天、280天、290天、300天、310天、320天、330天、340天、350天、360天、1年、2年、3年、4年或5年以防止分解(例如,与尚未与聚合物和/或纸或纤维基质接触的腔肠素化合物或其类似物或衍生物相比)。在一些实施方案中,与不包含聚合物或纸或纤维基质的组合物相比,组合物使化合物(即腔肠素或其类似物或衍生物)抵抗分解的半衰期(例如,与尚未与聚合物和/或纸或纤维基质接触的腔肠素化合物或其类似物或衍生物相比)增加至少约1.25倍、1.5倍、1.75倍、2倍、3倍、4倍、5倍、6倍、7倍、8倍、9倍、10倍、11倍、12倍、13倍、14倍、15倍、16倍、17倍、18倍、19倍、20倍、21倍、22倍、23倍、24倍或25倍。本文还提供一种改善选自腔肠素及其类似物或衍生物的化合物的溶解性的方法,其包括使所述化合物与有效量的聚合物和/或纸或纤维基质接触,其中与尚未与所述聚合物接触的化合物相比,所述腔肠素化合物或其类似物或衍生物的溶解性得到改善。与尚未与聚合物和/或纸或纤维基质接触的相应化合物相比,化合物在水溶液中的溶解性可以得到改善。在冻干粉、滴落流延膜或“滴”的重构之后或由于其上或其中已经放置有化合物的纸或纤维基质或其他固体支撑材料的再水合,当存在聚合物时,化合物的溶解性可以得到改善。所述组合物可增加化合物(即腔肠素或其类似物或衍生物)在例如纯水或水溶液中的溶解性,所述水溶液诸如为还包含缓冲液、盐、蛋白质、还原剂、自由基清除剂、表面活性剂等或这些组分的任意组合的那些。所述组合物可增加化合物在例如水性缓冲液诸如ph为约6.5至约7.5(例如,ph为约6.5、6.6、6.7、6.8、6.9、7.0、7.1、7.2、7.3、7.4或7.5或其间的任何范围)的磷酸盐缓冲盐水(pbs)或在诸如荧光素酶测定缓冲液的另一种合适的缓冲液中的溶解性。所述组合物可增加化合物在例如生物或环境流体如来自受试者的生物样品、培养基(例如组织培养基)等中的溶解度。例如,与不含聚合物和/或纸或纤维基质的组合物相比,所述组合物可使化合物在光存在下的溶解度增加约1.1倍、1.2倍、1.3倍、1.4倍、1.5倍、1.6倍、1.7倍、1.8倍、1.9倍、2.0倍、2.1倍、2.2倍、2.3倍、2.4倍、2.5倍、2.6倍、2.7倍、2.8倍、2.9倍、3.0倍、3.1倍、3.2倍、3.3倍、3.4倍、3.5倍、3.6倍、3.7倍、3.8倍、3.9倍、4.0倍、4.1倍、4.2倍、4.3倍、4.4倍、4.5倍、4.6倍、4.7倍、4.8倍、4.9倍或5.0倍或更多倍。本文还提供一种改善选自腔肠素及其类似物或衍生物的化合物的重构速率的方法,其包括使所述化合物与有效量的聚合物和/或纸或纤维基质接触,其中与尚未与聚合物或纸或纤维基质接触的化合物相比,所述化合物的重构速率得到改善。所述组合物可增加化合物在例如纯水或水溶液中的重构速率,所述水溶液诸如为还包含缓冲液、盐、蛋白质、还原剂、表面活性剂等或这样的组分的任意组合的那些。所述组合物可增加化合物在例如水性缓冲液诸如ph为约6.5至约7.5(例如,ph为约6.5、6.6、6.7、6.8、6.9、7.0、7.1、7.2、7.3、7.4或7.5或其间的任何范围)的磷酸盐缓冲盐水(pbs)或在诸如荧光素酶测定缓冲液的另一种合适的缓冲液中的重构速率。所述组合物可增加化合物在例如生物或环境流体如来自受试者的生物样品、培养基(例如组织培养基)等中的溶解度。例如,与不含聚合物的组合物相比,所述组合物可使化合物(例如,腔肠素化合物或其类似物或衍生物)在光存在下的重构速率增加约1.1倍、1.2倍、1.3倍、1.4倍、1.5倍、1.6倍、1.7倍、1.8倍、1.9倍、2.0倍、2.1倍、2.2倍、2.3倍、2.4倍、2.5倍、2.6倍、2.7倍、2.8倍、2.9倍、3.0倍、3.1倍、3.2倍、3.3倍、3.4倍、3.5倍、3.6倍、3.7倍、3.8倍、3.9倍、4.0倍、4.1倍、4.2倍、4.3倍、4.4倍、4.5倍、4.6倍、4.7倍、4.8倍、4.9倍或5.0倍或更多倍。组合物可具有本文公开的性质的任意组合。例如,组合物可具有如本文所述的增加的溶解性、如本文所述的改善的重构速率、如本文所述的增加的稳定性和/或如本文所公开的增加的半衰期。组合物可具有所公开的特征之一或所公开的特征的任意组合,并且还可具有其他改善的性质。在本文所述方法的实施方案中,接触步骤可包括以下步骤:将化合物(即腔肠素或其类似物或衍生物)溶解在第一溶剂中以形成第一溶液;将所述第一溶液与聚合物和/或纸或纤维基质混合以形成混合物;和干燥所述混合物。在一些实施方案中,接触步骤包括以下步骤:将所述化合物溶解在第一溶剂中以形成第一溶液;将所述聚合物溶解在第二溶剂中以形成第二溶液;将所述第一溶液和所述第二溶液混合以形成混合物;和干燥所述混合物。在一些实施方案中,接触步骤包括以下步骤:将所述化合物溶解在溶剂中以形成第一溶液;将所述第一溶液施加到所述纸或纤维基质上;和干燥纸或纤维基质。在一些实施方案中,接触步骤包括以下步骤:将所述化合物溶解在第一溶剂中以形成第一溶液;将所述聚合物溶解在第二溶剂中以形成第二溶液;将所述第一溶液和所述第二溶液合并以形成第三溶液;将所述第三溶液施加到纸或纤维基质;和干燥所述纸或纤维基质。在一些实施方案中,干燥步骤包括冻干。在一些实施方案中,干燥步骤包括空气干燥。在一些实施方案中,干燥步骤包括在环境温度下在惰性气氛下(例如,在氮气或氩气下)干燥。在一些实施方案中,干燥步骤包括在升高的温度(例如,30℃)下干燥。在一些实施方案中,干燥步骤包括真空干燥。在一些实施方案中,可以将所述方法中使用的一种或所有溶液脱氧。脱氧可通过在真空下使溶液脱气、通过使惰性气体(例如,氮气或氩气)鼓泡通过溶液等来实现。组合物可通过使用它们作为荧光素酶的底物以产生发光并分析重构后来自组合物的发光来测试。“发光”是指在适当条件下,例如在诸如腔肠素类似物的合适底物存在下荧光素酶的光输出。光输出可作为发光反应开始时的光输出的瞬时或接近瞬时量度来测量(有时称为“t=0”发光或“闪光”),所述发光反应可在添加腔肠素底物时开始。在各种实施方案中,发光反应在溶液中进行。所述溶液可含有裂解物,例如来自原核或真核表达系统中的细胞的裂解物。所述溶液可含有纯化的蛋白质、肽或用发光酶组分标记的小分子。在其他实施方案中,表达发生在无细胞系统中,或者荧光素酶蛋白分泌到胞外介质中,使得在后一种情况下,不必产生裂解物。在一些实施方案中,通过将适当的材料,例如本公开的组合物、缓冲液等添加到含有发光蛋白的反应室(例如,例如96孔板的多孔板的孔、试管或小瓶、比色皿等)中来开始反应。所述反应室可位于读出装置中,所述读出装置可例如使用光度计、光电倍增管或照相机(例如,智能手机照相机、ccd照相机或任何其他可记录图像的手持式装置)测量光输出。光输出或发光也可随时间而测量,例如在相同的反应室中持续数秒、数分钟、数小时等的时间段。光输出或发光可报道为随时间的平均值、信号衰减的半衰期、一段时间内的信号总和或峰值输出。发光可以相对光单位(rlu)测量。在某些实施方案中,组合物可通过将其用作刺虾荧光素酶的底物来测试。在再其他实施方案中,将荧光素酶和/或组合物引入宿主,并对所述宿主或其部分进行发光测量,所述宿主或其部分可包括整个生物体或细胞、组织、外植体或其提取物。在其他实施方案中,发光反应在固体支撑物上进行。所述固体支撑物可为(例如)珠粒、树脂、磁性颗粒、膜或表面,诸如小瓶、微量滴定板、盒、比色皿、拭子等的表面。然后,这种反应可位于可以测量来自具体固体支撑物形式的光输出的读出装置中。在其他实施方案中,在体内进行发光反应以便于全动物成像。用于将底物注射到动物中的媒介物必须是无毒的,并且与哺乳动物生物学高度相容,这显著地限制了可用的选择。普鲁兰多糖和本文所述的许多其他聚合物是无毒的,甚至被批准作为食品添加剂,这使得它们特别适合作为可注射溶液的组分。此外,诸如呋瑞吗嗪的腔肠素类似物在简单缓冲液如pbs中的改善的溶解度和重构对于诸如通过静脉内注射、腹膜内注射、颅内施用等施用到动物是理想的。组合物组分可在注射前合并,并且优良的重构使得样品快速均质化,这对于其中存在不溶解的微晶可能是致命的动物工作是重要的。一旦将底物制剂引入动物体内(例如静脉内或腹膜内注射),则将镇静的动物置于成像室中并分析生物发光的体内产生。在某些实施方案中,本文公开的组合物作为试剂盒的一部分提供。所述组合物可容纳在单个容器中。在一些实施方案中,所述试剂盒还可包括一种或多种荧光素酶(以多肽、多核苷酸或两者的形式)以及使得使用者能够执行诸如本文所公开的那些测定的测定的合适的试剂和指导说明。所述试剂盒还可包括一种或多种缓冲液,诸如本文公开的那些。所述试剂盒可包括用于储存组合物和/或容纳组合物的单个容器的指导说明。本公开的试剂盒中所包括的指导说明可被粘附到包装材料上或可作为包装插页而包括。虽然指导说明通常是书写或印刷的材料,但它们不限于此类。本公开预期能够存储这类指导说明并且将其传达给终端用户的任何媒介。这样的媒介包括但不限于电子存储介质(例如,磁盘、磁带、磁片盒、芯片)、光学介质(例如,cdrom)等。如本文所用,术语“指导说明”可包括提供指导说明的网站(internetsite)的地址。实验在本文实施方案的开发期间进行的实验证明本文所述的组合物和方法的效用。除非另外指明,否则普鲁兰多糖自sigma-aldrich(cas号9057-02-7)获得。实施例中使用的缩写包括以下:att为6-氮杂-2-硫代胸腺嘧啶;etoh为乙醇;fz为呋瑞吗嗪;hplc为高效液相色谱;ngb为荧光素酶测定缓冲液(promega目录号n112);pbs为磷酸盐缓冲盐水;并且tfa为三氟乙酸。实施例1呋瑞吗嗪-普鲁兰多糖组合物样品制备如下。对于以下条件中的每一种,将所有底物和添加剂在不同百分比w/v的普鲁兰多糖水溶液中以所列浓度合并。在每种情况下,底物从乙醇储备溶液添加,使得在含有聚合物的最终溶液中的乙醇总量(v/v)不超过10%v/v。条件1:用0%、2.5%、5%或10%(w/v)普鲁兰多糖水溶液制备溶液。制备30mm呋瑞吗嗪在乙醇中的储备溶液。将4μl呋瑞吗嗪储备液添加到46μl含有普鲁兰多糖的溶液中,其中呋瑞吗嗪的最终浓度为2mm。在所有情况下,最终溶液中乙醇的总浓度<10%v/v。将样品冷冻,然后冻干过夜以形成粉末状产品。条件2:如上所述制备15%(w/v)普鲁兰多糖、200mm三(羟甲基)甲基甘氨酸和2mm呋瑞吗嗪在<10%v/v乙醇/水中的溶液。将一系列60μl等分试样移液到石蜡膜上,且允许在25℃下在黑暗中干燥至少3小时以形成硬的可延展的“滴”。条件3:如上所述制备15%(w/v)普鲁兰多糖和2mm呋瑞吗嗪在<10%v/v乙醇/水中的溶液。将一系列60μl等分试样移液到石蜡膜上,且允许在25℃下在黑暗中干燥至少3小时。通过根据需要进行涡旋将配制的呋瑞吗嗪溶解到ngb或pbs,ph7.0中来测试样品。在每种情况下,将样品在5ml缓冲液中稀释到10μm呋瑞吗嗪的最终工作浓度。经验结果如下。具有2.5%(w/v)普鲁兰多糖的根据条件1的样品在不到一分钟内容易地进入ngb和pbs,ph7.0溶液中。5%(w/v)和10%(w/v)的根据条件1的样品在几分钟内完全溶解于pbs,ph7.0中。根据条件2的样品需要进一步涡旋,并且需要约10-15分钟以完全溶解在pbs,ph7.0中。不含普鲁兰多糖的根据条件1的样品需要大约10分钟以完全溶解在pbs(根据经验确定),ph7.0中。在4℃下储存样品五周后,对于20μm储备液,用1xngb将样品稀释到6ml,或者对于20μm储备液,用1xpbs,ph7.0将样品稀释到6ml。纯化的(nluc)荧光素酶以最终1x浓度添加(其中2x储备液已从1000x酶,promega#e499的储备液开始在pbs或ngb中制备)。对照样品包含在具有10μm最终底物的测定缓冲液中的nluc。在发光仪(特别是探险多模微孔板阅读器–promega目录号gm3000)上使用动态读数收集总发光,以100μl的总测定体积在固体白色非结合表面(nbs)板上执行测定。在pbs中重构的样品的动力学迹线显示在图1a中,并且在ngb中重构的样品的动力学迹线显示在图1b中。图1c显示冻干饼和膜滴制剂的图像。来自图1a中指定时间点的数据呈现在图2a至图2c的条形图中,并且来自图1b中指定时间点的数据呈现在图3a至图3c的条形图中。图1至图3中所示的结果证明呋瑞吗嗪组合物在中性缓冲液中的溶解度增加,而不需要有机溶剂或特殊的缓冲条件。相对于市售呋瑞吗嗪制剂,来自呋瑞吗嗪组合物的发光更强。实施例2重构的呋瑞吗嗪组合物的吸光度将散装固体呋瑞吗嗪在乙醇中稀释到最终浓度为10mm(溶液1)。将干燥的普鲁兰多糖溶解在纯水中,最终浓度为0%、2.5%、5%、10%、15%w/v(分别为溶液2a、2b、2c、2d和2e)。将45μl溶液2a-e移液到单独的1.5ml弹扣管型小瓶中。然后将5μl溶液1添加到每个小瓶中并剧烈移液以混合,从而形成溶液3a-e,其各自含有在50μl溶液中最终浓度为1mm(19.08μg)的呋瑞吗嗪。混合后,将含有溶液3a-e的小瓶置于干冰中冷冻1小时。然后将这些冷冻的储备液冻干过夜以形成含有呋瑞吗嗪的干燥普鲁兰基质。将呋瑞吗嗪(19.08μg)在普鲁兰多糖基质(0%-15%w/v)中的粉末制剂在0.5mlpbs缓冲液,ph6.8中稀释,在室温下平衡30分钟,且读出在254nm处吸光度。在pbs缓冲液中重构后,用增加量的普鲁兰多糖配制的干燥呋瑞吗嗪(50nmol)的吸收光谱显示在图4a中。用普鲁兰多糖的配制的呋瑞吗嗪导致水溶液中呋瑞吗嗪吸光度的增加。根据比尔定律,使用在甲醇中的呋瑞吗嗪的消光系数(21000m-1cm-1),在254nm处测量的吸光度,确定呋瑞吗嗪的浓度。散装呋瑞吗嗪具有0.0571的吸光度,对应于0.0082mm的计算浓度。具有2.5%-5%w/v普鲁兰多糖的呋瑞吗嗪制剂导致0.2204和0.2467的吸收,分别给出0.032mm和0.035mm的计算浓度。用10-15%w/v普鲁兰多糖配制的呋瑞吗嗪导致0.3964和0.3836的吸光度,分别给出在pbs中0.055mm和0.052mm的计算浓度。图4a中展示的吸光度数据的汇总可见于图4c中,图4c显示与不含普鲁兰多糖的样品相比,当用普鲁兰多糖配制呋瑞吗嗪时,溶液中呋瑞吗嗪(fz)浓度增加。单独地,将与上述样品类似地制备的呋瑞吗嗪(95.4μg)在普鲁兰多糖基质(0%-15%w/v)中的干燥制剂在0.5mlpbs缓冲液,ph6.8中稀释,在室温下平衡30分钟,并且读出在254nm处的吸光度。在pbs缓冲液中重构后,用增加量的普鲁兰多糖配制的呋瑞吗嗪(95μg)的吸光度显示在图4b中。与仅含呋瑞吗嗪而不含普鲁兰多糖的条件相比,用增加浓度的普鲁兰多糖基质配制的固体呋瑞吗嗪导致吸光度增加,并因此导致pbs缓冲液中呋瑞吗嗪浓度增加。实施例3储存的样品的重构将固体呋瑞吗嗪溶解在乙醇中,且将溶解的溶液添加到普鲁兰多糖(0%或15%w/v)的水溶液中,使得在50μl含有<10%v/v乙醇的溶液中的总浓度为1mm呋瑞吗嗪。将样品冷冻干燥或在环境温度下干燥。图5显示证明这些组合物重构到pbs,ph7.0中的能力的图像。在环境温度下干燥的具有15%w/v普鲁兰多糖的“滴”制剂在短暂移液后便进入溶液中。具有15%w/v普鲁兰多糖的冷冻干燥的样品在添加pbs后立即溶解。不含普鲁兰多糖的样品即使涡旋15分钟后也未完全溶解在pbs中,证明在pbs中的溶解度较低。实施例4普鲁兰多糖样品的吸光度测试纯2.5%w/v普鲁兰多糖和纯10%w/v普鲁兰多糖在pbs,ph6.8中的样品的吸光度。在210-600nm范围内的吸收光谱示于图6a(2.5%)和图6b(10%)中。这些光谱证明普鲁兰多糖在与呋瑞吗嗪相同的波长范围内不吸收,并且在含有呋瑞吗嗪的样品中不会人为地增强吸收信号。实施例5呋瑞吗嗪样品的hplc分析将散装固体呋瑞吗嗪在乙醇中稀释到最终浓度为10mm(溶液1)。将干燥的普鲁兰多糖溶解在纯水中,达到0%、2.5%、5%、10%或15%w/v的最终浓度(分别为溶液2a、2b、2c、2d和2e)。将45μl的溶液2a-2e移液到单独的1.5ml弹扣管型小瓶中。然后将5μl的溶液1添加到每个小瓶中并剧烈移液以混合,从而形成溶液3a-e,其各自含有最终浓度为1mm的呋瑞吗嗪。混合后,将含有溶液3a-e的小瓶置于干冰中冷冻1小时。然后将这些冷冻的储备液冻干过夜以形成含有呋瑞吗嗪的干燥普鲁兰基质。所有hplc迹线的一般方法:在小弹扣盖管中,用0.5mlpbs,ph6.8将上述呋瑞吗嗪样品(含有19.08μg呋瑞吗嗪)稀释到38.16μg/ml。将15μl的所述溶液在5小时内纯净地注入hplc(具有插页的小瓶)中以评估随时间的稳定性和溶解性。仪器:synergimax-rp50x4.6mm,2.54u。溶剂:0.1%tfa/乙腈水溶液。将市售的呋瑞吗嗪(5mm,promega目录号n113)在pbs中稀释到38.16μg/ml,并且也进行比较。在用0.5mlpbs,ph6.8稀释后立即获得样品hplc迹线并且在稀释后5小时获得样品的hplc迹线,并且所述迹线分别显示在图7(0%普鲁兰多糖–(a)0小时,(b)5小时)、图8(2.5%普鲁兰多糖–(a)0小时,(b)5小时)、图9(15%普鲁兰多糖–(a)0小时,(a)5小时)和图10(荧光素酶测定底物–(a)0小时,(b)5小时)中。(类似地获得5%普鲁兰多糖和10%普鲁兰多糖制剂和市售呋瑞吗嗪样品的迹线,数据未显示。)在保留时间5-10-5.13分钟下的峰(每个光谱中的主峰)表示呋瑞吗嗪。在5.36-5.37分钟的保留时间下的峰(用星号标记)表示氨基吡嗪,呋瑞吗嗪的已知降解产物(光谱证实)。具体的峰和面积百分比汇总在表1中。表1.图11和图12显示对来自图7至图10中所示的hplc迹线以及经由相同方法在额外时间点获得的迹线的编译和处理的数据的分析。图11a显示如通过在254nm处的吸光度所测量的每个样品的纯度分析,每条迹线均归一化为时间0。制备为具有普鲁兰多糖的干制剂的所有条件在水溶液中均显示出高纯度水平,并且没有显著的吸光度损失。缺乏普鲁兰多糖的条件(0%条件以及市售呋瑞吗嗪溶液,promega目录号n113)由于化学降解而在大约6小时内显示出明显的吸光度损失。图11b显示在pbs中具有增加量的普鲁兰多糖(0%-15%w/v)的配制的呋瑞吗嗪样品(50nmol)的峰面积的分析。(这些分析是针对图11a中分析的相同迹线进行)。市售呋瑞吗嗪和图11a中条形图中的0%条件的纯度损失也对应于峰面积的减少,指明信号损失不是由于溶解度随时间的变化,而是由于荧光素酶测定底物和0%普鲁兰多糖条件在实验的过程中的降解。因此,普鲁兰多糖的存在不仅有助于改善呋瑞吗嗪的水溶性,而且还有助于防止其在溶液中降解。图12显示在如上所述的样品中呋瑞吗嗪的氨基吡嗪副产物的形成。所述数据均表明普鲁兰多糖的存在有助于防止溶液中氨基吡嗪的形成。在pbs中重构后的5.5小时内,含有普鲁兰多糖的呋瑞吗嗪制剂显示最少的氨基吡嗪形成。相反,缺乏普鲁兰多糖的散装呋瑞吗嗪(0%条件)以及市售荧光素酶检测底物制剂在实验的过程中都显示氨基吡嗪增加了大约12%。所述数据与图11b中所示的纯度变化一致,这是由于在荧光素酶测定底物和0%普鲁兰多糖样品中呋瑞吗嗪的降解。实施例6纸基质上的呋瑞吗嗪组合物通过使用标准的3.2mm手持打孔器(品牌)从903蛋白保存卡上压出直径为3.2mm的圆形“斑点”,产生纸斑点。在乙醇中制备200μm和2μm的呋瑞吗嗪储备溶液。将5μl的这些溶液施加到每个纸斑点上,并在真空下干燥60分钟。然后将这些斑点在4℃下在黑暗中储存,直到进行测试。在测试时,将每个斑点置于标准96孔板的单个孔中,并用100μl的pbs缓冲液,ph7.0重构,其含有最终浓度为2ng/ml的纯化的(nluc)酶。呋瑞吗嗪的最终工作浓度分别为10μm和0.1μm。新鲜制备的市售荧光素酶检测底物以10μm和0.1μm制备以进行比较。结果示于图13中。图13a显示纸斑点样品和新鲜制备的市售荧光素酶测定底物样品的rlu随时间的变化。图13b显示每个样品在时间0的初始rlu。图13c显示穿孔斑点在管中的图像。这些结果证明,配制的呋瑞吗嗪可以干燥到固体基质/纸中,并在以后用非有机水性缓冲液条件重构。实施例7纸基质上的呋瑞吗嗪组合物这个实验基于国际专利公开案第wo2014/151736号中公开的结构互补测定。通过首先在495μl含有20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖的蔗糖蛋白缓冲液中稀释5μl山羊抗小鼠igg3-smbit(0.4mg/ml)来制备含有测定组分的903蛋白保存卡。然后将5μl的所述储备溶液添加到903卡上的位置2和4,并允许在35℃下干燥1小时。将5μl山羊抗小鼠igg3-lgbit(0.4mg/ml)在495μl相同的蔗糖蛋白缓冲液中稀释,且将5μl的所述溶液直接添加到903蛋白卡的位置2和4。然后将903卡在35℃下再次干燥1小时。在乙醇中制备5mm的呋瑞吗嗪储备液,且将5μl的所述储备液添加到卡位置至条件1、2和4。然后将卡置于高真空下15分钟。将卡保持在4℃或25℃下,且通过添加酶缀合的igg在几个时间点测试活性。在位置1处添加在pbs中的10pg新鲜标记抗体,以测试底物活性。记录图像,且示于图14a中:左–用标准相机拍摄的图像;中–使用las300成像仪拍摄的图像;右–使用iphone相机拍摄的图像。添加酶后,斑点1、2和4在此时间点均产生生物发光,指明底物保持了活性。类似地制备额外的样品组,且在4℃或25℃下保存3个月。记录图像,且示于图14b中:左–用标准相机拍摄的图像;中–添加在pbs中的10pg标记的抗体后在4℃下储存的卡的图像,以确定斑点1、2和3的底物活性,其中斑点4仅接受pbs作为阴性对照;右–在pbs中添加10pg标记的抗体后在25℃下储存的卡的图像。仅斑点2发光,而斑点1则不发光。这个实施例表明,蔗糖蛋白负载缓冲液的全部或一些组分(20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖)是在这个时间点和温度下具有底物活性所必需的,并且呋瑞吗嗪可以一起干燥在固体纸基质上,并且在4℃或25℃下储存延长的时间后重构。实施例8具有缓冲液和添加剂的在纸基质上的呋瑞吗嗪组合物这个实施例的目的是证明添加剂对总体重构效率和测定性能的影响。将样品在不同温度下储存,以模拟一定范围的热应力源,并测试这些条件下的总体性能和稳定性。903蛋白保护斑点卡(3.2mm冲孔)、蔗糖蛋白缓冲液(20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖(在使用前的晚上准备));在乙醇中的200μm呋瑞吗嗪溶液;6-氮杂-2-硫代胸腺嘧啶(att)在水中的20mm和50mm储备液;以及硫脲在水中的20mm和100mm储备液。向3.2mm903蛋白保存卡斑点中添加5μl的在乙醇中的200μm呋瑞吗嗪,以及各种额外组分,如下:样品1:呋瑞吗嗪样品2:呋瑞吗嗪+蔗糖蛋白缓冲液样品3:呋瑞吗嗪+att(20mm)样品4:呋瑞吗嗪+att(50mm)样品5:呋瑞吗嗪+att(20mm)+蔗糖蛋白缓冲液样品6:呋瑞吗嗪+att(50mm)+蔗糖蛋白缓冲液样品7:呋瑞吗嗪+硫脲(20mm)样品8:呋瑞吗嗪+硫脲(100mm)样品9:呋瑞吗嗪+硫脲(20mm)+蔗糖蛋白缓冲液样品10:呋瑞吗嗪+硫脲(100mm)+蔗糖蛋白缓冲液在添加其他组分(呋瑞吗嗪、att和/或硫脲)之前,将含有蛋白缓冲液的斑点在35℃下干燥1小时。当使用att时,将5μl的适当溶液添加到斑点中,然后在真空下干燥30分钟(使用20mm溶液时提供1mmatt的最终浓度,并且使用50mm溶液时提供2.5mmatt的最终浓度)。当使用硫脲时,将5μl的适当溶液添加到斑点中,然后在真空下干燥30分钟(使用20mm溶液时提供1mm的最终浓度,并且使用100mm溶液时提供5mm的最终浓度)。在测试之前,制作斑点并将其在4℃下储存5天。rlu实验条件–测定缓冲液:pbs,ph7.0;板:nbs实心白色板(3600)。使用不同最终浓度的nluc酶(20μg/ml、2μg/ml或0.2μg/ml)。数据呈现在图15a至图15d中,其中图15a至图15c显示在不同浓度的nluc酶(分别为20μg/ml、2μg/ml和0.2μg/ml)下来自发光反应的原始rlu,并且图15d显示在一种浓度(0.2μg/ml)下的nluc酶的%活性。这个数据表明,与其他制剂相比,一旦在pbs中重构,添加诸如att或硫脲的添加剂可有助于改善总体rlu和信号稳定性。实施例9具有不同聚合物的在纸基质上的呋瑞吗嗪组合物材料和方法:903蛋白保护斑点卡(3.2mm冲孔);呋瑞吗嗪。在测试前一天,用下述组分制备蛋白缓冲液。蛋白缓冲液1:纯净水蛋白缓冲液2:20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖蛋白缓冲液3:20mmna3po4、5%w/vbsa、0.25%v/v吐温20、2.5%w/v普鲁兰多糖蛋白缓冲液4:20mmna3po4、5%w/vbsa、0.25%v/v吐温20、2.5%w/v海藻糖将5μl的蛋白缓冲液1-4之一施加到每个斑点上,且允许斑点在35℃下干燥1小时。然后,将5μl新鲜制备的呋瑞吗嗪在乙醇中的200μm溶液施加到每个斑点,且将斑点在真空下干燥30分钟。将斑点在黑暗中分别在4℃、25℃和35℃下储存。对于发光测量,在测试时,将每个斑点置于标准96孔板的单个孔中,并用100μl的pbs缓冲液,ph7.0重构,其含有最终浓度为8ng/ml的纯化的(nluc)酶。立即开始动力学读数。制备后立即测试的斑点的结果显示在图16中,其中显示新鲜制备的底物的迹线用于比较。在4℃、25℃和37℃下储存一天后测试的斑点的结果分别显示在图17a、图17b和图17c中。在4℃、25℃和37℃下储存三天后测试的斑点的结果分别显示在图18a、图18b和图18c中。这些数据指明信号对于纸基质上的呋瑞吗嗪组合物更稳定,但总体信号较低。尽管样品仍然产生可用和稳定的信号,但在将呋瑞吗嗪添加到斑点之前,添加具有添加剂的蛋白缓冲液可能会阻止足够的呋瑞吗嗪完全进入纸中。实施例10纸基质中的配制的呋瑞吗嗪底物的加速稳定性研究测试纸呋瑞吗嗪样品,以确定与已知的呋瑞吗嗪制剂(底物,promega目录号n113,和活细胞底物,promega目录号n205)相比较,制剂对呋瑞吗嗪的热稳定性和功能完整性的影响,如由rlu所测量。903蛋白保护斑点卡(3.2mm冲孔)按如下方式处理。对于条件1和条件2,用5μl水(条件1)或蛋白缓冲液(20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖-条件2)预处理纸斑点。条件3是用5μl缺少蔗糖组分的蛋白缓冲液(20mmna3po4、5%w/vbsa、0.25%v/v吐温20)预处理而制备的。然后将所有条件在35℃下干燥60分钟。在乙醇中制备200μm呋瑞吗嗪的储备溶液,且将5μl的所述储备液添加到如上所述的条件1和条件2中。对于条件3,在2.5%普鲁兰多糖在具有<10%v/v乙醇的水中的混合物中制备200μm呋瑞吗嗪的储备液。然后将5μl的所述溶液添加到条件3,然后将所有斑点额外地在减压下干燥30分钟。然后将斑点在黑暗中在25℃或60℃下储存。在测量时,将来自每种条件的一个斑点置于单个孔中,且用含有nluc的pbs稀释。呋瑞吗嗪的最终理论浓度为10μm,且nluc的最终浓度为1ng/ml。编译的rlu数据显示在图19中,所述数据是在重构和测试之前在(a)60℃和(b)25℃下储存不同时间段的样品的数据。图19还显示在重构和测试之前将样品在(c)60℃和(d)25℃下储存不同时间段后在时间0的酶活性百分比的数据。扩展上述实验,使其包括高浓度(最终浓度为1mm和100μm)的呋瑞吗嗪和低浓度(最终浓度为10μm)的呋瑞吗嗪(图20)。每种条件如上所述制备:将斑点用水、蛋白缓冲液或缺少蔗糖的蛋白缓冲液预处理。在前两种条件下,将5μl的呋瑞吗嗪在乙醇中的2mm或200μm溶液添加到每个斑点中,然后在35℃下额外干燥30分钟。在第三条件下,20mm呋瑞吗嗪储备液或200μm呋瑞吗嗪储备液在2.5%普鲁兰多糖在具有<10%v/v乙醇的水中的混合物中制备。然后将5μl的所述溶液添加到条件3中,且将所有斑点在35℃下额外干燥30分钟。然后将斑点在黑暗中在25℃或60℃下储存。图20显示在重构和测试之前在(a)60℃和(b)25℃下储存不同时间段的样品的编译的rlu数据。图20还显示样品在重构和测试之前在(c)60℃和(d)25℃下储存不同时间段之后在时间0时酶活性百分比的数据。通过增加呋瑞吗嗪的负载浓度,maxrlu以及活性百分比都得到了总体改善。然而,在相当浓度下与含有蛋白缓冲液或蛋白缓冲液和普鲁兰多糖的两种预处理相比,未接受预处理(水)的斑点总体上性能仍然较好。实施例11在纸样品中呋瑞吗嗪制剂的干燥方法的影响用水或蛋白缓冲液(20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖)处理3.2mm冲孔的903蛋白保存卡斑点,并且将其在35℃下干燥1小时。制备呋瑞吗嗪在乙醇中的10mm储备溶液,且将20μl的所述溶液添加到980μl的2.5%(w/v)普鲁兰多糖或5%(w/v)普鲁兰多糖在水中的溶液中。充分混合之后,将5μl的所述溶液添加到每个斑点。将斑点在真空中或在黑暗中在环境温度下干燥2小时。干燥之后,将斑点在4℃下在黑暗中储存过夜。为了测试,将斑点添加到96孔nbs板的单个孔中。将100μl在pbs缓冲液,ph7.4中的1.068nmnluc溶液添加到每个孔中。将所述板置于光度计中并读取长达60分钟。每个斑点一式三份地运行。结果显示在图21中,其中图21a显示在真空下干燥的样品的数据,且图21b显示在环境空气下干燥的样品的数据。不论斑点是在真空中还是在环境温度下干燥,底物性能似乎均未受到显著影响。图21c显示图21a的汇总数据,指明普鲁兰多糖的存在降低了总体rlu输出。经验观察指明,普鲁兰多糖的存在使纸基质的表面变硬和成蜡质。这可能已经阻止了底物接近蛋白质,导致较低的光输出。所述观察结果还指明将不同组分添加到纸基质中的顺序可在总体功能中起作用。比较另一组斑点,在添加底物之后在环境温度下或在35℃下进行第二次干燥。将每个斑点都用水、蔗糖蛋白缓冲液(20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖)或普鲁兰多糖蛋白缓冲液(20mmna3po4、5%w/vbsa、0.25%v/v吐温20、2.5%w/v普鲁兰多糖)预处理并允许在35℃下干燥1小时。在乙醇中制备200μm的呋瑞吗嗪储备液,且将5μl的所述呋瑞吗嗪储备液添加到每个斑点中。然后允许斑点在黑暗中在环境温度下或在35℃下静置30分钟。然后将斑点在25℃下或在60℃下在黑暗中储存长达5天。在测试时,将与每种条件对应的斑点置于标准96孔板的孔中,且在每个孔中用100μlpbs溶液,ph7.0和2ng/mlnluc再水合,溶液中呋瑞吗嗪的最终浓度为10μm。结果显示在图22中。与在环境温度下第二次干燥的斑点相比,在35℃下第二次干燥的斑点显示出更高的rlu输出。这些结果在整个条件(蛋白缓冲液预处理或水对照)或斑点是否在25℃或60℃下储存高达5天上是一致的(maxrlu值显示在图22a和图22b中且%活性显示在图22c和图22d中)。这些结果表明,干燥方法的差异对总体底物性能有影响,并且在35℃下第二次干燥斑点对于底物性能是有利的。实施例12粉状普鲁兰多糖制剂的加速底物测试测试粉状呋瑞吗嗪样品,以确定与已知呋瑞吗嗪制剂(底物,promega目录号n113和活细胞底物,promega目录号n205)相比,如通过rlu和hplc测量,普鲁兰多糖制剂对呋瑞吗嗪的热稳定性和功能完整性的影响。材料和方法:将散装的固体呋瑞吗嗪在乙醇中稀释到最终浓度为10mm(溶液1);将干燥的普鲁兰多糖溶解在纯水中至最终浓度为0%、2.5%、5%、10%和15%w/v(分别为溶液2a、2b、2c、2d和2e)。将45μl的溶液2a-e移液到单独的1.5ml弹扣管型小瓶中。然后将5μl的溶液1添加到每个小瓶中,剧烈移液混合以形成溶液3a-e,其各自含有最终浓度为1mm的呋瑞吗嗪。混合后,将含有溶液3a-e的小瓶置于干冰中冷冻1小时。然后将这些冷冻的储备液冻干过夜以形成含有呋瑞吗嗪的干燥普鲁兰基质。用于测试的具体粉状呋瑞吗嗪样品制备如下:1)将1mm(总共50nmol)呋瑞吗嗪储备液制备为具有0%普鲁兰多糖的粉状制剂2)将1mm(总共50nmol)呋瑞吗嗪储备液制备为具有2.5%普鲁兰多糖的粉状制剂3)将1mm(总共50nmol)呋瑞吗嗪储备液制备为具有5%普鲁兰多糖的粉状制剂4)将1mm(总共50nmol)呋瑞吗嗪储备液制备为n113溶液(promega目录号n113)5)将1mm(总共50nmol)呋瑞吗嗪储备液制备为n205溶液(promega目录号n205)(注:在n113溶液之后约15小时制备n205溶液)6)散装呋瑞吗嗪(50nmol,从乙醇的储备溶液中分装出来)在hplc测试之前,将一半样品在25℃下储存,且将另一半在60℃下储存更长的时间,然后进行测试。为了进行hplc测试,将配制的呋瑞吗嗪(19.08μg)在小弹扣盖型管中用0.5mlpbs缓冲液,ph6.8稀释。将管涡旋约15秒钟,然后允许在室温下在黑暗中平衡30分钟。将15μl样品纯净地注入hplc(无插页的小瓶),0.1%tfa/乙腈水溶液,synergimax-rp50x4.6mm,2.54u。在0小时(图23a)或在60℃下储存48小时之后(图23b),包含5%w/v普鲁兰多糖的样品的hplc迹线显示仅有最少降解。在0小时(图24a)或在60℃下储存48小时之后(图24b),n113样品的hplc迹线显示显著更多的降解。获得其他样品的hplc数据(未显示),且处理所述数据以显示图25中的热稳定性迹线。测量曲线下方的面积并绘制35天。“散装”是指制造的固体呋瑞吗嗪。“0%普鲁兰多糖”是指将呋瑞吗嗪溶解在乙醇的储备溶液中,添加到水中(不含普鲁兰多糖)并冻干。图25a和图25b显示在25℃和60℃下作为原始峰面积的热稳定性,而图25c和图25d显示在25℃和60℃下作为峰面积百分比的热稳定性。当在室温或60℃下储存时,由固体呋瑞吗嗪组成的制剂显示出高水平和一致的化学完整性。相比之下,在荧光素酶测定底物(promega目录号n113)和活细胞底物(promega目录号n205)溶液中配制的呋瑞吗嗪当在升高的温度下储存时在测量的时间内显示出峰高和峰面积的明显损失。为了进行发光测量,将粉状呋瑞吗嗪样品#1-5在pbs中重构,而样品#6在乙醇中重构(全部为500μl)。将样品在室温下平衡30分钟。然后将样品进一步以1:5稀释(从100μm稀释至20μm),然后再以1:100稀释(从20μm稀释至0.2μm)。将50μl的所述溶液添加到96孔板的孔中,读取背景,然后添加(nluc)酶。(在添加之前,将商业nluc储备样品在pbs中稀释至2ng/ml的浓度,且向每个孔中添加50μl。)稀释后,最终浓度为0.1μm呋瑞吗嗪和1ng/mlnluc。然后确定rlu。(背景是不添加nluc的2x底物溶液的读数。)编译的rlu数据显示在图26中。每个图例中的数字与以下制剂相对应:1-0%普鲁兰多糖(注–所述样品遇到到溶解性问题,并且可能尚未完全重构);2-2.5%普鲁兰多糖冻干饼制剂;3-5%普鲁兰多糖冻干饼制剂;4-荧光素酶检测底物(promega目录号n113);5-活细胞底物(n205);6-散装呋瑞吗嗪(在乙醇中重构)。图26a至图26c中显示如上所述使用50μm底物(图26a)、10μm底物(图26b)或0.1μm底物(图26c)在重构和测试之前将样品在60℃下储存不同时间段后的数据。图26d至图26f中显示如上所述使用50μm底物(图26d)、10μm底物(图26e)或0.1μm底物(图26f)在重构和测试之前将样品在25℃下储存不同时间段后的数据。图27显示酶活性百分比的数据。每个图例中的数字与以下制剂相对应:1-0%普鲁兰多糖(注–所述样品都遇到溶解性问题,并且可能尚未完全重构);2-2.5%普鲁兰多糖冻干饼制剂;3-5%普鲁兰多糖冻干饼制剂;4-荧光素酶检测底物(promega目录号n113);5-活细胞底物(n205);6-散装呋瑞吗嗪(在乙醇中重构)。图27a至图27c显示如上所述使用50μm底物(图27a)、10μm底物(图27b)或0.1μm底物(图27c)在重构和测试之前将样品在60℃下储存不同时间段后在时间0时的酶活性,并且图27d至图27f显示如上所述使用50μm底物(图27d)、10μm底物(图27e)或0.1μm底物(图27f)在重构和测试之前将样品在25℃下储存不同时间段后在时间0时的酶活性。如由荧光素酶测定中的rlu输出所示,固体呋瑞吗嗪样品在暴露于高温后显示一致的化学完整性。相反,在市售n113溶液和n205溶液中配制的呋瑞吗嗪在高温下储存后显示发光信号随时间的损失。(注:样品6溶解在乙醇中,在较高的浓度下抑制nluc酶活性。)实施例13配制的呋瑞吗嗪膜涂覆的微量滴定板配制的呋瑞吗嗪膜直接形成到微量滴定板上。在微量滴定板的孔中直接制备含有在2.5%(w/v)普鲁兰多糖或5%(w/v)普鲁兰多糖中的200mm呋瑞吗嗪的膜。在图29中看到这种形式的代表性图像(为了清楚和呈现目的而人工着色)。孔涂层如下制备:制备2mm呋瑞吗嗪在乙醇中的储备液(溶液1)。单独地,在水中制备2.5%和5%w/v普鲁兰多糖的溶液(分别为溶液2和溶液3)。将45μl的溶液2或溶液3添加到标准96孔板的单个孔中。然后将5μl的溶液1添加到每个含有溶液2或溶液3的孔中,并彻底移液以混合。最终溶液中乙醇的浓度必须小于5%v/v。较高浓度的乙醇会导致普鲁兰多糖从溶液中析出。然后允许板在黑暗中在环境条件下干燥3小时。将孔中的膜用100μlpbs,ph7.0再水合,然后在振荡器上在50μl/孔的pbs中立即或在30分钟的预平衡期后,向每个孔中添加2ng/mlnluc,对于所有条件,在溶液中呋瑞吗嗪的最终浓度为10μm。读出rlu,并将其与新鲜制备的市售呋瑞吗嗪底物(活细胞底物,promega目录号n205)进行比较。数据显示在图28中,其中(a)数据显示为未经预平衡的原始rlu,(b)数据显示为未经预平衡的活性,并且(c)数据显示为经预平衡的原始rlu。所述实施例强调呋瑞吗嗪可在硬质表面上的基于普鲁兰多糖的膜中干燥,且在指定的时间重构。基于视觉观察,所述膜也比散装固体呋瑞吗嗪更快且更完全地重构。所述数据还表明,在pbs微量滴定板中基于呋瑞吗嗪-普鲁兰多糖的膜的预平衡导致光输出显著降低。图29显示使用与上述相同的方法制成的呋瑞吗嗪涂膜板的图像,但是添加了食用色素以能够使膜涂层可视化。图30a显示与图28中呈现的数据所述的相同形式制剂的动力学读数,但呋瑞吗嗪的负载浓度更高(在100μl中最终为20μm),并且在一些情况下,含有膜的呋瑞吗嗪制剂作为完整溶液一起成膜。图30b显示与图30a中描述的相同实验的活性百分比。图30c显示涂膜的微量滴定板在储存一段时间后的稳定性研究结果,第10天仍保留约35%的活性。实施例14配制的呋瑞吗嗪的纯度、稳定性和副产物形成的hplc和质谱分析如实施例12中所述用在0%、2.5%和5%w/v普鲁兰多糖中的19.07μg的呋瑞吗嗪制备在冻干的普鲁兰多糖基质中配制的呋瑞吗嗪。将样品,包括散装呋瑞吗嗪、荧光素酶测定底物(promega目录号n113)和活细胞底物(promega目录号n205),在25℃或60℃下储存35天。将样品在pbs缓冲液中重构,或者在散装呋瑞吗嗪样品和0%普鲁兰多糖样品的情况下在乙醇中重构,允许在室温下平衡30分钟,然后在hplc上分析呋瑞吗嗪降解途径的已知副产物。吸光度数据显示在图31中:a-散装呋瑞吗嗪;b-0%普鲁兰多糖;c-2.5%普鲁兰多糖;d-5%普鲁兰多糖;e-荧光素酶检测底物;和f-活细胞底物。在每种情况下,相对于市售的基于溶液的储存制剂(promega目录号n113和目录号n205),固体形式的配制的呋瑞吗嗪显示显著减少的降解产物。图32显示相对于呋瑞吗嗪峰的单种副产物的面积百分比:a-散装呋瑞吗嗪;b-0%普鲁兰多糖;c-2.5%普鲁兰多糖;d-5%普鲁兰多糖;e-荧光素酶检测底物;和f-活细胞底物。在固体普鲁兰多糖制剂中,呋瑞吗嗪是主峰,副产物的形成量极少,尤其是在室温下储存时(每种情况下为左条)。相比之下,在35天后,当以商业制剂在25℃(左条)或60℃(右条)下储存时,呋瑞吗嗪几乎完全损失。实施例15在室温下储存6个月时配制的呋瑞吗嗪组合物底物活性如实施例1,条件1和条件3中所述,将19μg呋瑞吗嗪配制成在15%w/v普鲁兰多糖中制备的冻干饼或膜滴。将样品在25℃下在环境光存在下储存六个月。两种制剂均用100μlpbs,ph7.0和1ng/mlnanoluc(nluc)重构,溶液中呋瑞吗嗪的最终浓度为10μm。读出rlu,并将其与新鲜制备的市售呋瑞吗嗪底物(活细胞底物,promega目录号n205)相比较。所述实验的结果显示在图33中(a-原始rlu,b-自时间0的活性百分比)。在环境温度和光线下储存6个月后,当暴露于荧光素酶时,在普鲁兰多糖基质中配制的固体呋瑞吗嗪仍然可行。实施例16在不同的固体支撑基质上的配制的呋瑞吗嗪活性和稳定性测试四种不同类型的纸的不同性质,包括底物保留率和对底物完整性的影响。纸类型包括:1.粗玻璃纤维:glassmicrofiber934-ah(ahlstrom,颗粒保留度:1.5μm,厚度:435μm);2.细玻璃纤维:玻璃纤维诊断垫(emdmillipore),gfdx103000,批号495362;3.纤维素:纤维素样品垫(emdmillipore),cfsp20300m,批号11065;和4.903蛋白保存卡将每个纸样品切成7x7mm的正方形。制备10mm的呋瑞吗嗪储备液,且将10μl的所述储备液添加到每个纸基质中。将样品在35℃下干燥30分钟。将这些卡在黑暗中在25℃或60℃下储存72小时。然后将样品置于玻璃小瓶中,且添加1ml乙醇。将小瓶超声处理10秒,且将溶剂提取,过滤并通过分析型hplc分析。这些实验的结果显示在图34中。图34a显示在从纸或纤维基质中提取之后呋瑞吗嗪峰的原始面积。从纸中提取并从溶液中分析的呋瑞吗嗪的量也受纸类型的影响(图34b)。对于被提取回溶液中的底物,与散装呋瑞吗嗪相比,当将呋瑞吗嗪干燥到纸或纤维基质上时,呋瑞吗嗪的降解速率稍快。另外,呋瑞吗嗪底物可有效地干燥且由多种固体表面重构(图34c)。结合报道蛋白lgtrip进行额外实验,以确定纸上的底物稳定性。为了制备纸表面,准备含有200μl5umlgtrip(3546)(seqidno:3;参见,例如,美国专利申请第62/684,014号,通过引用整体并入本文)、5mmatt和5mm抗坏血酸的小瓶。将约5μl的所述溶液添加到每个斑点,然后允许斑点在35℃下干燥1小时。干燥后,制备1mm呋瑞吗嗪在乙醇中的储备液。将约5μl的所述溶液添加到每个斑点,且允许在35℃下额外干燥30分钟。用底物和lgtrip输入测试不同的材料。在测试时,添加新鲜的nluc以分离底物。图35a显示当将新鲜的nanoluc添加到干燥的lgtrip和底物中时在由表面的重构产生的三种不同固相材料(whatman903、ahlstrom237和ahlstrom6613h)中的生物发光信号。alhstrom6613h似乎对随时间的信号输出有害。总体上,测定组分的稳定性可受到其所嵌入的固体基质材料的组成的影响。图35b显示来自whatman903纸的生物发光信号,所述纸含有lgtrip和底物两者,并且在环境条件下储存超过25天。在测试时,将斑点暴露于在pbs中的1nm二肽中。总体上,所述实验表明,在环境温度下延长的储存时间后,没有显著的来自材料的信号损失。实施例17添加剂对不同固相支撑基质上的配制的呋瑞吗嗪活性和稳定性的影响将不同的添加剂与具有呋瑞吗嗪的溶液混合,且将其干燥到纸表面上。这些实验旨在改善在纸基质内干燥时的总体底物完整性。在乙醇中制备10mm抗坏血酸溶液。然后将所述溶液添加到散装呋瑞吗嗪中,制成在乙醇中含有1:1抗坏血酸和呋瑞吗嗪的溶液。然后将10μl的所述溶液添加到先前实施例中描述的相同纸基质中。将样品在35℃下干燥30分钟。然后将斑点在25℃下或在60℃下在黑暗中储存长达72天。将样品置于玻璃小瓶中,且添加1ml乙醇。将小瓶超声处理10秒,且将溶剂提取,过滤并通过分析型hplc分析。这些实验的结果描述在图36中。呋瑞吗嗪峰的原始面积绘制在图36a中,与不含抗坏血酸添加剂的样品相比,呋瑞吗嗪的吸光度更好。在呋瑞吗嗪向溶液中的总体回收百分比(图36b)以及呋瑞吗嗪纯度(图36c)方面也观察到了这种效果。纯度增加了约15-20%,这表明抗坏血酸的存在有助于限制在纸上储存时呋瑞吗嗪底物的热降解或化学降解。实施例18化学预处理不同固相支撑基质对配制的呋瑞吗嗪活性和稳定性的影响将纸基质(ahlstromglassmicrofiber934-ah和903蛋白保存卡)在30%w/v柠檬酸溶液中浸泡30分钟,然后允许在35℃下干燥过夜。制备10mm呋瑞吗嗪在etoh中的储备液,并将10μl的储备液添加到7x7mm纸卡中,且在35℃下干燥30分钟。然后将这些卡在室温或60℃下在黑暗中储存72小时。在读出时,将卡用1ml乙醇提取并超声处理15秒。然后将提取的溶剂过滤并注入分析型hplc。这些实验的结果显示在图37中。呋瑞吗嗪峰的原始面积显示在图37a中。与未进行柠檬酸预处理的纸基质相比,在施加呋瑞吗嗪底物之前用30%柠檬酸溶液预处理纸基质对提取到乙醇中之后底物的总体纯度影响最小(图37c)。用乙醇提取之后,回收到溶液中的底物量也存在有限的改善(图37b)。实施例19机械预处理不同固相支撑基质对呋瑞吗嗪活性和稳定性的影响将纸基质(ahlstromglassmicrofiber934-ah和903蛋白保存卡)在水中浸泡30分钟,然后在减压下干燥过夜,以使存在于纸基质内的孔塌陷或收缩。制备10mm呋瑞吗嗪在乙醇中的储备液,且将10μl的储备液添加到7x7mm纸卡中,且在35℃下干燥30分钟。然后将这些卡在室温或60℃下在黑暗中储存72小时。在读出时,将卡用1ml乙醇提取并超声处理15秒。将提取的溶液过滤并注入分析型hplc中以便分析。所述实验的结果显示在图38中,其中呋瑞吗嗪峰的原始面积显示在图38a中,回收率百分比显示在图38b中,且纯度显示在图38c中。与未预处理的纸相比,在已添加底物并将其干燥至预先在压力下干燥的纸上的情况下,在底物纯度或到溶液中的回收率方面没有显著改善。实施例20添加剂对不同固相支撑基质上的配制的呋瑞吗嗪活性和稳定性的影响将不同的添加剂与具有呋瑞吗嗪的溶液混合,且将其干燥到纸表面上。这一系列的实验旨在帮助改善在纸基质内干燥时的总体底物完整性。在乙醇中制备10mm柠檬酸溶液。将所述溶液添加到散装呋瑞吗嗪中,制成在乙醇中含有1:1柠檬酸和呋瑞吗嗪的溶液。然后将10μl的所述溶液添加到先前实施例中描述的相同纸基质中。将样品在35℃下干燥30分钟。将这些卡在黑暗中在25℃或60℃下储存72小时。将样品置于玻璃小瓶中,且添加1ml乙醇。将小瓶超声处理10秒,且将溶剂过滤并通过分析型hplc分析。这些实验的结果描述在图39中。在存在柠檬酸(a)和不存在柠檬酸(b)的情况下在纸中干燥的呋瑞吗嗪的呋瑞吗嗪峰的原始面积绘制在图39a和图39b中。在存在柠檬酸(c)和不存在柠檬酸(d)的情况下在纸中干燥的呋瑞吗嗪的254nm处的纯度绘制在图39c和图39d中。这些绘图显示当在具有柠檬酸的混合物中干燥时呋瑞吗嗪的吸光度更好。这种吸光度增加对应于约10-20%的纯度增加,表明柠檬酸的存在有助于限制在所述实验的过程中呋瑞吗嗪底物的热化学降解。实施例21在存在蔗糖蛋白负载缓冲液的情况下柠檬酸和抗坏血酸对配制的呋瑞吗嗪活性和稳定性的影响在存在或不存在蔗糖蛋白缓冲液(20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖)的情况下测试柠檬酸和抗坏血酸对呋瑞吗嗪活性和稳定性的影响。如上所述,斑点由903蛋白保存卡制备。将每个斑点用蔗糖蛋白缓冲液或水预处理,且允许在35℃下干燥1小时。在乙醇中或在具有200μm柠檬酸或200μm抗坏血酸的乙醇溶液中制备200μm呋瑞吗嗪的储备液。将5μl含有相等摩尔浓度的柠檬酸或抗坏血酸的呋瑞吗嗪或呋瑞吗嗪溶液添加到每个斑点。然后将斑点在35℃下再次干燥1小时。然后将这些斑点在25℃下在黑暗中储存长达12天。在测试时,将与每种条件对应的斑点置于标准96孔板的孔中,且在每个孔中用100μlpbs溶液,ph7.0和2ng/mlnluc再水合,溶液中呋瑞吗嗪的最终浓度为10μm。读出rlu,并将其与新鲜制备的市售呋瑞吗嗪底物(活细胞底物,promega目录号n205)相比较。这些实验的结果显示在图40中。在纸上,用蔗糖蛋白缓冲液预处理的斑点在12天的时间内显示明显的信号损失(图40a)。与用水或在存在抗坏血酸或柠檬酸的情况下的水预处理的条件相比较,这些结果对应于底物活性百分比的几乎完全损失,这显示在12天内明显的稳定性和信号输出(图40b)。这些结果的汇总显示在图40c中。尤其是与单独的水预处理相比较,当在纸表面上干燥并储存时,抗坏血酸和柠檬酸可有助于保持底物完整性。然而,对于长期储存和重构,蔗糖蛋白缓冲液内的一种或多种组分可对底物生存力具有负面影响。实施例22单独或批量的斑点储存对呋瑞吗嗪活性和稳定性的影响如上所述,测试具体储存工序对由903蛋白保存卡制备的纸斑点的影响。将每个斑点用水预处理,然后在35℃下干燥1小时。在乙醇中制备200μm呋瑞吗嗪的储备液,且将5μl的所述溶液添加到每个斑点。然后将斑点在35℃下额外干燥30-60分钟。然后将斑点分离,并单独地储存在加盖的管中,或者在25℃下在黑暗中在一个小瓶中一起储存(批量储存)长达12天。在测试时,将与每种条件对应的斑点置于标准96孔板的孔中,且在每个孔中用100μlpbs溶液,ph7.0和2ng/mlnluc再水合,溶液中呋瑞吗嗪的最终浓度为10μm。这些实验的结果描述在图40中。单独储存的斑点显示比批量储存的斑点高的maxrlu(图41a)。这些结果与观察到的活性百分比一致(图41b)。这些结果表明,储存方法也可对总体底物性能具有影响。与批量储存的斑点相比,在单个容器中储存可有助于将环境暴露限于诸如光、空气和水分的不利因素,在每次取出要测试的斑点时,这些斑点都会暴露于这些环境因素。实施例23从反应孔中去除斑点后的信号产生如实施例6中所述,斑点由903蛋白保存卡制备。每个斑点用蔗糖蛋白缓冲液(20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖)或用水预处理,且允许在35℃下干燥1小时。在乙醇或具有200μm柠檬酸盐或200μm抗坏血酸盐的乙醇溶液中制备200μm呋瑞吗嗪的储备液。将5μl的呋瑞吗嗪或含有相等摩尔比的柠檬酸盐或抗坏血酸盐的呋瑞吗嗪溶液添加到斑点中。然后将斑点在35c下额外干燥一小时。然后将斑点在25℃下在黑暗中储存长达5天。在测试时,将斑点用含有2ng/mlnluc酶的pbs,ph7.0重构,且动态读出rlu。45分钟之后,将斑点从孔中物理去除,并置于含有新鲜pbs溶液,ph7.0和2ng/mlnluc的新孔中,且在先前含有斑点的孔和含有转移的纸斑点的新孔中继续读出动力学rlu信号。图42a展示先前含有斑点的孔和转移有斑点的新孔的动力学rlu值(由底物配制后的+指明)。汇总的rlu结果展示在图42b中,比较了rlu结果45分钟时原始读出rlu、刚去除后的现在空孔以及刚将斑点转移到含有新鲜酶的新孔后取得的rlu值。从原始斑点读数到去除斑点的孔的rlu值没有变化,指明底物从纸基质中释放并平衡到周围的溶液中。在含有转移的斑点的孔中恢复较低的信号,指明底物制剂在纸基质本身中保留了一些。通过将从孔中转移出斑点之前存在的rlu信号与在去除斑点或将其置于新孔中之后保留的信号进行比较,计算出每种条件的信号恢复百分比(图42c)。在将斑点转移到含有新鲜pbs溶液,ph7.0和2ng/mlnluc的新孔中后,在新孔中观察到信号百分比的约一半。这指明残留的底物保留在纸本身中,而大多数底物被释放到原始孔的溶液中。实施例24bsa和糖对呋瑞吗嗪活性和稳定性的影响制备10种不同版本的蛋白负载缓冲液,以确定在固体表面干燥并重构之后bsa和糖组分对呋瑞吗嗪活性和稳定性是否有影响。制备并测试的缓冲液如下:1.蛋白缓冲液1:20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖2.蛋白缓冲液2:20mmna3po4、5%w/vbsa、0.25%v/v吐温20、10%w/v蔗糖、5mm抗坏血酸盐3.蛋白缓冲液3:20mmna3po4、0.25%v/v吐温20、10%w/v蔗糖4.蛋白缓冲液4:20mmna3po4、0.25%v/v吐温20、10%w/v蔗糖、5mm抗坏血酸盐5.蛋白缓冲液5:20mmna3po4、5%w/vbsa、0.25%v/v吐温206.蛋白缓冲液6:20mmna3po4、5%w/vbsa、0.25%v/v吐温20、5mm抗坏血酸盐7.蛋白缓冲液7:20mmna3po4、5%w/vbsa、0.25%v/v吐温20、2.5%普鲁兰多糖8.蛋白缓冲液8:20mmna3po4、5%w/vbsa、0.25%v/v吐温20、2.5%普鲁兰多糖、5mm抗坏血酸盐9.蛋白缓冲液9:20mmna3po4、0.25%v/v吐温20、2.5%普鲁兰多糖10.蛋白缓冲液10:20mmna3po4、0.25%v/v吐温20、2.5%普鲁兰多糖、5mm抗坏血酸盐确定每种缓冲液的ph,并在表2中列出。表2.缓冲液ph19.9329.04311.11410.53511.6969.0079.8989.00911.451010.45如实施例6中所述,由903蛋白保存卡制备斑点。将每个斑点用缓冲液1-10处理,然后在35℃下干燥1小时。在乙醇中制备200μm的呋瑞吗嗪储备液,且将5μl的所述溶液添加到每个斑点。然后将斑点在35℃下额外干燥一小时。在测试时,将与每种条件对应的斑点置于标准96孔板的孔中,且在每个孔中用100μlpbs溶液,ph7.0和2ng/mlnluc再水合,溶液中呋瑞吗嗪的最终浓度为10μm。读出rlu,并将其与新鲜制备的市售呋瑞吗嗪底物(活细胞底物,promega目录号n205)相比较。这些结果描述在图43中。通过去除bsa,信号有少量降低,这在抗坏血酸盐存在下恢复(缓冲液3和缓冲液4,图43a)。然而,当去除蔗糖组分时,观察到信号显著降低(缓冲液5和缓冲液6)。在抗坏血酸盐存在下,或者如果用2.5%w/v普鲁兰多糖代替蔗糖组分,则所述信号不会恢复(缓冲液7和缓冲液8)。当负载缓冲液中既没有bsa也没有蔗糖时,观察到最低的信号。动力学结果显示在图43b中。在缺少蔗糖、bsa或两者的条件中,信号在实验的过程中急剧下降,而在其他条件中则未观察到。抗坏血酸盐的存在限制在这些条件中的信号衰减率(缓冲液3对缓冲液4、缓冲液5对缓冲液6、或缓冲液9对缓冲液10)。这些差异对应于活性百分比的明显变化(图43c)。缓冲液3、5和9的溶液动力学rlu读数较差。这些缓冲液还具有最高的ph值(表2),指明ph值在903纸上的底物性能方面也可发挥作用。实施例25单种缓冲液组分对呋瑞吗嗪活性和稳定性的影响制备八种不同的蛋白负载缓冲液,以确定在储存在固体纸表面上的同时具体缓冲液组分对呋瑞吗嗪的活性和稳定性是否有影响。制备并测试的缓冲液如下:1.缓冲液1:水2.缓冲液2:水+5mm抗坏血酸盐3.缓冲液3:bsa4.缓冲液4:bsa+5mm抗坏血酸盐5.缓冲液5:na3po4+吐温206.缓冲液6:na3po4+吐温20+5mm抗坏血酸盐7.缓冲液7:bsa+na3po4+吐温208.缓冲液8:bsa+na3po4+吐温20+5mm抗坏血酸盐将所有缓冲液的ph固定为7,然后将其添加到纸斑点。斑点是如实施例6中所述由903蛋白保存卡制备的。将每个斑点用缓冲液1-8处理,然后在35℃下干燥1小时。在乙醇中制备200μm呋瑞吗嗪储备液,且将5μl的所述溶液添加到每个斑点中。然后将斑点在35℃下额外干燥一小时。在测试时,将与每种条件对应的斑点置于标准96孔板的单独孔中,且在每个孔中用100μlpbs溶液,ph7.0和2ng/mlnluc再水合,溶液中呋瑞吗嗪的最终浓度为10μm。读出rlu,并将其与新鲜制备的市售呋瑞吗嗪底物(活细胞底物,promega目录号n205)相比较。这些结果显示在图44中。用含有抗坏血酸盐、bsa或二者的组合的缓冲液预处理的斑点在25℃下在黑暗中储存的同时在8天内显示出良好的稳定性(图44a)。缺乏bsa或抗坏血酸盐且含有吐温20以及高含量盐的条件显示明显的原始信号损失。在最初的几天中,活性百分比也存在明显损失(图44b)。这些结果表明,在干燥并储存在固体表面上的同时,吐温20和/或高盐的存在可对底物完整性具有负面影响,如由总体rlu产量的下降所见。抗坏血酸的存在有助于抵消这种影响。从第0天起的代表性动力学迹线显示在图44c中。在缺乏蛋白缓冲液的组分的条件(缓冲液1或缓冲液2)中,信号损失率更高。实施例26prionex对呋瑞吗嗪活性和稳定性的影响制备六种不同的蛋白负载缓冲液,以确定在储存在固体表面上的同时用prionex代替bsa对呋瑞吗嗪的活性和稳定性是否有影响。测试的缓冲液如下:1.缓冲液1:水2.缓冲液2:水+5mm抗坏血酸盐3.缓冲液3:1%v/vprionex4.缓冲液4:1%v/vprionex+5mm抗坏血酸盐5.缓冲液5:0.5%v/vprionex6.缓冲液6:0.5%v/vprionex+5mm抗坏血酸盐将每种缓冲液的ph保持在ph7。斑点是如实施例6中所述由903蛋白保存卡制备的。将每种缓冲液用缓冲液1-6处理,然后在35℃下干燥1小时。在乙醇中制备200μm呋瑞吗嗪储备液,且将5μl的所述溶液添加到每个斑点中。然后将斑点在35℃下额外干燥30分钟。然后将斑点在25℃下在黑暗中储存长达20天。在测试时,将与每种条件对应的斑点置于标准96孔板的单独孔中,且在每个孔中用100μlpbs溶液,ph7.0和2ng/mlnluc再水合,溶液中呋瑞吗嗪的最终浓度为10μm。读出rlu,并将其与新鲜制备的市售呋瑞吗嗪底物(活细胞底物,promega目录号n205)相比较。结果描述在图44中。在所有情况下,在实验的过程中均观察到高水平的rlu输出。仅用水预处理的条件在三周内显示出一些信号损失(图45a)。测试第一天的动力学数据显示在图45b中。与缺乏prionex的条件相比,prionex的存在有助于稳定重构后的信号,且限制信号衰减。实施例27att对配制的呋瑞吗嗪活性和稳定性的影响制备六种不同的蛋白负载缓冲液,以确定在储存在固体纸表面上的同时att的存在对呋瑞吗嗪活性和稳定性是否有影响。制备并测试的负载缓冲液如下:1.水+5mm抗坏血酸盐2.水+5mm抗坏血酸盐+5mmatt3.1%prionex+5mm抗坏血酸盐4.1%prionex+5mm抗坏血酸盐+5mmatt5.0.5%prionex+5mm抗坏血酸盐6.0.5%prionex+5mm抗坏血酸盐+5mmatt将每种缓冲液的ph控制到ph7。斑点是如实施例6中所述由903蛋白保存卡制备的。将每种缓冲液用缓冲液1-6处理,然后在35℃下干燥1小时。在乙醇中制备200μm呋瑞吗嗪储备液,且将5μl的所述溶液添加到每个斑点中。然后将斑点在35℃下额外干燥一小时。然后将斑点在25℃下在黑暗中储存长达23天。在测试时,将与每种条件对应的斑点置于标准96孔板的单独孔中,且在每个孔中用100μlpbs溶液,ph7.0和2ng/mlnluc再水合,溶液中呋瑞吗嗪的最终浓度为10μm。读出rlu,并将其与新鲜制备的市售呋瑞吗嗪底物(活细胞底物,promega目录号n205)相比较。结果描述在图45中。在所有情况下,均观察到高rlu输出(图46a)。储存22天后,斑点的动力学轨迹在实验的过程中也显示出高且稳定的信号(图46b)。所有的本发明条件都有利于在环境温度下在固体表面上底物的活性和储存稳定性。实施例28冻干定向到微量滴定板中的配制的呋瑞吗嗪制备呋瑞吗嗪且直接在微量滴定板孔内冻干。制备产生含有直接在标准96孔微量滴定板(costar目录号3912)的孔中制备的在5%(w/v)普鲁兰多糖中的200μm或2mm呋瑞吗嗪的冻干粉状制剂的孔。这种形式的代表性图像显示在图47a中。如下制备板:制备乙醇中的2mm和200μm呋瑞吗嗪储备液(溶液1)。单独地,在水中制备5%w/v普鲁兰多糖的溶液(溶液2)。将45μl的溶液2添加到单个孔中。然后将5μl溶液1添加到每个包含溶液2的孔中,并彻底移液以混合。将5μl的纯乙醇添加到溶液2中作为阴性对照。将板置于干冰上冷冻1小时,然后冻干过夜。含有呋瑞吗嗪饼的板在每个孔中用100μlpbs,ph7.0和2ng/mlnluc再水合,呋瑞吗嗪的最终浓度分别为10μm或100μm。读出rlu并将其与新鲜制备的市售呋瑞吗嗪底物(活细胞底物,promega目录号n205)或在5%w/v普鲁兰多糖存在下的新鲜活细胞底物进行比较。动力学数据显示在图47b中。所述实施例表明,冻干粉制剂形式可直接在诸如微量滴定板的固体表面上制备,且使用诸如pbs的水性缓冲液重构。实施例29底物添加的分层形式图48显示两部分分层系统的预言性实施例,所述系统包括在单个纸卡上的单独表面组分,或在同一表面上单独处理的组分,其分别含有底物或检测组分。使用时,将表面的两侧折叠在一起,使得每个表面彼此紧密接触。然后将含有目标分析物的样品溶液添加到折叠的表面材料中。溶液的存在将导致不同的组分在固体基质内再水合并混合,导致生物发光复合物的互补诱导形成。所述过程与底物结合将产生可被检测和分析的光。实施例30抗坏血酸钠对底物制剂的影响将一体积的荧光素酶测定底物(promega目录号n113)与50体积的含有浓度为0mm至300mm的抗坏血酸钠的荧光素酶测定缓冲液(promega目录号#n112)合并。将溶液在37℃下孵育,然后在几个时间点进行测定。将根据制造商的指导说明使用的荧光素酶测定底物(在实验的过程期间在-20℃下储存,并在每个时间点重构)用作阳性对照。在每个时间点,将表达酶的细胞培养物用作样品。将一体积的重构的荧光素酶测定缓冲液与一体积的样品混合。3分钟后,用bio-tekh196孔板读数器测量发光强度。对于每个样品,将发光强度减去背景并归一化为-20℃对照信号。如图49中所示,将抗坏血酸钠添加到荧光素酶测定缓冲液中减少重构后的试剂活性损失。当将底物在含有300mm抗坏血酸钠的荧光素酶测定缓冲液中重构且在37℃下保持23小时时,发光强度为对照的66%,相比之下,在不存在抗坏血酸钠的情况下为38%。在37℃下41小时之后,发光强度为31%,相比之下,9%。随着抗坏血酸钠量的减少,稳定作用减弱。请注意,来自含有3mm抗坏血酸钠的缓冲液条件的结果最有可能是由于实验误差。实施例31羟丙基-β-环糊精对底物制剂的影响通过在含有200mmmesph6.0、200mm羟丙基-β-环糊精(hp-β-cd)和600mm抗坏血酸钠的缓冲液中以1:25稀释储备液来制备4x呋瑞吗嗪溶液。使用virtisadvantage冻干机将溶液冻干48小时。然后将这些冻干制剂在高温(37℃)下储存历时实验的持续时间。在24小时和48小时之后,将沉淀物在荧光素酶测定缓冲液中重构,使得溶液中组分的最终浓度为2x呋瑞吗嗪(自储备液以1:50稀释)、100mmmesph6.0、100mmhp-β-cd和300mm抗坏血酸钠。为了进行比较,在荧光素酶测定缓冲液中制备底物,并将其在37℃下孵育历时实验的持续期间。根据制造商的指导说明使用的底物(在实验的过程期间在-20℃下储存,并在每个时间点重构)用作阳性对照。在每种情况下,将一体积的重构的荧光素酶测定底物与一体积的样品混合。3分钟后,用bio-teksynergyh196孔板读数器测量发光强度。将表达nanoluc的细胞培养物用作样品。对于每个样品,将发光强度减去背景并归一化为-20℃对照信号。冻干前,向缓冲液中添加hp-β-cd和抗坏血酸钠允许沉淀物直接溶解在缓冲液中(不添加溶剂),并在37℃下保持稳定48小时的时间,如图50中所示。在37℃下孵育的工作浓度底物在荧光素酶测定缓冲液中的非冻干溶液在相同的时间后显示出90%的活性降低。此外,重要的是要注意,当将沉淀物与标准试剂盒制剂进行比较时,观察到一些信号增强。实施例32单独和组合的缓冲液添加剂对底物制剂的影响将呋瑞吗嗪以1:50稀释到具有以下最终组成的缓冲液中:-缓冲液-缓冲液+300mm抗坏血酸钠-缓冲液+100mm羟丙基-β-环糊精(hp-β-cd)-缓冲液+300mm抗坏血酸钠+100mmhp-β-cd。将一体积表达nanoluc的细胞培养物添加到一体积的每种缓冲液中并混合。3分钟后,用标准板读数器测量发光强度。按照相同的工序,通过将一种体积的细胞培养基与每种缓冲液混合来测量背景强度。这些实验结果表明,hp-β-cd是信号增强的主要诱因。如图51a中所示,与单独使用缓冲液的溶液相比,hp-β-cd使信号增强15%至20%。不存在报道酶时的背景信号(图51b)表明信号的增加不是由于背景信号的增加。实施例33混合聚合物底物制剂对底物稳定性的影响在含有200mmhp-β-cd、600mm抗坏血酸钠和10%w/v普鲁兰多糖的mes,ph6.0溶液中冻干底物的制剂(1:50稀释)。冷冻干燥后,将小瓶用手盖上盖子(不抽真空)。将一些小瓶储存在37℃的孵育箱中,而其他小瓶则在室温下留在实验室的工作台上。在每次测量之前,将小瓶以其原始体积的两倍再水合,使得每种组分的最终浓度为100mmhp-β-cd、300mm抗坏血酸钠和5%普鲁兰多糖。根据制造商的指导说明使用的底物(在实验的过程期间在-20℃下储存,并在每个时间点重构)用作阳性对照。在每种情况下,将一体积的重构的荧光素酶测定底物与一体积的样品混合。3分钟后,用bio-teksynergyh196孔板读数器测量发光强度。将表达nanoluc的细胞培养物用作样品。对于每个样品,将发光强度减去背景并归一化为-20℃对照信号。如图52中所示,冻干制剂中普鲁兰多糖的存在允许底物在室温下和在37℃下储存时在15天的时间内保留其活性。据信普鲁兰多糖的添加提供对氧气和水分的屏障,并且当与先前所述的添加剂组合时,提供稳定的基质,所述基质具有在数周至数月内保留呋瑞吗嗪的活性的潜力。当与惰性气体组合时,这种储存方法显示出有望获得所述底物的特别长时间的稳定性的希望。实施例34f-127配制的jrw-0238将2.5mg的f-127(sigmaaldrich)批量装入5ml的顶弹扣盖型eppendorf管中。将聚合物在水浴中加热至70℃直至熔融,成为澄清溶液。在etoh中制备174mm腔肠素类似物jrw-0238的储备溶液。将5μl的所述储备液添加到熔融的聚合物中,且移液以混合。制备两种单独的条件:条件1-添加底物后,将底物/聚合物溶液在高真空下干燥30分钟。条件2-添加底物后,将底物/聚合物溶液进一步用45μl水稀释,冷冻并冻干过夜。最终的干燥配制的底物的代表性实施例显示在图53中。将来自条件1和条件2两者的样品在水中重构,稀释至100μm,并经由分析型hplc分析化学完整性(图54)。与新鲜制备的底物(在etoh中的100μmjrw-0238,图54a)相比,配制的底物条件均未显示出任何显著的化学降解(图54b和图54c)。峰信息汇总在表3中。表3.来自两种条件的重构样品在环境温度下在黑暗中放置。24小时后,在由条件1制备的样品中观察到少量沉淀。在实验的过程中,由条件2制备的溶液保持澄清。这一系列实验表明,腔肠素类似物的固体制剂可用合成聚合物制备,并改善了在水性介质中的总体动力学溶解性,而无需有机溶剂或稳定剂。然而,所述制备方法可对热力学溶解性具有影响。在环境温度下24小时后,冻干的条件(条件2)仍在溶液中。这与来自条件1的样品形成对比,条件1的样品在水中重构后24小时内开始从溶液中沉淀出来。实施例35用f-127配制的呋瑞吗嗪对于腔肠素类似物呋瑞吗嗪,也制备了所述制剂。将2.5mg的f-127(sigmaaldrich)批量装入1.5ml顶弹盖型eppendorf管中。将聚合物在水浴中加热至70℃直至熔融。在etoh中制备10mm呋瑞吗嗪的储备溶液。将5μl的所述储备液添加到熔融的聚合物中,且移液以混合。制备两种单独的条件:条件1–添加底物后,将溶液真空干燥30分钟。条件2–添加底物后,将底物/聚合物溶液进一步用45μl水稀释,冷冻,然后冻干过夜。将条件1和条件2的样品均用水稀释,稀释至100μm,并通过分析型hplc分析底物的完整性(图55)。与新鲜制备的呋瑞吗嗪相比(图55a),条件1显示出相当大的降解(图55b)。这可能是由于重构所述样品所需的大量超声处理所致。相反,来自条件2的重构样品没有显示出明显的降解(图55c)。峰信息汇总在表4中。表4.这一系列实验表明,包括呋瑞吗嗪的腔肠素类似物的固体制剂可用合成聚合物制备,并改善了在水性介质中的总体动力学溶解性,而无需有机溶剂或稳定剂。实施例36配制的jrw-0238在水中的最大浓度将25mg的f-127批量装入1.5ml顶弹扣盖型eppendorf管中。将聚合物在水浴中加热至70℃直至熔融。将3.4mgjrw-0238溶解在50μletoh中,然后添加到热聚合物中并通过移液混合。使用额外的50μletoh洗涤并帮助将底物转移到聚合物溶液中。在减压而不加热的情况下去除溶剂。以类似的方式制备四个小瓶,并且所有小瓶都含有7.3:1w/w的聚合物和底物。如下所述,使用不同体积的水来制备初始的水性储备液:小瓶1:一起注入聚合物和底物后,将溶液溶解在500μl水中。一定的超声处理后,所有物质均溶解。将样品冷冻并冻干过夜。使用5%w/v聚合物的情况下,确定底物的计算浓度为17.4mm。小瓶2:一起注入聚合物和底物后,将溶液溶解在400μl水中。一定的超声处理后,所有物质均溶解。将样品冷冻并冻干过夜。使用6.25%w/v聚合物的情况下,确定底物的计算浓度为21.4mm。小瓶3:一起注入聚合物和底物后,将溶液溶解在250μl水中。一定的超声处理后,所有物质均溶解。将样品冷冻并冻干过夜。使用10%w/v聚合物的情况下,确定底物的计算浓度为34.4mm。小瓶4:一起注入聚合物和底物后,将溶液溶解在100μl水中。一定的超声处理后,所有物质均溶解。将样品冷冻并冻干过夜。使用25%w/v聚合物的情况下,确定底物的计算浓度为85.4mm。冻干后,分别用500μl、400μl、250μl或100μl水重构每个样品。每种条件中的所有物质都已溶解。这些溶液的代表性图像显示在图56中。在环境温度下24小时后,将重构的储备液离心,并且没有观察到沉淀。显示在溶液中静置24小时后重构的底物的化学完整性的代表性hplc迹线显示在图57中。没有观察到显著的化学降解。峰信息汇总在表5中。表5.这些实验指明,通过用固态聚合物配制,可以在水中获得高浓度的腔肠素类似物jrw-0238,而在环境条件下不会对化学完整性造成任何损失。实施例37较低的聚合物/底物比,而不损失可观察的底物溶解性将23.8mg、20.4mg、17mg、13.6mg、10.2mg和6.8mg的f-127批量装入单个1.5ml顶弹扣盖型eppendorf管中。将聚合物在水浴中加热至70℃直至熔融。将23.7mgjrw-0238溶解在350μletoh中,且将50μl的所述储备液添加到每个含有热聚合物的小瓶中;通过移液充分混合。然后将小瓶置于高真空下30分钟以去除所有有机溶剂。每个小瓶用500μl水稀释至jrw-0238的最终浓度为17.4mm,分别具有7x、6x、5x、4x、3x或2xw/w聚合物/底物。将每个管冷冻并冻干过夜。在测试时,将500μl水添加到每个小瓶中并涡旋直至所有物质溶解。初始重构后,除了相对于底物含有2xw/w聚合物的样品外,所有样品都是透明的(图58a)。仅观察到所述样品稍微混浊。在室温下在溶液中1小时后,除了相对于底物含有2xw/w聚合物的样品外,观察到重构的底物仍然在溶液中(图58b)。实施例38用于全动物成像的固体制剂为了在小鼠模型中全动物成像,固体配制的jrw-0238的储备样品如下制备:将90mg的f-127批量装入玻璃螺旋盖小瓶中。然后将聚合物在水浴中加热至70℃直至熔融(变成澄清溶液)。将12.5mg的jrw-0238溶解在250μl的etoh中,并添加到热聚合物中,用薄刮刀充分混合。然后减压去除溶剂。将所述浓缩的样品用3.646ml水稀释,以制备8.7mm底物在水中的母液。然后将480μl的所述水性储备液等分到1.5ml螺旋盖小瓶中,冷冻并冻干过夜。所述制剂的代表性图像显示在图59a。在测试时,将480μl的水添加到小瓶中并涡旋约15秒,直到所有材料都溶解(图59b)。经工程改造以表达antares蛋白构建体(参见美国专利第9,908,918号)(nanoluc和可激发青色的橙红色荧光蛋白(cyofp)的融合体)的转基因小鼠受试者(平均年龄:6个月)使用异氟烷麻醉且经由腹膜内注射(i.p.)或皮下注射(s.c.)注射480μl的重构底物溶液。然后在注射后使用ami成像系统每分钟对每只小鼠进行成像。图60a显示来自经i.p.注射重构的jrw-0238的五只动物的平均rlu的迹线。图60b是当测量到最大光输出时每只小鼠的代表性图像。图61a显示来自经s.c.注射重构的jrw-0238的五只动物的平均rlu的迹线。图61b显示当测量到最大光输出时每只小鼠受试者的代表性图像。总之,这些结果指明,体内成像可用腔肠素类似物实现,所述腔肠素类似物作为干燥制剂制备,在使用时在水中重构,且经i.p.或s.c.注射途径注射到活动物受试者中。应当理解,前述详细描述和所附实施例仅是说明性的,并且不应被视为对本公开范围的限制,本公开的范围仅由所附权利要求及其等同物来限定。对所公开的实施方式的各种改变和修改对于本领域的技术人员将是显而易见的。在不脱离本公开的精神和范围的情况下,可以进行这样的改变和修改,包括但不限于与本发明的化学结构、取代基、衍生物、中间体、合成、组合物、制剂或使用方法有关的那些。实施例39大规模制备聚合物呋瑞吗嗪制剂将干燥的呋瑞吗嗪制剂按比例放大到更大的体积,并证明可以在制造条件下制备这些组合物。饼中呋瑞吗嗪的浓度为200um。可将饼重构为10ml的储备液,提供2x呋瑞吗嗪储备液(20um)。然后可将其用样品以1:1稀释,最终浓度为10um。为了制备本体溶液,将50ml的milli-q纯化水添加到1.25g普鲁兰多糖、35.7mgatt和44mg抗坏血酸盐中,并且混合直至所有固体都溶解。最终溶液分别含有2.5%w/v普鲁兰多糖以及5mmatt和5mm抗坏血酸盐。将29.4ml的普鲁兰多糖溶液计量到50ml塑料小瓶中。添加600μl制备为10mmetoh储备液的呋瑞吗嗪并充分混合。在溶液中观察到少量的稀薄的针状沉淀。所述沉淀最有可能是由于普鲁兰多糖聚合物与溶液中的etoh相互作用。这不会影响制备的成功或最终材料的性质。使用10ml琥珀色玻璃小瓶。将1ml的呋瑞吗嗪-普鲁兰储备溶液等分到10ml的琥珀色玻璃小瓶中,并将橡胶塞部分地插入小瓶中。所用的冻干机(virtisgenesis12el冻干机)具有4ft2的搁板表面和总共三个搁板。制冷系统由2个两级压缩机组成。真空/压力控制通过单个真空泵和一个调节控制阀实现,所述调节控制阀将氮气排放到冻干室中,以平衡真空泵的吸力并将压力保持在指定的设定点。搁板可经由液压活塞压缩。将一个含有178x10个小瓶(包含十四种不同制剂的组合)的手动分配产品的小托盘装载到处于+4.7℃的温度的冷冻干燥机中的单个搁板上。然后将产品在-50℃的搁板温度下进行冷冻步骤2小时,然后开始冷凝器步骤。在运行期间,冷凝器温度在-5℃和-87℃之间。接下来抽真空,并在75毫托和200毫托的压力设定点运行。在整个运行中显示在这两个压力设定点上的良好控制。冻干配方/循环的所有步骤均按程序执行。基于产品探针的平均温度,升华持续约7.5小时,并且解吸持续约16.1小时。运行结束时,将小瓶用氮气回填,并用完全插入的塞子在约600托的压力下(约740托为大气压)密封。冻干后,向每个含有20x呋瑞吗嗪的冻干饼的玻璃小瓶中施用氮气,以填充小瓶的顶部空间,用盖完全密封,并将小瓶分别在25℃或60℃下储存。在冻干后的各个时间点,将配制的呋瑞吗嗪用10ml含有0.01%bsa的pbs,ph7.0重构,并手动摇动小瓶,且允许其在室温下平衡5分钟。将50ul配制的呋瑞吗嗪储备溶液添加到50ul在含有0.01%bsa的pbs,ph7中的1ng/ml纯化的酶(nluc)(promega目录号e499)中(最终[nluc]=0.5ng/ml)。对于每个时间点数据收集,使用的对照是从-20℃新鲜取样的活细胞底物(promega目录号n205)的10um最终溶液。在发光仪(探险多模微孔板阅读器–promega目录号gm3000)上使用动态读数收集总发光,在固体白色非结合表面(nbs)板上执行测定并分析。图62a展示在时间点“第0天”的冻干配制的呋瑞吗嗪,其显示小瓶含有在小瓶底部均匀分布的均匀饼,而外观上没有任何明显的缺陷,指明制剂和冻干方案是合适的。图62b展示在如上所述使用配制的呋瑞吗嗪在用缓冲液重构后表示为原始rlu的活性结果。配制的呋瑞吗嗪和对照底物(活细胞底物,promega目录号n205)性能一样。这是开始加速稳定性研究的基线读数。然后将一部分的小瓶或对照底物置于60℃或25℃下。在不同的时间点重构一个新的小瓶,且使用纯化的酶分析其活性。图63显示如监测34天来自在25℃(蓝色闭环)或60℃(红色正方形)下储存的配制样品的原始rlu,来自在25℃(绿色三角形)或60℃(橙色倒三角形)下储存的活细胞底物的原始rlu,以及保持在-20℃(黑色菱形)下的新鲜制备的对照活细胞底物的原始rlu。将在第0天重构的小瓶保持在溶液中,保持在室温下,并且在18天内取样以确定活性(浅蓝色开口环)。数据表明,配制的呋瑞吗嗪在测试的时间内在两种测试温度下保持活性,并且显示相对于溶解在有机溶剂中的呋瑞吗嗪有所改善。添加缓冲液后,所有配制的呋瑞吗嗪在5分钟内重构,这与固体呋瑞吗嗪的行为形成鲜明对比。图62和图63中的结果证明,呋瑞吗嗪组合物可以更大规模和在包括在玻璃小瓶中和在惰性气氛下的更严格质量控制条件下制备。所述组合物可在环境温度或升高的温度下储存延长的时间,并且在中性缓冲液中重构,而无需有机溶剂或特殊的缓冲条件。即使在水性缓冲液中重构后,所述组合物在溶液中和在环境条件下储存长达24-48小时也不会损失任何显著的性能,并且保持一定的活性长达18天。实施例40配制的jrw-1744的制备6-(3-氨基-2-氟苯基)-8-苄基-2-(呋喃-2-基甲基)咪唑并[1,2-α]吡嗪-3(7h)-酮以与实施例34和实施例38中的jrw-0238类似的方式制备jrw-1744的配制的实施例。固体配制的jrw-1744的储备样品制备如下:将77mg的f-127(约7.2xw/w)批量装入玻璃螺旋盖小瓶中。然后将聚合物在水浴中加热至80℃直至熔融(变成透明溶液)。将10.8mg的jrw-1744溶解在少量的etoh中,并添加到热聚合物中,用薄刮刀充分混合。使用额外的etoh(总量多达2ml)以将所有底物完全转移并溶解到聚合物溶液中。然后减压去除溶剂。然后将所述浓缩的样品置于高真空下1小时以去除残留的etoh,产生橙色固体。将所述固体在3.0ml水中稀释并超声处理,制备8.7mmjrw-1744在水中的母液。然后将480μl所述水性储备液的等分试样转移到1.5ml螺旋盖小瓶中,冷冻并冻干过夜。实施例41配制的jrw-1743的制备6-(3-氨基-2-氟苯基)-8-(2-氟苄基)-2-(呋喃-2-基甲基)咪唑并[1,2-α]吡嗪-3(7h)-酮以与实施例34和实施例38中的jrw-0238类似的方式制备jrw-1743的配制的实施例。配制的jrw-1743的储备样品制备如下:将72mg(7.2xw/w)的f-127批量装入并置于玻璃螺旋盖小瓶中。然后将聚合物在80℃的水浴中加热直至其完全熔融(图64a)。将10.0mg的固体jrw-1743溶解在少量etoh中,并在用薄刮刀搅拌的同时将其转移到热聚合物中。使用额外的etoh(总量多达2ml)来帮助将底物转移到聚合物溶液中。然后在减压下去除溶剂,使聚合物/底物混合物浓缩成橙红色凝胶。然后将所述浓缩的样品置于高真空下1小时以去除任何残留的etoh。为了在f-127中制备配制的jrw-1743的母料,向凝胶中添加2.6ml水,且将所得溶液超声处理直至其完全均匀(图64b)。在所述体积下,jrw-1743的最终浓度经计算为8.7mm。然后将480μl的所述水性储备液的等分试样转移到1.5ml螺旋盖小瓶中,冷冻并冻干过夜,产生含有jrw-1743的冻干饼(图64c)。将一个含有配制的jrw-1743的小瓶在480ul水中重构(图64c,中和右)。执行水中底物浓度的吸光度测量,并且指明发现所述溶液中jrw-1743的工作浓度为8.5mm,相比之下,理论浓度为约8.7mm(图65)。序列seqidno:1-天然成熟的刺虾荧光素酶氨基酸序列ftladfvgdwqqtagynqdqvleqgglsslfqalgvsvtpiqkvvlsgenglkadihviipyeglsgfqmgliemifkvvypvddhhfkiilhygtlvidgvtpnmidyfgrpypgiavfdgkqitvtgtlwngnkiyderlinpdgsllfrvtingvtrlseqidno:2-nluc氨基酸序列mvftledfvgdwrqtagynldqvleqggvsslfqnlgvsvtpipiivlsgenglkidihviipyeglsgdqmgqiekififvvypvddhhfkvilhygtlvidgvtpnmidyfgrpyegiavfdgkkitvtgtlwngnkiiderlinpdgsllfrvtingvtgwrlcerilaseqidno:3-lgtrip(3546)mkhhhhhhvftlddfvgdweqtaaynldqvleqggvssllqnlavsvtpimrivrsgenalkidihviipyeglsadqmaqieevfkvvypvddhhfkvilpygtlvidgvtpnklnyfgrpyegiavfdgkkitttgtlwngnkiiderlitpdd。序列表<110>普洛麦格公司m·达特t·史密斯t·柯克兰t·马赫莱特k·伍德<120>用于稳定腔肠素及其类似物和衍生物的组合物和方法<130>prmg-35852.601<150>us62/805,517<151>2019-02-14<150>us62/740,622<151>2018-10-03<160>3<170>patentinversion3.5<210>1<211>169<212>prt<213>深海虾<400>1phethrleualaaspphevalglyasptrpglnglnthralaglytyr151015asnglnaspglnvalleugluglnglyglyleuserserleuphegln202530alaleuglyvalservalthrproileglnlysvalvalleusergly354045gluasnglyleulysalaaspilehisvalileileprotyrglugly505560leuserglypheglnmetglyleuileglumetilephelysvalval65707580tyrprovalaspasphishisphelysileileleuhistyrglythr859095leuvalileaspglyvalthrproasnmetileasptyrpheglyarg100105110protyrproglyilealavalpheaspglylysglnilethrvalthr115120125glythrleutrpasnglyasnlysiletyraspgluargleuileasn130135140proaspglyserleuleupheargvalthrileasnglyvalthrgly145150155160trpargleucysgluasnileleuala165<210>2<211>171<212>prt<213>人工序列(artificialsequence)<220><223>合成的<400>2metvalphethrleugluaspphevalglyasptrpargglnthrala151015glytyrasnleuaspglnvalleugluglnglyglyvalserserleu202530pheglnasnleuglyvalservalthrproileglnargilevalleu354045serglygluasnglyleulysileaspilehisvalileileprotyr505560gluglyleuserglyaspglnmetglyglnileglulysilephelys65707580valvaltyrprovalaspasphishisphelysvalileleuhistyr859095glythrleuvalileaspglyvalthrproasnmetileasptyrphe100105110glyargprotyrgluglyilealavalpheaspglylyslysilethr115120125valthrglythrleutrpasnglyasnlysileileaspgluargleu130135140ileasnproaspglyserleuleupheargvalthrileasnglyval145150155160thrglytrpargleucysgluargileleuala165170<210>3<211>155<212>prt<213>人工序列<220><223>合成的<400>3metlyshishishishishishisvalphethrleuaspasppheval151015glyasptrpgluglnthralaalatyrasnleuaspglnvalleuglu202530glnglyglyvalserserleuleuglnasnleualavalservalthr354045proilemetargilevalargserglygluasnalaleulysileasp505560ilehisvalileileprotyrgluglyleuseralaaspglnmetala65707580glnileglugluvalphelysvalvaltyrprovalaspasphishis859095phelysvalileleuprotyrglythrleuvalileaspglyvalthr100105110proasnlysleuasntyrpheglyargprotyrgluglyilealaval115120125pheaspglylyslysilethrthrthrglythrleutrpasnglyasn130135140lysileileaspgluargleuilethrproasp145150155当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1