一种基于MLPA-NGS技术的DMD和SMA的拷贝数变异检测试剂盒及其用途的制作方法
一种基于mlpa-ngs技术的dmd和sma的拷贝数变异检测试剂盒及其用途
技术领域
[0001]
本发明涉及基因检测领域,具体涉及一种基于mlpa-ngs技术的dmd和sma的拷贝数变异检测试剂盒及其用途。
背景技术:
[0002]
杜氏肌营养不良(duchenne muscular dystrophy,dmd)是一种x连锁的致死性隐性遗传病,为儿童期最常见的遗传性肌肉病,发病率约为1/3500活产男婴。以进行性肌肉变性、无力和肌肉萎缩为特点,临床表现为早期生长发育轻度延迟,学会走路后常见上楼和蹲起费力,多数患儿在5岁时症状明显而得以确诊,未经治疗的情况下肌力逐渐下降,约十几岁后丧失行走能力而依赖轮椅生活,随后呼吸、骨骼、心脏并发症逐渐出现,平均死亡年龄约19岁。此外也可出现非进行性认知功能障碍。dmd是由于编码抗肌萎缩蛋白(dystrophin)的基因(dmd;locus xp21.2)突变的结果,也被称为抗肌萎缩蛋白病。
[0003]
在dmd的变异中,大约2/3来自母亲,不到1/3是新发突变。携带致病基因的男性发病,而女性不出现或出现轻微临床症状。携带致病基因的母亲有50%的几率将突变的dmd基因遗传给下一代。
[0004]
约70%的dmd患者是由于dmd基因中一个或多个外显子的拷贝数变异引起的,其中缺失突变的两个热区为外显子45~54和外显子3~22;重复突变的热区主要为3~11和21~37外显子区域;其余的30%为点突变或微缺失。点突变没有显著的分布热点。
[0005]
对于dmd的基因检测方法主要包括:多重pcr技术,多重连接依赖性探针扩增(mlpa)技术,ngs技术,芯片技术等,目前最为常用的手段为mlpa技术。
[0006]
脊髓性肌萎缩症(spinal muscular atrophy,sma)是一组以脊髓前角细胞(有时也累及脑干运动神经元)变性和缺失为特征的遗传性疾病,临床表现为肌无力和肌萎缩,人群发病率为1/6 000~1/10 000,携带者频率为1/40~1/60,是儿童期常染色体隐性遗传性疾病。sma的致病基因是smn基因,该基因包括8个外显子,同一条染色体上有二个非常相似的拷贝,一般命名为smn1和smn2,二个拷贝之间仅在各自的3’端有5bp不同,其中2bp在外显子7和8上,利用这一碱基差异可区分smn1、smn2及用作sma的分子学诊断。数据显示,sma患者中,约95%为smn1基因第7和第8外显子纯合缺失或第7外显子纯合缺失所致,5%为smn1杂合缺失、点突变或smn1基因转化为smn2基因所致。2013年上海对1 741例无症状孕妇进行sma携带者筛查,检出smn1拷贝数为1的sma携带者45例,上海地区正常人群此致病基因携带率约为1/39。
[0007]
对于sma的基因检测有多种方法,如sanger法测序,短片段多重定量pcr(qmpsf),限制性片段长度多态性(rflp),实时荧光定量pcr(real-timepcr),变性高效液相色谱(dhplc),聚合酶链式限制性片段长度多态性分析(pcr-rflp)等,但目前最为常用的方法是mlpa方法。
技术实现要素:
[0008]
为了克服现有技术的上述缺陷,本发明的目的在于提供一种基于mlpa-ngs技术的dmd和sma的拷贝数变异检测试剂盒及其用途。
[0009]
本发明公开的试剂盒可以同时检测dmd基因的79个外显子和smn基因的8个外显子,并可给出smn1和smn2的外显子7和外显子8的拷贝数,更加方便快捷,为后续的研究能够提供大量和快速的数据。
[0010]
一种基于mlpa-ngs技术的dmd和sma的拷贝数变异检测试剂盒,包括:
[0011]
dmd探针集,所述dmd探针集如seq no.1-160所示;通过所述针对性地对dmd基因79个外显子的80个位点(第一外显子包含两个检测位点)进行检测,从而反映dmd基因各外显子的拷贝数。这对于全面检测dmd的拷贝数变异,防止漏检是极为重要的;
[0012]
smn探针集,所述smn探针集如seq no.161-184所示;
[0013]
以检测smn1的第7、8外显子,smn2的第7、8外显子的相对拷贝数,而且为不区分smn1和smn2的所有8个外显子分别设计了检测探针。如检测发现smn1的第7、8外显子杂合缺失,其它不加区分的外显子的相对拷贝数为3,那么,就可以相互印证地表明smn1的第7、8外显子杂合缺失是真实的,可信的,双证据的;
[0014]
如果检测发现smn1的第7外显子为杂合缺失,而smn2第7外显子为扩增(3
×
),而其它不区分smn1和smn2的外显子的相对拷贝数仍然为4,那么,就可以推断smn1的第7外显子转化为smn2的第7外显子,而不是发生了smn1的真实的缺失和smn2的真实的扩增。
[0015]
引物集,所述引物集如seq no.215-234所示,所述引物集为带有index的、扩增后无需加接头可直接进行高通量测序的引物的集合;
[0016]
所述引物集包括用于扩增连接产物的上游引物集和下游引物集。每条上游引物上带有一个8个碱基的index,同样地,每条下游引物也带有一个8碱基的index。每个样品在扩增时,只需要使用一条上游引物和一条下游引物。当多个带有不同index的产物混合后,根据index序列可区分样品。
[0017]
在本发明的一个优选实施例中,所述试剂盒当中还包括内参探针集或外参探针集,所述内参探针集如seq no.185-210所示;
[0018]
所述内参基因探针集所包含的位点,分别位于第4、5、6、7、9、17、x、y染色体上,染色体位置具有很好的代表性,同时避开了容易变异的第21号染色体,作为内参基因具有很好的稳定性;而x、y染色体检测不但可判断x、y的拷贝数,而且可以进一步地判断受检者性别。内参基因作为判断dmd基因和smn基因相对拷贝数的主要参考依据,在基因组中是稳定的。
[0019]
所述外参探针集如seq no.211-214所示;
[0020]
所述外参探针集所包含的探针,是作为预先添加的模板使用的,其两端已经预置了扩增引物的结合位点。该预加模板浓度极低,在dna解链、探针与模板杂交、探针连接等步骤正常的情况下,不会影响正常连接探针的扩增;在体系中未添加gdna,或杂交失败,或连接失败的情况下,由于仅有这些预加模板可作为扩增的模板,其在最终扩增产物中占比极高。如果扩增产物中不但其它探针无影无踪,而且连外参探针都没有扩增产物,那么可以推测扩增环节存在问题。
[0021]
在本发明的一个优选实施例中,所述dmd探针集、smn探针集、内参基因探针集、外
参探针集混合得dmd-sma探针工作液,所述混合探针所用的溶液为探针溶解液(任选ae溶液或pbs溶液或其他探针溶解液,稀释倍数范围为0-10x),混合后每条探针的浓度为以2fmol/μl为参照上下浮动1000倍以内;
[0022]
所述外参探针集当中的addref1,addref2,addref3,addref4的拷贝数分别为300,80,20,5拷贝/μl。
[0023]
在本发明的一个优选实施例中,所述试剂盒当中还包括对照dna标本、dmd阳性gdna标本、dmd阴性gdna标本、sma阳性gdna标本或sma阴性gdna标本当中的任意一种或多种,其可在对待检测者进行dmd和sma基因检测时作为对照,从而便于根据检测结果对待检测者的类型进行判定。
[0024]
由于dmd和sma变异位点和种类较多,对上述dmd阳性标本的种类、sma阳性标本的种类不作严格限制,只要变异位置明确、检测效果明确、不影响对待测样本的正确分析即可。
[0025]
对上述各对照组gdna标本的浓度不作严格限制,只要其浓度范围不影响sma致病基因的正常检测即可,可以为本领域的常规浓度范围,例如10-200ng/μl。
[0026]
在本发明的一个优选实施例中,所述试剂盒当中还包括用于探针与gdna杂交的杂交缓冲液,用于探针连接的连接缓冲液及连接酶,用于扩增的pcr缓冲液、dntp或taq酶当中的任意一种或多种。
[0027]
在本发明的一个优选实施例中,所述试剂盒当中还包括的增强剂、优化剂或稳定剂当中的任意一种或多种。
[0028]
一种基于mlpa-ngs技术的dmd和sma的拷贝数变异检测试剂盒的应用,所述应用为采用所述试剂盒以待检测者基因组dna为模板进行mlpa-ngs检测。
[0029]
本发明的有益效果在于:
[0030]
本发明公开的试剂盒可以同时检测dmd基因的79个外显子和smn基因的8个外显子,并可给出smn1和smn2的外显子7和外显子8的拷贝数,更加方便快捷,为后续的研究能够提供大量和快速的数据。
附图说明
[0031]
图1为本发明所用的mlpa-ngs技术的流程模式图。
[0032]
图2为具体样本的mlpa-ngs的dmd检测结果与dmd的mlpa结果示意图。
[0033]
图3为具体男性样本的mlpa-ngs的dmd检测结果与dmd的mlpa结果示意图。
[0034]
图4为具体样本的mlpa-ngs的dmd检测结果与dmd的mlpa结果示意图。
[0035]
图5为具体样本的mlpa-ngs的dmd检测结果与dmd的mlpa结果示意图。
[0036]
图6为具体样本的mlpa-ngs的sma检测结果与sma的mlpa结果示意图。
[0037]
图7为具体样本的mlpa-ngs的sma检测结果与sma的mlpa结果示意图。
[0038]
图8为具体样本的mlpa-ngs的sma检测结果与sma的mlpa结果示意图。
具体实施方式
[0039]
如图1所示的mlpa-ngs技术,是一种将mlpa技术与ngs技术融合在一起的技术,兼有mlpa技术对cnv及snv检测的高精度和ngs技术对目的片段检测的高通量,是一种高通量
的mlpa技术。经典的mlpa技术通过探针杂交、连接、多重pcr的方式可同时检测60多个位点,扩增产物因长度不同以毛细管电泳予以区分。
[0040]
而mlpa-ngs技术将长度检测改为序列本身检测,在多重pcr环节为mlpa连接片段引入ngs的通用接头序列,融合产物直接进行高通量测序,通过序列分析每对连接好的探针的reads数判断靶基因的相对拷贝数。
[0041]
由于不需要通过扩增产物的长度区分各个片段,产物可设计成近乎一样长,大大突破mlpa每次只能检测60多个位点的限制,并避免长探针制备的复杂步骤。与一般的ngs技术相同,接头序列中可置入用于区分不同样本的标签序列。
[0042]
因而在确保检测拷贝数精度的同时,实现了检测位点的高通量和检测样本的高通量。
[0043]
本发明的工作原理在于:
[0044]
本发明以mlpa-ngs技术为基础,先将探针与目的片段杂交,加入连接酶使探针连接,使用ngs接头引物对连接片段扩增,然后对扩增产物进行二代测序,继而对测序文件进行reads分析,从而实现对受检样品dmd和sma基因各外显子拷贝数变异的鉴定。
[0045]
本发明的具体实施方式将从1.探针集和引物集;2.实验步骤;3.实验结果等方面进行阐述。测试共用45个样本,选不同类型的典型病例举例,以作说明。
[0046]
1.探针集和引物集
[0047]
为了提高mlpa-ngs检测的准确性,发明人为dmd基因和smn基因的每个外显子设计一对探针,并在各个染色体上选择一些基因设计内参基因,设计与基因组无结合位点的、充当外部模板的外参探针,以及用于探针扩增的通用引物。所有探针中,属于右侧探针的,在引物合成时在其5’端添加磷酸基团,可保证绝大部分右侧探针上都能连有磷酸基团,保证了连接的实现。然后将探针以一定浓度配置成探针混合液,制备成可与目的基因杂交的探针杂交液。
[0048]
发明人制备了多种dmd阳性对照样本,dmd阴性对照样本,sma阳性对照样本,sma阴性对照样本,用于准确地检测目的样本。
[0049]
进一步地,杂交探针可分为4个探针集,分别是:dmd探针集,sma探针集,内参基因探针集,外参探针集。除探针外,还包括用于对探针进行扩增的引物集。每个探针集和引物集中包括的探针及引物的序列或探针在人基因组中的位置罗列如下:
[0050]
1.1dmd探针集(如seq no.1-160所示)
[0051]
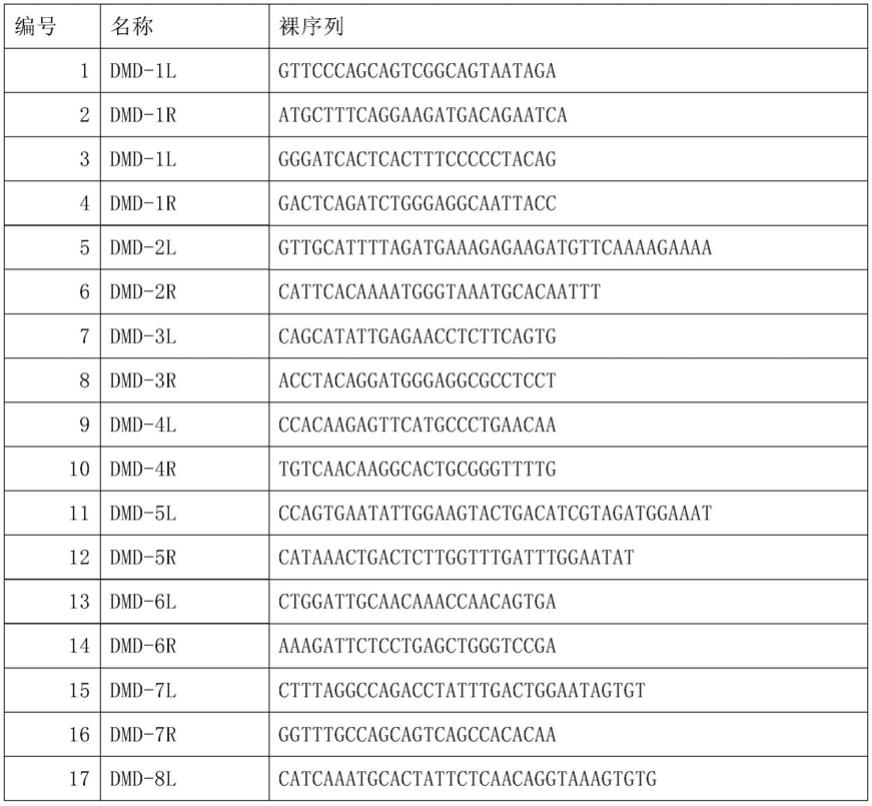
seq no.1-160为dmd检测各外显子所用探针的名称和序列。每行第一列为探针编号,第二列为探针名称,名称中数字为外显子编号,其中外显子1设计了两对探针,l代表左侧探针,r代表右侧探针;每行第三列为探针在染色体上的位置,该列最后带有rc的,表示使用的是染色体上的反向互补序列。染色体参考版本为grch38。凡是l端探针,在其5’端一律带有一段通用序列,其序列自5’端开始,为:cctacacgacgctcttccgatct。凡是r端探针,合成时在其5’端添加磷酸基团,在其3’端带有一段通用序列,其序列自3’端方向开始为:agccccaagggattcccaacctga。
[0052]
1.2sma探针集(如seq no.161-184所示)
[0053]
seq no.161-184为sma检测各外显子所用探针的名称和序列。每行第一列为探针编号,第二列为探针名称,名称中1,2表示该探针既用于smn1,也用于smn2,其后e1等为外显
子编号,第7,8外显子另外设计了可区分smn1和smn2的探针,l代表左侧探针,r代表右侧探针;每行第三列为探针在染色体上的位置,该列最后带有rc的,表示使用的是染色体上的反向互补序列。由于smn1和smn2极为相似,所选择的探针在smn1和smn2上完全相同,因此有两个序列位置。染色体参考版本为grch38。凡是l端探针,在其5’端一律带有一段通用序列,其序列自5’端开始,为:
[0054]
cctacacgacgctcttccgatct。凡是r端探针,合成时在其5’端一律添加一个磷酸基团,在其3’端一律带有一段通用序列,其序列自3’端的方向开始,为:agccccaagggattcccaacctga。
[0055]
1.3内参基因探针集(如seq no.185-210所示)
[0056]
seq no.185-210为分布于各个染色体上的用于内参的探针序列。每行第一列为探针编号,第二列为探针名称,名称中l代表左侧探针,r代表右侧探针;每行第三列为探针在染色体上的位置,该列最后带有rc的,表示使用的是染色体上的反向互补序列。染色体参考版本为grch38。凡是l端探针,在其5’端一律带有一段通用序列,其序列自5’端开始,为:cctacacgacgctcttccgatct。凡是r端探针,在其5’端在合成时一律带有一个磷酸基团,在其3’端一律带有一段通用序列,其序列自3’端开始,为:agccccaagggattcccaacctga。
[0057]
1.4外参探针集(如seq no.211-214所示)
[0058]
以下为4种外参模板序列。每行第一列为序列的编号,第二列为名称,第三列为模板序列的中间部分,模板方向为5
’-3’
,两端各包含一段通用序列,用于通用引物扩增时的结合位点。每条探针5’端带有的通用序列,自5’端开始为:cctacacgacgctcttccgatct。每条探针3’端带有的序列,3’端开始为:agccccaagggattcccaacctga。两端通用引物结合区域与中间部分序列共同构成完整的外参模板。这些序列的非n部分纯粹为识别其本身而设计,无特别含义,设计者具有很大的改动空间。
[0059]
1.5引物集(如seq no.215-234所示)
[0060]
seq no.215-222为以连接的探针为模板,扩增产物可用于ngs双端测序的上游扩增引物,共8条,每个探针上都带有一个8碱基的index。引物序列的方向为5
’-3’
。
[0061]
seq no.223-234为以连接的探针为模板,扩增产物可用于ngs双端测序的下游扩增引物,共12条,每个探针上都带有一个8碱基的index。引物序列的方向为5
’-3’
。8条上游引物和12条下游引物,由于所带index皆不同,其组合可实现在一个lane中同时检测96个样品。在上游引物中,index的序列是可以变动的。
[0062]
具体序列表如下表1所示:
[0063]
表1
[0064]
[0065]
[0066]
[0067]
[0068]
[0069]
[0070]
[0071][0072]
1.6探针集的配置
[0073]
在探针合成时,凡是右侧探针,一律在其5’端引入磷酸基团。将dmd探针集、sma探针集、内参引物探针集使用0.1倍的ae进行等量混合,最后稀释为每条探针2fmol/μl的浓度,且使每微升所含addref1,addref2,addref3,addref4等四种外参探针的拷贝数,其理论值分别是300,80,20,5拷贝/μl。探针集配制后命名为dmd-sma探针工作液。
[0074]
1.7质控样本
[0075]
发明人通过mlpa实验结果,准备了dmd阳性样本,dmd阴性样本、smn阳性样本、smn阴性样本。这些样本将作为对照用于未知样本的检测。
[0076]
质控标准见实验步骤中的说明。
[0077]
本发明的试剂盒的使用方法为:
[0078]
提取待检测者的基因组dna;
[0079]
将待检测者基因组dna进行加热解链,将dmd-sma探针工作液加入,并在60℃的环境中退火16-20小时;
[0080]
在54℃的温度下加入连接缓冲液和连接酶,并闭管保持15-25分钟完成连接,98℃加热5分钟灭活连接酶;
[0081]
取10μl连接产物为模板,按一般的pcr体系,加入相应的上游引物和下游引物进行扩增,使不同的模板带上不同的index;
[0082]
将不同的扩增产物混合,按illumina提供的方法进行ngs测序,获得fastq文件;
[0083]
通过序列分析探针,并统计每个位点对应探针的reads数;
[0084]
进一步分析dmd和sma基因是否有异常及异常情况。
[0085]
本发明可以一次性检测多个标本,只需将不同样本的扩增产物混合,即可在同一个ngs测序仪的lane中进行测序,因此检测速度快,操作简便,检测成本低,从而有利于作为临床患者诊断和携带者筛查,适合大规模筛查应用,可以作于dmd基因和sma基因患者诊断、分子流行病学调查、孕前和产前筛查。
[0086]
具体的实验步骤为:
[0087]
2实验步骤
[0088]
2.1试剂盒的组成
[0089]
试剂盒包括:dmd-sma探针工作液、f501-f508正向扩增引物、r701-r712反向扩增引物、dmd阳性样本,dmd阴性样本、smn阳性样本、smn阴性样本、mlpa缓冲液、连接缓冲液a、连接缓冲液b、连接酶ligase-65、hs taq酶及缓冲液。其中,mlpa缓冲液、连接缓冲液a、连接缓冲液b、连接酶ligase-65购自mrc-holland公司,hs taq酶及缓冲液购自takara公司。
[0090]
储存条件:全部组分保存在-15℃到-25℃或-80℃。
[0091]
为了保证实验效果,试剂盒应在一年之内使用完毕。
[0092]
2.2检测方法
[0093]
2.2.1dna变性
[0094]
取0.2ml pcr反应管,每管加入5μl dna溶液,98℃变性5min,降至室温25℃。
[0095]
2.2.2探针与样本dna的杂交
[0096]
配制3μl混匀的探针混合液:1.5μl mlpa缓冲液+1.5μl dmd-sma探针工作液。将探针混合物加入上述pcr管中,95℃温育1min,60℃杂交过夜。
[0097]
2.2.3杂交探针的连接
[0098]
配制32μl连接酶混合物:25μl dh2o+3μl连接缓冲液a+3μl连接缓冲液b+1μl连接酶ligase-65。pcr仪温度降至54℃,不取出pcr管,打开管盖,加入32μl连接酶混合物,混匀,54℃温育15min,98℃加热5min灭活连接酶,20℃温育。
[0099]
2.2.4连接探针的pcr扩增
[0100]
配制30μl pcr混合液:20.75μl dh2o、4μl hs taq酶buffer、0.25μlhs taq酶、3μl dntp,1μl正向扩增引物、1μl反向扩增引物。取出pcr管,室温下加入10μl前述连接产物,开始pcr反应。反应条件为:95℃30s,60℃30s,72℃60s,35个循环;72℃孵育20min,最后15℃孵育。不同样品使用带有不同index的上下游引物,以便区分不同样本。
[0101]
2.2.5ngs上机测序
[0102]
从每个pcr扩增产物中各取适量样本,混合均匀,使用qubit 2.0对文库浓度进行初步定量,使用agi lent 2100检测文库dna片段的完整性及插入片段大小。样品合格,使用illumina高通量测序仪(如hiseq2500/hiseq4000/hiseqx/miseq)进行双端150bp测序,获得测序的fastq文件。
[0103]
为了保证数据质量,每个样品测序的raw base不少于0.02g,推荐为0.05g以上。
[0104]
2.2.6数据分析
[0105]
对于从高通量测序仪上获得的fastq文件,使用python编写程序,首先统计每对探针连接位点两边各10个碱基组成的序列在所有reads中各出现的次数,此值可视为各探针的扩增reads;其次,将每对dmd和sma探针的reads与部分内参基因的探针reads数的平均值相比,获得dmd-sma各对探针的相对扩增量,最后再以待测样本的各个相对扩增量与健康对照样本的各个相对扩增量比较,获得各个待测样本的各个检测位点的相对拷贝数。分析各个阳性样本、阴性样本,是否通过了质量控制标准,以判断检测的准确性。一般而言,相对拷贝数的检测值应在理论值上下30%的范围内波动。由于发明人使用的是takara hs taq酶,未使用扩增均一性更好的酶,个别样品的个别位点的波动范围可能会增加。设定的质控标准是:
[0106]
dmd阳性样本:男性样本,外显子3-44半合子缺失。设定的检测质量的判断标准是:对于缺失位点(理论拷贝数为0),其相对拷贝数小于0.05,对于未缺失位点(理论拷贝数为1),其相对拷贝数在0.7-1.3之间。
[0107]
dmd阴性样本:男性样本。设定的检测质量的判断标准是:dmd上所有位点的相对拷贝数(理论拷贝数为1)在0.7-1.3之间。
[0108]
sma阳性样本:女性样本,外显子7纯合缺失,外显子8杂合缺失。设定的检测质量的判断标准是:对于纯合缺失的外显子7的位点,其相对拷贝数小于0.05,对于smn1外显子8杂合缺失(理论拷贝数为1),其相对拷贝数在0.7-1.3之间,对于外显子1-8的不区分smn1和smn2的位点(理论拷贝数为4),其相对拷贝数在3.5-5之间,个别探针偏差可适当放宽。
[0109]
sma阴性样本:男性样本。设定的检测质量的判断标准是:对于区分smn1和smn2的外显子7和外显子8位点(理论拷贝数为2),其相对拷贝数在1.4-2.7之间,对于不区分smn1和smn2的外显子1-8(理论拷贝数为4),其相对拷贝数在3.5-5之间,个别探针偏差可适当放宽。
[0110]
2.3mlpa对照试验
[0111]
用于dmd检测的mlpa对照试验,使用的是salsa mlpa probemix p034和p035两个试剂盒;用于sma检测的mlpa对照试验,使用的是salsa mlpa probemix p460 sma试剂盒。方法按mlpa试剂盒提供的说明书执行。
[0112]
2.4实例数目
[0113]
发明人在5个已经做过mlpa检测的sma样本(其中三个为阳性),40个已经做过mlpa的dmd样本(其中24个为阳性)进行了检测。
[0114]
3实验结果
[0115]
发明人使用dmd-sma检测试剂盒对45个样本进行检测,其中40个为已经做过mlpa的dmd样本,5个为已经做过mlpa的sma样本。比较mlpa-ngs结果与mlpa结果,二者完全一致。
下面试举几例进行说明。
[0116]
3.1一例dmd半合型缺失标本的结果
[0117]
样本1,男,mlpa检测显示,外显子3至外显子25半合缺失。mlpa-ngs检测也显示,外显子3至外显子25半合缺失。未缺失位点的相对拷贝数在0.8-1.3以内,符合质控设定。外显子3至外显子25虽有信号,但信号的相对拷贝数低于0.05,符合质控设定。因此,检测质量合格,检验结果与mlpa一致。见图2。
[0118]
图2显示了某个样本的mlpa-ngs的dmd检测结果与dmd的mlpa结果(dnd半合型缺失标本的结果)。其中mlpa-ngs结果的图中,自左至右的位点依次是:外显子1,外显子1,外显子2-外显子79,即外显子1使用了两个位点,其它是一个位点,共80个位点,其余对照基因位点用于计算dmd位点的相对拷贝数,在图中未示。mlpa的图分两部分,分别为检测dmd基因位点的两个mlpa探针集,每个探针集的顺序依探针扩增长度排序。左边探针集的顺序依次是:otc-6,dmd-1,dmd-41,dmd-21,dmd-61,dmd-2,fgd1-11,dmd-42,dmd-22,dmd-62,mid1-14,dmd-3,dmd-43,dmd-23,ppef1-10,dmd-63,dmd-4,dmd-44,dmd-24,dmd-64,col4a5-41,dmd-5,dmd-45,dmd-25,dmd-65,dmd-6,dmd-46,dmd-26,dmd-66,atp7a-1,dmd-7,dmd-47,dmd-27,dmd-67,dmd-8,dmd-48,dmd-28,dmd-68,aifm1-15,dmd-9,dmd-49,dmd-29,dmd-69,f8-19,dmd-10,dmd-50,dmd-30,dmd-70,dcx-4。右边探针集的顺序依次是:phex-9,dmd-11,dmd-51,dmd-31,dmd-71,dmd-12,atp7a-2,dmd-52,dmd-32,dmd-72,dmd-13,dmd-53,dmd-33,mid1-11,dmd-73,dmd-14,dmd-54,dmd-34,dmd-74,arhgef6-4,dmd-15,dmd-55,cdkl5-22,dmd-35,dmd-75,dmd-16,dmd-56,dmd-36,dmd-76,frmd7-1,dmd-17,dmd-57,dmd-37,dmd-77,dmd-18,dmd-58,dmd-38,dmd-78,gjb1-3,dmd-19,dmd-59,dmd-39,dmd-79,dmd-20,dmd-60,dmd-40,dmd-dp427c,dcx-4。mlpa-ngs实验和mlpa实验皆显示,dmd基因3-25号外显子存在半合缺失,两种方法结果一致。
[0119]
3.2一例dnd半合型扩增标本的结果
[0120]
样本2,男,mlpa检测显示,外显子3至外显子7半合扩增。mlpa-ngs检测也显示,外显子3至外显子7半合缺失。未扩增位点的相对拷贝数在0.8-1.3以内,符合质控设定。扩增位点的相对拷贝数在1.7-2.1之间,符合质控设定。因此,检测质量合格,检验结果与mlpa一致。见图3。
[0121]
3.3一例dnd杂合型缺失标本的结果
[0122]
样本3,女,mlpa检测显示,外显子45至外显子47杂合缺失。mlpa-ngs检测也显示,外显子45至外显子47杂合缺失。未缺失位点的相对拷贝数在1.6-2.3以内,符合质控设定。缺失位点的相对拷贝数在0.8-1.1之间,符合质控设定。因此,检测质量合格,检验结果与mlpa一致。见图4。
[0123]
3.4一例dnd未见cnv标本的结果
[0124]
样本4,女,mlpa没有检测到该样本存在外显子拷贝数变异。mlpa-ngs检测也显示,检测正常。所有位点的相对拷贝数在1.5-2.4之间,符合质控设定。因此,检测质量合格,检验结果与mlpa一致。见图5。
[0125]
3.5一例sma异常标本的结果
[0126]
样本5,女,mlpa检测显示,smn1基因外显子7纯合缺失,外显子8杂合缺失,smn2外显子7拷贝数增加(4
×
)。mlpa-ngs检测结果与此相同。不区分smn1和smn2的外显子1-8,相
对拷贝数在3.5-4.5之间,符合质控设定。因此,检测质量合格,检验结果与mlpa一致。见图6。
[0127]
3.6一例sma异常标本的结果
[0128]
样本6,男,mlpa检测显示,smn1基因外显子7,8纯合缺失。mlpa-ngs检测结果与此相同。不区分smn1和smn2的外显子1-8,相对拷贝数在2-3之间。发明人推测,smn1是在两条染色体上缺失的,导致不区分smn1和smn2的外显子1-8从预测值的4个拷贝,跌落到2个拷贝,这个结果与smn1基因外显子7,8纯合缺失的结果一致。因此,检测质量合格。见图7。
[0129]
3.7一例sma未见异常标本的结果
[0130]
样本7,女,mlpa检测显示,smn1基因外显子7,8正常(理论上是2个拷贝)。mlpa-ngs结果显示,不区分smn1和smn2的外显子1-8,相对拷贝数在3.7-4.7之间,与理论值4个拷贝相符。因此,检测质量合格,检验结果符合质控。见图8。
[0131]
45个实例的结果显示,基于mlpa-ngs技术开发的dmd-sma检测试剂盒,检测结果可靠,耗时短,操作方便,价格低廉,适合对此类病人的检测和疑似病例的筛查。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1