使用GATA1基因疗法用于治疗DBA的组合物和方法与流程
使用gata1基因疗法用于治疗dba的组合物和方法
1.相关申请的交叉引用
2.根据35 u.s.c.
§
119(e),本技术要求2019年6月10日提交的美国临时申请号62/859,369的权益,以引用的方式将其内容整体并入本文。
3.政府支持
4.本发明是在由美国国立卫生研究院授予的基金号:r1 dk103794和r33 hl120791的政府支持下完成的。美国政府对本发明享有一定的权利。
5.序列表
6.本技术包含已以ascii格式用电子方式提交的序列表,并在此以引用的方式将其整体并入。所述ascii副本创建于2020年6月3日,名为701039-094470wopt_sl.txt,大小为188,598字节。
技术领域
7.本文描述的技术涉及用于治疗diamond-blackfan贫血的gata-1基因疗法的组合物和方法及其用途。
背景技术:
8.diamond-blackfan贫血(dba)是一组罕见的遗传性骨髓衰竭综合征(ibmfs)之一,其特征在于红细胞衰竭、存在先天异常和癌症易感性。dba通常在儿童生命的第一年被诊断出来。患有dba的儿童无法制造足够的红血细胞,该细胞将氧携带至身体的所有其它细胞。在患有dba的儿童中,许多将会变成红血细胞的细胞在其发育之前死亡。除了为遗传性骨髓衰竭综合征之外,dba还被归类为核糖体病,因为在超过50%的病例中,该综合征似乎是由小亚基或大亚基相关的核糖体蛋白二者之一的单倍不足(haploinsufficiency)引起的。
9.dba的特征在于红血(红系)细胞及其前体的产生特异性减少,而其它造血谱系没有缺陷。在过去十年中,核糖体蛋白基因rps19的突变的阐明和随后9个其它核糖体蛋白基因的突变的发现产生了dba是核糖体生物发生紊乱的假设。然而,尽管在这些病例中对所有核糖体蛋白和其它候选基因进行了系统测序,但有约50%的dba病例具有尚未鉴别的分子突变。
10.gata-1基因位于x染色体并编码调控红细胞发育的转录因子。最近,在diamond-blackfan贫血(dba)患者中发现了gata-1中的功能丧失突变。然而,目前还没有专门针对红系细胞中的gata-1增强的治疗。因此,需要直接针对红系细胞中gata-1功能障碍的治疗方法以提供有效的治疗。
技术实现要素:
11.最近的研究表明,红系细胞中gata-1增强可能对diamond-blackfan贫血(dba)具有治疗作用。然而,在体内增加包括gata-1在内的治疗性蛋白质的谱系特异性表达仍然具有挑战性。尝试用现有技术增加gata1表达必然增加细胞(例如hsc)中gata1的表达,在此情
况下,它对受试者是极大的危害,否定了任何可能的治疗效果。
12.如本文所述,本发明人鉴别出专门在早期红系祖细胞中而不是在造血干细胞中增加gata1的谱系特异性表达的组合物和方法,以作为用于治疗diamond-blackfan贫血的基因治疗方法。dba的特征在于红血(红系)细胞及其前体的产生特异性减少,而其它造血谱系没有缺陷。
13.在任意实施方式的一个方面,本文描述了核酸序列,所述核酸序列包含至少一个异源调控序列以及编码gata结合因子1(gata1)多肽的序列,所述异源调控序列选自于造血增强子元件和用于hsc限制性mirna的mirna结合位点。
14.在任意方面的一些实施方式中,所述核酸序列包含至少一个造血增强子元件。
15.在任意方面的一些实施方式中,所述增强子元件包含与选自于由以下序列所组成的组中的核苷酸序列具有至少80%同源性的序列:seq id no:10、seq id no:11、seq id no:12、seq id no:38和/或seq id no:39。
16.在任意方面的一些实施方式中,所述增强子元件包含选自于由以下所组成的组的基因的增强子元件:kell金属内肽酶(kel);5'氨基乙酰丙酸合酶2(alas2);和血型糖蛋白a(gypa)。
17.在任意方面的一些实施方式中,所述核酸序列包含用于至少一个hsc限制性mirna的至少一个mirna结合位点。
18.在任意方面的一些实施方式中,用于至少一个hsc限制性mirna的至少一个mirna结合位点选自于由以下所组成的组:用于mir10at、mir125、mir155、mir130at、mir142t、mir196bt、mir99、mir126mir126、mir181、mir193、mir223t、mir542和let7e的mir结合位点。
19.在任意方面的一些实施方式中,所述核酸序列包含至少一个造血增强子元件以及用于至少一个hsc限制性mirna的至少一个mirna结合位点。
20.在任意方面的一些实施方式中,包含:a.异源5'utr,所述异源5'utr包含:i.除gata1以外的造血转录因子的5'utr序列,ii.至少20个核苷酸的序列,和/或iii.1-25个上游密码子uaug;和/或b.造血增强子微小基因(minigene)。
21.在任意实施方式的一个方面,本文描述了包含5'utr和编码gata结合因子1(gata1)多肽的序列的核酸序列,所述5'utr包含:i.除gata1以外的造血转录因子的5'utr序列;ii.至少20个核苷酸的序列;和/或iii.1-25个上游密码子uaug。
22.在任意方面的一些实施方式中,所述5'utr包含选自于由以下所组成的组的基因的5'utr:runt相关转录因子1(runx1)、lim domain only 2(lmo2)或ets变体6(etv6)。
23.在任意方面的一些实施方式中,所述核酸序列进一步包含至少一个造血增强子元件、用于hsc限制性mirna的mirna结合位点和/或造血增强子微小基因(g1hem)。
24.在任意实施方式的一个方面,本文描述了包含造血增强子微小基因(g1hem)、编码gata结合因子1(gata1)多肽的序列的核酸序列。
25.在任意方面的一些实施方式中,造血增强子微小基因(mg1hem)包含与核苷酸序列seq id no:13具有至少80%同源性的序列。
26.在任意方面的一些实施方式中,所述核酸序列进一步包含5'utr、和/或至少一个造血增强子元件、和/或用于hsc限制性mirna的至少一个mirna结合位点,所述5'utr包含:i.除gata1以外的造血转录因子的5'utr序列;ii.至少20个核苷酸的序列;和/或iii.1-25
个上游密码子uaug。
27.在任意方面的一些实施方式中,所述核酸序列进一步包含5'utr、至少一个造血增强子元件和/或用于hsc限制性mirna的至少一个mirna结合位点,所述5'utr包含选自于由runt相关转录因子1(runx1)组成的组的基因的5'utr。
28.在任意方面的一些实施方式中,所述核酸序列包含与a和b的元件可操作地连接的启动子。
29.在任意方面的一些实施方式中,所述启动子不为gata1启动子。
30.在任意方面的一些实施方式中,所述启动子包含延伸因子1-α1(eef1a1)的启动子序列。
31.在任意方面的一些实施方式中,编码gata结合因子1(gata1)多肽的序列包含与编码人gata1多肽的核苷酸序列具有至少60%序列同一性的序列。
32.在任意方面的一些实施方式中,所述核酸序列包含:与编码gata1多肽的序列可操作地连接的转录后调控元件。
33.在任意方面的一些实施方式中,所述转录后调控元件包括土拨鼠肝炎病毒转录后调控元件(wpre)。
34.在任意方面的一些实施方式中,所述核酸序列进一步包含内部核糖体进入位点。
35.在任意方面的一些实施方式中,所述内部核糖体进入位点与标志物基因可操作地连接,并且其中,所述标志物基因编码光学可见的蛋白质或酶。
36.在任意方面的一些实施方式中,所述序列包含选自于seq id no 8、seq id no 9和seq id no 62的序列。
37.在任意方面的一些实施方式中,所述核酸序列为载体。
38.在任意方面的一些实施方式中,所述载体为质粒、或腺病毒载体、慢病毒载体或逆转录病毒载体。
39.在任意实施方式的一个方面,本文描述了包含所述核酸序列的慢病毒颗粒。
40.在任意实施方式的一个方面,本文描述了包含核酸序列或颗粒以及药学上可接受的运载体的组合物。
41.在任意实施方式的一个方面,本文描述了治疗有需要的受试者中的diamond-blackfan贫血的方法,所述方法包括向患者给予治疗有效量的核酸序列、颗粒或组合物。
42.在任意实施方式的一个方面,本文描述了恢复早期红系祖细胞细胞特异性gata1表达的方法,所述方法包括使包含早期红系祖细胞的细胞群与核酸序列、颗粒或组合物接触。
43.在任意方面的一些实施方式中,所述早期红系祖细胞包含dba相关的基因突变。
44.在任意实施方式的一个方面,本文描述了本文所述的核酸序列、颗粒或组合物用于治疗有需要的受试者中的diamond-blackfan贫血的用途。
附图说明
45.图1描绘了参与diamond-blackfan贫血(dba)发病机制的分子途径的示意图。
46.图2a、图2b和图2c证明了降低的核糖体水平以及dba分子病变。
47.图3证明了来自具有rp基因突变的dba患者(此处示出的患者中存在rps19、rpl5和
rpl35a突变)的造血干细胞(hspc)中gata1表达水平降低。
48.图4a、图4b和图4c证明了通过gata1慢病毒转导在dba患者hspc中挽救红系谱系定型(commitment)和分化(通过形态学评估,图4b)以及终末分化标志物(图4c;底部)。图4a.示出的三名患者在rps19(患者2和患者3)和rpl35a(患者1)处有突变。
49.图5描绘了允许受调控的gata1表达的要求保护的载体的示意图。内源性gata1基因座示出于上方,以及下方示出了prrl.ppt.efs载体(包括具有安全性修饰的自我灭活型长末端重复元件[ltr]和土拨鼠肝炎病毒转录后调控元件)。所述载体包含内源性gata1启动子或短ef1α(efs)启动子二者之一。gata1 cdna经密码子优化以改善表达。图5按出现顺序分别公开了seq id no 67-seq id no 69。
[0050]
图6描绘了要求保护的gata1载体在原代人造血细胞中使用的示意图。
[0051]
图7描绘了在早期红系祖细胞中而不是在造血干细胞中实现gata1发育忠实型(developmentally faithful)表达的载体的各种组合的示意图。
[0052]
图8a和图8b示出了人gata1的基因组图和两个载体的示意图。图8a证明了人gata1上游的染色质可及性。图8b.两个载体在早期红系祖细胞中而不是在造血干细胞中实现gata1的发育忠实型表达。
[0053]
图9a、图9b、图9c、图9d和图9e描绘了包括对照载体的五种载体,以在早期红系祖细胞中而不是在造血干细胞中实现gata1的发育忠实型表达。图9a.r18 ef-1αires gfp对照。图9b.r21 ef-1αires gfp mir126。图9c.r49 ef-1α1peak增强子gfp。图9d.r50 3peak增强子gfp。图9e.具有增强子和mir126结合位点的gata1载体。
[0054]
图10示出了用r18 ef-1αires gfp对照转染的细胞在体外分化期间,cd71和cd235a的第4天、第9天和第11天的facs分析图。随着细胞从第1象限移动到第4象限,它们在红系谱系中逐渐成熟。
[0055]
图11示出了用r21 ef-1αires gfp转染的细胞的facs分析图。
[0056]
图12示出了用r21 ef-1αires gfp mir126转染的细胞的facs分析图。
[0057]
图13示出了用r49 ef-1α1peak增强子gfp转染的细胞的facs分析图。
[0058]
图14示出了用r49 ef-1α3peak增强子gfp转染的细胞的facs分析图。
[0059]
图15示出了用r18 ef-1αires gfp对照、r21 ef-1αires gfp mir126、r49 ef-1α1peak增强子gfp、r50 3peak增强子gfp转染的细胞的facs分析图。
[0060]
图16证明了人gata增强子的r50 3peak增强子gfp优先驱动红系转基因表达而不是cd34+细胞。
[0061]
图17描绘了使用mir126、mir223t、1peak、3peak、1peak-mir126、1peak-mir223t、3peak-mir126、3peak-mir223t、和ef1a-gfp的hsc d4的facs分析图。实验概述:d0:将cd34+细胞解冻到ssii+cc100+tpo,在5%o2下培养。d2:慢病毒感染,在ssii+cc100+tpo中过夜复苏。hsc d3:分开培养,一半在hsc条件下,一半在rbc分化条件下。hsc d4和d7:通过流式细胞术分析。rbc d4:通过流式细胞术分析(每3-4天继续)。
[0062]
图18a和图18b示出了描绘在第4天(图18a)和第7天(图18b)cd34+cd38-cd45ra-cd90+亚群中的gfp表达的柱状图。
[0063]
图19描绘了使用mir126、mir223t、1peak、3peak、1peak-mir126、1peak-mir223t、3peak-mir126、3peak-mir223t、和ef1a-gfp的rbc d4的facs分析图。
[0064]
图20示出了描绘cd71+cd235+的rbc d4的gfp表达的柱状图。
[0065]
图21描绘了红系亚群cd71-cd235-、cd71+cd235-和cd71+cd235+中gfp的%。
[0066]
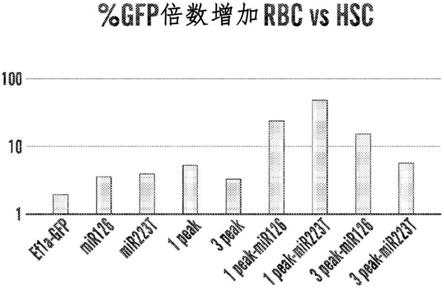
图22示出了描绘rbc相对于hsc的%gfp倍数增加的柱状图。示出了ef1a-gfp、mir126、mir223t、1peak、3peak、1peak-mir126、1peak-mir223t、3peak-mir126和3peak-mir223t的结果。
[0067]
图23示出了rps19敲低损害红系分化的facs分析图。实验概述:d0:将细胞解冻至i期培养基中。d2:用shrna lenti+/-gata1表达构建体进行旋转感染(spinfect)。d4:开始puro选择。d6:移除puro。d7流式分析。
[0068]
图24示出了通过gata1过表达挽救的rps19敲低的facs分析图。
[0069]
图25示出了通过gata1过表达挽救的rps19敲低的facs分析图。
[0070]
图26示出了描绘ef1a-gfp、ef1a-gata-ires-gfp、1peak-gata-gfp、3peak-gata-gfp和hmd-gata-gfp的cd235+/cd235-水平的柱状图。
[0071]
图27示出了描绘gata1基因疗法载体治愈dba的关键特征和实验验证的总结的示意图。
[0072]
图28a、图29b、图28c和图28d示出了gata1发育上受调控表达体外挽救dba表型。图28a.从hspc到网织红细胞按降序排列的人gata1上游的可接近的染色质(顶部)和慢病毒载体实现受调控的gata1表达的示意图(底部)。图28b.在原代人hspc中rps19的shrna敲低损害红系发育,并被gata1表达挽救。图28c.鼠类g1e细胞的红系分化通过受调控的gata1表达而实现。图28d.与hsc相比,红系祖细胞中的gfp比率显示出发育上受调控的表达。
[0073]
图29a、图29b和图29c示出了红系分化期间的外源性gata1的表达。图29a.红系前体的分化首先表达cd71,然后是cd235,最后在终末红系分化过程中丧失cd71。图29b.在感染gata1病毒后,第4天表达cd71(深灰色)或cd71和cd235两者(浅灰色)的红系祖细胞的百分比较高。图29c.与cd71+cd235+细胞相比,cd71-cd235+细胞的gfp表达比率揭示了hg1e在终末红系分化期间的表达降低,模拟了内源性gata1表达。
[0074]
图30a和图30b。rps19编辑后受调控的gata1挽救红系模块。图30a.gata1感染后,也表达cd235的cd71+细胞的比例较高。图30b.受调控的gata1促进红系集落形成。
具体实施方式
[0075]
如本文所述,红系细胞中gata-1增强可在diamond-blackfan贫血(dba)中具有治疗作用。然而,增加红系细胞中gata-1表达的现有方法也必然增加在其它细胞类型中的表达(例如在造血干细胞中)。这些脱靶效应会导致破坏性的副作用,并且必须避免,以便为受试者提供实际治疗。也就是说,在体内增加包括gata-1在内的治疗性蛋白质的谱系特异性表达已被证明具有挑战性,且尚未成功完成。
[0076]
如本文所述,本发明人鉴别出包含可恢复早期红系祖细胞特异性gata1表达的调控序列的核酸序列,从而允许对dba治疗的方法。简而言之,本文所述的方法涉及作为dba的疗法在早期红系祖细胞中而不是在造血干细胞中增加gata1的谱系特异性表达的组合物和方法。更具体而言,本文描述了通过使早期红系祖细胞群与如本文所述的核酸序列、颗粒或组合物接触来恢复早期红系祖细胞细胞特异性gata1表达的方法,所述早期红系祖细胞群包括但不限于包含dba相关基因突变的细胞。
[0077]
dba的特征在于红血(红系)细胞及其前体的产生特异性减少,而其它造血谱系没有缺陷。本文提供了治疗有需要的受试者中diamond-blackfan贫血的方法,该方法包括给予治疗有效量的如本文所述的核酸序列、颗粒或组合物,包括但不限于用于开发广泛适用于dba患者的造血基因治疗方法的具有特定基因调控元件的载体。
[0078]
此外,本文提供了恢复早期红系祖细胞细胞特异性gata1表达的方法,该方法包括使包含早期红系祖细胞的细胞群与如本文所述的核酸序列、颗粒或组合物接触。
[0079]
diamond-blackfan贫血(dba)是通常在婴儿期出现的先天性红系发育不全。dba导致红血细胞计数低(贫血),而不显著影响其它血液成分(血小板和白血细胞)。约47%的受影响个体同时具有多种先天异常,包括颅面畸形、拇指或上肢异常、心脏缺陷、泌尿生殖系统畸形和腭裂。有时观测到低出生体重和普遍的生长延迟。dba患者具有发生白血病和其它恶性肿瘤的适度风险。
[0080]
dba的特征在于红血(红系)细胞及其前体的产生特异性减少,而其它造血谱系没有缺陷。在超过50%的病例中,dba由编码核糖体蛋白的11个基因(包括rpl5、rpl11、rpl35a、rps10、rps17、rps19、rps24和rps26基因)之一中的杂合性功能丧失突变(heterozygous loss-of-function mutations)(单倍不足)引起。这些和其它与diamond-blackfan贫血相关的基因为制造核糖体蛋白提供了指导。大约25%的患diamond-blackfan贫血的个体的rps19基因具有突变。大约另外25%到35%的患有此紊乱的个体在rpl5、rpl11、rpl35a、rps10、rps17、rps24或rps26基因中具有突变。任何这些基因的突变都被认为导致关于核糖体功能的问题。令人惊讶的是,此类泛在表达的核糖体蛋白的突变导致此种特定的人紊乱。研究表明,功能性核糖体短缺可能会增加骨髓中造血细胞的自我毁灭,从而导致贫血。细胞分裂的异常调控或凋亡的不当触发可能会带来影响一些具有diamond-blackfan贫血的人的其它健康问题。已经提出了关于这些疾病的根本的发病机制的许多理论。然而,这些模型无法解释dba和其它核糖体紊乱的精细细胞类型特异性。
[0081]
核糖体蛋白的单倍不足可引起人的其它细胞类型特异性疾病,包括先天性无脾和t细胞淋巴细胞性白血病。令人惊讶的是,此类泛在表达的核糖体蛋白的突变导致此类特定的人紊乱。已经提出了关于这些疾病的根本的发病机制的许多理论。然而,这些模型无法解释dba和其它核糖体疾病的精细细胞类型特异性。
[0082]
在各种实施方式中,本文描述了恢复早期红系祖细胞细胞特异性gata1表达的方法,所述方法包括使包含早期红系祖细胞的细胞群与如本文所述的核酸序列、颗粒或组合物接触。此外,预期本文所述的核酸序列、颗粒或组合物可用于通过向有需要治疗dba的患者给予治疗有效量的如本文所述的核酸序列、颗粒或组合物来治疗dba。
[0083]
如本文所用,“gata-1”、“gata1”或“gata结合蛋白1”是由gata1基因编码的蛋白。由该基因编码的蛋白是gata转录因子家族的蛋白质。该蛋白通过调控胎儿血红蛋白向成人血红蛋白的转换从而在红系发育中发挥重要作用。gata1基因位于x染色体(xp11.23),且编码调控红细胞发育的转录因子。gata-1中的功能丧失突变与造血紊乱有关,包括dba。
[0084]
gata-1多肽具有三个功能结构域:n-末端反式激活结构域(td)(其对转录激活活性必不可少),n-末端锌指(nf),以及c-末端锌指(cf)(其负责与dna结合)。在患有红细胞生成异常性贫血、血小板减少、地中海贫血和红细胞生成性卟啉症的家族中鉴别到了外显子4的突变。还描述了相关的种系突变。dba中gata-1的功能丧失突变发生在gata-1基因外显子
2的供体剪接位点,且导致外显子跳跃。
[0085]
许多种类的gata1序列是已知的,例如人gata1(gata1 ncbi gene id为2623)mrna序列(例如nm_002049.3、xm_011543897.2、xm_011543898.2和xm_024452363.1)和多肽序列(例如np_002040.1、xp_011542199.1、xp_011542200.1、xp_024308131.1)是本领域已知的。这些序列连同任意天然存在的等位基因、剪接变体及其催化相同反应的加工形式一起被考虑用于本文所述的方法和组合物中。
[0086]
在任意方面的一些实施方式中,gata1核酸包括或源自具有以下核酸序列ccds14305.1(seq id no:1)的人gata1。
[0087][0088]
在任意方面的一些实施方式中,gata1 mrna序列包括或源自具有以下序列nm_002049.3(seq id no:2)的人gata1:
[0089][0090]
在任意方面的一些实施方式中,gata1 mrna序列包括或源自具有以下序列xm_011543898.2(seq id no:3)的人gata1:
[0091][0092]
在任意方面的一些实施方式中,gata1 mrna序列包括或源自具有以下序列xm_024452363.1(seq id no:4)的人gata1:
[0093]
[0094][0095]
在任意方面的一些实施方式中,gata1 mrna序列包括或源自具有以下序列xm_011543897.2(seq id no:5)的人gata1:
[0096][0097]
在任意方面的一些实施方式中,gata1多肽包括或源自具有以下氨基酸序列np_002040.1(seq id no:6)的人gata1:
[0098][0099]
在任意方面的一些实施方式中,gata1多肽包括或源自具有以下氨基酸序列xp_011542199.1(seq id no:7)的人gata1:
[0100][0101]
在任意方面的一些实施方式中,gata1多肽包括或源自具有以下氨基酸序列xp_011542200.1(seq id no:64)的人gata1:
[0102][0103]
在任意方面的一些实施方式中,gata1多肽包括或源自具有以下氨基酸序列xp_024308131.1(seq id no:65)的人gata1:
[0104][0105]
在任意方面的一些实施方式中,编码gata结合因子1(gata1)多肽的序列包含与编码人gata1多肽的核苷酸序列具有至少60%序列同一性。在任意方面的一些实施方式中,编码gata结合因子1(gata1)多肽的序列包含编码人gata1多肽的核苷酸序列。
[0106]
在任意方面的一些实施方式中,编码gata1多肽的序列包含以下序列、由以下序列组成或基本上由以下序列组成:选自于seq id no:1-seq id no:5中的任一种的核酸序列。在任意方面的一些实施方式中,编码gata1多肽的序列包含以下序列、由以下序列组成或基本上由以下序列组成:与seq id no.1-seq id no.5中的一个具有至少60%、至少80%、至少85%、至少90%、至少95%、至少98%或更高的序列同一性的核酸序列。在任意方面的一些实施方式中,编码gata1多肽的序列包含以下序列、由以下序列组成或基本上由以下序列组成:与seq id no.1-seq id no.5中的一个具有至少60%、至少80%、至少85%、至少90%、至少95%、至少98%或更高的序列同一性的核酸序列,所述序列编码保留gata1野生型活性的多肽,例如,其具有如本文所述的转录因子活性。
[0107]
在任意方面的一些实施方式中,gata1多肽包含以下序列、由以下序列组成或基本上由以下序列组成:选自于seq id no.6、seq id no.7、seq id no.64和/或seq id no.65中的任一种的氨基酸序列。在任意方面的一些实施方式中,gata1多肽包含以下序列、由以下序列组成或基本上由以下序列组成:与seq id no.6、seq id no.7、seq id no.64和/或seq id no.65中的一个具有至少60%、至少80%、至少85%、至少90%、至少95%、至少98%或更高的序列同一性的氨基酸序列。在任意方面的一些实施方式中,gata1多肽包含以下序列、由以下序列组成或基本上由以下序列组成:与seq id no.6、seq id no.7、seq id no.64和/或seq id no.65中的一个具有至少60%、至少80%、至少85%、至少90%、至少
95%、至少98%或更高的序列同一性的氨基酸序列,所述序列保留gata1野生型活性,例如,其具有如本文所述的转录因子活性。
[0108]
造血干细胞(hsc)是产生其它血细胞的干细胞。此过程称为造血作用。此过程发生在位于大多数骨骼中央的红骨髓中。在胚胎发育中,红骨髓源自称为中胚层的胚胎层。造血作用是产生所有成熟血细胞的过程。它必须在巨大的生产需求与精确调控循环中每种血细胞类型数量的需求之间取得平衡。在脊椎动物中,绝大多数造血作用发生在骨髓中,并且源自多能且能够进行广泛自我更新的数量有限的hsc。hsc发现于成体的骨髓中,尤其是在骨盆、股骨和胸骨中。它们也发现于脐带血中,且少量发现于外周血中。哺乳动物造血作用产生大约10种不同的细胞类型,其中最丰富的属于红系谱系。红细胞生成引起大量红血细胞的产生,红血细胞负责为发育中的胚胎、胎儿和成体组织提供氧。它们还有助于维持血液粘度并提供血管发育和重塑所需的剪切应力。
[0109]
如本文所用,术语“造血干细胞”或“hsc”是指能够最终分化成造血系统的所有细胞类型的克隆源性的(clonogenic)、自我更新的多能细胞,包括b细胞、t细胞、nk细胞、淋巴样树突细胞、髓样树突细胞、粒细胞、巨噬细胞、巨核细胞和红系细胞。与造血系统的其它细胞一样,hsc可通过特征性细胞标志物的组的存在来界定。在任意方面的一些实施方式中,hsc可为表达cd34、cd90或其组合的细胞。用于识别hsc的其它标志物特征包括但不限于:emcn
+
、cd34
+
、cd59
+
、cd90
+
、cd117
+
、cd133
+
、cd38-、lin-、cd150
+
、cd48-和cd244-。
[0110]
来自dba患者的hsc中gata1蛋白水平受到遏制,并且在那些细胞中特异性地增加gata1表达可改善dba的红系谱系定型缺陷特征。需要调控终末红细胞生成过程中gata1的表达。
[0111]
在任意实施方式的一个方面,本文描述了包含a)至少一个异源调控序列以及b)编码gata结合因子1(gata1)多肽的序列的核酸序列,所述异源调控序列选自于i)造血增强子元件和/或ii)用于hsc限制性mirna的结合位点。
[0112]
如本文公开的调控序列包括但不限于启动子、增强子和其它表达控制元件(例如聚腺苷酸化信号),它们控制与它们可操作地连接的基因的转录或翻译。此类调控序列描述于例如goeddel;gene expression technology.methods in enzymology 185,academic press,san diego,calif.(1990)中。用于哺乳动物宿主细胞表达的调控序列的实例包括指导在哺乳动物细胞中高水平蛋白质表达的病毒元件,例如源自巨细胞病毒(cmv)、猿猴病毒40(sv40)、腺病毒(例如腺病毒主要晚期启动子(admlp))和多瘤病毒的启动子和/或增强子。或者,可使用非病毒调控序列,例如泛素启动子、延伸因子1-α1(eef1a1)启动子或β-珠蛋白启动子。真核启动子是位于基因上游的dna调控区域,其结合转录因子ii d(tfiid)并且允许转录起始复合物组分的后续协调,从而促进rna聚合酶ii的募集以及转录的起始。
[0113]
在任意方面的一些实施方式中,本文公开了允许造血祖细胞中gata1精细受调控的表达以改善dba中的红细胞生成而不对造血作用产生不利影响的异源调控序列或其组合。
[0114]
如本文所用,“hsc限制性的”,例如当用于调控序列时,是与造血谱系的其它细胞(例如红细胞或红系前体)相比优先发生于或存在于hsc中的活性或元件。在任意方面的一些实施方式中,活性或元件以相比造血谱系的其它细胞(例如红细胞或红系前体)而言至少10x、至少100x或更高的水平发生或存在于hsc中。更具体而言,hsc限制性mirna是在hsc中
以比在造血谱系的其它细胞(例如红细胞或红系前体)中更高(例如,10x、100x或更高)水平表达的mirna。
[0115]
术语“异源”是指非天然存在的元件的组合。例如,异源调控序列是与所考虑的编码序列可操作地连接的非天然发现的调控序列。在任意方面的一些实施方式中,异源调控序列可为在该物种中非天然发现的调控序列。
[0116]
如本文所用,“调控序列”是指能够增加或降低特定基因、核酸序列或多肽的表达的核酸序列。
[0117]
在任意方面的一些实施方式中,异源调控序列是造血增强子元件。造血增强子元件是在造血细胞中(例如在hsc中和/或红系谱系的其它细胞中)有活性的增强子元件。在一些实施方式中,造血增强子元件在经历红细胞生成的细胞中是有活性的。造血增强子元件不一定在前述细胞的任一种中都具有排他性活性(exclusively active)。或者,在任意方面的一些实施方式中,造血增强子元件可为hsc限制性的和/或限制于红系前体/祖细胞。在一些实施方式中,增强子元件位于编码gata1的序列的远端(例如其为远端增强子元件)。本领域技术人员可通过查阅(例如在万维网上免费获得的关于红系谱系中的一种或多种细胞类型的表达数据)并鉴别在那些细胞中表达或高度表达的基因来容易地鉴别合适的增强子元件。
[0118]
在任意方面的一些实施方式中,所述异源增强子元件包含以下核酸序列:nc_000023.11:48638900-48639300,位于智人x染色体,grch38.p12初级组装(seq id no:10):
[0119][0120]
在任意方面的一些实施方式中,所述异源增强子元件包含以下核酸序列:nc_000023.11:48641200-48641700,位于智人x染色体,grch38.p12初级组装(seq id no:11):
[0121][0122]
在任意方面的一些实施方式中,所述异源增强子元件包含以下核酸序列:
[0123]
nc_000023.11:48644250-48645100,位于智人x染色体,grch38.p12初级组装(seq id no:12):
[0124][0125][0126]
在任意方面的一些实施方式中,所述异源增强子元件包含以下核酸序列(seq id no:38):
[0127][0128]
在任意方面的一些实施方式中,所述异源增强子元件包含以下核酸序列(seq id no:39):
[0129][0130]
在任意方面的一些实施方式中,所述造血增强子元件包含以下序列、由以下序列组成或基本上由以下序列组成:与选自于由seq id no:10、seq id no:11、seq id no:12、seq id no:38和/或seq id no:39所组成的组中的核苷酸序列具有至少80%同源性的序
列。在任意方面的一些实施方式中,造血增强子元件包含以下序列、由以下序列组成或基本上由以下序列组成:至少与seq id no:10、seq id no:11、seq id no:12、seq id no:38和/或seq id no:39中的一个具有至少60%、至少80%、至少85%、至少90%、至少95%、至少98%或更高的序列同一性的序列。在任意方面的一些实施方式中,本文所述的核酸序列包含至少1个、或至少2个、或至少3个、或至少4个、或至少5个、或至少6个、或至少7个、或至少10个、或至少11个、或至少12个、或至少13个、或至少14个、或至少15个、或至少16个、或至少17个、或至少20个、或至少25个、或至少30个造血增强子元件。在使用三个前述造血增强子元件的亚群中,造血增强子元件的任意组合可用于本文所述方面的各个实施方式中的每一个。例如,本文特别考虑可使用3个造血增强子元件的任意成对组合(例如表1中所示的任意组合)。
[0131]
表1:增强子元件的预期示例性组合由“x”表示
[0132][0133]
在任意方面的一些实施方式中,所述造血增强子元件可为选自于由以下所组成的组的基因的增强子元件:kell金属内肽酶(kel)、5'-氨基乙酰丙酸合酶2(alas2)、血型糖蛋白a(gypa)。
[0134]
如本文所用,“kel”、“ece3”、“cd238”或“kell金属内肽酶”是ii型跨膜糖蛋白,所述ii型跨膜糖蛋白是高度多态性的kell血型抗原。许多种类的kel序列是已知的,例如人kel(kel ncbi gene id为3792)、核酸序列(例如ng_007492.2)、mrna序列(例如nm_000420.3)和多肽序列(例如,np_000411.1)是本领域已知的。这些连同任何天然存在的等位基因、剪接变体及其催化相同反应的加工形式一起被考虑用于本文所述的方法和组合物中。
[0135]
在任意方面的一些实施方式中,kel增强子元件包括或源自具有以下核酸序列ng_007492.2(seq id no:40)的人kel序列:
[0136]
ng_007492.2:5001-26303智人kell金属内肽酶(kell血型)(kel),refseqgene位于7号染色体
[0137]
[0138]
[0139]
[0140]
[0141]
[0142]
[0143]
[0144][0145]
如本文所用,“alas2”、“asb”、“anh1”或“5'-氨基乙酰丙酸合酶2”是红系特异性线粒体定位酶。许多种类的alas2序列是已知的,例如人alas2(alas2 ncbi gene id为212)、核酸序列(例如ng_008983.1)、mrna序列(例如nm_001037967.3)和多肽序列(例如np_001033056.1)是本领域已知的。这些连同任何天然存在的等位基因、剪接变体及其催化相同反应的加工形式一起被考虑用于本文所述的方法和组合物中。
[0146]
在任意方面的一些实施方式中,alas2增强子元件包括或源自具有以下核酸序列ng_008983.1(seq id no:41)的人alas2序列:
[0147]
ng_008983.1:5088-27010智人5'-氨基乙酰丙酸合酶2(alas2),refseqgene(lrg_1163)位于x染色体
[0148]
[0149]
[0150]
[0151]
[0152]
[0153]
[0154]
[0155][0156]
如本文所用,“gypa”、“gpa”、“mn”或“血型糖蛋白a”是人红细胞膜的唾液酸糖蛋白,其带有mn和ss血型的抗原决定簇。许多种类的序列是已知的,例如人gypa(gypa ncbi gene id为2993)、核酸序列(例如ng_007470.3)、mrna序列(例如nm_001308190.1)和多肽序列(例如np_001295119.1)是本领域已知的。这些连同任何天然存在的等位基因、剪接变体及其催化相同反应的加工形式一起被考虑用于本文所述的方法和组合物中。
[0157]
在任意方面的一些实施方式中,gypa增强子元件包括或源自具有以下核酸序列ng_007470.3(seq id no:42)的人gypa序列:
[0158]
ng_007470.3:5001-36438智人血型糖蛋白a(mns血型)(gypa),refseqgene位于4号染色体
[0159]
[0160]
[0161]
[0162]
[0163]
[0164]
[0165]
[0166]
[0167]
[0168]
[0169][0170]
本文所述的核酸中使用的增强子元件可为增强子元件序列的单个实体,或者一个或多个单独的独特增强子元件序列的串联或重复。串联和重复可包含单个序列的2个、3个、4个、5个或更多个实体,或2个、3个、4个、5个或更多个可区分增强子元件序列的集合(例如来自一个基因的不同元件或来自不同基因的不同元件)。
[0171]
在任意方面的一些实施方式中,所述造血增强子元件位于距gata-1基因的开放阅读框的边界至少约5kb,例如距gata-1基因的开放阅读框的边界至少约5kb、至少约6kb、至少约7kb、至少约8kb、至少约9kb、至少约10kb或更远。在任意方面的一些实施方式中,所述造血增强子元件序列位于距gata-1基因的开放阅读框的边界至少5kb,例如距gata-1基因的开放阅读框的边界至少5kb、至少6kb、至少7kb、至少8kb、至少9kb、至少10kb或更远。在任意方面的一些实施方式中,所述造血增强子元件序列位于距gata-1基因的开放阅读框的边界约5kb,例如距gata-1基因的开放阅读框的边界约5kb、约6kb、约7kb、约8kb、约9kb或约10kb。在任意方面的一些实施方式中,所述造血增强子元件序列可在基因间(intergenic)序列中或在间插基因(intervening gene)的序列中。在本文所述的任意方面的一些实施方式中,可在距开放阅读框末端约500bp至约10kb(例如距开放阅读框约1kb至约9kb、约2kb至约8kb、约3kb至约7kb、或约4kb至约6kb)的序列内鉴别靶序列。在本文所述的任意方面的一些实施方式中,所述造血增强子元件序列可位于距开放阅读框末端500bp至10kb(例如距开放阅读框1kb至9kb、2kb至8kb、3kb至7kb、或4kb至6kb)的序列内。
[0172]
在任意方面的一些实施方式中,所述异源调控序列是gata1造血增强子微小基因(g1hem)。g1hem可允许gata1特异性在早期红系祖细胞中谱系特异性的表达但不在造血干细胞中表达,例如作为治疗diamond-blackfan贫血的基因治疗方法。gata1造血增强子微小基因(g1hem)包含4个不同调控元件的连结,以实现gata1特异性在早期红系祖细胞中谱系特异性表达。如本文公开的g1hem元件包括-3kb造血增强子、上游双gata基序、上游caccc盒以及gata1的第一内含子的区段。事实上,此微小基因中存在的979个核苷酸足以适当地驱动gata1 cdna挽救gata1敲除小鼠并允许表面上正常的红细胞生成。
[0173]
在任意方面的一些实施方式中,gata1造血增强子微小基因(g1hem)包含以下核酸序列(seq id no:13):
[0174][0175]
在任意方面的一些实施方式中,本文描述了gata1造血增强子微小基因(g1hem),所述gata1造血增强子微小基因(g1hem)包含与seq id no:13具有至少80%同源性的序列、由与seq id no:13具有至少80%同源性的序列组成或基本上由与seq id no:13具有至少80%同源性的序列组成。在任意方面的一些实施方式中,gata1造血增强子微小基因(g1hem)包含以下序列、由以下序列组成或基本上由以下序列组成:与seq id no:13具有至少60%、至少80%、至少85%、至少90%、至少95%、至少98%或更高序列同一性的序列。
[0176]
在任意方面的一些实施方式中,所述核酸序列包含至少1个、或至少2个、或至少3个、或至少4个、或至少5个、或至少6个、或至少7个、或至少10个、或至少11个、或至少12个、或至少13个、或至少14个、或至少15个、或至少16个、或至少17个、或至少20个、或至少25个、或至少30个gata1造血增强子微小基因(g1hem)。
[0177]
在任意方面的一些实施方式中,gata1造血增强子微小基因位于距gata-1基因的开放阅读框的边界至少约5kb,例如距gata-1基因的开放阅读框的边界至少约5kb、至少约6kb、至少约7kb、至少约8kb、至少约9kb、至少约10kb或更远。在任意方面的一些实施方式中,gata1造血增强子微小基因序列位于距gata-1基因的开放阅读框的边界至少5kb,例如距gata-1基因的开放阅读框的边界至少5kb、至少6kb、至少7kb、至少8kb、至少9kb、至少10kb或更远。在任意方面的一些实施方式中,gata1造血增强子微小基因位于距gata-1基因的开放阅读框的边界约5kb,例如距gata-1基因的开放阅读框的边界约5kb、约6kb、约7kb、约8kb、约9kb或约10kb。在任意方面的一些实施方式中,gata1造血增强子微小基因序列可在基因间序列中或在间插基因的序列中。在本文描述的任意方面的一些实施方式中,gata1造血增强子微小基因序列可位于距所述开放阅读框的末端约500bp至约10kb(例如距所述开放阅读框约1kb至约9kb、约2kb至约8kb、约3kb至约7kb、或约4kb至约6kb)。在本文所述的任意方面的一些实施方式中,gata1造血增强子微小基因序列位于距开放阅读框的末端500bp至10kb(例如距开放阅读框1kb至9kb、2kb至8kb、3kb至7kb、或4kb至6kb)。
[0178]
在任意方面的一些实施方式中,本文公开了hsc限制性mirna的结合位点,所述结合位点允许gata1在造血祖细胞中的调控表达以改善dba中的红细胞生成而不会对造血作用有不利影响。
[0179]
hsc限制性mirna的非限制性实例包括mir10at、mir125、mir155、mir130at、
mir142t、mir196bt、mir99、mir126、mir181、mir193、mir223t、mir542和let7e。这些mirna的序列的许多种类是本领域已知的,例如人mir10at、mir125、mir155、mir130at、mir142t、mir196bt、mir99、mir126mir126、mir181、mir193、mir223t、mir542和let7e。
[0180]
这些mirna中的各自的结合位点在本领域中同样是已知的并且包括在mirbase、mirdb和/或targetscan上容易获得的那些。简而言之,动物mirna结合位点将与mirna序列的至少“种子区域”(6-8nt长度)互补。本文所述的mirna各自的种子区域是公开可得的,例如在targetscan和本文表2中提供的seq id no:43-seq id no:55。
[0181]
在任意方面的一些实施方式中,本文描述的给定mirna的结合位点可为如下序列:所述序列包含与该mirna的种子区域互补的序列、由与该mirna的种子区域互补的序列组成、或基本上由与该mirna的种子区域互补的序列组成。在任意方面的一些实施方式中,本文所述的核酸序列可包含与单个hsc限制性mirna的种子区域互补的序列的2个、3个、4个或更多个重复。这样的序列可包括个体序列的重复和/或不同序列的串联组合。
[0182]
在任意方面的一些实施方式中,本文所述的两个或更多个mirna的结合位点可为如下序列:所述序列包含与那些mirna的种子区域互补的序列、由与那些mirna的种子区域互补的序列组成、或基本上由与那些mirna的种子区域互补的序列组成。在任意方面的一些实施方式中,本文所述的两个或更多个mirna的结合位点可为如下序列:所述序列包含具有与那些mirna的种子区域互补的序列的2个、3个、4个或更多个重复的序列,由具有与那些mirna的种子区域互补的序列的2个、3个、4个或更多个重复的序列组成,或基本上由具有与那些mirna的种子区域互补的序列的2个、3个、4个或更多个重复的序列组成。这样的序列可包括个体序列的重复和/或不同序列的串联组合。
[0183]
在任意方面的一些实施方式中,本文所述的一个或多个mirna的结合位点可为如下序列:所述序列包含选自于seq id no:31-seq id no:37的一个或多个序列、由选自于seq id no:31-seq id no:37的一个或多个序列组成、或基本上由选自于seq id no:31-seq id no:37的一个或多个序列组成。在任意方面的一些实施方式中,本文所述的一个或多个mirna的结合位点可为如下序列:所述序列包含具有2个、3个、4个或更多个选自seq id no:31-seq id no:37的序列的序列,由具有2个、3个、4个或更多个选自seq id no:31-seq id no:37的序列的序列组成、或基本上由具有2个、3个、4个或更多个选自seq id no:31-seq id no:37的序列的序列组成。这样的序列可包括个体序列的重复和/或不同序列的串联组合。在任意方面的一些实施方式中,本文所述的核酸序列可包含以下序列:所述序列包含选自于seq id no:31-seq id no:37的序列的4个重复、由选自于seq id no:31-seq id no:37的序列的4个重复组成、或基本上由选自于seq id no:31-seq id no:37的序列的4个重复组成。
[0184]
表2:hsc限制性mirna的名称、mirbase登录号、核苷酸序列、示例性种子区域和mirna结合位点的示例性核苷酸序列的非限制性实例。
[0185]
[0186][0187]
在任意实施方式的一个方面中,本文描述了包含用于至少一个hsc限制性mirna的至少一个mirna结合位点的核酸序列,所述用于至少一个hsc限制性mirna的至少一个mirna结合位点选自于由以下mir结合位点所组成的组:用于mir10at、mir125、mir155、mir130at、mir142t、mir196bt、mir99、mir126、mir181、mir193、mir223t、mir542和let7e的mir结合位点。在任意实施方式的一个方面中,本文描述了包含至少一个、或至少两个、或至少三个、或至少四个、或至少五个、或至少六个、或至少七个、或至少八个、或至少十个、或至少十一个、或至少十二个用于至少一个hsc限制性mirna的结合位点的核酸序列,所述结合位点选自于由以下mir结合位点所组成的组:用于mir10at、mir125、mir155、mir130at、mir142t、mir196bt、mir99、mir126、mir181、mir193、mir223t、mir542和let7e的mir结合位点。在使用用于前述mirna的mirna结合位点的亚群里,mirna结合位点的任意组合可用于本文所述方面的各种实施方式中的每一个。例如,本文特别考虑可使用用于12个mirna的结合位点的任意成对组合(例如,表3中示出的任意组合)。
[0188]
在任意实施方式的一个方面中,本文描述了包含至少一个造血增强子元件和用于至少一个hsc限制性mirna的至少一个mirna结合位点的核酸序列。在任意实施方式的一个方面中,本文描述了包含至少一个造血增强子元件和用于至少一个hsc限制性mirna的至少一个结合位点和编码gata1多肽的序列的核酸序列。
[0189]
表3:所考虑的mirna结合位点的示例性组合由“x”表示
[0190]
[0191][0192]
在任意方面的一些实施方式中,mirna结合位点位于距gata-1基因的开放阅读框的边界至少约5kb,例如距gata-1基因的开放阅读框的边界至少约5kb、至少约6kb、至少约7kb、至少约8kb、至少约9kb、至少约10kb或更远。在任意方面的一些实施方式中,mirna结合位点序列位于距gata-1基因的开放阅读框的边界至少5kb,例如距gata-1基因的开放阅读框的边界至少5kb、至少6kb、至少7kb、至少8kb、至少9kb、至少10kb或更远。在任意方面的一些实施方式中,mirna结合位点序列位于距gata-1基因的开放阅读框的边界约5kb,例如距gata-1基因的开放阅读框的边界约5kb、约6kb、约7kb、约8kb、约9kb或约10kb。在任意方面的一些实施方式中,mirna结合位点序列可在基因间序列中或在间插基因的序列中。在本文描述的任何方面的一些实施方式中,靶序列位于距开放阅读框的末端约500bp至约10kb(例如距开放阅读框约1kb至约9kb、约2kb至约8kb、约3kb至约7kb或约4kb至约6kb)的序列内。在本文所述的任意方面的一些实施方式中,mirna结合位点序列位于距开放阅读框的末端500bp至10kb(例如距开放阅读框1kb至9kb、2kb至8kb、3kb至7kb或4kb至6kb)。
[0193]
在任意方面的一些实施方式中,本文公开了包含编码gata1多肽的序列和异源5'utr的核酸序列。此类组合允许gata1特异性地在早期红系祖细胞中谱系特异性表达。
[0194]
基因表达的cap分析用于定义正在进行红系谱系定型(在该阶段中出现红系分化中的功能缺陷)的hspc中用于转录本的5'非翻译区域(utr)。在基系(baseline)时高度翻译并且具有短且非结构的5'utr的转录本倾向于成为在rp单倍不足的背景下翻译水平下调的转录本。5'utr或“5'非翻译区域”或5'前导序列是指未翻译的mrna区域。本文描述了以下发
现:在所有造血主要转录因子中,只有gata1具有短的5'utr,以及用其它转录因子(包括但不限于runx1、lmo2或etv6)的5'utr替换该5'utr改变gata1造血转录因子的翻译。
[0195]
在任意实施方式的一个方面,本文描述了包含以下的核酸序列:i)异源5'utr和ii)编码gata1多肽的核酸序列,所述异源5'utr包含a)除gata1以外的造血转录因子的5'utr序列,b)至少20个核苷酸的序列,和/或c)1-25个上游密码子uaug。在任意方面的一些实施方式中,本文所述的核酸序列可进一步包含异源5'utr,所述异源5'utr包含a)除gata1以外的造血转录因子的5'utr序列,b)至少20个核苷酸的序列,和/或c)1-25个上游密码子uaug。
[0196]
5'utr的长度可通过突变(例如置换、删除或插入)所述5'utr来修饰。所述5'utr可通过突变天然存在的起始密码子或翻译起始位点来进一步修饰,以使得密码子不再作为起始密码子起作用并且翻译可在替代起始位点起始。
[0197]
在任意方面的一些实施方式中,除gata1以外的造血转录因子的5'utr序列可为选自于由以下所组成的组的基因的5'utr:runt相关转录因子1(runxl)、lim domain only 2(lmo2)以及ets变体6(etv6)。
[0198]
如本文所用,“runx1”、“anl1”或“runt相关转录因子1”是指异二聚体核心结合因子(cbf)转录因子的α亚基,该转录因子被认为与正常造血作用的改善有关。runx1本身是转录因子,并且与cbfb辅因子复合形成cbf。关于runx1的序列的许多种类是已知的,例如人runx1(runx1 ncbi gene id为861)mrna序列(例如nm_001001890.2)和多肽序列(例如np_001001890.1)是本领域已知的。这些序列连同任何天然存在的等位基因、剪接变体及其催化相同反应的加工形式一起被考虑用于本文所述的方法和组合物中。
[0199]
在任意方面的一些实施方式中,runx1 5'utr包括如下的5'utr,所述5'utr含有以下核酸序列、由以下核酸序列组成、基本上由以下核酸序列组成或衍生自以下核酸序列:ng_011402.2:940414-1201911智人runx家族转录因子1(runx1),refseqgene(lrg_482),位于21号染色体,(seq id no:14):
[0200][0201]
如本文所用,“lmo2”、“ttg2”或“lim domain only 2”是指卵黄囊红细胞生成所需的富含半胱氨酸的两个lim结构域的蛋白。关于lmo2的序列的许多种类是已知的,例如人lmo2(lmo2 ncbi gene id为4005)mrna序列(例如nm_001142315.1)和多肽序列(例如np_001135787.1)是本领域已知的。这些序列连同任何天然存在的等位基因、剪接变体及其催化相同反应的加工形式一起被考虑用于本文所述的方法和组合物中。
[0202]
在任意方面的一些实施方式中,lmo2 5'utr包括以下的5'utr,所述5'utr含有以下核酸序列、由以下核酸序列组成、基本上由以下核酸序列组成或衍生自以下核酸序列:nc_000011.10:c33892289-33858576智人11号染色体,grch38.p12,(seq id no:15):
[0203][0204]
如本文所用,“etv6”、“tel”或“ets变体6”是指具有两个功能结构域的转录因子:n-末端指向(n-terminal pointed,pnt)结构域,其参与自身和其它蛋白质的蛋白质-蛋白质相互作用;以及c-末端dna结合结构域。关于etv6的序列的许多种类是已知的,例如人etv6(etv6 ncbi gene id为2120)mrna序列(例如nm_001987.4)和多肽序列(例如np_001978.1)是本领域已知的。这些序列连同任何天然存在的等位基因、剪接变体及其催化相同反应的加工形式一起被考虑用于本文所述的方法和组合物中。
[0205]
在任意方面的一些实施方式中,etv6 5'utr包括以下的5'utr,所述5'utr含有以下核酸序列、由以下核酸序列组成、基本上由以下核酸序列组成或衍生自以下核酸序列:ng_011443.1:5001-250549智人ets变体6(etv6),refseqgene(lrg_609),位于12号染色体(seq id no:16):
[0206][0207]
本文所述的核酸序列/元件能够可操作地连接,使得它们可直接或间接相互作用以执行预期的功能(例如介导或调节核酸序列的表达)。“可操作地连接”是指元件的布置,其中如此描述的部件被配置以执行它们的通常功能。因此,与开放阅读框可操作地连接的控制元件能够影响所述开放阅读框的表达。控制元件不需要与开放阅读框相邻,只要它们起到指导其表达的作用。因此,例如间插的未翻译但已转录的序列可存在于启动子序列和开放阅读框之间,所述启动子序列仍可被视为与所述开放阅读框“可操作地连接”。可操作地连接的序列的相互作用能够例如由与可操作地连接的序列相互作用的蛋白质介导。
[0208]
在任意方面的一些实施方式中,启动子能够可操作地连接至本文公开的元件中的任一个,例如包含异源5'utr的核酸序列、至少一个远端造血干细胞(hsc)限制性增强子元件、用于hsc限制性mirna的结合位点和/或编码gata1多肽的核酸。在任意方面的一些实施方式中,所述启动子不为gata1启动子。
[0209]
在任意方面的一些实施方式中,所述启动子包含延伸因子1-α1(eef1a1)的启动子序列。如本文所用,“eef1a1”、“ccs-3”或“leng7”是指延伸因子-1复合物的α亚基,其负责将氨酰基trna酶促递送至核糖体。关于eef1a1的序列的许多种类是已知的,例如人eef1a1(eef1a1ncbi gene id为1915)是本领域已知的。在任意方面的一些实施方式中,eef1a1启动子包括以下的启动子,所述启动子含有以下核酸序列、由以下核酸序列组成、基本上由以下核酸序列组成或衍生自以下核酸序列:nc_000006.12:c73521032-73515750智人6号染色体,grch38.p12初级组装(seq id no:17):
[0210][0211]
[0212][0213]
复杂的细胞和发育过程取决于mrna和蛋白质水平及活性的精确时空调控。此类调控主要发生在转录、转录后和翻译后水平。转录后调控是在rna水平上控制基因表达,因此介于基因的转录和翻译之间。转录后调控可通过蛋白质-rna和rna-rna相互作用二者来控制。如本文所用,转录后调控元件包括核苷酸序列,包括但不限于土拨鼠肝炎病毒转录后调控元件。在任意方面的一些实施方式中,本文所述的核酸序列可进一步包含与编码gata1多肽的序列可操作地连接的转录后调控元件。
[0214]
在任意方面的一些实施方式中,转录后调控元件包括土拨鼠肝炎病毒转录后调控元件。土拨鼠肝炎病毒(whp)转录后调控元件(缩写为wpre)是在转录时产生增强表达的三级结构的dna序列。wpre是具有γ、α和β组分的由三部分组成的调控元件。
[0215]
在任意方面的一些实施方式中,土拨鼠肝炎病毒转录后调控元件(wpre)包含以下核苷酸序列(seq id no:56)、由以下核苷酸序列(seq id no:56)组成或基本上由以下核苷酸序列(seq id no:56)组成:
[0216][0217]
在任意方面的一些实施方式中,土拨鼠肝炎病毒转录后调控元件(wpre)包含以下核苷酸序列(seq id no:63)、由以下核苷酸序列(seq id no:63)组成或基本上由以下核苷酸序列(seq id no:63)组成:
no:66)组成:
[0224][0225]
在任意方面的一些实施方式中,本文描述了包含与seq id no:66的核苷酸序列具有至少80%同源性的序列的ires。在任意方面的一些实施方式中,ires包含与seq id no:66具有至少60%、至少80%、至少85%、至少90%、至少95%、至少98%或更高序列同一性的序列。在任意方面的一些实施方式中,ires包含与seq id no:66具有至少60%、至少80%、至少85%、至少90%、至少95%、至少98%或更高的序列同一性并保留了seq id no:66的野生型活性的序列。
[0226]
本文所述的核酸序列可包含多个ires,例如核酸序列可包含至少1个、或至少2个、或至少3个、或至少4个、或至少5个、或至少6个、或至少7个、或至少10个、或至少11个、或至少12个、或至少13个、或至少14个、或至少15个、或至少16个、或至少17个、或至少20个、或至少25个、或至少30个ires序列。
[0227]
在任意方面的一些实施方式中,ires位于距gata-1基因的开放阅读框的边界至少约5kb,例如距gata-1基因的开放阅读框的边界至少约5kb、至少约6kb、至少约7kb、至少约8kb、至少约9kb、至少约10kb或更远。在任意方面的一些实施方式中,ires序列位于距gata-1基因的开放阅读框的边界至少5kb,例如距gata-1基因的开放阅读框的边界至少5kb、至少6kb、至少7kb、至少8kb、至少9kb、至少10kb或更远。在任意方面的一些实施方式中,ires序列位于距gata-1基因的开放阅读框的边界约5kb,例如距gata-1基因的开放阅读框的边界约5kb、约6kb、约7kb、约8kb、约9kb或约10kb。在任意方面的一些实施方式中,ires序列可在基因间序列中或在间插基因的序列中。在本文所述的任意方面的一些实施方式中,ires序列可位于距开放阅读框的末端约500bp至约10kb(例如距开放阅读框约1kb至约9kb、约2kb至约8kb、约3kb至约7kb或约4kb至约6kb)的序列中。在本文所述的任意方面的一些实施方式中,ires序列可位于距开放阅读框的末端500bp至10kb(例如距开放阅读框1kb至9kb、2kb至8kb、3kb至7kb或4kb至6kb)的序列内。
[0228]
在任意方面的一些实施方式中,本文所述的核酸序列可进一步包含自剪切2a多肽。自剪切的肽或2a肽是能够诱导其作为一部分的多肽(例如本文所述的重组gata-1)的剪切的多肽。因此,2a肽可用于将较长的肽剪切成两个较短的肽,从而可以用单个转录本生成两个肽。2a肽来源于病毒基因组中的2a区域。2a-肽介导的剪切在翻译后开始。所述剪切通过破坏2a肽c末端中脯氨酸(p)和甘氨酸(g)之间的肽键触发。2a多肽可包含至少10个、至少15个、至少20个、至少25个、至少30个或至少40个氨基酸。
[0229]
在任意方面的一些实施方式中,2a肽能够与ires元件组合在单个核酸序列中,从而产生在单个转录本内编码的三个单独的多肽。
[0230]
可用于本文所述方法的示例性2a肽包括但不限于p2a、e2a、f2a和t2a(也参见表4,seq id no:57-seq id no:60)。f2a来源于口蹄疫病毒18;e2a来源于马甲型鼻炎病毒;p2a来源于猪捷申病毒-1 2a;t2a来源于明脉扁刺蛾(thosea asigna)病毒2a。
[0231]
表4:能够用于本文所述的各种实施方式的2a肽的名称和序列。可在所列2a肽的n末端添加任选的接头“gsg”(gly-ser-gly)(粗体)。
[0232][0233]
在任意方面的一些实施方式中,ires和/或自剪切2a多肽能够可操作地连接至标志物基因(例如编码光学可检测蛋白质或酶的标志物基因)。光学可检测蛋白质/酶可包含光学可检测标记和/或具有产生可检测信号的能力(例如通过催化将化合物转化为可检测产物的反应)。可检测标记可包括例如吸光部分或荧光部分。可检测标记、标志物基因、检测它们的方法以及将它们掺入试剂(例如抗体和核酸探针)中的方法是本领域公知的。
[0234]
光学可检测标记/信号可包括人眼可见的标记/信号或用光学装置可检测的标记/信号,例如通过光谱、光化学、生物化学、免疫化学、电磁、放射化学或化学手段(例如荧光、化学荧光或化学发光),或任何其它适当的方式。可检测标记可包括但不限于放射性同位素、生物发光化合物、生色团、抗体、化学发光化合物、荧光化合物、金属螯合物和酶。
[0235]
标志物基因是本领域公知的,例如可包括但不限于:天然荧光蛋白,例如维多利亚多管发光水母(aequorea victoria)的绿色荧光蛋白(gfp)(cubitt,a.b.等.1995.understanding,improving,and using green fluorescent proteins.trends biochem.sci.20:448-455;chalfie,m.和prasher,d.c.u.s.pat.no:5,491,084);编码β-半乳糖苷酶的lacz基因;辣根过氧化物酶;碱性磷酸酶;苹果酸脱氢酶;葡萄球菌核酸酶;δ-v-类固醇异构酶;酵母醇脱氢酶;α-甘油磷酸脱氢酶;磷酸丙糖异构酶;辣根过氧化物酶;碱性磷酸酶;天冬酰胺酶;葡萄糖氧化酶;β-半乳糖苷酶;核糖核酸酶;脲酶;过氧化氢酶;葡萄糖-vi-磷酸脱氢酶;葡萄糖淀粉酶;和乙酰胆碱酯酶。
[0236]
在任意方面的一些实施方式中,本文所述的核酸序列可包含以下序列、由以下序列组成或基本上由以下序列组成:选自于seq id no:8、seq id no:9、seq id no:61和seq id no:62。
[0237]
seq id no:61(也被称为r18 ef1a ires gfp)包含ef1a启动子,与编码gfp的核苷酸序列可操作地连接的ires序列:
[0238]
[0239]
[0240][0241][0242]
seq id no:8(也被称为r21 mir126)包含ef1a启动子,以及与编码gfp和用于hsc限制性mirna mir126的四个mirna结合位点的核苷酸序列可操作地连接的ires序列:
[0243]
[0244]
[0245][0246]
seq id no:9(也被称为r49 1peak增强子)包含与编码gfp的核苷酸序列可操作地连接的ires序列和一个造血增强子元件:
[0247]
[0248]
[0249][0250]
seq id no:62(也被称为r50 3peak增强子)包含与编码gfp的核苷酸序列可操作地连接的ires序列和三个造血增强子元件:
[0251]
[0252]
[0253][0254]
在任意方面的一些实施方式中,本文所述的核酸序列是载体或包含在载体中或在载体中提供。所述载体可为例如质粒、病毒载体,或腺病毒载体、慢病毒载体或逆转录病毒载体。如本文所用,术语“逆转录病毒”是指将其基因组的拷贝插入其侵入的宿主细胞的dna中,从而改变该细胞的基因组的rna病毒。此类病毒是单链rna病毒或双链dna病毒中的一者。在任意方面的一些实施方式中,逆转录病毒是α逆转录病毒。如本文所用,术语“慢病毒”是指复合逆转录病毒的组(或属)。慢病毒能够感染非分裂细胞类型以及活跃分裂的细胞类型,而标准逆转录病毒只能感染有丝分裂活跃的细胞类型。示例性慢病毒包括但不限于:hiv(人类免疫缺陷病毒;包括1型hiv和2型hiv);梅迪-维斯那病毒(visna-maedi virus,
vmv)病毒;山羊关节炎脑炎病毒(caev);马传染性贫血病毒(eiav);猫免疫缺陷病毒(fiv);牛免疫缺陷病毒(biv);和猴免疫缺陷病毒(siv)。如本文所用,术语“腺病毒”是指具有包含双链dna基因组的二十面体核壳的无包膜病毒。如本文所用,术语“病毒载体”是指核酸载体构建体,所述核酸载体构建体包含至少一个病毒来源的元件并具有被包装到病毒载体颗粒中的能力。病毒载体可含有本文所述的核酸代替非必需的病毒基因。所述载体和/或颗粒可用于在体外或体内将任意核酸转移至细胞中的目的。许多形式的病毒载体是本领域已知的。
[0255]
在任意方面的一些实施方式中,本文所述的核酸序列和/或载体包含在病毒颗粒(例如慢病毒颗粒)中、以病毒颗粒(例如慢病毒颗粒)提供或位于病毒颗粒(例如慢病毒颗粒)中。
[0256]
在任意实施方式的一个方面中,本文描述了包含如本文所述的核酸序列、载体或颗粒以及药学上可接受的运载体的组合物。
[0257]
在任意实施方式的一个方面中,本文描述了包含本文所述的核酸序列(和/或包含此类核酸序列的载体或病毒颗粒)和任选的药学上可接受的运载体的药物组合物。在任意方面的一些实施方式中,所述药物组合物的活性成分包含如本文所述的核酸(和/或包含此类核酸序列的载体或病毒颗粒)。在任意方面的一些实施方式中,所述药物组合物的活性成分由如本文所述的核酸(和/或包含此类核酸序列的载体或病毒颗粒)组成。药学上可接受的运载体和稀释剂包括盐水、水性缓冲溶液、溶剂和/或分散介质。此类运载体和稀释剂的使用是本领域公知的。可用作药学上可接受的运载体的材料的一些非限制性实例包括:(1)糖类,例如乳糖、葡萄糖和蔗糖;(2)淀粉,例如玉米淀粉和马铃薯淀粉;(3)纤维素及其衍生物,例如羧甲基纤维素钠、甲基纤维素、乙基纤维素、微晶纤维素和醋酸纤维素;(4)黄蓍胶粉;(5)麦芽;(6)明胶;(7)润滑剂,例如硬脂酸镁、十二烷基硫酸钠和滑石;(8)赋形剂,例如可可脂和栓剂蜡;(9)油类,例如花生油、棉籽油、红花油、芝麻油、橄榄油、玉米油和大豆油;(10)二元醇类,例如丙二醇;(11)多元醇,例如甘油、山梨糖醇、甘露糖醇和聚乙二醇(peg);(12)酯类,油酸乙酯和月桂酸乙酯;(13)琼脂;(14)缓冲剂,例如氢氧化镁和氢氧化铝;(15)海藻酸;(16)无热原水;(17)等渗盐水;(18)林格氏溶液;(19)乙醇;(20)ph缓冲溶液;(21)聚酯、聚碳酸酯和/或聚酸酐;(22)填充剂,例如多肽和氨基酸;(23)血清组分,例如血清白蛋白、hdl和ldl;(22)c
2-c
12
醇,例如乙醇;以及(23)用于药物制剂的其它无毒相容物质。润湿剂、着色剂、脱模剂、包衣剂、甜味剂、调味剂、芳香剂、防腐剂和抗氧化剂也可存在于所述制剂中。例如“赋形剂”、“运载体”、“药学上可接受的运载体”等术语在本文中可互换使用。在任意方面的一些实施方式中,所述运载体抑制活性剂的降解,例如抑制包含编码如本文所述的gata结合因子1(gata1)多肽的序列的核酸的降解。
[0258]
在任意方面的一些实施方式中,包含如本文所述的核酸序列(和/或包含此类核酸序列的载体或病毒颗粒)的药物组合物可为肠胃外剂型,所述核酸序列包含编码gata结合因子1(gata1)多肽的序列。由于肠胃外剂型的给予通常绕过患者对污染物的天然防御,肠胃外剂型优选为无菌的或能够在给予患者之前被灭菌。肠胃外剂型的实例包括但不限于即用型注射液、溶解或悬浮于药学上可接受的注射用媒介中的即用型干燥产品、即用型注射剂、和乳液。此外,可制备用于给予患者的控释肠胃外剂型,包括但不限于型剂型和剂量倾泻。
[0259]
可用于提供包含如本文所述的核酸序列(和/或包含此类核酸序列的载体或病毒颗粒)的药物组合物的肠胃外剂型的合适媒介是本领域技术人员众所公知的,所述核酸序列包含编码gata结合因子1(gata1)多肽的序列。实例不受限地包括:无菌水;注射用水usp;盐水溶液;葡萄糖溶液;水性媒介(例如但不限于氯化钠注射液、林格氏注射液、葡萄糖注射液、右旋糖和氯化钠注射液、和乳酸林格氏注射液);水混溶的媒介(例如但不限于乙醇、聚乙二醇和丙二醇);以及非水性媒介(例如但不限于玉米油、棉籽油、花生油、芝麻油、油酸乙酯、肉豆蔻酸异丙酯和苯甲酸苄酯)。改变或修饰本文公开的药物组合物的药学上可接受的盐的溶解度的化合物也可并入本公开的肠胃外剂型,包括常规和控释肠胃外剂型。
[0260]
包含如本文所述的含有编码gata结合因子1(gata1)多肽的序列的核酸序列(和/或包含此类核酸序列的载体或病毒颗粒)的药物组合物也可配制为适用于口服给药,例如作为离散剂型,例如但不限于片剂(包括但不限于刻痕或包衣片剂)、丸剂、囊片、胶囊剂、咀嚼片剂、粉包、扁囊剂、锭剂、口腔膜剂(wafers)、气溶胶喷雾剂或液体,例如但不限于糖浆剂、酏剂、溶液剂、或在水性液体、非水性液体、水包油乳液或油包水乳液中的悬浮剂。此类组合物含有预定量的公开化合物的药学上可接受的盐,并且可通过本领域技术人员公知的药学方法制备。通常参见remington:the science and practice of pharmacy,第21版,lippincott,williams和wilkins,philadelphia pa.(2005)。
[0261]
常规剂型通常提供从制剂中快速或立即的药物释放。依据药物的药理学和药代动力学,使用常规剂型会导致患者血液和其它组织中药物浓度的大幅波动。这些波动会影响许多参数,例如剂量频率、作用开始、功效持续时间、治疗血液水平的维持、毒性、副作用等。有利地,控释制剂可用于控制药物的作用开始、作用持续时间、治疗窗口内的血浆水平和峰血液水平。特别是,控释或延迟释放剂型或制剂可用于确保实现药物的最大有效性,同时使潜在的不良作用和安全问题最小化,这都可能发生在使药物剂量不足(即低于最低治疗水平进行)以及超过关于该药物的毒性水平中。在任意方面的一些实施方式中,包含如本文公开的含有编码gata结合因子1(gata1)多肽的序列的核酸序列(和/或含有此类核酸序列的载体或病毒颗粒)可以以缓释制剂给药。
[0262]
控释药物产品具有改善药物疗法的普遍目的,优于它们的非控释对应物所实现的药物疗法。理想地,在医学治疗中使用优化设计的控释制品的特征在于使用最少的药物物质以在最小量的时间内治愈或控制病症。控释制剂的优点包括:1)延长的药物活性;2)减少的剂量频率;3)增加的患者依从性;4)使用更少的总药物;5)局部或系统性副作用减少;6)药物积累的最小化;7)血液水平波动减少;8)治疗功效改善;9)药物活性的增强或丧失减少;以及10)疾病或病症控制速度改善。kim,cherng-ju,controlled release dosage form design,2(technomic publishing,lancaster,pa.:2000)。
[0263]
大多数控释制剂被设计为最初释放一定量的迅速产生所需治疗效果的药物(活性成分),并且逐渐且持续地释放其它量的药物以在延长的一段时间内维持该水平的治疗或预防效果。为了在体内维持该恒定的药物水平,药物必须以一定的速率从剂型中释放,这将取代从体内被代谢和排出的药物量。活性成分的控释可通过各种条件刺激,包括但不限于ph、离子强度、渗透压、温度、酶、水和其它生理条件或化合物。
[0264]
多种已知的控释或延迟释放剂型、制剂和设备可适用于与本公开的盐和组合物一起使用。实例包括但不限于美国专利号:3,845,770、3,916,899、3,536,809、3,598,123、4,
008,719、5674,533、5,059,595、5,591,767、5,120,548、5,073,543、5,639,476、5,354,556、5,733,566和6,365,185b1中所描述的;通过引用的方式将其各自并入本文。这些剂型可用于提供一种或多种活性成分的缓释或控释,使用例如羟丙基甲基纤维素、其它聚合物基质、凝胶、渗透膜、渗透系统(例如(alza corporation,mountain view,calif.usa))或它们的组合,以提供不同比例的期望的释放谱。
[0265]
在实施方式的一些方面,本文描述了治疗有需要的受试者中diamond-blackfan贫血的方法,所述方法包括向患者给予治疗有效量的如本文所述的核酸序列、颗粒或组合物。
[0266]
本文所述的组合物可给予患有或诊断为患有dba的受试者。在任意方面的一些实施方式中,本文所述的方法包括向受试者给予有效量的本文所述的组合物(例如有效量的如本文所述的包含编码gata结合因子1(gata1)多肽的序列的核酸),以缓解dba的症状。如本文所用,“缓解症状”是改善与dba相关的任意病症或症状。通过任意标准测量,与对等的未处理对照相比,此种减少为至少5%、10%、20%、40%、50%、60%、80%、90%、95%、99%或更多。将本文所述的组合物给予受试者的多种手段是本领域技术人员已知的。此类方法可包括但不限于口服、肠胃外、静脉内、肌内、皮下、经皮、气道(气溶胶)、肺、皮肤、局部或注射给予。给予可为局部的或系统性的。
[0267]
如本文所用的术语“有效量”是指缓解疾病或紊乱的至少一种或多种症状所需的活性剂的量,并且涉及提供期望效果的足够量的药理学组合物。因此,术语“治疗有效量”是指当给予典型受试者时足以提供特定效果的活性剂的量。如本文所用的有效量,在各种情况下,还包括足以延迟疾病症状的发展,改变疾病症状的进程(例如但不限于减缓疾病症状的进展)或逆转疾病的症状的量。因此,具体说明确切的“有效量”通常不可行。然而,对于任何给定的情况,合适的“有效量”可由本领域普通技术人员仅使用常规实验来确定。
[0268]
有效量、毒性和治疗功效可通过细胞培养物或实验动物中的标准药学程序来确定,例如用于确定ld50(使50%群体致死的剂量)和ed50(在50%群体中治疗有效的剂量)。剂量可依据所采用的剂型和所使用的给药途径而变化。毒性和治疗效果之间的剂量比为治疗指数,并且可表示为ld50/ed50比值。优选表现出大的治疗指数的组合物和方法。治疗有效剂量可从细胞培养试验中初步估计。此外,可在动物模型中制定剂量以达到循环血浆浓度范围,该范围包括在细胞培养中或在合适的动物模型中确定的ic50(即达到了对症状的半数最大抑制的活性剂的浓度)。例如,可通过高效液相色谱法测量血浆中的水平。任何特定剂量的效果可通过合适的生物测定(例如其中的红血细胞和/或红细胞生成水平的测定等)来监测。剂量可由医生确定,并在必要时进行调整以适应观察到的治疗效果。
[0269]
如本文所述的组合物的剂量可由医生确定并在必要时进行调整以适应观察到的治疗效果。关于治疗的持续时间和频率,熟练的临床医生通常监测受试者以确定何时治疗提供治疗益处,并确定是否增加或降低剂量、增加或降低给予频率、停止治疗、恢复治疗、或对治疗方案进行其它改变。依据许多临床因素(例如受试者对活性剂的敏感性),剂量计划可以从每周一次到每天一次不等。期望的激活剂量或量可一次性给予或分成亚剂量给予,例如2-4个亚剂量并在一段时间内(例如以一天中的适当间隔或其它适当的计划)给予。在任意方面的一些实施方式中,给予可为长期的,例如在数周或数月的时间段内每天一个或多个剂量和/或治疗。剂量和/或治疗计划的实例为在1周、2周、3周、4周、1个月、2个月、3个月、4个月、5个月或6个月或更长时间的时段内每天、每天两次、每天三次或每天四次或更多
次给予。可以在一段时间内(例如5分钟、10分钟、15分钟、20分钟或25分钟内)给予包含如本文公开的含有编码gata结合因子1(gata1)多肽的序列的核酸序列(和/或含有此类核酸序列的载体或病毒颗粒)的组合物。
[0270]
在任意方面的一些实施方式中,在初始治疗方案之后,治疗可在较低频率的基础上给予。例如,每两周治疗三个月后,治疗可每月、六个月、或一年或更长时间重复一次。根据本文所述的方法的治疗可将病症的标志物或症状的水平减少至少10%、至少15%、至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%、或至少90%或更多。
[0271]
根据本文所述的方法,如本文公开的包含编码gata结合因子1(gata1)多肽的序列的核酸序列(和/或包含此类核酸序列的载体或病毒颗粒)的给予的剂量范围取决于,例如抑制剂的形式、其效力、以及本文所述病症的症状、标志物或指标的期望减少程度(例如百分比)。通常,剂量将随患者的年龄、病症和性别而变化并且可由本领域技术人员确定。在任何并发症的情况中,剂量也可由个体医生调整。
[0272]
如本文所公开的包含编码gata结合因子1(gata1)多肽的序列的核酸序列(和/或包含此类核酸序列的载体或病毒颗粒)在例如dba或本文所述的任何其它病症的治疗中的功效或诱导如本文所述的反应的功效可由熟练的临床医生确定。然而,如果在根据本文所述的方法进行治疗后,本文所述的病症的体征或症状中的一种或多种以有益的方式改变,其它临床上可接受的症状得到改善或甚至好转,或期望的反应被诱导(例如至少10%),治疗被认为是如本文所使用的术语“有效治疗”。例如,可通过测量根据本文所述的方法治疗的病症的标志物、指标、症状和/或发病率或任何其它适当的可测量参数来评估功效。也可通过个体未能恶化(通过住院治疗评估)或对医疗干预的需要(即疾病的进展停止)来测量功效。测量这些指标的方法是本领域技术人员已知的和/或在本文中有所描述。治疗包括对个体或动物(一些非限制性实例包括人或动物)的疾病的任何治疗,并且包括:(1)抑制疾病,例如防止症状恶化;或(2)减轻疾病的严重程度,例如引起症状的消退。疾病治疗的有效量是指当给予有需要的受试者时足以引起对于该疾病的如本文所定义的术语所述的有效治疗的量。可通过评估病症或期望反应的物理指标来确定药剂的功效。通过测量此类参数中的任一个或参数的任意组合来监测给药和/或治疗的功效完全在本领域技术人员的能力内。可在本文所述的病症的动物模型中评估功效,例如dba的治疗。
[0273]
在任意实施方式的一个方面中,本文描述了恢复早期红系祖细胞细胞特异性gata1表达的方法,所述方法包括:使包含早期红系祖细胞的细胞群与如本文所述的核酸序列、颗粒或组合物接触。
[0274]
在任意方面的一些实施方式中,早期红系祖细胞包含dba相关的基因突变,包括但不限于表5中所列的那些。在任意方面的一些实施方式中,红系祖细胞包含一个或多个dba相关的基因突变。dba相关的基因突变是本领域众所公知的,并且包括但不限于表5中列出的突变(例如,参见int j hematol.2010oct;92(3):413-8)。
[0275]
表5:示例性dba相关的基因突变
[0276][0277]
在任意方面的一些实施方式中,以非限制性实例的方式,gata-1的水平可通过蛋白质印迹、免疫沉淀、酶联免疫吸附测定(elisa)、放射免疫测定(ria)、夹心式测定、荧光原位杂交(fish)、免疫组织学染色、放射免疫测定、免疫荧光测定、质谱和/或免疫电泳测定来测量。
[0278]
rna和/或dna分子可从生物样品(例如血液样品)中分离、衍生或扩增。用于检测mrna表达的技术是本领域技术人员已知的,并且可以包括但不限于pcr程序、rt-pcr、定量rt-pcr、northern印迹测定、差异基因表达、rnase保护测定、基于微阵列的分析、下一代测序、杂交方法等。
[0279]
通常而言,pcr程序描述了基因扩增的方法,所述方法包括(i)引物与核酸样品或文库中的特定基因或序列的序列特异性杂交;(ii)后续扩增,所述扩增涉及使用热稳定的dna聚合酶的多轮退火、延伸和变性;以及(iii)筛选pcr产物中正确大小的条带。所使用的引物是足够长且合适的序列的寡核苷酸以提供聚合的起始,即每个引物被专门设计为与待扩增的基因组基因座的链互补。在替代的实施方式中,本文所述的基因表达产物的mrna水平可以通过逆转录(rt)pcr以及通过定量rt-pcr(qrt-pcr)或实时pcr方法来确定。rt-pcr和qrt-pcr的方法是本领域公知的。
[0280]
在任意方面的一些实施方式中,mrna的水平可通过定量测序技术(例如定量下一代测序技术)来测量。对核酸序列进行测序的方法是本领域公知的。简而言之,可使从受试者获得的样品与一个或多个引物接触,所述一个或多个引物和靶基因序列侧翼的单链核酸序列特异性杂交并合成互补链。在一些下一代技术中,将连接头(双链或单链)连接到样品中的核酸分子,然后从连接头或连接头兼容的引物开始合成。在一些第三代技术中,可以例如通过确定探针杂交的位置和模式,或测量单个分子在其通过传感器时的一个或多个特征(例如当核酸分子通过纳米孔时电场的调制)来确定所述序列。示例性的测序方法包括但不限于:sanger测序、双脱氧链终止、高通量测序、下一代测序、454测序、solid测序、polony测序、illumina测序、ion torrent测序、通过杂交测序、纳米孔测序、helioscope测序、单分子实时测序、rnap测序等。用于执行这些测序方法的方法和方案是本领域已知的,参见例如“next generation genome sequencing”,michal janitz编著,wiley-vch;“high-throughput next generation sequencing”,kwon和ricke编著,humanna press,2011;以及sambrook等,molecular cloning:a laboratory manual(第4版),cold spring harbor laboratory press,cold spring harbor,n.y.,usa(2012);以引用的方式将它们的整体并入本文。
[0281]
核酸和核糖核酸(rna)分子可使用本领域公知的多种程序中的任一种从特定生物
样品中分离,选择的特定分离程序适合于特定生物样品。例如,冻融和碱裂解程序可对从固体材料中获取核酸分子有用;加热和碱裂解程序可对从尿液中获取核酸分子有用;以及蛋白酶k提取可用于从血液中获取核酸(roiff,a等,pcr:clinical diagnostics and research,springer(1994))。
[0282]
在任意方面的一些实施方式中,本文所述的试剂(例如抗体试剂和/或核酸探针)中的一种或多种可包含可检测标记和/或包含产生可检测信号的能力(例如通过催化反应以将化合物转化为可检测的产物)。可检测标记可包括例如吸光染料、荧光染料或放射性标记。可检测标记、检测它们的方法以及将它们掺入试剂(例如抗体和核酸探针)中的方法是本领域公知的。
[0283]
在任意方面的一些实施方式中,可检测标记可包括可通过光谱、光化学、生物化学、免疫化学、电磁、放射化学或化学手段(例如荧光、化学荧光或化学发光),或者任何其它适当的手段来检测的标记。本文所述方法中使用的可检测标记可为初级标记(其中标记包含可直接检测或产生可直接检测部分的部分)或二级标记(其中可检测标记结合另一部分以产生可检测信号,例如在使用二级和三级抗体的免疫标记中很常见)。可检测标记可通过共价或非共价手段与试剂连接。或者,例如可通过直接对分子进行标记来连接可检测标记,所述分子经由配体-受体结合对排列或其它此类特异性识别分子实现与试剂结合。可检测标记可包括但不限于放射性同位素、生物发光化合物、生色团、抗体、化学发光化合物、荧光化合物、金属螯合物和酶。
[0284]
在其它实施方式中,检测试剂由荧光化合物标记。当荧光标记的试剂暴露在适当波长的光下时,由于荧光可检测到它的存在。在任意方面的一些实施方式中,可检测标记可为荧光染料分子或荧光团,所述荧光染料分子或荧光团包括但不限于荧光素、藻红蛋白、藻蓝蛋白、邻苯二甲醛、荧光胺、cy3tm、cy5tm、异藻蓝蛋白、德克萨斯红、peridenin叶绿素、花菁、串联偶联物(例如藻红蛋白-cy5tm)、绿色荧光蛋白、罗丹明、异硫氰酸荧光素(fitc)和俄勒冈绿tm、罗丹明及衍生物(例如德克萨斯红和四罗丹明异硫氰酸酯(tritc))、生物素、藻红蛋白、amca、cydyestm、6-羧基荧光素(carboxyfhiorescein,通常缩写为fam和f)、6-羧基-2',4',7',4,7-六氯荧光素(hex)、6-羧基-4',5'-二氯-2',7'-二甲氧基荧光素(joe或j)、n,n,n',n'-四甲基-6羧基罗丹明(tamra或t)、6-羧基-x-罗丹明(rox或r)、5-羧基罗丹明-6g(r6g5或g5)、6-羧基罗丹明-6g(r6g6或g6)和罗丹明110、花菁染料(例如cy3、cy5和cy7染料)、香豆素(例如伞形酮)、苯甲亚胺染料(例如hoechst 33258)、菲啶染料(例如德克萨斯红)、乙锭染料、吖啶染料、咔唑染料、吩噁嗪染料、卟啉染料、聚甲炔染料(例如花菁染料,如cy3、cy5等)、bodipy染料和喹啉染料。在任意方面的一些实施方式中,可检测标记可为放射性标记,包括但不限于3h、125i、35s、14c、32p和33p。在任意方面的一些实施方式中,可检测标记可为酶,包括但不限于辣根过氧化物酶和碱性磷酸酶。酶标记可产生例如化学发光信号、颜色信号或荧光信号。考虑用于可检测标记的抗体试剂的酶包括但不限于苹果酸脱氢酶、葡萄球菌核酸酶、δ-v-类固醇异构酶、酵母醇脱氢酶、α-甘油磷酸脱氢酶、磷酸丙糖异构酶、辣根过氧化物酶、碱性磷酸酶、天冬酰胺酶、葡萄糖氧化酶、β-半乳糖苷酶、核糖核酸酶、脲酶、过氧化氢酶、葡萄糖-vi-磷酸脱氢酶、葡萄糖淀粉酶和乙酰胆碱酯酶。在任意方面的一些实施方式中,可检测标记是化学发光标记,包括但不限于光泽精、鲁米诺、萤光素、异鲁米诺、theromatic吖啶酯、咪唑、吖啶盐和草酸酯。在任意方面的一些实施方式中,
可检测标记可为光谱比色标记,包括但不限于胶体金或有色玻璃或塑料(例如聚苯乙烯、聚丙烯和乳胶)珠。
[0285]
在任意方面的一些实施方式中,检测试剂也可用可检测标签进行标记,例如c-myc、ha、vsv-g、hsv、flag、v5、his或生物素。也可使用其它检测系统,例如生物素-链霉亲和素系统。在该系统中,与感兴趣的生物标志物有免疫反应性(即特异性)的抗体被生物素化。使用链霉亲和素-过氧化物酶偶联物和显色底物确定与生物标志物结合的生物素化抗体的量。此类链霉亲和素过氧化物酶检测试剂盒是可商业获得的,例如从dako;carpinteria,ca。还可使用荧光发射金属(例如152eu或镧系元素的其它金属)可检测地标记试剂。这些金属可使用诸如二乙烯三胺五乙酸(dtpa)或乙二胺四乙酸(edta)之类的金属螯合基团附接至所述试剂。
[0286]
低于参比水平的水平可为以下水平:相对于参比水平,低至少约5%、至少约10%、至少约15%、至少约20%、至少约50%、至少约60%、至少约80%、至少约90%或更少的水平。在任意方面的一些实施方式中,低于参比水平的水平可为统计学上显著低于参比水平的水平。
[0287]
高于参比水平的水平可为以下水平:与参比水平相比而言,高至少约10%、至少约20%、至少约50%、至少约60%、至少约80%、至少约90%、至少约100%、至少约200%、至少约300%、至少约500%或更多的水平。在任意方面的一些实施方式中,高于参比水平的水平可为统计学上显著高于参比水平的水平。
[0288]
在任意方面的一些实施方式中,所述参比可为未患有或未被诊断为患有和/或未表现出肺部感染和/或肺部炎症的体征或症状的受试者群体中靶标的水平。在任意方面的一些实施方式中,所述参比还可为对照样品、对照个体的合并样品或基于它们的数值或数值范围中靶标的水平。在任意方面的一些实施方式中,所述参比可为在较早时间点从同一受试者获得的样品中靶标的水平,例如本文所述的方法可用于确定受试者对给定的疗法的敏感性或反应是否随着时间而改变。
[0289]
在前述方面的一些实施方式中,可将给定基因的表达水平相对于一个或多个参比基因或参比蛋白质的表达水平来进行归一化。
[0290]
在任意方面的一些实施方式中,参比水平可为以下样品中的水平:相似细胞类型,样品类型,样品处理,和/或从具有与待确定中性粒细胞积聚和/或polyp的水平的样品/受试者相似的年龄、性别和其它人口统计学参数的受试者获得的的样品。在任意方面的一些实施方式中,测试样品和对照参比样品为相同类型,即从相同的生物来源获得并且包含相同的组成,例如相同数量和类型的细胞。
[0291]
如本文所用,术语“样品”或“测试样品”表示从生物有机体获取或分离的样品(例如来自受试者的血液或血浆样品)。在任意方面的一些实施方式中,本发明包括生物样品的若干实例。在任意方面的一些实施方式中,生物样品是细胞、或组织、或外周血、或体液。示例性生物样品包括但不限于活体检查切片、肿瘤样品、生物流体样品、血液、血清、血浆、尿、精子、粘液、组织活体检查切片、器官活体检查切片、滑液、胆汁液、脑脊液、黏膜分泌物、积液、汗、唾液和/或组织样品等。该术语还包括上述样品的混合物。术语“测试样品”还包括未处理或预处理(或预先加工)的生物样品。在任意方面的一些实施方式中,测试样品可包含来自受试者的细胞。在任意方面的一些实施方式中,测试样品可为肺样品、肺抽出物、痰样
品、气道样品、血清样品等。
[0292]
测试样品可通过从受试者中移取样品来获得,但也可通过使用先前分离的样品(例如在先前的时间点分离以及由同一人或另一人分离)来完成。
[0293]
在任意方面的一些实施方式中,测试样品可为未处理的测试样品。如本文所用,短语“未处理的测试样品”是指除稀释和/或悬浮在溶液中之外没有进行任何先前样品预处理的测试样品。用于处理测试样品的示例性方法包括但不限于离心、过滤、超声、均质化、加热、冷冻和解冻及它们的组合。在任意方面的一些实施方式中,测试样品可为冷冻测试样品,例如冷冻组织。在采用本文所述的方法、测定和系统之前,可将冷冻样品解冻。解冻后,冷冻样品可在进行本文所述的方法、测定和系统之前进行离心。在任意方面的一些实施方式中,测试样品是澄清的测试样品,例如通过离心和收集包含澄清的测试样品的上清液。在任意方面的一些实施方式中,测试样品可为预先加工的测试样品,例如由选自于由离心、过滤、解冻、纯化及它们的任意组合所组成的组中的处理所产生的上清液或滤液。在任意方面的一些实施方式中,可用化学和/或生物试剂处理测试样品。在加工过程中,可使用化学和/或生物试剂来保护和/或维持样品包括其中的生物分子(例如核酸和蛋白质)的稳定性。一种示例性试剂为蛋白酶抑制剂,所述蛋白酶抑制剂通常用于在加工过程中保护或维持蛋白质的稳定性。技术人员非常了解适用于对确定如本文所述的表达产物的水平所需的生物样品进行预先加工的方法和过程。
[0294]
为方便起见,以下提供了本说明书、实施例和所附权利要求中使用的一些术语和短语的含义。除非另有说明或上下文中隐含,以下术语和短语包括以下提供的含义。提供所述定义旨在帮助描述特定的实施方式,而非旨在限制所要求保护的发明,因为本发明的范围仅由权利要求限制。除非另有定义,本文使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常理解的含义相同的含义。如果本领域中术语的使用与本文提供的其定义之间存在明显差异,应以本说明书中提供的定义为准。
[0295]
为方便起见,将本说明书、实施例和所附权利要求中即本文使用的某些术语收集于此。
[0296]
术语“降低(decrease)”、“减少(reduced/reduction)”、或“抑制(inhibit)”在本文中均用于表示统计学上显著量的降低。在任意方面的一些实施方式中,“减少”或“降低”或“抑制”通常是指与参比水平(例如不存在给定的治疗或药剂)相比,至少10%的降低,并且可包括例如至少约10%、至少约20%、至少约25%、至少约30%、至少约35%、至少约40%、至少约45%、至少约50%、至少约55%、至少约60%、至少约65%、至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%、至少约98%、至少约99%或更多的降低。如本文所用,“减少”或“抑制”不包括与参比水平相比的完全抑制或减少。“完全抑制”为与参比水平相比的100%的抑制。对于不具有给定紊乱的个体,降低可优选地下降至在正常范围内可接受的水平。
[0297]
术语“增加(increased/increase)”、“增强(enhance)”或“激活(activate)”在本文中均用于表示统计学上显著量的增加。在任意方面的一些实施方式中,术语“增加”、“增强”或“激活”可表示与参比水平相比至少10%的增加,例如与参考水平相比至少约20%、或至少约30%、或至少约40%、或至少约50%、或至少约60%、或至少约70%、或至少约80%、或至少约90%的增加或高达并包括100%增加或介于10%-100%之间的任意增加,或与参
比水平相比至少约2倍、或至少约3倍、或至少约4倍、或至少约5倍或至少约10倍的增加,或介于2倍和10倍之间或更多的任意增加。在标志物或症状的上下文中,“增加”是关于该水平的统计学上显著的增加。
[0298]
如本文所用,“受试者”意指人或动物。通常,动物是脊椎动物,例如灵长类动物、啮齿动物、家养动物或狩猎动物。灵长类动物包括黑猩猩、食蟹猴(cynomologous monkeys)、蜘蛛猴和猕猴(例如恒河猴)。啮齿动物包括小鼠、大鼠、土拨鼠、雪貂、兔子和仓鼠。家养动物和狩猎动物包括牛、马、猪、鹿、野牛、水牛、猫科物种(例如家猫)、犬科物种(例如狗、狐狸、狼)、鸟类物种(例如鸡、鸸鹋、鸵鸟)以及鱼类(例如鳟鱼、鲶鱼和鲑鱼)。在任意方面的一些实施方式中,受试者为哺乳动物,例如灵长类动物(例如人)。术语“个体”、“患者”和“受试者”在本文中可互换使用。
[0299]
优选地,受试者是哺乳动物。哺乳动物可为人、非人灵长类动物、小鼠、大鼠、狗、猫、马或牛,但不限于这些实例。人以外的哺乳动物可有利地用作代表病症的物模型的受试者。受试者可为雄性或雌性。
[0300]
受试者可为先前已被诊断患有或被鉴定为遭受或具有需要治疗的病症或与此类病症相关的一种或多种并发症的受试者,并且任选地已经经历了该病症或与该病症相关的一种或多种并发症的治疗的受试者。或者,受试者也可为先前未被诊断为患有该病症或与该病症相关的一种或多种并发症的受试者。例如,受试者可为表现出关于该病症或与该病症相关的一种或多种并发症的一种或多种风险因素的受试者或不表现出风险因素的受试者。
[0301]
对特定病症的治疗的“有需要的受试者”可为患有该病症、被诊断为患有该病症或处于发展为该病症的风险中的受试者。
[0302]
在本文所述的各种实施方式中,进一步考虑包括所述的特定多肽的任意的变体(天然存在的或其它方式)、等位基因、同系物、保守修饰变体和/或保守置换变体。对于氨基酸序列,本领域技术人员将认识到,改变了编码序列中的单个氨基酸或小部分氨基酸的对核酸、肽、多肽或蛋白质序列的个体替换、删除或添加是“保守修饰的变体”,其中的改变使得氨基酸被化学上相似的氨基酸置换,并保留了多肽的期望活性。此类保守修饰的变体包括并且不排除符合本公开的多态性变体、种间同系物和等位基因。
[0303]
给定的氨基酸可被具有相似生理化学特征的残基替换,例如用一个脂肪族残基置换另一个(例如ile、val、leu或ala置换为另一个),或用一个极性残基置换另一个(例如lys和arg之间;glu和asp之间;或gln和asn之间)。其它此类保守置换(例如具有相似疏水特性的整个区域的置换)是公知的。可在本文所述的任意一种测定中测试包含保守氨基酸置换的多肽以确认期望的活性(例如天然或参比多肽的活性和特异性)得以保留。
[0304]
氨基酸可根据其侧链性质的相似性进行分组(在a.l.lehninger,in biochemistry,第2版,pp.73-75,worth publishers,new york(1975)中):(1)非极性:ala(a)、val(v)、leu(l)、ile(i)、pro(p)、phe(f)、trp(w)、met(m);(2)不带电荷极性:gly(g)、ser(s)、thr(t)、cys(c)、tyr(y)、asn(n)、gln(q);(3)酸性:asp(d)、glu(e);(4)碱性:lys(k)、arg(r)、his(h)。或者,天然存在的残基可基于常见的侧链特性分组:(1)疏水性:正亮氨酸、met、ala、val、leu、ile;(2)中性亲水性:cys、ser、thr、asn、gln;(3)酸性:asp、glu;(4)碱性:his、lys、arg;(5)影响链取向的残基:gly、pro;(6)芳香族:trp、tyr、phe。非保守
置换将需要将这些分类之一的成员交换为另一个分类。特定的保守置换包括例如;ala变为gly或变为ser;arg变为lys;asn变为gln或变为his;asp变为glu;cys变为ser;gln变为asn;glu变为asp;gly变为ala或变为pro;his变为asn或变为gln;ile变为leu或变为val;leu变为ile或变为val;lys变为arg、变为gln或变为glu;met变为leu、变为tyr或变为ile;phe变为met、变为leu或变为tyr;ser变为thr;thr变为ser;trp变为tyr;tyr变为trp;和/或phe变为val、变为ile或变为leu。
[0305]
术语“mirna”和“microrna”是指源自内源性基因的21-25nt的非编码rna。它们由更长(约75nt)的发夹样前体(称为pre-mirna)加工而成。microrna组装为称为mirnp的复合物,并通过反义互补性识别它们的靶标。如果microrna与其靶标100%匹配(即互补性是完全的),则靶标mrna被剪切,且mirna的作用类似于sirna。如果匹配不完全(即互补性是部分的),则靶标mrna的翻译被阻断。
[0306]
术语“mirna靶位点”或“microrna靶位点”是指mrna靶标中microrna的特异性靶结合序列。mirna与其靶位点之间的互补性不必是完全的。
[0307]
如本文所用,术语“蛋白质”和“多肽”在本文中可互换使用,以指代通过相邻残基的α-氨基基团和羧基基团之间的肽键彼此连接的一系列氨基酸残基。术语“蛋白质”和“多肽”是指氨基酸的聚合物,包括修饰的氨基酸(例如磷酸化、糖化、糖基化等)和氨基酸类似物,无论其大小或功能如何。“蛋白质”和“多肽”通常用于指相对大的多肽,而术语“肽”通常用于指小的多肽,但这些术语在本领域中的用法重叠。当涉及基因产物及其片段时,术语“蛋白质”和“多肽”在本文中可互换使用。因此,示例性多肽或蛋白质包括基因产物、天然存在的蛋白质、同系物、直系同源物、旁系同源物、片段,和上述的其它等同物、变体、片段和类似物。
[0308]
在任意方面的一些实施方式中,本文所述的多肽(或编码此类多肽的核酸)可为本文所述的氨基酸序列之一的功能片段。如本文所用,“功能片段”是根据本文下文描述的测定保留至少50%的野生型参比多肽活性的肽片段或区段。功能片段可包含本文公开的序列的保守置换。
[0309]
在任意方面的一些实施方式中,本文所述的多肽可为本文所述的序列的变体。在任意方面的一些实施方式中,所述变体是保守修饰的变体。例如,保守置换变体可通过天然核苷酸序列的突变来获得。如本文所指,“变体”是与天然或参比多肽基本上同源的多肽,但由于一个或多个删除、插入或置换而具有与天然或参比多肽的氨基酸序列不同的氨基酸序列。编码变体多肽的dna序列当与天然或参比dna序列相比时,包含含有一个或多个核苷酸添加、删除或置换的序列,但编码保留活性的变体蛋白质或其片段。多种多样的基于pcr位点特异性诱变方法是本领域已知的并且可由普通技术人员来实施。
[0310]
变体氨基酸或dna序列可为与天然或参比序列具有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或更多的同一性。例如可通过使用万维网上用于此目的的常用的免费可得的计算机程序(例如具有默认设置的blastp或blastn)比较这两个序列,来确定天然序列和突变序列之间的同源性程度(同一性百分比)。
[0311]
天然氨基酸序列的改变可通过本领域技术人员已知的多种技术中的任一种来实现。可例如通过合成含有突变序列的寡核苷酸并且其侧翼有限制性位点以能够与天然序列
的片段连接,从而在特定基因座引入突变。连接后,所得的重建序列编码具有所需氨基酸插入、置换或删除的类似物。或者,可采用寡核苷酸定向的位点特异性诱变程序来提供具有根据所需的置换、删除或插入而改变的特定密码子的经改变的核苷酸序列。进行此类改变的技术已经非常成熟,且包括例如由以下公开的技术:walder等,(gene 42:133,1986);bauer等,(gene 37:73,1985);craik(biotechniques,january 1985,12-19);smith等,(genetic engineering:principles and methods,plenum press,1981)和美国专利号4,518,584和4,737,462,通过引用的方式将它们的整体并入本文。任何不参与维持多肽正确构象的半胱氨酸残基也可被置换,通常置换为丝氨酸替换,以提高分子的氧化稳定性并防止异常交联。相反,可将一个或多个半胱氨酸键添加到多肽中以提高其稳定性或促进寡聚化。
[0312]
如本文所用,术语“红细胞生成”是产生红血细胞的过程,该过程从红细胞生成的干细胞发育为成熟红血细胞。如本文所用,术语“红系细胞”是指红血细胞。
[0313]
如本文所用,术语“核酸”或“核酸序列”是指合并核糖核酸、脱氧核糖核酸或其类似物的单元的任意分子,优选聚合的分子。所述核酸可为单链或双链。单链核酸可为变性的双链dna的一条核酸链。或者,它可为不是源自任何双链dna的单链核酸。在任意实施方式的一个方面中,核酸可为dna。在另一方面中,核酸可为rna。合适的dna可包括例如基因组dna或cdna。合适的rna可包括例如mrna。
[0314]
术语“表达”是指涉及产生rna和蛋白质以及适当时位分泌蛋白质的细胞过程,在适用的情况下包括但不限于例如转录、转录本加工、翻译、和蛋白质折叠、修饰和加工。表达可指源自本发明的一个或多个核酸片段的有义(mrna)或反义rna的转录和稳定积累和/或指mrna翻译为多肽。
[0315]
在任意方面的一些实施方式中,本文所述的生物标志物、靶标或基因/多肽的表达是组织特异性的。在任意方面的一些实施方式中,本文所述的生物标志物、靶标或基因/多肽的表达是整体的。在任意方面的一些实施方式中,本文所述的生物标志物、靶标或基因/多肽的表达是系统性的。
[0316]
如本文所用,“表达产物”包括从基因转录的rna,和通过翻译从基因转录的mrna获得的多肽。术语“基因”意指当与适当的调控序列可操作地连接时在体外或体内转录(dna)成为rna的核酸序列。所述基因可包括或可不包括编码区域之前和之后的区域,例如5'非翻译(5'utr)或“前导”序列以及3'utr或“尾部(trailer)”序列,以及各个编码片段(外显子)之间的插入序列(内含子)。
[0317]
如本文所用,“5'utr”或“5'非翻译区域”或“5'前导序列”是指不翻译的mrna区域。5'utr通常在转录起始位点开始,并刚好在编码区域的翻译起始位点或起始密码子(通常是mrna中的aug,dna序列中的atg)之前结束。5'utr的长度可通过突变来修饰,例如5'utr的置换、删除或插入。5'utr可通过突变天然存在的起始密码子或翻译起始位点而进一步修饰,从而使得所述密码子不再作为起始密码子起作用并且翻译可在替代的起始位点起始。
[0318]
如本文所用,“表达增强子”、“增强子序列”或“增强子元件”是指能够增强与它们可操作地连接的下游异源开放阅读框(orf)的表达的核酸序列。
[0319]
如本文所用,术语“转录后调控”是指在rna水平上,介于基因的转录和翻译之间对基因表达的控制。
[0320]
如本文所用,术语“可操作地连接”是指直接或间接相互作用以执行预期功能(例
如介导或调制核酸序列的表达)的序列。可操作地连接的序列的相互作用可以例如由与可操作地连接的序列相互作用的蛋白质介导。通常,它是指转录调控序列与转录序列的功能关系。例如,启动子序列如果在合适的宿主细胞或其它表达系统中刺激或调制开放阅读框的转录,则它与开放阅读框可操作地连接。通常,与转录序列可操作地连接的启动子转录调控序列与该转录序列在物理上连续,即它们是顺式作用的。然而,一些转录调控序列(例如增强子)不需要在物理上与它们所增强转录的开放阅读框连续或位于它们所增强转录的开放阅读框紧临。
[0321]
在本发明的上下文中,“标志物”是指表达产物(例如核酸或多肽),与从对照受试者(例如健康受试者)采集的可比较的样品相比,所述表达产物在取自具有增加的中性粒细胞积累和/或polyp的受试者的样品中差异地存在。术语“生物标志物”与术语“标志物”可互换使用。
[0322]
在任意方面的一些实施方式中,本文所述的方法涉及测量、检测或确定至少一种标志物的水平。如本文所用,术语“检测”或“测量”是指观测来自例如探针、标记或靶分子的信号,以指示样品中分析物的存在。本领域已知的用于检测特定标记部分的任何方法均可用于检测。示例性检测方法包括但不限于光谱、荧光、光化学、生物化学、免疫化学、电学、光学或化学方法。在任意方面的一些实施方式中,测量可为定量观测。
[0323]
在任意方面的一些实施方式中,可对如本文所述的多肽、核酸或细胞进行工程化。如本文所用,“工程化的”是指已被人的手操纵的方面。例如,当多肽的至少一个方面(例如其序列)已经由人的手操纵使得与自然界中存在的方面不同时,所述多肽被认为是“工程化的”。按照通常的做法以及本领域技术人员所理解,工程化细胞的后代通常仍然被称为“工程化的”,即使实际操作是在先前实体上进行的。
[0324]
如本文所用,术语“远端”是指基因上游的核酸序列,其可包含额外的调控元件(例如远端启动子元件是可与它们所调控的基因相距许多千碱基的调控dna序列)。dna或rna的每条链各自都有5'端和3'端,因脱氧核糖(或核糖)环上的碳位置而得名。如本文所用,术语“上游”是指其中发生rna转录的分别在dna和/或rna中5'至3'方向的遗传密码的相对位置。
[0325]
术语“外源性”是指存在于并非其天然来源的细胞中的物质。术语“外源性”当在本文中使用时可指已通过人的手参与的过程导入至生物系统(例如细胞或生物体)中的核酸(例如,编码多肽的核酸)或多肽,在该系统中它通常不存在并且希望将所述核酸或多肽引入此类细胞或生物体。或者,“外源性”可指已通过人的手参与的过程导入至生物系统(例如细胞或生物体)中的核酸或多肽,在该系统中它以相对低的量存在并且希望增加该细胞或生物体中所述核酸或多肽的量(例如以产生异位表达或水平)。相反,术语“内源性”是指生物系统或细胞的天然物质。如本文所用,“异位的”是指以不寻常的位置和/或量存在的物质。异位的物质可为通常在给定细胞中存在的物质,但量少得多和/或在不同时间被发现。异位的还包括物质,例如在其自然环境中的给定细胞中并非天然存在或表达的多肽或核酸。
[0326]
在任意方面的一些实施方式中,本文所述的核酸(例如抑制性核酸)当其包含在载体中时被提供或被给予。在本文所述的一些方面中,核酸序列与载体可操作地连接。如本文所用,术语“载体”是指设计用于递送至宿主细胞或用于在不同宿主细胞之间转移的核酸构建体。如本文所用,载体可为病毒的或非病毒的。
[0327]
术语“载体”包括当与适当的控制元件相关联时能够复制并且可将基因序列转移至细胞的任意遗传元件。载体可包括但不限于克隆载体、表达载体、质粒、噬菌体、转座子、粘粒、染色体、病毒、病毒粒子等。载体可为质粒或慢病毒载体。
[0328]
如本文所用,术语“病毒载体”是指包括病毒来源的至少一个元件并且具有被包装到病毒载体颗粒中的能力的核酸载体构建体。病毒载体可包含代替了非必需病毒基因的如本文所述的编码多肽的核酸。所述载体和/或颗粒可用于在体外或体内两者之一中将任意核酸转移至细胞中的目的。病毒载体的多种形式在本领域中是已知的。
[0329]“重组载体”是指包括异源核酸序列或能够在体内表达的“转基因”的载体。应当理解,在任意方面的一些实施方式中,本文所述的载体可与其它合适的组合物和疗法组合。在任意方面的一些实施方式中,载体是附加型的。合适的附加型载体的使用提供了在受试者中以高拷贝数的染色体外dna维持感兴趣的核苷酸的手段,从而消除染色体整合的潜在影响。在任意方面的一些实施方式中,所述载体是重组的(例如它包含源自至少两个不同来源的序列)。在任意方面的一些实施方式中,所述载体包含源自至少两个不同物种的序列。在任意方面的一些实施方式中,所述载体包含源自至少两个不同基因的序列,例如它包含融合蛋白或编码表达产物的核酸,所述核酸与至少一个非天然(例如异源)遗传控制元件(例如启动子、抑制子、激活子、增强子、反应元件等)可操作地连接。
[0330]
如本文所用,术语“异源的”是指源自外来物种的核酸序列或多肽,或者如果来自相同物种,则其原始形式基本上被修饰。
[0331]
在任意方面的一些实施方式中,本文所述的载体或核酸是密码子优化的,例如核酸序列的天然或野生型序列已被改变或工程化以包括替代密码子,从而使得改变的或工程化的核酸编码与天然/野生型序列相同的多肽表达产物,但将在期望的表达系统中以改善的效率进行转录和/或翻译。在任意方面的一些实施方式中,表达系统是除天然/野生型序列(或从此类生物体获得的细胞)的来源之外的生物体。在任意方面的一些实施方式中,本文所述的载体和/或核酸序列是密码子优化的,以在哺乳动物或哺乳动物细胞(例如小鼠、小鼠细胞或人细胞)中表达。在任意方面的一些实施方式中,本文所述的载体和/或核酸序列是密码子优化的,以在人细胞中表达。在任意方面的一些实施方式中,本文所述的载体和/或核酸序列是密码子优化的,以在酵母或酵母细胞中表达。在任意方面的一些实施方式中,本文所述的载体和/或核酸序列是密码子优化的,以在细胞中表达。在任意方面的一些实施方式中,本文所述的载体和/或核酸序列是密码子优化的,以在大肠杆菌(e.coli)细胞中表达。
[0332]
如本文所用,术语“表达载体”是指指导由与载体上的转录调控序列连接的序列表达rna或多肽的载体。表达的序列通常但不必须与细胞为异源的。表达载体可包含附加的元件,例如表达载体可具有两个复制系统,从而允许其在两种生物体中维持(例如在人细胞中用于表达和在原核宿主中用于克隆和扩增)。
[0333]
术语“调控序列”旨在包括启动子、增强子和其它表达控制元件(例如聚腺苷酸化信号),从而控制与其可操作地连接的基因的转录或翻译。在例如goeddel;gene expression technology.methods in enzymology 185,academic press,san diego,calif.(1990)中描述了此类调控序列。用于哺乳动物宿主细胞表达的调控序列的实例包括指导在哺乳动物细胞中高水平蛋白质表达的病毒元件,例如源自巨细胞病毒(cmv)、猿猴病
毒40(sv40)、腺病毒(例如腺病毒主要晚期启动子(admlp))和多瘤病毒的启动子和/或增强子。或者,可使用非病毒调控序列,例如泛素启动子、延伸因子1-α1(eef1a1)启动子或β-珠蛋白启动子。真核启动子是位于基因上游的dna调控区域,其结合转录因子ii d(tfiid)并允许转录起始复合物的组分的后续协调,促进rna聚合酶ii的募集和转录的起始。具有复杂启动子的基因可能会选择性地利用调控元件(例如增强子和沉默子),允许根据需要进行不同水平的表达。
[0334]
如本文所用,术语“治疗(treat/treatment/treating)”或“缓解(amelioration)”是指治疗性治疗,其中目的是逆转、减轻、缓解、抑制、减慢或停止与疾病或紊乱相关的病症的进展或严重程度,例如肺部感染和/或肺部炎症。术语“治疗”包括减少或减轻病症相关的病症、疾病或紊乱的至少一种副作用或症状。如果一种或多种症状或临床标志物减少,治疗通常是“有效的”。或者,如果疾病的进展减少或停止,治疗是“有效的”。也就是说,“治疗”不仅包括症状或标志物的改善,还包括与在没有治疗的情况下预期的情况相比,中止或至少减缓症状的进展或恶化。有益的或期望的临床结果包括但不限于减轻一种或多种症状、减小疾病程度、稳定(即不恶化)疾病状态、延迟或减缓疾病进展、缓解或缓和疾病状态、减退(无论是部分还是全部)和/或降低的死亡率,无论是可检测的还是不可检测的。疾病的术语“治疗”还包括提供疾病的症状或副作用的减轻(包括姑息治疗)。
[0335]
如本文所用,术语“药物组合物”是指与药学上可接受的运载体(例如制药工业中常用的载体)组合的活性剂。短语“药学上可接受的”在本文中用于指在合理医学判断范围内适合与人和动物组织接触使用而不会过度的毒性、刺激、过敏反应或其它问题或并发症,与合理的收益/风险比相称的那些化合物、材料、组合物和/或剂型。在任意方面的一些实施方式中,药学上可接受的运载体可为除水之外的运载体。在任意方面的一些实施方式中,药学上可接受的运载体可为乳膏、乳液、凝胶、脂质体、纳米颗粒和/或油膏。在任意方面的一些实施方式中,药学上可接受的运载体可为人工或工程化的运载体,例如活性成分在自然界中不被发现的运载体。
[0336]
如本文所用,术语“给予”是指通过使得在期望位点至少部分递送药剂的方法或途径将如本文所公开的化合物放置到受试者中。包含本文所公开的化合物的药物组合物可以通过在受试者中产生有效治疗的任何适当途径给予。在任意方面的一些实施方式中,给予包括人的身体活动,例如注射、摄取动作、涂抹动作和/或递送装置或机器的操作。此类活动可以例如由医学专业人员和/或被治疗的受试者进行。
[0337]
如本文所用,“接触”是指用于将药剂递送或暴露于至少一个细胞的任何合适方式。示例性递送方法包括但不限于直接递送至细胞培养基、灌注、注射或本领域技术人员公知的其它递送方法。在任意方面的一些实施方式中,接触包括人的身体活动(例如注射;分配、混合和/或倾析的行为);和/或操作递送设备或机器。
[0338]
术语“统计学上显著的”或“显著地”是指统计学显著性并且通常意指两个标准差(2sd)或更大的差异。
[0339]
除在操作实例中或在另外指明的情况下之外,本文使用的表示成分或反应条件的量的所有数字应理解为在所有情况下由术语“约”修饰。与百分比结合使用时,术语“约”可表示
±
1%。
[0340]
如本文所用,术语“包括/包含”意指除所呈现的定义的要素之外,还可存在其它的
protocols in molecular biology(cpmb),frederick m.ausubel(编著),john wiley and sons,2014(isbn 047150338x,9780471503385),current protocols in protein science(cpps),john e.coligan(编著),john wiley and sons,inc.,2005;以及current protocols in immunology(cpi)(john e.coligan,ada m kruisbeek,david h margulies,ethan m shevach,warren strobe,(编著)john wiley and sons,inc.,2003(isbn 0471142735,9780471142737);通过引用的方式将它们全部以其整体并入本文。
[0347]
其它术语在本文中本发明的各个方面的描述内定义。
[0348]
为了描述和公开的目的,以引用的方式将本技术全文所引用的所有专利和其它出版物(包括参考文献、颁发的专利、公布的专利申请和共同未决的专利申请)明确并入本文,例如此类出版物中描述的方法学可能与本文所述的技术结合使用。提供这些公开文本仅因为它们在本技术的申请日之前公开。在这方面的任何内容都不应被解释为承认因在先发明或任何其它原因而本发明人无权先于此类公开。所有关于日期的陈述或关于这些文件内容的表示均基于申请人可获得的信息,并不构成对这些文件的日期或内容的正确性的任何承认。
[0349]
本公开的实施方式的描述并非旨在是详尽的或将本公开限制为所公开的精确形式。虽然出于说明的目的本文中描述了本公开的特定实施方式和实例,但是如相关领域的技术人员将认识到的,在本公开的范围内各种等效修饰是可能的。例如,虽然方法步骤或功能以给定的顺序呈现,但替代实施方式可以以不同的顺序执行功能,或者可基本同时地执行功能。本文提供的本公开的教导可适当地应用于其它程序或方法。可组合本文描述的各种实施方式以提供进一步的实施方式。如果需要,可修改本公开的方面以采用以上参考文献和应用的组成、功能和概念来提供本公开的更进一步的实施方式。此外,出于生物功能等效性的考虑,可在不影响生物或化学活动的种类或量的情况下对蛋白质结构进行一些改变。根据详细描述,可对本公开做出这些和其它改变。所有这些修饰都旨在包括在所附权利要求的范围内。
[0350]
前述实施方式的任一个的特定要素可组合或替代其它实施方式中的要素。此外,虽然已经在这些实施方式的上下文中描述了与本公开的某些实施方式相关的优点,但其它实施方式也可展现出此类优点,并且并非所有实施方式都必须展现出此类优点以落入本公开的范围内。
[0351]
本文所述的技术的一些实施方式可根据以下编号段落中的任一项来定义:
[0352]
1.一种核酸序列,所述核酸序列包含
[0353]
a.至少一个异源调控序列,所述异源调控序列选自于造血增强子元件和用于hsc限制性mirna的mirna结合位点;以及
[0354]
b.编码gata结合因子1(gata1)多肽的序列。
[0355]
2.如段落1所述的核酸序列,所述核酸序列包含至少一个造血增强子元件。
[0356]
3.如段落2所述的核酸序列,其中,所述增强子元件包含与选自于由以下序列组成的组中的核苷酸序列具有至少80%同源性的序列:seq id no:10、seq id no:11、seq id no:12、seq id no:38和/或seq id no:39。
[0357]
4.如段落2所述的核酸序列,其中,所述增强子元件包含选自于由以下组成的组的基因的增强子元件:
[0358]
kell金属内肽酶(kel);5'氨基乙酰丙酸合酶2(alas2);和血型糖蛋白a(gypa)。
[0359]
5.如段落1-4中任一项所述的核酸序列,所述核酸序列包含用于至少一个hsc限制性mirna的至少一个mirna结合位点。
[0360]
6.如段落1-5中任一项所述的核酸序列,其中,所述用于至少一个hsc限制性mirna的至少一个mirna结合位点选自于由用于以下的mir结合位点所组成的组:mir10at、mir125、mir155、mir130at、mir142t、mir196bt、mir99、mir126mir126、mir181、mir193、mir223t、mir542和let7e。
[0361]
7.如段落1-6中任一项所述的核酸序列,所述核酸序列包含至少一个造血增强子元件以及用于至少一个hsc限制性mirna的至少一个mirna结合位点。
[0362]
8.如段落1-7中任一项所述的核酸序列,所述核酸序列进一步包含:
[0363]
a.异源5'utr,所述异源5'utr包含:
[0364]
i.除gata1以外的造血转录因子的5'utr序列,
[0365]
ii.至少20个核苷酸的序列,和/或
[0366]
iii.1-25个上游密码子uaug;和/或
[0367]
b.造血增强子微小基因。
[0368]
9.一种核酸序列,所述核酸序列包含
[0369]
a.5'utr,所述5'utr包含:
[0370]
i.除gata1以外的造血转录因子的5'utr序列;
[0371]
ii.至少20个核苷酸的序列;和/或
[0372]
iii.1-25个上游密码子uaug;
[0373]
b.编码gata结合因子1(gata1)多肽的序列。
[0374]
10.如段落1-9中任一项所述的核酸序列,其中,所述5'utr包含选自于由以下组成的组的基因的5'utr:runt相关转录因子1(runx1)、lim domain only 2(lmo2)或ets变体6(etv6)。
[0375]
11.如段落1-10中任一项所述的核酸序列,所述核酸序列进一步包含至少一个造血增强子元件、用于hsc限制性mirna的mirna结合位点和/或造血增强子微小基因(g1hem)。
[0376]
12.一种核酸序列,所述核酸序列包含:
[0377]
a.造血增强子微小基因(g1hem);
[0378]
b.编码gata结合因子1(gata1)多肽的序列。
[0379]
13.如段落12所述的核酸序列,其中,所述造血增强子微小基因(mg1hem)包含与核苷酸序列seq id no:13具有至少80%同源性的序列。
[0380]
14.如段落12-13中任一项所述的核酸序列,所述核酸序列进一步包含5'utr、和/或至少一个造血增强子元件;和/或用于hsc限制性mirna的至少一个mirna结合位点,
[0381]
所述5'utr包含:
[0382]
i.除gata1以外的造血转录因子的5'utr序列,
[0383]
ii.至少20个核苷酸的序列,和/或
[0384]
iii.1-25个上游密码子uaug。
[0385]
15.如段落14所述的核酸序列,其中,所述除gata1以外的造血转录因子的5'utr序列为选自于由以下组成的组的基因的5'utr序列:runt相关转录因子1(runx1);
[0386]
至少一个造血增强子元件;
[0387]
和/或用于hsc限制性mirna的至少一个mirna结合位点。
[0388]
16.如段落1-15中任一项所述的核酸序列,其中,所述用于至少一个hsc限制性mirna的结合位点包含选自于seq id no:31-seq id no:37和seq id no:43-seq id no:55的序列。
[0389]
17.如段落1-16中任一项所述的核酸序列,其中,所述造血增强子元件包含与选自于seq id no:10、seq id no:11、seq id no:12、seq id no:38和seq id no:39的序列具有至少80%序列同一性的序列。
[0390]
18.如段落1-17中任一项所述的核酸序列,其中,所述5'utr序列包含与选自于seq id no:14、seq id no:15和seq id no:16的序列具有至少80%序列同一性的序列。
[0391]
19.如段落1-18中任一项所述的核酸序列,其中,所述序列包含与a和b的元件可操作地连接的启动子。
[0392]
20.如段落19所述的核酸序列,其中,所述启动子不为gata1启动子。
[0393]
21.如段落20所述的核酸序列,其中,所述启动子包含延伸因子1-α1(eef1a1)的启动子序列。
[0394]
22.如段落1-21中任一项所述的核酸序列,其中,所述编码gata结合因子1(gata1)多肽的序列包含与编码人gata1多肽的核苷酸序列具有至少60%序列同一性的序列。
[0395]
23.如段落1-22中任一项所述的核酸序列,所述核酸序列进一步包含:
[0396]
与编码所述gata1多肽的序列可操作地连接的转录后调控元件。
[0397]
24.如段落23所述的核酸序列,其中,所述转录后调控元件包括土拨鼠肝炎病毒转录后调控元件(wpre)。
[0398]
25.如段落1-24中任一项所述的核酸序列,所述核酸序列进一步包含内部核糖体进入位点。
[0399]
26.如段落25所述的核酸序列,其中,所述内部核糖体进入位点与标志物基因可操作地连接,并且其中,所述标志物基因编码光学可见的蛋白质或酶。
[0400]
27.如段落1-26中任一项所述的核酸序列,其中,所述序列包含选自于seq id no:8、seq id no:9、seq id no:61和seq id no:62的序列。
[0401]
28.如段落1-27中任一项所述的核酸序列,其中,所述核酸序列为载体。
[0402]
29.如段落28所述的核酸序列,其中,所述载体为质粒、或腺病毒载体、慢病毒载体或逆转录病毒载体。
[0403]
30.一种包含如段落1-30中任一项所述的核酸序列的慢病毒颗粒。
[0404]
31.一种组合物,所述组合物包含如段落1-31中任一项所述的核酸序列或颗粒以及药学上可接受的运载体。
[0405]
32.一种治疗有需要的受试者中的diamond-blackfan贫血的方法,所述方法包括向所述患者给予治疗有效量的如段落1-31中任一项所述的核酸序列、颗粒或组合物。
[0406]
33.一种恢复早期红系祖细胞细胞特异性gata1表达的方法,所述方法包括使包含早期红系祖细胞的细胞群与如段落1-31中任一项所述的核酸序列、颗粒或组合物接触。
[0407]
34.如段落33所述的方法,其中,所述早期红系祖细胞包含dba相关的基因突变。
[0408]
本文描述的技术的一些实施方式可根据以下编号段落中的任一项来定义:
[0409]
1.一种核酸序列,所述核酸序列包含
[0410]
a.至少一个异源调控序列,所述异源调控序列选自于造血增强子元件和用于hsc限制性mirna的mirna结合位点;以及
[0411]
b.编码gata结合因子1(gata1)多肽的序列。
[0412]
2.如段落1所述的核酸序列,所述核酸序列包含至少一个造血增强子元件。
[0413]
3.如段落2所述的核酸序列,其中,所述增强子元件包含与选自于由以下序列所组成的组中的核苷酸序列具有至少80%同源性的序列:seq id no:10、seq id no:11、seq id no:12、seq id no:38和/或seq id no:39。
[0414]
4.如段落2所述的核酸序列,其中,所述增强子元件包含选自于由以下所组成的组的基因的增强子元件:
[0415]
kell金属内肽酶(kel);5'氨基乙酰丙酸合酶2(alas2);和血型糖蛋白a(gypa)。
[0416]
5.如段落1-4中任一项所述的核酸序列,所述核酸序列包含用于至少一个hsc限制性mirna的至少一个mirna结合位点。
[0417]
6.如段落1-5中任一项所述的核酸序列,其中,所述用于至少一个hsc限制性mirna的至少一个mirna结合位点选自于由用于以下的mir结合位点所组成的组:mir10at、mir125、mir155、mir130at、mir142t、mir196bt、mir99、mir126mir126、mir181、mir193、mir223t、mir542和let7e。
[0418]
7.如段落1-6中任一项所述的核酸序列,所述核酸序列包含至少一个造血增强子元件以及用于至少一个hsc限制性mirna的至少一个mirna结合位点。
[0419]
8.如段落1-7中任一项所述的核酸序列,所述核酸序列进一步包含:
[0420]
a.异源5'utr,所述异源5'utr包含:
[0421]
i.除gata1以外的造血转录因子的5'utr序列,
[0422]
ii.至少20个核苷酸的序列,和/或
[0423]
iii.1-25个上游密码子uaug;和/或
[0424]
b.造血增强子微小基因。
[0425]
9.一种核酸序列,所述核酸序列包含:
[0426]
a.5'utr,所述5'utr包含:
[0427]
i.除gata1以外的造血转录因子的5'utr序列,
[0428]
ii.至少20个核苷酸的序列,和/或
[0429]
iii.1-25个上游密码子uaug;
[0430]
b.编码gata结合因子1(gata1)多肽的序列。
[0431]
10.如段落1-9中任一项所述的核酸序列,其中,所述5'utr包含选自于由以下所组成的组的基因的5'utr:runt相关转录因子1(runx1)、lim domain only 2(lmo2)或ets变体6(etv6)。
[0432]
11.如段落1-10中任一项所述的核酸序列,所述核酸序列进一步包含至少一个造血增强子元件、用于hsc限制性mirna的mirna结合位点和/或造血增强子微小基因(g1hem)。
[0433]
12.一种核酸序列,所述核酸序列包含
[0434]
a.造血增强子微小基因(g1hem);
[0435]
b.编码gata结合因子1(gata1)多肽的序列。
[0436]
13.如段落12所述的核酸序列,其中,所述造血增强子微小基因(mg1hem)包含与核苷酸序列seq id no:13具有至少80%同源性的序列。
[0437]
14.如段落12-13中任一项所述的核酸序列,所述核酸序列进一步包含5'utr、和/或至少一个造血增强子元件、和/或用于hsc限制性mirna的至少一个mirna结合位点,
[0438]
所述5'utr包含:
[0439]
i.除gata1以外的造血转录因子的5'utr序列;
[0440]
ii.至少20个核苷酸的序列;和/或
[0441]
iii.1-25个上游密码子uaug。
[0442]
15.如段落14所述的核酸序列,其中,所述除gata1以外的造血转录因子的5'utr序列为选自于由以下所组成的组的基因的5'utr序列:runt相关转录因子1(runx1);
[0443]
至少一个造血增强子元件;
[0444]
和/或用于hsc限制性mirna的至少一个mirna结合位点。
[0445]
16.如段落1-15中任一项所述的核酸序列,其中,所述用于至少一个hsc限制性mirna的结合位点包含选自于seq id no:31-seq id no:37和seq id no:43-seq id no:55的序列。
[0446]
17.如段落1-16中任一项所述的核酸序列,其中,所述造血增强子元件包含与选自于seq id no:10、seq id no:11、seq id no:12、seq id no:38和seq id no:39的序列具有至少80%序列同一性的序列。
[0447]
18.如段落1-17中任一项所述的核酸序列,其中,所述5'utr序列包含与选自于seq id no:14、seq id no:15和seq id no:16的序列具有至少80%序列同一性的序列。
[0448]
19.如段落1-18中任一项所述的核酸序列,其中,所述序列包含与a和b的元件可操作地连接的启动子。
[0449]
20.如段落19所述的核酸序列,其中,所述启动子不为gata1启动子。
[0450]
21.如段落20所述的核酸序列,其中,所述启动子包含延伸因子1-α1(eef1a1)的启动子序列。
[0451]
22.如段落1-21中任一项所述的核酸序列,其中,所述编码gata结合因子1(gata1)多肽的序列包含与编码人gata1多肽的核苷酸序列具有至少60%序列同一性的序列。
[0452]
23.如段落1-22中任一项所述的核酸序列,所述核酸序列进一步包含:
[0453]
与编码所述gata1多肽的序列可操作地连接的转录后调控元件。
[0454]
24.如段落23所述的核酸序列,其中,所述转录后调控元件包括土拨鼠肝炎病毒转录后调控元件(wpre)。
[0455]
25.如段落1-24中任一项所述的核酸序列,所述核酸序列进一步包含内部核糖体进入位点。
[0456]
26.如段落25所述的核酸序列,其中,所述内部核糖体进入位点与标志物基因可操作地连接,并且其中,所述标志物基因编码光学可见的蛋白质或酶。
[0457]
27.如段落1-26中任一项所述的核酸序列,其中,所述序列包含选自于seq id no:8、seq id no:9、seq id no:61和seq id no:62的序列。
[0458]
28.如段落1-27中任一项所述的核酸序列,其中,所述核酸序列为载体。
[0459]
29.如段落28所述的核酸序列,其中,所述载体为质粒、或腺病毒载体、慢病毒载体
或逆转录病毒载体。
[0460]
30.一种包含如段落1-30中任一项所述的核酸序列的慢病毒颗粒。
[0461]
31.一种组合物,所述组合物包含如段落1-31中任一项所述的核酸序列或颗粒以及药学上可接受的运载体。
[0462]
32.一种治疗有需要的受试者中的diamond-blackfan贫血的方法,所述方法包括向患者给予治疗有效量的如段落1-31中任一项所述的核酸序列、颗粒或组合物。
[0463]
33.一种恢复早期红系祖细胞细胞特异性gata1表达的方法,所述方法包括使包含早期红系祖细胞的细胞群与如段落1-31中任一项所述的核酸序列、颗粒或组合物接触。
[0464]
34.如段落33所述的方法,其中,所述早期红系祖细胞包含dba相关的基因突变。
[0465]
35.如段落1-31中任一项所述的核酸序列、颗粒或组合物用于治疗有需要的受试者中的diamond-blackfan贫血的用途。
[0466]
本文描述的技术通过以下实施例进一步说明,这些实施例绝不应被解释为进一步限制。
[0467]
实施例
[0468]
实施例1:使用gata1基因疗法治疗dba的方法
[0469]
diamond-blackfan贫血(dba),也称为先天性发育不良性贫血,是1938年首次描述的病症,且其特征在于患者骨髓中缺乏红血细胞祖细胞和前体细胞,而造血作用的所有其它方面以表面上正常的方式发生(1,2)。估计每100,000至200,000例活产婴儿中大约有1例出现dba(3),尽管考虑到许多被发现具有可变表达能力或可能被误诊的个体,这可能低估了。几十年来,dba的诊断主要基于临床标准进行,并辅以生物标志物红细胞腺苷脱氨酶的使用,该酶在~80%的dba患者中升高(3)。
[0470]
经过跨越1990年代的大部分时间的广泛绘制工作,1999年通过鉴定在19号染色体上具有易位的个体发现了第一个在dba中发生突变的基因(4)。令人惊讶的是,在大约20%-25%的dba病例中,在这个最初的突变基因(该基因是泛在表达的核糖体蛋白(rp)基因rps19)中鉴别出杂合性功能丧失突变(heterozygous loss of function mutations)。这立即引发了很多关于潜在机制的猜测,以及是否可能参与rps19的核糖体或非核糖体作用。许多随后的研究表明,由于rp单倍不足,受损的核糖体生物发生似乎是导致此种表型的主要因素,表明了核糖体活性/水平在此种表型中的作用(5)。然而,该紊乱的红系特异性的潜在基础仍然是个谜。
[0471]
在dba患者的同期群(cohort)中的后续研究采用靶向测序、使用单核苷酸多态性微阵列/比较基因组杂交评估拷贝数变异或全外显子组测序,揭示了总共19个不同的rp具有杂合性功能丧失突变,该突变导致rp单倍不足(6,7)。总的来说,这些突变解释了大约60%-80%的dba病例的病因。这19个rp基因突变不均匀地分布在整个核糖体中,并且涉及核糖体的大亚基(60s)和小亚基(40s)两者。核糖体的特定结构区域没有突变的聚集(8)。最近,通过在超过450名诊断为dba的患者的同期群上的全外显子组测序,本发明人已鉴别出另外7个rp基因突变,使与该紊乱有关的rp基因总数达到26个,共同解释了大约80%的dba病例潜在的基础(构成核糖体的rp的近1/3)(9)。
[0472]
尽管在了解dba的大部分遗传原因方面取得了进展,但仍存在两个主要限制。尽管关于大多数dba病例中的杂合性rp功能缺失突变有强有力的发现结果,但这如何能导致dba
中红系特异性造血缺陷仍然成谜(10)。其次,目前可用于治疗dba患者的疗法非常有限(3,10)。一些患者对皮质类固醇有反应,但通常存在明显的副作用,限制了该疗法在大多数患者中的长期有效性。许多患者需要长期红血细胞输注,这可能与严重且难以控制的铁过载有关。最后,一些患者可通过使用同种异体的骨髓移植治愈,但鉴于在这种情况下非亲缘关系的供体移植表现出的不良结果,通常这仅限于那些有匹配的同胞供体的患者(11)。迄今为止,仅开发了有限的候选实验疗法,并且遗憾的是,许多在后期的临床前或临床研究中并未显示出稳健的功效(12)。因此,迫切需要新的和改善的dba疗法,这种疗法可对患有这种病症的大多数患者有效,该病症由于主要影响rp基因的大量不同的突变所引起。
[0473]
考虑到这些局限性,本发明人推断通过人类遗传学结合机械跟踪的使用对dba进一步研究可让我们进一步了解这种紊乱,并允许我们确定改善的治疗策略。本发明人随后鉴别出了该紊乱中的第一个非rp基因突变。本发明人鉴别出数名诊断为dba的患者具有损害造血主转录因子gata1的长蛋白形式产生的突变(13)。随后也报道了数名其它具有类似突变类型的患者(14-16)。虽然这些发现表明gata1突变可能引起类似于dba的表型,但更常见的rp基因突变与gata1突变之间是否存在分子联系尚不清楚。
[0474]
本发明人测试了rp单倍不足(dba的最常见病因)是否会改变gata1翻译。本发明人可以证明使用在rp单倍不足的背景下gata1mrna翻译受损的dba患者样品中以及原代人造血干细胞和祖细胞(hspc)中的两种rp抑制,而各种其它红系重要转录本在这种情况下在它们的翻译方面不受影响(15)。此外,本发明人证明了通过慢病毒表达增加gata1蛋白水平足以挽救来自具有各种rp基因突变的dba患者的单核细胞中存在的红系分化缺陷(达到在正常个体中所见的水平)。这些结果产生了如图1所示的关于dba的发病机制的模型。
[0475]
然而,仍然存在许多问题。(1)目前尚不清楚在rp单倍不足的背景下核糖体具体是如何被改变的。在这种情况下,核糖体的组成可能会发生变化,尽管在这种状况下发现的28个不同的rp突变使这看起来不太可能。另一种,虽然并不相互排斥,但在rp单倍不足的背景下,但可能是核糖体水平降低。(2)超出最初研究中专门测试的转录本的转录本范围以及这些转录本的共同特征尚不清楚。(3)出现这些缺陷的造血阶段也不清楚。
[0476]
然后,本发明人采用核糖体谱分析方法以在基因组水平上更好地了解哪些转录本受到由于dba相关的分子病变引起的这种核糖体水平降低的影响(19,20)。本发明人能够从正在经历红系谱系定型(红系分化功能缺陷出现的阶段)的rp单倍不足hspc获得高质量的核糖体分析数据。重要的是,通过对该数据的分析,本发明人可以证实,在rp单倍不足的背景下(类似于rps19或rpl5阻抑),约500个转录本的有限组显示出最显著的翻译效率变化。与本发明人早期从多核糖体分析中得到的靶向发现一致,在翻译效率方面,gata1 mrna是下调最大的转录本之一。有趣的是,显示翻译下调的大多数其它转录本是核糖体或核糖体相关因子的所有组分,包括所有rp和各种翻译起始和延伸因子。通过使用基因表达的cap分析进行进一步分析来定义这些转录本的5'非翻译区域(utr),本发明人可以证实那些在基系时翻译程度最高且具有短且非结构化5'utr的转录本趋向于成为在rp单倍不足的背景下在翻译水平上下调的转录本。有趣的是,在所有造血主转录因子中,只有gata1具有短的5'utr,并且本发明人可证实用其它主调控子(如runx1、lmo2或etv6)的那些5'utr替换该5'utr改变了这个关键的造血转录因子的翻译。
[0477]
最后,本发明人还证明了这在dba患者体内发生,并且本发明人评估了出现这些病
变出现的造血作用阶段。本发明人通过骨髓活检标本中gata1的免疫组织化学和使用细胞内流式细胞术两者均表明dba患者的造血祖细胞中gata1水平减少。重要的是,本发明人证明了与对照样品相比,即使在其中具有gata1最早表达的来自dba患者骨髓细胞的非常原始的cd34+cd38-hspc上,gata1水平也减少(图3)。此外,本发明人发现即使gata1水平在更成熟的cd34+cd38+hspc中增加,dba患者细胞中的gata1水平继续降低。这些结果与造血谱系定型发生在干细胞和祖细胞最原始阶段的出现模式一致,并证明了这些发现与人类疾病的相关性(21-23)。
[0478]
所有这些机制发现对于提高对dba发病机制的理解具有重要意义。然而,如何为dba开发更好的疗法仍然存在挑战。如上所讨论,目前唯一可用的疗法是长期使用皮质类固醇、定期血液输注或同种异体造血干细胞移植(10)。替代的且有价值的方法是将自体造血干细胞移植与基因疗法联用(24)。事实上,已经尝试开发慢病毒载体以增加rps19的产生(25)。鉴于dba患者中存在多效性rp基因突变(迄今为止已鉴别出28个突变),难以想象这种方法如何对大多数患者有用。鉴于本发明人发现gata1蛋白产生受损是所有dba病例的基础,并且增加gata1蛋白足以挽救这些患者中存在的红系分化缺陷,开发gata1基因疗法是实现dba患者治愈性治疗的有价值的方法。如下文详细讨论的,主要限制是造血干细胞(hsc)区室中gata1的表达将引起干细胞早熟分化,并且需要调控终末红细胞生成过程中gata1的表达。
[0479]
虽然在来自dba患者的hspc中gata1蛋白水平受到阻抑并且增加gata1表达可缓解dba的红系谱系定型缺陷特征,但gata1的失调表达可能是有问题的。用外源性gata1表达可能使hsc经历早熟分化,并且有效的终末红细胞生成需要gata1水平的调控。
[0480]
基于本发明人的机理研究,开发用于治疗dba的gata1基因疗法是引人注目的,并且似乎是有前途的方法。本发明人已经能够证明,增加gata1表达可挽救来自dba患者的原代hspc中的红系分化缺陷,这些dba患者在各种rp基因中具有各种分子病变。此外,本发明人还能够表明,他们可通过基于rna干扰的方法在建模与原代hspc中的各种dba相关分子病变中有规律地产生相同的结果(15,17)。在这些情况下,增加的gata1表达通过慢病毒的使用而实现,其中包含改变的5'utr和3'utr元件的gata1 cdna处于慢病毒ltr的转录控制下,该ltr显示出高水平和泛在的表达。出于治疗目的,此类表达必须在分化过程的各个阶段进行调控和调整。必须控制gata1水平以避免任何造血作用的干扰。
[0481]
先前的研究表明,小鼠hsc中gata1的外源性不受调控的表达可促进向巨核细胞和红系谱系的早熟分化,同时阻止能够长期植入的自我更新hsc的维持(26,27)。事实上,外源性gata1表达可重新编程其它造血谱系以承担红系命运(26)。然而,gata1转基因受调控的表达可允许长期维持hsc(27)。为了在人类环境中支持这些发现,本发明人利用了无血清培养系统,该系统允许在培养的几天过程中维持长期植入的人hsc(能够植入免疫缺陷异种移植受体)。在这种背景下,由慢病毒ltr元件调控的外源性gata1表达的引入引起这些细胞的早熟分化,而对照细胞保持其表型和功能能力以产生长期造血移植。这些发现扩展了先前发表的小鼠模型结果(26)。这些结果还共同强调需要阻止早期hsc中的gata1表达以允许有效植入,这是治愈性慢病毒基因疗法所必需的。此外,在终末红系分化期间gata1水平不能过度升高,因为这会损害有效的红细胞生成(28)。为了解决这些问题,本发明人进行了一系列研究以鉴别将允许由慢病毒载体而来的gata1受调控表达的关键调控元件。
[0482]
为了实现用于有效基因疗法的gata1的调控表达,本发明人采用两种互补和协同的方法来确保不会有潜在有害的异位表达,同时还在红系分化期间调控gata1的水平。本文中预期可单独使用任一方法,或者它们可组合使用。
[0483]
基因疗法载体中使用的第一调控元件是gata1造血增强子微小基因(g1hem),所述gata1造血增强子微小基因连接4个不同的调控元件以在造血作用中实现gata1的忠实表达(27,29)。这些元件包括-3kb造血增强子、上游双gata基序、上游caccc盒和gata1的第一内含子的区段。事实上,此微小基因中存在的979个核苷酸足以适当地驱动gata1 cdna表达以挽救gata1基因敲除小鼠并允许表面上正常的红细胞生成。
[0484]
为了开发临床上可用并涉及上述讨论的第一转录调控元件的gata1表达载体,本发明人利用已在人类临床研究中被证明有效的安全且设计良好的载体。在多种人造血细胞类型中表现出受控和良好调控的外源性cdna表达并已用于临床环境(30)的prrl.ppt.efs载体就是这样一种载体。g1hem可整合到gata1 cdna的上游,该gata1 cdna由内源性启动子或由修饰的(缩短的)泛在ef1α启动子(efs)来双双驱动,这作为替代和互补的方法。重要的是,如上所讨论,来自小鼠的g1hem中包含的gata1调控元件能够仅在gata1正常表达的细胞类型中驱动标志物基因的调控表达,并且足以允许使用gata1 cdna适当挽救敲除小鼠(27,31)。
[0485]
本发明人已经生产了总共4种不同的载体(图6中所示的2种,两种小鼠和人调控元件用于所有情况)。本发明人在gata1 cdna之后并入了自剪切2a肽(p2a)元件,然后是venus荧光标志物,以便能够实时地迅速跟踪那些表达gata1的细胞。使用流式细胞测定量化了在测试的各种造血细胞类型中看到的venus表达的程度。可通过对特定群体进行细胞分选来评估正常表达这种转录因子的细胞类型中gata1表达的增加程度。最后,使用这种原代细胞培养方法,本发明人可评估随gata1表达而发生的表型变化(32-34)。这种有力的方法允许本发明人使用与体内造血作用的过程直接相关的改进方法同时确定有效性、特异性和对造血分化的影响。每个载体都在2-3个独立的原代人造血细胞样本中进行测试,以弄清表达的特异性和有效性。
[0486]
虽然上面讨论的构成g1hem的转录调控元件允许gata1 cdna受调控的表达,但研究表明,使用该调控元件在hsc区室中可能存在泄漏表达(27)。由于这可能会严重影响获得长期植入的能力(26),因此必须防止在hsc区室中的表达。为了实现这一点,本发明人在土拨鼠肝炎病毒(pre)的转录后调控元件之后(例如在经修饰的prrl.ppt.ees衍生物中),并入了第二基因调控元件hsc限制性microrna(mir)的结合元件mir126。在pre之后插入三个重复的mir126结合元件阻止转基因在hsc区室中的表达。同样地,本发明人还用g1hem和gata1cdna修饰prrl.ppt.efs以包括这些mir126元件。在原代人造血细胞中进行体外测试以确保有效和选择性的表达。将要被移植到nod.cg-kitw-41j tyr+prkdcscid i12rgtm1wjl(nbsgw)小鼠模型中的hsc可被转导,该模型先前已成功并广泛用于生产人造血异种移植模型(36)。然后可在植入16周后使用表型标志物量化、二次移植到nbsgw受体中以及通过评估表型hsc区室中的venus表达来测试hsc功能。
[0487]
本文描述了临床级慢病毒载体的开发,该载体允许gata1 cdna受调控的表达以在基因疗法中使用。原代人造血细胞中的体外和体内研究允许筛选多个独立的载体,这些载体并入了mir126结合元件和转录调控元件(g1hem或其衍生物)的关键组二者。
[0488]
参考文献:
[0489]
1.nathan dg,clarke bj,hillman dg,alter bp,housman de.erythroid precursors in congenital hypoplastic(diamond-blackfan)anemia.the journal of clinical investigation.1978;61(2):489-98.doi:10.1172/jci108960.pubmed pmid:621285;pmcid:pmc372560.
[0490]
2.iskander d,psaila b,gerrard g,chaidos a,en foong h,harrington y,kamik lc,roberts i,de la fuente j,karadimitris a.elucidation of the ep defect in diamond-blackfan anemia by characterization and prospective isolation of human eps.blood.2015;125(16):2553-7.doi:10.1182/blood-2014-10-608042.pubmed pmid:25755292.
[0491]
3.vlachos a,ball s,dahl n,alter bp,sheth s,ramenghi u,meerpohl j,karlsson s,liu jm,leblanc t,paley c,kang em,leder ej,atsidaftos e,sbimamura a,bessler m,glader b,lipton jm,participants of sixth annual daniella maria arturi international consensus c.diagnosing and treating diamond blackfan anaemia:results of an international clinical consensus conference.br j haematol.2008;142(6):859-76.doi:10.1111/j.1365-2141.2008.07269.x.pubmed pmid:18671700;pmcid:pmc2654478.
[0492]
4.draptchinskaia n,gustavsson p,andersson b,pettersson m,willig tn,dianzani i,ball s,tchernia g,klar j,matsson h,tentler d,mohandas n,carlsson b,dahl n.the gene encoding ribosomal protein s19is mutated in diamond-blackfananaemia.nat genet.1999:21(2):169-75.doi:10.1038/5951.pubmed pmid:9988267.
[0493]
5.flygare j,karlsson s.diamond-blackfan anemia:erythropoiesis lost in translation.blood.2007:109(8):3152-4.doi:10.1182/blood-2006-09-001222.pubmed pmid:17164339.
[0494]
6.mirabello l,khincha pp,ellis sr,giri n,brodie s,chandrasekharappa sc,donovan fx,zhou w,hicks bd,boland jf,yeager m,jones k,zhu b,wang m,alter bp,savage sa.novel and known ribosomal causes of diamond-blackfan anaemia identified through comprehensive genomic characterisation.j med genet.2017.doi:10.1136/jmedgenet-2016-104346.pubmed pmid:28280134.
[0495]
7.landowski m,o
′
donohue mf,buros c,ghazvinian r,montel-lehry n,vlachos a,sieff ca,newburger pe,niewiadomska e,matysiak m,glader b,atsidaftos e,lipton jm,beggs ah,gleizes pe,gazda ht.novel deletion of rpl15identified by array-comparative genomic hybridization in diamond-blackfan anemia.hum genet.2013;132(11):1265-74.doi:10.1007/s00439-013-1326-z.pubmed pmid:23812780;pmcid:pmc3797874.
[0496]
8.khatter h,myasnikov ag,natehiar sk,klaholz bp.structure of the human 80s ribosome.nature.2015;520(7549):640-5.doi:10.1038/nature14427.pubmed pmid:25901680.
[0497]
9.ulirseh jc,verboon jm,kazerounian s,guo mh,yuan d,ludwig ls,handsaker re,abdulhay nj,fiorini c,genovese g,lim et,cheng a,cummings bb,chao kr,beggs ah,genetti ca,sieff ca,newburger pe,niewiadomska e,matysiak m,vlachos a,lipton jm,atsidaftos e,glader b,narla a,gleizes pe,o
′
donohue mf,montel-lehry n,amor dj,mccarroll sa,o
′
donnell-luria ah,gupta n,gabriel sb,macarthur dg.lander es,lek m,da costa l,nathan dg,korostelev aa,do r,sankaran vg,gazda ht.the genetic landscape of diamond-blackfan anemia.am j hum genet.2018;103(6):930-47.doi:10.1016/j.ajhg.2018.10027.pubmed pmid:30503522.
[0498]
10.lipton jm,ellis sr.diamond-blackfan anemia:diagnosis,treatment,and molecular pathogenesis.hematology/oncologyclinics of north america.2009;23(2):261-82.doi:10.1016/i.hoc.2009.01.004.pubmed pmid:19327583;pmcid:pmc2886591.
[0499]
11.roy v,perez ws,eapen m,marsh jc,pasquini m,pasquini r,mustafa mm.bredeson cn,non-malignant marrow disorders working committee of the international bone marrow transplant r.bone marrow transplantation for diamond-blackfan anemia.biol blood marrow transplant.2005;11(8):600-8.doi:10.1016/j.bbmt.2005.05.005.pubmed pmid:16041310.
[0500]
12.narla a,vlachos a,nathan dg.diamond blackfan anemia treatment:past,present,and future.semin hematol.2011;48(2):117-23.doi:10.1053/j.seminhematol.2011.01.004.pubmed pmid:21435508;pmcid:pmc3073777.
[0501]
13.sankaran vg,ghazvinian r,dor,thiru p,vergilio ja,beggs ah,sieff ca.orkin sh,nathan dg.lander es,gazda ht.exome sequencing identifies gatal mutationsresulting in diamond-blackfan anemia.the journal of clinical investigation.2012;122(7):2439-43.doi:10.1172/jci63597.pubmed pmid:22706301;pmcid:pmc3386831.
[0502]
14.parrella s,aspesi a,quarello p,garelli e,pavesi e,carando a,nardi m,ellis sr,ramenghi u,dianzani i.loss of gata-l full length as a cause of diamond-blackfan anemia phenotype.pediatr blood cancer.2014:61(7):1319-21.doi:10.1002/pbc.24944.pubmed pmid:24453067;pmcid:pmc4684094.
[0503]
15ludwig ls,gazda ht,eng jc,eichhorn sw,thiru p,ghazvinian r,george ti,gotlib jr,beggs ah,sieffca,lodish hf,lander es,sankaran vg.altered translation ofgatal in diamond-blackfan anemia.nature medicine.2014;20(7):748-53.doi:10.1038/nm.3557.pubmed pmid:24952648;pmcid:pmc4087046.
[0504]
16klar j,khalfallah a,arzoo ps,gazda ht,dahl n.recurrent gata1 mutations in diamond-blackfan anaemia.br j haematol.2014;166(6):949-51.doi:10.1111/bjh.12919.pubmed pmid:24766296.
[0505]
17.khajuria rk,munschauer m,ulirsch jc,fiorini c,ludwigls,mcfarlandsk,abdulhay nj,specht h,keshishian h,mani dr,jovanovic m,ellis sr,fulco cp,engreitz jm,schutz s,lian j,gripp kw,weinberg ok,pinkus gs.gehrke l,
converts lymphoid and myelomonocytic progenitors into the megakaryocyte/erythrocyte lineages.immunity.2003;19(3):451-62.pubmed pmid:14499119.
[0515]
27.takai j,moriguchi t,suzuki m,yu l,ohneda k,yamamoto m.the gata1 5
′
region harbors distinct cis-regulatory modules that direct gene activation in erythroid cells and gene inactivation in hscs.blood.2013;122(20):3450-60.doi:10.1182/blood-2013-01-476911.pubmed pmid:24021675.
[0516]
28.whyatt d,lindeboom f,karis a,ferreira r,milot e,hendriks r,de bruijn m,langeveld a,gribnau j,grosveld f,philipsen s.an intrinsic but cell-nonautonomous defect in gata-1-overexpressing mouse erythroid cells.nature.2000;406(6795):519-24.doi:10.1038/35020086.pubmed pmid:10952313.
[0517]
29.ohneda k,shimizu r,nishimura s,muraosa y,takahashi s,engel jd,yamamoto m.a minigene containing four discrete cis elements recapitulates gata-1 gene expression in vivo.genes cells.2002;7(12):1243-54.pubmed pmid:12485164.
[0518]
30.schambach a,bohne j,chandra s,will e,margison gp,williams da,baum c.equal potency of gammaretroviral and lentiviral sin vectors for expression of o6-methylguanine-dna methyltransferase in hematopoietic cells.mol ther.2006;13(2):391-400.epub 2005/10/18.doi:10.1016/j.ymthe.2005.08.012.pubmed pmid:16226060.
[0519]
31.shimizu r,hasegawa a,ottolenghi s,ronchi a,yamamoto m.verification of the in vivo activity of three distinct cis-acting elements within the gatal gene promoter-proximal enhancer in mice.genes cells.2013;18(11):1032-41.epub 2013/10/15.doi:101111/gtc.12096.pubmed pmid:24118212.
[0520]
32.sankaran vg,ludwig ls,sicinska e,xu j,bauer de,eng jc,patterson hc.metcalf ra,natkunam y,orkin sh,sicinski p,lander es,lodish hf.cyclin d3 coordinatesthecellcycle during differentiation to regulate erythrocyte size and number.genes dev.2012;26(18):2075-87.epub 2012/08/30.doi:10.1101/gad.197020.112.pubmed pmid:22929040;pmcid:3444733.
[0521]
33.sankaran vg,menne tf,scepanovic d,vergilio ja,ji p,kim j,thiru p,orkin sh,lander es,lodish hf.microrna-15a and-16-1 act via myb to elevate fetalhemoglobin expression in human trisomy 13.proc natl acad sci u s a.2011;108(4):1519-24.epub 2011/01/06.doi:10.1073/pnas.1018384108pubmed pmid:21205891;pmcid:3029749.
[0522]
34.sankaran vg,xu j,byron r,greisman ha,fisher c,weatherall dj,sabath de,groudine m,orkin sh,premawardhena a,bender ma.a functional element necessary for fetal hemoglobin silencing.n engl j med.2011;365(9):807-14.epub 2011/09/02.doi:10.1056/nejmoal 103070.pubmed pmid:21879898;pmcid:3174767.
[0523]
35.gentner b,visigalli i,hiranatsu h,lechman e,ungari s,giustacchini a,schira g,amendola m,quattrini a,martino s,orlacchio a,dick je,biffi a,
naldini l.identification of hematopoietic stem cell-specific mirnas enables gene therapy of globoid cell leukodystrophy.sci transl med.2010;2(58):58ra84.doi:10.1126/scitranslmed.3001522.pubmed pmid:21084719.
[0524]
36.fiorini c,abdulhay nj,mcfarland sk,munschauer m,ulirsch jc,chiarle r,sankaran vg.developmentally-faithful and effective human erythropoiesis in immunodeficient and kit mutant mice.am j hematol.2017;92(9):e513-e9.doi:10.1002/ajh.24805.pubmed pmid:28568895;pmcid:pmc5546987.
[0525]
37.ito e,konno y,toki t,terui k.molecular pathogenesis in diamond-blackfan anemia.int j hematol.2010oct;92(3):413-8.
[0526]
实施例2:作为用于diamond-blackfan贫血的疗法而用于gata1谱系特异性表达的载体设计
[0527]
在任意方面的一些实施方式中,本文描述了以下慢病毒载体的各种组合(图7):
[0528]
1)慢病毒骨架:基于phiv-gfp的第三代自灭活慢病毒骨架(welm等,cell stem cell.2008jan 10.2(1):90-102),由ef1a启动子驱动并含有ires-gfp序列用于初始表征和测试,但将从最终载体序列中移除。
[0529]
2)小鼠gata1造血增强子微小基因(mg1hem):小鼠gata1转录起始位点上游的3个序列和来自小鼠gata1的第一内含子的第四序列的连结,这些序列已被证明忠实地允许gata1在红系细胞中而非造血干细胞中表达(takai等,blood.2013nov 14122(20):3450-3460)。
[0530]
3)最小启动子(minp):来自小鼠gata1的5
′
utr或来自萤火虫荧光素酶报告载体pgl4.25两者之一,genbank登录号dq904457.1。
[0531]
4)具有密码子优化的人gata1 cdna(gata1),用于在人细胞中进行最优表达,具有或不具有flag标签。
[0532]
5)土拨鼠肝炎病毒转录后调控元件(wpre),用于增强转基因mrna的稳定性。
[0533]
6)mir126结合位点(mir126 bs):重复序列,其与mir126结合(mir126是在造血干细胞中表达的microrna),并使得干细胞区室中转基因表达降低(gentner等,sci trans med.2010nov 172(58):58-84)。
[0534]
参考文献:
[0535]
welm et al cell stem cell.2008 jan 10.2(1):90-102.gentner et al.sci trans med.2010 nov 172(58):58-84.
[0536]
实施例3:作为用于diamond-blackfan贫血疗法的gata1基因疗法
[0537]
通过本发明人的临床前研究表明,红系细胞中的gata-1增强显示了对diamond-blackfan贫血(dba)的治疗效果。在此,本发明人展示了进一步实验的结果,这些实验证明红系前体中而非造血干细胞中gata1表达的受调控增加提供了在dba中的治疗效果。
[0538]
用于dba的临床相关gata1基因疗法载体必须实现四个关键功能
[0539]
(图27)。首先,尽管需要将基因疗法载体整合到长期的、未分化的造血干细胞(lt-hsc)的基因组中,但在干细胞区室中gata1转基因的表达必须很少,因为在hsc中的gata1表达导致自我更新干细胞的丢失。其次,为了克服作为dba标志的红系分化缺陷,一旦早期祖细胞致力于红系分化,基因疗法载体必须驱动在早期祖细胞中的稳健表达。第三,为了模拟
内源性gata1表达模式并实现正常的终末红系分化,基因疗法载体的表达应在红系发育后期下降。第四,发育上受调控增加的gata1表达必须足以克服实验模型系统和原代患者样品中由核糖体蛋白单倍不足引起的红系成熟阻滞。
[0540]
为了设计包含上述四个关键特征的载体,本发明人首先分析了gata1上游的可及性染色质的峰,并鉴别了在分化的红系细胞中而不是在hsc或其它早期祖细胞中开放的染色质。本发明人提供了证据,这些dna区域包含负责gata1的红系特异性表达的调控元件。本发明人通过将dna的3个区域与gata1上游的开放染色质连结,构建了人gata1增强子(hg1e)元件(图28a)。本发明人开发了通过在两个基因之间包含内部核糖体进入位点(ires)序列,使用hg1e元件来驱动gata1和gfp表达的载体。作为实现发育上受调控的转基因表达的额外机制,本发明人将hg1e元件与先前用于限制hsc区室中的转基因表达的mir223t结合位点组合。
[0541]
为了评估hg1e-gata1或hg1e-gata1-mir构建体是否能够驱动gata1表达的充分增加,本发明人使用了dba的体外模型。用靶向dba基因rps19的shrna载体感染原代人cd34+hspc,本发明人先前已经证明,该载体可模拟dba特有的体外红系分化缺陷。本发明人将红系比率定义为在红细胞生成条件下培养时表达红系标志物的细胞的比例。当与hg1e-gata1或hg1e-gata1-mir载体共感染时,在rps19敲低后,cd34+hspc的红细胞比率恢复到与用hmd-gata1载体组成型gata1过表达相当的水平,显示出dba表型的挽救(图28b)。作为hg1e-gata1和hg1e-gata1-mir载体可驱动足够的具有生理相关性的gata1表达的进一步证据,本发明人使用了缺乏内源性gata1表达的g1e鼠造血细胞系。用hg1e-gata1和hg1e-gata1-mir载体感染g1e细胞诱导终末红系分化,如通过ter119表达所测量的(图28c)。
[0542]
已经在红系祖细胞中实现了功能上充分增加的gata1表达,本发明人试图确定本发明人的新调控元件是否能够限制lt-hsc区室中的gata1表达,因为这些细胞中的gata1表达会损害骨髓中干细胞的维持。本发明人用hg1e-gata1或hg1e-gata1-mir载体感染cd34+hspc,并在能够在体外短期维持hsc的条件下培养它们。感染后两天,通过流式细胞术评估lt-hsc标志物的表面表达和gfp表达,以量化lt-hsc中的转基因表达。然后,将这些细胞转移到促进红系发育的介质中,并在分化的红系前体中测量gfp表达。与具有组成型gata1表达的hmd-gata1病毒相比,感染hg1e-gata1和hg1e-gata1-mir病毒的细胞中,红系细胞中gfp表达与hsc中gfp的比率(rbcgfp/hscgfp比率)显著增加(图28d)。增加的rbcgfp/hscgfp比率是由于hsc中实验载体的表达受限。这些数据表明,红系前体中受调控的、增加的gata1表达足以克服两种不同的体外dba模型中的分化阻滞,并且在lt-hsc区室中具有受限制的表达。gata1表达的这种发育忠实型的增加表明,基于受调控的gata1过表达的基因疗法可有望治愈diamond-blackfan贫血。
[0543]
为了进一步研究在发育中的红系细胞中来自hg1e-gata1载体的gata1的表达,本发明人使用三相培养系统在体外诱导人hspc分化为完全血红蛋白化、无核的红血细胞。在体外分化期间,发育中的红系祖细胞和前体首先表达高水平的转铁蛋白受体cd71。几天后,血型糖蛋白a(cd235a)高度表达,随后在终末分化的rbc中cd71表达丧失(图5a)。在用hmd-gata1或hg1e-gata1转导后,通过表达cd71的细胞百分比测量,与阴性对照相比,已经准备好进行红系细胞发育的细胞经历更快速的早期分化(图29b)。接下来,本发明人将终末分化的cd71-cd235a+亚群中的gfp表达与更原始的cd71+cd235a+亚群中的gfp表达进行了比较
(红细胞gfp/祖细胞gfp)。在终末分化的红细胞中,来自hg1e-gata1载体的gfp表达显著降低,忠实地概括了终末分化期间gata1表达降低的模式。值得注意但并非出乎意料的是,在hmd-gata1样品中未观察到这种降低的gfp表达,表明终末分化受损且gata1表达不受调控(图29c)。
[0544]
接下来,本发明人尝试通过使用crispr/cas9介导的rps19基因破坏来概括从健康成年供体分离的原代hspc中的rps19单倍不足。本发明人表明,rps19的有效编辑导致红系成熟阻滞,并且在早期红系培养期间表达cd71的细胞显著更少。然后,本发明人用hmd-空、hmd-gata1或hg1e-gata1病毒转导rps19编辑的hspc。培养第4天在致力于红系分化的细胞中(通过cd71表达测量),感染有hmd-gata1或hg1e-gata1病毒的群体具有更多的cd235表达(图30a),证实了gata1表达受调控的增加的能力,从而挽救如在dba中所见的由核糖体蛋白丧失所引起的红系分化中的阻滞。最后,在rps19编辑后甲基纤维素集落形成测定中检测到的红系集落显著减少,这部分地被hg1e-gata1挽救(图30b)。总之,本发明人的数据表明hg1e-gata1载体满足成为治愈dba的基因疗法所需的所有四个标准(图27)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1