桦木醇环烯烃衍生物及其用途和制备方法
1.本发明属于桦木醇环烯烃衍生物的合成领域,特别涉及一种桦木醇环烯烃衍生物及其用途和基于桦木醇烯烃衍生物的闭环复分解反应方法。
背景技术:
2.桦木醇是五环三萜类化合物,是中药桦树皮的主要成分,具有抗菌、抗病毒、抗肿瘤和抗炎等活性,已在食品、护肤品以及医药行业广泛应用。桦木醇衍生物具有类桦木醇的生物活性,已广泛用于设计并制备生物医用材料,有利于其高值化和功能化产物的开发和利用。
3.闭环复分解反应是一种制备聚烯烃材料的重要手段,该反应即分子内的烯烃复分解反应,含有两个碳碳不饱和键(一般为末端烯烃)的链状分子在金属卡宾的参与下发生复分解,伴随失去一分子烯烃得到不饱和环体系,借助该反应途径可以有效制备功能聚烯烃,并具有合成简便、单体组分和功能化属性可调的优点,是功能性聚烯烃制备的理想方法。该技术可实现桦木醇环烯烃衍生物的制备,该产物具有类桦木醇的生物活性,可作为有机单体进行开环聚合,进一步制备聚烯烃,实现聚烯烃的改性和功能化,具有一定的先进性。
技术实现要素:
4.本发明所要解决的技术问题是提供一种桦木醇环烯烃衍生物有机单体的合成方法,以制备具有抗菌活性的可聚合的环烯烃有机单体,可以在聚烯烃抗菌制品中得到应用。
5.为了解决上述技术问题,本发明得到了一种基于桦木醇及其衍生物的环烯烃有机单体,其结构如下:
[0006][0007]
其中,r为cnh2n,n=2~8。
[0008]
以上基于桦木醇环烯烃衍生物的有机单体通过抗菌活性测试发现,其具有广谱的具有广谱抑菌作用。
[0009]
一种基于桦木醇环烯烃衍生物的有机单体,其制备方法包括如下步骤:
[0010]
(1)首先将桦木醇烯烃衍生物置于真空干燥装置中干燥24h。然后将溶剂、桦木醇烯烃衍生物加入圆底烧瓶中,在磁力搅拌器上以700-1000r/min的速度,于冰水浴条件下,通入氩气鼓泡0.5-2h。随后将催化剂溶液以注射器快速注入圆底烧瓶中。上述混合物在室温条件下反应24-48h,反应期间始终保持室温和恒定的转速。最后加入淬灭剂淬灭催化剂
24h,得到粗产物。反应结束后,过滤除去不溶物,经30-35℃下旋蒸蒸发溶剂后得到上柱样品。最后,将样品填充至硅胶柱中进行层析分离得到目标产物,将目标产物于30-35℃下旋蒸后放入真空烘箱中,于室温下干燥24h,得到所需桦木醇环烯烃衍生物有机单体。
[0011]
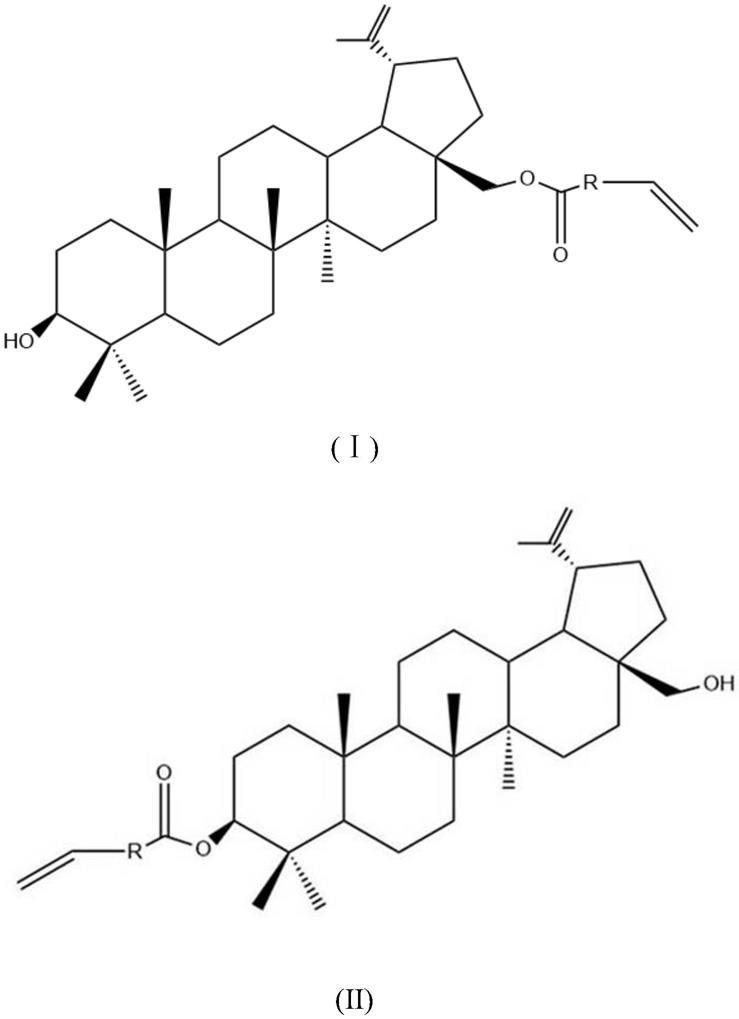
优选地,上述制备方法中桦木醇烯烃衍生物,应具有式ⅰ中所示结构,式中r选自c2h4,c3h6,c4h8,c5h
10
,c6h
12
,c7h
14
,c8h
16
等中的一种。
[0012][0013]
在实验中,上述制备方法中桦木醇烯烃衍生物,也可具备下述式ii中所示结构:
[0014][0015]
式中,r为c
nh2n
,n=2~8。
[0016]
上述制备方法中催化剂为schrock金属卡宾催化剂或grubbs金属卡宾催化剂中的一种。
[0017]
上述制备方法中淬灭剂为乙烯基乙醚。
[0018]
上述制备方法中溶液为二氯甲烷、氯仿、四氢呋喃和二甲基亚砜中的一种。
[0019]
本发明选择抗菌型桦木醇烯烃衍生物作为原料,通过关环复分解的方法制得了具
有聚合活性的抗菌型桦木醇环烯体衍生物,该有机单体可与其他烯烃单体共聚,制备功能性聚烯烃制品。
[0020]
与现有技术相比,本发明的有益效果在于:
[0021]
(1)本发明在制备功能化聚烯烃的领域内,能够有效解决极性单体对催化剂和聚合过程的影响,并且反应条件温和、反应速率快、等规度高,这样的特点能够最大程度发挥桦木醇基聚烯烃的生物活性。
[0022]
(2)本发明能够解决烯烃分子结构中缺乏极性基团,导致其抗静电性、降解性以及染色性差等缺点,能赋予聚烯烃以抗菌等生物活性。
附图说明
[0023]
图1为所选用桦木醇烯烃衍生物的结构示意图;
[0024]
图2为实施例1中一种桦木醇环烯烃衍生物有机单体的合成路线图;
[0025]
图3为实施例1、2、3中一种桦木醇环烯烃衍生物有机单体的红外测试谱图;
[0026]
图4为实施例1、2中一种桦木醇环烯烃衍生物有机单体的抗菌测试结果;
具体实施方式
[0027]
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
[0028]
实施例1
[0029]
一种桦木醇环烯烃衍生物有机单体的合成方法:
[0030]
(1)首先将十一碳烯酸-28-桦木酯置于真空干燥装置中干燥24h。然后称取1.0g十一碳烯酸-28-桦木酯加入500ml圆底烧瓶中,加入150ml二氯甲烷溶解。在磁力搅拌器上以700r/min的速度,于冰水浴条件下,通入氩气鼓泡30min。
[0031]
(2)在手套箱中称取grubbsⅰ催化剂67mg,以5ml二氯甲烷溶解后转移至10ml注射器内,并利用皮塞将针头堵住后迅速转移注射进上述圆底烧瓶中。上述混合物在室温条件下反应24h,反应期间始终保持室温和恒定的转速。最后加入5ml乙烯基乙醚淬灭催化剂反应24h,得到粗产物。
[0032]
(3)反应结束后进行后处理,将步骤(2)中的产物在35℃下旋蒸浓缩得到湿法制样的层析柱产物。
[0033]
(4)称取300目层析硅胶400.0g加入1000ml烧杯中,再量取800.0ml体积比为石油醚:乙酸乙酯=8:1的洗脱剂,用玻璃棒搅拌均匀,加入直径为60mm、有效长度为305mm的层析柱中,压实至层析柱体积的2/3左右;再加入约2cm厚石英砂,并用胶头滴管加入步骤(3)得到的层析柱产物,尽量使样品分布均匀,再填入约3cm的石英砂,并加入一定量的石油醚作为缓冲液。
[0034]
(5)配制洗脱液(乙酸乙酯/石油醚)并完成湿法上柱。打开节门阀,进行洗脱,同时在硅胶板上点板,进一步放置在洗脱液展缸中进行显色处理。根据洗脱顺序的不同,将对应试管中的产物用烧瓶收集并在35℃下进行旋蒸处理,得到褐色结晶状固体,并放置真空烘
箱中室温干燥24h,得到目标产物十一碳环烯酸-28-桦木酯(cubet)。
[0035]
其中目标产物的核磁结构如下:1h nmr(600mhz,chloroform-d)δ4.71(d,j=2.3hz,1h),4.65
–
4.57(m,1h),4.32
–
4.24(m,1h),3.86(d,j=11.0hz,1h),3.25
–
3.15(m,1h),2.46(dt,j=11.3,5.7hz,1h),2.34(t,j=7.5hz,2h).
[0036]
实施例2:一种桦木醇环烯烃衍生物有机单体的合成方法:
[0037]
(1)首先将五碳烯酸-28-桦木酯置于真空干燥装置中干燥24h。然后称取1.0g五碳烯酸-28-桦木酯加入500ml圆底烧瓶中,加入150ml二氯甲烷溶解。在磁力搅拌器上以1000r/min的速度,于冰水浴条件下,通入氩气鼓泡30min。
[0038]
(2)在手套箱中称取grubbsⅰ催化剂78.5mg,并以5ml二氯甲烷溶解后转移至10ml注射器内,并利用皮塞将针头堵住后迅速转移注射进上述圆底烧瓶中。上述混合物在室温条件下反应24h,反应期间始终保持室温和恒定的转速。最后加入5ml乙烯基乙醚淬灭催化剂反应24h,得到粗产物。
[0039]
(3)反应结束后进行后处理,将步骤(2)中的产物在35℃下旋蒸浓缩得到湿法制样的层析柱产物。
[0040]
(4)称取300目层析硅胶400.0g加入1000ml烧杯中,再量取800.0ml体积比为石油醚:乙酸乙酯=3:1的洗脱剂,用玻璃棒搅拌均匀,加入直径为60mm、有效长度为305mm的层析柱中,压实至层析柱体积的2/3左右;再加入约2cm厚石英砂,并用胶头滴管加入步骤(3)得到的层析柱产物,尽量使样品分布均匀,再填入约3cm的石英砂,并加入一定量的石油醚作为缓冲液。
[0041]
(5)配制洗脱液(乙酸乙酯/石油醚)并完成湿法上柱。打开节门阀,进行洗脱,同时在硅胶板上点板,进一步放置在洗脱液展缸中进行显色处理。根据洗脱顺序的不同,将对应试管中的产物用烧瓶收集并在35℃下进行旋蒸处理,得到黄色蜡状固体,并放置真空烘箱中室温干燥24h,得到目标产物五碳环烯酸-28-桦木酯(cpbet)。
[0042]
其中cpbet的核磁谱图如下:1h nmr(600mhz,acetonitrile-d3)δ4.70
–
4.67(m,1h),4.60
–
4.57(m,1h),4.26(ddd,j=11.0,4.7,1.9hz,1h),3.85(dd,j=11.3,4.8hz,1h),3.18(dd,j=11.5,4.7hz,1h),2.63(s,2h),2.44
–
2.41(m,1h),2.38(dd,j=4.2,2.3hz,2h),2.36(s,1h),2.32(dd,j=7.8,3.7hz,1h).
[0043]
实施例3:一种桦木醇环烯烃衍生物有机单体的合成方法:
[0044]
(1)首先将七碳烯酸-28-桦木酯置于真空干燥装置中干燥24h。然后称取2.0g七碳烯酸-28-桦木酯加入500ml圆底烧瓶中,加入300ml二氯甲烷溶解。在磁力搅拌器上以1000r/min的速度,于冰水浴条件下,通入氩气鼓泡60min。
[0045]
(2)在手套箱中称取grubbsⅰ催化剂149mg,并以10ml二氯甲烷溶解后转移至10ml注射器内,并利用皮塞将针头堵住后迅速转移注射进上述圆底烧瓶中。上述混合物在室温条件下反应24h,反应期间始终保持室温和恒定的转速。最后加入10ml乙烯基乙醚淬灭催化剂反应24h,得到粗产物。
[0046]
(3)反应结束后进行后处理,将步骤(2)中的产物在35℃下旋蒸浓缩得到湿法制样的层析柱产物。
[0047]
(4)称取300目层析硅胶400.0g加入1000ml烧杯中,再量取800.0ml体积比为石油醚:乙酸乙酯=3:1的洗脱剂,用玻璃棒搅拌均匀,加入直径为60mm、有效长度为305mm的层
析柱中,压实至层析柱体积的2/3左右;再加入约2cm厚石英砂,并用胶头滴管加入步骤(3)得到的层析柱产物,尽量使样品分布均匀,再填入约3cm的石英砂,并加入一定量的石油醚作为缓冲液。
[0048]
(5)配制洗脱液(乙酸乙酯/石油醚)并完成湿法上柱。打开节门阀,进行洗脱,同时在硅胶板上点板,进一步放置在洗脱液展缸中进行显色处理。根据洗脱顺序的不同,将对应试管中的产物用烧瓶收集并在35℃下进行旋蒸处理,得到褐色结晶状固体,并放置真空烘箱中室温干燥24h,得到目标产物七碳环烯酸-28-桦木酯(chbet)。
[0049]
其中,chbet的核磁结构如下:1h nmr(600mhz,chloroform-d)δ4.71(d,j=2.3hz,1h),4.65
–
4.59(m,1h),4.28(dd,j=11.0,1.9hz,1h),3.86(d,j=11.3hz,1h),3.21(dd,j=11.5,4.7hz,1h),2.47(td,j=11.1,5.5hz,1h),2.35(td,j=7.5,4.9hz,2h).
[0050]
制得桦木醇环烯烃衍生物实施例1的合成路线图如图2所示;制得桦木醇基环烯烃衍生物的ft-ir如图3所示,确定其化学结构;
[0051]
图4为桦木醇环烯烃衍生物的抑菌圈实验,结果表明:桦木醇及其衍生物均具有一定的抗菌活性。对比桦木醇、十一碳烯酸-28-桦木酯(ubet)、实施例1和实施例2的结果,其抑菌圈直径分别为5、11、18和10mm。因此,实施例1的抗菌效果明显优于实施例2、桦木醇及其烯烃衍生物,由此可知,相同条件下的桦木醇环烯烃衍生物相较于桦木醇及其衍生物均具有更高的抑菌活性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1