一种生物炭基零价铁与微生物协同修复铬污染土壤的方法与流程
本发明涉及土壤环境的修复方法,具体涉及了一种生物炭基零价铁与微生物协同修复铬污染土壤的方法。
背景技术:
铬作为重要的化工原料之一被广泛应用于冶金、电镀、制革、印染等行业中。由于生产过程的渗漏、废水的不达标排放以及含铬废渣的渗滤等,导致大量铬进入场地周边土壤和地下水。在土壤环境中,铬的主要存在形态为三价铬(cr(iii))和六价铬(cr(vi))。三价铬易被土壤胶体和矿物质通过吸附、配位、络合、沉淀等作用固定于土壤中,其迁移性和生物有效性较低。六价铬由于带负电,不易被土壤矿物和胶体所吸附而游离在土壤间隙中,具有较高的水溶性、迁移性和生物可利用性;其对人体有致癌作用,毒性是cr(iii)的100倍以上。同时,铬在土壤中的存在形态也对其毒性有很大影响,根据五步连续提取法可将土壤中铬的赋存形态分为水溶态、交换态、碳酸盐结合态、铁锰结合态、有机结合态和残渣态六种形态。由于后三种形态的铬基本上被固定在土壤颗粒或矿物中,具有较高稳定性,主要是前三种形态的铬起毒性作用。
目前,铬污染土壤的修复主要依照以下两种途径。一种是将铬从土壤中去除,或者降低其浓度至土壤背景值以下,如客土法、植物修复法等。另一种是改变铬在土壤中的存在价态以及形态,如化学还原法、生物还原法等,以降低其在土壤-植物以及土壤-地下水中的迁移性、生物毒性及生物有效性。此途径因不破坏土壤结构、成本低且操作简便,适用于较大重金属污染面积土壤的修复而受到重视并逐渐在行业内得到应用。
使用纳米铁或零价铁对铬污染土壤进行原位修复是近年来发展起来的一个新技术。具有大比表面积、强吸附能力和高还原性的fe0可通过吸附、还原和沉淀作用将cro42-还原为低毒性、难溶的形态固定在土壤中,反应式如下:
cro42-+fe0+4h2o→cr3++fe3++8oh-
(1-x)fe3++(x)cr3++2h2o→fe(1-x)cr(x)ooh(s)+3h+
fe0可直接将电子传递给cr(vi)使其还原成cr(iii),也可利用fe0腐蚀过程中产生的fe2+或h2将cr(vi)还原。随后生成氢氧化物沉淀和铬铁沉淀物覆盖在fe0表面或包覆于生成的含铁活性矿物中,进一步降低铬的可提取性和生物有效性。但相关研究表明,铬铁沉淀物作为一种难溶的惰性矿物沉积在fe0表面,会阻隔fe0与cr(vi)之间的电子传递,阻碍六价铬的还原反应直至反应终止,最终导致吸附在fe0表面的cr(vi)重新释放到土壤环境中,使污染修复效果大打折扣。此外,零价铁比表面积大、反应活性高且具有磁性的性质,使其极易凝聚成团,而且其被氧化倾向性很强,在保存、运输和反应过程中易被周围环境介质(如h2o和o2)氧化,使其还未与cr(vi)接触就失活。
技术实现要素:
本发明针对零价铁在修复铬污染土壤时容易团聚和被氧化问题,提供一种生物炭基零价铁与微生物协同修复铬污染土壤的方法。
为实现上述目的,本发明采用如下技术方案:
一种生物炭基零价铁与微生物协同修复铬污染土壤的方法,其包括以下步骤:
(1)生物炭基零价铁制备:将生物质加至可溶性铁盐溶液进行改性,过滤,焙烧改性的生物质,获得生物炭基零价铁修复材料;
(2)菌种驯化:从铬污染场地土壤中筛选出能以有机质和氢气作为电子供体,六价铬、三价铁、硫酸盐、硝酸盐和氧气作为电子受体进行代谢活动的优势菌种,对优势菌种进行驯化和扩培;
(3)修复:将步骤(1)制得的生物炭基零价铁和步骤(2)驯化培养所得的优势菌种与待修复铬污染土壤混合均匀,加水调节土壤含水率并在常温下进行修复。
进一步地,步骤(1)中所述可溶性铁盐为氯化铁、硝酸铁或柠檬酸铁。
进一步地,所述可溶性铁盐的浓度为0.1~1mol/l。
进一步地,所述生物质的粒径为0.5~5mm,所述生物质与可溶性铁盐溶液体积比为1:5~1:2,搅拌时间为4~12h。
进一步地,步骤(1)中所述改性的步骤为用氨水调节溶液ph值至5~7,所述氨水的浓度为10%。
进一步地,步骤(1)中所述烘干温度为70~80℃,焙烧温度600~800℃。
进一步地,所获得生物炭基零价铁颗粒粒径为0.3~4mm,零价铁粒径为0.1~200μm,铁含量为0.5~3.5%。
进一步地,所述步骤(2)中对优势菌种进行扩培的菌种培养液中葡萄糖浓度为100~1000mg/l,并采用六价cr浓度梯度法对菌种进行驯化,六价铬浓度为5~30mg/l。
进一步地,步骤(3)中所述生物炭基零价铁投加量为0.1~1g/kg,所述优势菌种投加量为20~400mg/kg,土壤含水率50~60%。
进一步地,步骤(3)中所述铬污染土壤ph值为5~6.5,粒径为100~5000μm,铬污染浓度为50~250mg/kg。
进一步地,步骤(3)中修复时间为3~21d,温度为20~30℃。
进一步地,步骤(1)中所述焙烧在绝氧条件下进行。
与现有技术相比,本发明具有如下优点和有益效果:
1.本发明的生物炭基零价铁与微生物协同修复铬污染土壤的方法,以价廉易得、无毒无害、可生物降解的生物炭为基质负载零价铁,不仅可提高零价铁的分散性,还可阻隔零价铁与氧气的接触来保持其还原特性,以增强零价铁的活性,克服零价铁在原位修复技术中易团聚、氧化的问题。此外,生物炭可为微生物提供栖息表面,还可作为生长基质为微生物提供能量,提高微生物活性,增强其还原cr(vi)的速率。
2.本发明的生物炭基零价铁与微生物协同修复铬污染土壤的方法,微生物可消耗土壤缝隙渗入的溶解氧,防止零价铁与氧气直接接触而钝化,同时微生物还能利用零价铁腐蚀产生的氢气作为电子供体直接还原土壤中的cr(vi),并通过自身代谢作用将零价铁表面钝化层的fe3+还原成溶解性较好的fe2+,加快零价铁的腐蚀和表面活性位点的更新。除此之外,微生物还能通过分泌胞外聚合物,诱导零价铁腐蚀释放的fe2+生成纤铁矿、磁铁矿和绿锈等高活性矿物,进一步提升零价铁对cr(vi)的吸附、还原和固定能力。通过生物炭基零价铁和微生物的协同作用,可在降低修复成本的同时大幅度提高铬污染土壤的修复效果。
3.本发明的生物炭基零价铁与微生物协同修复铬污染土壤的方法,生物炭(bc)表面分布大量含氧活性官能团,因此,其具有较高阳离子交换量,可固定土壤中的无机养分并为微生物提供栖息的表面,进而提高土壤肥效和增加土壤生物多样性。此外,生物炭和零价铁之间还存在微电解作用,可提升零价铁腐蚀和释放h2的速度,进而加快其在铬污染土壤修复过程中对铬的吸附还原进程,提高铬污染土壤的修复效果。
附图说明:
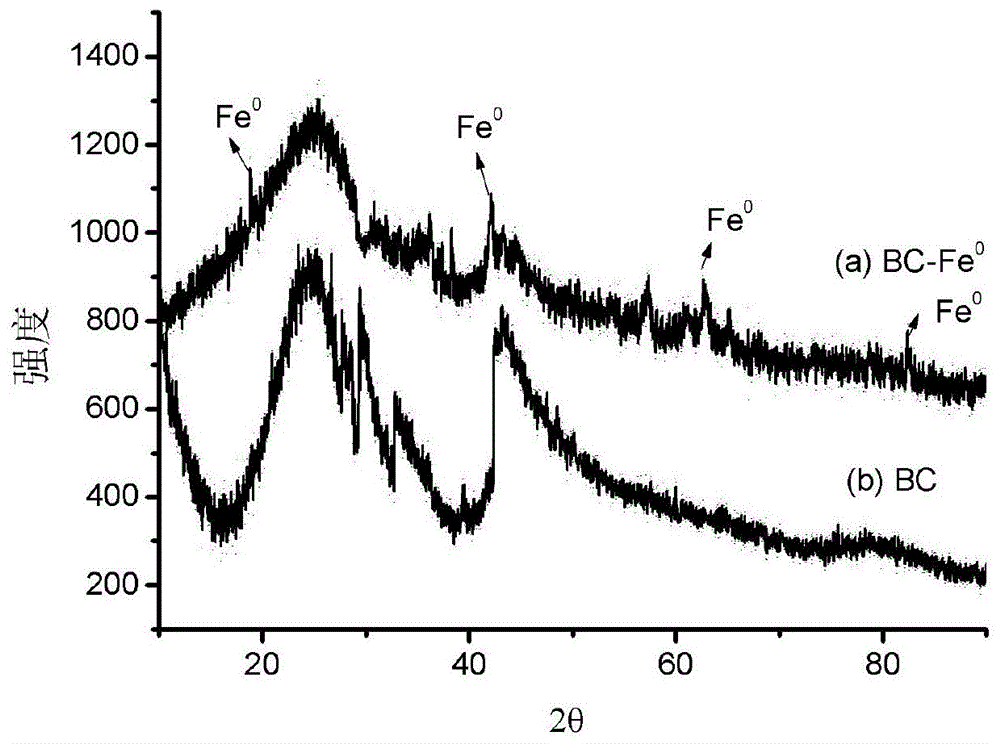
图1为生物炭基零价铁反应前后的x射线衍射图(xrd);
图2为生物炭基零价铁反应前的扫描电镜图(sem);
图3为生物炭基零价铁反应后的扫描电镜图(sem);
图4为生物炭基零价铁与微生物协同反应后的扫描电镜图(sem)之一;
图5为生物炭基零价铁与微生物协同反应后的扫描电镜图(sem)之二;
图6为生物炭基零价铁与微生物协同反应后的扫描电镜图(sem)之三。
具体实施方式:
以下结合具体实施例及附图对本发明技术方案作进一步详细的描述,但本发明的实施方式及保护范围不限于此。
实施例1
将0.6g生物质加至100ml浓度为0.5mol/l的氯化铁溶液中,在60rpm条件下搅拌8h使之混合均匀,然后加入浓度为10%的氨水,调节溶液ph至5~7,滤出生物质并用去离子水清洗数次,80℃烘干后于绝氧条件下600℃焙烧8h,获得生物炭基零价铁修复材料bc-fe0(fecl3)。
将0.6g生物质加至100ml浓度为0.5mol/l的硝酸铁溶液中,在60rpm条件下搅拌8h使之混合均匀,然后加入浓度为10%的氨水,调节溶液调节溶液ph至5~7,滤出生物质并用去离子水清洗数次,80℃烘干后于绝氧条件下600℃焙烧8h,获得生物炭基零价铁修复材料bc-fe0(fe(no3)3)。
将0.6g生物质加至100ml浓度为0.5mol/l的柠檬酸铁溶液中,在60rpm条件下搅拌8h使之混合均匀,然后加入浓度为10%的氨水,调节溶液调节溶液ph至5~7,滤出生物质并用去离子水清洗数次,80℃烘干后于绝氧条件下600℃焙烧8h,获得生物炭基零价铁修复材料bc-fe0(fec6h5o7)。
从铬污染场地采集受铬污染土壤2kg,用水调节土壤含水率为60wt%,添加葡萄糖1g/kg并与土样充分混合,在厌氧培养箱中以n2:h2:co2为85%:10%:5%的混合气于30℃条件下培养5d后,再加入1g/kg葡萄糖基质,调节含水率为60wt%,于同样的反应条件培养5d。经三个周期培养后取出土壤,加入1土壤体积清水,与土壤充分混合后离心,得到铬还原优势菌液,经检验其包含铁还原细菌、反硝化菌和硫酸还原菌等。该铬还原优势菌液能以葡萄糖和氢气为电子供体,六价铬、硝酸盐、硫酸盐和三价铁作为电子受体进行代谢活动,对六价铬、硝酸盐和硫酸盐还原能力分别可达125mg/(gmlss.d)、1000mg/(gmlss.d)和450mg/(gmlss.d)。为进一步提高菌种还原六价铬的能力及数量,在厌氧培养箱中以葡萄糖和氢气作为电子供体进行培养和扩培,培养液中加入清水、1000mg/l葡萄糖、75mg/l硫酸镁、45mg/l氯化铵以及25mg/l磷酸氢二钾,并采用cr(vi)浓度梯度法(5~25mg/l)对菌种进行驯化,当菌种对培养液中浓度为30mg/l的cr(vi)的还原率达到90%时制成微生物浓度为2g/l的菌悬液。
称取10g浓度为200mg/kg的铬污染土壤,移至50ml离心管中,土壤原土ph值为6.2,用水调节土壤含水量为60%,加入浓度为0.25g/kg生物炭基零价铁及浓度为80mg/kg的菌悬液,混合均匀后加盖密封并在常温30℃下静置培养14d。反应结束后加定量去离子水在4000rpm条件下离心10min,测定上清液铬浓度。
各修复材料对土壤中水溶态六价铬/总铬的去除效果列于表1。从表1可知,在三种生物炭基零价铁的制备方法中,硝酸铁制备的材料对水溶态六价铬/总铬的去除效果最好,氯化铁制备的材料次之。
表1各修复材料对铬污染土壤中水溶态六价铬/总铬的去除效果对比
实施例2
生物炭基零价铁(bc-fe0(fecl3))与菌悬液制备方法与实施例1相同。称取10g浓度为200mg/kg的铬污染土壤,移至50ml离心管中,土壤原土ph值为6.2,用水调节土壤含水量为60%,加入浓度为0.25g/kg零价铁或生物炭基零价铁及浓度为80mg/kg的菌悬液,混合均匀后加盖密封并分别在常温20℃、25℃和30℃下静置培养14d。反应结束后加定量去离子水在4000rpm条件下离心10min,测定上清液铬浓度;通过多步连续提取法测定修复后土壤中铬赋存形态的变化。
修复过程设置4种反应体系:1.空白体系,包括空白或铬污染土壤和bc单独处理体系;2.微生物体系(cell),包括单独cell体系和cell+bc体系;3.零价铁体系(fe0),包括单独fe0体系和单独bc-fe0体系;4.零价铁+微生物体系(fe0+cell),包括fe0+cell体系和bc-fe0+cell体系。实验结束后,将经bc-fe0体系和bc-fe0+cell体系修复后的土壤放入-80℃冰箱中冷冻2h后取出,迅速放入冷冻干燥器中干燥48h。将干燥后的混合物取出,在厌氧手套箱(n2:h2=95:5)中用磁铁分离出反应后的铁粉颗粒,同时在相同操作条件下收集反应前的零价铁颗粒并采用x射线衍射仪和扫描电镜对其进行分析,考察其表面形貌和结构的变化情况,实验结果如图1~6所示。
30℃时,反应前后土壤中铬的污染状况及铬的赋存形态分别列于表2和表3。从表2可知,相较于fe0,bc-fe0因分散性和抗氧化性得到提高,从而对土壤水溶态铬的去除能力提高了0.6倍。在bc-fe0+cell体系中,零价铁对土壤水溶态六价铬和总铬的去除能力分别达到48mgcr/gfe0和67mgtotalcr/gfe0,比单独fe0体系分别提高了5.9和4.6倍。从图4、图5和图6还可以看出,在微生物协同作用下,零价铁表面生成了更多的高活性铁矿物,如纤铁矿、硫铁矿和绿锈,这些活性矿物使得零价铁吸附、还原和固定cr(vi)的能力得到大幅度地提高。此外,从表3可知,经bc-fe0+cell体系修复后,土壤中铬的赋存形态都从高毒性、可生物利用的易溶态(水溶态、可交换态和碳酸盐结合态)转变为低毒害、难生物利用的固定态(铁锰结合态、有机态和残渣态)。由此可见,零价铁协同微生物能大幅度提升零价铁对污染土壤中六价铬的吸附、还原和固定效果。
25℃和20℃条件下各修复体系中土壤中铬的污染状况分别列于表4和表5。从表4和表5可知,温度从20℃升高到25℃时,cell体系、fe0体系、fe0+cell体系和bc-fe0+cell体系对总铬的去除能力分别提高了33%、10%、14%和19%。由此可见,温度变化对cell体系影响较大,对零价铁+微生物体系影响次之,对fe0体系影响最小。
表230℃时各修复体系对铬污染土壤中水溶态六价铬/总铬的去除效果对比
表3生物炭基零价铁及生物炭基零价铁与微生物协同修复后土壤中铬赋存形态的变化
表425℃时各修复体系对铬污染土壤中水溶态六价铬/总铬的去除效果对比
表520℃时各修复体系对铬污染土壤中水溶态六价铬/总铬的去除效果对比
实施例3
生物炭基零价铁(bc-fe0(fecl3))与菌悬液制备方法与实施例1相同。称取10g浓度为200mg/kg的铬污染土壤,移至50ml离心管中,土壤原土ph值为6.2,用水调节土壤含水量为60%,加入浓度为0.05、0.125、0.25、0.5或1g/kg生物炭基零价铁及浓度为80mg/kg的菌悬液,混合均匀后加盖密封并分别在常温30℃下静置培养14d。反应结束后加定量去离子水在4000rpm条件下离心10min,测定上清液铬浓度。由表6可知,生物炭基零价铁投加量从0.05增至1g/kg时,反应14d后对土壤水溶态六价铬的去除能力从23mgcr/gfe0升至53mgcr/gfe0,对总铬的去除能力从34mgtotalcr/gfe0升至79mgtotalcr/gfe0,但生物炭基零价铁投加量超过0.25g/kg时,协同体系对铬污染土壤中水溶态六价铬/总铬的去除能力没有明显的提升,说明此时微生物浓度为主要的限速因子。表6生物炭基零价铁投加量对铬污染土壤水溶态六价铬/总铬的去除效果对比
实施例4
生物炭基零价铁(bc-fe0(fecl3))与菌悬液制备方法与实施例1相同。称取10g浓度为200mg/kg的铬污染土壤,移至50ml离心管中,土壤原土ph值为6.2,用水调节土壤含水量为60%,加入浓度为0.25g/kg生物炭基零价铁及浓度为20、40、80或160mg/kg的菌悬液,混合均匀后加盖密封并分别在常温30℃下静置培养14d。反应结束后加定量去离子水在4000rpm条件下离心10min,测定上清液铬浓度。由表7可知,微生物浓度从20增至160mg/kg时,反应14d后协同体系对土壤水溶态六价铬的去除能力从26mgcr/gfe0升至54mgcr/gfe0,对总铬的去除能力从33mgtotalcr/gfe0升至76mgtotalcr/gfe0,但微生物浓度超过80mg/kg时,协同体系对铬污染土壤中水溶态六价铬/总铬的去除能力没有明显的提升,说明此时零价铁投加量是铬去除的主要限制因素。
表7微生物浓度对铬污染土壤水溶态六价铬/总铬的去除效果对比
以上所述,仅为本发明的较佳实施例而已,并非对本发明作任何形式上的限制。凡本领域的技术人员,应该理解,上述实施例和说明书中描述的只是说明发明的原理,在不脱离本发明技术精神和范围的前提下,本发明还会有些许更动、修饰与演变的等同变化,凡依据本发明的实质技术对以上实施例所做的任何等同变化的更动、修饰与演变等,均应包含在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!