一种铜离子印迹交联壳聚糖微球的制备方法与流程
本发明属于材料科学领域,具体涉及一种铜离子印迹交联壳聚糖微球的制备方法。
背景技术
随着我国工业的发展,越来越多含有hg2+、ni2+、cu2+、pb2+、cd2+等重金属离子的污水被排放到环境水体中。重金属具有毒性大、难降解、易在生物体内富集等特点,且重金属很难被降解,最终通过食物链沉积到人体中,对生态环境和人体健康造成了极大的危害。铜与人体中某些组织的亲和力特别大,结合后会抑制酶的活性,从而对人体产生毒害作用。另外,铜又是很重要的有价金属,流失于污水中也是一种资源浪费。因此回收有价金属铜和去除水中污染的铜显得十分必要。目前,从废水中去除铜离子的方法主要有化学沉淀法、离子交换法、溶剂萃取法、膜分离法等。但这些方法存在各自的缺点,如处理效果不好,处理成本高、工艺流程复杂等。吸附法作为一种有效的分离技术,具有分离效率高、操作简单、分离产物易于回收等优点,在重金属离子处理方面具有广泛的应用前景。
分子印迹技术是制备对某一特定的目标分子具有特异选择性的印迹聚合物技术。分子印迹聚合物有3大特点:预定性、识别性和实用性。分子印迹还具有制备简单、稳定性强、抗恶劣环境能力强、可长期保存等优点,在色谱分离、膜分离、仿生传感器、选择性催化等方面有广泛的应用。由于壳聚糖链上众多的氨基和羟基为其结构修饰和合成分子印迹聚合物提供了可能,因此,近年来将其用于分子印迹材料合成,开展具有特定吸附功能的聚合物研究成为热点。
壳聚糖作为一种天然有机高分子絮凝剂,具有环境相容性好、可再生、资源丰富以及高度可降解性等优点,已经在生物科学及多个领域包括水处理、化妆品和制药等领域得到广泛应用。壳聚糖的分子链中含有反应性基团氨基和羟基,在酸性溶液中会形成阳离子聚电解质,显示出良好的絮凝性能,能与许多金属离子(hg2+、ni2+、cu2+、pb2+、cd2+、ag+等)形成稳定的螯合物,且其特殊的多孔结构,使其具有较大的比表面积,吸附金属离子的容量大,但是易溶于酸性溶液。近年来,不少学者研究了在壳聚糖的线性分子链上进行化学改性,以提高其吸附量或吸附选择性等,常见采用化学交联的方法改善壳聚糖的酸溶性。
交联壳聚糖是在一定条件下对壳聚糖进行分子内或分子间交联改性,壳聚糖交联产物不仅可以提高对重金属离子的吸附能力,也可明显改善壳聚糖自身的机械性能和酸溶性,提高抗降解性,增强分子稳定性。交联反应虽然解决了树脂强度和可重复使用性能,但也导致了吸附性能较未交联时差,其主要原因是交联反应往往发生在活性较高的氨基上,而氨基上引入了其它的基团后,增加了氮原子同金属离子配位的空间位阻。
技术实现要素:
本发明的目的在于提供一种铜离子印迹交联壳聚糖微球的制备方法,旨在解决壳聚糖的酸溶性问题,提高交联壳聚糖的吸附性能。
本发明采取的技术方案为:
一种铜离子印迹交联壳聚糖微球的制备方法,包括以下步骤:
(1)cu2+印迹壳聚糖微球的制备
按照乙酸溶液、壳聚糖、一水乙酸铜的用量比为100ml∶1-3g∶0.25g,将浓度为3%的乙酸溶液与壳聚糖混合,超声溶解完全后,再加入一水乙酸铜充分溶解,得到乙酸铜-壳聚糖溶液;
按照乙酸铜-壳聚糖溶液与氨水溶液的体积比为1∶2,将乙酸铜-壳聚糖溶液滴入到体积分数为12-12.5%的氨水溶液中,浸泡固化24-28h,得到cu2+印迹壳聚糖微球;若将微球置于去离子水中湿态保存,为湿态cu2+印迹壳聚糖微球;若将微球在45℃烘干,可得干态cu2+印迹壳聚糖微球。
(2)cu2+印迹交联壳聚糖微球的制备
在烧杯中加入去离子水,然后加入步骤(1)制备的cu2+印迹壳聚糖微球和环氧氯丙烷,所加入的环氧氯丙烷与步骤(1)中的壳聚糖的用量比为1-3ml∶1-3g,在60-80℃下搅拌交联2-3h,然后对交联后的微球进行cu2+洗脱,直至洗脱液中检测不出cu2+为止,再用去离子水洗涤至ph=6,得到cu2+印迹交联壳聚糖微球。若将微球置于去离子水中湿态保存,则为湿态cu2+印迹交联壳聚糖微球;若将微球在45℃烘干,可得干态cu2+印迹交联壳聚糖微球。
步骤(1)中,乙酸铜-壳聚糖溶液滴入到氨水溶液中的具体方法如下:用7号针管取乙酸铜-壳聚糖溶液,调节针头与氨水液面距离为15cm,以28-32滴/min的速度滴入到氨水溶液中。
步骤(2)中,洗脱cu2+的具体方法如下:在60℃下用100ml浓度为1mol/l稀盐酸洗脱cu2+1h后,在洗脱液中滴加1-2滴浓度为5.4g/l铜试剂,洗脱废液呈深褐色并出现絮状物;用去离子水将微球洗涤多次,再加入50ml稀盐酸洗脱cu2+0.5h后,洗脱废液呈褐色;重复洗脱数次至洗脱废液为无色,说明微球中的模板cu2+已全部洗脱,然后用去离子水洗涤至ph=6。
本发明采用以上技术方案,以壳聚糖为功能单体,采用分子印迹技术,cu2+离子作为印迹模板使氨基、羟基的空间位置被固定,再利用环氧氯丙烷进行交联反应,最后通过盐酸洗脱使印迹模板cu2+脱除并使-nh2得到释放,从而制得对铜离子具有较高吸附能力和选择吸附性能的铜离子印迹交联壳聚糖微球,且吸附、洗脱速率快,操作简单易行,可再生循环使用,为铜的高效回收提供一种新的技术,对解决环境污染和资源回收利用具有重要意义。
附图说明
图1为本发明实施例1、实施例2产物的ft-ir谱图,a为壳聚糖,b为cu2+印迹壳聚糖,c为cu2+印迹交联壳聚糖;
图2为本发明实施例1、实施例2产物的xrd谱图,a为壳聚糖,b为cu2+印迹壳聚糖,c为cu2+印迹交联壳聚糖;
图3为本发明实施例1、实施例2产物的sem图,a为壳聚糖,b为cu2+印迹壳聚糖,c为cu2+印迹交联壳聚糖;
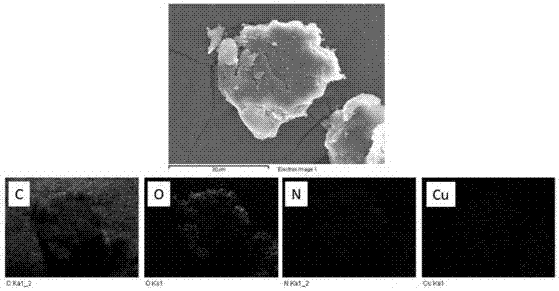
图4为本发明实施例1产物的edx图;
图5为本发明实施例2产物的edx图。
具体实施方式
下面结合具体实例进一步阐明本发明。
一种铜离子印迹交联壳聚糖微球的制备方法,包括以下步骤:
(1)cu2+印迹壳聚糖微球的制备
按照乙酸溶液、壳聚糖、一水乙酸铜的用量比为100ml∶1-3g∶0.25g,将浓度为3%的乙酸溶液与壳聚糖混合,超声溶解完全后,再加入一水乙酸铜充分溶解,得到乙酸铜-壳聚糖溶液;
用7号针管取乙酸铜-壳聚糖溶液,调节针头与氨水液面距离为15cm,以28-32滴/min的速度滴入到体积分数为12-12.5%氨水溶液中(乙酸铜-壳聚糖溶液与氨水溶液的体积比为1∶2),浸泡固化24-28h,得到cu2+印迹壳聚糖微球;若将微球置于去离子水中湿态保存,为湿态cu2+印迹壳聚糖微球;若将微球在45℃烘干,可得干态cu2+印迹壳聚糖微球。
(2)cu2+印迹交联壳聚糖微球的制备
在烧杯中加入去离子水,然后加入步骤(1)制备的cu2+印迹壳聚糖微球和环氧氯丙烷,所加入的环氧氯丙烷与步骤(1)中的壳聚糖的用量比为1-3ml∶1-3g,在60-80℃下搅拌交联2-3h,然后对交联后的微球进行cu2+洗脱,直至洗脱液中检测不出cu2+为止,再用去离子水洗涤至ph=6,得到cu2+印迹交联壳聚糖微球。若将微球置于去离子水中湿态保存,则为湿态cu2+印迹交联壳聚糖微球;若将微球在45℃烘干,可得干态cu2+印迹交联壳聚糖微球。
其中,洗脱cu2+的具体方法如下:在60℃下用100ml浓度为1mol/l稀盐酸洗脱cu2+1h后,在洗脱液中滴加1-2滴浓度为5.4g/l铜试剂,洗脱废液呈深褐色并出现絮状物;用去离子水将微球洗涤多次,再加入50ml稀盐酸洗脱cu2+0.5h后,洗脱废液呈褐色;重复洗脱数次至洗脱废液为无色,说明微球中的模板cu2+已全部洗脱,然后用去离子水洗涤至ph=6。
实施例1
cu2+印迹壳聚糖微球的制备
量取100ml浓度为3%的乙酸溶液于烧杯中,加入1.5g的壳聚糖粉末,超声溶解完全后,再加入0.25g一水乙酸铜充分溶解,得到乙酸铜-壳聚糖溶液;准确量取20ml乙酸铜-壳聚糖溶液,用7号针管取乙酸铜-壳聚糖溶液,调节针头与液面距离为15cm,以30滴/min的速度滴入到40ml体积分数为12.5%的稀氨水溶液中,浸泡固化24h,将微球置于去离子水中湿态保存,即得湿态cu2+印迹壳聚糖微球。
实施例2
cu2+印迹交联壳聚糖微球的制备
量取80ml的去离子水于烧杯中,加入实施例1中所制得的cu2+印迹壳聚糖微球,添加2.5ml环氧氯丙烷,在80℃下搅拌3h,进行充分交联。加入100ml浓度为1mol/l稀盐酸溶液,在60℃下洗脱cu2+多次,直至洗脱液中检测不出cu2+为止,用去离子水洗涤至ph=6,将微球置于去离子水中湿态保存,即得湿态cu2+印迹交联壳聚糖微球;若将微球在45℃烘干,可得干态cu2+印迹交联壳聚糖微球。
实施例3
以环氧氯丙烷为交联剂制备的cu2+印迹交联壳聚糖微球对铜离子的吸附效果
称取0.4075g实施例2制得的湿态cu2+印迹交联壳聚糖微球,置于浓度为338.7mg/l的铜溶液中,30℃下振荡吸附24h,以达到吸附平衡。采用可见分光光度计在最大吸收波长452nm处测定吸附前后铜溶液的吸光度,查cu2+吸光度-浓度标准曲线图,计算得出cu2+印迹交联壳聚糖微球对铜离子的吸附量为73.4mg/g。
对比例1
以乙二醛为交联剂制备的cu2+印迹交联壳聚糖微球对铜离子的吸附效果
(1)以乙二醛为交联剂的cu2+印迹交联壳聚糖微球的制备
量取80ml的去离子水于烧杯中,加入实施例1中所制得的cu2+印迹壳聚糖微球,添加2.5ml乙二醛,在80℃下搅拌3h,进行充分交联。加入100ml浓度为1mol/l稀盐酸溶液,在60℃下洗脱cu2+多次,直至洗脱液中检测不出cu2+为止,用去离子水洗涤至ph=6,将微球置于去离子水中湿态保存,即得湿态cu2+印迹交联壳聚糖微球;若将微球在45℃烘干,可得干态cu2+印迹交联壳聚糖微球。
(2)铜离子吸附试验
称取0.4075g步骤(1)制得的湿态cu2+印迹交联壳聚糖微球,置于浓度为338.7mg/l的铜溶液中,30℃下振荡吸附24h,以达到吸附平衡。采用可见分光光度计在最大吸收波长452nm处测定吸附前后铜溶液的吸光度,查cu2+吸光度-浓度标准曲线图,计算得出cu2+印迹交联壳聚糖微球对铜离子的吸附量为56.40mg/g。
对比例2
以戊二醛为交联剂制备的cu2+印迹交联壳聚糖微球对铜离子的吸附效果
(1)以戊二醛为交联剂的cu2+印迹交联壳聚糖微球的制备
量取80ml的去离子水于烧杯中,加入实施例1中所制得的cu2+印迹壳聚糖微球,添加2.5ml戊二醛,在80℃下搅拌3h,进行充分交联。加入100ml浓度为1mol/l稀盐酸溶液,在60℃下洗脱cu2+多次,直至洗脱液中检测不出cu2+为止,用去离子水洗涤至ph=6,将微球置于去离子水中湿态保存,即得湿态cu2+印迹交联壳聚糖微球;若将微球在45℃烘干,可得干态cu2+印迹交联壳聚糖微球。
(2)铜离子吸附试验
称取0.4075g步骤(1)制得的湿态cu2+印迹交联壳聚糖微球,置于浓度为338.7mg/l的铜溶液中,30℃下振荡吸附24h,以达到吸附平衡。采用可见分光光度计在最大吸收波长452nm处测定吸附前后铜溶液的吸光度,查cu2+吸光度-浓度标准曲线图,计算得出cu2+印迹交联壳聚糖微球对铜离子的吸附量为30.48mg/g。
由实施例3、对比例1、对比例2可知,分别采用环氧氯丙烷、乙二醛和戊二醛三种不同的交联剂,对比吸附效果,发现同等吸附条件下,以环氧氯丙烷为交联剂制备的cu2+印迹交联壳聚糖微球的吸附量最高,吸附效果最好。这是因为环氧基团与壳聚糖分子内的氨基反应形成羟基,对铜离子的螯合作用基本不变,吸附位点没有减少,因此吸附量不会降低。而采用乙二醛、戊二醛交联剂,醛的羰基与壳聚糖的氨基反应后生产相应的席夫碱,失去对铜离子的螯合作用,吸附位点减少,会导致吸附量降低。因此本申请最终采用环氧氯丙烷作为交联剂来制备cu2+印迹交联壳聚糖微球。
- 还没有人留言评论。精彩留言会获得点赞!