用于电解还原包含氧和第一金属的原料的方法和装置与流程
本发明涉及用于电解还原包含氧和第一金属的原料的方法和装置,特别地涉及通过还原金属氧化物进行的金属生产。
背景技术:
本发明涉及用于电解还原包含氧和第一金属的原料的方法。如现有技术已知的,电解工艺可用于例如将金属化合物或半金属化合物还原成金属、半金属或部分还原的化合物,或者用于还原金属化合物的混合物以形成合金。为了避免重复,除非另有说明,在此文献中术语金属用于涵盖所有这样的产物,例如金属、半金属、合金、金属间化合物。本领域技术人员将理解在适当的时候术语金属还可包括部分还原的产物。
近几年,对于通过直接还原固体金属氧化物原料来直接生产金属产生了很大的兴趣。一种这样的直接还原工艺为cambridge
已经提出了用于还原呈阴极连接的固体金属化合物形式的原料的其他还原方法,例如wo03/076690中所描述的
典型的直接还原工艺的实施通常使用基于碳的阳极材料。在还原工艺期间,基于碳的阳极材料被消耗并且阳极产物为碳的氧化物,例如气态一氧化碳或二氧化碳。在该工艺中碳的存在会导致降低工艺效率的许多问题以及导致由阴极上的还原而产生的金属的污染。对于许多产物,期望的是从系统中完全地消除碳。
已进行了大量的尝试以确保电解期间不被消耗的所谓的惰性阳极以及放出氧气作为阳极产物。常规易购得的材料中,氧化锡已表现一些有限的成就。已经提出了更特殊的基于钌酸钙的析氧阳极材料,但是该材料具有有限的机械强度、在操作期间遭受降解并且该材料是昂贵的。
铂已被用作用于还原氧化铀和其他金属氧化物的基于licl盐的阳极,但是必须非常小心地控制工艺条件以避免阳极的降解并且铂也是昂贵的。铂阳极对于工业规模的金属生产工艺不是经济可行的解决方案。
尽管可能期望用于fcc工艺中的析氧阳极,但是商业可行材料的实际实施似乎难以实现。此外,由于直接电解还原工艺中涉及的高温下氧的高度腐蚀性质,在使用析氧阳极中可产生另外的工程困难。
wo02/083993中提出了替代的阳极体系,其中电解池中的阳极由熔融银或熔融铜形成。在wo02/083993公开的方法中,从阴极上的金属氧化物中除去的氧通过电解质输送并且溶解在金属阳极中。然后通过局部降低一部分金属阳极上的氧分压来连续地除去溶解的氧。该替代的阳极体系具有有限的用途。氧的除去取决于氧能够扩散到熔融银或铜阳极材料中的速率。此外,速率还取决于通过局部降低一部分阳极上的分压而进行的连续除氧。因此,该工艺不是生产金属的商业可行的方法。
技术实现要素:
本发明提供了一种用于电解还原包含氧和第一金属的原料的方法和装置,如所附独立权利要求所限定的。本发明的优选和/或有利的特征在各个从属子权利要求中列出。
在第一方面中,可提供一种电解还原原料的方法,所述原料包含氧和第一金属,例如为包含氧和第一金属的化合物。所述方法包括以下步骤:将原料布置成与电解池内的阴极和熔融盐接触,将阳极布置成与电解池内的熔融盐接触,以及在阳极和阴极之间施加电势使得氧从原料中除去以形成经还原的原料。阳极包含熔融金属,其优选地为与包含于原料中的第一金属不同的金属。熔融金属可被称为第二金属。第二金属为铝或锡。虽然第二金属在室温下不熔化,但是当在阳极和阴极之间施加电势时,其在电池内的电解温度下熔化。从原料中除去的氧通过盐输送至阳极,在此氧与阳极的熔融金属反应形成包含熔融阳极金属和氧的氧化物。
该方面中所描述的本发明与wo02/083993的现有技术公开之间的关键不同在于本发明的熔融阳极金属在电解工艺中被消耗。换言之,熔融阳极金属为当与氧物类接触时容易被氧化以形成包含第二金属和氧的氧化物的金属。
在电解期间在阳极上形成的氧化物可为颗粒的形式,其可沉入熔融的金属中,从而暴露更多的用于氧化的熔融金属。在阳极上形成的氧化物可形成颗粒,其分散到熔融盐中并且暴露更多的用于后续氧化的熔融金属。在阳极上形成的氧化物可形成为溶解在金属内的液相。氧化物可在熔融阳极的表面上快速形成,并且可从熔融阳极的表面分散开。因此,氧化物的形成对氧化反应不会产生显著的动力学抑制。相比之下,wo02/083993的氧溶解到熔融金属阳极中取决于氧在熔融金属阳极中的溶解度、氧向熔融阳极中的扩散以及在降低的分压下氧脱离阳极的输送。
与惰性阳极相反,由于熔融金属阳极不放出氧气,用于氧化构造电池材料的电势被消除。例如,当使用“标准”惰性阳极时,需要选择特殊材料用于构造能够在升高的温度下耐氧的电池。
碳阳极的使用将导致co和co2放出。co和co2二者均为氧化剂,但是程度小于氧,并且可侵蚀构造材料。这可导致腐蚀产物进入熔体并随后进入产物。
优选的是在装置运行期间阳极上的第二金属处于接近并且仅仅高于其熔点的温度下,以减少由于过量汽化而造成的阳极材料的损失。
在装置运行期间,一定比例的来自阳极的第二金属优选地沉积在阴极上,在此其可沉积在经还原的原料上或与经还原的原料相互作用。因此,经还原的原料可包含第一金属(即原料中的金属氧化物的金属)和另外的一定比例的第二金属。
因此,经还原的原料可包含掺杂有一定比例的第二金属或与一定比例的第二金属合金化的第一金属。第一金属与一定比例的第二金属的掺杂或合金化可向经还原的原料中引入有利的物理或电学特性。例如,包含掺杂有一定比例的第二金属的第一金属的经还原的原料可表现出比仅包含第一金属的经还原的原料更高的介电常数。第一金属与一定比例的第二金属的掺杂或成合金化的其他益处可包括提高的抗拉强度、提高的电容、提高的电导率、降低的导电率、提高的熔点或降低的熔点。为了形成包含一定比例的第二金属的金属合金,使包含一定比例的第二金属(例如铝)的原料还原可能是有利的。例如,如果操作者希望制造ti-6al-4v合金,则可制备包含tio2、v2o5和al2o3的混合物的原料。在此情况下,产物中的铝污染物将不是问题。实际上,可改变氧化铝含量以反映源自阳极的另外的铝合金化。
经还原的原料可为包含不同比例的第二金属的金属合金。优选地,经还原的原料为包含第一金属和0.01重量%(wt%)至5重量%的第二金属的金属合金。例如,经还原的原料可包含0.01重量%至3.0重量%的第二金属或者0.05重量%至2.0重量%或0.10重量%至1.50重量%或0.50重量%至1.0重量%的第二金属。本发明可为使第一金属与一小部分第二金属合金化的便利方式,第二金属为铝或锡。
优选地,可控制包含于经还原的原料中的第二金属的比例。特别优选地,控制在阳极和阴极之间施加电势的时间的长度来确定经还原的原料中第二金属的比例。
第一金属为与第二金属不同的金属或合金。优选地,第一金属为选自以下的任意金属或选自以下的任意金属的合金:硅、钪、钛、钒、铬、锰、铁、钴、镍、锗、钇、锆、铌、钼、铀、锕系元素、铪、钽、钨、镧、铈、镨、钕、钐、锕、钍、镤、铀、镎和钚。
本领域技术人员将能够选择包含任何以上所列的第一金属的原料和包含铝或锡的阳极。
原料可为粉末或颗粒的形式或者可为由包含氧和第一金属的粉末状化合物形成的预成型的形状或微粒的形式。在一个优选的实施方案中,原料为平均粒径小于5mm,例如小于3mm或小于2mm的颗粒或粉末的形式。
原料优选地可为第一金属的氧化物,例如二氧化钛。原料可包含多于一种的不同金属的氧化物。原料可包含具有多种金属种类的复合氧化物。第一金属可为合金。例如,原料可为包含钛和另一金属的合金的氧化物。或者,原料可为金属酸盐(metallate)化合物,金属酸盐化合物为第一金属、氧和至少一种反应性金属的化合物,反应性金属优选地为第1族或第2族金属,例如选自钙、锂、钠和钾的金属。原料可为包含钛作为第一金属的金属酸盐,例如钛酸钙(如catio3)或钛酸锂(如li2tio3)。
第二金属(即阳极金属)可为工业纯的铝金属。或者,第二金属可为铝与一种或更多种其他元素的合金,例如共晶成分的合金。可期望的是具有共晶成分的合金以降低阳极金属的熔点,从而在更加有利的较低温度下操作该工艺。
第二金属(即阳极金属)可为工业纯的锡金属。或者,第二金属可为锡与一种或更多种其他元素的合金,例如共晶成分的合金。
当在阴极和阳极之间施加电势时,期望的是熔融金属处于低于1000℃的温度下。特别优选的是使工艺期间熔融盐的温度尽可能低以使熔融阳极上的蒸气压最小化并且因此使熔融阳极材料的损失最小化。因此,优选的是在电解期间使熔融盐保持在低于850℃,例如低于800℃或750℃或700℃的温度下。为了使过程期间包含阳极的第二金属是熔化的,熔融盐必须保持在高于或等于第二金属的熔点的温度下。例如当阳极金属为工业纯的铝金属时,熔融盐应保持在高于660℃的温度下。当阳极金属为工业纯的锡金属时,熔融盐应保持在高于232℃的温度下。
可使用任何适用于电解工艺的盐。在ffc工艺中通常使用的盐包括含氯化钙的盐。熔融盐可为含钙的盐,优选地包含氯化钙的盐。由于期望低温操作,特别期望的是熔融盐为含锂的盐,例如优选地包含氯化锂的盐。盐可包含氯化锂和氧化锂。
新鲜的盐可包含残余的碳酸盐并且这些碳酸盐可在阴极上沉积碳,从而增加产物的碳含量。因此,在还原钽酸盐之前预电解盐以除去残留的碳酸盐是有利的。一旦被使用,盐优选地可再用于多次还原。使用经预电解的盐或用过的盐可产生具有较低碳酸盐含量的盐并且可有助于产生具有很低碳含量的钽。
在过程期间由于形成了第二金属与氧的氧化物,阳极上的第二金属被消耗。所述方法可有利地包括还原阳极上形成的氧化物(即包含第二金属和氧的氧化物)以回收和再利用第二金属的另一步骤。进一步还原氧化物的步骤可在电解反应已经完成之后进行。例如可通过碳热还原或标准的ffc还原来处理和还原形成的氧化物。回收的第二金属可返回至阳极。
还原包含第二金属和氧的氧化物的步骤可包括其中将阳极上的熔融材料不断地从阳极泵送至单独的槽或室(在其中熔融材料被还原以回收第二金属,然后第二金属被输送返回至阳极)的系统。由于阳极材料在其被消耗时不断地得到补充,这样的系统可使还原电池工作很长的时间或连续的一段时间。
在优选的实施方案中,原料可包含氧化钛并且阳极包含熔融铝。经还原的原料产物可为掺杂有铝的钛。掺杂有一定比例的铝的钛可具有与纯钛金属不同的物理特性。例如,用铝掺杂钛可改善其强度。经还原的原料可为包含0.01重量%(wt%)至5重量%的铝的钛合金。例如,经还原的原料可包含0.01重量%至3.0重量%的铝,或者0.05重量%至2.0重量%或0.10重量%至1.50重量%或0.50重量%至1.0重量%的铝。
在一个优选实施方案中,原料包含钛酸锂并且第二金属为铝。在一个特别优选的实施方案中,原料包含钛酸钙并且第二金属为铝。
当涉及到能量消耗时,与常规碳阳极相比,使用铝阳极可提供特定的优点。由于铝的过电势比碳的过电势低,与使用碳阳极的电池相比,使用铝阳极的电池可在更低的电压下实现电池原料的还原。例如,与使用碳阳极进行相似的还原的3v至3.5v相比,使用铝阳极的电池可在1.5v至2v的电压下运行。此工作电压的降低可具有明显有益的成本影响。
在另一些优选的实施方案中,原料可包含氧化钛而阳极包含熔融锡。经还原的原料产物可为掺杂有锡的钛。经还原的原料可为包含0.01重量%(wt%)至5重量%的锡的钛合金。例如,经还原的原料可包含0.01重量%至3.0重量%的锡或者0.05重量%至2.0重量%或0.10重量%至1.50重量%或0.50重量%至1.0重量%的锡。
在一个优选实施方案中,原料包含钛酸锂并且第二金属为锡。在一个特别优选的实施方案中,原料包含钛酸钙并且第二金属为锡。
从原料中除去的氧与阳极材料反应形成氧化物,意味着电池内没有氧气放出。这可具有显著的工程益处,因为其消除了处理高温氧尾气的必要性。
由于没有进行电解反应所需的碳,该工艺的产物(即经还原的原料)几乎没有碳污染。虽然在一些金属的直接电解还原中碳污染不是问题,但是对于其他应用和金属,任何水平的碳污染都是不期望的。使用该方法能够以商业可行的速率将氧化物材料直接还原成金属,同时消除碳污染。此外,虽然在电解期间阳极材料被消耗,但是可以回收由该消耗产生的氧化物、还原该氧化物并再利用阳极材料。
优选地,在还原工艺期间,在电解池内不存在与熔融盐接触的碳。特别优选地,由该工艺产生的经还原的原料可包含小于100ppm的碳,例如小于50ppm或小于25ppm碳。
该方法可用于回收金属材料,例如已经被氧污染的金属粉末。例如原料可为在氧的存在下被加热并因此被氧污染的金属粉末。这样的粉末可例如形成为3d打印工艺(如选择性激光烧结或选择性激光熔化)的废产物。可将在这样的工艺中未并入到产物中的粉末加热至高温并再次冷却,从而拾取不期望的氧。然后该方法可便利地用于回收被污染的粉末。
在第二方面中,用于通过电解还原包含氧和第一金属的原料来生产金属的装置包括布置成与熔融盐接触的阴极和阳极,阴极与原料接触而阳极包含熔融金属。熔融金属为铝或锡。
装置还可包括连接至阴极和阳极的电源。该电源能够在阴极和阳极之间施加电势使得在使用中从原料中除去氧。
具体实施方式
现在参照附图对本发明的特定实施方案进行描述,其中
图1为例示了根据本发明的一个或更多个方面的装置的示意图;以及
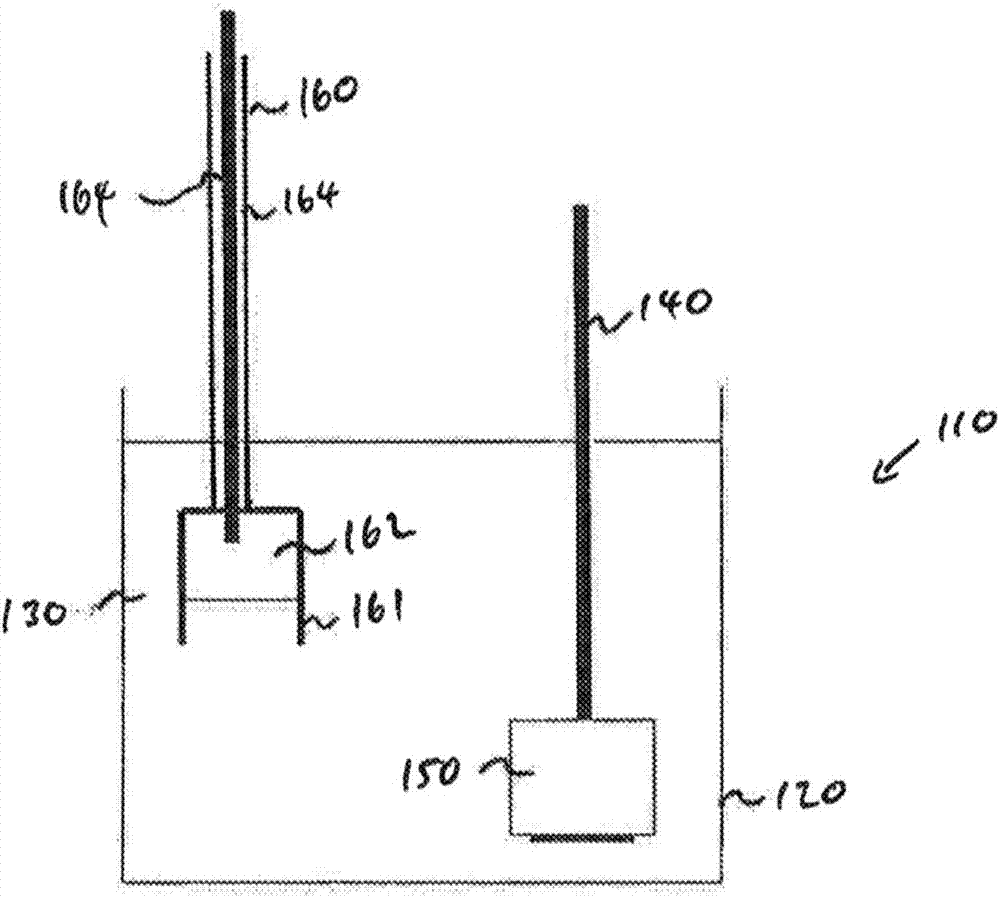
图2为根据本发明的一个或更多个方面的装置的第二实施方案的示意图。
图1示出了用于电解还原含氧原料(如氧化物原料)的电解装置10。装置10包括含有熔融盐30的坩埚20。包含金属氧化物50的粒料的阴极40被布置在熔融盐30里。阳极60也被布置在熔融盐里。阳极包括含有熔融金属62的坩埚61,和布置成一端与熔融盐62接触并且另一端偶接至电源的阳极连接棒63。阳极连接棒63被绝缘护套64包覆,使得连接棒63不与熔融盐30接触。
坩埚20可由任何合适的绝缘难熔材料制成。本发明的一个目的在于避免被碳污染,因此坩埚不是由碳材料制成的。合适的坩埚材料可为氧化铝。金属氧化物50可为任何合适的金属氧化物。采用直接电解工艺(例如ffc工艺)已经还原了大量的金属氧化物,并且在本领域是已知的。金属氧化物50可为例如二氧化钛或五氧化二钽的粒料。含有熔融金属62的坩埚61可为任何合适的材料,但是再次氧化铝可为优选的材料。阳极导棒63可被任何合适的绝缘材料64遮蔽,并且为了该目的,氧化铝可为合适的难熔材料。
熔融金属62为铝或锡,在工作温度下二者在熔融盐中均为液态。熔融盐62必须能够与从金属氧化物中除去的氧离子反应形成熔融金属种类的氧化物。熔融盐30可为用于电解还原的任何合适的熔融盐。例如盐可为氯化盐,例如包含一部分氧化钙的氯化钙盐。本发明优选的实施方案可使用基于锂的盐,例如氯化锂或包含一部分氧化锂的氯化锂。阳极60和阴极40连接至电源以使电势能够施加到一侧的阴极40和与其相连的金属氧化物50与另一侧的阳极60和与其相连的熔融金属62之间。
在图1中所示的装置的布置假定熔融金属62的密度比熔融盐30更高。该布置可为合适的,例如,其中盐为氯化锂盐而熔融金属为熔融铝。然而,在一些情况下,熔融金属的密度可能比用于还原的熔融盐更低。在这样的情况下,在图2中所示的装置布置可能是合适的。
图2例示了用于通过电解还原氧化物原料来生产金属的替代装置。装置110包括含有熔融盐130的坩埚120,阴极140包含金属氧化物150的粒料,并且阴极140和金属氧化物150的粒料被布置成与熔融盐130接触。将阳极160也布置成与熔融盐130接触,并且包括被绝缘材料164包覆的金属阳极连接棒163。阳极160的一端偶接至电源而阳极的另一端与含于坩埚161内的熔融盐162接触。使坩埚161颠倒以保持密度比熔融盐130更低的熔融金属162。该布置可能是合适的,例如,其中熔融金属为液态的铝-镁合金并且熔融盐为氯化钙。
本领域技术人员将能够查找数据图表以确定具体的熔融金属的密度是否比组合用于电解还原工艺的具体的熔融盐更高或更低。因此,可以直接地确定根据图1中所示的装置或根据图2中所示的装置是否最适于进行还原。
虽然图1和图2中所示的装置的说明示出了其中原料粒料附着至阴极的布置,但是清楚的是其他结构也在在本发明的范围内,例如氧化物原料可为颗粒或粉末的形式并且可仅保持在电解池中阴极板的表面上。
将参照图1用常用的术语对操作装置的方法进行描述。将包含金属氧化物50的阴极40和包含熔融金属62的阳极60布置成与电解池10的电解室20内的熔融盐30接触。氧化物50包含第一金属的氧化物。熔融金属为铝,其能够被氧化。在阳极和阴极之间施加电势使得氧从金属氧化物50中除去。该氧被从金属氧化物50输送至阳极,在此氧与熔融铝62反应形成氧化铝。因此氧从氧化物50中除去并且保留在熔融阳极金属的第二氧化物中。
用于通过这样的工艺(如ffc工艺)来操作这样的电解池以使氧被除去的参数是已知的。优选地,电势为使得氧从金属氧化物50中除去并被输送至阳极的熔融金属62,而不使熔融盐30发生任何显著的分解。该工艺的结果是金属氧化物50转化为金属而熔融金属62至少部分地转化为金属氧化物。然后还原的金属产物可从电解池中除去。
本发明人基于该一般性方法进行了大量的具体试验,并且这些在下文进行描述。采用多种技术分析实施例中所产生的金属产物。使用了以下技术。
采用eltracs800分析仪进行碳分析。
采用eltraon900分析仪进行氧分析。
采用micromeriticstristar表面积分析仪测量表面积。
采用malvernhydro2000mu粒径测定仪测量粒径。
实验1
用作阳极材料的铝为由acrosorganics提供的99.5%al粒(shot)。混合的氧化钛、氧化铌、氧化锆和氧化钽的原料粒料是通过四种氧化物粉末的湿混合、然后干燥、压制成粒料并且在1000℃下烧结2小时来制备的。
将28克混合氧化物50的原料粒料连接至钽棒40并用作阴极。将150克的铝62装入氧化铝坩埚61中,并且经由包覆在致密氧化铝管64中的钽连接棒63连接至电源。该构造用作阳极60。将1千克氯化钙30用作电解质并装入大的氧化铝坩埚20内。阳极和粒料布置在熔融盐30内并将盐的温度升至约830℃。
在恒定电流模式下操作电池。在阳极和阴极之间施加4安培的恒定电流持续23.4小时。在此期间,阳极和阴极之间的电势保持在大概1.5伏特。
在电解期间在阳极上没有气体放出。这是由于在熔融铝阳极62中形成氧化铝。在电解反应期间,通过336680库仑的总电荷。
在23.4小时的时间段之后,将阴极和阴极粒料除去并且发现阴极粒料50已经还原为金属合金。分析表明金属合金被铝污染。还原产物的氧分析提供2289ppm的平均值,82ppm的碳含量和4560ppm的铝含量。
氧化铝在还原温度下为固体。表面上形成的氧化铝可能被束缚在氧化铝坩埚中的熔融铝内,并且因此释放更多的熔融铝以与另外的氧离子反应。
实验2
为了证明本发明的方法提供的碳含量下降,使用碳阳极替代熔融铝阳极重复实验1。
混合的氧化钛、氧化铌、氧化锆和氧化钽的原料粒料是通过四种氧化物粉末的湿混合、然后干燥、压制成粒料并且在1000℃下烧结2小时来制备的。
将28克混合氧化物50的原料粒料连接至钽棒并用作阴极。碳阳极经由包覆在致密氧化铝管中的钽连接棒连接至电源。将1千克氯化钙用作电解质并装入大的氧化铝坩埚内。阳极和粒料布置在熔融盐内并将盐的温度升至约830℃。
在恒定电流模式下操作电池。在阳极和阴极之间施加4安培的恒定电流持续18小时。在此期间,阳极和阴极之间的电势保持在大概1.5伏特。
在电解反应期间,通过259039库仑的总电荷。
在18小时的时间段之后,将阴极和阴极粒料除去并且发现阴极粒料50已经还原成金属合金。还原产物的氧分析提供了4039ppm的平均氧值和3373ppm的碳含量。在经还原的金属合金中没有检测到铝。
这表明使用碳阳极产生碳含量为3373ppm(比当使用铝阳极时相同的经还原的原料中所产生的82ppm碳含量高得多)的经还原的原料。
实验3
将45克五氧化二钽50的粒料连接至钽棒40并用作阴极。将150克铝62装入氧化铝坩埚61中,并经由包覆在致密的氧化铝管64中的钽连接棒63连接至电源。该构造用作阳极60。将1.6千克氯化钙30用作电解质并装入大的氧化铝坩埚20内。将阳极和粒料布置在熔融盐30内并将盐的温度升至约830℃。
在恒定电流模式下操作电池。在阳极和阴极之间施加4安培的恒定电流持续20小时。在此期间,阳极和阴极之间的电势保持在大概1.5伏特至2.5伏特。
在电解期间在阳极上没有气体放出。这是由于在熔融铝阳极62中形成氧化铝。在电解反应期间,通过289391库仑的总电荷。
在还原之后,对所得的金属钽产物进行筛分并分析。发现被500μm筛截留的粗材料包含5590ppm的o、20ppm的c并且表面积为3.4464m2/g。通过筛的细材料包含5873ppm的o、87ppm的c并且表面积为1.3953m2/g。产物包含1.32重量%至2.01重量%的铝。
实验4
在另外的实施例中,由ilukanr95天然金红石粉末的样品制造28g粒料。对粉末进行筛分以选择由粒径范围为150微米至212微米的颗粒组成的部分。采用熔融铝阳极在氯化钙中还原粒料。还原产物的edx分析显示1.3重量%的铝含量。
- 还没有人留言评论。精彩留言会获得点赞!