一种测定奶粉、米粉和乳米粉中低聚半乳糖含量的方法及其应用与流程
本发明属于保健食品检测领域,具体涉及一种采用Xamide酰胺色谱柱测定奶粉、米粉和乳米粉中的低聚半乳糖含量的方法及其应用。
背景技术:
低聚半乳糖(Galactooligosaccharides,GOS)是一种活性低聚多糖,是以乳糖为底物,在具有半乳糖基转移活性的β-半乳糖苷酶作用下,首先将乳糖水解成半乳糖和葡萄糖,然后再将半乳糖转移到半乳糖分子上生成低聚半乳糖。一般情况下,低聚半乳糖的分子结构是在半乳糖或葡萄糖分子上连接1~7个半乳糖基,即Gal-(Gal)n-Glc/Gal(n为0-6),分子量约300-2000。低聚半乳糖是一种具有天然属性的功能性低聚糖,能促进肠内益生菌群如双歧杆菌、乳酸菌的增殖,同时促进肠胃蠕动,改善肠道功能,预防便秘;能改善钙铁锌等矿物质的吸收,防止骨质疏松,降低龋齿发病率;能改善脂类的代谢,降低血脂和胆固醇。因此,目前常作为一种新的功能性食品广泛应用于饼干、馅饼、面包、果酱、发酵乳、饮料、冰淇淋、糖果、奶粉、口服液等多种食品加工业。不仅如此,低聚半乳糖还被成为母乳化的益生元,成为婴幼儿食品的配方之一。
然而,由于低聚半乳糖属于一类低聚杂糖,该分离检测技术一直是当前研究的难点和重点。目前还没有固定的低聚半乳糖的标准品,不能直接测定其含量。因此,只能通过酶水解使低聚半乳糖转化为半乳糖的方式来计算低聚半乳糖的含量,即用水解后半乳糖的总量减去游离的半乳糖含量和无水乳糖水解产生的半乳糖含量,从而根据公式计算出待测样品中低聚半乳糖的含量。
根据相关文献报道,检测保健食品中的低聚半乳糖含量广泛应用的方法一般是采用糖柱、氨基柱或凝胶柱去分离GOS经酶水解后的产物,并通过高效液相色谱(HPLC)结合蒸发光散射检测器(ELSD)或示差折光检测器(RID)检测半乳糖。但是,保健食品中的成分较多,特别是高乳糖含量的奶粉、米粉及其混合物的酶水解产物如葡萄糖和半乳糖就具有多种旋光异构体,均属于大极性化合物,出峰时间接近,严重干扰了GOS的定量检测。因此,常规的分离液相柱均难以实现对这类化合物的有效分离,而且一般用来分离大极性化合物的氨基柱的稳定性较差。
另外,对于乳糖和半乳糖含量高的样品,乳糖和蔗果三糖的出峰时间相似,影响乳糖的出峰;根据检测原理,如果样品中乳糖含量过高,即低聚半乳糖含量和乳糖含量之比小于1:10的乳制品,例如配方奶粉,检测的误差就会加大,这个缺点也是AOAC方法不能弥补的。
综上所述,如何有效的分离低聚糖酶水解产物中葡萄糖、半乳糖及其多种旋光异构体,成了米粉、奶粉及其混合产品中低聚半乳糖定量分析的瓶颈,并且有效去除高乳糖含量乳制品中的乳糖干扰,这也是本发明重点解决的问题。
技术实现要素:
为克服上述技术缺陷,本发明提供了一种测定奶粉、米粉及其混合产品中低聚半乳糖含量的方法,该方法操作方便,能准确定量待测样品中的低聚半乳糖含量,所述混合产品包括乳米粉。
本发明的测定方法采用酰胺色谱柱在高效液相色谱-蒸发光散射检测器上进行。
所述方法包括以下检测步骤:
(1)提取和去除杂多糖干扰:称0.5g样品于50mL离心管中,加入纯水,用醋酸溶液调节pH至4~5,溶解振荡5min;加入杂多糖沉淀剂,振荡5-10min后,10000r/min离心,用定量滤纸过滤后得到澄清滤液,滤液低压浓缩至干,得到浓缩物;
(2)降低乳糖对结果的干扰:往所述步骤(1)中所得到的浓缩物中加入异丙醇-乙醇混合有机试剂,涡旋振荡5min,过滤,取滤渣,如此重复五次,滤渣低压浓缩至干获得浓缩物;
(3)制备酶解前待测液:将所述步骤(2)中得到的浓缩物用水定容至5ml,得待测样品溶液;取1mL过0.22μm滤膜至进样瓶中;
(4)制备酶解后待测液:取所述步骤(3)中的待测样品溶液2mL加入0.2mL的β-半乳糖苷酶,酶解,酶解后取1ml过0.22μm滤膜于进样瓶中;
(5)往空白样品中添加不同浓度水平的半乳糖标准品和乳糖标准品,建立所述半乳糖和所述乳糖的线性回归方程,确定线性范围,并且进行方法学考察验证;
(6)测定:在配备有蒸发光散射检测器的岛津LC-20AT系列高效液相色谱上,选择酰胺色谱柱,以乙腈-甲醇作为流动相,设置柱温和进样量,分别检测所述步骤(3)制备的酶解前待测液和所述步骤(4)制备的酶解后待测液,并记录对应的半乳糖和乳糖的峰面积;
(7)计算:先通过线性回归方程,计算酶解前后待测样品中的半乳糖含量以及乳糖含量,再用酶解后半乳糖的总量减去游离的半乳糖含量和乳糖酶解产生的半乳糖含量,经过公式计算出检测样品中低聚半乳糖的含量。
优选的,所述步骤(1)中的杂多糖沉淀剂为乙醇;所述乙醇的体积与所述步骤(1)中加入的纯水的体积的比例为4:1。
优选的,所述步骤(2)中的异丙醇和乙醇的体积比为4:1。
优选的,所述步骤(4)中的β-半乳糖苷酶活度为2000U/mL;酶解温度为55℃;酶解时间为0-6h。
优选的,所述步骤(5)中的半乳糖标准品和乳糖标准品设置为6个浓度水平,分别为500、800、1000、2000、4000和8000mg/kg。
优选的,所述步骤(6)中的酰胺色谱柱为华普XAmide色谱柱,4.6mm×250mm×5.6um;流动相乙腈和甲醇的体积比为50~80:50~20;柱温为30℃;进样量为2~10μL。
优选的,所述步骤(7)中的公式为GOS=k*(GB-GA-GL);其中,公式中GB为酶解后半乳糖的含量;GA为游离态半乳糖的含量;GL为乳糖酶解所产生半乳糖含量,为乳糖含量除以换算系数1.9;k为半乳糖转换成GOS的换算系数,k=(180+162n)/(180*n);所述换算系数k为1.49。
本发明使用的XAmide酰胺柱是一种亲水作用色谱柱,具有结构独特的中性酰胺键合相,亲水性突出,使用高比例的乙腈/水或缓冲盐做流动相可以保留在传统的反相色谱柱上很难保留的强极性化合物。相较氨基键合相和无键合相,Xamide的中性键合相较氨基键合相和无键合相纯硅胶具有更高的稳定性。
与现有技术相比,本方法采用XAmide酰胺柱作为分离色谱柱,稳定有效地分离低聚半乳糖的酶水解产物半乳糖和葡萄糖及其差向异构体等强极性物质;本发明方法操作简单、快捷、有效,能准确定量奶粉、米粉及其混合产品中低聚半乳糖的含量,线性范围宽,具有干扰少、检出限低、精确度高等优点,可以广泛应用于食品检测领域中乳制品低聚半乳糖的含量。
附图说明
图1是分离低聚半乳糖异构体的液相图,流动相为乙腈-甲醇=51:49(v/v);
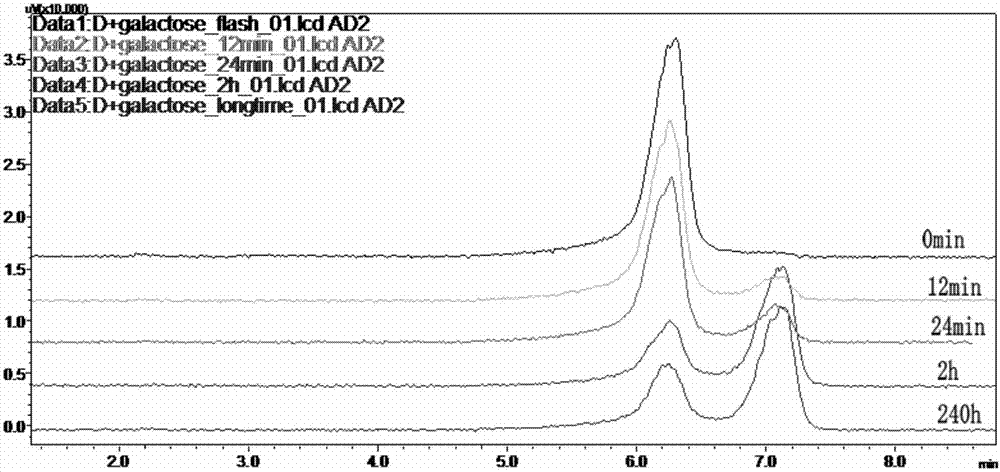
图2是半乳糖标准品在0min,12min,24min,2h,240h不同溶解时间的液相图;
图3是葡萄糖标准品在0min,12min,2h不同溶解时间的液相图;
图4是有效分离半乳糖和葡萄糖的重合液相图,流动相为乙腈-甲醇=51:49(v/v);
图5是分离半乳糖和葡萄糖的液相图,流动相为乙腈:水=70:30(v/v);
图6是不同进样体积下葡萄糖、半乳糖和乳糖的分离液相图;
图7是奶粉样品在酶解0min、18h和28h后的检测液相色谱全景图,流动相为乙腈:甲醇=51:49(v/v);
图8是米粉样品在酶解0min、30min、1.5h、3h、6h和9h后的检测液相色谱全景图,流动相为乙腈:甲醇=51:49(v/v);
图9是米粉样品采用乙醇-异丙醇(1:0)除乳糖干扰后的检测液相图;
图10是米粉样品采用乙醇-异丙醇(1:3)除乳糖干扰后的检测液相图;
图11是米粉样品采用乙醇-异丙醇(1:4)除乳糖干扰后的检测液相图;
图12是奶粉样品在不同酶解时间0min、30min、2h和4h后的检测液相色谱局部图,流动相为乙腈:甲醇=51:49(v/v);
图13是半乳糖的标准曲线;
图14是乳糖的标准曲线。
具体实施方式
为使本发明更加容易理解,下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围,下列实施例中未提及的具体实验方法,通常按照常规实验方法进行。
实施例一:检测方法的选择及优化
1、样品前处理方法
(1)提取和去除杂多糖干扰:称0.5g样品于50mL离心管中,加入10mL水,用醋酸溶液调节pH至4~5之间,溶解振荡5min;然后加入40mL乙醇,振荡5-10min后,10000r/min离心,用定量滤纸过滤后得到澄清滤液旋蒸至干。
(2)除乳糖干扰:往所述步骤(1)中所得到的浓缩物中加入50mL体积比为4:1的异丙醇-乙醇混合有机溶剂,涡旋振荡5min,过滤,取滤渣,如此重复五次,滤渣低压浓缩至干获得浓缩物。
(3)制备酶解前待测液:将所述步骤(2)中所得到的浓缩物用水定容至5ml,得待测样品溶液;取1mL过0.22μm滤膜至进样瓶中。
(4)制备酶解后待测液:取所述步骤(3)中所得到的待测样品溶液2mL加入0.2mL的β-半乳糖苷酶,酶解,酶解后取1ml过0.22μm滤膜于进样瓶中。
2、色谱条件的选择及优化
(1)色谱条件:岛津LC-20AT系列高效液相色谱系统,配备有蒸发光散射(ELSD)系统;流速为1ml/min,进样体积2~50μL。
(2)色谱柱:华普XAmide色谱柱,4.6mm×250mm×5.6um;结合柱效和稳定性俩方面考虑,柱温设定为室温,即30±10℃时,所述酰胺柱对糖的分离效果较好。
(3)流动相条件的选择及优化
本实施例首先往空白检测样品中添加低聚半乳糖作为混标,摸索能实现有效分离低聚半乳糖流动相条件,发现当流动相为乙腈-甲醇=50~80:50~20(V/V)时,低聚半乳糖的峰分离得较好。图1是乙腈-甲醇=51:49(V/V)作为流动相分离低聚半乳糖异构体的液相图,柱长250mm,柱温30℃,流速1mL/min。但是,低聚半乳糖是含3个到10个糖元的糖,有3糖、4糖、5糖、6糖、7糖、8糖、9糖和10糖,每种糖都有多个差向异构体,结构复杂,在6.0min~32.0min时会出现很多峰,并且由于没有固定的GOS标准品,无法直接检测到具体低聚半乳糖后进行加和,因而国际上通用的做法是采用酶解法进行检测,也就是通过酶水解使低聚半乳糖转化为半乳糖,用水解后半乳糖的总量减去游离的半乳糖含量和乳糖水解产生的半乳糖含量,从而根据公式GOS=k*(GB-GA-GL)计算出检测样品中低聚半乳糖的含量。其中,公式中GB为酶解后半乳糖的含量;GA为游离态半乳糖的含量;GL为乳糖酶解所产生半乳糖含量,为乳糖含量除以换算系数1.9;k为半乳糖转换成GOS的换算系数,k=(180+162n)/(180*n),该系数一般为1.49。
D-(+)-半乳糖有α-D-半乳糖和β-D-半乳糖两种构型,D-(+)-半乳糖在本研究体系下在刚溶解时只有1个响应峰(保留时间为6.25min),随着溶解时间的延长该响应峰面积慢慢减少,而保留时间为7.25min的响应峰面积慢慢增加,至2h以后达到平衡。类似的,D-(+)-葡萄糖也同样在刚溶解时只有1个响应峰(保留时间为6.25min),该峰面积随着溶解时间的延长而减少,而保留时间为6.75min的响应峰面积逐渐增加,在2h后达到平衡。图2是D-(+)-半乳糖标准品在不同溶解时间(0min,12min,24min,2h,240h)的液相图,图3是D-(+)-葡萄糖标准品在不同溶解时间(0min,12min,2h)的液相图,两液相图均显示,半乳糖和葡萄糖在溶解2h后差向异构化达到平衡,两种糖的差向异构体比值保持不变。
因此,常规分离条件下难以同时分离半乳糖和葡萄糖,而在本实施例中,采用具有酰胺基键和相的XAmide酰胺色谱柱能同时实现这两种单体差向异构体的有效分离。图4是有效分离半乳糖和葡萄糖的重合液相图。采用乙腈-甲醇作为流动相,当乙腈浓度比例达51%以上时,葡萄糖和半乳糖各自的两种差向异构体都能分离开,在乙腈-甲醇=51:49(v/v)的分离条件下,D-(+)-葡萄糖的差向异构体的保留时间分别为6.25min和6.75min;而D-(+)-半乳糖的差向异构体的出峰时间分别为6.25min和7.25min,即两种糖的第一个差向异构体的响应峰(6.25min)叠加,另外一个异构体的出峰时间存在差别,而且在溶解2h后差向异构化均趋向平衡,因而可以采用其中一个响应峰作为代表,计算半乳糖的含量。
进一步调整乙腈的浓度比例,随着比例的增大,图4中的3个色谱峰的保留时间相差也越大,相应的信号响应值也随着降低。当选择乙腈浓度比例为70%时,能较好分离葡萄糖和半乳糖的另一个异构体,且响应强度较高,适合于峰面积积分。图5是流动相为乙腈:水=70:30(v/v)时同时分离半乳糖和葡萄糖的液相图。
进一步调整样品进样量,随着进样量的减少,图5中半乳糖和葡萄糖的第二个差向异构体的保留时间越大,相应的信号响应值也随着降低。当乙腈浓度比例为70%,选择进样量为5~10uL时,能较好分离葡萄糖和半乳糖的另一个异构体,适合于峰面积积分。图6是不同进样体积下葡萄糖、半乳糖和乳糖的分离曲线。
3、沉淀剂的选择及优化
(1)杂质低聚葡萄糖峰的指认:在本发明方法前期对奶粉样品和米粉样品中的总物质成分进行分析的过程中,发现奶粉样品和米粉样品中都存在一些出峰时间和低聚半乳糖接近的4个疑峰,即1、2、3、4号,随着酶解时间延长,4号疑峰呈降低趋势,1、2、3号疑峰分别在不同时间段呈先增高后降低的趋势,其中1号峰位置与乳糖位置靠近,极容易误识别为乳糖。与完全不含低聚半乳糖的空白样品的分析结果对比并结合多种麦芽糖标准品对照,发现1、2、3、4峰分别代表麦芽糖、麦芽三糖、麦芽四糖和麦芽五糖,这些糖可由低聚葡萄糖酶解而成。图7是奶粉酶解0min、18h和28h后的检测液相色谱全景图,图8是米粉酶解0min、30min、1.5h、3h、6h和9h后的检测液相色谱局部图,流动相为乙腈:甲醇=51:49,柱温30℃。
(2)沉淀剂的选择和优化
本实施例对比考察了无机物如亚铁氰化钾-乙酸锌和有机溶剂如醇-水作为沉淀剂的沉淀效果,发现亚铁氰化钾-乙酸锌容易残留在样品中,对半乳糖苷酶有毒害作用,能使酶解失效;并且亚铁氰化钾-乙酸锌对纤维素,淀粉的沉淀效果不明显,处理后样品粘度仍然较高。而采用有机溶剂-水作沉淀剂,不仅可通过低压浓缩等方法除去残留的有机溶剂,使酶解成功进行,还可以沉淀大部分纤维素和淀粉。
为了选择出一种沉淀效果最好的沉淀剂,本发明还比较了甲醇-水、乙醇-水和乙腈-水等4种有机溶剂-水(4:1)双相体系对蛋白质、杂多糖等干扰杂质的沉淀能力,以及对低聚糖的提取能力。为了进一步考察以上4种有机溶剂-水双相体系是否容易引入低聚葡萄糖等杂糖,本实施例采用甲醇-水、乙醇-水和乙腈-水双相体系提取沉淀空白米粉样品(罐标无GOS)中的低聚糖,低压浓缩后重新定容,取一部分作为酶解前样品,另一部分溶液用半乳糖苷酶进行酶解,酶解时间为0min、30min和12h。表1为有机溶剂-水双相体系沉淀剂优化的实验结果,对比酶解前后分析结果,发现用乙醇水提取的空白米粉样品,随着酶解时间的变化其峰形并无明显变化,说明应用乙醇/水(4:1)并未引入低聚葡萄糖等杂糖;而用甲醇水提取的空白米粉样品容易引入多种杂糖。乙腈-水双相体系及乙醇-水双相体系的沉淀效果较好,而且对其他非低聚半乳糖的低聚糖类物质提取率不高;用甲醇-水双相体系配合pH调节能使得沉淀效果变好,对低聚糖提取能力较强。
表1
注:+表示存在杂糖干扰,-表示不存在杂糖干扰。
4、除乳糖干扰方法的确定
对于乳糖和半乳糖含量高的样品,乳糖和蔗果三糖的出峰时间相近,对GOS的检测存在一定干扰,乳糖含量越高检测误差越大。因此,在对高乳糖乳制品进行检测的过程中,去除乳糖干扰很有必要。
乙醇能溶解乳糖和低聚半乳糖,异丙醇能溶解微量乳糖,不能溶解低聚半乳糖,通过不同乙醇/异丙醇比例考察除乳糖干扰结果显示,当乙醇比异丙醇含量为4:1时,大部分乳糖可溶解于该混合溶剂中,低聚半乳糖几乎不能溶解于该混合溶剂中。因此,可将干燥提取物与该混合溶剂涡旋振荡后,过滤,收集几乎不含乳糖的滤渣,富集低聚半乳糖。滤液收集作为待测溶液,上机分析所述滤液中乳糖和低聚半乳糖的含量。色谱条件为:乙腈:水=75:25(v/v),30℃,色谱柱长度为250mm。
通过与乳糖和低聚半乳糖对照品的液相色谱图对比,保留时间为5.8min时的峰可指认为乳糖,7.5min以后的可指认为低聚半乳糖。图9是乙醇-异丙醇(1:0)除乳糖干扰液相图,图10是乙醇-异丙醇(1:3)除乳糖干扰液相图,图11是乙醇-异丙醇(1:4)除乳糖干扰液相图。通过对比实验结果发现,随着异丙醇比例的增加,低聚半乳糖溶解度逐渐变小,在4倍的异丙醇下几乎不溶解低聚半乳糖。色谱条件为:乙腈:水(51:49),30℃。
5、酶解时间的确定
以奶粉为酶解的对象进行对酶解时间考察,酶解时间分别设为0min、30min、2h、4h和6h,流动相为乙腈:水=75:25(v/v),30℃柱温。对比发现50μL的活度为2000U/mL的半乳糖苷酶在55℃下,反应液体积为10mL,仅用30min就能把所有的乳糖和低聚半乳糖酶解完全,图12为奶粉样品在不同酶解时间0min、30min、2h和4h下的检测液相色谱局部图。
实施例二:奶粉和米粉中低聚半乳糖的含量测定
1、标准稳定性研究
标准储备液三个月进行期间核查,比较新旧工作曲线的响应值。结果表明标准储备液在三个月内稳定。
2、方法学考察
(1)线性范围和线性回归方程
通过往空白样品中添加不同浓度水平的半乳糖标准品和乳糖标准品,分别绘制半乳糖和乳糖的标准曲线,在500mg/kg-8000mg/kg线性范围内半乳糖和乳糖质量浓度与峰面积线性关系良好,其线性回归方程及相关系数见表2,图13为半乳糖的标准曲线,图14为半乳糖的标准曲线。
表2
(2)精确度、重复性和回收率试验
回收率实验:本实验中都是添加低聚半乳糖混合物来计算回收率。在低聚半乳糖完全酶解的前提下,若半乳糖的回收率能达到要求即认为此法中GOS的回收率也能达到要求。浓度水平设为4个,每个浓度重复6次,测定方法的回收率。
精确度和重现性实验:分别测定含不同浓度的低聚半乳糖的奶粉和米粉样品,重复测定6次,计算相对标准偏差(RSD)。
表3为回收率、精确度和重现性的实验结果,结果表明方法的总体平均回收率为84%~118%,方法的相对标准偏差为1.78~5.81,回收率能够满足日常检测需要,而且RSD范围主要集中在2~5之间,说明本发明方法的精密度和重现性良好。
表3
实施例三:一种采用XAmide液相柱测定奶粉和米粉中低聚半乳糖的应用
采用以上两个实施例建立起的测定方法,对市场上19种奶粉和16种米粉样品进行了检测,分别获得酶解前后半乳糖和乳糖的含量,通过公式GOS=k*(GB-GA-GL)计算出检测样品中低聚半乳糖的含量。其中,公式中GB为酶解后半乳糖的含量;GA为游离态半乳糖的含量;GL为乳糖酶解所产生半乳糖含量,为乳糖含量除以换算系数1.9;k为半乳糖转换成GOS的换算系数,k=(180+162n)/(180*n),该系数一般为1.49。表4为不同品牌的奶粉的检测结果。
表5为不同品牌的米粉的检测结果
表4
表5
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
- 还没有人留言评论。精彩留言会获得点赞!