用于血型检测的微流控芯片的制作方法
本实用新型涉及一种微流控芯片,特别涉及一种用于血型检测的微流控芯片。
背景技术:
微流控芯片是当前微全分析系统(Micro Total Analysis Systems,μ-TAS)发展的热点领域,它是以芯片为载体,并通过与生物、化学、药物筛选等技术的结合,完成包括试剂加载、分离、反应、检测等在内整个过程的技术。近年来,随着生物芯片技术的快速发展,微流控芯片在生命科学领域,分析化学和生物医学领域发挥着越来越重要的作用。
输血相容性检测是确保临床输血安全的必要条件,主要检测内容包括三个部分:血型检定、抗体检定、交叉配血;根据输注成分的不同,也可分为红细胞血型相容性试验和血小板血型相容性试验。血型检定是确保献血者和受血者的血型一致,输注的红细胞或血小板不使受者产生相应的免疫抗体;抗体检定是检测受血者血清中不存在与输入的红细胞或血小板抗原相对应的特异性抗体;交叉配血则是直接观察受血者血清中是否存在与输注红细胞或血小板相对应的特异性抗体,以及输入的血浆中是否存在与受血者红细胞或血小板相对应的特异性抗体。这些特异性抗体一般都是指有临床意义的血型抗体,包括完全抗体和不完全抗体,可以说,输血相容性试验主要就是由血型血清学试验技术和相关试剂组成。
以红细胞血型检定为例,检查确定受血者和献血者的红细胞血型,最主要的就是判断ABO血型和RhD血型,因为它们的血型相容性对安全输血临床意义最大。人ABO血型是由其红细胞抗原和血液中的ABO抗体所决定,常规的检定是通过凝集试验:用抗-A和抗-B检查待测红细胞抗原,称为正定型;用A型和B型红细胞检查待测血清中的抗体,称为反定型,健康人正常情况下正反定型相符。唯有新生儿在出生4-6个月之内由于血液中ABO抗体活性太弱且含有来自母亲的抗体,因此新生儿血型只能用正定型方法来检定其ABO血型。相比之下,人RhD血型通常只检测D抗原,即用抗-D检查待测红细胞抗原。需要注意的是,由于RhD抗原的多表位性质,它在高加索人群和中国人群中的发生频率和表达情况有很大差异,需要应用不同的血型定型方案和不同的抗体试剂。
ABO血型检定在献血端对大批献血员的血型进行检测,一般采用纸卡法和微孔板法,纸卡法为手工操作,微孔板法适合自动化操作。发达国家的对献血员的ABO血型检定方法主要采用高通量,自动化的微孔板法;国内是两种方法并存,纸卡法在采血车或者边远基层地方仍广泛使用,其缺点是人为操作,效率较低,人为判读结果,受外界因素干扰较多,此外检测结果无法溯源。另一方面在输血前,如医院等用血机构还需要对ABO血型进行复核检测,必须采用试管法或微柱凝胶法等更可靠的检测方法。试管法为人工操作,步骤较为繁琐,需要多次洗涤等过程,虽然比纸卡法敏感准确,但其缺陷也和纸卡法相似;微柱凝胶法可自动化操作,但对待测标本、试剂质量和仪器要求非常高,且成本较高,这两种方法目前在国内外临床实际中均有采用。对于RhD血型检定,由于其凝集反应不如ABO的强,且反应时间略长,因此发达国家已不提倡用纸卡法或玻片法,推荐使用试管法、微孔板法和微柱凝胶法;而我国很多地方还在应用玻片法检测。
微孔板固相凝集试验和微柱凝胶免疫分析技术都是上世纪90年代开始出现,基于它们发展出目前自动化操作中广泛使用的微孔板法和微柱凝胶法。微孔板法以Immucor公司的Capture R技术最知名,国内尚无相似的产品。微柱凝胶法最早是瑞士达亚美(DiaMed)的专利,后被Bio-Rad收购,国内博讯1996年最早将微柱凝胶国产化,基于微柱凝胶法的血型检测试剂卡已经在国外广泛使用,国内也有大量使用,但是其不断升高的成本限制了试剂卡在国内和发展中国家市场的推广,其应用范围也有局限。微孔板法和微柱凝胶法本质上都是免疫凝集试验,各自具有固定的用途和地位,相互竞争,很长一段时间内不会被完全取代,限于其试剂和仪器的成本,国内及发展中国家市场和临床亟需一种能取代纸卡法和玻片法,同时成本低于微孔板法和微柱凝胶法的新产品。
技术实现要素:
针对现有技术存在的不足,本案提供了一种用于血型检测的微流控芯片。针对玻片法和试管法敏感性较差、结果判断依靠人工,需要较高经验、操作难以规范化和检验结果难以长期保存及溯源等问题,本案开发采用微流控芯片作为载体的ABO/RhDE血型检测系统解决方案,最终实现提高检测通量,简化操作,检验结果可溯源,提高检测精度与效率的目的。
为实现上述目的,本案通过以下技术方案实现:
一种用于血型检测的微流控芯片,其包括有圆盘和若干个均匀间隔分布于该圆盘上的微流体单元;其中,所述圆盘的轴心处设有用于固定于离心机的开口,所述开口边缘设有限位部;
所述微流体单元包括有加样腔体、废液腔体、多个定量腔体以及与每个所述定量腔体一一对应的检测腔体;所述加样腔体中设有加样口;所述加样腔体与所述定量腔体之间设置有节流流道;所述定量腔体与所述检测腔体之间设置有离心微阀;所述定量腔体与定量腔体之间设置有分样流道;所述废液腔体还连接有排气流道,所述排气流道中设置有排气口。
优选的是,所述的用于血型检测的微流控芯片,其中,所述加样口的直径为0.7-1.3mm。
优选的是,所述的用于血型检测的微流控芯片,其中,所述加样腔体的容积为50-150μL。
优选的是,所述的用于血型检测的微流控芯片,其中,所述节流流道的深度为0.4-0.8mm,宽度为0.5-1.3mm。
优选的是,所述的用于血型检测的微流控芯片,其中,所述定量腔体的容积为10-30μL。
优选的是,所述的用于血型检测的微流控芯片,其中,所述离心微阀的深度为0.4-0.8mm,宽度为0.1-0.3mm。
优选的是,所述的用于血型检测的微流控芯片,其中,所述检测腔体的直径为3-5mm,深度为0.4-0.8mm。
优选的是,所述的用于血型检测的微流控芯片,其中,所述废液腔体的容积为20-50μL。
优选的是,所述的用于血型检测的微流控芯片,其中,所述排气口的直径为0.7-1.3mm。
本实用新型的有益效果是:本案通过对微流控芯片结构的改进,提高了血型检测的检测通量,简化了检测操作,使得检验结果可溯源,同时也提高了检测精度与检测效率。
附图说明
图1为用于血型检测的微流控芯片的结构示意图。
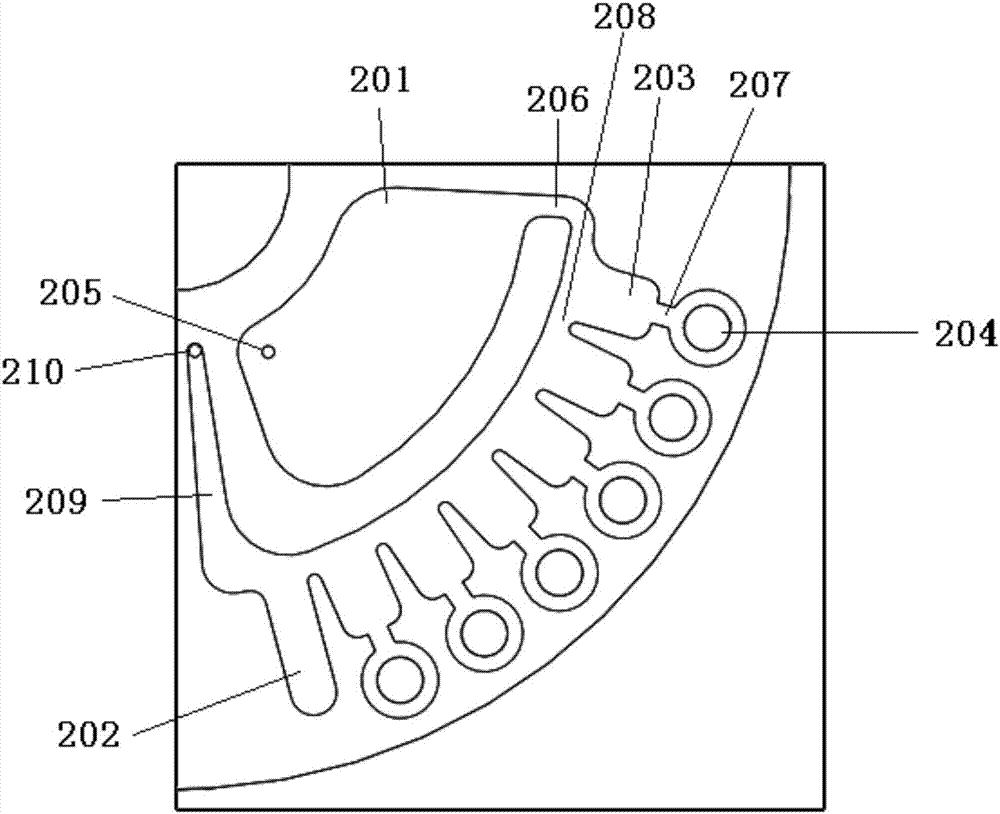
图2为微流体单元的放大图。
具体实施方式
下面结合附图对本实用新型做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
如图1和图2所示,本案列出一实施例的用于血型检测的微流控芯片,其包括有圆盘1和若干个均匀间隔分布于该圆盘1上的微流体单元2;其中,圆盘1的轴心处设有用于固定于离心机的开口3,开口3边缘设有限位部4;
微流体单元2包括有加样腔体201、废液腔体202、多个定量腔体203以及与每个定量腔体203一一对应的检测腔体204;加样腔体201中设有加样口205;加样腔体201与定量腔体203之间设置有节流流道206;定量腔体203与检测腔体204之间设置有离心微阀207;定量腔体203与定量腔体203之间设置有分样流道208;废液腔体202还连接有排气流道209,排气流道209中设置有排气口210。
其中,加样口205的直径优选为0.7-1.3mm。
其中,加样腔体201的容积优选为50-150μL。
其中,节流流道206的深度优选为0.4-0.8mm,宽度优选为0.5-1.3mm。
其中,定量腔体203的容积优选为10-30μL。
其中,离心微阀207为节流型流道,它的深度优选为0.4-0.8mm,宽度优选为0.1-0.3mm。
其中,检测腔体204一般为圆盘型,它的直径优选为3-5mm,深度优选为0.4-0.8mm。
其中,废液腔体202的容积优选为20-50μL。
其中,排气口210的直径优选为0.7-1.3mm。
本案微流控芯片适用于可实现离心旋转的设备上,利用离心力、毛细力来操控流体的运动,并利用两次离心过程,将样品从加样腔体201中依次离心至定量腔体203、检测腔体204,并在此整个过程中实现样品的定量、与试剂的混合以及在检测腔体204中接受光学的探测。其详细过程可描述为:
1)通过加样口205向加样腔体201加入样品;
2)低速离心,转速20-600rpm,时间15-30s,样品在离心力作用下,经过节流流道206、分样流道208后依次充满定量腔体203。多余的样品将流入废液腔体202。
3)再次离心,转速提高至900-1500rpm,时间5s,定量腔体203中的样品在离心力作用下将克服离心微阀207的阻力,进入检测腔体204。并在检测腔体204中与试剂混合。
4)往复式震荡离心,顺时针转速80-150rpm,时间3-5s,逆时针转速80-150rpm,时间3-5s;循环8-20次。此时样品将在震荡力的作用下与试剂充分反应;
5)检测腔体204接受外接的光学探测设备检测。
本案的微流控芯片是一次性的,使用完后即可丢弃,其材质优选为PMMA,芯片直径一般为60-100mm,厚度一般为1-2mm,可利用精密铣床一次性加工完成。检测腔体204中的试剂可以为冻干形式或风干形式预存放于检测腔体204中。
尽管本实用新型的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本实用新型的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本实用新型并不限于特定的细节和这里示出与描述的图例。
- 还没有人留言评论。精彩留言会获得点赞!