一种用于中药注射剂与溶媒配伍稳定性研究的筛选方法与流程
本发明属于制药领域,涉及一种评价中药注射剂与溶媒配伍稳定性研究的新方法,特别是涉及丹红注射液与不同溶媒配伍稳定性筛选方法。
背景技术:
中药注射剂是当代中药剂型的突破性创新,具有生物利用度高、作用迅速等特点,治疗急危重症具有良好的临床疗效。稳定性与安全性是中药注射剂临床应用的关键问题,与其它药物不规范的联合使用是引起中药注射剂不稳定性与不良反应的重要因素。因此,中药注射剂在临床上严禁与化学药物混合使用。但是,临床使用的中药注射剂多为浓缩溶液,在使用前必须先用溶媒稀释到合适的浓度,因此,中药注射剂与注射用溶媒的配伍是无法避免的,评价中药注射剂与注射用溶媒配伍的稳定性对于确保中药注射剂的规范安全使用具有非常重要的意义。
由于中药成分极为复杂,中药注射剂的绝大多数成分尚未明确,目前中药注射剂质量标准及稳定性评价中,或采用颜色、PH值、澄明度等物理指标,或采用紫外分光光度法测定某类成分的总含量,专属性差;或针对个别指标性成分或有效成分进行定量测定。无法反映中药注射剂多组分、多靶点的作用特点。因此在中药注射剂稳定性评价中,目前的方法反映中药注射剂整体成分和生物活性的变化,无法全面反映中药注射剂的安全性及有效性。
因此,建立一种综合评价中药注射剂与溶媒配伍稳定性的新策略至关重要。
技术实现要素:
发明目的:本发明所要解决的技术问题是克服现有技术的不足,提供一种综合评价中药注射剂与溶媒配伍稳定性的新筛选方法。
为了实现以上目的,本发明采取的技术方案为:
一种用于中药注射剂与溶媒配伍稳定性的筛选方法,它包括以下步骤:
将中药注射液与不同临床注射用溶媒配伍混合后,放置不同时间,采用超高效液相串联四级杆质谱联用技术,分析配伍后不同时间特征性成分的稳定性,选择出最佳的中药注射剂与溶媒配伍方案。如图6一种用于中药注射剂与溶媒配伍稳定性研究流程示意图。本发明提供的方法可以筛选注射剂与不同溶媒配伍之间的稳定性。
作为优选方案,以上所述的用于中药注射剂与溶媒配伍稳定性的筛选方法,中药注射液与注射用溶媒配伍混合后,采用超高效液相串联飞行时间质谱联用技术,对靶向成分分析,分析配伍后不同时间特征性成分的稳定性。
作为优选方案,以上所述的用于中药注射剂与溶媒配伍稳定性的筛选方法,对注射液中的全成分进行非靶向整体成分分析,分析配伍后不同时间全成分的稳定性。
作为优选方案,以上所述的用于中药注射剂与溶媒配伍稳定性的筛选方法,中药注射液与注射用溶媒配伍混合后,采用人脐静脉内皮细胞氧化性损伤评价体系,分析配伍后不同时间抗氧化活性的稳定性。
作为优选方案,以上所述的用于中药注射剂与溶媒配伍稳定性的筛选方法,放置时间为2,4,6小时。
作为优选方案,以上所述的用于中药注射剂与溶媒配伍稳定性的筛选方法,所述的中药注射液为丹红注射液。丹红注射液是由丹参750克和红花250克制成的注射液,如菏泽步长制药有限公司生产的丹红注射液,具有活血化瘀,通脉舒络功效。用于瘀血闭阻所致的胸痹及中风,证见:胸痛,胸闷,心悸,口眼歪斜,言语蹇涩,肢体麻木,活动不利等症;冠心病、心绞痛、心肌梗塞,缺血性脑病、脑血栓及肺心病所瘀诸症。
作为优选方案,以上所述的用于中药注射剂与溶媒配伍稳定性的筛选方法,所述的注射用溶媒为质量浓度0.9%氯化钠注射液、5%葡萄糖+0.9%氯化钠注射液、10%果糖注射液、5%其特征在于,对丹酚酸A,丹酚酸B,迷迭香酸,丹参素,原儿茶醛,咖啡酸和紫丁香苷7种靶向成分分析,分析配伍后不同时间特征性成分的稳定性。
作为优选方案,以上所述的用于中药注射剂与溶媒配伍稳定性的筛选方法,超高效液相串联飞行时间质谱联用技术的色谱条件:Acquity UPLC BEH C18色谱柱,柱温和自动进样器温度分别为30℃和10℃,进样量为1μl。以流动相A-0.1%甲酸水和流动相B-乙腈进行梯度洗脱,流速为0.4ml/min;
质谱条件:Xevo Triple Quadrupole Mass Spectrometer(TQ/MS),Waters SynaptTMQTOF/MS,离子源为电喷雾离子化-ESI源;扫描方式为多反应监测;毛细管电压3.0kV;离子源温度150℃;脱溶剂气温度550℃;干燥气流量1000l/h;锥孔气流量50l/h;碰撞气流量0.15ml/min。
作为优选方案,以上所述的用于中药注射剂与溶媒配伍稳定性的筛选方法,梯度洗脱程序为:
0-1.0min,3-3%B;1.0-6.0min,3-40%B;6.0-8.0min,40-95%B;8.0-9.0min,95-95%B;9.0-9.2min,95-3%B。
作为优选方案,以上所述的用于中药注射剂与溶媒配伍稳定性的筛选方法,将丹红注射液与不同溶媒配伍的混合液和人脐静脉内皮细胞预培养1h,然后加入双氧水共培养1h,建立抗氧化能力评价体系。作为优选采用维生素C等量抗氧化能力指数(VCEAC)反映注射液与溶媒配伍不同时间的稳定性。
附图说明
图1所测定7种成分:丹酚酸A、丹酚酸B、迷迭香酸、丹参素、原儿茶醛、咖啡酸和紫丁香苷的化学结构式图。
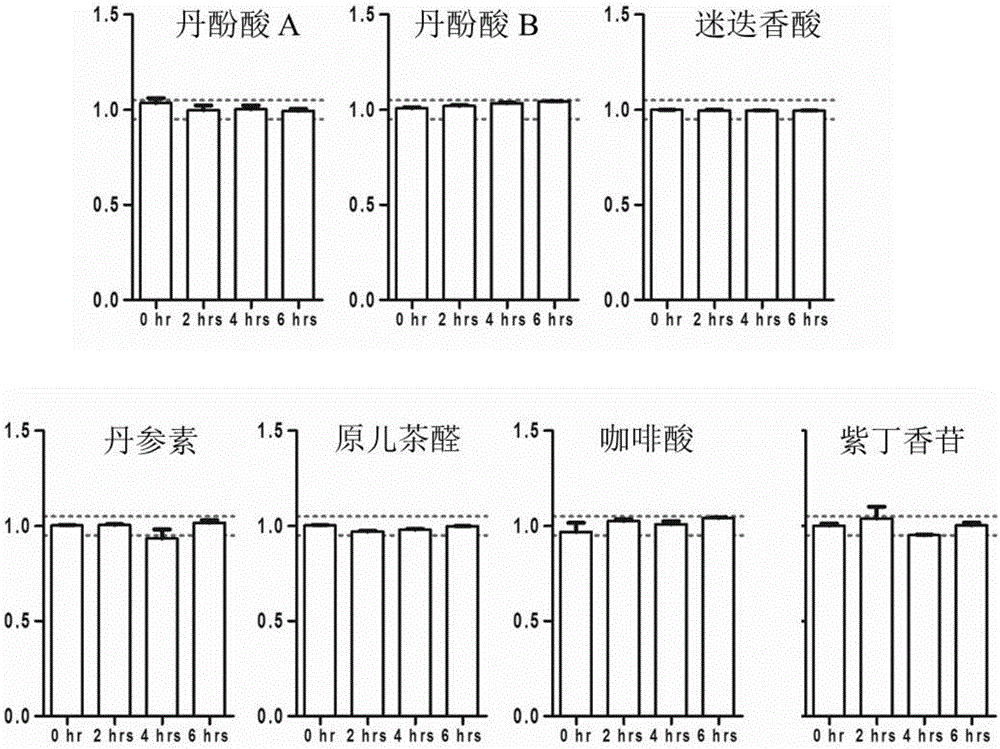
图2为丹红注射液开瓶后室温(25℃)下暴露不同时间(2,4,6小时),采用LC-TQ-MS方法分析7种成分丹酚酸A、丹酚酸B、迷迭香酸、丹参素、原儿茶醛、咖啡酸和紫丁香苷的含量变化图。成分变化在虚线之间的认为稳定。
图3为丹红注射液开瓶后室温(25℃)下暴露不同时间(2,4,6小时),对HUVEC细胞氧化性损伤的保护作用示意图。
图4为丹红注射液与不同注射用溶媒混合后室温(25℃)下放置不同时间(2,4,6小时),采用LC-TQ-MS分析7种成分丹酚酸A、丹酚酸B、迷迭香酸、丹参素、原儿茶醛、咖啡酸和紫丁香苷的含量变化图。三角形及圆形标注表示成分发生显著性改变。
图5丹红注射液与不同注射用溶媒混合后室温(25℃)下放置不同时间(2,4,6小时),对H2O2诱导的HUVEC氧化性损伤的保护能力图。
图6一种用于中药注射剂与溶媒配伍稳定性研究流程示意图。不同评价方法发现注射剂与不同溶媒配伍具有不同的稳定性。
具体实施方式
下面结合具体实施例,进一步阐明本发明,应理解这些实施例仅用于说明本发明而不用于限制本发明的范围,在阅读了本发明之后,本领域技术人员对本发明的各种等价形式的修改均落于本申请所附权利要求所限定的范围。
实施例1丹红注射液和质量浓度0.9%氯化钠注射液、5%葡萄糖0.9%氯化钠注射液、10%果糖注射液、5%木糖醇注射液、6%右旋糖苷40注射液和5%葡萄糖注射液的配伍稳定性研究。
1.实验方法
1.1色谱分析方法
色谱条件:Acquity UPLC BEH C18色谱柱(2.1mm i.d.×100mm,1.7μm;Waters),柱温和自动进样器温度分别为30℃和10℃,进样量为1μl。以流动相A(0.1%甲酸水)和B(乙腈)进行梯度洗脱:0-1.0min,3-3%B;1.0-6.0min,3-40%B;6.0-8.0min,40-95%B;8.0-9.0min,95-95%B;9.0-9.2min,95-3%B。流速为0.4ml/min。
质谱条件:Xevo Triple Quadrupole Mass Spectrometer(TQ/MS)(Waters Corp.,Milford,MA,USA),Waters SynaptTMQTOF/MS,离子源为电喷雾离子化(ESI源);扫描方式为多反应监测(MRM);毛细管电压3.0kV;离子源温度150℃;脱溶剂气温度550℃;干燥气流量1000l/h;锥孔气流量50l/h;碰撞气流量0.15ml/min。
1.2细胞培养方法
将96孔板中的HUVEC置于37℃,5%CO2的细胞培养箱中进行培养。培养基为添加10%FBS(v/v),1%P/S(v/v),1%ECGS(v/v)and 0.01%heparin(w/v)的F-12K混合培养基。
1.3丹红注射液与不同溶媒配伍的化学稳定性评价
取丹红注射液分别与0.9%氯化钠注射液,5%葡萄糖0.9%氯化钠注射液,10%果糖注射液,5%木糖醇注射液,6%右旋糖苷40注射液和5%葡萄糖注射液,按照1:7.25比例配伍后,室温条件下(25℃)放置0,2,4,6小时后进行LC-TQ-MS和LC-TOF-MS分析。分别评价7种代表性成分(结构式如图1)及全成分的变化,反映丹红注射液与不同溶媒配伍不同时间的化学稳定性。
1.4丹红注射液与不同溶媒配伍的生物活性稳定性评价
丹红注射液分别与0.9%氯化钠注射液,5%葡萄糖0.9%氯化钠注射液,10%果糖注射液,5%木糖醇注射液,6%右旋糖苷40注射液,5%葡萄糖注射液,按照1:7.25比例配伍后,25℃室温条件下(25℃)放置0,2,4,6小时后与HUVEC共培养1小时(10倍稀释),然后加入3mM H2O2培养1小时。维生素C作为阳性对照。采用MTT法测定570nm处的吸光度评价细胞活力。
1.5统计学处理
实验数据以平均值±S.D表示。组间差异采用Student T检验。显著性差异设定为P<0.05。
2.实验结果
2.1丹红注射液开瓶后室温下不同时间自身稳定性
如图2和图3所示,丹红注射液开瓶后室温下放置2,4,6小时,7种标志性成分丹酚酸A、丹酚酸B、迷迭香酸、丹参素、原儿茶醛、咖啡酸和紫丁香苷,整体成分以及抗氧化活性均无显著性变化,表明丹红注射液开瓶后自身化学及生物活性稳定性良好。这也进一步提示,如果丹红注射液与溶媒配伍后发生化学或者生物活性改变,那么稳定性的变化则来自丹红注射液与溶媒的配伍。
2.2丹红注射液与不同溶媒配伍后7种代表性成分的化学稳定性
如图4所示,丹红注射液与5%葡萄糖注射液配伍最为稳定,特征性成分含量无明显变化;且与0.9%氯化钠注射液配伍稳定;但与木糖醇注射液和右旋糖酐葡萄糖注射液配伍极不稳定,特征性成分含量均显著下降,且与木糖醇注射液配伍后最大降幅可达27%。
2.3丹红注射液与溶媒配伍后注射液整体成分化学稳定性
当丹红注射液与不同溶媒配伍后,与负离子模式相比,正离子模式下各样品的偏移距离较小,提示具有正离子模式响应的整体成分呈现出更好的稳定性。根据丹红注射液整体成分的分析结果,丹红注射液与0.9%氯化钠注射液配伍稳定性最好,在配伍后6h内整体成分未发生显著变化,其次是5%葡萄糖注射液配伍较为稳定。在所有溶媒中,丹红注射液与木糖醇注射液和右旋糖酐葡萄糖注射液的配伍稳定性最差,配伍4h后具有负离子响应的整体成分就发生显著性变化。
2.4丹红注射液与溶媒配伍后注射液生物活性稳定性
丹红注射液与不同溶媒配伍后,随配伍时间的增加,抗氧化活性不断降低(图5)。但是丹红注射液与不同溶媒配伍对抗氧化活性的影响程度不同。丹红注射液与5%葡萄糖溶液配伍6h,虽然抗氧化活性不断降低,但整体的抗氧化能力仍明显优于与其它溶媒配伍。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理和构思的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!