Glypican‑1蛋白在胰腺癌诊断中的应用、阳性外泌体浓度的检测方法及其用途与流程
本发明属于生物医学技术领域,具体涉及一种glypican-1蛋白在胰腺癌诊断中的应用、glypican-1阳性外泌体浓度的检测方法及其用途。
背景技术:
胰腺癌是一种恶性程度很高,诊断和治疗都很困难的消化道恶性肿瘤,其发病率和死亡率近年来明显上升。据美国临床肿瘤协会统计,全球男性胰腺癌患者病死率居恶性肿瘤的第8位,女性患者居第9位,胰腺癌患者5年生存率始终低于5%。更糟糕的是,胰腺癌早期并没有明显的征兆,病程短且发展快。80%的胰腺癌患者确诊后生存时间不超过1年。
目前,ca19-9水平是唯一一个临床接受的胰腺癌标志物,但其用途有限,因为它被认可仅用于监测胰腺癌进展或对治疗的反应,但不用于胰腺癌诊断或分期。另外,血清ca19-9水平可以区分健康人群和胰腺癌患者,但某些胰腺良性疾病亦可导致ca19-9的升高,这样,就大大降低了该指标对于诊断胰腺癌的敏感性与特异性。
现今,外泌体作为可诊断疾病的生物标志物越发受到关注。肿瘤来源的外泌体上含有的某些特异的蛋白质,对于肿瘤的诊断有着特殊的意义。然而现在大多数测定外泌体的方法都需要先对血液中外泌体进行提取后再检测,所需样品量大,并且耗时,低通量,价格昂贵,不足以应用于临床。纳米等离子体增强散射(npes)测定法能直接从微量血浆中量化肿瘤衍生的外泌体,而无需经过提取、鉴定等繁杂过程。并且通过识别某些特异性抗原,使得外泌体诊断肿瘤之路简便许多。
目前,国际上还没有关于npes测定外泌体含量的报道,也没有glypican-1蛋白对于胰腺癌诊断的价值评估,因此,纳米等离子体增强散射法检测glypican-1阳性外泌体浓度的提出和glypican-1蛋白的发现,填补了这方面的缺陷。
技术实现要素:
本发明要解决的技术问题是提供一种glypican-1蛋白在胰腺癌诊断中的应用、glypican-1阳性外泌体浓度的检测方法及其用途,采用的纳米等离子体增强散射(npes)测定法是一种灵敏、特异又简便的血浆中胰腺癌相关外泌体的量化方法,结合胰腺癌来源外泌体上特异的蛋白—glypican-1,可用于胰腺癌的诊断和分期。
为解决上述技术问题,本发明的实施例提供一种glypican-1蛋白的用途,用于制备诊断胰腺癌的产品。
其中,所述产品为芯片、检测试剂或检测试剂盒。
进一步,所述芯片包括蛋白芯片,所述检测试剂盒包括蛋白免疫检测试剂盒。
本发明实施例还提供一种glypican-1阳性外泌体浓度的检测方法,为纳米等离子体增强散射方法。
其中,所述纳米等离子体增强散射方法所用检测试剂包括以下组成:
(ⅰ)氨基功能化的玻璃载片(nh2玻璃)、甲醇、氮气(n2)流、50孔聚二甲基硅氧烷膜(pdms);
(ⅱ)磷酸盐缓冲洗涤液(pbs),ph值为7.4,其成分为:140mmnacl,2.7mmkcl,10mmna2hpo4,1.8mmkh2po4;
(ⅲ)封闭液为含5%牛血清蛋白(bsa)的pbs,ph值为7.4,其成分为:pbs,5%bsa;
(ⅳ)羧基功能化的金纳米颗粒(gnp):50nm金纳米球(辐射绿光)、25×60nm金纳米棒(辐射红光),当两者结合则信号加强并辐射黄光;
(ⅴ)mes溶液,ph值为4.7,其成分为:2-(n-吗啉代)乙磺酸,用纯水配制;
(ⅵ)浓度为5mm的edc/pbs溶液、edc/nhs溶液,edc系羟基胶乳微球偶联抗体,成分为1-乙基-3-(3二甲基氨基丙基)碳二亚胺盐酸盐,浓度为2mg/ml;nhs,全称n-羟基琥珀酰亚胺,浓度为1mg/ml;
(ⅶ)偶联缓冲液;
(ⅷ)抗体溶液(抗体上携带羧基):抗-cd63、抗-cd9、抗glypican-1;浓度为0.5mg/ml;
(ⅸ)标准品:已知质量的标准glypican-1+exo样品溶解于无exosome的血浆中,浓度为1μg/ml,并稀释至所需浓度(30000,15000,7500,3750,1870,938,469和234pg/所需);
(ⅹ)淬灭缓冲液:浓度为2mm的硫酸水溶液。
所述纳米等离子体增强散射方法的步骤为:在nh2功能化的玻片上,覆盖50孔聚二甲基硅氧烷膜,形成感应芯片,在感应芯片上用外泌体特异抗体-抗cd63覆盖,封闭后加入待测样品孵育,洗板,再加偶联了抗cd9抗体的金纳米棒和偶联了抗glypican-1抗体的金纳米球,孵育,洗板后在暗场显微镜下获得图像;通过计算机软件分析整个图像,以给出指示glypican-1阳性外泌体浓度的npes信号的面积比,通过标准品的浓度和相应的npes信号绘制标准曲线,待检样品中的glypican-1阳性外泌体的水平通过它的信号值并对应标准曲线得到。
进一步,所述纳米等离子体增强散射方法包括以下具体步骤:
(1)纳米金偶联抗体的制备:
a、用40μl羧基功能化金纳米球与20μlmes缓冲液(ph4.7)混合,然后加入20μledc/nhs溶液,室温孵育10min;
b、加入80μl偶联缓冲液、20μl抗-glypican-1溶液,然后在室温下振荡2小时以完成偶联过程;
c、然后用2μl淬灭缓冲液停止反应,并以6000rpm离心10分钟;
d、沉淀的gnp抗体用400μl磷酸盐缓冲洗涤液洗涤三次,然后重悬于40μl磷酸盐缓冲洗涤液中并在4℃下储存,完成羧基功能化金纳米球与抗-glypican-1的偶联;
e、利用步骤a-d的方法完成金纳米棒与抗-cd9的偶联;
(2)感应芯片的制备:将载玻片在甲醇中超声清洗5分钟,用去离子水彻底冲洗,在氮气(n2)流下干燥,完成玻片上氨基的功能化,再用50孔聚二甲基硅氧烷膜(pdms)覆盖玻璃;
(3)加入浓度为5mm的edc/pbs溶液,然后在玻片上每孔都填充10μl抗人cd63抗体进行包被,并在潮湿室中室温孵育2小时;
(4)弃去包被抗体,磷酸盐缓冲洗涤液300μl/孔,洗涤3次,加入封闭液10μl/孔,并在室温下孵育4小时;
(5)弃去封闭液,磷酸盐缓冲洗涤液300μl/孔,洗涤3次,加入标准品和待测血样5μl/孔,在潮湿室中室温孵育4小时;
(6)弃去标准品和血样,用磷酸盐缓冲洗涤液(pbs)洗涤3次,两种步骤(1)中偶联后的金纳米颗粒探针溶液各加入7μl,并在室温下孵育1小时,除去pdms膜,将载玻片用磷酸盐缓冲洗涤液(pbs)洗涤3次;
(7)装上盖玻片,用暗视野显微镜(dfm)成像,测量辐射光谱;
(8)通过计算机软件分析整个图像,以给出指示glypican-1阳性外泌体浓度的npes信号的面积比,通过标准品的浓度和相应的npes信号绘制标准曲线,待检样品中的glypican-1蛋白阳性的外泌体浓度通过它的信号值并对应标准曲线得到。
本发明实施例还提供一种上述的glypican-1阳性外泌体浓度的检测方法的用途,所述纳米等离子体增强散射方法用于检测胰腺癌血清中glypican-1蛋白阳性外泌体的含量。
本发明的上述技术方案的有益效果如下:本发明应用npes方法检测样品中的glypican-1蛋白阳性的外泌体的浓度,结果发现人血浆中含glypican-1蛋白的外泌体水平的升高与胰腺癌的发生发展存在密切联系,运用npes测定法能够对胰腺癌起到诊断及分期判断等作用。
附图说明
图1为westernblot检测胰腺癌来源的外泌体上特异的蛋白;
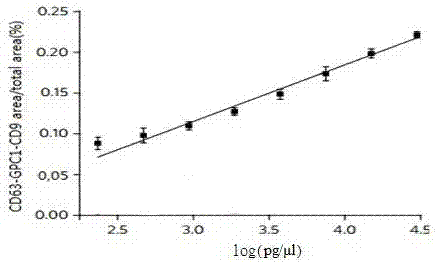
图2为npes法检测已知glypican-1+exo浓度的标准曲线;
图3为npes法测定三组人群血浆glypican-1阳性外泌体比较。
具体实施方式
为使本发明要解决的技术问题、技术方案和优点更加清楚,下面将结合附图及具体实施例进行详细描述。
实施例1
glypican-1蛋白用于制备诊断胰腺癌的产品。其中,所述产品为芯片、检测试剂或检测试剂盒。
优选的,所述芯片包括蛋白芯片,所述检测试剂盒包括蛋白免疫检测试剂盒。
实施例2
一种glypican-1阳性外泌体浓度的检测方法,为纳米等离子体增强散射方法。
所述纳米等离子体增强散射方法所用检测试剂包括以下组成:
(ⅰ)氨基功能化的玻璃载片(nh2玻璃)、甲醇、氮气(n2)流、50孔聚二甲基硅氧烷膜(pdms);
(ⅱ)磷酸盐缓冲洗涤液(pbs),ph值为7.4,其成分为:140mmnacl,2.7mmkcl,10mmna2hpo4,1.8mmkh2po4;
(ⅲ)封闭液为含5%牛血清蛋白(bsa)的pbs,ph值为7.4,其成分为:pbs,5%bsa;
(ⅳ)羧基功能化的金纳米颗粒(gnp):50nm金纳米球(辐射绿光)、25×60nm金纳米棒(辐射红光),当两者结合则信号加强并辐射黄光;
(ⅴ)mes溶液,ph值为4.7,其成分为:2-(n-吗啉代)乙磺酸,用纯水配制;
(ⅵ)浓度为5mm的edc/pbs溶液、edc/nhs溶液,用于活化抗体上的羟基。edc系羟基胶乳微球偶联抗体,主要用作交联剂,成分为1-乙基-3-(3二甲基氨基丙基)碳二亚胺盐酸盐,浓度为2mg/ml;nhs全称n-羟基琥珀酰亚胺,浓度为1mg/ml;
(ⅶ)偶联缓冲液;
(ⅷ)抗体溶液(抗体上携带羧基):抗-cd63、抗-cd9、抗glypican-1;浓度为0.5mg/ml;
(ⅸ)标准品:已知质量的标准glypican-1+exo样品溶解于无exosome的血浆中,浓度为1μg/ml;进一步稀释至所需浓度(30000,15000,7500,3750,1870,938,469和234pg/所需);
(ⅹ)淬灭缓冲液:浓度为2mm的硫酸水溶液。
所述纳米等离子体增强散射方法的步骤为:在nh2功能化的玻片上,覆盖50孔聚二甲基硅氧烷膜,形成感应芯片,在感应芯片上用外泌体特异抗体-抗cd63(见图1)覆盖,封闭后加入待测样品孵育,洗板,再加偶联了抗cd9抗体的金纳米棒和偶联了抗glypican-1抗体的金纳米球,孵育,洗板后在暗场显微镜下获得图像;通过计算机软件分析整个图像,以给出指示glypican-1阳性外泌体浓度的npes信号的面积比,通过标准品的浓度和相应的npes信号绘制标准曲线,待检样品中的glypican-1阳性外泌体的水平通过它的信号值并对应标准曲线得到。
具体步骤如下:
(1)纳米金偶联抗体的制备:
a、用40μl羧基功能化金纳米球与20μlmes缓冲液(ph4.7)混合,然后加入20μledc/nhs溶液,室温孵育10min;
b、加入80μl偶联缓冲液、20μl抗-glypican-1溶液,然后在室温下振荡2小时以完成偶联过程;
c、然后用2μl淬灭缓冲液停止反应,并以6000rpm离心10分钟;
d、沉淀的gnp抗体用400μl磷酸盐缓冲洗涤液洗涤三次,然后重悬于40μl磷酸盐缓冲洗涤液中并在4℃下储存,完成羧基功能化金纳米球与抗-glypican-1的偶联;
e、利用步骤a-d的方法完成金纳米棒与抗-cd9的偶联;
(2)感应芯片的制备:将载玻片在甲醇中超声清洗5分钟,用去离子水彻底冲洗,在氮气(n2)流下干燥,完成玻片上氨基的功能化,再用50孔聚二甲基硅氧烷膜(pdms)覆盖玻璃;
(3)加入浓度为5mm的edc/pbs溶液,然后在玻片上每孔都填充10μl抗人cd63抗体进行包被,并在潮湿室中室温孵育2小时;
(4)弃去包被抗体,磷酸盐缓冲洗涤液300μl/孔,洗涤3次,加入封闭液10μl/孔,并在室温下孵育4小时;
(5)弃去封闭液,磷酸盐缓冲洗涤液300μl/孔,洗涤3次,加入标准品和待测血样5μl/孔,在潮湿室中室温孵育4小时;
(6)弃去标准品和血样,用磷酸盐缓冲洗涤液(pbs)洗涤3次,两种步骤(1)中偶联后的金纳米颗粒探针溶液各加入7μl,并在室温下孵育1小时,除去pdms膜,将载玻片用磷酸盐缓冲洗涤液(pbs)洗涤3次;
(7)装上盖玻片,用暗视野显微镜(dfm)成像,测量辐射光谱;
(8)通过计算机软件分析整个图像,以给出指示glypican-1阳性外泌体浓度的npes信号的面积比,通过标准品的浓度和相应的npes信号绘制标准曲线(如图2),待检样品中的glypican-1蛋白阳性的外泌体浓度通过它的信号值并对应标准曲线得到,从而完成对胰腺癌患者的诊断及进一步临床应用。
本实施例的纳米等离子体增强散射方法检测胰腺癌血清中glypican-1蛋白阳性外泌体含量的原理是:感应芯片表面覆盖有可与外泌体表面特异蛋白(cd63)结合的抗体,将血样稀释并加至传感器芯片后,cd63抗体可捕获血液中外泌体,再加入抗glypican-1及抗cd9偶联的金纳米颗粒探针可与外泌体相应膜蛋白进一步结合,glypican-1是胰腺癌特有的蛋白,cd9是外泌体特有的cd9蛋白,只有胰腺癌细胞来源的外泌体会同时与两种纳米探针结合。最后,当两种探针在外泌体表面亲密接触后,会引发一种耦合效应,从而发射出黄色的光信号。
实施例3
上述的检测glypican-1阳性外泌体浓度的纳米等离子体增强散射方法用于检测胰腺癌血清中glypican-1蛋白阳性外泌体的含量,以用于胰腺癌的诊断和分期。
实验:用npes测定方法对48例正常人、48例胰腺炎和49例不同分期(8例一期,29例二期,12例三期)的胰腺癌患者的血浆进行检测,结果如图3所示,发现在胰腺癌患者的血浆中,代表glypican-1阳性的外泌体水平的纳米金辐射面积明显高于前两者,且随着肿瘤的演进,该指标也呈逐渐上升趋势。故npes测定glypican-1阳性的外泌体的方法可用于胰腺癌的诊断及分期判断等应用。
本发明的发明人之前运用蛋白印迹分析方法发现glypican-1蛋白在胰腺癌血清来源的外泌体上高表达,并且它的表达水平与胰腺癌的分期、预后相关。本发明运用自建的npes测定法检测发现,正常人、胰腺良性疾病患者外周血清的外泌体上均未检测出glypican-1蛋白,而胰腺癌患者外周血清来源的外泌体上的glypican-1蛋白水平明显升高,其差异有统计学意义。因此,血清外泌体上glypican-1蛋白对胰腺癌具有明确的诊断价值。
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明所述原理的前提下,还可以作出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!