血液检测方法与流程
本发明涉及一种生物样品检测方法,尤其涉及一种血液检测方法。
背景技术:
血液检验是健康检查中重要的检测项目之一。在临床血液检测上,主要处理过程分成三大步骤,分别是血液样本抽取、血液样本前处理以及进行检测。为了降低血球所造成的干扰,通常先将血液样本作前处理使血球和血浆分离后,再检测血浆中的标的物质,以得到精准的检测数值。
目前已知的血球和血浆分离方法是以离心、过滤、流体力学等方法来进行处理。然而,离心的方法有体型大、不易微小化、花费时间长、价格贵等缺点。过滤的方法具有花费时间长的问题。而流体力学的方法则会造成不易微小化及增加制作的难度。
因此,如何开发一种无需前处理的全血检测方法,实为目前本领域技术人员积极研究的课题之一。
技术实现要素:
本发明提供一种血液检测方法,其具有低检测极限及高灵敏度的特性,并且可使用人体全血进行检测以及减少血球的干扰。
本发明的一种血液检测方法,包括以下步骤。提供感测装置,其中感测装置包括基体以及至少一反应电极,反应电极相对于基体的栅极端而与基体彼此间隔设置。将血液放置于反应电极上,其中血液包括多个血球以及多个标的物质。将血液分离为第一部分以及第二部分,其中第一部分与反应电极接触,且第一部分所含的血球数低于以及所述第二部分所含的血球数。施加具有可调变脉波宽度与高度的脉波电压于反应电极,以使反应电极与基体的栅极端之间产生电场,并于脉波宽度内量测运算自基体产生的检测电流,以量测标的物质的性质。
在本发明的一实施例中,上述的电场为f,且0.1伏/厘米≤f≤10伏/厘米。
在本发明的一实施例中,上述的将血液分离为第一部分以及第二部分的方法可包括将放置有血液的感测装置倒置,以通过重力将血液分离为第一部分以及第二部分。
在本发明的一实施例中,上述的标的物质例如是心血管疾病生物标记。
在本发明的一实施例中,上述的心血管疾病生物标记例如是c反应蛋白(c-reactiveprotein,crp)、脑排钠利尿胜肽(brainnatriureticpeptide,bnp)、n端脑排钠利尿胜肽前体(n-terminalprobrainnatriureticpeptide,nt-probnp)或肌钙蛋白(troponini)。
在本发明的一实施例中,上述的感测装置可还包括受体,配置于反应电极的表面上,其中受体可与标的物质专一性地结合。
在本发明的一实施例中,上述的受体例如是抗体或适体。
在本发明的一实施例中,上述的脉波宽度不大于10-3秒
在本发明的一实施例中,上述的反应电极与基体的栅极端位于同一平面。
在本发明的一实施例中,上述的感测装置例如是高速电子迁移率场效晶体管、硅基场效晶体管、纳米线场效晶体管、纳米碳管场效晶体管、石墨烯场效晶体管或二硫化钼场效晶体管。
在本发明的一实施例中,上述的感测装置可包括多个反应电极,且多个反应电极彼此间隔设置。
在本发明的一实施例中,上述的感测装置还包括多个开关电路,每一反应电极连接至对应的开关电路。
基于上述,本发明的血液检测方法可直接使用全血进行检测,且可减少检测期间血球的干扰。此外,本发明的血液检测方法通过施加可调变脉波宽度与高度的脉波电压于反应电极,令反应电极与间隔设置的栅极端产生压差并具有电容效应,以克服屏蔽效应,而能直接于高盐浓度下检测血液中的标的物质。此外,本发明的检测法方具有增益效果,因此可检测出细微的电信号。
为让本发明的上述特征和优点能更明显易懂,下文特举实施例,并配合附图作详细说明如下。
附图说明
图1为依照本发明一实施例的感测装置的俯视示意图;
图2为依照本发明又一实施例的感测装置的俯视示意图;
图3为实验例1、比较例1与比较例2的电流变化对时间的关系图;
图4为实验例2~实验例6的δ增益值对浓度的关系图;
图5为实验例7~实验例10的δ增益值对浓度的关系图;
图6为实验例11~实验例15的δ增益值对浓度的关系图;
图7为实验例16~实验例19的增益值对浓度的关系图;
图8为实验例20~实验例22的增益值对浓度的关系图;
图9为实验例23~实验例26的δ增益值对浓度的关系图;
图10为实验例27~实验例30的δ增益值对浓度的关系图;
图11为实验例31~实验例34的δ增益值对浓度的关系图。
具体实施方式
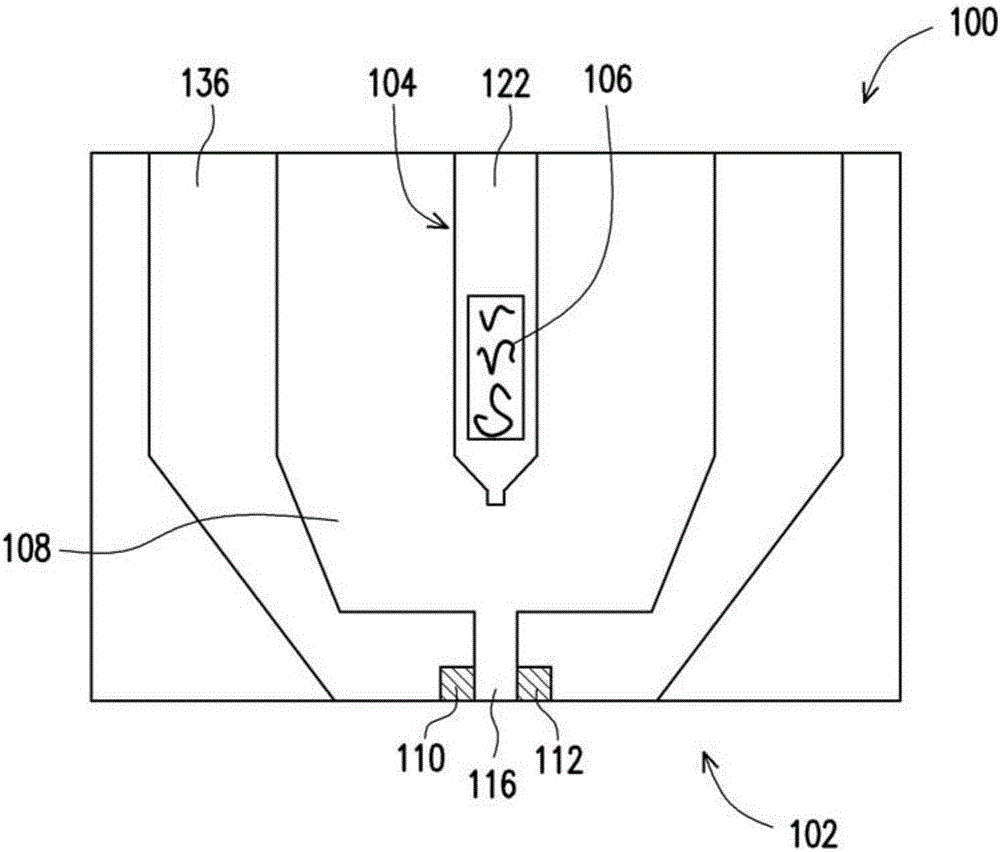
图1为依照本发明一实施例的感测装置的俯视示意图。
请参照图1,感测装置100包括基体102以及反应电极104,其中反应电极104与基体102彼此间隔设置。感测装置100例如是高速电子迁移率场效晶体管(highelectronmobilitytransistor,hemt)、硅基场效晶体管、纳米线场效晶体管、纳米碳管场效晶体管、石墨烯场效晶体管或二硫化钼场效晶体管,但本发明不限于此。在本实施例中,感测装置100为类似于高速电子迁移率场效晶体管的晶体管。
基体102包括基板108、源极端110、漏极端112以及设置于源极端110与漏极端112之间的栅极端116。在本实施例中,形成基底102的方法例如是在基板108上依序形成氮化镓(gan)层以及氮化铝镓(algan)层(未示出),并通过曝光显影制程于基板108上形成源极端110、漏极端112及栅极端116。
基板108的材料例如是硅或蓝宝石(sapphire)。氮化镓层以及氮化铝铟层(未示出)之间的低维异质结构界面可使得基体102具有卓越的载子传输特性。在本实施例中,形成于氮化镓层上的层的材料为氮化铝铟,但本发明不限于此。在另一实施例中,形成于氮化镓层上的层的材料可为具有压电性质的其他材料,如氮化铝镓。源极端110与漏极端112的材料可包括一种或一种以上的导电材料。导电材料例如是金属材料、金属化合物或其组合。源极端110与漏极端112分别通过线路136连接之外部电子元件(未示出)。
请再参照图1,反应电极104设置于基体102上。反应电极104包括位于基体102的顶面上的电极本体122,且电极本体122是由金属材料所构成。反应电极104可与栅极端116位于同一平面并间隔相对设置。更详细而言,电极本体122可与基体102的栅极端116位于同一平面并间隔相对设置,且电极本体122与基体102无电性连接。具体来说,电极本体122与栅极端116无电性连接。要说明的是,电极本体122的表面的材料是选自可与后续所选用的受体键结的材料。在本实施例中,电极本体122的表面的材料例如是金。
图2为依照本发明又一实施例的感测装置的俯视示意图。图2所示的感测装置200相似于图1所示的感测装置100,其不同之处在于感测装置200具有多个反应电极204,且多个反应电极204彼此间隔设置于基板208上,其他相同或相似的构件已于上述进行详尽的描述,于此不再重复赘述。
请参照图2,感测装置200包括多个反应电极204,且多个反应电极204对应至同一个基体202。如此一来,感测装置200可同时对同种或是不同种的分析物进行多次检测,不仅可提升检测结果的信赖度,也可降低检测所需的时间。除此之外,由于多个反应电极204共用同一个基体202,并且仅需更换使用后的反应电极204即可进行下一次检测,使得检测所需的费用能够降低。
在一实施例中,感测装置200还包括多个开关电路232,每一反应电极204与相对应的开关电路232连接,如此可选择性地控制所欲使用的反应电极204,使得感测装置200适合应用于各种量测方法,例如在不同时间下对同样的分析物进行检测,以观察其浓度与时间的变化量。在一些实施例中,开关电路232位于反应电极204的相对两侧。位于反应电极204一侧的开关电路232连接至栅极电压vg;而位于反应电极204另一侧的开关电路232连接至栅极端216。此外,在进行量测时,基体202的源极端210接地,并对漏极端212施加漏极电压vd。
本发明也提出一种使用如上述的感测装置所进行的血液检测方法。接下来,将以图1所示的感测装置100来说明本发明的血液检测方法。
首先,提供感测装置100,其中感测装置100包括基体102以及至少一反应电极104,反应电极104相对于基体102的栅极端116而与基体102彼此间隔设置。在本实施例中,可将受体106键结在电极本体122的表面上,其中受体106可与后续所欲检测的标的物质专一性地结合。受体106例如是抗体或适体(aptamer)。
接着,将血液放置于反应电极104上,其中血液包括多个血球以及多个标的物质。在本实施例中,血液为未经前处理的血液(即全血)。在本实施例中,标的物质例如是心血管疾病生物标记。心血管疾病生物标记例如是c反应蛋白(c-reactiveprotein,crp)、脑排钠利尿胜肽(brainnatriureticpeptide,bnp)、n端脑排钠利尿胜肽前体(n-terminalprobrainnatriureticpeptide,nt-probnp)或心肌钙蛋白l(cardiactroponinl,ctnl)。在本实施例中,上述的心血管疾病生物标记可与各自对应的受体专一性地结合。
然后,将血液分离为第一部分以及第二部分,其中第一部分与反应电极104接触,且第一部分所含的血球数低于以及第二部分所含的血球数。在本实施例中,将血液分离为第一部分以及第二部分的方法例如是将放置有血液的感测装置100倒置,以通过重力将血液分离为第一部分以及第二部分。具体来说,在倒置感测装置100的过程中,重力会使血液中的血球远离电极本体122的表面。也就是说,血液中的血球与血浆可因重力而分离。在一实施例中,血液的第一部分即为血浆部分,而第二部分即为血球部分,而反应电极104仅与含有少量血球的血浆部分直接接触。在本实施例中,是通过倒置感测装置100的方式而利用重力使血液中的血球远离反应电极104的表面,但本发明不限于此,也可以使用其他方式将血液中的血球远离反应电极104的表面。此外,在反应电极104与第一部分接触的过程中,第一部分(血浆部分)中的标的物质与键结在电极本体122的表面上的受体106进行专一性的结合。
在本实施例中,由于反应电极104仅与血浆部分直接接触,因此在对标的物质的检测的过程中可避免血球部分的干扰,进而得到更为精准的检测结果。
之后,施加脉波电压v于反应电极104,以使反应电极104与基体102的栅极端116之间产生电场f,并量测运算自基体102产生的检测电流i,以量测标的物质的性质(例如浓度)。具体来说,先给予基体102一固定电压后,再对反应电极104施加脉波电压v,从而使反应电极104与栅极端116之间产生压差。因此,当标的物质与对应的受体专一性键结时,通过施加脉波电压v产生的压差而能使反应电极104与栅极端116之间具有一电容效应,进而得到由电容效应所贡献的电流值。在一实施例中,电场f介于0.1伏/厘米至10伏/厘米之间(0.1伏/厘米≤f≤10伏/厘米)。在另一实施例中,电场f介于0.5伏/厘米至10伏/厘米之间(0.5伏/厘米≤f≤10伏/厘米)。在又一实施例中,电场f介于0.5伏/厘米至1.0伏/厘米之间(0.1伏/厘米≤f≤1.0伏/厘米)。所施加的电场f在上述范围内,可具有低检测极限及高灵敏度。
值得一提的是,利用此电容效应进行检测时,能量测受体与标的物质在反应未达平衡状态前的动态信息。也就是说,通过量测反应未达平衡状态前的动态信息,而能克服现有因为须在平衡状态时量测,人类血液因高盐浓度于平衡时产生的屏蔽效应,也毋须将人类血液进行繁复的稀释步骤。
在本实施例中,脉波电压的脉波宽度与高度的大小可依据使用者所欲分析的检测时间及检测所需的电压大小进行调整。在一实施例中,脉波宽度是选用小于受体与心血管疾病生物标记在反应未达平衡的时间,脉波宽度不大于10-3秒,但本发明不限于此。在一实际例中,脉波高度例如是0.5v,但本发明不限于此。
在一实施例中,所施加的电压可为单一脉波(漏极电压=2v;栅极电压=0.5v;栅极脉波宽度=0.5μs)或是双相脉波(漏极电压=2v;栅极电压=0.5v;栅极循环脉波宽度=1ms)。在一实施例中,可连续性地施加脉波电压。
在本实施例中,可选择性地对所量测运算自晶体管产生的检测电流进行转换,例如将检测电流相对脉波宽度进行积分转换,此时即为对电流与时间进行积分,而可得知特定时间于基体102的源极端110所累积的总电荷量。
在本实施例中,是先将血液分离为血清部分以及血球部分后再施加电压进行检测,但本发明不限于此。在另一实施例中,是在施加电压的过程中将血液分离为血清部分以及血球部分。在本实施例中,由于反应电极仅与含有少量血浆部分直接接触,因此在对标的物质的检测的过程中已排除了血球部分的干扰,因此可得到更为精准的检测结果。此外,由于本实施例不需对全血先进行前处理而可直接进行全血检测,因此也可降低全血检测的成本与时间。
以下,通过实验例来详细说明本发明所提出的血液检测方法及其特性,然而,下述实验例并非用以限制本发明。此外,此外,下述实验例中所述的增益值(gain)表示平衡电流值与初始电流值(即背景电流)之间的差值(即平衡电流值-初始电流值=增益值)。初始电流值可表示对反应电极施加初始电压所获得的电流值。在本实施例中,初始电压可小于栅极电压,但本发明不以此为限。平衡电流值可表示对反应电极施加一定时间的栅极电压vg后所得到的电流值。
实验例1
在实验例1中,使用图1所示的感测装置100来进行检测。将人体全血滴加至感测装置的反应电极后,将感测装置倒置并检测不同时间的电流变化。
比较例1
使用与实验例1大致上相同的方式进行测试,其差异仅在将人体全血滴加至感测装置的反应电极后直接检测不同时间的电流值而不将感测装置倒置。
比较例2
使用与实验例1大致上相同的方式进行测试,其差异仅在使用含有4%牛血清蛋白(bovineserumalbumin,bsa)的磷酸盐缓冲溶液(phosphatebuffersaline,pbs)来代替人体全血。要说明的是,由于血清蛋白是血液中最大量的蛋白质,因此含有牛血清蛋白的磷酸盐缓冲溶液可模拟人体血清。
图3为实验例1、比较例1与比较例2的电流变化对时间的关系图。
由图3可以看出,实验例1在检测期间,电信号不会随时间增加而改变。反观比较例1,在经过4分钟后,电信号明显下降。由上述的结果可知,由于实验例1在检测期间将感测装置倒置,重力有助于将血液中的血球与血浆分离,因此可减少血球所造成的干扰问题。而在比较例1中,重力会导致血球沉淀,一旦大量的血球靠近反应电极表面时,则会干扰到电信号。
为了可清楚说明本发明的血液检测方法,以下以33个实验例进行说明。
要说明的是,为了确保受体确实键结于反应电极的电极本体上,因此,在进行量测之前,会先进行如下量测,以确认受体确实键结于反应电极的电极本体的表面上。
首先,取磷酸盐缓冲溶液(或人体全血)滴至反应电极与基体上,且使缓冲溶液覆盖且连结反应电极的电极本体与基体的栅极端,并施加脉波宽度与高度分别为50μs及0.5v的脉波电压于该反应电极上,量测基体的源极端而得到一由磷酸盐缓冲溶液(或人体全血)所贡献的电流值。接着,移除磷酸盐缓冲溶液(或人体全血),再将受体(抗体或适体)滴至反应电极的电极本体上,使受体与反应电极的电极本体反应键结,随后再于反应电极与基体之间滴上磷酸盐缓冲溶液(或人体全血),并以上述相同条件的脉波电压量测基体的而源极端而得到由受体所贡献的电流值。当受体所贡献的电流值与磷酸盐缓冲溶液(或人体全血)所贡献的电流值不同时,即可判定受体确实键结于该反应电极的电极本体的表面上。
实验例2
在实验例2中,使用图2所示的感测装置200来进行检测,其中在感测装置的反应电极上已键结有c反应蛋白的专一性适体。
以磷酸盐缓冲溶液(phosphatebuffersaline,pbs)配制含有4%牛血清蛋白(bovineserumalbumin,bsa)的参考蛋白液,并将参考蛋白液滴至反应电极与基体的间隙之间,量测的条件如下:vd=2v;vg=0.1v;脉冲时间=100μs。并于基体的源极端量测得到第一电流i1。
接着,以冲堤缓冲溶液(elutionbuffer)将反应电极与基体之间的牛血清蛋白溶液洗去。以上述含有4%牛血清蛋白的参考蛋白液作为溶剂,并以c反应蛋白作为溶质,调配浓度为0.5mg/l的c反应蛋白溶液。
接着,将c反应蛋白溶液滴至反应电极上后,并以上述相同量测条件(vd=2v;vg=0.1v;脉冲时间=100μs)的进行量测,以得到第二电流i2。
最后,将第二电流i2扣除第一电流i1即得到检测电流i。
要说明的是,实验例1选用含有牛血清蛋白的溶液作为溶剂的目的在于:由于血清蛋白是血液中最大量的蛋白质,使该配体液更接近于实际的人体血液环境,且先行滴上参考蛋白液量测该第一电流i1的步骤,能作为一背景值,因此,通过量测c反应蛋白溶液所贡献的第二电流i2减去参考蛋白(bsa)所产生的第一电流i1,即能得到仅是由c反应蛋白与受体结合后所贡献的检测电流i。
实验例3~实验例6
使用与实验例2大致上相同的方式进行测试,其差异仅在于:实验例3~实验例6所配制的c反应蛋白溶液的浓度分别为1.0mg/l、3.0mg/l、5.0mg/l以及10.0mg/l。
图4为实验例2~实验例6的δ增益值对浓度的关系图。由图4可知,δ增益值随着c反应蛋白的浓度增加而上升,且具有明显的趋势。
实验例7
使用与实验例1大致上相同的方式进行测试,其差异仅在于:实施例7的感测装置的反应电极上是键结有心肌钙蛋白l(cardiactroponinl,ctnl)的专一性单株抗体。此外,实施例7使用含有4%牛血清蛋白的参考蛋白液作为溶剂,并以心肌钙蛋白l作为溶质,调配浓度为1pm的心肌钙蛋白溶液进行量测。
实验例8~实验例10
使用与实验例7大致上相同的方式进行测试,其差异仅在于:实验例8~实验例10所配制的心肌钙蛋白溶液的浓度分别为10pm、50pm以及100pm。
图5为实验例7~实验例10的δ增益值对浓度的关系图。由图5可知,δ增益值随着心肌钙蛋白l的浓度增加而下降,且具有明显的趋势。
实验例11
在实验例11中,使用图2所示的感测装置200来进行检测,其中在感测装置的反应电极上已键结有c反应蛋白的专一性适体。
将人体全血滴至反应电极与基体的间隙之间,并将感测装置倒置,量测的条件如下:vd=2v;vg=0.1v;脉冲时间=100μs。并于基体的源极端量测得到第一电流i1。
接着,以冲堤缓冲溶液(elutionbuffer)将反应电极与基体之间的人体全血洗去。以上述人体全血作为溶剂,并以c反应蛋白作为溶质,调配浓度为1.28mg/l的c反应蛋白溶液。
接着,将上述c反应蛋白溶液滴至反应电极上后,将感测装置倒置,并以上述相同量测条件(vd=2v;vg=0.1v;脉冲时间=100μs)的进行量测,以得到第二电流i2。
最后,将第二电流i2扣除第一电流i1即得到检测电流i。
实验例12~实验例15
使用与实验例2大致上相同的方式进行测试,其差异仅在于:实验例12~实验例15所配制的c反应蛋白溶液的浓度分别为3.26mg/l、4.26mg/l、5.26mg/l以及11.26mg/l。
图6为实验例11~实验例15的δ增益值对浓度的关系图。由图6可知,δ增益值随着c反应蛋白的浓度增加而上升,且具有明显的趋势。
实验例16
使用与实验例11大致上相同的方式进行测试,其差异仅在于:实施例16的感测装置的反应电极上是键结有n端脑排钠利尿胜肽前体(n-terminalprobrainnatriureticpeptide,nt-probnp)的专一性适体。此外,实验例16使用人类全血作为溶剂,并以n端脑排钠利尿胜肽前体作为溶质,调配浓度为100pg/ml的nt-probnp溶液。
实验例17~实验例19
使用与实验例16大致上相同的方式进行测试,其差异仅在于:实验例17~实验例19所配制的nt-probnp溶液的浓度分别为450pg/ml、900pg/ml以及1800pg/ml。
图7为实验例16~实验例19的增益值对浓度的关系图。由图7可知,增益值随着n端脑排钠利尿胜肽前体浓度增加而下降,且具有明显趋势。
实验例20
使用与实验例11大致上相同的方式进行测试,其差异仅在于:实施例20的感测装置的反应电极上是键结有心肌钙蛋白l(cardiactroponinl,ctnl)的专一性适体。此外,实验例16使用人类全血作为溶剂,并以心肌钙蛋白l作为溶质,调配浓度为1ng/ml的心肌钙蛋白溶液。
实验例21~实验例22
使用与实验例20大致上相同的方式进行测试,其差异仅在于:实验例21~实验例22所配制的心肌钙蛋白溶液的浓度分别为2.0ng/ml以及3.0ng/ml。
图8为实验例20~实验例22的增益值对浓度的关系图。由图8可知,增益值随着心肌钙蛋白l的浓度增加而下降,且具有明显的趋势。
实验例23
使用与实验例11大致上相同的方式进行测试,其差异仅在于:实施例23的感测装置的反应电极上是键结有c反应蛋白的专一性单株抗体。此外,实施例23使用人体全血作为溶剂,并以c反应蛋白作为溶质,调配浓度为0.5mg/l的c反应蛋白溶液。
实验例24~实验例26
使用与实验例23大致上相同的方式进行测试,其差异仅在于实验例24~实验例26所配制的c反应蛋白溶液的浓度分别为1.0mg/l、3.0mg/l、以及10.0mg/l。
图9为实验例23~实验例26的δ增益值对浓度的关系图。由图9可知,δ增益值随着c反应蛋白的浓度增加而上升,且具有明显的趋势。
实验例27
使用与实验例11大致上相同的方式进行测试,其差异仅在于:实施例27的感测装置的反应电极上是键结有脑排钠利尿胜肽(brainnatriureticpeptide,bnp)的专一性单株抗体。此外,实施例27使用人体全血作为溶剂,并以脑排钠利尿胜肽作为溶质,调配浓度为50pg/l的脑排钠利尿胜肽溶液。
实验例28~实验例30
使用与实验例27大致上相同的方式进行测试,其差异仅在于实验例28~实验例30所配制的脑排钠利尿胜肽溶液的浓度分别为100pg/l、500pg/l以及1000pg/l。
图10为实验例27~实验例30的δ增益值对浓度的关系图。由图10可知,δ增益值随着脑排钠利尿胜肽的浓度增加而上升,且具有明显的趋势。
实验例31
使用与实验例11大致上相同的方式进行测试,其差异仅在于:实施例31的感测装置的反应电极上是键结有心肌钙蛋白l(cardiactroponinl,ctnl)的专一性单株抗体。此外,实施例31使用人体全血作为溶剂,并以心肌钙蛋白l作为溶质,调配浓度为0.024ng/l的心肌钙蛋白溶液。
实验例32~实验例34
使用与实验例29大致上相同的方式进行测试,其差异仅在于实验例32~实验例34所配制的心肌钙蛋白溶液的浓度分别为0.24ng/l、2.4ng/l以及24ng/l。
图11为实验例31~实验例34的δ增益值对浓度的关系图。由图11可知,δ增益值随着心肌钙蛋白l的浓度增加而下降,且具有明显的趋势。
综上所述,本实施例的血液检测方法可直接使用全血进行检测,且可减少检测期间血球的干扰。此外,本实施例的血液检测方法通过施加可调变脉波宽度与高度的脉波电压于反应电极,令反应电极与间隔设置的栅极端产生压差并具有电容效应,以克服屏蔽效应,而能直接于高盐浓度下检测血液中的标的物质。此外,本实施例的检测法方具有增益效果,因此可检测出细微的电信号。
虽然本发明已以实施例揭示如上,然其并非用以限定本发明,任何所属技术领域中技术人员,在不脱离本发明的精神和范围内,当可作些许的更改与润饰,故本发明的保护范围当视权利要求所界定者为准。
- 还没有人留言评论。精彩留言会获得点赞!