一种癌胚抗原(CEA)免疫检测试剂及其制备和检测方法与流程
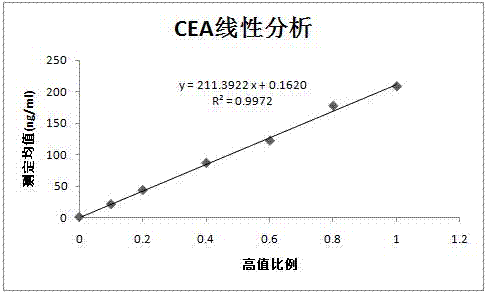
本发明涉及一种癌胚抗原检测试剂及其制备和检测方法,具体涉及一种癌胚抗原均相酶免疫检测试剂及其制备和检测方法。技术背景癌胚抗原(Carcinoembryonicantigen,CEA)是由Gold和Freeman等于1965年首次于结肠癌和胎儿肠组织中发现。在胚胎发育过程中,CEA作为细胞表面蛋白,主要形成于胃肠道和胰腺,并分泌于体液中。成人CEA的合成并未完全停止,也存在于许多与胃肠或肺来源有关的外胚层组织的癌细胞中。CEA主要在肝脏内灭活,半衰期为14d,生物活性目前仍不清楚,但可能与免疫抑制细胞的粘附有关。CEA是由45%-55%糖和50%蛋白质组成的瘤胎糖蛋白,相对分子质量为180-200kD,有9个抗原决定簇,其基因家族包括2个亚组的17个活化基因,属于非器官特异性肿瘤相关抗原。血清CEA升高主要见于:70%-90%的结肠腺癌患者CEA阳性,在其他恶性肿瘤中的阳性率顺序为胃癌、胰腺癌、小肠腺癌、肺癌、肝癌、乳腺癌、泌尿系癌肿。良性肿瘤、炎症和退行性疾病(例如胆汁淤积、结肠息肉、酒精性肝硬化患者、慢性肝炎、胰腺炎、溃疡性结肠炎、肺气肿)CEA含量会轻度或中度上升,但通常不超过10ng/ml。吸烟者中约有30%CEA大于5ng/ml。CEA可以作为良性与恶性肿瘤的鉴别诊断依据,其测定还用于指导肿瘤治疗及随访,能为病情判断、预后及疗效观察提供重要依据。检测CEA的常用方法有放射免疫法(RIA)、化学发光法、电化学发光法、金标记免疫渗滤层析、时间分辨荧光免疫分析法及酶联免疫吸附法(ELISA)等。放射免疫法最早用于CEA的检测,但在检测过程中容易产生放射性污染,且准确度低,需要专业的放射免疫仪器,在普通实验室难以开展,现阶段已很少使用。其余方法中,或者步骤繁琐,或者耗时较长,或者需要复杂昂贵的仪器设备,或者需要专业操作人员等,都不利于广泛应用于临床检测。均相酶免疫检测法灵敏度高、重复性好、稳定性强,操作简便并且可以在全自动生化分析仪上同时测定多个样品,实现癌胚抗原的高通量、快速化测定,有利于临床大规模推广使用。技术实现要素:本发明为了克服现有技术存在的缺陷,采用癌胚抗原特异性抗体及指示剂制备出癌胚抗原均相酶免疫检测试剂,该试剂可与各种类型自动生化分析仪联用,有助于实现癌胚抗原高通量、快速化检测,且对检测人员要求不高,有利于临床推广。本发明的目的在于提供一种癌胚抗原均相酶免疫检测试剂,其特征在于:含有癌胚抗原特异性抗体和指示剂。所述指示剂为酶试剂,其由癌胚抗原酶标偶联物和酶的底物组成,酶标偶联物为葡萄糖脱氢酶-癌胚抗原酶标偶联物,酶的底物为葡萄糖。所述的酶标偶联物为葡萄糖脱氢酶和癌胚抗原偶联形成。一种癌胚抗原免疫检测试剂的制备方法,其特征在于,包括如下步骤:(1)均相酶底物溶液的制备:将NAD+和葡萄糖用TRIS缓冲液溶解,配制得到均相酶底物;(2)葡萄糖脱氢酶-癌胚抗原酶标偶联物的制备:制备葡萄糖脱氢酶溶液(GDH),将GDH与癌胚抗原偶联,纯化偶联产物;(3)癌胚抗原均相酶免疫检测试剂的制备:试剂1(R1):由TRIS缓冲液、癌胚抗原特异性抗体、均相酶底物混合而成;试剂2(R2):由TRIS缓冲液、葡萄糖脱氢酶-癌胚抗原酶标偶联物混合而成。前述的一种癌胚抗原免疫检测试剂的制备方法,所述的步骤(1)具体过程为:将氧化态的烟酰胺腺嘌呤二核苷酸NAD+、葡萄糖用55mM、pH=8.0的TRIS缓冲液溶解制成均相酶底物。所述NAD+与葡萄糖的最终浓度均为22.50mM。前述的一种癌胚抗原免疫检测试剂的制备方法,所述的步骤(2)具体过程为:1)葡萄糖脱氢酶溶液的制备:a.称取8mgMgCl2、100mgNaCl和15.6mg的葡萄糖脱氢酶(100KU),室温下按顺序溶解于18ml50mMpH=9.0的TRIS缓冲液;b.按顺序加入337.5mg还原态的烟酰胺腺嘌呤二核苷酸NADH、140.2mg葡萄糖以及1.125mL卡必醇;c.逐滴加入3mL的二甲亚砜。2)葡萄糖脱氢酶-癌胚抗原酶标偶联物的制备:将癌胚抗原逐滴加入上述制得的葡萄糖脱氢酶溶液中,2-8℃搅拌过夜。所述癌胚抗原与葡萄糖脱氢酶的质量比为1:1000-1000:1。最后,通过G-25凝胶层析柱纯化酶标偶联物,于2-8℃下储存。前述的一种癌胚抗原免疫检测试剂的制备方法,所述的步骤(3)具体过程为:试剂1:将癌胚抗原抗体加入到上述均相酶底物中。抗体与均相酶底物体积比为1:100-1:10000,优选1:1000。试剂2:将葡萄糖脱氢酶-癌胚抗原酶标偶联物加到120mMpH=8.2的TRIS缓冲液中,上述偶联物与TRIS缓冲液的体积比为1:100-1:10000,优选1:3000。利用癌胚抗原免疫检测试剂的检测方法,其特征在于,包括以下步骤:1)将待测样本与癌胚抗原特异性抗体接触;2)根据待测样本中癌胚抗原与癌胚抗原特异性抗体的结合情况,利用指示剂判断样本中癌胚抗原的含量。所述待测样本为各种生理样本,例如血清、血浆、唾液或尿液等。优选的,待测样本为EDTA抗凝血浆。本发明的有益之处在于:本发明的癌胚抗原均相酶免疫检测试剂灵敏度高、重复性好、稳定性强,操作简便并且可以在全自动生化分析仪上同时测定多个样品,实现癌胚抗原的高通量、快速化测定,有利于临床大规模推广使用。附图说明图1是癌胚抗原均相酶免疫反应校准曲线图。图2是癌胚抗原均相酶免疫检测试剂线性范围图。图3是癌胚抗原均相酶免疫检测试剂相关性分析图。具体实施方式本发明所采用的技术原理是:样本中的抗原与酶标抗原竞争性结合抗体,待测样本中癌胚抗原的量越多,均相酶溶液中游离的酶标抗原的量就越多,酶促反应越快,导致吸光度值(OD)上升。本发明中所指的“抗体”不仅仅指完整的抗体分子,也包括保留完整抗体特异性结合能力的抗体片段或者衍生物。本发明的抗体可以是多克隆抗体也可以是单克隆抗体,优选多克隆抗体。一种癌胚抗原均相酶免疫检测试剂,包括:癌胚抗原特异性抗体、用于检测癌胚抗原特异性抗体-癌胚抗原复合物的指示剂。指示剂选自酶试剂、放射性同位素、荧光试剂或发光试剂中的一种,优选为酶试剂;所述的酶试剂由癌胚抗原酶标偶联物和酶的底物组成,酶标偶联物为葡萄糖脱氢酶-癌胚抗原酶标偶联物,其可通过化学合成方法得到,酶的底物为葡萄糖。上述癌胚抗原均相酶检测试剂的检测方法,包括以下步骤:1)将待测样本与癌胚抗原特异性抗体接触;2)根据待测样本中癌胚抗原与癌胚抗原特异性抗体的结合情况,利用指示剂判断样本中癌胚抗原的含量。所述待测样本为各种生理样本,例如血清、血浆、唾液或尿液等。优选的,待测样本为EDTA抗凝血浆。下面结合具体的实施例,进一步说明本发明。实施例一:均相酶底物的制备:将氧化态的烟酰胺腺嘌呤二核苷酸NAD+、葡萄糖用55mM、pH=8.0的TRIS缓冲液溶解制成均相酶底物。所述NAD+与葡萄糖的最终浓度均为22.50mM。实施例二:葡萄糖脱氢酶溶液的制备:a.称取8mgMgCl2、100mgNaCl和15.6mg的葡萄糖脱氢酶(100KU),室温下按顺序溶解于18ml50mMpH=9.0的TRIS缓冲液;b.按顺序加入337.5mg还原态的烟酰胺腺嘌呤二核苷酸NADH、140.2mg葡萄糖以及1.125mL卡必醇;c.逐滴加入3mL的二甲亚砜。实施例三:葡萄糖脱氢酶-癌胚抗原酶标偶联物的制备:将癌胚抗原逐滴加入上述制得的葡萄糖脱氢酶溶液中,2-8℃搅拌过夜。所述癌胚抗原与葡萄糖脱氢酶的质量比为1:1000-1000:1。最后,通过G-25凝胶层析柱纯化酶标偶联物,于2-8℃下储存。实施例四:癌胚抗原均相酶免疫检测试剂的制备:癌胚抗原均相酶免疫检测试剂,包括:癌胚抗原特异性抗体、用于检测癌胚抗原特异性抗体-癌胚抗原复合物的指示剂。指示剂选自酶试剂、放射性同位素、荧光试剂或发光试剂中的一种,优选为酶试剂;所述的酶试剂由癌胚抗原酶标偶联物和酶的底物组成,酶标偶联物为葡萄糖脱氢酶-癌胚抗原酶标偶联物,其可通过化学合成方法得到,酶的底物为葡萄糖。癌胚抗原均相酶免疫检测试剂在使用之前,为了避免指示试剂中的酶标偶联物和酶的底物发生反应,酶标偶联物和酶的底物是分开放置的,不混合,所以将酶的底物与上述癌胚抗原抗体混合在一起,也就是说,癌胚抗原均相酶免疫检测试剂包括两种分开设置的试剂,具体如下:1.试剂1的制备:将癌胚抗原特异抗体加到上述均相酶底物中,抗体与均相酶底物体积比为1:100-1:10000,在本实施例中具体的比例为1:1000。2.试剂2的制备:将葡萄糖脱氢酶-癌胚抗原酶标偶联物加到120mMpH=8.2的TRIS缓冲液中,上述偶联物与TRIS缓冲液的体积比为1:100-1:10000,在本实施例中具体的比例为1:3000。上述癌胚抗原免疫检测试剂的使用方法,包括以下步骤:1)将待测样本与癌胚抗原特异性抗体接触;2)根据待测样本中癌胚抗原与癌胚抗原特异性抗体的结合情况,利用指示剂判断样本中癌胚抗原的含量。具体的,检测时,将待测样本加到试剂1中,待测样本中的癌胚抗原与试剂1中的癌胚抗原抗体发生特异性结合,生成癌胚抗原抗体-癌胚抗原复合物;再加入试剂2,此时试剂2中的葡萄糖脱氢酶-癌胚抗原偶联物与试剂1中的酶底物混合接触,发生酶促反应,构成检测癌胚抗原特异性抗体-癌胚抗原复合物的指示剂,指示剂根据待测样本中癌胚抗原与癌胚抗原特异性抗体的结合情况判断待测样本中癌胚抗原的含量。由于葡萄糖脱氢酶-癌胚抗原偶联物与待测样本中的癌胚抗原竞争性结合癌胚抗原特异性抗体,所以,待测样本中癌胚抗原的量越多,均相酶溶液中游离的葡萄糖脱氢酶-癌胚抗原偶联物的量就越多,酶促反应越快,导致吸光度值(OD)上升。所述待测样本为各种生理样本,例如血清、血浆、唾液或尿液等。作为一种优选的方案,上述待测样本为EDTA抗凝血浆。实施例五:癌胚抗原均相酶免疫检测1.获得校准曲线:设置OlympusAU400全自动生化分析仪反应参数,操作过程为:先加试剂1,再加校准品,最后加入试剂2。加入试剂2后,测试波长为340nm处不同时间点的吸光度值,算出不同校准品浓度时的反应速率,实际操作过程中需不断调整试剂1和试剂2的体积比例,同时调整测光点,最后得出比较理想的反应校准曲线图,如图1所示。2.生化分析仪检测:以奥林巴斯AU400全自动生化分析仪操作为例:加入15μL样本,然后加入150μL试剂1,混匀孵育5min,加入150μL试剂2,混匀孵育30s,然后开始读取吸光度A1,再孵育5min后,读取吸光度A2,计算ΔA=A2-A1。反应条件:主/副波长:340/410nm;反应温度:37℃;方法学:终点法;反应方向:上升;定标方式:多点非线性。校准品浓度:0.00,10.00,20.00,40.00,80.00,160.00ng/mL。3.利用该校准曲线测定低、中、高浓度质控样本10次,上述质控样本为:将癌胚抗原校准品溶解于人血清中,浓度分别为2.50ng/ml,50.00ng/ml,100.00ng/ml。检测数据及数据分析见表1。表1样本测定及精密度评估样本低中高样本浓度(ng/ml)2.5050.00100.0012.4852.47100.2222.5653.28101.1232.5149.7198.3542.4552.68102.1452.5250.75104.2862.5551.32103.0272.4351.0195.3382.4948.5398.4992.5950.21100.59102.5749.86101.26平均值(ng/ml)2.5250.98100.48标准差(SD)0.05301.49192.5769精密度(CV%)2.102.932.56检测结果表明:本发明的均相酶免疫检测试剂测定的准确度高,精密度好,CV均低于3%。实施例六:癌胚抗原均相酶免疫检测线性分析癌胚抗原均相酶免疫检测试剂线性范围的评价结果见表2。表2癌胚抗原均相酶免疫检测试剂线性范围评价结果低值高值123均值理论值绝对偏差相对偏差(%)100.210.180.230.210.160.0531.250.90.120.8720.3220.6320.6121.30-0.69-3.240.80.242.8743.2842.6142.9242.440.481.130.60.485.2587.7385.1986.0684.721.341.580.40.6120.11121.18123.36121.55127.00-5.45-4.290.20.8176.93175.09179.28177.10169.287.824.6201210.28208.57205.15208.00211.55-3.55-1.68用接近线性范围下限的低浓度样本(0.21)稀释接近线性范围上限的高浓度样本(211.55),混合成6个稀释浓度,每个浓度重复测定3次,计算平均值。利用软件计算回归方程y=211.3922x+0.1620,R2=0.9972。实验结果表明,本发明癌胚抗原均相酶免疫检测试剂具有良好的线性范围。通过本发明的均相酶免疫检测试剂得到线性分析曲线,见图2。实施例七:癌胚抗原均相酶免疫检测试剂相关性分析对包括50例正常样本和10例异常样本在内的60例临床标本分别使用北京利德曼的磁微粒化学发光试剂盒和本发明的均相酶免疫检测试剂进行相关性分析,测定的数据见表3。表3真实样本测定值样本号均相酶免疫法测定值(ng/ml)磁微粒化学发光法测定值(ng/ml)14.894.9223.733.6734.394.3843.353.3253.022.9564.084.1373.233.1782.972.9292.582.61104.504.53112.142.16122.492.44132.292.37142.852.74152.932.88162.252.14173.433.51182.962.87193.914.05205.485.46219.259.38223.843.97233.733.78243.613.57253.123.03262.172.14274.484.25284.354.38293.463.51304.044.11318.898.85322.993.02337.066.98341.971.83352.492.45362.872.81374.985.02384.684.753914.4814.22402.742.68417.317.35424.994.87439.799.80444.744.72458.368.23463.693.71472.822.88483.593.65495.996.07503.053.04513.123.19523.533.58532.442.72542.011.96553.253.21562.923.09576.776.68583.743.72592.692.76604.544.55对上述数据作图,见图3,得到的线性方程为:y=0.9908x+0.0340,相关系数R2=0.9984,表明本发明的检测试剂测定的癌胚抗原临床标本准确度高。由于本发明的检测过程是由仪器全自动化完成,所以对检测人员的要求不高,易于实现和推广使用。需要说明的是,以上所述仅为本发明的实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书及附图内容所做的等效结构或等效流程变换,或直接或间接运用在其他相关
技术领域:
,均同理包括在本发明的专利保护范围内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1