一种碳酸酯类电解液及金属锂电池
1.本申请涉及锂金属二次电池的技术领域,尤其涉及一种碳酸酯类电解液及金属锂电池。
背景技术:
2.锂金属负极具有较高的理论比容量(3860mah g
‑1)和较低的电极电势(
‑
3.04v),因此可作为具有最高理论能量密度的金属离子电池的理想负极,具有巨大的开发潜力。然而,锂金属负极在充放电过程中容易形成锂枝晶而导致电池短路,而且表面固态电解质界面(sei)破裂会导致电解液消耗和库伦效率降低等问题。
3.通常,可采用向电解液中加入添加剂(如硝酸盐)的方式,调解锂离子沉积行为,提升sei的锂离子电导率,改善sei的物化性质,抑制锂枝晶的生长。然而,由于硝酸盐在碳酸酯类电解液中的溶解度较低,一般只能应用于醚类电解液中,而醚类电解液的氧化截止电压较低,不能和高压正极材料匹配,因此限制了其在高能量密度的金属锂电池中的应用。
技术实现要素:
4.有鉴于此,本申请提供一种能够提高硝酸盐在碳酸酯类电解液中的溶解度的电解液。
5.另外,还有必要提供一种由上述电解液制备的金属锂电池。
6.为实现上述目的,本申请提供了一种碳酸酯类电解液,包括锂盐、硝酸盐、助溶剂和溶剂,所述助溶剂包括冠醚及其衍生物,其中,所述助溶剂的分子结构中具有空穴,所述硝酸盐中阳离子的直径d1与所述助溶剂中空穴的直径d2之间的比值为0.7
‑
1.3。
7.在一些可能的实现方式中,d1与d2的比值为0.9
‑
1.1。
8.在一些可能的实现方式中,所述硝酸盐为硝酸锂、硝酸钠、硝酸钾、硝酸铷、硝酸铯、硝酸镁、硝酸钙、硝酸锶及硝酸钡中的一种或多种。
9.在一些可能的实现方式中,所述冠醚为12
‑
冠
‑
4,15
‑
冠
‑
5,18
‑
冠
‑
6及21
‑
冠
‑
7中的一种或多种。
10.在一些可能的实现方式中,在所述碳酸酯类电解液中,所述硝酸盐的浓度为0.05
‑
1mol/l,所述助溶剂的浓度为0.025
‑
3mol/l。
11.在一些可能的实现方式中,所述锂盐为六氟磷酸锂、双三氟甲磺酰亚胺锂、三氟甲磺酸锂、四氟硼酸锂、高氯酸锂、六氟砷酸锂、双(全氟乙基磺酰)亚胺锂、双氟磺酰亚胺锂、双草酸硼酸锂、(三氟甲基磺酰)亚胺锂及(正全氟丁基磺酰)亚胺锂中的一种或多种。
12.在一些可能的实现方式中,所述溶剂为碳酸乙烯酯、氟代碳酸乙烯酯、碳酸二甲酯、碳酸甲乙酯、碳酸二乙酯、碳酸丙烯酯、γ
‑
丁内酯、乙酸乙酯、甲酸甲酯、四氢呋喃、2
‑
甲基
‑
四氢呋喃、二甲氧基甲烷、1,2
‑
二甲氧基乙烷、乙腈、戊二腈、己二腈、磷酸三甲酯、环丁砜、甲乙砜、3
‑
(甲基磺酰基)
‑1‑
丙烯及3
‑
(甲基磺酰基)
‑1‑
丙炔中的一种或多种。
13.本申请还提供一种金属锂电池,包括正极、负极以及设于所述正极和所述负极之
间的隔膜,所述金属锂电池还包括所述的碳酸酯类电解液。
14.本申请中提供的碳酸酯类电解液中,硝酸盐为电解液提供硝酸根离子和阳离子,助溶剂易于阳离子发生配位反应,形成冠醚
‑
阳离子配位化合物,使得电解液中游离出更多的硝酸根离子,提高硝酸盐的溶解度。因此,使得硝酸盐可以应用于碳酸酯类电解液中,
附图说明
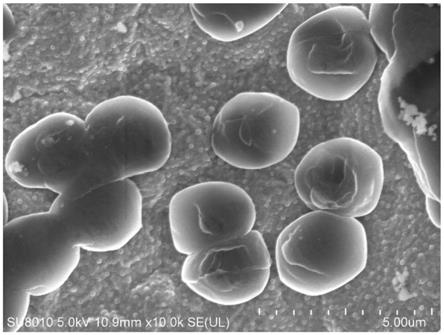
15.图1为实施例1中锂沉积10min的锂晶核的扫描隧道显微镜图。
16.图2为实施例1中锂沉积2h的扫描隧道显微镜图。
17.图3为对比例1中锂沉积10min的锂晶核的扫描隧道显微镜图。
18.图4为对比例1中锂沉积2h的扫描隧道显微镜图。
具体实施方式
19.下面详细描述本发明的实施例。下面通过参考附图描述的实施例是示例性的,仅用于解释本发明,而不能理解为对本发明的限制。
20.在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不一定指的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。
21.本申请提供一种碳酸酯类电解液,包括锂盐、硝酸盐、助溶剂和溶剂。所述助溶剂包括冠醚和冠醚的衍生物中的至少一种。其中,硝酸盐用于提供硝酸根离子和金属阳离子。冠醚和冠醚的衍生物中均具有空穴。冠醚和冠醚的衍生物可通过空穴与阳离子发生配位反应形成冠醚
‑
阳离子配位化合物。其中,阳离子的直径d1与空穴的直径d2之间的比值为0.7
‑
1.3。
22.在本申请的碳酸酯类电解液中,由于助溶剂能够与阳离子发生配位反应,形成冠醚
‑
阳离子配位化合物,使得电解液中释放出更多的游离的硝酸根离子,进而提升硝酸盐在电解液中的溶解度。同时,也克服了阳离子在金属锂电池中电极表面不稳定易发生共沉积或嵌入电极的现象。
23.同时,冠醚
‑
阳离子配位化合物在金属锂电池的电极表面具有很强的稳定性,不会与锂离子发生共沉积现象,但是可以吸附在锂枝晶的表面,在锂枝晶的表面形成“屏蔽”,冠醚
‑
阳离子配位化合物在锂枝晶表面具有“屏蔽效应”,进一步抑制锂枝晶生长,提高金属锂电池库伦效率。
24.另外,硝酸盐中的硝酸根可以吸附在金属锂电池的电极的表面,能够诱导锂离子形成球状晶核,还能在金属锂电池中电极的表面分解,形成利于锂离子传到锂离子导体的li3n,加速锂离子的平面沉积,也能够抑制锂枝晶生长。
25.而且,由于碳酸酯类电解液和高电压正极材料有很好的匹配性,因此能够用于制备高能量密度的金属锂电池。
26.其中,当硝酸盐中阳离子的直径d1与助溶剂的空穴直径d2的比值小于0.7或大于1.3,电解液中阳离子与助溶剂形成的配位化合物不稳定,极易分解。
27.在一些实施方式中,d1与d2的比值为0.9
‑
1.1,优选为0.85
‑
1。
28.在一些实施方式中,所述硝酸盐为硝酸锂、硝酸钠、硝酸钾、硝酸铷、硝酸铯、硝酸镁、硝酸钙、硝酸锶及硝酸钡中的一种或多种。
29.在一些实施方式中,所述冠醚为12
‑
冠
‑
4,15
‑
冠
‑
5,18
‑
冠
‑
6及21
‑
冠
‑
7中的一种或多种。
30.在一些实施方式中,在所述碳酸酯类电解液中,所述硝酸盐的浓度为0.05
‑
1mol/l,所述助溶剂的浓度为0.025
‑
3mol/l。
31.当电解液中硝酸盐的浓度小于0.05mol/l时,对抑制锂枝晶效果不明显,当硝酸盐的浓度大于1mol/l时,硝酸盐在电解液中的含量较多,会出现部分不溶解现象。当助溶剂的浓度小于0.025mol/l时,对提高硝酸盐的溶解度不明显;当助溶剂的浓度大于3mol/l时,会提高生产成本。
32.在一些实施方式中,所述锂盐为六氟磷酸锂、双三氟甲磺酰亚胺锂、三氟甲磺酸锂、四氟硼酸锂、高氯酸锂、六氟砷酸锂、双(全氟乙基磺酰)亚胺锂、双氟磺酰亚胺锂、双草酸硼酸锂、(三氟甲基磺酰)亚胺锂及(正全氟丁基磺酰)亚胺锂中的一种或多种。
33.在一些实施方式中,所述溶剂为碳酸乙烯酯、氟代碳酸乙烯酯、碳酸二甲酯、碳酸甲乙酯、碳酸二乙酯、碳酸丙烯酯、γ
‑
丁内酯、乙酸乙酯、甲酸甲酯、四氢呋喃、2
‑
甲基
‑
四氢呋喃、二甲氧基甲烷、1,2
‑
二甲氧基乙烷、乙腈、戊二腈、己二腈、磷酸三甲酯、环丁砜、甲乙砜、3
‑
(甲基磺酰基)
‑1‑
丙烯、3
‑
(甲基磺酰基)
‑1‑
丙炔中的一种或多种。
34.本申请还提供一种金属锂电池,包括所述碳酸酯类电解液,还包括正极、隔膜和负极。
35.本申请提供的金属锂电池中的电解液可以改善锂离子沉积,提高锂离子电导率,抑制锂枝晶的生长,提高金属锂电池的电化学性能。
36.下面将结合实施例对本发明的方案进行解释。本领域技术人员将会理解,下面示例仅用于解释本发明,而不能理解为对本发明的限制。除另有交待,以下实施例中涉及的未特别交待的试剂、软件及仪器,都是常规市售产品或者开源的。
37.实施例1
38.电解液的制备:
39.室温下,在氩气保护手套箱中,配制10ml的电解液。
40.首先,将0.01mol lipf6加入到氟代碳酸乙烯酯、碳酸乙烯酯和碳酸二乙酯的混合溶剂中,得到混合液,其中,氟代碳酸乙烯酯:碳酸乙烯酯:碳酸二乙酯的体积比为2:9:9。在混合液中加入0.001mol的硝酸铷和0.001mol的18
‑
冠
‑
6,充分搅拌1h,得到均一的电解液,其中,硝酸铷中的阳离子(rb
+
)的直径d1与18
‑
冠
‑
6的中心空穴直径d2之比为1。
41.金属锂电池的制备:
42.采用铜箔作为正极,锂箔作为负极,celgard隔膜作为隔膜,取上述制备的60μl的电解液组装成扣式电池。
43.实施例2
44.实施例2与实施例1的不同之处在于:电解液的制备中,将硝酸铷替换为硝酸钾。
45.实施例3
46.实施例3与实施例1的不同之处在于:电解液的制备中,将硝酸铷替换为硝酸钠,将
18
‑
冠
‑
6替换为15
‑
冠
‑
5。
47.实施例4
48.实施例4与实施例1的不同之处在于:电解液的制备中,将0.001mol的硝酸铷改为0.0015mol,0.001mol的18
‑
冠
‑
6改为0.0015mol。
49.实施例5
50.实施例5与实施例1的不同之处在于:电解液的制备中,将硝酸铷替换为硝酸铯,将18
‑
冠
‑
6替换为21
‑
冠
‑
7。
51.实施例6
52.实施例6与实施例1的不同之处在于:电解液的制备中,将硝酸铷替换为硝酸镁,将18
‑
冠
‑
6替换为12
‑
冠
‑
4。
53.实施例7
54.实施例7与实施例1的不同之处在于:电解液的制备中,将硝酸铷替换为硝酸钙,将18
‑
冠
‑
6替换为15
‑
冠
‑
5。
55.实施例8
56.实施例8与实施例1的不同之处在于:电解液的制备中,将硝酸铷替换为硝酸钡。
57.实施例9
58.实施例9与实施例1的不同之处在于:电解液的制备中,将硝酸铷替换为硝酸锶。
59.实施例10
60.实施例10与实施例1的不同之处在于:电解液的制备中,将0.001mol的硝酸铷替换为0.002mol的硝酸锂,将0.001mol的18
‑
冠
‑
6替换为0.002mol的12
‑
冠
‑
4。
61.对比例1
62.对比例1与实施例1的不同之处在于:电解液的制备中,不加入硝酸铷和18
‑
冠
‑
6。
63.对比例2
64.对比例2与实施例1的不同之处在于:电解液的制备中,不加入18
‑
冠
‑
6,硝酸铷无法溶解于混合液中,且仍然为白色沉积状。
65.金属锂电池的制备中,取上述电解液的上清液组装于电池内。
66.对比例3
67.对比例3与实施例1的不同之处在于:电解液的制备中,不加入硝酸铷。
68.对比例4
69.对比例4与实施例1的不同之处在于:电解液的制备中,将硝酸铷替换为硝酸铯,将18
‑
冠
‑
6替换为12
‑
冠
‑
4,硝酸铯无法溶解于混合液中。
70.金属锂电池的制备中,取上述电解液的上清液组装于电池内。
71.对比例5
72.对比例5与实施例1的不同之处在于:电解液的制备中,将硝酸铷替换为硝酸锂,将18
‑
冠
‑
6替换为21
‑
冠
‑
7,硝酸锂无法溶解于混合液中。
73.金属锂电池的制备中,取上述电解液的上清液组装于电池内。
74.直径d1:d2比值的计算方式:如表1和表2,计算离子直径与冠醚的空穴直径的比值,即得到d1:d2的比值,其中冠醚的空穴直径以表2中直径范围的中间值计算。
75.表1离子直径
76.li
+
na
+
k
+
rb
+
cs
+
mg
2+
ca
2+
sr
2+
ba
2+
1.522.042.762.963.341.442.002.362.70
77.表2几种冠醚的空穴直径
78.12
‑
冠
‑
415
‑
冠
‑
518
‑
冠
‑
621
‑
冠
‑
71.20
‑
1.501.70
‑
2.202.60
‑
3.203.40
‑
4.30
79.对各实施例和对比例制备的金属锂电池进行电化学性能测试。其中,电化学性能测试为:采用电化学工作站,以0.5ma/cm
‑2放电2h,以0.5ma/cm
‑2充电1.0v,循环150周,记录库伦效率。测试结果记录于表3中。
80.表3实施例1
‑
10和对比例1
‑
5的电解液的条件及金属锂电池性能
[0081][0082]
在表3中,实施例1
‑
10制备的金属锂电池的前10周和前150周的平均库伦效率均大于对比例1,表明在碳酸丙烯酯类的电解液中,加入硝酸盐和助溶剂冠醚有助于提高金属锂电池的库伦效率。
[0083]
实施例1制备的金属锂电池的前10周和前150周的平均库伦效率均大于对比例2和对比例3,表明加入助溶剂有助于提高硝酸盐的溶解度,从而提高金属锂电池的库伦效率。
[0084]
在同时添加了硝酸盐和助溶剂冠醚的条件下,相较于实施例5和实施例6,由于对比例4中直径d1和d2的比值过大时,因此平均库伦效率较低,这是因为d1和d2的比值过大时硝酸盐中阳离子与助溶剂冠醚形成的配位化合物极不稳定。
[0085]
另外,相较于实施例5,由于对比例5中直径d1和d2的比值过小时,因此平均库伦效率较低,这是由于d1和d2的比值过小时硝酸盐中阳离子与助溶剂冠醚形成的配位化合物也极不稳定,易分解。
[0086]
在本申请中,由于硝酸盐的浓度大于1mol/l时,硝酸盐很难完全溶解,故并未对大于1mol/l的硝酸盐实验进一步探究。
[0087]
参考图1至图4,为了进一步测试电解液中硝酸盐和助溶剂对锂沉积的影响,进一步采用电化学工作站,以0.5ma/cm
‑2分别在实施例1和对比例1的铜箔上沉积10min和2h,之后,在氩气保护手套箱中拆开扣式电池后,对铜箔表面进行扫描隧道显微镜测试。结果表明,沉积10min后,实施例1的锂晶核形貌呈球状晶核,对比例1的锂晶核形貌呈针状晶核;当沉积2h后,实施例1的锂晶核形貌呈平面沉积,对比例1的锂晶核形貌呈枝晶状沉积。这也说明,加入有硝酸盐和助溶剂的碳酸酯类电解液可以调节锂沉积方式,使锂沉积形成球状晶核并沿着平面生长,改善锂沉积的形貌。
[0088]
同时,本申请中还对实施例2
‑
10和对比例2
‑
5中分别沉积10min和2h的铜箔表面进行扫描隧道显微镜测试,其结果表明,沉积10min后,实施例2
‑
10的锂晶核形貌均呈球状晶核,对比例2
‑
5的锂晶核形貌均呈针状晶核。当沉积2h后,实施例2
‑
10的锂晶核形貌呈平面沉积,对比例2
‑
5的锂晶核形貌均呈枝晶状沉积。这也再次证明了硝酸盐和助溶剂同时加入碳酸酯类电解液中可以调节锂沉积方式。
[0089]
以上实施方式仅用以说明本发明的技术方案而非限制,尽管参照以上实施方式对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或等同替换都不应脱离本发明技术方案的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1