从牡蛎肉生成3,5‑二羟基‑4‑甲氧基苄醇的生成方法与流程
本发明涉及从牡蛎肉生成3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的生成方法。
背景技术:
牡蛎、例如长牡蛎(Crassostrea gigas)是属于珍珠贝目牡蛎科的双壳类,其栖息地遍及以日本为代表的东亚全域。近年来,在法国、澳大利亚也养殖着长牡蛎,作为在世界中最常供人们食用的牡蛎而闻名。
由于牡蛎的营养价值高,因而自古以来被人们食用,如前述那样除了糖原和蛋白质之外,还大量地包含钙、锌、硒、铜、锰等矿物质。
另外,作为源自牡蛎的抗氧化物,报告有如下的抗氧化物:作为酶性抗氧化物质的SOD、CAT、GPx、以及Prx6,作为非酶性抗氧化物质的金属硫蛋白、解偶联蛋白5(UCP5)、抗坏血酸、α-生育酚、β-胡萝卜素。
现有技术文献
专利文献
专利文献1:日本特开2010-193756号公报
技术实现要素:
发明想要解决的课题
近年来,本件发明的发明人成功地发现源自牡蛎的优异的所谓新型抗氧化物质3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol),进一步确定了其化学结构,而且也成功地进行前述抗氧化物质的化学合成,而且,也成功地在不源自牡蛎的情况下或者源自牡蛎的情况下这两种情况下,都提供以优异的所谓3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)为有效成分的新型抗氧化剂以及抗氧化剂组合物。
但是,从生的牡蛎肉内没有发现3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol),关于是否可通过任何的萃取、制造从而从生的牡蛎肉中萃取、生成前述3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的有效成分,这是未确认的状态。
这样,本申请发明人在由生的牡蛎肉制成包含了很多有效成分的牡蛎肉浸膏之时,成功地发现一种生成方法,其可在牡蛎肉浸膏的萃取阶段生成从当初的生的牡蛎肉中完全没有发现的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
于是,本发明的目的在于提供一种生成方法,其可在牡蛎肉浸膏的萃取阶段生成从当初的生的牡蛎肉中完全没有发现的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
用于解决问题的方案
本发明的特征在于,
通过将在生的状态下没有检测到3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的生牡蛎肉以6小时以上在98℃至100℃进行加热,从而从前述加热处理了的牡蛎肉液生成3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol);
或者,其特征在于,
通过以至少9小时以上、90℃以上将在生的状态下没有检测到3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的生牡蛎肉进行加热,从而从前述加热处理了的牡蛎肉液生成3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol);
或者,其特征在于,
将在生的状态下没有检测到3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的生牡蛎肉加入于萃取溶液内而萃取出牡蛎肉浸膏,将所萃取的牡蛎肉浸膏萃取液在1个大气压的状态下以至少10小时以上在90℃以上进行加热,从而从前述加热了的牡蛎肉萃取液生成3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol);
或者,其特征在于,
通过在1个大气压以上的加压状态下将在生的状态下没有检测到3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的生牡蛎肉进行加热,从而从在前述加压状态下加热了的牡蛎肉液生成3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol);
或者,其特征在于,
通过在3个大气压以上的加压状态下以至少1小时以上在90℃以上将在生的状态下没有检测到3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的生牡蛎肉进行加热,从而从在前述加压状态下加热了的牡蛎肉液生成3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol);
或者,其特征在于,
将在生的状态下没有检测到3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的生牡蛎肉加入于萃取溶液内而萃取出牡蛎肉浸膏,将所萃取的牡蛎肉浸膏萃取液在3个大气压以上的加压状态下以至少1小时以上在90℃以上进行加热,从而从在前述加压状态下加热了的牡蛎肉浸膏萃取液生成3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
发明的效果
本发明起到如下的优异效果:可通过将前述牡蛎肉进行加热或者加压从而生成从当初的生的牡蛎肉中完全没有发现的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
附图说明
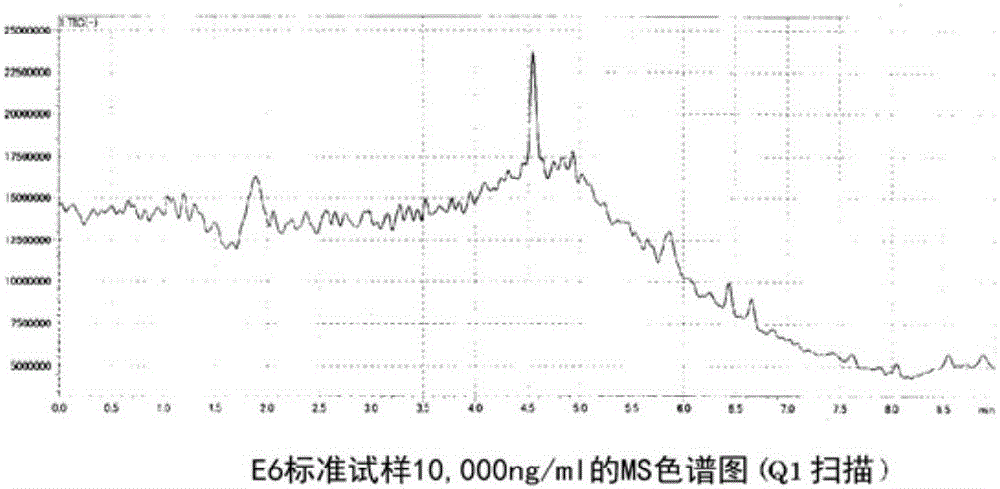
图1所示为E6标准试样10,000ng/ml的MS色谱图(Q1scan)的说明图。
图2所示为E6标准试样10,000ng/ml的MS光谱(Q1scan)的说明图。
图3所示为E6标准试样10,000ng/ml的MS色谱图(product ion scan)的说明图。
图4所示为E6标准试样10,000ng/ml的产品离子(precursor ion:m/z 169.10)的说明图。
图5所示为E6标准试样100ng/ml的MRM色谱图的说明图。
图6所示为E6标准试样的校正曲线的说明图。
图7所示为在牡蛎浸膏萃取后,在标准大气压下加热了2小时的样品中的E6的MRM色谱图的说明图。
图8所示为在牡蛎浸膏萃取后,在标准大气压下加热了18小时的样品中的E6的MRM色谱图的说明图。
图9所示为在牡蛎浸膏萃取后,在3atm下加热了1小时的样品中的E6的MRM色谱图的说明图。
图10所示为在牡蛎浸膏萃取后,在3atm下加热了2小时的样品中的E6的MRM色谱图的说明图。
图11所示为标准大气压下的加热实验样品的E6的LC-MS/MS分析结果的说明图。
图12所示为标准大气压下的加热实验样品的E6的LC-MS/MS分析结果的说明图。
图13所示为使用了压力釜的加压加热实验样品的E6的LC-MS/MS分析结果的说明图。
图14所示为分析结果的说明图。
图15是说明分析条件的说明图。
图16是分析报告(1)的说明图。
图17是分析报告(2)的说明图。
具体实施方式
以下,基于图中所示的一个实施例说明本发明。
实施例
(关于测定仪器以及测定方法)
对于在生牡蛎肉以及牡蛎肉浸膏的萃取液中是否存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol:以下称为E6),另外究竟以怎样的浓度存在,进行测定、分析之时,使用了高速色谱仪质谱仪(LCMS-8040:SHIMADZU制)。
1)LC-MS/MS的分析条件
LC-MS/MS的分析条件示于表1。
LC分析条件:分离柱使用了ODS的Shim-Pack VP-ODS(150mmL×2.0mmI.D.,5μm)。流动相A使用0.05%乙酸水溶液,流动相B使用乙腈,进行了梯度分析(流动相B:0min 5%→7min 100%→9.5min 5%→14min 5%)。流速设定为0.25ml/min,色谱柱恒温箱温度设定为40℃。试样注入量设为了1μL。E6利用负离子离子模式而检测,因而测定全都利用负离子离子模式进行。
MS/MS分析条件:离子化法使用了电喷射离子化法、(Electrospray Ionization:ESI法)。作为MS的参数,设为DL温度:250℃、雾化气体(nebulizer gas):流量3L/min、加热块(heat block)(BH)温度:400℃、干燥气体流量:15L/min。
表1.LC-MS/MS的各参数的设定值
2)E6标准试样的MS光谱
首先,生成成为基准的E6的试样,使用该E6的标准试样而进行各种分析,根据各分析结果,确认出在E6中究竟具有怎样的特性。
首先,利用Q1扫描(MS范围m/z 50至500)测定了E6的标准试样10,000ng/ml,结果为在保持时间4.4至4.6分钟处检测出峰(图1)。
而且,根据该峰部分的MS光谱,作为源自E6的信号,可确认出作为脱质子化离子[M-H]-的前体离子m/z 169.3(图2)。
3)E6的标准试样的产品离子扫描光谱
接着,在定性分析中,使用了Q1扫描、产品离子扫描。关于产品离子扫描,设定作为E6的脱质子化离子[M-H]-的前体离子m/z 169.1,利用碰撞能量10V、20V、30V进行了分析。
在E6的标准试样10,000ng/ml的产品离子扫描中,在保持时间4.4至4.6分钟处检测出峰(图3)。
而后,根据源自峰部分的MS光谱(图4),可获得E6的标准试样的产品离子的图案。
4)E6的标准试样的MRM色谱图
在定量分析中,使用了多重反应监测(MRM)。MRM转换根据自动最优化而确定。使用了Q1/Q3=169.1/154.1(定量用转换)、169.1/136.9、169.1/125.1(定性用转换)。予以说明,各自的碰撞能量设定为15V、28V、13V。
在上述的条件下,测定了E6的标准试样100ng/ml的MRM色谱图,结果为在保持时间5.2至5.5分钟处检测出峰(图5)。
而且,检测出E6特有的转换(Q1/Q3=169.1/154.1、169.1/136.9、169.1/125.1),因而确认了峰为E6。
予以说明,关于保持时间,根据LC的泵压等装置的设置环境等,有时会产生少许的偏差。然而,Q1/Q3=169.1/154.1、169.1/136.9、169.1/125.1无需变动。
5)E6的定量分析
对于E6的标准试样(1-1,000ng/ml),各浓度各3次利用MRM进行测定,制成了E6的校正曲线。校正曲线的相关系数R为0.99991。
关于该校正曲线的使用,将牡蛎肉浸膏的萃取液进行加热、加压处理,将该样品的特性与该校正曲线相比较,由此在检测各自的E6浓度的数值中使用。
以上是,通过对成为E6(即3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol))的基准的试样进行分析而得到的检测结果。
而且判明,将后述的牡蛎肉的萃取液以预定时间进行了加热、加压时,获得相同检测结果,获得相同特性,另外,将萃取液以预定时间加热、加压时,则发现E6,即,3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
6)加热加压实验样品的MRM色谱图
首先,最初,将生牡蛎肉进行押压,压碎,从而液体化。而后,在该液体化了的生牡蛎中,对于是否存在怎样的浓度的E6即3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol),进行了测定。
但是,在该液体化了的生牡蛎中,在保持时间5.2至5.5分钟处完全没有观察到峰,将该生牡蛎肉进行押压,压碎,在液体化了的样品中完全没有发现E6。
接着,在加热实验(没有加压)中,将1L的纯水加入于1kg的生牡蛎,在标准大气压下以1小时在例如90℃以上加热,然后将去除了固形物(煮牡蛎)的牡蛎浸膏(萃取液)在例如90℃以上进行了长时间加热。
而且,在前述加热状态下,每隔2小时进行取样(在16小时至19小时为每隔1小时),向该取样出的萃取液中,按照该萃取液的乙醇浓度例如为70%的方式加入100%乙醇,将其萃取液进行离心分离(8100G、10分钟),获得了上清液。
而后,将前述上清液稀释约100倍,稀释约100倍而得到的上清液中的E6浓度通过MRM而测定出(图11、图12)。
例如,图7示出,将牡蛎浸膏萃取后的萃取液在标准大气压下加热了2小时的样品中的E6的MRM色谱图。
如根据图7而理解的那样,在保持时间5.2至5.5分钟处完全没有观察到峰。由此可理解为,将牡蛎浸膏萃取后的萃取液在标准大气压下加热了2小时的情况下,没有检测到E6。
接着,图8示出,对于牡蛎浸膏萃取后的萃取液,在标准大气压下加热了18小时的样品中的E6的MRM色谱图。于是,在保持时间5.2至5.5分钟确认出单一的峰,可理解为检测出E6(图8)。
而且,根据前述图6中所示的E6标准试样的校正曲线与MRM色谱图的解析,可理解E6浓度为4.86±0.10μg/ml(图11、图12)。
进一步,加热了18小时之时的液量为125.38g,因此从1kg生牡蛎生成的E6的总量为609±13μg。
另外,在存在有加压的加热实验中,向20kg的牡蛎中加入20L的纯水,在标准大气压下加热了2小时,然后去除固形物(煮牡蛎),使用压力釜(KAJIWARA、OAMVPα-C-08EL)在3个大气压下加热2小时。
每隔1小时进行取样,按照乙醇浓度为70%的方式加入100%乙醇,然后进行离心分离(8100G、10分钟),获得了上清液。进一步,将该上清液稀释约100倍,通过MRM测定该样品中的E6浓度从而获得了图13的结果。
于是,图9示出将牡蛎浸膏萃取后的萃取液在3atm下加热了1小时的样品中的E6的MRM色谱图,在保持时间5.2至5.5分钟处确认出单一的峰,检测出E6。
而且,根据前述图6中所示的E6标准试样的校正曲线与MRM色谱图的解析,从而E6浓度为1.7±0.10μg/mL(图13)。
在3个大气压下加热了1小时之时的液量为21.2kg,因此从20kg生牡蛎生成的E6的总量为36040±2120μg。换算为每1kg生牡蛎时,则所生成的E6为1802±106μg(图13)。
与没有加压的加热实验(在标准大气压下加热了18小时的牡蛎萃取浸膏)相比,存在有加压的情况下(在3个大气压下加热了1小时的牡蛎萃取浸膏)大概看来,E6浓度低。
但是可理解为:存在有加压的情况下,样品中的水分蒸发量少并且获得的液量多,因而按照每1kg牡蛎进行比较时,则与没有加压的情况相比,E6的产量为约3倍多。
图10示出对于牡蛎浸膏萃取后的萃取液,在3atm下加热了2小时的样品中的E6的MRM色谱图。
在保持时间5.2至5.5分钟处确认出单一的峰,检测有E6(图10)。
而后,根据前述图6中所示的E6标准试样的校正曲线与MRM色谱图的解析,从而E6浓度为3.5±0.39μg/mL(图13)。
这样地,在3个大气压下加热了1小时之时的液量为19.1kg,因此从生牡蛎20kg生成的E6的总量为66850±7449μg。换算为每1kg生牡蛎时,则所生成的E6为3343±373μg(图13)。
与没有加压的加热实验(在标准大气压下加热了18小时的牡蛎萃取浸膏)相比,在存在有加压的情况下(在3个大气压下加热了2小时的牡蛎萃取浸膏)大致看来E6浓度低。
但是,在存在有加压的情况下,样品中的水分蒸发量少并且获得的液量多,因而按照每1kg牡蛎进行比较时,则与没有加压的情况相比,E6的产量为约5.5倍多。
根据这些事实可确认,E6通过长时间的加热而生成,进一步利用加压而使得收集量变多。
此处,根据上述的分析结果而简要说明本实施例。
首先,将生牡蛎肉进行押压,压碎,从而液体化。
而后,在该液体化了的生牡蛎中,对于是否存在怎样的浓度的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。
然后,将生牡蛎进行押压,压碎,从液体化而得到的液体中,完全没有检测到3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。即,在生牡蛎肉当初的细胞中,没有发现3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
接着,如前所述,向萃取容器中按成为约1对1的比例加入生牡蛎肉与萃取用溶液体例如蒸馏水,将加入了前述生牡蛎肉的萃取用液体在1个大气压下在1小时内在例如92℃至94℃的高温进行了加热萃取。
这是所谓的称为加热萃取的牡蛎肉浸膏的萃取方法,利用该方法,可在前述萃取用液体内萃取到从前以来在生牡蛎肉中存在的很多有效成分。此处,将萃取到在生牡蛎肉中存在的很多有效成分并且去除了生牡蛎肉的前述萃取用液体,称为萃取液。
但是,在该萃取液之中也没有检测到3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。予以说明,萃取了其它的有效成分。
接着,对于前述的萃取液,其后在1个大气压下进行了2小时的加热处理(前面同样的92℃至94℃)。算入当初的萃取时间,总计是3小时的加热处理。
然而,在进行了该3小时的加热处理的萃取液中,也没有发现3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在。如图7所示。
进一步,在1个大气压下以4小时(加入萃取时间时则合计为5小时)对于前述萃取液进行加热处理(92℃至94℃),对于在该萃取液中是否存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。
在该5小时的加热处理(92℃至94℃)中,该萃取液内的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在量为0.09(μg/ml),这在浓度测定的数值方面是定量极限以下的数值,没有获得确实地存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)这样的可靠性。
接着,在1个大气压下以6小时(加入萃取时间时则合计为7小时),对于前述萃取液进行加热处理(92℃至94℃),对于在该萃取液中是否存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定,但是即使在该萃取液中,3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在量也为0.12(μg/ml),仍然是作为浓度数值而言定量极限以下的数值,在此情况下,也没有获得确实地存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)这样的可靠性。
但是,在1个大气压下以6小时(加入萃取时间时则合计为7小时)对于前述萃取液在98℃至100℃的高温下进行加热处理,为了评价在该萃取液中是否存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol),因而使用HPLC(Prominence LC-20A,Shimadzu),进行了E6的存在测定(图14、图15、图16、图17)。
而后,在该萃取液中,关于3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在,可发现作为浓度数值而言定量极限以上的数值。
即,在此情况下,获得了存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)这样的可靠性。
这样地,在100℃附近的高温进行了加热处理的情况下,即使通过6小时以上的加热处理,关于3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)即E6,也可发现作为浓度数值而言定量极限以上的数值。
进一步,在1个大气压下以8小时(加入萃取时间时则9小时)对于前述萃取液进行加热处理(92℃至94℃),对于在该萃取液中是否存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。
然而,即使在该萃取液中也无法确实地确认3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在。即,获得了0.29(μg/ml)这样的数值,但是仍然是浓度测定的定量极限以下的数值。
接着,在1个大气压下以10小时(加入萃取时间时则11小时)对于前述的萃取液进行加热处理(92℃至94℃),对于在该萃取液中是否存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。
而后,对于在进行了该长时间加热处理(92℃至94℃)的萃取液内是否发现预定浓度的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在进行了确认。
于是,可计量出0.54(μg/ml)这样的首先超过浓度测定的定量极限的数值,可确认出在进行了前述合计11小时的加热处理的萃取液内,明显地存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。这表示,每1kg牡蛎生成了215.8μg的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
进一步,在1个大气压下以12小时(算入当初的萃取时间时,则合计13小时)对于前述萃取液进行加热处理,对于在该萃取液中是否存在预定浓度的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。
而后,对于在该萃取液内是否发现3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在进行确认,结果可测定出0.86(μg/ml)这样的进一步超过定量极限的增加了的数值。
而且,这表示,每1kg牡蛎生成了288.4μg的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
进一步,在1个大气压下以14小时(算入前述萃取时间的1小时时,则合计15小时)对于前述萃取液,进行加热处理,对于在该萃取液中是否存在预定浓度的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。
而后,对在该萃取液内是否发现3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在进行确认,结果可测定出1.42(μg/ml)这样的进一步超过定量极限的数值,可确认:当进行长时间加热处理时,则在萃取液内进一步增加地存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
而且,在此情况下表示,每1kg牡蛎生成了373.9μg的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
接着,在1个大气压下以16小时(算入萃取时间而为17小时)对于前述萃取液进行加热处理,对于在该萃取液中是否存在预定浓度的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。
而后,对于在该萃取液内是否发现3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在进行确认,结果可测定出2.63(μg/ml)这样的再次增加了的数值,可确认通过长时间的热处理而增加地存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
在此情况下表示,每1kg牡蛎生成了478.6μg的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
进一步,在1个大气压下以17小时(算入萃取时间而为18小时)对于前述萃取液进行加热处理,对于在该萃取液中是否存在预定浓度的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。
而后,对于在该萃取液内是否发现3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在进行确认,结果可测定出再次增加了的3.42(μg/ml)这样的数值,可确认存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
在此情况下表示的是,每1kg牡蛎生成了519.5μg的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
接着,在1个大气压下以18小时(加入萃取时间而为19小时)对于前述萃取液进行加热处理,对于在该萃取液中是否存在预定浓度的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。
于是,可测定到作为进一步增加了的浓度数值4.86(μg/ml)这样的数值。如图8所示。
这表示,每1kg牡蛎生成了609.3μg的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
进一步,在1个大气压下以19小时(算入萃取时间的1小时而20小时)对于前述萃取液进行长时间的加热处理,对于在该萃取液中是否存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)进行了测定。而后,对于在该萃取液内是否发现预定浓度的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的存在进行确认,结果可测定出6.49(μg/ml)这样的数值,可确认进一步增加地存在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
而且,在此情况下表示,每1kg牡蛎生成了581.3μg的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
这样地,当初3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)在生牡蛎中完全不存在,并且另外在1个大气压下以1小时进行了牡蛎肉浸膏的加热萃取的萃取液中也完全不存在,没有检测到,但是确认了,越将该萃取液进行极其长时间的加热,另外,越将加热温度设为100℃附近则越增加地生成。
其结果,在将牡蛎肉浸膏的萃取液在1个大气压下加热处理了19小时(加入萃取时间的1小时时则为20小时)的情况下,将萃取液的比重设为1时,则由1kg生牡蛎生成了581μg(6.49μg×89.57g)的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
进一步,如前所述,对萃取液在1个大气压下进行了2小时至8小时加热处理的情况下,完全没有检测到预定浓度的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol),但是如根据图13而理解的那样,对于萃取液(去除了生牡蛎的萃取液体)在3个大气压下加热处理了1小时的情况下,获得3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的浓度为1.7(μg/ml)这样的数值,根据该数值,从20kg生牡蛎获得液量21.2kg,从而将前述萃取液的比重设为1时,则在3个大气压、1小时的加热处理中,由1kg生牡蛎生成了3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)1820μg。
进一步,在对于前述萃取液在3个大气压下加热处理了2小时的情况下,获得3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的浓度为3.5(μg/ml)这样的数值,根据该数值,从生牡蛎20kg获得液量19.1kg,将前述萃取液的比重设为1时,则在3个大气压、2小时的加热处理中,由生牡蛎1kg生成了3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)3342.5μg。
予以说明,在1个大气压以上的加压状态下进行了预定时间例如50分钟以上的加热处理的情况下,与加热温度通过加压而升高的情况相互结合,从而在3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)的浓度数值方面,可发现定量极限以上的数值。
这样地判明了,通过对进行了前述加热萃取的牡蛎肉浸膏的萃取液进行加热及/或加压处理,从而明确地生成本来在生牡蛎肉中没有发现的3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。而且判明了,越将加热时间设为长时间,则越增加地生成3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
进一步可确认,在进行了3个大气压的加压处理的情况下,即使是短时间的处理时间也生成3,5-二羟基-4-甲氧基苄醇(3,5-dihydroxy-4-methoxybenzyl alcohol)。
- 还没有人留言评论。精彩留言会获得点赞!