一种基因-光热联合的纳米粒及其制备方法和应用与流程
本发明属生物技术领域,涉及载基因纳米粒,具体涉及一种基因-光热联合的纳米粒及其制备方法和在用于制备抗肿瘤制剂中的应用。
背景技术:
据资料显示,在肿瘤治疗的干预手段中,有关设计和制备多功能的治疗平台,有效整合两种治疗模式如手术、化疗、放疗、基因治疗、光热治疗或光动力学疗法等,可降低药物剂量,减少副作用,克服多药耐药,提高抗肿瘤效果,已引起国内外学者广泛关注;这种智能化的纳米平台通常需要充分结合有机和无机杂化纳米材料的优势,方可更好发挥联合治疗效果。
其中,首先,基因治疗是一种有潜力的肿瘤治疗手段;由于外源基因在体液中易降解且细胞转染效率低,因此基因治疗需要通过载体来实现有效的基因转染;在目前的众多基因载体中,病毒载体转染效率高,但存在免疫原性等潜在安全隐患;非病毒载体虽然安全性较高,但是转染效率有限;近年来致力研究的聚乙烯亚氨(简称pei)非病毒基因载体,因其易于内涵体逃逸、转染效率高,成为基因治疗载体的金标准;然而,过量使用pei,特别是高分子量的pei,会产生严重的细胞毒性和溶血性;为克服此缺陷,有研究将pei嫁接到无机纳米粒,如具有大比表面积介孔纳米球表面,以其作为支撑,一方面在保证有效的基因转染的基础上,可以显著的降低pei使用量;另一方面,介孔纳米球特殊的三维球形结构使其表面能低,空间位阻小,利于进一步表面修饰,并且其内部的孔结构,可用于装载小分子药物,实现多模式联合治疗;因此,pei嫁接的介孔纳米材料在肿瘤基因治疗方面具有显著的优势;
其次,光热治疗因其侵入性低、治疗的时空可控性等优势,成为肿瘤治疗的一种有效策略。sp2杂化的碳纳米材料,如:零维富勒烯、一维碳纳米管、二维石墨烯,已被广泛应用于肿瘤光热治疗;有研究公开了三维介孔碳纳米球(简称mcn)逐渐被应用于生物医学领域,与石墨烯和碳纳米管不同,mcn边缘平滑,对细胞损伤非常小,且具有孔状结构,利于包载药物;更重要的是,其分散的具有sp2杂化的碳孔壁作为产热点,具有较高的光热转换能力,可用于近红外介导的光热治疗。
基于此,本发明拟提供一种载基因纳米粒,尤其是一种基因-光热联合治疗纳米粒及其制备方法和在用于制备抗肿瘤药物制剂中的应用。
技术实现要素:
本发明的目的是提供一种载基因纳米粒,尤其是一种基因-光热联合的纳米粒及其制备方法和在用于制备抗肿瘤药物制剂中的应用。
本发明使用氧化介孔碳纳米球(omcn)作为支撑材料,表面共价连接pei,制备一种基因-光热联合治疗的纳米粒,利用pei的正电荷负载基因药物实现基因治疗,利用omcn的产热性能实现光热治疗;同时,本发明使用乳腺癌荷瘤裸鼠为疾病动物模型,考察了纳米粒的抗肿瘤效果,结果显示,能有效地提高肿瘤治疗效果。
本发明提供了一种新的高效低毒的光热-基因联合治疗肿瘤的治疗平台。
本发明的光热-基因联合治疗纳米粒在用于制备抗肿瘤中,能有效发挥各自的优势,用于基因和光热联合治疗乳腺癌,与单一治疗相比,具有更优疗效;本发明所制备的pei嫁接omcn的载体,与单纯omcn相比,表面修饰pei后808nm的吸收增加,产热能力提高,与单纯pei相比,通过omcn做支撑,细胞毒性降低,基因转染能力增强。
本发明提供了一种基于omcn和pei的载基因纳米粒的制备方法,
本发明制备pei嫁接的omcn(op)的步骤如下:精确称量定量的omcn,分散于适量体积的edc溶液(溶于一定ph值的mes缓冲液)和定量体积的nhs溶液(溶于一定ph值的mes缓冲液)中,搅拌一定时间,激活羧基,加入过量pei搅拌一定时间,离心水洗纯化,即得op;
上述合成方法中,mes缓冲液的ph值范围为5~6.5;
上述合成方法中,edc溶液的浓度为10mg·ml-1,nhs溶液的浓度为4mg·ml-1;
上述合成方法中,omcn:edc:nhs的质量比为1:(2~5):(0.8~2);
上述合成方法中,omcn与edc/nhs反应时间为2~3h;
上述合成方法中,omcn与pei的质量比为1:(2~6);
上述合成方法中,omcn与pei的反应时间为24h~48h;
上述合成方法中,离心速率为8000rpm~12000rpm,离心时间为8min~12min;
本发明制备基于op的载基因纳米粒的步骤如下:精确称量定量op与定量质粒dna混合,漩涡一定时间,室温孵育一定时间,即得op的载基因纳米粒;
上述制备方法中,op与质粒dna的质量比为1:(0.1~1);
上述制备方法中,漩涡时间为30s,室温孵育时间为20min~4h;
上述所制备的基于op的载基因纳米粒,使用编码ing4的质粒dna所制备的纳米粒,简称opi,使用编码绿色荧光蛋白的质粒dna所制备的纳米粒,简称ope,使用编码荧光素酶的质粒dna所制备的纳米粒,简称opg。
本发明通过透射电镜观察op和opi的形貌,通过x射线光电子能谱测定opi的元素组成,结果显示,所制备的纳米粒为球形,含有o、n、c和p元素;
本发明通过zeta电位测定仪测定不同载体材料和纳米粒的表面电荷,结果显示omcn荷负电,表面修饰阳离子pei后荷正电,负载阴性质粒dna后电荷降低,符合规律;
本发明通过紫外-可见分光光度计获取载体的紫外-可见吸收光谱曲线,结果显示,在808nm处omcn和op均有吸收,omcn经pei修饰后吸收增强;
本发明使用808纳米的近红外激光照射,测定op的热效应,。固定照射能量强度为4.5w/cm2,测定不同浓度op的热效应曲线;固定op浓度为45μg/ml,测定不同能量强度照射下op的热效应曲线,结果显示,op的热效应呈浓度依赖性和能量强度依赖性;
本发明使用琼脂糖凝胶电泳考察op包载质粒dna的能力,以及近红外光触发下质粒dna从载体材料中释放的效应,结果显示,op具有良好的包封质粒dna的能力,在近红外光触发下,op和质粒dna的结合会逐渐松散,利于基因药物的释放;
本发明通过倒置荧光显微镜观察ope和单纯pei在mcf-7乳腺癌细胞上的基因转染效率差异,结果显示,ope具有高gfp表达效率,同样条件下,pei介导的基因表达效率明显降低,细胞毒性大;
本发明使用cck-8检测法定量评价不同处理对mcf-7乳腺癌细胞的毒性,制备opg和opi成系列浓度,与mcf-7细胞避光孵育6h,对光热治疗组,使用近红外激光照射5分钟,能量密度为4.5w/cm2,继续孵育42h,按照cck-8使用说明定量检测细胞毒性,结果显示,细胞毒性随着纳米粒浓度增加而增加,同一浓度下,包载治疗基因的opi对mcf-7细胞毒性比包载报告基因的opg大,对于同一种纳米粒,近红外光照射后细胞毒性增加;
本发明使用共聚焦显微镜观察mcf-7细胞经不同处理后的死亡-存活情况,opg和opi分别与mcf-7细胞避光孵育6h,浓度为45μg/ml,对光热治疗组,使用近红外激光照射5分钟,能量密度为4.5w/cm2,继续孵育42h,按照live-dead试剂染色说明进行细胞染色,激光共聚焦显微镜下观察,活细胞呈绿色,死细胞呈红色,结果显示,基因和光热治疗联合治疗组(opi+nir组)的肿瘤细胞死亡明显高于单纯的光热治疗组(opg+nir组)或单纯的基因治疗组(opi组),提示联合治疗的良好效果,结果还显示,包载报告基因的opg组没有观察到明显细胞毒性。
本发明使用红外热成像仪检测体内热效应效果,构建mcf-7荷瘤裸鼠模型,尾静脉注射生理盐水和opi后经808nm激光照射5min,能量密度为1w/cm2,热成像仪记录不同时间点的热效应图像和温度,结果显示,opi组随着近红外照射时间延长,温度提高,明显高于生理盐水组,提示opi良好的热效应;
本发明使用tunel法测定mcf-7荷瘤裸鼠尾静脉注射不同制剂后的细胞凋亡情况,构建mcf-7荷瘤裸鼠模型,尾静脉注射生理盐水、游离阿霉素、opg和opi,光热治疗组另经808nm激光照射5min,能量密度为1w/cm2,每隔两天处理一次,共处理2次,处死裸鼠,取皮下肿瘤,冰冻切片,按照tunel试剂盒说明测定凋亡情况,并用dapi进行细胞核染色,蓝色表示dapi染色的细胞核,绿色表示fitc标记的凋亡细胞,结果显示,基因和光热治疗联合治疗组(opi+nir组)的肿瘤死亡明显高于单纯的光热治疗组(opg+nir组)或单纯的基因治疗组(opi组),提示联合治疗的良好效果。
本发明的突出优点及特征在于,提供一种基于omcn和pei的载基因纳米粒的制备方法,所述的载基因纳米粒中,能有效发挥各自的优势,用于基因和光热联合治疗乳腺癌,与单一治疗相比,具有更优疗效,本发明所制备的pei嫁接omcn的载体,与单纯omcn相比,表面修饰pei后808nm的吸收增加,产热能力提高,与单纯pei相比,通过omcn做支撑,细胞毒性降低,基因转染能力增强。
本发明为肿瘤治疗提供了新的高效低毒的光热-基因联合的干预技术,有助于提高肿瘤治疗效果。
附图说明
图1载体材料和纳米粒的物理表征结果,
其中,a:op的透射电镜图(插入图:opi的透射电镜图),
b:opi的x射线光电子能谱图。
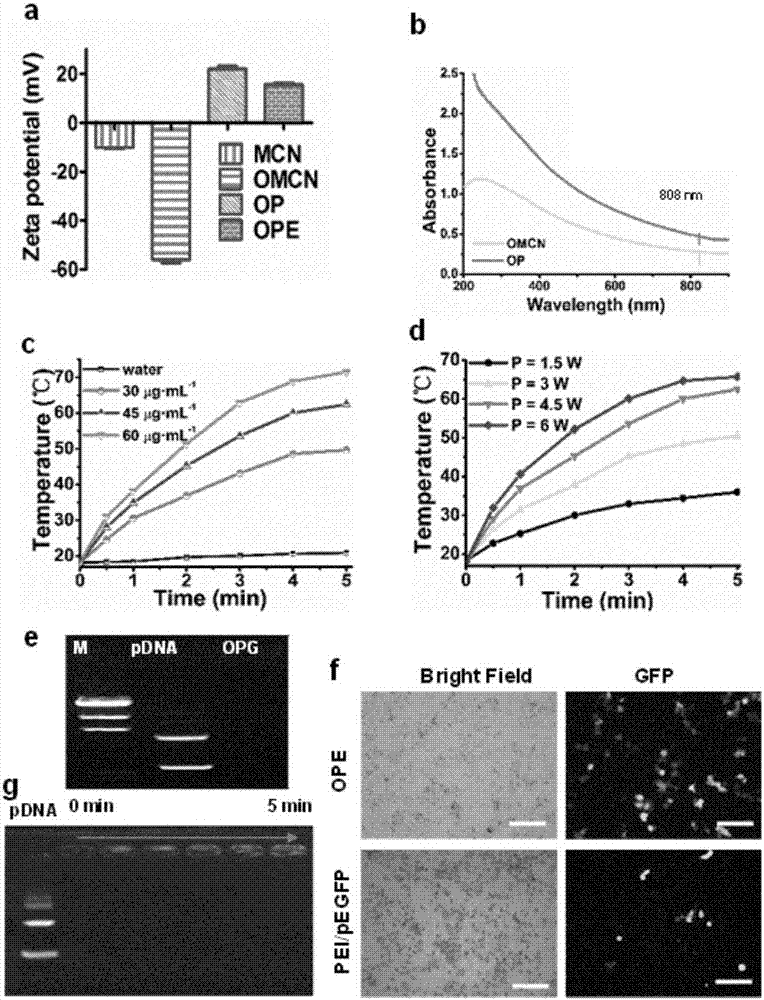
图2载体材料和纳米粒的性质表征结果,
其中,a:不同载体材料和纳米粒的zeta电位结果,
b:omcn和op的紫外-可见吸收光谱曲线,
c:固定808nm激光照射能量强度为4.5w/cm2,不同浓度op的热效应曲线,
d:固定浓度为45μg/ml,不同能量强度近红外激光照射下op的热效应曲线,
e:琼脂糖凝胶电泳结果,
f:不同纳米粒在mcf-7乳腺癌细胞上的基因转染效果,
g:近红外光触发的dna释放结果。
图3cck-8检测法定量评价不同处理对mcf-7乳腺癌细胞的毒性结果。
图4共聚焦显微镜观察mcf-7细胞经不同处理后的死亡-存活情况,
其中,绿色表示活细胞,红色表示死细胞,bar=200μm。
图5mcf-7荷瘤裸鼠尾静脉注射生理盐水和opi后经808nm激光照射的体内热效应结果,
其中:能量强度为1w/cm2,持续时间为5min,
a:热成像图谱,
b:相应的热效应定量测定结果。
图6tunel法测定mcf-7荷瘤裸鼠尾静脉注射不同制剂后的细胞凋亡结果,
其中:蓝色表示dapi染色的细胞核,绿色表示fitc标记的凋亡细胞。
具体实施方式
实施例1.
精确称量1mgomcn分散于0.2mledc溶液(10mg·ml-1,ph5.0的mes缓冲液)和0.2mlnhs溶液(4mg·ml-1,ph5.0的mes缓冲液)中搅拌2h,激活羧基,加入过量pei(与omcn的质量比为2:1)搅拌24h,8000rpm离心12min,水洗纯化,即得op。
实施例2.
精确称量1mgomcn分散于0.2mledc溶液(10mg·ml-1,ph6.0的mes缓冲液)和0.2mlnhs溶液(4mg·ml-1,ph6.0的mes缓冲液)中搅拌2h,激活羧基,加入过量pei(与omcn的质量比为2:1)搅拌24h,8000rpm离心12min,水洗纯化,即得op。
实施例3.
精确称量1mgomcn分散于0.5mledc溶液(10mg·ml-1,ph6.0的mes缓冲液)和0.5mlnhs溶液(4mg·ml-1,ph6.0的mes缓冲液)中搅拌2h,激活羧基,加入过量pei(与omcn的质量比为2:1)搅拌24h,8000rpm离心12min,水洗纯化,即得op。
实施例4.
精确称量1mgomcn分散于0.2mledc溶液(10mg·ml-1,ph6.0的mes缓冲液)和0.2mlnhs溶液(4mg·ml-1,ph6.0的mes缓冲液)中搅拌3h,激活羧基,加入过量pei(与omcn的质量比为2:1)搅拌24h,8000rpm离心12min,水洗纯化,即得op。
实施例5.
精确称量1mgomcn分散于0.2mledc溶液(10mg·ml-1,ph6.0的mes缓冲液)和0.2mlnhs溶液(4mg·ml-1,ph6.0的mes缓冲液)中搅拌2h,激活羧基,加入过量pei(与omcn的质量比为4:1)搅拌24h,8000rpm离心12min,水洗纯化,即得op。
实施例6.
精确称量1mgomcn分散于0.2mledc溶液(10mg·ml-1,ph6.0的mes缓冲液)和0.2mlnhs溶液(4mg·ml-1,ph6.0的mes缓冲液)中搅拌2h,激活羧基,加入过量pei(与omcn的质量比为6:1)搅拌24h,8000rpm离心12min,水洗纯化,即得op。
实施例7.
精确称量1mgomcn分散于0.2mledc溶液(10mg·ml-1,ph6.0的mes缓冲液)和0.2mlnhs溶液(4mg·ml-1,ph6.0的mes缓冲液)中搅拌2h,激活羧基,加入过量pei(与omcn的质量比为2:1)搅拌36h,8000rpm离心12min,水洗纯化,即得op。
实施例8.
精确称量1mgomcn分散于0.2mledc溶液(10mg·ml-1,ph6.0的mes缓冲液)和0.2mlnhs溶液(4mg·ml-1,ph6.0的mes缓冲液)中搅拌2h,激活羧基,加入过量pei(与omcn的质量比为2:1)搅拌48h,8000rpm离心12min,水洗纯化,即得op。
实施例9.
精确称量1mgomcn分散于0.2mledc溶液(10mg·ml-1,ph6.0的mes缓冲液)和0.2mlnhs溶液(4mg·ml-1,ph6.0的mes缓冲液)中搅拌2h,激活羧基,加入过量pei(与omcn的质量比为2:1)搅拌24h,10000rpm离心10min,水洗纯化,即得op。
实施例10.
精确称量1mgomcn分散于0.2mledc溶液(10mg·ml-1,ph6.0的mes缓冲液)和0.2mlnhs溶液(4mg·ml-1,ph6.0的mes缓冲液)中搅拌2h,激活羧基,加入过量pei(与omcn的质量比为2:1)搅拌24h,12000rpm离心8min,水洗纯化,即得op。
实施例11.
精确称量1mg实施例2合成的op与0.5mg编码生长抑制因子4(ing4)的质粒dna混合,漩涡30s,室温孵育30min,即得op的载基因纳米粒opi。
实施例12.
精确称量1mg实施例2合成的op与0.1mg编码ing4的质粒dna混合,漩涡30s,室温孵育30min,即得op的载基因纳米粒opi。
实施例13.
精确称量1mg实施例2合成的op与1mg编码ing4的质粒dna混合,漩涡30s,室温孵育30min,即得op的载基因纳米粒opi。
实施例14.
精确称量1mg实施例2合成的op与0.5mg编码ing4的质粒dna混合,漩涡30s,室温孵育20min,即得op的载基因纳米粒opi。
实施例15.
精确称量1mg实施例2合成的op与0.5mg编码ing4的质粒dna混合,漩涡30s,室温孵育2h,即得op的载基因纳米粒opi。
实施例16.
精确称量1mg实施例2合成的op与0.5mg编码ing4的质粒dna混合,漩涡30s,室温孵育4h,即得op的载基因纳米粒opi。
实施例17.
精确称量1mg实施例2合成的op与0.5mg编码绿色荧光蛋白的质粒dna混合,漩涡30s,室温孵育30min,即得op的载基因纳米粒ope。
实施例18.
精确称量1mg实施例2合成的op与0.5mg编码荧光素酶的质粒dna混合,漩涡30s,室温孵育30min,即得op的载基因纳米粒opg。
实施例19.
通过jem2100f透射电镜观察实施例2合成的op和实施例11制备的opi的形貌,结果显示所合成的纳米载体及载基因后的纳米粒均呈球形,表面较为圆整,有一层明显聚合物包裹(如图1a所示)。
实施例20.
通过phi-5000cescasystemx射线光电子能谱观察实施例11制备的opi的元素组成,结果显示所制备的纳米粒中含有o、n、c和p元素(如图1b所示)。
实施例21.
通过zeta电位测定仪测定不同载体材料和纳米粒的表面电荷,结果显示omcn荷负电,表面修饰阳离子pei后荷正电,负载阴性质粒dna后电荷降低,符合规律(如图2a所示)。
实施例22.
通过紫外-可见分光光度计获取载体的实施例2所合成的op以及omcn的紫外-可见吸收光谱曲线,结果显示,在808nm处omcn和op均有吸收,omcn经pei修饰后808nm处的吸收增强(如图2b所示)。
实施例23.
使用808纳米的近红外激光照射,测定实施例2所合成op的热效应。固定照射能量强度为4.5w/cm2,测定不同浓度op的热效应曲线。结果显示,随着op的浓度增加,热效应增加,op的热效应呈浓度依赖性(如图2c所示)。
实施例24.
使用808纳米的近红外激光照射,测定实施例2所合成op的热效应。固定op浓度为45μg/ml,测定不同能量强度照射下op的热效应曲线。结果显示,随着能量照射强度增加,热效应增加,op的热效应呈能量强度依赖性(如图2d所示)。
实施例25.
使用琼脂糖凝胶电泳考察实施例2所合成op包载质粒dna的能力。结果显示,所合成op具有良好的包封质粒dna的能力(如图2e所示)。
实施例26.
通过倒置荧光显微镜观察实施例17所制备ope和单纯pei在mcf-7乳腺癌细胞上的基因转染效率差异。结果显示,ope具有高gfp表达效率,同样条件下,pei介导的基因表达效率明显降低,细胞毒性大(如图2f所示)。
实施例27.
使用琼脂糖凝胶电泳考察实施例18所制备opg在近红外光触发下质粒dna从载体材料中释放的效应。结果显示,在近红外光触发下,op和质粒dna的结合会逐渐松散,基因药物逐渐释放(如图2g所示)。
实施例28.
使用cck-8检测法定量评价不同处理对mcf-7乳腺癌细胞的毒性。将实施例18所制备的opg和实施例11所制备的opi配制成系列浓度,与mcf-7细胞避光孵育6h,对光热治疗组用近红外激光照射5分钟,能量密度为4.5w/cm2,继续孵育42h,按照cck-8使用说明定量检测细胞毒性。结果显示,细胞毒性随着纳米粒浓度增加而增加,同一浓度下,包载治疗基因的opi对mcf-7细胞毒性比包载报告基因的opg大,对于同一种纳米粒,近红外光照射后细胞毒性增加(如图3所示)。
实施例29.
使用共聚焦显微镜观察mcf-7细胞经不同处理后的死亡-存活情况。将实施例18所制备的opg和实施例11所制备的opi分别与mcf-7细胞避光孵育6h,浓度为45μg/ml,对光热治疗组用近红外激光照射5分钟,能量密度为4.5w/cm2,继续孵育42h,按照live-dead试剂染色说明进行细胞染色,激光共聚焦显微镜下观察,活细胞呈绿色,死细胞呈红色。结果显示,基因和光热治疗联合治疗组(opi+nir组)的肿瘤细胞死亡明显高于单纯的光热治疗组(opg+nir组)或单纯的基因治疗组(opi组),提示协同的联合治疗效果。结果还显示,包载报告基因的opg没有明显的细胞毒性(如图4所示)。
实施例30.
使用热成像仪检测荷瘤裸鼠体内热效应效果。构建mcf-7荷瘤裸鼠模型,尾静脉注射生理盐水和实施例11所制备的opi后经808nm激光照射5min,能量密度为1w/cm2,热成像仪记录不同时间点的热效应图像和温度。结果显示,opi组随着近红外照射时间延长,产热温度提高,明显高于生理盐水组,提示opi在体内具有良好的热效应(如图5所示)。
实施例31.
使用tunel法测定mcf-7荷瘤裸鼠尾静脉注射不同制剂后的细胞凋亡情况。构建mcf-7荷瘤裸鼠模型,尾静脉注射生理盐水、游离阿霉素、实施例18所制备的opg和实施例11所制备的opi,光热治疗组另经808nm激光照射5min,能量密度为1w/cm2,每隔两天处理一次,共处理2次。处死裸鼠,取皮下肿瘤,冰冻切片,按照tunel试剂盒说明测定凋亡情况,蓝色表示dapi染色的细胞核,绿色表示fitc标记的凋亡细胞。结果显示,基因和光热联合治疗组(opi+nir组)的肿瘤死亡效果明显高于单纯的光热治疗组(opg+nir组)或单纯的基因治疗组(opi组),提示联合治疗的协同效果(如图6所示)。
- 还没有人留言评论。精彩留言会获得点赞!