没药甾酮Z在制备抗抑郁症药物中的应用的制作方法
本发明涉及一种没药甾酮Z的用途。
背景技术:
作为抗菌、治外伤、抗黏膜炎症的植物药物,没药在古埃及、印度等地已有相当长的使用历史,具有抗微生物、抗炎、抗氧化、提高免疫力、调节代谢稳态等功效,广泛用于胸腹瘀痛、跌打损伤、痈肿疮疡、关节炎、肥胖、脂质代谢紊乱等疾病的治疗。在中枢神经系统,没药具有温和的镇定作用,是古埃及和印度等地区传统用于治疗过度思虑、忧虑和心神不宁的主要药物之一。在种属上,没药为橄榄科植物地丁树Commiphora myrrha Engl或哈地丁树Commiphora molmol Engl的干燥树脂,分为天然没药和胶质没药,主要含25%-45%没药树脂、3%-8%挥发油、55%-60%树胶和少量苦味质、没药酸、甲酸、乙酸等。没药甾酮系没药树脂的主要成分之一,分为Z和E两种同分异构体。
现代药理学研究表明,没药甾酮Z为没药的主要有效活性效成分,具有降血脂、抗氧化、抗炎、改善认知等多种药理学活性。虽然有关没药活性成份没药甾酮Z的基础应用研究已成为天然药物研究与开发的热点,但其在抗抑郁症方面的应用目前还没有任何文献报道。
抑郁症是现代社会一种常见的心境障碍疾病,以显著而持久的心境低落为主要临床特征,严重者可出现自杀念头。抑郁症的发病与不良社会应激与遗传等多种因素有关。脑内与抑郁症发病密切相关的结构主要有海马等边缘系统脑区和伏隔核等奖赏系统脑区。氟西汀、丙咪嗪等是目前临床常用抗抑郁药,这些药物的抗抑郁机制在过去几十年里一直被认为与中枢单胺类递质系统有关,但存在用药周期长、疗效不显著等缺点。
技术实现要素:
本发明的目的在于提供一种药物的新用途,是没药甾酮Z在制备抗抑郁症药物中的应用。
本发明的技术解决方案是:
一种没药甾酮Z在制备抗抑郁症药物中的应用。
所述的药物含没药甾酮Z及其药学上可接受的盐、酯或肟及一种或一种以上药学上可以接受的载体。
化学结构:没药甾酮Z(Z-guggulsterone),MW=312.45。
本发明所述没药甾酮Z及其药学上可接受的盐、酯或肟可以以单一药物形式给药,也可与其它药物联合给药。
本发明所述化合物中药学上可接受的盐包括各种无机或有机酸盐如磷酸盐、延胡索酸盐、盐酸盐、酒石酸盐、硫酸盐、柠檬酸盐、氢溴酸盐、乳酸盐、马来酸盐扁桃酸盐和草酸盐等及各种无机或有机碱盐如三羟甲基氨基甲烷、氢氧化钠和N-甲基-葡萄糖胺等。
本发明所述化合物中药学上可接受的酯包括但不限于C1-C6烷基酯、C3-C6直链苄基酯或烷基酯。
本发明所述没药甾酮Z的羰基与不同胺类化合物形成的潜在肟类化合物。
本发明所述没药甾酮Z及其药学上可接受的盐、酯或肟可以单独使用或以药物组合物形式使用。药物组合物包括作为活性成分的没药甾酮Z及其药学上可接受的盐、酯或肟及可以作为药用的载体。可药用载体不会破坏本发明化合物或其可药用盐的药学活性,其有效量,即起药物载体作用量对人体无毒。
可用药物载体或辅料为药学工作者一般所熟知的用于固体制剂、半固体制剂、液体制剂和吸入制剂的常规制剂,其中药物载体包括但不限于以下物质:氧化铝、卵磷脂、离子交换材料、硬脂酸铝、自乳化药物传递系统(SEDDS)如d-维生素E聚乙二醇1000琥珀酸酯、吐温或其它类似聚合介质等药物制剂用的表面活性剂、人血清白蛋白、缓冲物质如磷酸盐、氨基乙酸、山梨酸、山梨酸钾、饱和植物脂肪酸部分甘油酯混合、水、盐、磷酸氢二钠、硫酸盐精蛋白、氯化钠、磷酸氢钾、硅胶和锌盐等。聚乙烯吡咯酮、羧甲基纤维素钠、聚乙烯醇、纤维素物质、聚丙烯酸酯、乙烯-聚氧乙烯-嵌段聚合物、环糊精、羊毛脂等均可用于促进本发明化合物及其药用盐、酯或肟的药物传递。
其它可药用辅料如崩解剂(如交联羧甲基淀粉钠、交联羧甲基纤维素钠、低取代羟丙基纤维素和交联PVP)、填充剂(如淀粉、无水乳糖、乳糖珠粒和葡萄糖)、粘合剂(如微晶纤维素)、润滑剂(如硬脂酸镁)、吸收促进剂、甜味剂、香味剂、稀释剂、润湿剂、赋形剂、溶剂、增溶剂和着色剂等也可加入本发明的药物组合物中。
本发明所述的没药甾酮Z及其药学上可接受的盐、酯或肟以及药物组合物可通过肠道或者非肠道途径给药。非肠道给药制剂包括注射剂、软膏剂、霜剂、贴剂、喷雾剂等;给药途径包括皮下、皮内、动脉内、肌内、静脉内、关节内、滑液内、鞘内、胸骨内、病灶内、颅内注射或输注,或局部、经鼻、口服、直肠、经颊、舌下、阴道、粘膜、皮内、气管、尿道给药。
本发明所述的没药甾酮Z及其药学上可接受的盐、酯或肟及药物组合物的治疗有效量为0.001-100mg/kg/d之间,可用于相关疾病的单一用药或联合用药治疗,为本领域技术人员能够理解的范围。
本发明提供了没药甾酮Z在制备抗抑郁症药物中的应用,效果好。
附图说明
下面结合附图和实施例对本发明作进一步说明。
图1、图2、图3为不同浓度没药甾酮Z对CUS所致小鼠悬尾不动时间的影响。
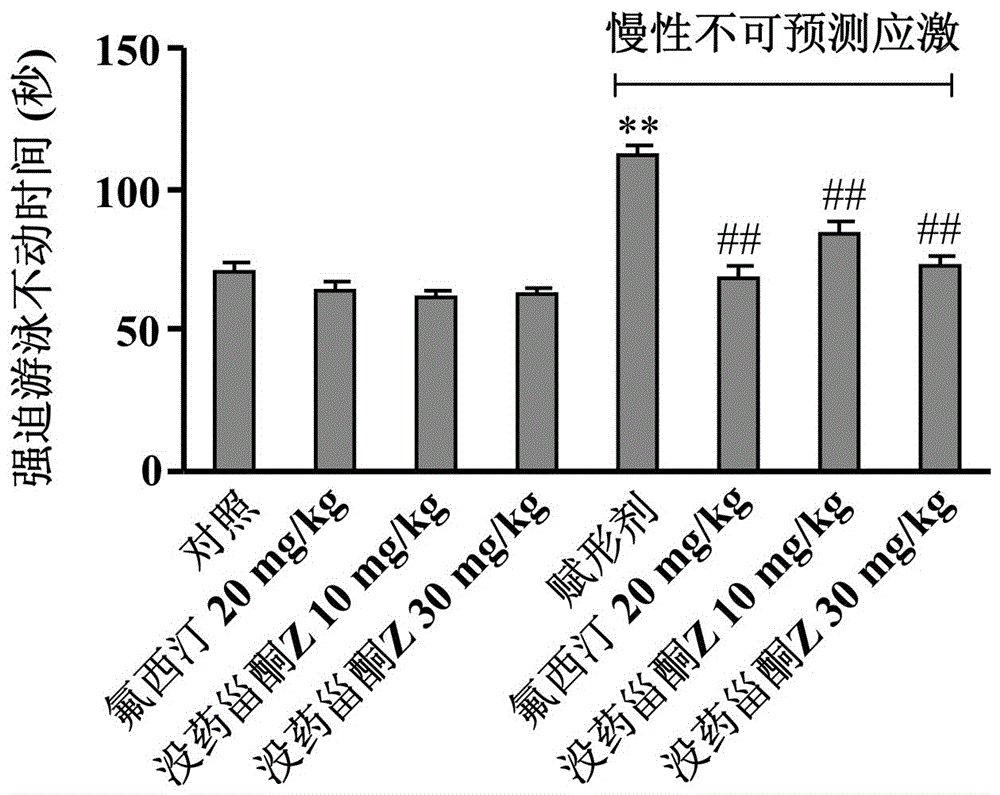
图4为不同浓度没药甾酮Z对CUS所致小鼠强迫游泳不动时间的影响。
图5、图6、为不同浓度没药甾酮Z对CUS所致小鼠糖水消耗量的影响。
图7、图8、图9、图10为不同浓度没药甾酮Z对CUS所致小鼠海马DCX+细胞数的影响。
图11、图12、图13为没药甾酮Z处理前后各组小鼠海马DCX+细胞数的统计结果。
图14、图15为不同浓度没药甾酮Z对CUS所致小鼠海马DCX蛋白表达的影响。
图16、图17、图18、图19为没药甾酮Z处理前后各组海马DCX蛋白表达变化的统计结果。
具体实施方式
一种没药甾酮Z在制备抗抑郁症药物中的应用。
所述的药物含没药甾酮Z及其药学上可接受的盐、酯或肟及一种或一种以上药学上可以接受的载体。
化学结构:没药甾酮Z(Z-guggulsterone),MW=312.45。
所述化合物中药学上可接受的盐包括各种无机或有机酸盐如磷酸盐、延胡索酸盐、盐酸盐、酒石酸盐、硫酸盐、柠檬酸盐、氢溴酸盐、乳酸盐、马来酸盐扁桃酸盐和草酸盐等及各种无机或有机碱盐如三羟甲基氨基甲烷、氢氧化钠和N-甲基-葡萄糖胺等。
所述化合物中药学上可接受的酯包括但不限于C1-C6烷基酯、C3-C6直链苄基酯或烷基酯。
所述没药甾酮Z的羰基与不同胺类化合物形成的潜在肟类化合物。
所述没药甾酮Z及其药学上可接受的盐、酯或肟可以单独使用或以药物组合物形式使用。药物组合物包括作为活性成分的没药甾酮Z及其药学上可接受的盐、酯或肟及可以作为药用的载体。可药用载体不会破坏本发明化合物或其可药用盐的药学活性,其有效量,即起药物载体作用量对人体无毒。
可用药物载体或辅料为药学工作者一般所熟知的用于固体制剂、半固体制剂、液体制剂和吸入制剂的常规制剂,其中药物载体包括但不限于以下物质:氧化铝、卵磷脂、离子交换材料、硬脂酸铝、自乳化药物传递系统(SEDDS)如d-维生素E聚乙二醇1000琥珀酸酯、吐温或其它类似聚合介质等药物制剂用的表面活性剂、人血清白蛋白、缓冲物质如磷酸盐、氨基乙酸、山梨酸、山梨酸钾、饱和植物脂肪酸部分甘油酯混合、水、盐、磷酸氢二钠、硫酸盐精蛋白、氯化钠、磷酸氢钾、硅胶和锌盐等。聚乙烯吡咯酮、羧甲基纤维素钠、聚乙烯醇、纤维素物质、聚丙烯酸酯、乙烯-聚氧乙烯-嵌段聚合物、环糊精、羊毛脂等均可用于促进本发明化合物及其药用盐、酯或肟的药物传递。
其它可药用辅料如崩解剂(如交联羧甲基淀粉钠、交联羧甲基纤维素钠、低取代羟丙基纤维素和交联PVP)、填充剂(如淀粉、无水乳糖、乳糖珠粒和葡萄糖)、粘合剂(如微晶纤维素)、润滑剂(如硬脂酸镁)、吸收促进剂、甜味剂、香味剂、稀释剂、润湿剂、赋形剂、溶剂、增溶剂和着色剂等也可加入本发明的药物组合物中。
所述的没药甾酮Z及其药学上可接受的盐、酯或肟以及药物组合物可通过肠道或者非肠道途径给药。非肠道给药制剂包括注射剂、软膏剂、霜剂、贴剂、喷雾剂等;给药途径包括皮下、皮内、动脉内、肌内、静脉内、关节内、滑液内、鞘内、胸骨内、病灶内、颅内注射或输注,或局部、经鼻、口服、直肠、经颊、舌下、阴道、粘膜、皮内、气管、尿道给药。
所述的没药甾酮Z及其药学上可接受的盐、酯或肟及药物组合物的治疗有效量为0.001-100mg/kg/d之间,可用于相关疾病的单一用药或联合用药治疗,为本领域技术人员能够理解的范围。
实验:
首先应用“慢性不可预测应激”构建C57BL/6J小鼠抑郁症模型。所采用的慢性不可预测应激刺激包括:笼子摇晃、整晚开灯、4℃环境、幽闭、白天关灯、湿笼、45°笼子倾斜、缺水、饥饿。具体刺激条件如下:1.笼子摇晃:将小鼠置于脱色摇床上的塑料盒内,转速调至200,时间调至60分钟;2.整晚开灯:早上7点开灯,一直持续到第二天早上7点;3. 4℃环境:将小鼠置于实验盒内,放在4℃环境中,持续1小时;4.幽闭:将小鼠置于实验盒内,仅留供其呼吸的空隙,然后将实验盒置于暗环境中2小时;5.白天关灯:将小鼠置于全封闭的暗房内3小时;6.湿笼:在鼠笼内倒入饮用水,水位应完全覆盖垫料,让小鼠在此环境中待12小时;7. 45°笼子倾斜:将鼠笼一端抬高,在笼底放置一个铁盒子使鼠笼倾斜45°;8.缺水:去除水瓶12小时;9.饥饿:去除食物12小时。造模25天后,开始没药甾酮Z腹腔注射,连续给药12天。
造模和给药结束后,采用悬尾、强迫游泳和糖水消耗实验评价化合物的抗抑郁作用,具体方案如下:
1.强迫游泳实验:第35天给药结束后,将小鼠放置在高25厘米、直径10厘米的透明玻璃容器内(装有约10厘米高的饮用水、水温25±1℃)6分钟,记录最后4分钟内小鼠不动时间(此处不动时间是指小鼠不挣扎、简单悬浮在水面或做一些简单的动作以维持其头部悬浮在水面的时间)。
2.悬尾实验:第36天将小鼠距尾巴根部1厘米处用胶带悬挂在大约50厘米高的支架上6分钟,记录最后4分钟内小鼠悬尾不动时间(此处不动时间是指小鼠没有明显头部或肢体动作的时间)。
3.旷场实验:第36天将小鼠放在高40厘米、宽100厘米、长100厘米、并含有25个小方格的旷场箱内5分钟,记录各组小鼠在周围和中心区域的活动度。
4.糖水消耗实验:第38天在每一个鼠笼上放置一瓶普通饮用水和一瓶1%蔗糖水溶液,适应两天,且每6小时调换一下水瓶位置。然后对小鼠进行饥饿、缺水处理24小时。第42天,将两瓶事先称好重量的水瓶放置在鼠笼上,30分钟后调换水瓶位置,测量1小时内小鼠饮水情况。糖水偏好值为糖水消耗量与总液体消耗量比值的百分比。
5.行为学试验后取各组海马组织,行免疫荧光和蛋白免疫印迹实验。
悬尾和强迫游泳结果显示,注射赋形剂“二甲基亚砜(DMSO)”的慢性不可预测应激小鼠悬尾(图1)和游泳(图2)不动时间均明显高于对照组小鼠(**与对照组比P<0.01),而慢性不可预测应激+没药甾酮Z(10或30mg/kg)组小鼠悬尾不动时间明显低于赋形剂组(#与赋形剂组比P<0.05或##与赋形剂组比P<0.01)。糖水消耗结果显示,注射赋形剂的慢性不可预测应激组小鼠糖水消耗量明显低于对照组小鼠(**与对照组比P<0.01),而慢性不可预测应激+没药甾酮Z(10或30mg/kg)组小鼠糖水消耗量明显高于赋形剂组(图3,#与赋形剂组比P<0.05或##与赋形剂组比P<0.01)。
由于小鼠自发性活动度的下降也会导致悬尾和强迫游泳实验中不动时间延长的现象,因此,为了排序这一因素的影响,我们用旷场实验检测了各组小鼠活动度的变化,结果显示慢性不可预测应激、氟西汀(20mg/kg)、没药甾酮Z(10或30mg/kg)均不影响小鼠活动度(图4,包括周围区域、中心区域和总活动度)。
鉴于BDNF信号功能失调是抑郁症发生的关键,我们采用了蛋白免疫印迹技术,评价了没药甾酮Z对小鼠海马BDNF信号的影响。结果显示,慢性不可预测应激+DMSO组小鼠海马BDNF蛋白表达量与正常对照组相比显著减少(*与对照组比P<0.05),不同浓度没药甾酮Z(10或30mg/kg)处理后小鼠海马BDNF蛋白表达量减少得到显著缓解(图5,图6,#与赋形剂组比P<0.05)。
鉴于海马神经再生与抑郁症的发生密切相关,我们继续评价了没药甾酮Z对小鼠海马神经再生的影响。免疫荧光结果显示,慢性不可预测应激+DMSO组小鼠海马DCX阳性细胞数与正常对照组相比显著减少(**与对照组比P<0.01),不同浓度没药甾酮Z(10或30mg/kg)处理后,小鼠海马DCX阳性细胞数减少得到显著缓解(图7,图8,#与赋形剂组比P<0.05或##与赋形剂组比P<0.01);蛋白免疫印迹结果显示,慢性不可预测应激组小鼠海马DCX蛋白表达量与正常对照组小鼠相比显著减少(*与对照组比P<0.05),不同浓度没药甾酮Z(10或30mg/kg)处理后小鼠海马DCX蛋白表达减少得到显著逆转(图9,图10,#与赋形剂组比P<0.05)。
图11显示BDNF抑制剂K252a(25μg/kg)取消了没药甾酮Z(30mg/kg)对慢性不可预测应激模型小鼠悬尾不动时间的改善作用(**与对照组比P<0.01,##与赋形剂组比P<0.01);图12显示BDNF抑制剂K252a(25μg/kg)取消了没药甾酮Z(30mg/kg)对慢性不可预测应激模型小鼠强迫游泳不动时间的改善作用(**与对照组比P<0.01,##与赋形剂组比P<0.01);图13显示BDNF抑制剂K252a(25μg/kg)取消了没药甾酮Z(30mg/kg)对慢性不可预测应激模型小鼠糖水消耗量减少的改善作用(**与对照组比P<0.01,##与赋形剂组比P<0.01);
图14、图15显示BDNF抑制剂K252a(25μg/kg)取消了没药甾酮Z(30mg/kg)对慢性不可预测应激模型小鼠海马BDNF蛋白减少的改善作用(*与对照组比P<0.05,#与赋形剂组比P<0.05)。
图16、图17显示BDNF抑制剂K252a(25μg/kg)取消了没药甾酮Z(30mg/kg)对慢性不可预测应激模型小鼠海马DCX阳性细胞数减少的改善作用(**与对照组比P<0.01,##与赋形剂组比P<0.01)。图18、图19显示BDNF抑制剂K252a(25μg/kg)取消了没药甾酮Z(30mg/kg)对慢性不可预测应激模型小鼠海马DCX蛋白减少的改善作用(**与对照组比P<0.01,#与赋形剂组比P<0.05)。
- 还没有人留言评论。精彩留言会获得点赞!