用于眼科药物递送的自乳化药物递送体系(SEDDS)的制作方法
发明人:yumnashabaik、jimjiao和chetanpujara
相关申请的交叉引用
本申请要求2015年3月5日提交的美国临时申请号62/128,798的权益,所述临时申请以引用的方式整体并入本文。
发明领域
本文提供能够经历自乳化的新型眼科组合物。当与水性介质(包括但不限于泪膜的水性介质)接触时,这些组合物自发地自乳化。关于液滴尺寸,所得到的乳液处于次微米至纳米范围内。
发明背景
估计通过局部眼科施用而递送的药物的生物利用度为施加剂量的约5%。这个目标部位处的生理条件对于药物递送提出多个挑战,其包括穿过角膜的渗透性差,以及由于眼泪排出而引起的停留时间短。这些和其他因素限制眼组织暴露于药物,并且导致观察到的生物利用度极低。
用于眼部治疗的制剂在例如美国专利公开号2006/0182771a1中有所描述。用于施用脂溶性活性成分的眼科组合物在wo2011/154985a1中有所描述。添加粘度增强剂或使用具有热、ph或离子敏感的胶凝特性的聚合物已经被用来增加眼部停留时间。粘度增强剂的使用受限于粘度不应干扰易从滴瓶施加的事实,并且出于生物相容性原因可排除聚合物的添加。
自乳化药物递送体系(sedds)是油、表面活性剂(含或不含助表面活性剂)和共溶剂的各向同性混合物,当在温和搅拌下暴露于水性介质时其自发地乳化。sedds最常被研究来通过口服施用而改善水溶性差的药物的生物利用度。共溶剂的添加对于自乳化体系的形成是重要的,因为共溶剂显著降低界面张力。在这样做时,共溶剂产生具有足够柔韧性的流体界面膜,以承受在宽泛的组成范围上形成微乳液所需的不同曲率。
预浓缩油、表面活性剂和共溶剂的组成决定在水相中分散后所得乳液的性质。由smedds(自微乳化药物递送体系)产生的微乳液是热力学稳定的,而常规的乳液是动力学稳定的。根据脂质制剂分类体系(lfcs),smedds的特征在于水溶性组分的含量较高。这些体系可实现尺寸较小的液滴分散体和光学净度,所述光学净度是用于改善当前现有眼科乳液制剂的期望特征。snedds(自纳米乳化药物递送体系)及其所得的纳米乳液共享smedds和微乳液的许多有利特征,但仅限于动力学稳定的分散体。
提供以下参考文献作为背景:
·phasetransitionwater-in-oilmicroemulsionsasoculardrugdeliverysystems:invitroandinvivoevaluation,internationaljournalofpharmaceutics,328(2007)65-71
·oilinwatermicroemulsionsforoculardelivery:evaluationofocularirritationandprecornealretention,journalofcontrolledrelease,111(2006)145-152
·formulationofself-emulsifyingdrugdeliverysystems,advanceddrugdeliveryreviews,25(1),第47-58页
·newperspectivesonlipidandsurfactantbaseddrugdeliverysystemsfororaldeliveryofpoorlysolubledrugs,journalofpharmacyandpharmacology,62(11),第1622-1636页
·potentialsandchallengesinself-nanoemulsifyingdrugdeliverysystems,2012,expertopinionondrugdelivery,9(10),第1305-1317页
·roleofexcipientsinsuccessfuldevelopmentofself-emulsifying/microemulsifyingdrugdeliverysystem(sedds/smedds),drugdevelopmentandindustrialpharmacy,39(1),第1-19页
·self-emulsifyingdrugdeliverysystems(sedds):formulationdevelopment,characterization,andapplications,criticalreviewsintherapeuticdrugcarriersystems,26(5),第427-521页
·spontaneousemulsification:mechanisms,physicochemicalaspects,modeling,andapplicationsjournalofdispersionscienceandtechnology,23(1-3),第219-268页
存在尚未满足的改善眼部药物递送的需求。一些已经描述用于眼科应用的自乳化组合物,但是这些是其中已经存在水包油型乳液的水性组合物,而不是期望的可用于例如水敏感性药物的眼部药物递送的非水性sedds。参见美国专利公开号2004/0185068。
非水性sedds制剂中的眼部药物递送先前尚未公开,并且具有提供若干优点的潜力。表面活性剂/助表面活性剂组合通常可对药物渗透到眼组织中具有增强作用。来自sedds制剂的改善的生物利用度也可由相变体系引起,在所述相变体系中含水量的变化可增加粘度,从而导致眼部停留时间延长。生物利用度也可由于药物以溶解状态递送并且因为眼组织对纳米尺寸颗粒的潜在直接摄取而有所改善。sedds制剂的其他优点包括对热或水解降解敏感的活性药物成分(api)的稳定性增强,因为这些体系是非水性的并且不需要在制备期间在高温下加工。
虽然在本领域中已知自乳化体系作为配制和递送水溶性差的药物的方法,但是为了在泪液中实现快速和自发的乳化,使用以滴眼剂形式的自乳化预浓缩物(即非水性制剂)是新型应用。当前,尚无已知的市售局部眼科药物被配制为snedds或smedds预浓缩物。
发明概述
描述能够自乳化的非水性制剂及其使用和制备方法。所鉴定的制剂意图用作眼科药物递送媒介物,其能够在模拟泪液的水性介质中自乳化。在一些实施方案中,自乳化药物递送体系(sedds)制剂的油组分由单一长链或中链甘油三酯或者中链甘油单酯/甘油二酯构成。在其他实施方案中,油组分是多于一种油的共混物,其由与长链甘油三酯或中链甘油三酯共混的甘油单酯/甘油二酯组成。
在一些实施方案中,油组分可以是天然油(诸如蓖麻油)或合成油(诸如
在一些实施方案中,表面活性剂可以是
在一些实施方案中,共溶剂可以是peg400、peg300或丙二醇。
在一些实施方案中,sedds制剂可与用来治疗眼科病症的治疗药物组合使用,并且可局部递送至眼睛。
本文所提供的组合物易于制备,具有简单和直接遵循的很少的制造步骤。
附图简述
图1示出用于制造本文所提供的sedds的示例性方法。
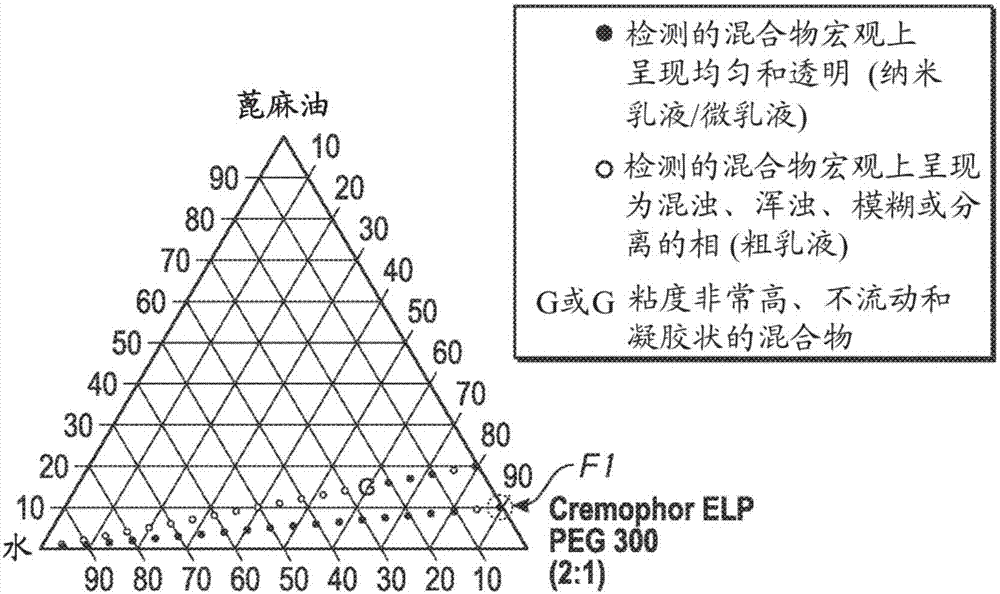
图2示出伪三元相图,其示出由蓖麻油、
图3示出伪三元相图,其示出由蓖麻油、
图4示出伪三元相图,其示出由
图5示出伪三元相图,其示出由
图6示出伪三元相图,其示出由
图7示出伪三元相图,其示出由
图8示出伪三元相图,其示出由蓖麻油、
图9绘制粘度作为由蓖麻油、
图10示出伪三元相图,其示出由
图11绘制粘度作为由
图12a-f示出制剂f1至f11与模拟泪液(stf)的稀释相容性。
图13a-d示出载药制剂f12和f13的稀释度。
发明详述
已经鉴定包含油、表面活性剂和共溶剂的各向同性混合物的新型非水性眼科组合物。这些组合物自乳化,并且不需要高剪切均质化或其他形式的高能机械搅拌来形成水包油型分散体。所得到的水包油型乳液含有纳米尺寸液滴,并且呈现光学澄清或透明。
当作为非水性预浓缩sedds制剂直接施加至眼睛时,所鉴定的组合物另外能够在泪膜的水性介质中原位自乳化。此外,可通过几个简单的步骤容易地制备所鉴定的制剂。将所有组分即油、表面活性剂和共溶剂以适当量添加到一起并混合直到均匀组合。然后可添加亲脂性、水溶性差的药物并搅拌直到完全溶解。
所鉴定的组合物非常适合用作将治疗药物局部递送至眼睛表面以用于治疗各种适应症的赋形剂。对所有制剂与模拟泪液的相容性进行确认,以确保泪液的组成不会对sedds制剂自发分散的能力产生负面影响。本文所使用的模拟泪液由氯化钠、氯化钙、磷酸氢二钠、溶菌酶、白蛋白、粘蛋白和纯净水构成,其中ph调节至约7.2。
如本文所提供,“非水性”眼科组合物或制剂是基本上未有意添加水作为组合物的组分或成分的组合物或制剂。在一些实施方案中,“非水性”眼科组合物或制剂是含有不超过1重量%水的组合物或制剂。在一些实施方案中,本文所提供的非水性眼科组合物含有少于0.5重量%、少于0.25重量%、少于0.1重量%、少于0.05重量%或少于0.01重量%的水。应理解,“少于”一定百分比的水是指从零至指定的量,在由本领域技术人员已知的仪器检测的水的可接受范围内。
如本文所提供,“水溶性差的药物”是指在水中溶解度低的药理活性剂。在本文所提供的组合物中,施用途径是局部施加或滴注至眼睛。因此,如本文所提供,“水溶性差的药物”是指溶解度差得足以使得药物的局部眼科递送不切实际。以往,关于口服药物的溶解度,由美国药典(usp34,5.30)提供的标准已经指导从业人员。还已经开发出生物医药分类体系(“bcs”),以基于溶解度、渗透性和与生物利用度相关的其他参数对药物进行分类。参见gordonl.amidon等人,aapsjournal,2009,11(4):740-746。当适用于局部眼科应用时,bcs体系可用来对可用于本文所提供的局部眼科组合物中的“水溶性差的药物”进行分类。溶解因子适用于如本文所述的模拟泪液,并且渗透性因子可适于眼睛表面处的特定条件。
一般来说,“水溶性差的药物”是指在可接受的ph范围(ph为约4.5-8.0)内通过简单的局部眼科溶液无法实现其治疗剂量的施用以及需要应用溶解手段(诸如胶束体系、共溶剂、络合、乳液或其他方法)来溶解药物的任何药物。
在一些实施方案中,水溶性差的药物选自由以下组成的组:抗生素、抗病毒剂、抗真菌剂、4-孕甾烯-11β-17-21-三醇-3,20-二酮衍生物、麻醉剂、抗炎剂(包括甾体抗炎剂和非甾体抗炎剂)、抗过敏剂、免疫抑制剂和降压剂。合适的药物的实例包括但不限于:环孢菌素、泼尼松龙、氯替泼诺、地塞米松、睾酮、倍氯米松(declomethasone)、利美索龙、氟米龙、倍他洛尔、左倍他洛尔、头孢菌素、两性霉素、氟康唑、四环素、溴莫尼定、布林佐胺、奈帕芬胺、贝西沙星、游霉素、新霉素和左卡巴斯汀(livocabastine)。
在一些实施方案中,水溶性差的药物是式i的4-孕甾烯-11β-17-21-三醇-3,20-二酮衍生物或其对映体、非对映体、水合物、溶剂合物、互变异构体或药学上可接受的盐:
其中:
r1是任选取代的c7-c11烷基、任选取代的c2-c8烯基、任选取代的c2-c8炔基、任选取代的c4或c6-8环烷基、任选取代的芳基、取代的苄基、任选取代的杂环、任选取代的c3-c10环烯基、任选取代的c5-c10环二烯、任选取代的(c3-c6)烷基、氨基、磺酰胺基、酰胺基,苯基除外。
这些4-孕甾烯-11β-17-21-三醇-3,20-二酮衍生物在美国专利公开号2013/0123223(以序列号13/673,623提交)中有所描述,所述美国专利的整体在此以引用的方式并入。下文提供式i范围内的附加实例。
在一些实施方案中,水溶性差的药物是上述式i的化合物,其中r1是
在一些实施方案中,水溶性差的药物是式i的化合物,其中r1是取代的芳基。
在一些实施方案中,水溶性差的药物是式i的化合物,其中r1是
在一些实施方案中,式i的化合物是:
在一些实施方案中,式i的化合物是:
在一些实施方案中,式i的化合物是:
在一些实施方案中,水溶性差的药物化合物是以下4-孕甾烯-11β-17-21-三醇-3,20-二酮衍生物中的一种,所述衍生物在美国专利公开号2013/0123226(以序列号13/673,074提交)中有所描述,所述美国专利的整体在此以引用的方式并入:
(8s,9s,10r,11s,13s,14s,17r)-17-乙醇酰基-11-羟基-10,13-二甲基-3-氧代-2,3,6,7,8,9,10,11,12,13,14,15,16,17-十四氢-1h-环戊并[a]菲-17-基苯乙酸酯;
(8s,9s,10r,11s,13s,14s,17r)-17-乙醇酰基-11-羟基-10,13-二甲基-3-氧代-2,3,6,7,8,9,10,11,12,13,14,15,16,17-十四氢-1h-环戊并[a]菲-17-基丁酸酯;
(8s,9s,10r,11s,13s,14s,17r)-17-乙醇酰基-11-羟基-10,13-二甲基-3-氧代-2,3,6,7,8,9,10,11,12,13,14,15,16,17-十四氢-1h-环戊并[a]菲-17-基丙酸酯;
(8s,9s,10r,11s,13s,14s,17r)-17-乙醇酰基-11-羟基-10,13-二甲基-3-氧代-2,3,6,7,8,9,10,11,12,13,14,15,16,17-十四氢-1h-环戊并[a]菲-17-基辛酸酯;
(8s,9s,10r,11s,13s,14s,17r)-17-乙醇酰基-11-羟基-10,13-二甲基-3-氧代-2,3,6,7,8,9,10,11,12,13,14,15,16,17-十四氢-1h-环戊并[a]菲-17-基己酸酯;
(8r,9r,10s,11r,13r,14r,17s)-17-乙醇酰基-11-羟基-10,13-二甲基-3-氧代-2,3,6,7,8,9,10,11,12,13,14,15,16,17-十四氢-1h-环戊并[a]菲-17-基苯甲酸酯;
(8s,9s,10r,11s,13s,14s,17r)-17-乙醇酰基-11-羟基-10,13-二甲基-3-氧代-2,3,6,7,8,9,10,11,12,13,14,15,16,17-十四氢-1h-环戊并[a]菲-17-基庚酸酯;
(8s,9s,10r,11s,13s,14s,17r)-17-乙醇酰基-11-羟基-10,13-二甲基-3-氧代-2,3,6,7,8,9,10,11,12,13,14,15,16,17-十四氢-1h-环戊并[a]菲-17-基2-甲基丙酸酯;以及
(8r,9r,10s,11r,13r,14r,17s)-17-乙醇酰基-11-羟基-10,13-二甲基-3-氧代-2,3,6,7,8,9,10,11,12,13,14,15,16,17-十四氢-1h-环戊并[a]菲-17-基rel-环戊烷羧酸酯。
常规乳液是具有相对较大的液滴尺寸的热力学不稳定体系,并且其通常表现出乳状外观。当乳液是仅由表面活性剂稳定的水或油的分散体时,乳液液滴随时间趋于聚结,这可导致相分离。
相比之下,本文所提供的sedds制剂形成“纳米尺寸乳液”,其中此类乳液包括由表面活性剂和任选的助表面活性剂稳定的亲水相和疏水相(例如,油和水)的分散体,这种分散体的特征在于含有纳米尺寸液滴。如本文所提供,“纳米尺寸”液滴的平均液滴尺寸可小于约1000nm,例如约5至800nm、约10至600nm、约10至约500nm、约20至约200nm、约10至约200nm以及其中所涵盖的较小范围。由于纳米尺寸液滴,纳米尺寸乳液通常将是光学透明的。
如本文所提供,纳米尺寸乳液可形成微乳液或纳米乳液。“微乳液”是通过使用表面活性剂和助表面活性剂稳定以降低界面张力的水或油的分散体,并且通常特征在于液滴尺寸小(通常液滴直径小于200nm)、热力学稳定和外观透明。“纳米乳液”是指具有纳米范围内的液滴尺寸(通常直径小于200nm)和透明外观的乳液,但由于油和水界面处的界面张力高,所述乳液热力学不稳定。有时可通过向现有乳液添加剪切力来产生纳米乳液。
使用sedds制剂呈现出下文所概括的多个优点:
1.通过使用sedds递送溶解状态下的亲脂性和水溶性差的药物,避免与固-液相转变和缓慢溶解过程相关的能量输入。这可改善药物的生物利用度。
2.在用泪液稀释时,可发生原位相转变而成为高粘度液体结晶体系。这可增加制剂在角膜上的停留时间并且改善药物生物利用度。
3.由于纳米尺寸颗粒被组织直接摄入的潜力,在分散时形成纳米尺寸液滴可进一步改善药物生物利用度。
4.用于制备sedds中的某些表面活性剂/助表面活性剂组合可对穿过角膜的药物渗透具有增强作用。
5.由于液滴尺寸小(例如小于200nm),自发的自乳化产生具有澄清外观的纳米尺寸乳液。此类纳米尺寸乳液并不引起如用常规乳液通常所经历的视力模糊,所述视力模糊归因于后者的较大液滴尺寸和乳白色外观。这可帮助改善患者的满意度和依从性。
6.在分散在水相中时产生微乳液的smedds的情况下,所得的微乳液是热力学稳定体系,并且不会随时间而破裂。
7.从最终制剂中排除水性组分可保护不稳定的api免于经历水解降解,并且潜在地延长产品的储存寿命。
8.sedds的制造是具有很少步骤的简单过程,其可在环境温度下进行,并且不需要大量的能量输入。因此,这可在制造期间为热敏感性api提供增强的稳定性。
在本文所提供的sedds组合物中,表面活性剂优选地选自但不限于具有hlb>12的非离子型表面活性剂。“hlb”是指亲水/亲脂平衡。hlb(亲水-亲脂平衡)是关于稳定乳液的能力对非离子型表面活性剂分等级的计算值。hlb的标度通常为1-20。具有高hlb值(例如>10)的表面活性剂用来稳定水包油型乳液,而具有低hlb值(例如<8)的表面活性剂用来稳定油包水型乳液。
具有hlb>12的非离子型表面活性剂的实例包括但不限于:聚山梨醇酯80(聚氧乙烯脱水山梨糖醇单油酸酯)、聚山梨醇酯40(聚氧乙烯脱水山梨糖醇单棕榈酸酯)、聚山梨醇酯20(聚氧乙烯脱水山梨糖醇单月桂酸酯)、
在一些实施方案中,用于本文所提供的组合物中的共溶剂可选自
用于本文所提供的sedds组合物中的油可以是天然、合成或半合成起源。油可选自由以下组成的组:单一长链甘油三酯、单一中链甘油三酯、中链甘油单酯和中链甘油二酯。在一些实施方案中,油是与长链甘油三酯或中链甘油三酯共混的甘油单酯或甘油二酯的共混物。
在一些实施方案中,本文所提供的sedds组合物由约5%至约60%w/w的油构成。在一些实施方案中,组合物含有约10%至约40%w/w的油。
在一些实施方案中,油选自由以下组成的组:蓖麻油、棉籽油、大豆油、橄榄油、玉米油、红花油、芝麻油、辛酸/癸酸甘油酯(诸如
在一些实施方案中,提供油的组合。在一些实施方案中,油的组合是以下的两种或更多种:蓖麻油、
在一些实施方案中,油是按重量计1∶1的蓖麻油和
在一些实施方案中,油是按重量计1∶1的
在一些实施方案中,组合物包含蓖麻油、
在一些实施方案中,组合物包含蓖麻油、
在一些实施方案中,组合物包含
在一些实施方案中,组合物包含
在一些实施方案中,组合物包含
在一些实施方案中,组合物包含
在一些实施方案中,组合物包含按重量计3∶1的蓖麻油和
在一些实施方案中,组合物包含按重量计2∶1的
在一个实施方案中,组合物包含约10%至约40%w/w蓖麻油,其中组合物还包含
在一个实施方案中,组合物包含约10%至约40%w/w的蓖麻油知
在一个实施方案中,组合物包含约10%至约40%w/w的
在一个实施方案中,组合物包含约10%至约40%w/w的
在一个实施方案中,组合物包含约10%至约40%w/w的
在一个实施方案中,组合物包含约10%至约40%w/w的
在一个实施方案中,组合物包含约10%至约40%w/w的蓖麻油知
在一个实施方案中,组合物包含约10%至约40%w/w的
此外,助表面活性剂可任选地与本文所提供的表面活性剂组合使用。在一些实施方案中,助表面活性剂是非离子型,具有hlb<10,并且选自由以下组成的组:span83、span80、span60、span40、span20、capryoltm90和lauroglycoltm90或其组合。
在一些实施方案中,并且在不受理论或作用机制约束的情况下,本文所提供的非水性sedds组合物由于在所述组合物中缺乏水性环境而并不含有或需要防腐剂。在一些实施方案中,本文所提供的非水性sedds组合物并不含有抗微生物防腐剂。
在一些实施方案中,本文提供含有本文所提供的sedds组合物的试剂盒。在一些实施方案中,试剂盒是适合于眼科施用的多剂量瓶。在一些实施方案中,试剂盒是适合于眼科施用的单剂量小瓶或容器。此类试剂盒可用于直接施加至需要治疗眼睛疾病或病症的患者的眼睛。
在一些实施方案中,试剂盒包括两个瓶、容器或隔室,所述两个瓶、容器或隔室中的一个含有本文所提供的非水性sedds组合物,并且所述两个瓶、容器或隔室中的另一个包含眼科可接受的水溶液。在将组合的溶液施用至患者的眼睛之前不久,这些两部分体系可由医生或患者组合。
用于制备的方法
本文所提供的自乳化体系可通过以下简单步骤制备(参见图1):
1.称取适当量的表面活性剂(对于在室温下为糊状固体的表面活性剂,需要温和加热);
2.如果需要,添加适当量的助表面活性剂并混合组合;
3.添加适当量的共溶剂并混合组合;
4.添加所需量的油并混合组合;
5.添加药物活性成分并混合溶解;
6.使用适当的灭菌方法和产品灌装。
实施例
实施例1:
以下实施例用于其中油组分是来自植物来源的长链甘油三酯的sedds制剂。油与表面活性剂/共溶剂之比在1∶9或2∶8下变化。在下文图2中的相图中可看到用水稀释至最终含水量为95%w/w对乳液外观的作用。将表面活性剂与共溶剂之比保持恒定在2∶1,使得可孤立增加含油量对自乳化和产生澄清纳米尺寸乳液的能力的作用。基于相图中所指示的有利稀释选择具有10%w/w含油量的制剂f1(表2)。随后对用模拟泪液稀释f1进行确认,并且其示出对纳米尺寸乳液形成没有影响(图12)。
表2
实施例2:
以下实施例用于其中油组分是以1∶1比率与中链甘油单酯/甘油二酯共混的长链甘油三酯的sedds制剂。与单独使用长链甘油三酯相比,在油组分中包含中链甘油单酯/甘油二酯意图改善纳米尺寸乳化的区域。将表面活性剂与共溶剂之比保持恒定在2∶1,并且将油的含量从制剂的10%w/w增加至50%。将制剂稀释至最终含水量为95%w/w,并且结果在下文图3中的相图中示出。制剂f2和f3被选择,并且分别含有20%w/w和10%w/w的含油量。组成可参见下文的表3和表4。随后也对用模拟泪液稀释进行确认,并且其示出对纳米尺寸乳液形成没有影响(图12)。
表3
表4
实施例3:
以下实施例用于含有中链甘油三酯
表5
实施例4:
以下实施例用于由作为油相的
表6
表7
表8
表9
实施例5:
以下实施例用于由作为油相的
表10
表11
实施例6:
在这个实施例中,使用
表12
实施例7:
在这个实施例中,使用以3∶1比率的蓖麻油和
表13
实施例8:
在这个实施例中,使用中等链长的两种合成油
表14
研究了在所选制剂(f1-f13)中掺入亲脂性药物。使用三种模型药物:醋酸泼尼松龙、泼尼松龙(无水)和4-孕甾烯-11b-17-21-三醇-3,20-二酮衍生物(“皮质醇类似物”)。这些化合物是基于其在常规悬浮液或溶液制剂中水溶性差和易降解而选择的。下文(表15)是这些化合物在制剂f1-f13中可达到的最大平衡溶解度。
表15.制剂中的药物溶解度
对在制剂中掺入药物对用水性介质稀释时自乳化能力的作用进行确认。选择f12和f13,并且用磷酸盐缓冲盐水稀释载药制剂。稀释时纳米尺寸乳液的形成不受两种制剂中药物的存在的影响(图13)。
眼部耐受性研究:
使用新西兰白色雌性兔子对用于我们的制剂中的各种药物级赋形剂的眼部耐受性进行体内评估。共有十个测试组,每组三只兔子,用来测试列于下文的表16中的物质。通过将一滴最低浓度的物质滴注到第一只兔子的左眼进行每组中的给药。如果不耐受,则停止给药。如果耐受,将相同浓度的一滴滴注到第二只兔子的左眼,然后对于第三只兔子同样如此。如果3只兔子耐受某一浓度,用下一个较高浓度(如果适用)以相同模式继续给药。
最大耐受剂量以及“不耐受”观察结果的原因列于下文的表16中。样品组成(具体来说,用来稀释测试物质的媒介物)列于下一个表(表17)中。
表16.在新西兰白兔中体内测试的物质的眼部耐受性结果
表17.测试物质的样品描述
在测试的三种油中,蓖麻油和
除非本文另外指明或与上下文明显矛盾,否则本文(尤其在以下权利要求书的上下文中)所使用的术语“一个/种”、“所述”以及类似的指代语应解读为涵盖单数和复数指代语。除非本文另外指明或以其他方式与上下文明显矛盾,否则可按任何合适的顺序来执行本文所述的所有方法。本文所提供的任何和所有实例或示例性语言(例如,“诸如”)的使用仅意图更好地阐明本发明,而不会对任何权利要求的范围构成限制。本说明书中的语言不应解读为指示任何未要求保护的要素是实践本发明所必需的。
本文所公开的替代要素或实施方案的分组不应解读为限制。每个组成员可单独或者以与组中的其他成员或本文存在的其他要素的任何组合被提及和要求保护。出于便利和/或可专利性的原因,预期组中的一个或多个成员可包括在组中或从组中删除。当出现任何这种包括或删除时,本说明书被认为包含所修改的组,因此满足所附权利要求书中使用的所有马库什组的书面说明。
最后,应理解,本文所公开的实施方案是对权利要求书的原理进行说明。可采用的其他修改在权利要求书的范围之内。因此,通过实例而非限制,可根据本文的教义使用替代实施方案。因此,权利要求书并不限于确切示出和描述的实施方案。
- 还没有人留言评论。精彩留言会获得点赞!