一种超声引导下介入治疗引导系统及其使用方法与流程
本发明属于介入治疗领域,具体涉及一种超声引导下介入治疗引导系统及其使用方法。
背景技术:
经皮动脉导管封堵术、经皮房间隔缺损封堵术等经典介入治疗术式,自上世纪问世以来,在世界范围内广泛开展。这些术式的共同特点是:经外周血管穿刺后,在放射线的引导下,配合造影剂的应用,将导丝、导管插入心脏,经导管将封堵器等置于病变位置,已到达治疗目。但上述的这些手术在术中必须使用放射线照射,对患者及医务人员均存在辐射损伤的风险,不仅会对骨髓、生殖器及甲状腺等器官的功能产生影响,而且也大大增加癌症的发病率,尤其对于处于生长发育阶段的儿童患者。医务人员在术中穿防护服来保护自己的同时,沉重的铅衣也增加了手术的强度,对健康造成损害。而且术中常需要使用造影剂,有造成过敏、肾功能衰竭等并发症的风险。另一方面,传统的放射线引导下的介入治疗精确度差,手术难道及风险大。
超声替代放射线进行经皮介入治疗具有精准、无辐射、无造影剂的优势,具有广阔的应用前景,但是由于超声的工作原理与放射线工作原理完全不同,超声是一个切面一个切面的逐个扫描,不像放射线是投影式探测,所以以超声为唯一引导手段时,最大的困难在于超声不能像放射线一样准 确判断导管头端在心脏内的位置,对手术过程中的准确定位造成困难,增加手术难度及风险。
因此,如何开发出一种以超声为引导方法的安全高效的介入治疗引导系统,以降低手术难度、增加手术成功率、减少医疗损伤及费用,成为本领域迫切需要解决的技术问题。
技术实现要素:
为解决上述技术问题,本发明提供一种超声引导下介入治疗引导系统,包括球囊导管和导丝,导管具有导丝通道,且导管外标有刻度,涂有亲水涂层;
所述球囊导管包括带有可装载止血阀的导管和一个设置在所述导管头端外侧的可膨胀球囊,所述球囊与所述导管实现密封套接;
所述导管内设有两个沿其长度方向平行且彼此独立的通道,其中位于中央贯穿整个导管的为主通道,主通道外侧的另一通道为副通道,所述主通道的开口设置于所述导管的两端,形成主开口;
副通道开口设置于所述主通道的头端外侧,所述球囊对应密封套接在位于副通道开口的远端,形成与主通道互不干扰的可膨胀密封空间;
所述副通道的另一侧开口则连接有充盈阀门,用于向所述副通道内注入或抽吸气体或液体使球囊膨胀或吸瘪;
所述导管的长度尺寸为60-150cm;所述主通道的直径尺寸适于通过0.035(0.89mm)英寸的导丝。
所述导管为两通道导管,主通道外的副通道与指引球囊套接,其中,所述指引球囊由反复操作不变形的菲薄超弹性材料制作,最大直径为0.5-1.0cm。
所述导管BCD段弧度直径为14mm、20mm、28mm,角度为45°、60°、75°、90°。
所述导丝由细钢丝缠绕一根钢缆编织而成,标有刻度,头部柔软部分长度3-8cm,体尾部硬度增加;导丝表面有能够强力吸附超声造影剂的特殊涂层;导丝直径0.035(0.89mm)英寸,长度为150-260cm。
所述球囊及导管通道工作状态下均由超声造影剂充盈。
所述导管头端弧形部分采用特殊的冷塑性材料,在冰水中可以根据手术的需要,改变不同的弧度。
所述导管各接口可与现有的医疗设备实现无障碍连接。
本发明还提供了一种上述超声引导下介入治疗引导系统的使用方法,其特征在于,可以应用于超声引导下经皮房间隔缺损封堵术、超声引导下经皮动脉导管未闭封堵术、超声引导下经皮室间隔缺损封堵术、超声引导下经皮肺动脉瓣狭窄扩张术、超声引导下经皮主动脉瓣狭窄扩张术等先天性心脏病的介入治疗。
以超声引导下经皮房间隔缺损封堵术为例,本介入治疗引导系统使用方法具体包括如下步骤。
(1)手术在普通心脏外科手术室进行,患者取仰卧位,采用利多卡因等局部麻醉;对于不配合的患儿行基础麻醉;所有患者均无需气管插管。
(2)选择合适型号的引导系统,穿刺右侧股静脉,并测量右锁骨中线第三肋间到穿刺点的距离,标记为工作距离;在导管上从D点往A点方向测量,并标记达到工作距离时的刻度。
(3)将导丝插入导管内,导丝尖端伸出导管外2-4cm,经导丝通道充盈口向导管腔内注入少量超声造影剂,经股静脉送入导管及导丝,未遇阻力时继续推进,将导管及导丝插入到达工作距离后,经球囊通道充盈口注入预定量的超声造影剂使球囊充盈,超声即可在右心房内发现导管的球囊头端,如房间隔缺损较大,直接超声引导导管球囊头端跨过房间隔缺损,如房间隔缺损较小,超声引导导管球囊头端对准房间隔缺损,导丝经导管跨过房间隔缺损,进入左房,回抽造影剂,使球囊吸瘪,导管头端可轻易跨过房间隔。
(4)导丝通过超声造影剂填充的主通道,吸附造影剂,在超声引导下通过导管头端的指引到达左心房,同时导丝配合导管头端球囊的强显影及刻度,导丝进入的深度大于导管深度3-5cm,导丝到位后,固定导丝,回抽球囊内造影剂,使球囊吸瘪后,退出导管。
(5)根据房间隔缺损直径选择相应大小的封堵器及输送系统,经导丝送入输送鞘 管,送入长度参照球囊导管进入长度,并在超声下观察输送鞘管通过房间隔缺损到达左心房;退出输送鞘管的内芯及导丝,保持输送鞘管外鞘位于左房内,沿输送鞘管送入封堵器,释放封堵器左房侧后,回撤输送鞘管,使封堵器左房侧紧贴房间隔缺损的左房壁;固定输送杆,回撤输送鞘管,将封堵 器从鞘管内完全释放,回送输送杆,使封堵器的右房侧紧贴房间隔缺损的右房壁;超声检查封堵效果,如果封堵器形态好,且无残余分流及对周围结构的不良影响,逆时针旋转输送钢缆释放封堵器,退出输送鞘,常规压迫止血,加压包扎,手术结束。
以超声引导下经股静脉动脉导管未闭封堵术为例,本介入治疗引导系统使使用方法具体包括如下步骤。
(1)手术在普通心脏外科手术室进行,患者取仰卧位,采用利多卡因等局部麻醉;对于不配合的患儿行基础麻醉;所有患者均无需气管插管。
(2) 选择合适型号的引导系统,穿刺右侧股静脉,并测量胸骨右缘第三肋间到穿刺点的距离,标记为工作距离;在导管上从D点往A点方向测量,并标记达到工作距离时的刻度。
(3)将导丝插入导管内,导丝尖端伸出导管外2-4cm,经导丝通道充盈口向导管腔内注入少量超声造影剂,经股静脉送入导管及导丝,未遇阻力时继续推进,将导管及导丝插入到达工作距离后,经球囊通道充盈口注入预定量的超声造影剂使球囊充盈,超声即可在右心房内发现导管的球囊头端,超声引导导管球囊头端对三尖瓣, 继续推进导管跨过三尖瓣,进入右心室,超声引导下,旋转导管,在导丝的帮助下,使导管向右心室流出道推进,必要时回抽球囊内造影剂,使球囊吸瘪后,导管即可通过肺动脉瓣进入主肺动脉。
(4) 超声探头于胸骨左侧第二肋间显示动脉导管,超声引导下,调整导管头端,对准动脉导管的肺动脉侧开口,推进导丝,通过动脉导管进入降主动脉。导丝进入的深度大于导管深度5-10cm,导丝到位后,固定导丝,回抽球囊内造影剂,使球囊吸瘪后,退出导管。
(5)根据动脉导管直径选择相应大小的封堵器及输送系统。经导丝送入输送鞘管,送入长度参照球囊导管进入长度,并在超声下引导下将输送鞘管通过动脉导管到达降主动脉,进入的深度大于球囊导管深度5-10cm。退出输送鞘管的内芯及导丝,保持输送鞘管外鞘位于降主动脉内,沿输送鞘管送入封堵器,释放封堵器主动脉侧后,回撤输送鞘管,使封堵器主动脉侧紧贴动脉导管的主动脉侧;固定输送杆,回撤输送鞘管,将封堵 器从鞘管内完全释放,回送输送杆,使封堵器腰部镶嵌在动脉导管内。超声观察是否有明显的腰征,检查封堵效果,如果封堵器形态好,且无残余分流及对周围结构的不良影响,逆时针旋转输送钢缆释放封堵器,退出输送鞘,常规压迫止血,加压包扎,手术结束。
本介入治疗引导系统在其他先天性心脏病介入治疗中的使用方法,不在一一叙述。
本发明所述的球囊导管,由于其指引球囊会在充盈气体或液体后膨胀,其截面积相比于导管的截面积会大大增加,而且充分利用了超声造影剂的优势,此时应用超声探测会非常容易探测 到导管头端的位置,能安全的将导管及导丝送到病变部位。因此,采用此介入治疗引导系统,可以安全有效的采用超声进行探测引导,以避免现有技术中射线引导带 来的潜在危害。
本发明所述引导系统,可分别根据患者的年龄,所患先天性心脏病的种类选择合适型号的结构进行操作。
附图说明
为了使本发明的内容更容易被清楚的理解,下面根据本发明的具 体实施例并结合附图,对本发明作进一步详细的说明,其中,
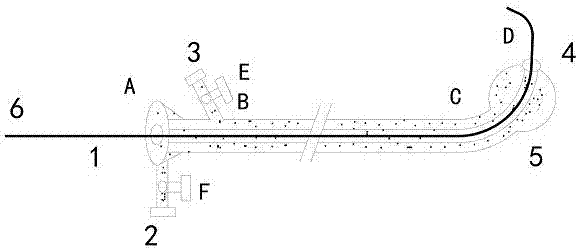
图1为本发明所述引导系统在超声造影剂未注入导丝通道和球囊通道,导丝未吸附超声造影剂,球囊因弹性回缩紧贴导管壁的结构示意图;
图2为本发明所述引导系统在超声造影剂通过充盈口2和3,分别注入导丝通道和球囊通道,导丝吸附超声造影剂,同时球囊被超声造影剂充盈而膨胀的结构示意图。
图中,1为带有可拆卸止血阀的主通道入口,2为主通道充盈口,3为副通道充盈口,4为主通道出口, 5为指引球囊,6为引导导丝,ABCD为导管主线,BCD为导管的弧度段,E为与副通道充盈阀门,F为与主通道充盈阀门。
具体实施方式
本发明所述的一种超声引导下介入治疗引导系统,包括球囊导管和导丝,导管具有导丝通道,且导管外标有刻度,涂有亲水涂层;
所述球囊导管包括带有可装载止血阀的导管和一个设置在所述导管头端外侧的可膨胀球囊,所述球囊与所述导管实现密封套接;
所述导管内设有两个沿其长度方向平行且彼此独立的通道,其中位于中央贯穿整个导管的为主通道,主通道外侧的另一通道为副通道,所述主通道的开口设置于所述导管的两端,形成主开口;
副通道开口设置于所述主通道的头端外侧,所述球囊对应密封套接在位于副通道开口的远端,形成与主通道互不干扰的可膨胀密封空间;
各个所述通道的另一侧开口则分别连接有充盈阀门,用于向各个所述通道 内注入或抽吸气体或液体膨胀或吸瘪球囊。
进一步的,所述导管的长度尺寸为60-150cm;所述主通道的直径尺寸适于通过0.035(0.89mm)英寸的导丝;
所述导管为两通道导管,主通道外的副通道与指引球囊套接,其中,所述指引球囊由反复膨胀不变形的菲薄超弹性材料制作,最大直径为0.5-1.0cm;
所述导管BCD段弧度直径为14mm, 20mm, 28mm,角度有45°、60°、75°、90°。
进一步的,所述导丝由细钢丝缠绕一根钢缆编织而成,标有刻度,头部柔软部分长度3-8cm,体尾部硬度增加;导丝表面有能够强力吸附超声造影剂的特殊涂层,导丝直径0.035(0.89mm)英寸,长度为150-260cm。
所述球囊及导管通道工作状态下均由超声造影剂充盈。
所述导管头端弧形部分采用特殊的冷塑性材料,在冰水中可以根据手术的需要,改变不同的弧度。
所述导管及导丝均标有刻度,参考术前所测的工作距离,导丝配合导管头端球囊的强显影及刻度,能够准确掌握导管及导丝进入人体的深度,有效避免进入过深导致心脏穿孔等并发症。主通道带有可装载的止血阀,可以与现有的设备无障碍连接。既能避免术中出血,同时可以通过止血阀的充盈开关向主通道内注入超声造影剂,随着导丝的进入,造影剂会充填进导丝缝隙及表面,增强导丝在超声检测下的可见性。
当导管进入人体接近工作距离时,向副通道内注入超声造影剂,头端球囊逐渐膨起,超声易于探测,超声引导导管头端到达病变部位,导丝通过导管的引导跨过缺损,建立轨道,为手术操作的关键步骤。导管球囊充盈起的头端,不易进入心脏瓣膜的腱索间隙,从而避免造成腱索断裂导致瓣膜关闭不全的并发症。导管头端设计为钝而柔软,减少对组织的损伤。指引球囊为菲薄的超弹性的材料,反复操作不变形。注入空气或液体时能膨起,抽出空气或液体时吸瘪,吸瘪后的球囊会紧贴导管,不增加导管的直径,从而不影响导管的通过性。
此引导系统,充分利用超声造影剂的微气泡能显著增强超声背向散射强度,可以通过肺循环,对人体无害的特性。造影剂微气泡在超声的作用下会发生振动,散射强超声信号。理论上,气泡粒子的散射截面要比同样大小的固体粒子(例如铁)大1亿倍。所以气泡组成的造影剂的造影效果比别的散射体优越。通过往球囊或导管中中注入超声造影剂,可以得到很强的超声回波。在图像上能更清晰的显示球囊和导管的位置。因此该引导系统,与现有的普通固体导管相比,超声监测更清晰,更易于超声引导。
实施例1
如图1所示,所述的球囊导管为导管设有三个通道的球囊导管结构。其中,所述的一种超声引导下介入治疗引导系统,包括球囊导管和导丝,导管具有导丝通道,且导管外标有刻度,涂有亲水涂层;
所述球囊导管包括带有可装载止血阀的导管和一个设置在所述导管头端外侧的可膨胀球囊,所述球囊与所述导管实现密封套接;
所述导管内设有两个沿其长度方向平行且彼此独立的通道,其中位于中央贯穿整个导管的为主通道,主通道外侧的另一通道为副通道,所述主通道的开口设置于所述导管的两端,形成主开口;
副通道开口设置于所述主通道的头端外侧,所述球囊对应密封套接在位于副通道开口的远端,形成与主通道互不干扰的可膨胀密封空间;
各个所述通道的另一侧开口则分别连接有充盈阀门,用于向各个所述通道 内注入或抽吸气体或液体膨胀或吸瘪球囊。
进一步的,所述导管的长度AD段尺寸为60、80cm;所述主通道的直径尺寸适于通过0.035(0.89mm)英寸的导丝。
所述导丝的长度尺寸为150cm;
所述导管为两通道导管,主通道外的副通道与指引球囊套接,其中,所述指引球囊由反复操作不变形的菲薄超弹性材料制作,直径为0.5-1.0cm;
所述导管BCD段弧度直径为14mm、20mm,角度有45°、60°、75°、90°。
其中,所述指引球囊的最大直径为0.5cm,所述指引球囊与所述导管外壁相套接的长度段CD为0.5cm。
实施例2
本实施例所述球囊导管与实施例1的结构相同,其区别仅在于进一步的,所述导管的长度AD段尺寸为120、150cm;所述导丝的长度尺寸为260cm;
所述导管BCD段弧度直径为28mm,角度有45°、60°、75°、90°;
所述指引球囊的最大直径为1.0cm,所述指引球囊与所述导管外壁相套接的长度段CD为1.0cm。
实施例3
上述实施例1和2所述的介入治疗引导系统可适用于不同年龄段患者,及不同先天性心脏病的介入治疗。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!