一种沙门氏菌的体内磁引导投送方法与流程
本发明涉及一种基于磁小体、磁性微囊和体外磁力引导设备组合构建的沙门氏菌体内磁引导投送方法,具体地说,涉及含有磁小体的趋磁沙门氏菌和装载趋磁沙门氏菌的磁性微囊,并通过在体外的非接触式磁引导设备,组合实现的一种沙门氏菌在体内靶向投送的方法,属于生物医学应用领域。
背景技术:
传统的分子药物靶向输送方法存在药物不能足够精确和足量到达病患处的问题,故要提高抗肿瘤治疗因子的靶向效率和杀伤效果,需要依托新型的靶向转运载体。相比于其他的转运载体,沙门氏菌具有趋低氧、嗜肿瘤组织特性。借助趋化受体和动力鞭毛,它可以感测、移动、聚集、并在实体瘤内扩增,但由于沙门氏菌自驱动力较弱,且体内血管环境复杂,使之不易到达靶器官肿瘤组织。
趋磁细菌是一类能够沿着磁场方向运动的细菌的总称,其最显著的特征是在胞内特殊的原核细胞器—磁小体。磁小体是具有外膜包被、纳米级、在胞内成链状排列的fe3o4或fe3s4磁性颗粒,如同指南针一样为趋磁细菌导航[文献1]。kolinkoi等利用基因转染技术在具有光合作用的红螺菌体内合成磁性纳米颗粒,即磁小体链,开创了趋磁细菌的人工合成方法[文献2]。进一步,martel利用核磁共振(mri)梯度场实现了趋磁细菌在人造血管中的运动控制[文献3]。加拿大生物医学工程研究所-纳米机器人实验室尝试在体外控制载药趋磁细菌的移动方向,突破了大分子药物难以弥散到实体瘤乏氧区的难题[文献4]。但以上的研究多基于体外的模拟试验,难以克服体内复杂环境对细菌投送的影响,故需研发一种趋磁细菌在体内靶向投送的方法。
文献1:alphandérye.applicationsofmagnetosomesynthesizedbymagnetotacticbacteriainmedicine.frontbioengbiotechnol.2014,2(5):1-6
文献2:kolinkoi,lohea,borgs,.raschdorfo,joglerc,tuq,posfaim,tompae,plitzkojm,brachmanna,wannerg,mullerr,zhangy,schulerd.biosynthesisofmagneticnanostructuresinaforeignorganismbytransferofbacterialmagnetosomegeneclusters.natnanotechnol.2014,9(3):193-197
文献3:martels,felfoulo,mathieujb,chanua,tamazs,mohammadim,mankiewiczm,tabatabaein.mri-basedmedicalnanoroboticplatformforthecontrolofmagneticnanoparticlesandflagellatedbacteriafortargetinterventionsinhumancapillaries.intjrobres.2009,28(9):1169-1182
文献4:taherkhanis,mohammadm,daoudj,martels,tabrizianm.covalentbindingofnanoliposomestothesurfaceofmagnetotacticbacteriaforthesynthesisofself-propelledtherapeuticagents.acsnano.2014,8(5):5049-5060
技术实现要素:
针对现有技术中存在的技术问题,本发明的目的在于提供一种含有趋磁沙门氏菌的磁性微囊,以及利用该磁性微囊在体外磁引导设备作用下体内趋磁沙门氏菌的靶向投送方法。
本发明通过以下技术方案实现。
一种磁性微囊,包括:
由含趋磁沙门氏菌的培养液和降解液混合得到的混合液滴,所述趋磁沙门氏菌内含有磁小体;
磷酸甘油酯微滴,其中包含所述混合液滴;以及
磁性水凝胶外壳,其包裹在所述磷酸甘油酯微滴之外。
优选地,所述降解液为海藻酸钠水凝胶降解液。
优选地,所述混合液滴中的含趋磁沙门氏菌的培养液的细菌密度为1×105个/毫升;所述海藻酸钠水凝胶的浓度为0.01克/毫升。
优选地,所述水凝胶外壳通过包含四氧化三铁磁性纳米粒子的海藻酸溶液和氯化钙溶液发生交联反应形成。
优选地,所述包含四氧化三铁磁性纳米粒子的海藻酸溶液中的磁性纳米粒子浓度为0.005克/毫升。
优选地,所述磁小体的是由质粒ptps-abg6复合体和质粒ptps-xyz复合体通过电穿孔方法构建。
本发明还提供了根据以上技术方案中任一项所述的磁性微囊的制造方法,包括以下步骤:
将趋磁沙门氏菌的菌液接种于不含抗生素的lysogenybroth(lb)培养液,振荡培养至对数生长中期,离心收集菌体,用预冷的无菌去离子水洗涤2次,洗涤后的细菌悬于冰预冷的无菌去离子水,用电穿孔法将ptps-abg6、ptps-xyz质粒转染至沙门氏菌,构建磁小体基因,从而实现沙门氏菌的趋磁性。
利用半导体工艺的软光刻技术,加工微流道芯片;
将含所述减毒沙门氏菌的lb培养液和0.0162克/毫升的海藻酸钠水凝胶降解液混合;
通过注射泵,将该混合液,磷酸甘油酯、包含四氧化三铁磁性纳米粒子的海藻酸溶液和矿物油分别注入所述微流道芯片,形成海藻酸溶液包裹磷酸甘油酯微滴再包含混合液微滴的结构;
海藻酸溶液被矿物油液体夹断,形成海藻酸液微滴,该微液滴被注入氯化钙溶液中,海藻酸微滴将和氯化钙溶液发生交联反应,形成水凝胶外壳,从而形成磁性微囊结构。
优选地,所述微流道的深度为100微米。
本发明还提供了一种沙门氏菌的磁引导投送方法,包括以下步骤:
步骤一、制造包含所述沙门氏菌的根据以上技术方案之一所述的磁性微囊;
步骤二、将所述磁性微囊投递到目标位置附近的第一位置;
步骤三、利用磁力引导设备的磁场引导所述磁性微囊到达目标位置附近的第二位置;
步骤四、所述磁性微囊在所述第二位置破裂,从而释放所述沙门氏菌;之后,使所述沙门氏菌在磁场梯度的引导下,移动到目标位置。
优选地,所述磁力引导设备包括机械臂和电磁镊;通过所述机械臂能够调节所述电磁镊的尖端位置,从而形成所述磁场梯度。
优选地,在所述步骤四中,含有所述沙门氏菌的磁性微囊通过其自身内部包裹的降解液使其定时破裂,从而将所述沙门氏菌释放。
有益效果:
本发明通过基于微流控技术构建包裹趋磁沙门氏菌的磁性微囊;最后基于这种包裹沙门氏菌的磁性微囊,构建基于机械臂控制的磁力引导的靶向投递方法,可实现集器官内介入、大血管微囊磁导投递与小血管沙门氏菌磁导自趋于一体的主动式三级投递系统,突破治疗因子的高靶向性、高浓度的投送,可以克服目前伴多器官转移的晚期结直肠癌治疗方法效率低、特异性不高的问题,为提高靶向药物的治疗效率提供新的途径。
附图说明
图1是本发明的方法示意图
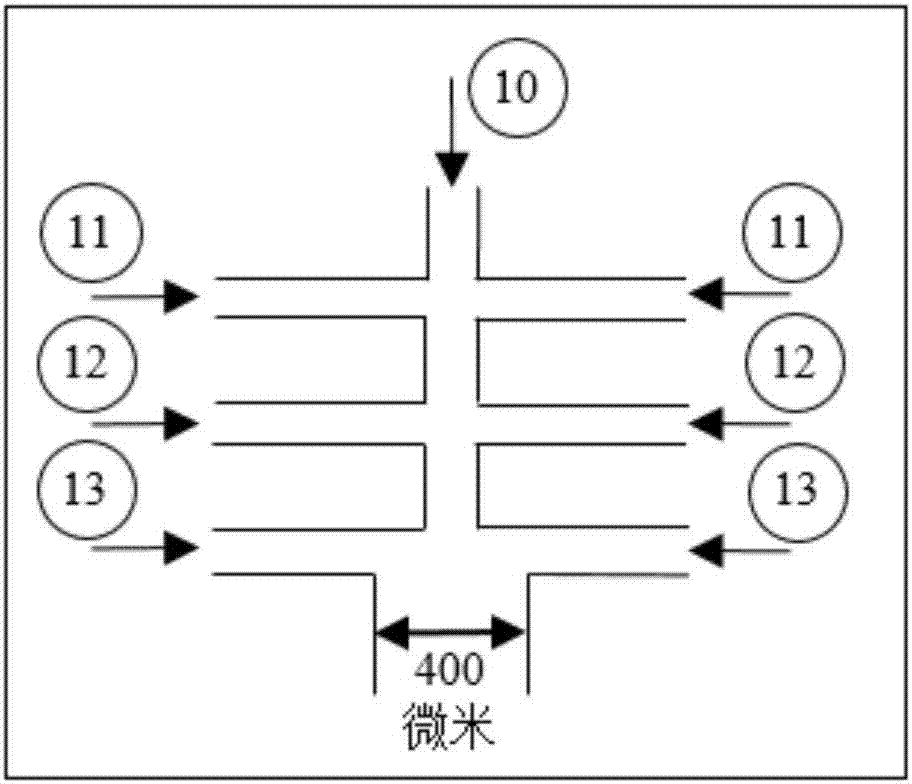
图2是微流道结构示意图
图3中的局部位置16的细节图
附图标记:1.沙门氏菌鞭毛;2.沙门氏菌;3.包裹沙门氏菌磁性微囊;4.介入管道;5.肝脏;6.机械臂;7.尖端电磁镊;8.电磁镊铁芯尖端;9.螺线管;10含有沙门氏菌的培养液和海藻酸钠水凝胶降解液的混合液注入微流道;11.磷酸甘油酯注入微流道;12.海藻酸钠溶液注入微流道;13.矿物油注入微流道,14.肝脏中血管,15.肿瘤,16.肿瘤位置。
具体实施方式
在此的术语“微流控”所指的是一种精确控制和操控微尺度流体,尤其特指亚微米结构的技术。
根据本发明的磁引导靶向投送方法如图1所示,所述投送方法步骤如下;
步骤一、基于微流控技术加工包含趋磁沙门氏菌的磁性微囊。
步骤二、通过临床医学中介入的方法,将本发明所述的含有趋磁沙门氏菌的磁性微囊准确投递至肝脏大血管位置。
步骤三、将本发明所述的包含趋磁沙门氏菌的磁性微囊在由所述磁力引导设备的磁场引导下随着血流进入靶器官;通过磁力引导设备中的机械臂调节电磁镊的尖端位置,沿着通向肿瘤的血管的方向,形成磁力梯度。磁性微囊可以沿着磁力梯度到达通向肿瘤的小血管前段(血管直径小于磁性微囊的直径)。磁性微囊在体内的空间位置通过核磁设备(mri)进行实时监测。
步骤四、在小血管前段,本发明所述的含有沙门氏菌的磁性微囊通过其自身内部包裹的降解液使其定时破裂,从而将所述重组减毒沙门氏菌释放;之后,便进入所述趋磁沙门氏菌的由于具有趋磁性的自驱动阶段,在这一阶段,所述趋磁沙门氏菌运动的动力主要是由自身携带的鞭毛提供,其运动的方向由磁力梯度来控制,磁力梯度覆盖肿瘤位置,从而引导沙门氏菌移动至肿瘤位置,从而完成所述含有沙门氏菌的磁性载体的靶向投送
本发明的一个优选实施例的投送过程如下:
(1)将减毒沙门氏菌的菌液接种于不含抗生素的lysogenybroth(lb)培养液,振荡培养至对数生长中期,离心收集菌体,用预冷的无菌去离子水洗涤细胞2次,洗涤后的细菌悬于冰预冷的无菌去离子水,用电穿孔法(multiporator4308eppendorf电转仪)将ptps-abg6、ptps-xyz转染至减毒沙门氏菌,从而实现减毒沙门氏菌的趋磁性。
(2)利用半导体工艺的软光刻技术,加工polydimethylsiloxane(pdms)微流道。如图2所示,所述微流道包括含有沙门氏菌的培养液和海藻酸钠水凝胶降解液的混合液注入微流道10、磷酸甘油酯注入微流道11、海藻酸钠溶液注入微流道12,以及矿物油注入微流道13。在一优选的实施例中,该微流道的深度为大约100微米,出口宽度为大约400微米。将含减毒沙门氏菌的lb培养液(细菌密度:1×105个/毫升)和0.0162克/毫升的sodiumcitratetribasicdihydrate海藻酸钠水凝胶降解液混合,之后,按照图2所示,通过注射泵,将该混合液,磷酸甘油酯、包含四氧化三铁磁性纳米粒子的海藻酸溶液(磁性粒子浓度:0.005克/毫升,海藻酸溶液浓度:0.01克/毫升)和矿物油分别注入该芯片,形成海藻酸溶液包裹磷酸甘油酯微滴再包含混合液微滴的结构。再次,海藻酸溶液被矿物油液体夹断,形成海藻酸液微滴,该微液滴被注入氯化钙溶液中,海藻酸微滴将和氯化钙溶液发生交联反应,形成水凝胶外壳,从而形成磁性微囊结构。
(3)通过临床医疗中介入的方法,将磁性微囊准确投递至靶向器官大血管位置,接着,磁性微囊可在由机械臂控制的尖端电磁镊的磁场引导下随着血流进入靶器官。尖端电磁镊由直径为1毫米的铜线和圆柱形软铁铁芯两部分组成,铜线绕铁芯一端形成5000匝的螺线管,铁芯另一端被加工成尖端,用于汇聚磁场。如图1所示,尖端电磁镊铁芯包括一基本呈圆柱形的部分,以及连接于该圆柱的一端的基本呈圆锥形的部分。其中该基本呈圆柱形的部分的长度大约22厘米,截面直径大约为16厘米。该基本呈圆锥形的部分的底面尺寸与该圆柱形部分的端面尺寸基本相同,高度可根据实际需要设计。在核磁共振成像系统的引导下,确定肿瘤具体位置,通过机械臂调节电磁镊的尖端位置,沿着通向肿瘤的血管的方向,形成磁力梯度。磁性微囊可以沿着磁力梯度到达通向肿瘤的小血管前段。在小血管前段,磁性微囊通过其自身内部包裹的降解液使其定时破裂,从而将微囊内的减毒沙门氏细菌释放。之后,便进入趋磁细菌的自驱动阶段,在这一阶段,趋磁减毒沙门氏菌运动的动力主要是由自身携带的鞭毛提供,其运动的方向由体外磁场梯度来控制,体外磁场梯度穿过肿瘤位置,引导沙门氏菌移动至肿瘤位置,从而完成重组减毒沙门氏菌的靶向投递。
- 还没有人留言评论。精彩留言会获得点赞!