用于校正光学信号的方法和装置与流程
本申请是中国申请号为201480016308.3、国际申请日为2014年3月6日的pct申请pct/us2014/021298的、发明名称为“用于校正光学信号的方法和装置”的发明专利申请的分案申请。
相关申请交叉引用
本申请要求于2013年3月14日提交的、题为“methodanddeviceforcorrectingopticalsignals”的美国临时专利申请61/785,087的权益,该申请在此通过引用整体并入。
背景技术:
本发明涉及用于监测植入物的方法和装置,并具体地涉及用于校正从植入物发射的发光信号的方法和装置。
在某些个体中,对分析物(例如葡萄糖、乳酸盐或氧)水平的监测对于他们的健康是很重要的。高水平或低水平的葡萄糖,或其他分析物,可能有不利影响或预示特定的健康状态。葡萄糖的监测对于患有糖尿病的个体特别重要,他们中的一个子集必须确定何时需要胰岛素以降低他们体内的葡萄糖水平或者何时需要额外的葡萄糖以提高他们体内的葡萄糖水平。
被许多患有糖尿病的个体用来亲自监测他们的血糖水平的常规技术包括定期抽取血液,将该血液施加到测试条,并使用量热、电化学或光度检测法来确定血糖水平。这种技术不允许连续或自动监测体内的葡萄糖水平,而通常必须在周期性基础上手动执行。不幸的是,葡萄糖水平的检查的一致性在个体之间变化很大。许多糖尿病患者发现定期测试不方便,并且他们有时会忘记测试他们的葡萄糖水平或者没有时间进行适当的测试。此外,一些个体希望避免与测试相关联的疼痛。未受监控的葡萄糖可能导致高血糖或低血糖发作。监测个体分析物水平的植入式传感器将允许个体更容易地监测他们的葡萄糖或其他分析物水平。
各种装置已经被开发用于监测血流中或各种组织的间质液中的分析物(例如,葡萄糖)。许多这些装置使用被插入到患者血管中或皮下的传感器。因为高散射存在下的低荧光水平,这些植入式传感器通常难以光学地读取或监测,前述高散射归因于皮肤状况的动态变化(例如,血液水平和水合作用)。皮肤是高度散射的,并且该散射可以主导光传播。散射是由组织中折射率变化所引起的,并且,皮肤中的主要散射组分归于脂质、胶原蛋白和其他生物组分。主要的吸收是由血液、黑色素、水和其他组分所引起的。
一个装置(公开于yu的已公布美国专利申请20090221891中),包括葡萄糖分析部件。当传感器被植入体内时,通过外部光学器件经皮读出光学信号。荧光计,分别对供体发色团和受体发色团测量激发光强度、环境光强度以及发光和环境光的复合强度。通过握持荧光计接近皮肤并对准传感器来进行测量。提供的最终输出是来自这两个发色团的发光强度之间的归一化比值,该比值可以使用校准数据被转换为分析物浓度。校准曲线通过测量响应对葡萄糖浓度而被经验性地建立。尽管该装置提供了一些光学信号校正,但获得准确读数可能仍然是困难的,这归因于导致从植入物发射的光的光学散射和吸收的动态的皮肤变化。
merritt的美国专利申请20110028806公开了另一种用于测量血糖水平的方法和系统。一组光电二极管检测从一个或多个发射器(例如多个led)发射到患者皮肤中的光能量的发光和反射。结合到葡萄糖的小分子代谢物报道子(reporter)(smmrs)被引入角质层和表皮的组织以提供更易于检测的发光。使用在接近激发波长处进行的反射强度测量来校准测试结果。此外,该方法包括测量第二发光和反射强度,以归一化来自第一组测量的数据。第一发光和反射强度测量在使用smmr处理的部位处进行。第二发光和反射强度测量在未处理的背景部位处进行。然后使用背景测量通过波长归一化来校正背景组织发光和吸收。尽管该方法对于背景发光和反射提供了一些光信号校正,但是从表皮中的葡萄糖结合分子获得准确和/或一致的葡萄糖读数可能仍然是困难的。
仍然需要这样一种小型的、紧凑的装置,该装置可以准确和一致地监测植入式传感器,并提供信号给分析者,而基本上不限制患者的运动和活动。当分析物水平处于或接近阈值水平时,分析物的连续和/或自动监测可以对患者提供警告。例如,如果葡萄糖是分析物,那么该监测装置可以被配置成警告患者当前正在发生或即将发生高血糖或低血糖。那么患者就可以采取适当的行动。
技术实现要素:
根据一个方面,提供一种方法,用于校正从植入物发射的至少一个分析物相关光学信号。该植入物通常被埋置在哺乳动物身体的组织中。该植入物能够响应于激发波长范围内的激发光,发射处于发射波长范围内的分析物相关光学信号。该方法包括发送激发波长范围内的第一激发光穿过组织到植入物,并且响应于该第一激发光测量从组织发射的发射波长范围内的第一光学信号。该方法还包括发送处于发射波长范围内的第二激发光到组织中,并且响应于该第二激发光测量从组织发射的发射波长范围内的第二光学信号。根据所测量的信号计算至少一个校正的信号值。
根据另一个方面,提供一种光学检测装置,用于监测埋置在哺乳动物身体的组织中的植入物。该植入物能够响应于激发波长范围内的激发光,发射处于发射波长范围内的至少一个分析物相关光学信号。该装置包括第一光源,该第一光源被布置成发送激发波长范围内的第一激发光穿过组织到植入物。第二光源,被布置成发送处于发射波长范围内的第二激发光到组织中。至少一个检测器,被布置成响应于第一激发光测量从组织发射的发射波长范围内的第一光学信号,以及被布置成响应于第二激发光测量从组织发射的发射波长范围内的第二光学信号。
根据另一个方面,提供一种方法,用于校正至少一个从埋置在哺乳动物身体的组织中的植入物发射的分析物相关光学信号。该植入物能够响应于激发波长范围内的激发光,发射处于发射波长范围内的分析物相关光学信号。该方法包括发送激发波长范围内的第一激发光穿过组织到植入物,并且响应于该第一激发光测量从组织发射的发射波长范围内的第一光学信号。该方法还包括发送激发波长范围内的第二激发光到组织中,并且响应于该第二激发光测量从组织发射的发射波长范围内的第二光学信号。第二激发光和响应于第二激发光发射的光形成光路,该光路从植入物被横向间隔开足够的距离,以避免来自植入物报道子(例如,发光、发光、生物发光或磷光报道子)的显著贡献。根据所测量的光学信号计算至少一个校正的信号值。
根据另一个方面,提供一种光学检测装置,用于监测埋置在哺乳动物身体的组织中的植入物。该植入物能够响应于激发波长范围内的激发光,发射处于发射波长范围内的至少一个分析物相关光学信号。该装置包括第一光源,该第一光源被布置成发送激发波长范围内的第一激发光穿过组织到植入物。第一检测器,被布置成响应于第一激发光测量从组织发射的发射波长范围内的第一光学信号。第二光源,被布置成发送激发波长范围内的第二激发光到组织中。第二检测器,被布置成响应于第二激发光测量从组织发射的发射波长范围内的第二光。第二光源和第二检测器被相对于彼此放置,使得第二激发光和响应于该第二激发光发射的光形成光路,该光路从植入物被横向间隔开足够的距离,以避免来自植入物报道子的显著贡献。
附图说明
本发明的前述方面和优点通过阅读下面的详细描述并通过参考以下附图将变得更好理解,其中:
图1示出根据本发明一个实施例的用于监测植入物的光学检测装置的示意性侧视图。
图2示出根据本发明另一个实施例的用于监测植入物的光学检测装置的示意性侧视图。
图3示出根据本发明另一个实施例的光学检测装置的一些方面的示意性侧视图。
图4示出根据本发明另一个实施例的光学检测装置的示意性俯视图。
图5示出图4的装置的示意性剖面图。
图6示出根据本发明一些实施例的光学检测装置的示意性侧视图。
图7示出根据本发明一些实施例的光学检测装置的示意性俯视图。
图8示出图7的装置的示意性剖面图。
图9示出根据本发明一些实施例的光学检测装置的示意性俯视图。
图10示出图9的装置的示意性剖面图。
图11示出根据本发明一些实施例的光学检测装置的示意性俯视图。
图12示出图11的装置的示意性分解图。
具体实施方式
在下面的描述中,应当理解,结构之间所有描述的连接可以是直接操作性连接或者是通过中间结构的间接操作性连接。一组要素包括一个或多个要素。对要素的任何描述应理解为是指至少一个要素。多个要素包括至少两个要素。除非另有要求,任何描述的方法步骤不需要一定以特定的所示出顺序执行。源自第二要素的第一要素(例如数据)包括等于该第二要素的第一要素,以及通过处理第二要素和任选的其他数据所生成的第一要素。根据参数做出确定或决策包括根据该参数和可选的根据其他数据做出确定或决策。除非另有规定,一些数量/数据的指标可以是该数量/数据本身,或者不同于该数量/数据本身的指标。本发明的一些实施例中描述的计算机程序可以是独立的软件实体或其他计算机程序的子实体(例如,子例程,代码对象)。计算机可读介质包括非暂时性介质如磁的、光学的和半导体的存储介质(例如硬盘驱动器,光盘,闪存,dram),以及通信链路,例如导电电缆和光纤链路。根据一些实施例,本发明提供(尤其是)计算机系统,该计算机系统包括被编程以执行此处描述的方法的硬件(例如,一个或多个处理器和相关的存储器),以及编码指令以执行此处描述的方法的计算机可读介质。
以下的说明以举例的方式而未必是以限制的方式阐明了本发明的实施例。
图1示出根据本发明第一实施例的光学检测装置10的示意性侧视图,该光学检测装置10用于监测植入式传感器或植入物12。植入物12被埋置在哺乳动物身体的组织中(在各种实施例中,其可以是组织的一部分,该部分附接于或不附接于身体的其余部分)。植入物12通常被埋置在皮肤14的表面之下。植入物12被埋置在皮肤14的表面之下的第一深度处,该第一深度优选为足够的深度,以将植入物安置在皮下组织中(例如,皮肤14的表面之下1至5mm范围内)。在一些实施例中,植入物12被埋置在处于皮肤14的表面之下大于或等于2mm的深度处的组织中,并且在其他实施例中,植入物12被埋置在处于皮肤表面之下大于或等于4mm的深度处的组织中。
植入物12能够响应于激发波长范围内的激发光,发射至少一个发射波长范围内的分析物相关光学信号。分析物可以包括,例如,个体体内的葡萄糖或其他分析物。合适的光学信号包括,但不限于,发光、生物发光、磷光、自发光和漫反射信号。在优选的实施例中,植入物12包含一个或多个发光染料,该发光染料的光发射强度根据个体体内的目标分析物的量或存在而变化。
第一光源16被布置为从皮肤14的表面发送激发波长范围内的第一激发光到植入物12。第二光源18被布置为从皮肤14的表面发送第二激发光到组织15中。第二激发光优选处于分析物相关发光信号的发射波长范围内(例如,发射峰)。合适的光源包括,但不限于,激光,半导体激光,发光二极管(led),有机led。
至少一个检测器,并且更优选至少两个检测器20、22随光源16、18布置。第一检测器20被放置以响应于来自第一光源16的第一激发光来测量在皮肤14的表面处发射的发射波长范围内的第一光学信号(例如,光的强度)。检测器20还被布置成响应于第二激发光来测量从组织15发射的穿过皮肤14表面的发射波长范围内的第二光学信号。合适的检测器包括,但不限于,光电二极管或ccd。尽管对于一些实施例来说多个检测器是优选的,人们也可以使用单个通用检测器。检测器20、22优选经过滤(例如,二向色滤光片或其它合适的滤光片)以测量在相应波长范围内发射的光学信号。在这个例子中,对葡萄糖浓度敏感的合适发光染料是alexa647,alexa647响应于约600至650nm范围内(吸收峰647nm)的激发光(吸收),并且发射波长在约670至750nm范围内,具有约680nm的发射峰。
在装置10的操作中,针对漫反射和/或自身荧光校正从植入物12发射的分析物相关发光信号。光源16被激活以从皮肤14的表面发送激发波长范围内的第一激发光到植入物12。第一检测器20响应于该第一激发光在皮肤14的表面处测量从组织15发射的处于发射波长范围内的第一光学信号,正如由从光源16到植入物12到第一检测器20的第一光路24所表示的那样。光路24提供了初级的分析物相关光学信号。第二光源18被激活以从皮肤14的表面发送第二激发光到位于皮肤14的表面之下的组织15中的第二深度。第二激发光基本上处于分析物相关发光信号的发射波长范围内(例如,发射峰)。第一检测器20响应于第二激发光测量从组织15发射穿过皮肤14的表面的处于发射波长范围内的第二光学信号,正如由第二光路26所表示的那样。
第二光学信号可以用作参考信号,以针对组织15中光的漫反射或散射而校正初级的分析物相关光学信号。在一些实施例中,在皮肤14表面之下光路26延伸所达的第二深度可以基本上等于植入物12被埋置所处的第一深度(例如,在皮肤14表面之下1至5mm深度处的皮下组织中)。在一些实施例中,第二光学信号的光路26延伸到大于或等于皮肤14的表面之下2mm的深度,并且在其他实施例中,第二光学信号的光路26延伸到大于或等于皮肤的表面之下4mm的深度。
一个附加校正因子可以可选地通过激活第一光源16以从皮肤14的表面发送第三激发光到组织15中的第三深度来获得,该第三激发光处于激发波长范围内。在一些实施例中,第三深度可以不同于第一深度和第二深度,并且第三深度可以在皮肤14的表面之下1至5mm范围内。第二检测器22测量响应于第三激发光从组织15发射穿过皮肤14的表面的激发波长范围内的第三光学信号,如由第三光路28所表示的那样。根据所测量的光学信号计算至少一个校正的信号值。在一个例子中,来自植入物的初级分析物相关信号可以被校正为:
校正信号=s(ls1,d1)*c(ls2,d1)*c(ls1,d2)(1)
在上面的式子(1)中,项s(ls1,dl)表示第一光学信号,第一光学信号是从第一光路24测量得到的初级的分析物相关光学信号,该第一光路24从第一光源16到植入物12到第一检测器20。项c(ls2,dl)表示第二光学信号,第二光学信号是从第二光路26测量得到的校正因子信号,该第二光路26从第二光源18到第一检测器20。项c(ls1,d2)表示可选的第三光学信号,第三光学信号是从第三光路28测量得到的附加校正因子信号,该第三光路28从第一光源16到第二检测器22。
因此,从植入物12发射的初级的分析物相关光学信号可以针对分析物相关光学信号的发射波长范围内的漫反射或散射而被校正,以解决组织15中信号的光学散射或吸收。分析物相关光学信号可以可选地针对激发波长范围内的散射、反射或衰减而被校正,以解决皮肤属性中的动态变化。通过一个或多个参考信号来校正分析物相关信号的一个优点是:准确和/或一致的葡萄糖值可以从对发射自位于组织中相对较深处(例如在皮下区域中)的植入物的光进行的测量而被确定。从植入物12发射的光可能被植入物和皮肤14的表面之间的组织15强烈调整。除了针对激发光和背景或环境光的校正之外(如果需要的话),本发明的实施例提供了针对从组织15发射的光的调整而进行校正的手段。
另一个优点在于,用于校正因子(例如漫反射、自身荧光和/或背景光)的参考光学信号的测量是在几秒或更少时间内在与植入物12埋置的组织15相同区域中进行的,这样一来,在测量时间处,动态的皮肤或组织属性(该属性在身体不同区域中可能是变化的)对于校正信号与对于初级的分析物相关信号来说基本上是相同的。在对分析物相关信号、漫反射校正信号和/或自身荧光校正信号执行光学读取之前,可以进行暗读取以解决背景或环境光,并且该读取可以用来进一步校正信号,例如,通过背景减除。对校正因子的光学读取的优选顺序为背景减除、自身荧光校正和漫反射校正,尽管不需特定顺序。
在一些实施例中,分析物浓度(例如,葡萄糖水平)从校正的信号值而被确定。优选地,使用查找表或校准曲线根据校正的信号值来确定分析物浓度。查找表或校准曲线可以在包含于光学器件的微处理器中。在一些实施例中,微处理器被编程以存储所测量的信号值和/或计算校正的信号值。替代性地,这些功能可以在独立的处理器中或与该光学装置通信的外部计算机中执行。外部处理器或计算机接收表示所测量的光学信号的数据,并计算校正的信号值和分析物浓度。替代性地,可以提供多个处理器,例如,在与一个或多个外部处理器或计算机通信(无线地或通过电线)的光学装置中提供一个或多个处理器。
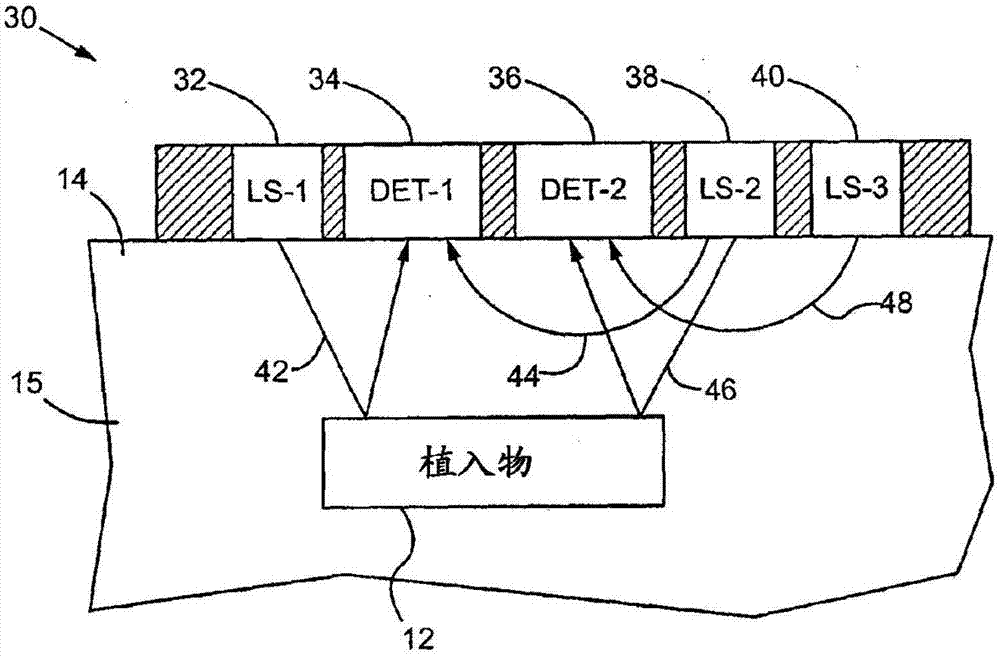
图2示出用于监测植入物12的光学检测装置30的另一个实施例。在这个实施例中,植入物12还能够响应于第二激发波长范围(该第二激发波长范围可以共享第一发射波长范围或与之重叠)内的激发光,发射第二发射波长范围内的至少一个分析物不相关光学信号。植入物12优选含有分析物不相关发光染料,该分析物不相关发光染料用于控制非分析物在报道子染料上的物理或化学作用(例如,光漂白或ph)。多种染料可以使用。该分析物不相关光学信号不受组织15中存在的分析物所调整并提供用于归一化、偏移校正或内部校准的数据。该分析物不相关信号可以补偿非分析物的影响,该影响是化学的或生理学的(例如,氧、ph、氧化还原条件)或光学的(例如,水、光吸收/散射化合物、血红蛋白)。替代性地,该分析物不相关信号可以由植入物12中的稳定参考染料所提供。合适的稳定参考材料包括,但不限于,镧系元素掺杂的晶体,镧系元素的纳米颗粒,量子点,螯合的镧系元素染料和金属(例如,金或银)纳米颗粒。稳定参考染料可以为其他信号提供参考信号(例如,用于确定光漂白)。
第二实施例不同于上面描述的第一实施例,在于装置30包括第三光源40用于发送激发光穿过皮肤14的表面到组织15中。在装置30的操作中,使用三个参考信号来校正从植入物12发射的分析物相关发光信号。第一光源32被激活以发送第一激发波长范围内的激发光,从皮肤14的表面,穿过组织15,到植入物12。第一检测器34响应于第一激发光在皮肤14的表面处测量从组织15发射的第一发射波长范围内的第一光学信号,正如由第一光路42所表示的,该第一光路42从第一光源32到植入物12且到第一检测器34。该第一光学信号是初级分析物相关光学信号。
第二光源38被激活以从皮肤14的表面发送第二激发光到组织15中的第二深度。该第二激发光优选处于初级分析物相关光学信号的第一发射波长范围内(例如,发射峰)。第一检测器34响应于第二激发光在皮肤14的表面处测量从组织15发射的发射波长范围内的第二光学信号,正如由第二光路44所表示的那样。第二光学信号可以被用来校正植入物12和皮肤14的表面之间的组织15中光的漫反射或散射。在一些实施例中,第二光路44的深度可以基本上等于植入物12被埋置所处的第一深度(优选在皮肤14的表面之下1至5mm的皮下组织中)。在一些实施例中,第二光学信号的光路44延伸到大于或等于皮肤14的表面之下2mm的深度,并且在其他实施例中,第二光学信号的光路44延伸到大于或等于皮肤的表面之下4mm的深度。
接着,光源38被激活以从皮肤14的表面发送第二激发波长范围内的第三激发光到植入物12。第二检测器36响应于该第三激发光在皮肤14的表面处测量从组织15发射的第二发射波长范围内的第三光学信号,正如由第三光路46所表示的那样。在这个实施例中,第三光学信号是分析物不相关发光信号。接着,第三光源40被激活以从皮肤14的表面发送第四激发光到组织15中。第四激发光优选处于分析物不相关发光信号的发射波长范围内。检测器36响应于第四激发光在皮肤14的表面处测量从组织15发射的该发射波长范围内的第四光学信号,正如第四光路48所表示的那样。根据所测量的光学信号计算至少一个校正的信号值。在一个例子中,来自植入物12的初级分析物相关信号可以被校正为:
校正信号=s(ls1,d1)*c(ls2,d1)/[s(ls2,d2)*c(ls3,d2)](2)
在上面的式子(2)中,项s(ls1,dl)表示第一光学信号,第一光学信号是从第一光路42测量得到的初级分析物相关信号,该第一光路42从第一光源32到植入物12到第一检测器34。项c(ls2,dl)表示第二光学信号,第二光学信号是从第二光路44测量得到的校正因子信号,该第二光路44从第二光源38到第一检测器34。项s(ls2,d2)表示第三光学信号,第三光学信号是从第三光路46测量得到的分析物不相关信号,该第三光路46从第二光源38延伸到植入物12到第二检测器36。项c(ls3,d2)表示第四光学信号,第四光学信号是从第四光路48测量得到的校正因子信号,该第四光路48从第三光源40延伸到第二检测器36。
在一些实施例中,其中利用两个植入物报道子(例如,发光染料),下面这样是可能的,即植入物报道子的激发(吸收)或发射波长范围可以共享或者重叠。例如,在图2的实施例中,第一染料(其提供分析物相关发光信号)的发射波长范围与第二染料(其提供分析物不相关发光信号)的激发波长范围共享或重叠。在另一个实施例中,第一染料和第二染料可以共享或重叠激发波长范围(这样就可以使用共同的光源),并发射不同发射波长范围内的光学信号。在另一个实施例中,第一染料和第二染料可以由不同激发波长范围内的光所激发并发射相同或重叠的一个或多个发射波长范围的光学信号。
图3示出相对于皮肤14的表面之下植入物12的第一深度d1的组织15中不同深度d2、d3、d4处的光学询问(interrogation)。检测器52、54、56的布置与光源50之间的间距s1、s2、s3确定相应光路的深度d2、d3、d4。在一些实施例中,对光学信号校正的读取在多个深度处执行,正如由相应的光路所表示的那样,并且,用于校正的参考光学信号的测量值被平均用于校正因子。在一些实施例中,参考光学信号的光路延伸到组织15中的深度d2,该深度d2大于植入物12被埋置所处的深度d1。参考光学信号的光路也可以延伸到组织15中的深度d3,使得该光路穿过植入物12。
当光学装置具有光源和检测器之间间距的多种可能组合时(如图3-9所示),实现方式可以更灵活,因为植入物12的深度可以是应用特定的。在一个实施例中,至少一个分析物不相关信号(其可以由稳定参考染料发射)被用于确定一条或多条光路和所得的一个或多个光学信号的适当深度,该一个或多个光学信号被测量以针对漫反射和/或自身荧光来校正分析物相关信号。优选地,使用查找表基于从植入物发射的分析物不相关发光信号的所测量的强度,来确定应当使用归一化光学信号的哪一个或多个可能的深度,或者更具体地,哪一对或多对光源/检测器配对。查找表可以是在包含于光学器件的微处理器中,或者是在独立的处理器中或与该光学装置通信的外部计算机中,其接收表示所测量的光学信号的数据(例如,在所选波长内测量的光的强度)。
在一些实施例中,处理器被编程为确定(例如,通过计算或查找表)被分配给一个或多个漫反射信号的测量结果的量或权重。被分配给所测量的漫反射信号的量或权重然后可以被用于校正或归一化一个或多个植入物报道子信号(例如,从植入物发射的初级分析物相关信号),以计算校正的信号值。该量或权重优选根据分析物不相关光学信号(例如,来自稳定参考染料)的强度而被确定。分析物不相关光学信号的强度可以随植入物在组织中的深度而变化。例如,如果植入物被埋置在皮肤的表面之下2mm的深度处的组织中,在组织中光衰减的量将可能小于如果该植入物被埋置在4mm深度处。比起从埋置于较大深度处的植入物发射的那些信号,从较浅的植入物发射的报道子光学信号可能需要较小的针对漫反射和/或自身荧光的校正因子。在一些实施例中,用于校正或归一化分析物相关光学信号的漫反射校正因子与深度成正比,并且,根据分析物不相关信号的测量结果来确定被分配给漫反射测量结果的量或权重。
图4示出光学装置60的另一个实施例,在该实施例中,光学装置60具有附加光源和检测器,光源和检测器之间的间距有多种可能的组合。光源和检测器被布置在适于放置在皮肤表面上的传感器贴片62中,下面更详细地描述光源和检测器。至少一个,并且更优选三个中心激发器光源64a、64b和64c被放置以通过贴片62中的中心通路66发送激发光。中心通路66可以包含一个或多个光波导。至少一个检测器,并且更优选由三个中心检测器68a、68b和68c组成的内环围绕中心通路66布置。同样优选的是,具有多个外环激发器光源和外环检测器(在这个例子中为25个外环光源和检测器)的外环70基本上呈环形图案布置,提供可能的光通道的多种排列。激发光源和检测带的组合是光通道。光学装置60的一个可能的实现方式的例子现在将参考图4-11和表1给出,该例子描述了12条光通道。
表1
如表1所示,光通道1-3用以测量来自植入物的三个报道子染料信号,包括分析物特异性信号、分析物不相关信号和稳定参考染料信号。光通道1用以测量来自植入物的分析物特异性发光信号,例如强度随葡萄糖水平变化的光信号。其他实施例可以包括来自植入物的多个分析物相关信号。光通道2用以测量分析物不相关对照,该分析物不相关对照针对报道子染料上的非分析物物理或化学作用(例如,光漂白,ph)。光通道3用以测量稳定参考染料(例如,镧系元素)。
如列于表1和示于图4,各光通道1-3包括一个相应配对,配对为三个中心激发器光源64a、64b和64c中的一个与三个中心检测器68a、68b和68c中对应的一个。图6示出了植入物报道子的光学检测的光路的示意性侧视图。激发光通过中心通路66(其优选包括单片波导)被发送,从皮肤14的表面,穿过组织15,并且到植入物12。中心检测器68a、68b和68c响应于激发光在皮肤14的表面处测量从组织15发射的相应发射波长范围内的光学信号。
用于分析物相关信号的合适染料是alexa647,染料alexa647响应于约600至650nm的激发波长范围(激发峰647nm)内的激发光,并且在约670至750nm的发射波长范围内,发射峰约为680nm。用于分析物不相关信号的合适染料是alexa750,染料alexa750响应于约700至760nm的激发波长范围(激发峰750nm)内的激发光,并且在约770至850nm的发射波长范围内,发射峰约为780nm。合适的稳定参考染料是铒,铒具有约650至670nm的第一激发光波长范围(激发峰约650nm),约800至815nm的第二激发波长范围(约805nm的激发峰),以及约980至1050nm的发射波长范围(约1020nm的发射峰)。在另一个实施例中,铒和alexa647可以从相同光源被激发,其优点在于,多个光源之间功率归一化的可选步骤被减少或被消除。
再次参照表1,光通道4-6提供激发器功率归一化信号,这在使用多于一个光源的实施例中是优选的。激发器功率归一化信号被用于对由各光源输出的激发光的功率的差异进行归一化,其中,各光源的输出功率可能略有不同。如图4-5所示,从中心通路66传播到外环70的激发光的衰减被测量,减少或消除由植入物12的报道子(例如,荧光团)的贡献。光通道4-6包括配对的组合,配对为三个中心激发器光源64a、64b和64c以及外环检测器6的配对。替代性地,可以使用多个检测器来检测激发器功率归一化信号的强度,优选外环检测器。对于激发器功率归一化信号,植入物报道子的激发波长范围内的激发光被发送到组织15中。从组织15发射的激发波长范围内的光学信号通过检测器6而被检测。植入物报道子的校正的信号值可以针对相应光源的激发器功率而被归一化,例如,通过将对报道子所测量的光学信号除以激发波长范围内的激发光的所测量的强度。
光学通道7-9(表1)提供漫反射测量结果以校正来自植入物的发光染料报道子信号。如图7-8所示,外部检测器6测量由组织15所造成的光学信号的衰减,该光学信号处于植入物12的发光报道子染料的发射波长范围内。光通道7-9包括外部激发器光源71a、71b和71c中的三个,它们被布置在外环70中,在这个例子中,它们中的每一个与检测器6配对,并且优选地被放置成提供各光源/检测器组合之间的一系列距离,从而对植入物12的各发光报道子染料计算漫反射校正值。在替代性实施例中,可以使用多个检测器而不是利用检测器6来测量所有三个光学信号。
光通道10-12(表1)提供自身荧光和环境光的测量,以校正来自植入物的发光染料报道子信号。如图9-10所示,光通道10-12包括布置在外环70中的外部激发器光源和外环检测器的三个配对73a、73b和73c。外部激发器光源和外部检测器的三个配对73a、73b和73c提供了植入物12的三个报道子发光染料的相同激发和发射光谱,并且位于外环70上远离植入物12。具体地,用于一个或多个自身荧光测量的每一个外部激发器光源/检测器配对相对于彼此而被放置,使得激发光和响应于该激发光发射的光形成光路78,光路78从植入物12被横向间隔开足够的距离,以避免来自植入物荧光团的显著贡献。
优选横向间隔s4大于或等于0.25cm,更优选大于0.5cm,并且最优选大于1cm。还优选光路78的深度延伸约1-5mm到皮肤14的表面之下的组织15中。当使用多个配对时,各光路可以具有基本上相同的深度或不同的深度,并且所测量的自身荧光光学信号的强度可以被平均以获得校正因子。优选来自一个或多个植入物报道子(例如,荧光团)的、对自身荧光测量的贡献小于所测量的强度的30%,更优选小于20%,最优选小于10%。
图11示出传感器贴片62的俯视图,该传感器贴片62具有用于激发光的中心通路66。贴片62的优选尺寸可以是,例如,约16mm的直径和约1.6mm的厚度t。图12示出了贴片62的示意性分解图,该贴片62包括堆叠的多个层。在一些实施例中,层可以包括具有约200um优选厚度的塑料盖80、具有约100um优选厚度的光控制膜82、具有约200um优选厚度的滤光片84、具有约100um优选厚度的另一个光控制膜86、具有约200um优选厚度的硅层88、具有约400um优选厚度的印刷电路板(pcb)90、具有约300um优选厚度的电池92和具有约200um厚度的壳体94。pcb90可以包括微处理器,该微处理器被编程为存储所测量的值和/或如前面所述计算校正的信号值。光控制膜是透镜阵列,该透镜阵列在其背侧上具有孔阵列。
本领域技术人员应当清楚,所描述发明的实施例可以包括有线或无线手持式阅读器、无线皮肤贴片阅读器、台上仪器、成像系统、手持式装置(例如,手机或移动通信装置)、智能电话附件和应用程序,或者利用所公开的光学器件和算法的任何其他配置。
组织的光学异质性在某些情况下可能是显著的。因此,利用单个光源和单个检测器以确保每一种颜色通过相同光路(该光路穿过组织)可以是有利的。在一个实施例中,光源可以被安放一组可移动滤光片,该滤光片处于光源和皮肤的表面之间。同样,可以利用单个光检测器代替分开的、离散的检测器元件。通过使用可移动或可更换的滤光片以允许测量多个波长,检测器可以被用来检测不同颜色。更换或移动滤光片可以由控制转盘、滤光带或其他手段的机械致动器来实现。替代性地,光学滤光片可以涂有一种材料,当经受电流、电势、温度或其他可控的影响时,该材料将改变光学滤光特性,使得单个光检测器可用来检测多种颜色。
本领域技术人员应当清楚,上述实施例可以以多种方式改变而不脱离本发明的范围。例如,一个或多个光源、一个或多个检测器、滤光片和/或连接光学部件的光纤的多种不同的排列或布置可以用于实现本发明的装置和方法。例如,在一些实施例中,光源和检测器被连同光纤或电缆布置,以发送激发光到皮肤中并测量从皮肤发射的光学信号,而不必须在直接在个体的皮肤上放置光源和检测器。在替代性实施例中,装置的尺寸和/或波长范围的目前的优选值可能不同。因此,本发明的范围应当由随后的权利要求及其合法等同物来确定。
- 还没有人留言评论。精彩留言会获得点赞!