用于增强肝再生的方法与流程
该国际申请要求2016年2月22日递交的美国临时申请第62/298139号的优先权的益处,其全部内容通过参照结合于此。
政府许可权
该发明在美国国立卫生研究院授予的r01ag043483和r01dk098656的政府资助下完成。政府拥有本发明的某些权利。
发明领域
本发明主要涉及用于加速和/或增强肝再生的方法和组合物,并且更具体地(但是非排他性地)涉及烟酰胺腺嘌呤二核苷酸(nad)前体和nad消耗抑制剂在用于在肝损伤之前或之后加速和/或增强肝再生的方法、药盒和制剂中的用途。
发明背景
肝的再生能力对于外科手术切除或者创伤或化学品诱发的损伤的恢复至关重要。在肝再生期间,烟酰胺腺嘌呤二核苷酸(nad)的浓度至少部分地由于前体的代谢竞争而下降。
发明概述
本发明通过提供nad前体和nad消耗抑制剂作为增强和加速肝再生的治疗来满足本领域的需求。
在一个方面,本发明包括用于在有需要的哺乳动物中增强肝再生的方法。方法可包括给予治疗有效量的增加烟酰胺腺嘌呤二核苷酸(nad)活性的药物。
在一些实施方案中,本发明包括用于在有需要的哺乳动物中增强肝再生的方法。方法可包括给予治疗有效量的增加烟酰胺腺嘌呤二核苷酸(nad)活性的药物和sirtuin1(sirt1)激动剂。
在一些实施方案中,增加nad活性的药物可为nad前体。例如,nad前体可包括用于合成nad的从头途径的中间体、nad补救途径的中间体和烟酰胺核苷激酶途径的中间体中的一种或多种。
在一些实施方案中,用于合成nad的从头途径的中间体可包括色氨酸、烟酸、烟酸腺嘌呤二核苷酸、烟酸单核苷酸、喹啉酸、3-羟基邻氨基苯甲酸、3-羟基犬尿氨酸、犬尿氨酸、n-甲酰基犬尿氨酸或其药学上可接受的盐。在一些实施方案中,nad补救途径的中间体可包括烟酰胺、烟酰胺单核苷酸或其药学上可接受的盐。在一些实施方案中,烟酰胺核苷激酶途径的中间体可包括烟酰胺核苷、烟酸核苷或其药学上可接受的盐。
在一些实施方案中,nad前体可包括色氨酸、烟酸、烟酸核苷、烟酰胺核苷(nr)、烟酰胺、nadp和nad本身及其药学上可接受的盐中的一种或多种。
在一些实施方案中,增加nad活性的药物可为nad消耗抑制剂。nad消耗抑制剂可为聚adp-核糖聚合酶(parp)抑制剂、cd38抑制剂及其药学上可接受的盐中的一种或多种。
另一方面,本发明可包括一种用于提供在有需要的哺乳动物中增强肝再生的方法的药盒。在一些实施方案中,药盒可包含以单位剂型存在的治疗有效量的烟酰胺腺嘌呤二核苷酸(nad)前体或nad消耗抑制剂。在一些实施方案中,药盒可包含以单位剂型存在的治疗有效量的增加烟酰胺腺嘌呤二核苷酸(nad)活性的药物和sirtuin1(sirt1)激动剂。
另一方面,本发明可包括一种用于在有需要的哺乳动物中增强肝再生的药用组合物。在一些实施方案中,组合物可包含烟酰胺腺嘌呤二核苷酸(nad)前体或nad消耗抑制剂及生理学上相容的载体介质。在一些实施方案中,组合物可包含治疗有效量的增加烟酰胺腺嘌呤二核苷酸(nad)活性的药物和sirtuin1(sirt1)激动剂及生理学上相容的载体介质。
附图简述
本发明示例性实施方案的前述概述和以下详述当结合附图阅读时可得到进一步理解,其中:
图1说明烟酰胺核苷促进肝再生。用剂量为~500mg/kg/天的烟酰胺核苷(nr)治疗10-14周龄雄性c57bl6/j小鼠。14天之后,动物经受2/3部分肝切除术并在48小时后进行分析(n=6/组)。(小图a)再生肝的显微照片。(小图b)正再生的肝中的edu掺入。插图显示nr治疗的肝的放大视图。(小图c)edu阳性肝细胞的量化。(小图d)肝体重比。(小图e)phx前后的肝nad含量。(小图f)用h&e以40x染色,显示有丝分裂图像及微囊泡和巨囊泡脂肪变化的代表性肝切片。(小图g)跨多个高倍视野的有丝分裂图像的量化。(小图h)oilredo染色以检测中性脂质。(小图i)肝切除前后nr和安慰剂/h2o治疗的小鼠的肝甘油三酯含量。误差棒表示s.e.m。*,p0.05;**,p0.01;***,p0.001。
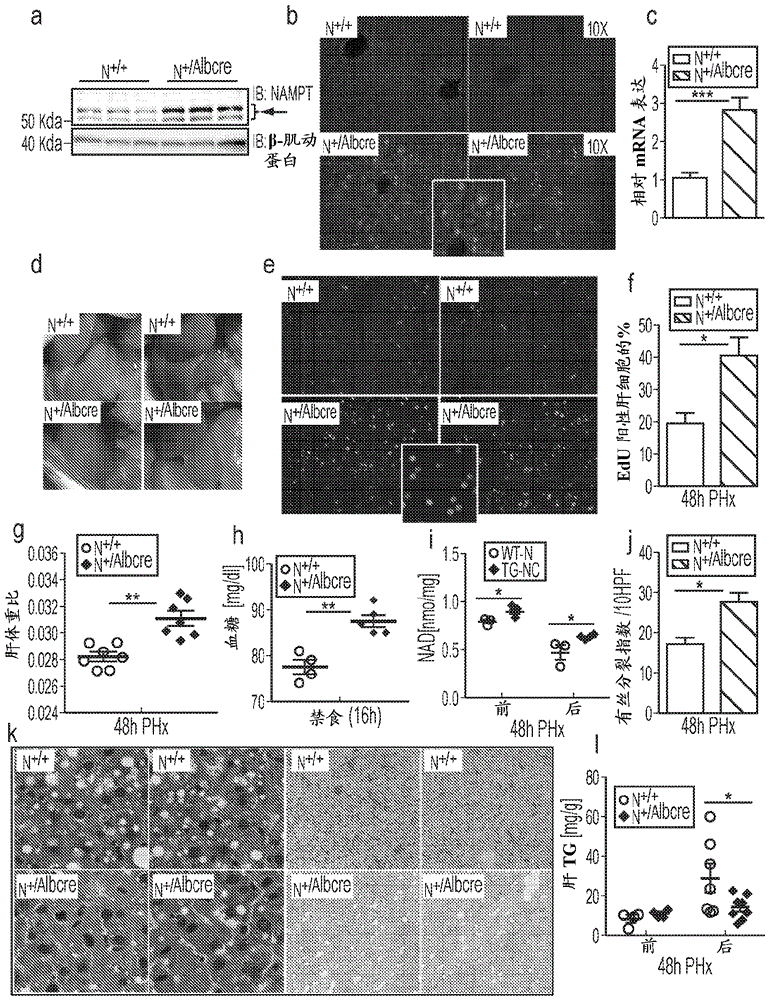
图2说明nampt的肝细胞特异性过度表达促进肝再生。除了alb-cre外携带nampt的cre诱导型等位基因的小鼠(表示为n+/albcre)和同窝对照(n+/+)经受2/3部分肝切除术并在48小时后进行分析。(小图a)肝中的nampt蛋白和mrna表达。(小图b)显示n+/albcre小鼠的门静脉周围和中央静脉周围区域的nampt过度表达的免疫荧光。插图显示n+/albcre的放大视图。(小图c)肝中nampt的mrna表达。(小图d)正再生的肝的显微照片。(小图e)通过经免疫荧光检测的edu鉴定(测定中表示为绿色)并用dapi复染(测定中表示为蓝色)的正增殖的肝细胞。插图显示n+/albcre的放大视图。(小图f)edu阳性肝细胞的量化(n=5/组)。(小图g)肝体重比。(小图h)空腹血糖。(小图i)phx前后的肝nad含量。(小图j和k)通过在高倍率下计数h&e染色切片中的肝细胞中的有丝分裂图像测定的有丝分裂指数。显示用h&e染色的代表性肝切片。(小图l)通过oilredo和肝甘油三酯测定法测定的肝脂质含量。误差棒表示s.e.m。*,p0.05;**,p0.01;***,p0.001。
图3说明成年发生的nampt过度表达对于再生表型是足够的。携带nampt的cre诱导型等位基因的小鼠用aav-cre感染(表示为naavcre)和同窝对照(naavgfp或wtaavcre)经受2/3部分肝切除术并在36小时后进行分析。(小图a)显示naavcre小鼠的门静脉周围和中央静脉周围区域的nampt过度表达的免疫荧光。插图显示naavcre的放大视图。(小图b)空腹血糖。(小图c)正再生的肝的显微照片。(小图d)通过经免疫荧光检测的edu鉴定(测定中表示为绿色)并用dapi复染(测定中表示为蓝色)的正增殖的肝细胞。插图显示naavcre的放大视图。(小图e)edu阳性肝细胞的量化(n=5/组)。(小图f)肝体重比。(小图g)肝甘油三酯含量。(小图h)右图:用h&e染色的代表性肝切片。左图:根据oilredo的脂质聚集。误差棒表示s.e.m。*,p0.05;**,p0.01;***,p0.001。
图4说明肝细胞特异性的nampt丧失损害再生,并通过nr挽救。通过用表达cre重组酶的aav(aav-cre)注射携带两个floxed等位基因的动物来产生肝细胞特异性的nampt缺陷小鼠。感染aav-gfp的同窝小鼠用作对照。在感染之后5天和phx前2周开始用nr(~500mg/kg/天)治疗。在phx之后48小时实施分析。(小图a和b)肝中的nampt蛋白和mrna表达。(小图c)正再生的肝的显微照片。(小图d)通过经免疫荧光检测的edu鉴定(测定中表示为红色)并用dapi复染(测定中表示为蓝色)的正增殖的肝细胞。(小图e)edu阳性肝细胞的量化(n=5-6/组)。(小图f)肝体重比。(小图g)phx前后的肝nad含量。(小图h)通过在高倍率下计数h&e染色切片中的肝细胞中的有丝分裂图像测定的有丝分裂指数(n=5-6/组)。(小图i)用h&e(左图)和oilredo(右图)染色的代表性肝切片。(小图j)肝甘油三酯含量。误差棒表示s.e.m。*,p0.05;**,p0.01;***,p0.001。
图5说明肝细胞增殖与肝nad浓度呈强的相关性,并且与肝脂质含量呈反向关系。绘制来自个体动物的数据以研究nad、脂质代谢和肝细胞增殖之间的相关性。(小图a)nad浓度与肝细胞增殖之间呈正相关。(小图b)肝细胞增殖与甘油三酯含量之间呈反相关。(小图c)在nr治疗的小鼠的肝切除术之前或之后评价的肝atp含量(n=6/组)。(小图d和e)肝atp含量与nad和肝细胞增殖之间呈正相关。(小图f)建议的nad介导的再生模型。
图6说明肝细胞特异性的sirt1缺失损害再生并且通过nr部分挽救,如(小图a)用nr治疗的肝切片进行的sirt1敲除研究和(小图b)在来自sirt1敲除小鼠的受损肝中用nr进行的肝再生研究所示。
发明详述
肝为少数能够在哺乳动物中显著再生的结构之一,并且可从不到其初始质量的30%完全再生长。这种再生能力对于在比如创伤性损伤、接触肝毒素或感染性物质或外科手术切除等状况下的生存至关重要。肝功能的恢复高度依赖于增加恢复肝质量所必要的能量产生。然而,对于肝对急性和慢性损伤作出反应重要的机制和决定肝再生能力的生物途径尚未充分了解。因此,可加速肝损伤患者恢复正常肝功能的再生过程和速度的治疗方法备受关注。
鉴于上述情况,本发明提供用于在有需要的哺乳动物中增强肝再生和治疗肝疾病、障碍或损伤的方法、药盒和药用组合物。在一些实施方案中,方法、药盒和药用组合物可包括为烟酰胺腺嘌呤二核苷酸(nad)前体和/或nad消耗抑制剂的药物。
本文使用的“烟酰胺腺嘌呤二核苷酸(nad)前体”为导致nad增加的任何小分子。小分子可以还原或非还原形式存在。
本文使用的“nad消耗抑制剂”为引起nad可用性增加的抑制剂。nad可用性包括细胞或组织中的总nad增加或感兴趣的酶可用的nad量的增加。
发明的方法
在一个方面包括一种再生肝的方法。在一些实施方案中,提供一种治疗肝疾病、障碍或损伤的方法。在每种情况下,方法包括增加烟酰胺腺嘌呤二核苷酸(nad)。
增加nad。按照本发明,nad活性和/或含量可通过给予一种或多种药物来增加,所述药物(1)为烟酰胺腺嘌呤二核苷酸(nad)前体;和/或(2)起nad消耗抑制剂的作用。
在一些实施方案中,nad活性可通过给予nad或nadh以及通过合成nad来增加。nad可通过3种主要途径合成,即其中nad从色氨酸合成的从头途径、其中nad通过再循环降解的nad产物比如烟酰胺产生的nad补救途径,和其中烟酰胺核苷通过烟酰胺核苷激酶转化为烟酰胺单核苷酸的烟酰胺核苷激酶途径。因此,本发明的nad前体可包括用于合成nad的从头途径的中间体、nad补救途径的中间体和烟酰胺核苷激酶途径的中间体中的一种或多种。
在一些实施方案中,其中nad前体包括用于合成nad的从头途径的中间体,这种中间体可包括(非限制性地)色氨酸、烟酸、烟酸腺嘌呤二核苷酸、烟酸单核苷酸、喹啉酸、3-羟基邻氨基苯甲酸、3-羟基犬尿氨酸、犬尿氨酸、n-甲酰基犬尿氨酸或其药学上可接受的盐。
在其中nad前体包括烟酰胺核苷激酶途径的中间体的一些实施方案中,这种中间体可包括(非限制性地)烟酰胺、烟酰胺单核苷酸或其药学上可接受的盐。
在其中nad前体包括烟酰胺核苷激酶途径的中间体的一些实施方案中,这种中间体可包括(非限制性地)烟酰胺核苷、烟酸核苷或其药学上可接受的盐。
在一些实施方案中,nad前体可选自色氨酸、烟酸、烟酸核苷、烟酰胺核苷(nr)、烟酰胺、nadp和nad本身及其药学上可接受的盐。
在一些实施方案中,方法可包括给予nad消耗抑制剂。nad消耗抑制剂可包括聚adp-核糖聚合酶(parp)抑制剂、cd38抑制剂及其药学上可接受的盐中的一种或多种。在一些实施方案中,parp抑制剂可包括(但不限于)碘硝基香豆素、5-碘-6-硝基香豆素、3,4-二氢-5-甲基异喹啉酮、4-氨基-1,8-萘二甲酰亚胺、3-甲氧基苯甲酰胺、8-羟基-2-甲基-3-氢-喹唑啉-4-酮、3-(4-氯苯基)-喹喔啉-5-甲酰胺、2-(3'-甲氧基苯基)苯并咪唑-4-甲酰胺、苯甲酰胺、3-氨基苯甲酰胺、3-氨基邻苯二甲酰肼和1,5-二羟基异喹啉及其药学上可接受的盐中的一种或多种。
术语“药学上可接受的盐”指的是衍生自本领域已知的各种有机和无机反离子的盐。药学上可接受的酸加成盐可用无机酸和有机酸形成。可衍生盐的某些无机酸包括例如盐酸、氢溴酸、硫酸、硝酸和磷酸。可衍生盐的某些有机酸包括例如乙酸、丙酸、乙醇酸、丙酮酸、草酸、马来酸、丙二酸、琥珀酸、富马酸、酒石酸、枸橼酸、苯甲酸、肉桂酸、扁桃酸、甲磺酸、乙磺酸、对甲苯磺酸和水杨酸。药学上可接受的碱加成盐可用无机和有机碱形成。可衍生盐的无机碱包括例如钠、钾、锂、铵、钙、镁、铁、锌、铜、锰和铝。可衍生盐的有机碱包括例如伯、仲和叔胺、取代的胺(包括天然存在的取代的胺)、环胺和碱性离子交换树脂。具体实例包括异丙胺、三甲胺、二乙胺、三乙胺、三丙胺和乙醇胺。药学上可接受的碱加成盐选自铵、钾、钠、钙和镁盐。
sirt1激活。肝再生可通过组合增加nad活性的药物与增加sirt1活性的药物来增强。在一些实施方案中,本发明包括通过给予治疗有效量的增加烟酰胺腺嘌呤二核苷酸(nad)活性的药物和sirt1激动剂,用于在有需要的哺乳动物中增强肝再生的方法。因此,治疗有效量的增加烟酰胺腺嘌呤二核苷酸(nad)活性的药物和sirt1激动剂可共同给予有需要的患者。
本文使用的术语“共同给予”、“共同给予”、“与...组合给予”、“与...组合给予”、“同时”和“同时”包括给予受试者两种或更多种活性药用成分(在本发明的一个优选实施方案中,例如至少一种增加nad活性的药物和至少一种增加sirt1活性的药物),使得两种活性药用成分和/或其代谢物同时存在于受试者体内。共同给予包括以单独的组合物同时给予、以单独的组合物在不同时间给予或以其中存在两种或更多种活性药用成分的组合物给予。以单独的组合物同时给予和以其中存在两种药物的组合物给予为优选的。
本文使用的术语“激动剂”指的是增加蛋白或分子的生物活性的化合物或分子药物。例如,“sirt1”激动剂增加sirt1的生物活性。激动剂可刺激sirt1蛋白的酶活性,或者其可通过增加转录和/或翻译而导致增加sirt1的表达。sirt1激动剂的实例为已知的,并可包括例如小分子、激活抗体、蛋白(例如酶促共激活剂)和上游效应信号。激动剂可直接或间接通过其他效应分子激活sirt1活性。sirt1激动剂(即增加sirt1活性的药物)的实例包括例如白藜芦醇、srt2104(gsk2245840)、srt1460、紫铆因、非瑟酮、异烟酰胺(isonam)、白皮杉醇和槲皮素。在一些实施方案中,sirt1激动剂选自白藜芦醇、srt2104、srt1460及其组合。这种化合物的结构如下:
sirt1激动剂的实例进一步提供和描述于bonkowski等人,naturereviews(2016)17:679-690;美国专利申请公开第2011/0015192和2013/0338178号及美国专利第7829556和8247565号中,其全部内容通过参照结合于此。
肝疾病、障碍或损伤。本发明的方法在有需要的哺乳动物中增强肝再生。本发明的方法可包括给予治疗有效量的本文描述的一种或多种药物(例如至少一种增加nad活性的药物和/或至少一种增加sirt1活性的药物)。方法可包括当哺乳动物患有肝损伤时给予治疗有效量的药物。方法也可包括在肝损伤之前和/或肝损伤之后给予治疗有效量的药物。
本文使用的“肝再生”指的是现有肝细胞的复制或现有肝细胞功能的改善。
本文使用的术语“肝损伤”可涉及可包括创伤性肝损伤(例如由创伤性事件或事故引起的肝损害)、外科肝切除(例如实施以去除肝的选定部分的外科手术)、肝硬化、肝纤维化、肝感染、肝移植、胆管损伤引起的肝损害和化学品诱发性肝损伤的肝损害。化学品诱发性肝损伤可包括由肝毒性化学品引起的肝损害或者一种或多种化学品导致肝中毒的结果。例如,化学品诱发性肝损伤可包括由对乙酰氨基酚和乙醇或其代谢副产物引起的肝损害。
给予本发明的药物可通过本领域技术人员已知的任何手段完成。用于实践本发明方法的药物可以足以在其接受者中引起期望的治疗效果的量给予。因此,本文使用的术语“治疗有效量”指的是一种或多种药物的量,其(1)与在没有这种量的一种或多种药物的情况下处于类似状态的哺乳动物相比足以增强或以其他方式加速哺乳动物的肝再生;和/或(2)足以实现可检测的治疗、预防或改善效果。治疗有效量可依预期应用(体外或体内)或所治疗的患者和疾病状况(例如患者的体重、年龄和性别)、疾病状况的严重程度、给予方式等而变化,这可由本领域的普通技术人员容易地确定。该术语也适用于将在靶细胞、组织或蛋白中引起特定反应的剂量。具体剂量将依所选定的特定化合物、要遵循的给药方案、化合物是否与其他化合物组合给予、给予时机、所给予的组织及携带化合物的物理递送系统而变化。
本文使用的术语“给予”、“给予”或“给予”指的是(1)由健康从业者或其授权代理人或在他或她的指导下根据本公开提供、给予、给药和/或开具处方;和/或(2)根据本公开投入哺乳动物、被哺乳动物摄取或消耗。
本文使用的术语“治疗”、“治疗”和/或“治疗”可涉及意图治愈、改善、稳定、预防或控制疾病、障碍或病理状况(例如肝损伤)的疾病、障碍、损伤或病理状况(例如肝损伤)的管理。如本文所述,治疗也可包括在肝损伤之前或之后增强哺乳动物肝再生的干预。
在一些实施方案中,本发明的方法可包括在肝损伤之前约6个月、或约5个月、或约4个月、或约3个月、或约2个月、或约1个月、或约3周、或约2周、或约1周、或约6天、或约5天、或约4天、或约3天、或约2天、或约1天、或约1-23小时给予治疗有效量的药物。
在一些实施方案中,本发明的方法可包括在肝损伤之后约1-23小时、或约1天、或约2天、或约3天、或约4天、或约5天、或约6天、或约1周、或约2周、或约3周、或约1个月、或约2个月、或约3个月、或约4个月、或约5个月、或约6个月给予治疗有效量的药物。
在一些实施方案中,本发明的方法可包括基于每小时基础或基于每天基础(例如每天一次、每天两次、每天三次等)或基于每周基础(例如每周一次、每周两次、每周三次等)或基于每月基础给予哺乳动物治疗有效量的药物。
在一些实施方案中,本发明的方法可包括根据一种或多种给予途径给予哺乳动物治疗有效量的药物。在某些实施方案中,给予途径可选自颊、牙齿、宫颈内、肌内、吸入、颅内、淋巴管内、眼内、腹膜内、胸膜内、鞘内、气管内、子宫内、血管内、静脉内、膀胱内、鼻内、眼、口服、耳、胆灌注、心脏灌注、牙周、直肠、脊柱、皮下、舌下、局部、阴道内、透皮、输尿管、尿道及其组合。在选定的实施方案中,给予途径为口服。在一些实施方案中,例如给予哺乳动物治疗有效量的药物可包括通过在哺乳动物的食物和/或饮用水中放置药物而在哺乳动物的饮食中包含药物。
在一些实施方案中,本发明的方法可包括以选自以下的剂型给予哺乳动物治疗有效量的药物:大丸剂、气雾剂、计量气雾剂、咀嚼棒、胶囊剂、含有包衣小丸的胶囊剂、含有延迟释放小丸的胶囊剂、含有延长释放小丸的胶囊剂、浓缩物、乳膏、强化乳膏、栓剂乳膏、圆片(disc)、敷料、酏剂、乳剂、灌肠剂、延长释放纤维、延长释放薄膜、气体、凝胶、计量凝胶、颗粒剂、延迟释放颗粒剂、泡腾颗粒剂、口香糖、植入物、吸入剂、注射剂、可注射脂质复合物,可注射脂质体、插入物、延长释放插入物、宫内节育器、果冻、液体、延长释放液体、洗剂、强化洗剂、洗发水、油剂、软膏剂、强化软膏剂、糊剂、软锭剂、小丸剂、粉剂、皂液、脂膏溶液剂、溶液剂/滴剂、浓缩液、形成凝胶的溶液剂/滴剂、海绵、喷雾剂、计量喷雾剂、栓剂、混悬剂、混悬剂/滴剂、延长释放混悬剂、药签、糖浆剂、片剂、咀嚼片、含有包衣颗粒的片剂、延迟释放片、分散片、泡腾片、延长释放片、口腔崩解片、卫生棉条、带和糖锭/锭剂。
在一些实施方案中,本发明的方法可包括以按重量计等于或小于10g/kg、9.5g/kg、9.0g/kg、8.5g/kg、8.0g/kg、7.5g/kg、7.0g/kg、6.5g/kg、6.0g/kg、5.5g/kg、5.0g/kg、4.5g/kg、4.0g/kg、3.5g/kg、3.0g/kg、2.5g/kg、2.0g/kg、1.5g/kg、1.0g/kg、0.95g/kg、0.9g/kg、0.85g/kg、0.8g/kg、0.75g/kg、0.7g/kg、0.65g/kg、0.6g/kg、0.55g/kg、0.5g/kg、0.45g/kg、0.4g/kg、0.35g/kg、0.3g/kg、0.25g/kg、0.2g/kg、0.15g/kg、0.1g/kg、0.09g/kg、0.08g/kg、0.07g/kg、0.06g/kg、0.05g/kg、0.04g/kg、0.03g/kg、0.02g/kg、0.01g/kg、0.009g/kg、0.008g/kg、0.007g/kg、0.006g/kg、0.005g/kg、0.004g/kg、0.003g/kg、0.002g/kg、0.001g/kg、0.0009g/kg、0.0008g/kg、0.0007g/kg、0.0006g/kg、0.0005g/kg、0.0004g/kg、0.0003g/kg、0.0002g/kg或0.0001g/kg的剂量给予哺乳动物治疗有效量的药物,其中“g/kg”应理解为意指单位哺乳动物重量(kg)的药物重量(g)。
在一些实施方案中,本发明的方法可包括以按重量计大于0.0001g/kg、0.0002g/kg、0.0003g/kg、0.0004g/kg、0.0005g/kg、0.0006g/kg、0.0007g/kg、0.0008g/kg、0.0009g/kg、0.001g/kg、0.0015g/kg、0.002g/kg、0.0025g/kg、0.003g/kg、0.0035g/kg、0.004g/kg、0.0045g/kg、0.005g/kg、0.0055g/kg、0.006g/kg、0.0065g/kg、0.007g/kg、0.0075g/kg、0.008g/kg、0.0085g/kg、0.009g/kg、0.0095g/kg、0.01g/kg、0.015g/kg、0.02g/kg、0.025g/kg、0.03g/kg、0.035g/kg、0.04g/kg、0.045g/kg、0.05g/kg、0.055g/kg、0.06g/kg、0.065g/kg、0.07g/kg、0.075g/kg、0.08g/kg、0.085g/kg、0.09g/kg、0.095g/kg、0.1g/kg、0.15g/kg、0.2g/kg、0.25g/kg、0.3g/kg、0.35g/kg、0.4g/kg、0.45g/kg、0.5g/kg、0.55g/kg、0.6g/kg、0.65g/kg、0.7g/kg、0.75g/kg、0.8g/kg、0.85g/kg、0.9g/kg、0.95g/kg、1g/kg、1.5g/kg、2g/kg、2.5g/kg、3g/kg、3.5g/kg、4g/kg、4.5g/kg、5g/kg、5.5g/kg、6g/kg、6.5g/kg、7g/kg、7.5g/kg、8g/kg、8.5g/kg、9g/kg、9.5g/kg或10g/kg的剂量给予哺乳动物治疗有效量的药物,其中“g/kg”应理解为意指单位哺乳动物重量(kg)的药物重量(g)。
发明的药盒
按照本发明的前述方法,可提供一种药盒,其可包含以单位剂型存在的一种或多种药物(例如至少一种增加nad活性的药物和/或至少一种增加sirt1活性的药物)。本发明的药盒可用于本文描述的方法。在一些实施方案中,药盒可包含用于根据本发明方法使用药物的说明书。
发明的药用组合物
在一些实施方案中,本发明包括一种用于在有需要的哺乳动物中增强肝再生的药用组合物。在某些实施方案中,药用组合物可包含一种或多种药物(例如至少一种增加nad活性的药物和/或至少一种增加sirt1活性的药物)和生理学上相容的载体介质。
在一些实施方案中,本发明药用组合物中提供的任何药物的浓度例如小于药用组合物的100%、90%、80%、70%、60%、50%、40%、30%、20%、19%、18%、17%、16%、15%、14%、13%、12%、11%、10%、9%、8%、7%、6%、5%、4%、3%、2%、1%、0.5%、0.4%、0.3%、0.2%、0.1%、0.09%、0.08%、0.07%、0.06%、0.05%、0.04%、0.03%、0.02%、0.01%、0.009%、0.008%、0.007%、0.006%、0.005%、0.004%、0.003%、0.002%、0.001%、0.0009%、0.0008%、0.0007%、0.0006%、0.0005%、0.0004%、0.0003%、0.0002%或0.0001%w/w、w/v或v/v。
在一些实施方案中,本发明药用组合物中提供的任何药物的浓度大于药用组合物的90%、80%、70%、60%、50%、40%、30%、20%、19.75%、19.50%、19.25%、19%、18.75%、18.50%、18.25%、18%、17.75%、17.50%、17.25%、17%、16.75%、16.50%、16.25%、16%、15.75%、15.50%、15.25%、15%、14.75%、14.50%、14.25%、14%、13.75%、13.50%、13.25%、13%、12.75%、12.50%、12.25%、12%、11.75%、11.50%、11.25%、11%、10.75%、10.50%、10.25%、10%、9.75%、9.50%、9.25%、9%、8.75%、8.50%、8.25%、8%、7.75%、7.50%、7.25%、7%、6.75%、6.50%、6.25%、6%、5.75%、5.50%、5.25%、5%、4.75%、4.50%、4.25%、4%、3.75%、3.50%、3.25%、3%、2.75%、2.50%、2.25%、2%、1.75%、1.50%、1.25%、1%、0.5%、0.4%、0.3%、0.2%、0.1%、0.09%、0.08%、0.07%、0.06%、0.05%、0.04%、0.03%、0.02%、0.01%、0.009%、0.008%、0.007%、0.006%、0.005%、0.004%、0.003%、0.002%、0.001%、0.0009%、0.0008%、0.0007%、0.0006%、0.0005%、0.0004%、0.0003%、0.0002%或0.0001%w/w、w/v或v/v。
在一些实施方案中,药用组合物中任何药物的浓度在药用组合物的约0.0001%-约50%、约0.001%-约40%、约0.01%-约30%、约0.02%-约29%、约0.03%-约28%、约0.04%-约27%、约0.05%-约26%、约0.06%-约25%、约0.07%-约24%、约0.08%-约23%、约0.09%-约22%、约0.1%-约21%、约0.2%-约20%、约0.3%-约19%、约0.4%-约18%、约0.5%-约17%、约0.6%-约16%、约0.7%-约15%、约0.8%-约14%、约0.9%-约12%或约1%-约10%w/w、w/v或v/v的范围内。
在一些实施方案中,药用组合物中提供的任何药物的浓度在药用组合物的约0.001%-约10%、约0.01%-约5%、约0.02%-约4.5%、约0.03%-约4%、约0.04%-约3.5%、约0.05%-约3%、约0.06%-约2.5%、约0.07%-约2%、约0.08%-约1.5%、约0.09%-约1%、约0.1%-约0.9%w/w、w/v或v/v的范围内。
在一些实施方案中,药用组合物中提供的任何药物的量等于或少于10g、9.5g、9.0g、8.5g、8.0g、7.5g、7.0g、6.5g、6.0g、5.5g、5.0g、4.5g、4.0g、3.5g、3.0g、2.5g、2.0g、1.5g、1.0g、0.95g、0.9g、0.85g、0.8g、0.75g、0.7g、0.65g、0.6g、0.55g、0.5g、0.45g、0.4g、0.35g、0.3g、0.25g、0.2g、0.15g、0.1g、0.09g、0.08g、0.07g、0.06g、0.05g、0.04g、0.03g、0.02g、0.01g、0.009g、0.008g、0.007g、0.006g、0.005g、0.004g、0.003g、0.002g、0.001g、0.0009g、0.0008g、0.0007g、0.0006g、0.0005g、0.0004g、0.0003g、0.0002g或0.0001g。
在一些实施方案中,药用组合物中提供的药物的量大于0.0001g、0.0002g、0.0003g、0.0004g、0.0005g、0.0006g、0.0007g、0.0008g、0.0009g、0.001g、0.0015g、0.002g、0.0025g、0.003g、0.0035g、0.004g、0.0045g、0.005g、0.0055g、0.006g、0.0065g、0.007g、0.0075g、0.008g、0.0085g、0.009g、0.0095g、0.01g、0.015g、0.02g、0.025g、0.03g、0.035g、0.04g、0.045g、0.05g、0.055g、0.06g、0.065g、0.07g、0.075g、0.08g、0.085g、0.09g、0.095g、0.1g、0.15g、0.2g、0.25g、0.3g、0.35g、0.4g、0.45g、0.5g、0.55g、0.6g、0.65g、0.7g、0.75g、0.8g、0.85g、0.9g、0.95g、1g、1.5g、2g、2.5、3g、3.5、4g、4.5g、5g、5.5g、6g、6.5g、7g、7.5g、8g、8.5g、9g、9.5g或10g。
本发明的药物在广泛的剂量范围内有效。例如,在某些哺乳动物的治疗中,独立地在每天0.001-100g、0.01-75g、0.1-50g和1-50g范围内的剂量为可使用的剂量的实例。或者,在某些哺乳动物的治疗中,独立地在每天0.01-1000mg、0.5-500mg和1-50mg范围内的剂量为可使用的剂量的实例。准确的剂量取决于给予途径、给予药物的形式、待治疗哺乳动物的性别和年龄、待治疗受试者的体重及主治医师的偏好和经验。
本文使用的术语“生理学上相容的载体介质”包括适用于期望的特定剂型的任何和所有溶剂、稀释剂或其他液体媒介物、分散或悬浮助剂、表面活性剂、等渗剂、增稠或乳化剂、防腐剂、固体粘合剂、润滑剂、填充剂等。remington:thescienceandpracticeofpharmacy,第20版,a.r.genaro等人,part5,pharmaceuticalmanufacturing,pp.669-1015(lippincottwilliams&wilkins,baltimore,md/philadelphia,pa)(2000)公开了用于配制药用组合物的各种载体和用于其制备的已知技术。除非是任何常规药用载体介质与本发明中使用的任何一种药物不相容,比如由于产生不期望的生物效应或者另外地以有害方式与包含这种化合物或药物的制剂的任何其他组分相互作用,否则考虑其用途处于本发明的范围内。在某些实施方案中,生理学上相容的载体介质可为水。
在一些实施方案中,药用组合物可以单位剂型制备。在某些实施方案中,单位剂型可包括生理学上相容的载体介质,并可选自大丸剂、气雾剂、计量气雾剂、咀嚼棒、胶囊剂、含有包衣小丸的胶囊剂、含有延迟释放小丸的胶囊剂、含有延长释放小丸的胶囊剂、浓缩物、乳膏、强化乳膏、栓剂乳膏、圆片、敷料、酏剂、乳剂、灌肠剂、延长释放纤维、延长释放薄膜、气体、凝胶、计量凝胶、颗粒剂、延迟释放颗粒剂、泡腾颗粒剂、口香糖、植入物、吸入剂、注射剂、可注射脂质复合物,可注射脂质体、插入物、延长释放插入物、宫内节育器、果冻、液体、延长释放液体、洗剂、强化洗剂、洗发水、油剂、软膏剂、强化软膏剂、糊剂、软锭剂、小丸剂、粉剂、皂液、脂膏溶液剂、溶液剂/滴剂、浓缩液、形成凝胶的溶液剂/滴剂、海绵、喷雾剂、计量喷雾剂、栓剂、混悬剂、混悬剂/滴剂、延长释放混悬剂、药签、糖浆剂、片剂、咀嚼片、含有包衣颗粒的片剂、延迟释放片、分散片、泡腾片、延长释放片、口腔崩解片、卫生棉条、带和糖锭/锭剂。
本发明的方法、药盒和药用组合物可用于治疗哺乳动物。这种哺乳动物包括人以及非人哺乳动物。非人哺乳动物包括例如伴侣动物比如狗和猫、农业动物比如牲畜(包括牛、马等)及外来动物比如动物园动物。然而,在某些实施方案中,哺乳动物为人。
本发明证实补充的nad前体可改善肝损伤实验模型的结果。然而,部分肝切除术的恢复也可受到肝细胞中nampt表达水平的影响,并且一些缺乏nampt的哺乳动物中差的再生通过烟酰胺核苷完全挽救。
短暂肝脂肪变性为肝再生的一个特有的特征。在其他实验设置中,已表明nampt经nad合成赋予肝脂肪变性抗性。这些发现与当前的观察结果非常一致,当前的发现结果为,在给予nr或在肝细胞中过度表达nampt的小鼠中phx之后48小时几乎完全没有脂肪变性。在phx后36小时,在nr治疗的小鼠中可见一些脂肪变性,这表明在存在增强的nad合成的情况下脂质在再生期间仍然聚集,但更快被清除的可能性。这与其中通过以nad敏感方式再生肝来处理脂质以提供能量来源,同时保留葡萄糖以输出到血流中或用作代谢前体的模型一致。在没有足够nad浓度的情况下,脂质氧化和因此atp水平会下降,从而阻止细胞增殖。
不限于本发明的任何一种理论,尽管增加nad可用性可能仅通过其作为直接参与atp产生的酶的辅因子的作用和/或通过保留核酸合成的前体来改善再生,但其也可经其作为信号传导酶(包括sirtuin)的辅底物的作用起作用。在这方面,已知nampt会影响sirtuin1(sirt1)的去乙酰化酶活性。最近的研究表明,sirt1在肝脂质代谢和肝再生两方面都有作用。肝再生受损的老年小鼠表达低的肝sirt1,并且异位表达sirt1恢复肝细胞增殖以响应老年小鼠的部分肝切除术,而敲减sirt1损害年幼小鼠的再生。相比之下,由于胆汁酸调节的缺陷,过度表达sirt1的年幼小鼠在部分肝切除术后死亡率增加。nampt表达降低未损伤肝中的肝细胞甘油三酯水平,并且该效应与sirt1活性增加相关及通过过度表达sirt1进行表型模拟。因此,并且不限于本发明的任何一种理论,我们对nad再生增强观察到的脂肪变性减少可能反映了对脂质代谢的sirt1依赖性作用。另外,白藜芦醇为一种激活sirt1的小多酚,已显示改善损伤模型中的肝细胞存活,而且减慢复制。
总之,本发明证实可调节nad代谢以促进肝损伤的恢复。
以下实施例更详细描述本发明。提供这些实施例仅用于说明目的,并且绝不应认为是限制本发明。
实施例
为了直接测试nad可用性是否限制肝再生,在饮用水中给予nad前体烟酰胺核苷(nr)的小鼠中实施了部分肝切除术(一种确立的肝损伤模型)。为了探测nad代谢更特异性地在肝细胞中的作用,遗传策略被用于过度表达烟酰胺磷酸核糖转移酶(nampt)或使其缺失,其为一种nad生物合成的限速酶。结果证实nad可用性确实限制肝再生,并且表明增加肝nad含量的策略对于肝损伤或毒性损害可为保护性的。
动物、圈养和药物治疗:通过将携带caggs启动子被floxed终止盒分开的namptcdna的外源拷贝的动物(其回交于c57bl/6j背景(如前所述7))与携带白蛋白-cre的小鼠(jax品系b6.cg-tg(alb-cre)21mgn/j,库存编号003574)杂交,来获得在肝细胞中过度表达nampt的小鼠。缺乏白蛋白-cre的同窝小鼠用作对照。为了研究nampt过度表达的成年发生,8-9周龄的雄性namptfl/fl和namptwt/wt小鼠在眼眶后丛注射腺相关病毒,其在甲状腺素结合球蛋白(tbg)启动子(aav-cre)的控制下表达cre重组酶(aav-cre)或增强型绿色荧光蛋白(aav-gfp)。注射aav-gfp的namptfl/fl小鼠和注射aav-cre的namptwt/wt用作对照。对于nampt的诱导型缺失,采用最初由universitédeliège的oberdanleo创建并回交于c57/bl6背景的小鼠,其由washingtonuniversity的shin-ichiroimai慷慨提供。如上所述,携带两个floxed等位基因的8-9周龄雄性小鼠在眼眶后注射腺相关病毒,其在甲状腺素结合球蛋白(tbg)启动子的控制下表达cre重组酶(aav-cre)或增强型绿色荧光蛋白(aav-gfp)。在成年发生的过度表达和肝特异性敲除组两者中测量空腹血糖,并在aav感染之后>14天实施部分肝切除术。将动物以12小时光-暗循环在无病原体的屏障设施中以4-5只小鼠/笼分组圈养,可自由获取食物和水。对于仅含有野生型动物的实验,直接从jacksonlabs订购雄性c57bl/6j小鼠。对于烟酰胺核苷(nr)(chromadexinc.)补充实验,nr在防光瓶中以3.0mg/ml溶解于饮用水中,并且每3天更换一次。对于禁食和再喂养实验,将动物禁食16小时,在含有alpha-dri寝具的笼中随意获取水。在universityofpennsylvaniainstitutionalanimalcareandusecommittee的批准下,所有动物工作按照u.s.departmentofhealthandhumanservicesguideforthecareanduseoflaboratoryanimals实施。
部分肝切除术:10-14周龄的雄性转基因小鼠根据mitchell和willenbring的方案在上午8点到中午之间经历了部分肝切除术(phx)。简而言之,在异氟烷麻醉之后,进行腹侧中线切开。然后通过蒂结扎切除占70%肝的中叶和左侧叶。对于edu(5-乙炔基-2'-脱氧尿苷)标记(molecularprobes),在处死之前5小时,以16mg/kg的剂量给小鼠腹膜内注射标记试剂。如所表明的那样,在phx之后36小时或48小时处死动物。切除的和正再生的肝在液氮中快速冷冻,固定在4%多聚甲醛中,包埋在oct介质(tissue-teko.c.t化合物,sakura)中,或在液氮中以预先冷却的金属夹快速冷冻,用于nad和atp测定。涉及小鼠的所有外科手术程序均由institutionalanimalcareandusecommitteeprotocolsoftheuniversityofpennsylvania批准。
组织学、免疫组织化学和免疫荧光:在苏木精和伊红染色的载玻片上计数有丝分裂图像。将石蜡包埋的5μm厚的肝切片在二甲苯中脱石蜡,随后通过分级乙醇系列再水化,用gill3苏木精(thermoscientific)和伊红(sigma)染色。首先在较低放大倍率下筛选有丝分裂活性区域。为了量化,考虑了大多数有丝分裂活性区域中10个高倍视野(40x)的总有丝分裂计数。使用外加数字图像采集系统的光学显微镜以400x放大倍率拍摄代表性的显微照片。对于石蜡切片中nampt表达的免疫荧光检测,在r缓冲液(electronmicroscopysciencesct#62706-10)中回收抗原,随后在cas-block(invitrogen00-8120)中猝灭和封闭20分钟。然后将载玻片在含有一次兔多克隆抗nampt抗体(bethyllaboratories,稀释度1:1000)的加湿室中于4℃下孵育过夜。山羊抗兔igg(alexafluor488)以稀释度1:600用作二次抗体,并且载玻片用dapi(vectorlaboratories)进行复染。为了量化,细胞使用zeissaxioplan2成像系统在20x物镜下进行检查和成像,同时取中央静脉和门静脉区域。
edu染色:根据制造商的方案,使用click-itedualexafluor488或alexafluor594成像试剂盒(molecularprobes)对石蜡包埋的肝切片进行edu染色,并对每个肝的5-6个随机区域进行成像。通过在中央静脉和肝门三元体区域以200x手动计数并将dapi复染标准化,来确定edu阳性肝细胞的分数。
oilredo染色:将在oct中冷冻的肝样品以5μm厚度切片,并固定在10%中性缓冲福尔马林中。将载玻片置于丙二醇(sigma)中2分钟,然后在oilredo(sigma)中于60℃下孵育10分钟。然后将载玻片转移至85%丙二醇溶液中持续1分钟,并用苏木精(fisherscientific)复染。使用外加数字图像采集系统的nikone600明视野显微镜以200x放大倍率捕获代表性图像。
免疫印迹:对于蛋白印迹分析,将快速冷冻的肝块在组织裂解器(qiagen)中,于补充有halt磷酸酶抑制剂(thermoscientific)和完全蛋白酶抑制剂(roche)的ripa缓冲液中裂解。组织裂解物通过在4℃下以15000g离心15分钟预澄清。变性之后,将样品在4-15%sds-page凝胶上解析,在湿转移装置(bio-rad)上转移至pvdf膜(milipore)上,并使用抗nampt(bethyllaboratories,pbef(a300-372a),稀释度1:5000)和hrp缀合的β-肌动蛋白(abcam,ab49900)抗体进行探测。通过化学发光检测免疫反应性蛋白。使用supersignalwestfemto底物(pierce)在bio-rad成像站中捕获图像。
基因表达分析:用trizol(sigma-aldrich)从冷冻肝提取总rna。根据制造商的建议,用highcapacitycdna逆转录试剂盒(appliedbiosystems)逆转录1μgrna。利用sybrgreenmastermix(appliedbiosystems)在appliedbiosystems7900ht系统上实施实时pcr。对每个样品获得3个技术重复,并使用相对标准曲线方法来量化使用基因特异性引物获得的结果。tata盒结合蛋白基因(tbp)和β-肌动蛋白用作管家基因。
从肝提取nad代谢物:使用金属珠设定为20hz持续2分钟的组织裂解器(qiagen),在4℃下从在0.6m高氯酸中的50mg预先冷却钳冷冻肝提取nad。通过在4℃下以15000g持续10分钟使不溶性物质沉淀,并将澄清的上清液以冰冷的100mm磷酸盐缓冲液(ph8)稀释至1:100。如前所述7,通过自graeff和lee11的程序修改的96孔格式酶循环测定法测量nad。简而言之,在使用之前新鲜制备循环混合物,将5μlnad标准品或稀释的组织提取物与95μl循环混合物(包含在100mm磷酸盐缓冲液(ph8.0)中的2%乙醇、100g/ml醇脱氢酶、10g/ml心肌黄酶、20m刃天青、10m黄素单核苷酸、10mm烟酰胺、0.1%bsa)混合。使循环反应在室温下进行30分钟,并且基于试卤灵聚集速率测定nad的浓度,测量为在544nm处激发和在590nm处发射的荧光。
肝甘油三酯测定:使用组织裂解器在细胞裂解缓冲液(140mmnacl,50mmtris,ph7.4,0.1%triton-x)中提取25mg快速冷冻的肝组织。将样品以14000rpm离心15分钟,并使用甘油作为标准品,用triglycerideassaykit(stanbio)测定甘油三酯。
atp测定:根据制造商的方案,使用atp测定试剂盒(lifetechnologies),在~50mg快速冷冻肝的中和的酸提取物中测量atp。
葡萄糖测量:在禁食过夜(16小时)之后,使用onetouchultra葡萄糖分析仪从尾静脉测量血糖值。
统计:所有结果表示为平均值±sem。两组之间的比较使用未配对的双尾studentt检验分析。3组或更多组之间的比较使用prism6(graphpad)中的单因素anova进行分析,随后用studentt检验进行事后分析。对于相关矩阵,使用pearson相关系数分析数据。平均值之间的差异在p<0.05时定义为显著。
实施例1:烟酰胺核苷促进肝再生
为了测试nad可用性是否限制肝再生速率,在三分之二部分肝切除术(phx)之前14天开始,对野生型c57bl/6j小鼠的饮用水补充nr(3mg/ml,~500mg/kg)。尽管到phx后48小时,来自对照小鼠的正再生的肝苍白,具有特征性斑驳图案,但是来自nr治疗的小鼠的那些肝着色更均匀(图1,小图a),并且呈现肝细胞增殖大大增强,如通过dna中的edu掺入评价的那样(图1,小图b和c)。这通过肝质量的显著改善反映(图1,小图d)。值得注意的是,没有观察到给予nr的对照小鼠肝大小的变化,并且两组之间切除叶重量没有差异(数据未显示)。如预期的那样,nr治疗的小鼠肝中的nad含量在肝切除术之前(~35%)和之后(~58%)均增加(图1,小图e)。h&e染色切片的分析揭示在存在nr的情况下有丝分裂活性增加48%(图1,小图f和g)。此外,脂肪变化(肝再生早期阶段的特征)尽管在对照中很明显,但在nr治疗的小鼠不明显。这些包括特征在于存在微囊泡和巨囊泡脂滴两者的肝脂肪变性(图1,小图f和h)及肝甘油三酯的聚集(图1,小图i)。因此,nr治疗足以增加肝nad含量和显著促进肝再生,同时改善脂肪变化。
实施例2:肝细胞特异性nampt过度表达再现全身性nr对肝再生的作用
因为口服nr可具有影响肝再生速率的全身效应,因此实施测试以确定在肝细胞中的特异性nad合成是否足以再现前述观察结果。过度表达烟酰胺磷酸核糖转移酶(nampt)的小鼠品系以cre诱导型方式使用,与在白蛋白启动子控制下表达cre的小鼠杂交(图2,小图a-c)。nampt过度表达不均匀(图2,小图b),并且在门静脉周围和中央静脉周围区域附近明显突出。到phx后48小时,nampt过度表达的肝显得颜色更深且更均匀(图2,小图d),并且如对nr治疗观察到的那样,显著增强了edu掺入(图2,小图e和f)。这些变化与再生肝大小的增加相关(图2,小图g)。值得注意的是,尽管我们注意到空腹血糖水平轻度升高,但是肝细胞特异性过度表达nampt并未影响外科手术前的体重或肝重(图2,小图h)。phx前后肝nad含量均显著升高(图2,小图i)。有丝分裂指数增加,并且脂滴的聚集和甘油三酯含量显著减少(图2,小图j-l)。因此,nad生物合成的肝特异性增强再现全身性nr治疗对肝再生的关键作用。
实施例3:成年发生的过度表达对于nampt的有益作用是足够的
为了排除在nampt过度表达小鼠中改善再生可能继发于早期生活中的代谢适应的可能性,实施了其中cre经腺相关病毒(aav)在成年小鼠中递送的第二组实验。来自该实验的nampt过度表达小鼠与两组不同的同窝对照相比:携带floxed等位基因并感染编码gfp的aav的那些和感染aav-cre的野生型小鼠。仅在成年期间在其肝中过度表达nampt的小鼠呈现空腹葡萄糖轻度升高(图3,小图a和b)和肝细胞增殖增强,类似于具有终生过度表达的小鼠所获得的结果(图3,小图c-f)。尽管先前组小鼠在phx后48小时处死以使得能够量化有丝分裂图像,但是成年发生组在36小时处死以捕捉dna合成的峰值。如先前实验那样,nampt过度表达减轻急性肝脂肪变性和肝甘油三酯的聚集(图3,小图g和h)。
实施例4:肝细胞特异性nampt缺失损害肝再生,并且通过烟酰胺核苷(nr)完全挽救
nampt从脂肪组织和免疫细胞分泌,并且细胞外形式(enampt/pbef/visfatin)仍然具有催化活性。也已经观察到来自原代肝细胞的nampt分泌,并且因此,仍然形式上可能的是,在转基因小鼠的肝细胞中过度表达nampt会导致溢出到循环,其可对其他细胞类型具有nad依赖性作用。此外,enampt可具有独立于其催化活性的功能,提高nr和nampt过度表达可通过独立途径起作用以影响肝再生的可能性。为了解决这些问题,通过将aav-cre注射到携带nampt的两个floxed等位基因的成年动物中来产生肝细胞特异性nampt缺陷小鼠(图4,小图a和b)。感染aav-gfp的携带floxed等位基因的同窝小鼠用作对照。感染之后5天,将每组中的一半小鼠置于含有nr的饮用水,并在phx前治疗另外2周。在宏观上,namptfl/flaav-cre小鼠的再生肝苍白,具有点状皮下出血,这通过nr治疗来预防(图4,小图c)。phx之后头48小时期间的肝再生在namptko小鼠中显著受损,并通过nr治疗恢复(图4,小图d-f),nr治疗有效增加了两种基因型的nad含量(图4,小图g)。一致地,nr治疗在很大程度上恢复namptko小鼠的有丝分裂指数(图4,小图h和i),并且再次地,切除的叶重量没有变化,表明所有肝在损伤前都是正常大小。
组织学检查揭示namptfl/flaav-cre小鼠中明显的肝脂肪变性,包括微囊泡和巨囊泡脂滴两者(图4,小图i,上图)。相比之下,nr消除了正再生的野生型肝中的肝脂质聚集,并且几乎使nampt缺陷的正再生的肝的肝脂肪变化正常化(图4,小图i,下图)。肝甘油三酯也减少,nr治疗的namptfl/flaav-gfp小鼠减少~75%,而nr治疗的namptfl/flaav-cre小鼠减少~35%(图4,小图j)。这些结果证实,肝细胞中内源性nampt表达的丧失损害肝再生和使脂质代谢恶化,并且补充nad前体足以改善这些变化。
实施例5:肝nad含量与能量状态、甘油三酯聚集和肝细胞增殖强烈相关
为了进一步了解nad、脂质代谢和肝细胞增殖之间的关系,提供了一项测试以确定这些相关性是否在个体动物水平上保持为真。肝细胞增殖与肝nad含量呈显著正相关,并且与肝甘油三酯呈反相关(图5,小图a和b)。不限于任何一种理论,这可反映出需要最佳nad水平以使得脂质能够氧化,为细胞生长和分裂提供能量,或是由于在3-羟基酰基-coa脱氢酶(hadh)催化的脂肪酸氧化步骤和三羧酸循环(tca)中对nad的直接需要,或是由于其作为信号传导酶比如sirtuin的辅底物的作用。与该假设一致,atp水平在正再生的肝中显著降低,并通过nr治疗增强(图5,小图c)。此外,atp含量与nad和肝细胞增殖两者呈正相关(图5,小图d和e),表明nr可减轻肝的再生带来的能量压力。
建议的肝再生模型描绘于图5(小图f)。不受任何一种本发明理论的束缚,肝nad促进脂肪酸氧化,从而产生肝细胞生长和再生所必需的atp。nad在3-羟基酰基-coa脱氢酶(hadh)催化的脂肪酸氧化步骤及三羧酸循环(tca)中是直接需要的,但是也可经使用nad作为辅底物的信号传导酶比如sirt1间接起作用。nad浓度可基于nampt的表达进行调节,nampt催化自烟酰胺和磷酸核糖焦磷酸形成烟酰胺单核苷酸(nmn)。或者,nmn可通过nr激酶的作用从nr产生。
实施例6:肝细胞特异性的sirtuin1缺失损害再生,并通过nr部分挽救
实施研究以确定nr在sirt1缺失(这会损害再生过程)的情况下改善肝再生的能力。
在部分肝切除术(phx)之前,sirt1敲除和同窝对照用nr(500mg/kg/天)治疗2周。用苏木精和伊红染色的代表性肝切片揭示sirt1缺陷小鼠的急性肝脂肪变性,同时具有微囊泡和巨囊泡脂滴(图6,小图a)。nr治疗部分挽救了表型并减轻了肝脂肪变化。
在另一种测定中,phx后头36小时期间的肝再生在sirt1敲除小鼠中受损并通过nr治疗恢复。nr介导的肝组织恢复被描绘为与野生型和sirt1敲除小鼠两者的未治疗肝相比,再生肝大小的增加(图6,小图b)。
本文可引用一些专利和非专利出版物以描述本发明所属领域的状态。这些出版物中每一个的全部公开内容通过参照结合于此。
尽管以上已经描述和/或例示本发明的某些实施方案,但是根据前述公开,各种其他实施方案对于本领域技术人员是显而易见的。因此,本发明不限于所描述和/或例示的特定实施方案,而是能够进行相当大的变化和修改,而不背离附加权利要求的范围和精神。
此外,本文使用的术语“约”意指尺寸、大小、制剂、参数、形状及其他数量和特征不准确和不需准确,而是可根据需要为近似的和/或更大或更小,反映公差、转换因子、四舍五入、测量误差等及本领域技术人员已知的其他因素。通常,尺寸、大小、制剂、参数、形状或其他数量或特征为“约”或“近似”的,无论是否明确规定是这样。应该注意的是,非常不同的大小、形状和尺寸的实施方案可采用所描述的排列。
此外,当在附加权利要求中以初始和修改的形式使用时,过渡术语“包含”、“基本上由......组成”和“由...组成”在什么样的未记载的另外权利要求要素或步骤(如果有的话)被排除在权利要求范围之外的方面定义权利要求范围。术语“包含”打算为包容性或开放式的,并且不排除任何另外未记载的要素、方法、步骤或材料。术语“由......组成”排除除了权利要求中指定的那些要素、步骤或材料及在后者情况下通常与指定材料相关的杂质以外的任何要素、步骤或材料。术语“基本上由......组成”将权利要求的范围限制到指定元素、步骤或材料,及不实质性影响要求保护的发明的基本和新颖特征的那些。在备选实施方案中,体现本发明的本文描述的所有组合物、制剂、药盒和方法可通过任何过渡术语“包含”、“基本上由......组成”和“由......组成”更具体地定义。
参考文献
1.fanst,locm,liucl等人safetyofdonorsinlivedonorlivertransplantationusingrightlobegrafts.archsurg2000;135:336-40.
2.kubotak,makuuchim,kusakak等人measurementoflivervolumeandhepaticfunctionalreserveasaguidetodecision-makinginresectionalsurgeryforhepatictumors.hepatology1997;26:1176-81.
3.michalopoulosgk.liverregeneration.jcellphysiol2007;213:286-300.
4.ferrisgm,clarkjb.nicotinamidenucleotidesynthesisinregeneratingratliver.biochemj1971;121:655-62.
5.clarkjb,greenbaumal,mcleanp.theconcentrationandbiosynthesisofnicotinamidenucleotidesintheliversofratstreatedwithcarcinogens.biochemj1966;98:546-56.
6.clarkjb,pinders.controlofthesteady-stateconcentrationsofthenicotinamidenucleotidesinratliver.biochemj1969;114:321-30.
7.frederickdw,davisjg,davilaa,jr.等人increasingnadsynthesisinmusclevianicotinamidephosphoribosyltransferaseisnotsufficienttopromoteoxidativemetabolism.jbiolchem2015;290:1546-58.
8.yoonmj,yoshidam,johnsons等人sirt1-mediatedenamptsecretionfromadiposetissueregulateshypothalamicnad+andfunctioninmice.cellmetab2015;21:706-17.
9.mitchellc,willenbringh.areproducibleandwell-toleratedmethodfor2/3partialhepatectomyinmice.natprotoc2008;3:1167-70.
10.mitchellc,willenbringh.addendum:areproducibleandwell-toleratedmethodfor2/3partialhepatectomyinmice.natprotoc2014;9.
11.graeffr,leehc.anovelcyclingassayforcellularcadp-ribosewithnanomolarsensitivity.biochemj2002;361:379-84.
12.imais,kiessw.therapeuticpotentialofsirt1andnampt-mediatednadbiosynthesisintype2diabetes.frontbiosci(landmarked)2009;14:2983-95.
13.gartena,petzolds,kornera等人nampt:linkingnadbiology,metabolismandcancer.trendsendocrinolmetab2009;20:130-8.
14.gartena,petzolds,barnikol-oettlera等人nicotinamidephosphoribosyltransferase(nampt/pbef/visfatin)isconstitutivelyreleasedfromhumanhepatocytes.biochembiophysrescommun2010;391:376-81.
15.soncinid,caffai,zoppolig等人nicotinamidephosphoribosyltransferasepromotesepithelial-to-mesenchymaltransitionasasolublefactorindependentofitsenzymaticactivity.jbiolchem2014;289:34189-204.
16.hasmannm,schemaindai.fk866,ahighlyspecificnoncompetitiveinhibitorofnicotinamidephosphoribosyltransferase,representsanovelmechanismforinductionoftumorcellapoptosis.cancerres2003;63:7436-42.
17.pautam,rotllann,fernandez-hernandoa等人akt-mediatedfoxo1inhibitionisrequiredforliverregeneration.hepatology2015.
18.rudnickda.trimmingthefatfromliverregeneration.hepatology2005;42:1001-3.
19.rudnickda,davidsonno.functionalrelationshipsbetweenlipidmetabolismandliverregeneration.intjhepatol2012;2012:549241.
20.taor,weid,gaoh等人hepaticfoxosregulatelipidmetabolismviamodulationofexpressionofthenicotinamidephosphoribosyltransferasegene.jbiolchem2011;286:14681-90.
21.gartena,schusters,penkem等人physiologicalandpathophysiologicalrolesofnamptandnadmetabolism.natrevendocrinol2015;11:535-46.
22.dahltb,holms,aukrustp等人visfatin/nampt:amultifacetedmoleculewithdiverserolesinphysiologyandpathophysiology.annurevnutr2012;32:229-43.
23.purushothama,schugtt,xuq等人hepatocyte-specificdeletionofsirt1altersfattyacidmetabolismandresultsinhepaticsteatosisandinflammation.cellmetab2009;9:327-38.
24.garcia-rodriguezjl,barbier-torresl,fernandez-alvarezs等人sirt1controlsliverregenerationbyregulatingbileacidmetabolismthroughfarnesoidxreceptorandmammaliantargetofrapamycinsignaling.hepatology2014;59:1972-83.
25.jinj,iakovap,jiangy等人thereductionofsirt1inliversofoldmiceleadstoimpairedbodyhomeostasisandtoinhibitionofliverproliferation.hepatology2011;54:989-98.
26.wangy,jiangy,fanx等人hepato-protectiveeffectofresveratrolagainstacetaminophen-inducedliverinjuryisassociatedwithinhibitionofcyp-mediatedbioactivationandregulationofsirt1-p53signalingpathways.toxicollett2015;236:82-9.
- 还没有人留言评论。精彩留言会获得点赞!