一种治疗自身免疫性疾病和过敏的方法和试剂与流程
本发明涉及医疗领域,具体涉及一种治疗自身免疫性疾病和过敏的方法和试剂。一种用于药物应用的蛋白质,肽和抗原修饰以及用于治疗诸如自身免疫疾病和过敏的疾病的试剂。本发明公开了治疗自身免疫疾病和过敏的方法。本发明还涉及用基于细胞的疗法治疗自身免疫疾病的方法。
背景技术:
免疫反应是保护免受潜在致病微生物所必需的。然而不希望的免疫激活可能导致有害过程,导致自身组织的损伤或破坏。例如,在自身免疫疾病中发生不期望的免疫激活,其中抗体和/或t淋巴细胞与自身抗原反应而损害身体组织。在过敏反应中也是这种情况,其特征在于对某些环境问题的过度免疫反应并且可能导致导致组织破坏的炎症反应。这也是移植器官排斥的原因,其由宿主中存在的识别供体同种异体抗原或异种抗原的同种异体反应性t细胞介导。免疫耐受是对通常发生免疫应答的抗原的获得性特异性免疫应答缺乏。通常,为了诱导耐受,必须暴露于耐受性抗原,这导致某些淋巴细胞的死亡或功能性失活。该过程通常为对自身抗原的耐受性或自身耐受性。免疫抑制剂可用于预防或减少不希望的免疫反应,例如用于治疗患有自身免疫疾病或同种异体移植的患者。产生对不希望的免疫应答相关的免疫抑制的常规策略是基于广谱免疫抑制药物。另外,为了维持免疫抑制,免疫抑制药物治疗通常是终身使用。不幸的是,广谱免疫抑制剂的使用与严重副作用的风险相关,例如肿瘤,感染,肾毒性和代谢紊乱。因此,新的免疫抑制剂疗法将是有益的。
体外循环疗法是一种从患者的血液循环中取血以在其返回循环之前对其进行处理的过程。所有在体外携带血液的装置称为体外回路。它包括血液透析,血液滤过,血浆置换,血液成分分离术等。血浆置换术是从血液循环中去除,处理和返回(血液成分)血浆。该方法用于治疗多种疾病,包括免疫系统疾病,如重症肌无力,狼疮和血栓性血小板减少性紫癜。血液灌流/血液净化是一种用于从患者血液中去除有毒或不需要的物质的医疗过程。通常,该技术涉及使大量血液通过吸附剂物质。最常用于血液灌流/血液净化的吸附物质是树脂和活性炭。血液灌流/血液净化是一种体外形式的治疗,因为血液被泵送通过患者体外的装置。其主要用途包括在紧急情况下从血液中去除药物或毒性物质,从肾功能衰竭患者的血液中去除废物,以及作为肝移植前后患者的支持性治疗。血液成分分离术是一种医疗技术,其中供体或患者的血液通过分离出一种特定成分并将其余部分返回循环的装置。取决于被移除的物质,在血液成分分离术中使用不同的过程。
技术实现要素:
在一个方面,本发明公开了透皮药物递送系统,例如透皮贴剂,其用于治疗选自自身免疫疾病,过敏反应和抗药物抗体的病症,其包含引起所述病症的抗原和免疫抑制剂。抗原可以是b细胞抗原,mhc-肽复合物形式的t细胞抗原,或可以与mhc结合形成mhc-肽复合物的t细胞抗原的抗原肽(或其衍生物)。免疫抑制剂的实例选自雷帕霉素,福吉霉素和甲氨蝶呤。本发明还公开了通过向受试者施用皮肤上的所述透皮药物递送系统来治疗受试者的自身免疫疾病或过敏或抑制其抗药物抗体产生或诱导抗原特异性免疫耐受的方法。
另一方面,本发明公开了一种治疗选自自身免疫疾病,过敏变态反应和抗药物抗体的病症的缀合物,其包含引起该病症的抗原,第一免疫抑制剂和第二免疫抑制剂。抗原可以是b细胞抗原,mhc-肽复合物形式的t细胞抗原或可以与mhc结合的抗原肽(或其衍生物)。第一种免疫抑制剂选自siglec配体,例如唾液酸或聚唾液酸。第二免疫抑制剂的实例选自雷帕霉素,福吉霉素和甲氨蝶呤。本发明还公开了通过向受试者施用所述缀合物(例如皮下或静脉内注射)来治疗受试者的自身免疫疾病或过敏或抑制其抗药物抗体产生或诱导抗原特异性免疫耐受的方法。
在本发明的一个方面,表面上涂有自身抗原的固相支持吸附剂可用于血液净化,以从患者血液中除去自身免疫性t细胞或b细胞以治疗其自身免疫疾病,类似于先前描述的从患者中除去ctc治疗癌症的专利申请us13/444,201和us15/373,483。例如,具有涂覆有胰岛素和/或beta细胞表面抗原的吸附剂(例如颗粒)的血液净化器可用于去除自身免疫t细胞/b细胞克隆以治疗糖尿病。也可以用血细胞分离器/白细胞分离法将血淋巴细胞与血液分离,然后将分离的淋巴细胞通过亲和柱(表面涂有自体抗原)或与磁性颗粒混合(表面涂有自体抗原)以去除自身免疫t细胞或b细胞然后将血液/淋巴细胞返回患者体内。该方法类似于本发明人在us13/444,201和us15/373,483申请中描述的ctc去除,其不同之处在于靶标是对某些自身抗原具有亲和力的b细胞或t细胞。本发明公开了通过血液净化去除t细胞和b细胞以治疗由这些t细胞和/或b细胞克隆引起的疾病的方法。本申请的发明人的专利申请us13/444,201公开了使用包含用自身抗体特异性抗原包被的亲和基质的血液净化盒从血液中去除自身抗体的血液净化方法,装置和试剂。所述血液净化方法,装置和试剂可以进一步应用于患者的全血,以去除血液中对包被抗原特异的t细胞和b细胞,从而治疗由这些t细胞或b细胞克隆引起的免疫疾病。例如,所述专利申请pct/us2012/033153(美国申请号13444201)描述了使用包被有针对ctc的抗体的亲和基质从血液中去除ctc的方法,装置和试剂;当使用胰岛抗原包被亲和基质时相应的方法,装置和试剂可用于去除针对胰岛的循环t细胞,从而治疗糖尿病。在另一个实例中,当亲和基质包被双链dna(例如本发明中描述的与毒素或α-gal缀合的那些dna)时,所得的血液净化方法和装置可用于去除针对dna的自身免疫b细胞,因此可以用来治疗狼疮。抗原可以是b细胞抗原或t细胞抗原(mhc-肽复合物,例如用于mhc四聚体技术的那些,mhc和肽可以共价缀合)。
用于血液净化的固相支持物可以是柱,膜,纤维,颗粒或任何其它合适的表面,其具有适当的表面性质(包括多孔结构内部的表面),可以用于亲和分子的直接偶联或用于修饰后的偶联或用于表面衍生化/修饰。如果固体支持物是多孔的,其内部也可用于提供结合亲和分子。
本发明还公开了用于自身免疫疾病的抗原-药物缀合物或抗原-αgal缀合物。专利申请美国申请号13/444,201公开了治疗由某些外源抗原或自身抗原产生某些抗体或自身免疫t细胞引起的自身免疫疾病/疾病的方法。该方法包括两个步骤,第一步;通过血液纯化程序除去引起疾病的抗体或特异性抗体或b细胞/t细胞。或者,代替使用血液净化,用药物抑制产生引起疾病的抗体或特异性抗体。合适的药物包括能够抑制抗体产生的药物,例如肾上腺皮质类固醇,环孢菌素,雷帕霉素,甲氨蝶呤和霉酚酸。优选地,剂量足以抑制至少50%的抗体产生。第二步与us13/444,201申请中描述的步骤相同。当毒素/细胞抑制剂/灭活剂-抗原缀合物(例如热自杀抗原或免疫抑制药物,例如在维基百科的“免疫抑制药物”文章页中描述的那些)用于在第二步中灭活抗体产生和/或t细胞时(例如,通过将缀合物注射到由所述自身抗原引起的具有自身免疫疾病的个体,需要选择抗原的表位,使其仅与特异性b细胞/t细胞/抗体结合,而不与体内其他受体结合。例如,一些糖尿病是由于胰岛素抗体的产生,可以使用胰岛素表位-毒素缀合物通过以治疗有效量将其注射给患者而使产生胰岛素抗体的b细胞失活。需要选择该表位以仅与b细胞/t细胞/抗体结合,但不与其他人类细胞上的胰岛素受体结合。
许多主要疾病是由自身抗体(例如类风湿性关节炎和某些糖尿病)或不良抗体(例如过敏,移植排斥)引起的。目前的治疗不能从根部治愈,并且经常导致严重的副作用(例如使用类固醇)。adc(抗体-药物偶联物)近年来成为有前景的癌症治疗方法。抗原-药物偶联策略可用于自身抗体诱导的自身免疫疾病;选择性地灭活产生特异性抗体的b细胞克隆以从源头治疗。该原理在本申请的发明人的专利申请us13/444,201中描述。
在数十亿个b细胞克隆中,只有几个b细胞克隆产生针对某些抗原的特异性抗体;这些b细胞分泌单克隆抗体并呈现对靶抗原高度特异的膜结合抗体(bcr受体)。抗原-药物缀合物将以高亲和力/高特异性与这些b细胞结合并使它们失活。选择性地灭活这些b细胞克隆将消除用于治疗许多自身抗体诱导的疾病的有害抗体的产生,例如,狼疮,复发性流产,类风湿性关节炎,1型糖尿病,深静脉血栓形成,重症肌无力等。
可以通过进行伴随试验(elisa)以鉴定具有adc特异性自身抗体的患者(类似于赫赛汀的her2试验)来减少脱靶。使用固定有抗原的亲和柱去除大量循环自身抗体的血液净化(临床使用的治疗方法)在adc给药前的一次性治疗以提高b细胞的adc功效/选择性。在大多数情况下,不需要利用蛋白质缀合,肽表位或小分子抗原将足以用于adc构建,简化adc的开发/制造。每月给药将足以防止体细胞超突变。t细胞还呈递对靶抗原特异的t细胞受体,使用抗原-药物偶联物灭活这些t细胞克隆也可用于治疗许多t细胞介导的自身免疫主要疾病。
针对dna的自身抗体是系统性红斑狼疮(sle)中的关键致病因子,临床上使用dna包被的亲和柱从患者血液中去除这些抗体(血液净化)作为有效的sle治疗。抗原-药物缀合物可用于sle治疗。如图1所示,dna-连接子-mrtansine(利用药物abetimus采用的dna序列,从药物kadcyla采用的连接子/毒素,连接子可以针对b/t细胞进行优化)是用于sle治疗的adc的实例。使用的dna序列是用gtgtgtgtgtgtgtgtgtgt(seqidno:1)和cacacacacacacacacac(seqidno:2)形成的复合物。单链dna抗原也可用于灭活对单链dna特异的自身抗体生成细胞。它将选择性地灭活产生针对dna的自身抗体的特异性b细胞克隆,从来源治疗疾病。它可以通过固相合成轻松制备。可以将其静脉内注射给患有sle的患者进行治疗。将进行伴随测试以增加功效。在第一剂量adc给药之前,将患者用血液净化处理以除去抗dna抗体,以获得更好的治疗指数。
附图说明
图1显示了用于系统性红斑狼疮治疗的adc的示例
图2显示了表位(抗原)-αgal缀合物的一般结构的实例
图3显示了用于系统性红斑狼疮治疗的抗原-αgal偶联物的实例
图4显示了抗原-细胞灭活分子缀合物的实例
图5显示用于癌症治疗的vegf-细胞灭活分子缀合物的实例
图6显示通过灭活产生dna特异性自身抗体的b细胞来治疗狼疮的fitc-dna自身抗原缀合物的实例。
图7显示了药物与碳水化合物聚合物缀合以形成前药的实例。
图8显示了与雷帕霉素缀合的聚唾液酸通过酯键形成前药的实例。
图9显示了其中连接子是连接药物和聚合物骨架的甘氨酸的实例。
图10显示了基于透明质酸的甲氨蝶呤前药的实例。
图11显示了含有抗原和雷帕霉素的缀合物的结构的实例。
图12显示了3种不同形式的抗原-药物缀合物的实例。
图13显示了用于治疗自身免疫疾病或过敏反应或诱导免疫耐受的表位(抗原)-富含唾液酸的聚合物缀合物的实例。
图14显示了含有抗原和唾液酸/siglec配体的缀合物的实例。
图15显示了用于诱导免疫耐受和治疗自身免疫疾病或过敏的基于微球的药物结构的示意性实例。
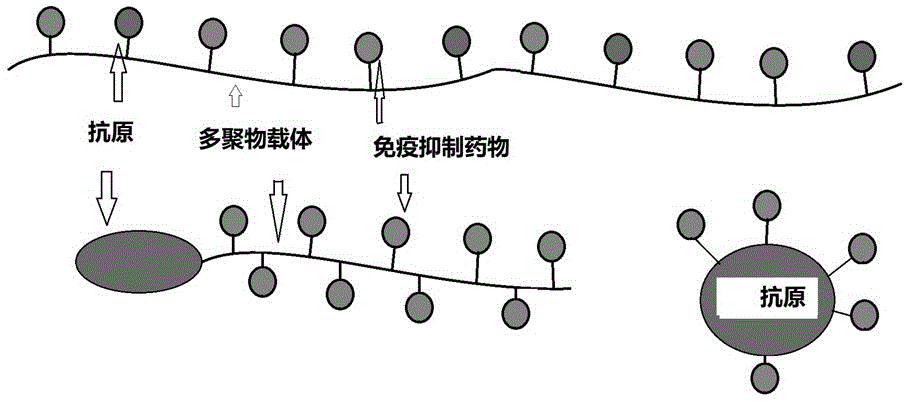
图16显示了使用与抗原,siglec配体和其他免疫抑制剂缀合的聚合物载体的不同形式;以及siglec配体和其他免疫抑制剂都与抗原偶联的示意。
图17显示了用于系统性红斑狼疮治疗的siglec配体-抗原偶联物的多个示意实例。
具体实施方式
在一些实施方案中,优选地,抗原不应与内源性受体结合,例如,可以使用不与胰岛素受体结合但可以与胰岛素自身抗体结合的胰岛素片段。
代替当前申请和先前申请us13/444,201中描述的表位(抗原)-毒素缀和物,也可以使用表位(抗原)-αgal(例如半乳糖-α-1,3-半乳糖)缀和物,其利用内源性抗αgal抗体使b细胞克隆或t细胞克隆失活,该克隆可以选择性地与表位(抗原)结合。可以从美国专利申请us12/450,384和其他出版物中得到αgal引用实例。
表位(抗原)-alphagal缀合物设计具有下结构式:α半乳糖基-(任选的连接子)-表位(抗原),其将允许对表位(抗原)特异的t细胞/b细胞与内源性抗gal抗体结合并且因此,由于结合的抗体而被消除/失活。示例如图2所示。
例如,抗原可以是由自身免疫b细胞/t细胞识别的胰岛素或胰岛素片段,或由糖尿病患者中的自身免疫t细胞识别的胰岛肽或β细胞的自身抗原(例如描述于clinimmunol.2004oct;113(1):29-37和procnatlacadsciusa.2003jul8;100(14):8384–8388)。该缀合物将选择性地使引起糖尿病的自身免疫b细胞/t细胞失活。对于t细胞抗原,它可以是mhc-肽复合物形式,其中肽可任选地与mhc共价连接。
t细胞通过其tcr受体识别t细胞抗原。t细胞抗原通常是mhc-表位结合复合物的形式。表位通常是由抗原呈递细胞(apc)处理的肽(有时是其他分子,例如碳水化合物)。在本发明的一些实施方案中,t细胞的抗原优选是形成的mhc-表位复合物或其片段/衍生物/模拟物,其对tcr的特异性亲和力高于单独的表位。它可以是单体形式或低聚物(二聚体,三聚体,四聚体,五聚体或甚至更高程度的聚合物)形式,例如目前广泛用于研究的mhc四聚体。例如,hla-a2insb10-18四聚体(doi:10.1073/pnas.0508621102)可以与细胞灭活剂与任选的连接子缀合,通过灭活自身免疫t细胞来治疗1型糖尿病。表位(例如肽)可以与mhc共价缀合,以通过众所周知的出版物中公开的众所周知的方法增加其稳定性。类似地,本发明中用于b细胞的抗原也可以是寡聚体或聚合物形式。然而,用于使b细胞失活的抗原不需要mhc成分。
可以选择性灭活产生针对dna的自身抗体的b细胞的示例性药物如图3所示,该药物可用于治疗狼疮。患者可以每周静脉注射500mg~1g的所述缀合物。注射治疗其狼疮,直到症状消失。
或者,可以使用tregitope肽-抗原缀合物代替毒素-抗原缀合物用于相同目的。它将选择性地灭活自身免疫t细胞,从而治疗相应的疾病。
载体系统可用于上述发明,如同本发明人申请us13/444,201中公开的。例如,可以使用脂质体或微粒或纳米颗粒。抗原固定在脂质体或颗粒的表面上,效应分子(例如αgal,鼠李糖,免疫抑制细胞因子,tregitope肽,毒素,sirna或mirna或其类似物,免疫抑制剂,反义分子)可以是包封在脂质体或颗粒的内部或共固定在脂质体或颗粒的表面上。
具有自身抗原或针对相同疾病的不同自身抗原的组合(因为有时患者具有对一组不同的自身抗原有特异性的t细胞/b细胞)涂覆在其表面上的固相支持吸附剂,可用于血液净化以去除来自患者血液的自身免疫性t细胞或b细胞,用于治疗其相应的自身免疫性疾病,类似于从患者体内移除ctc以治疗癌症(例如,单独使用涂有胰岛素和/或beta细胞表面抗原或它们的肽与mhc复合物的吸附剂的血液净化器可用于去除自身免疫b细胞或t细胞克隆以治疗糖尿病。该方法,程序类似于本发明人当前和先前专利申请中描述的ctc去除,不同之处是靶标是b细胞或对某些自身抗原具有亲和力的t细胞。用于t细胞去除的自身抗原优选是如前所述的mhc-表位的复合物。特定的自身免疫疾病有时会涉及多种自身抗原(例如gad65,胰岛素,前胰岛素等对于1型糖尿病患者,因此固相支持吸附剂可以是不同固相支持吸附剂的混合物,每种吸附剂涂有不同的自身抗原用于这种疾病;或者固相支持吸附剂包覆有与疾病有关的不同自身抗原的混合物,类似于上述败血症治疗的策略。可以对患者进行elisa测试以鉴定所涉及的抗原,并使用该信息选择合适的固相吸附剂进行治疗。
当固相载体(例如本发明和申请人先前专利申请中描述的那些,例如100um~2mm微粒或50nm~100um磁性颗粒)用mhc-表位复合物(单体或低聚物或聚合物形式,该复合物可以是共价的或非共价的,它可以用于从血液中或从患者体内收集的血液/血液成分去除血液中的针对这种自身抗原(mhc-表位复合物例如hla-a2insb10-18)的t细胞。t细胞将包括对该自身抗原特异的调节性t细胞和效应t细胞/细胞毒性t细胞和辅助性t细胞(例如糖尿病患者的hla-a2insb10-18)的混合物。效应t细胞/细胞毒性t细胞可以通过其表面标识物cd+用正选择方法从混合物中除去,通过例如众所周知的方法,例如磁珠/流式细胞术/亲和柱。treg可以基于其表面标识物通过众所周知的方法纯化/分离,例如在出版物和商业试剂盒中描述的那些(例如在www.bdbiosciences.com/us/applications/research/t-cell-immunology/regulatory-t-cells/m/745680/workflow/tregenrichment中描述的那些)。treg还可以通过将foxp3表达引入细胞中进行体外转化来制备(例如在moleculartherapy(2007)16,194-202中描述的)。制备/纯化的treg可以在体外扩增并任选地再次进一步纯化,然后注射回患者以治疗相应的自身免疫疾病。由此产生的treg是抗原特异性的,因此为靶疾病治疗提供了更好的功效和更低的脱靶效果(靶标例如糖尿病患者的hla-a2insb10-18)。该方法既去除效应t细胞又增加患者体内特异性抗原的treg细胞,从而为由所述抗原引起的自身免疫疾病提供更好的治疗效果。可以制备对参与特定疾病的不同自身抗原特异的treg混合物,并将其注射给对这些自身抗原具有自身免疫力的患者。treg还可以抑制相应的b细胞以抑制自身抗体的产生。有时t细胞抗原是通过apc从该b细胞抗原衍生的,因此treg也可用于治疗由自身免疫b细胞/自身抗体产生的自身免疫。
除了αgal之外,还可以使用其他分子/肽/蛋白质与特定抗原缀合,以选择性地灭活结合特异性抗原并与特定抗原反应的特定b细胞克隆或t细胞克隆。由此产生的试剂具有以下一般结构:
细胞灭活分子–任选的连接子-抗原
该试剂以治疗有效量和以治疗上可接受的制剂可以给予具有自身免疫疾病或过敏症患者的患者(例如,通过静脉内注射)由于所述抗原以治疗所述自身免疫疾病或过敏症。当抗原是治疗药物(例如重组蛋白)或其表位时,可以将其给予患者(例如通过静脉内注射)以抑制/防止患者的抗药物抗体(ada)的产生。它可用于诱导抗原特异性免疫耐受。细胞灭活分子的实例包括对免疫细胞的亲和配体(例如抗体或其片段,适体)或它们的组合(例如那些在用于癌症治疗中使用的双特异性抗体和triomab),诸如针对例如cd3的t淋巴细胞抗原的抗体,或抗cd3和cd28的双特异性抗体(或具有的fc的triomab),或与针对cd3的抗体或它的片段和b7的融合蛋白(例子在图4中示出),已经具有体内的免疫反应性的抗原(例如alpha-gal,l-鼠李糖),b7,超级抗原(例如葡萄球菌肠毒素a,sea),细胞因子(例如免疫细胞灭活细胞因子)和那些由本发明和先前专利申请以及参考文献中描述的。例如,l-鼠李糖可以通过糖苷键与peg3连接,peg3同时也与自身抗原缀合。
当抗细胞毒性免疫细胞激活受体如t细胞的cd3或nk细胞的cd16的抗体或其片段与抗原缀合时,它会募集/激活细胞毒性免疫细胞如t细胞或nk细胞,从而可以抑制/杀死可与抗原结合的靶b/t细胞(优选的靶t细胞的抗原是由其tcr识别的mhc-肽复合物);这类似于目前用于杀死癌细胞的双特异性抗体,其不同之处是在缀合物中使用自身抗原而不是抗癌细胞的抗体)。
例如,在一个实例中,针对nk细胞的cd16a的抗体或fab(该序列可以从affimed的tnadabafm13获得采用)通过其半胱氨酸与图1中所示的针对sle的连接子-抗原缀合以形成硫醇-马来酰亚胺方式连接。在抗体药物缀合物中广泛使用的连接和缀合方案是本领域技术人员熟知的。该抗原-抗cd16a抗体缀合物可用于治疗sle。一旦注射给患者(例如,每周200mg~1000mg,每周一次),它将与dna抗原特异性b细胞结合并吸引nk细胞杀死它,因此抑制针对dna抗原的自身抗体产生。或者,可以使用针对cd3的抗体或fab代替针对cd16的抗体或fab以制备缀合物。得到的缀合物可以吸引细胞毒性t细胞杀死抗原特异性b细胞以治疗相应的自身免疫疾病。
任选地,还可以将另外的亲和配体引入缀合物中以增加对b或t细胞的亲和力和特异性。例如,抗cd20抗体也可以通过连接子掺入缀合物中以增加针对b细胞的靶向,这是一种类似于三特异性抗体的方案。
另一种细胞灭活分子是sea。sea是一种微生物超级抗原,可激活t淋巴细胞并诱导各种细胞因子的产生,包括干扰素-γ(ifn-γ),肿瘤坏死因子-α(tnf-α)和细胞溶解性孔形成穿孔素和/或瘤内ctl分泌的颗粒酶b。这里使用的sea基因的实例可以携带由dohlsten小组构建的d227a突变,其与主要组织相容性复合物类(mhc)ii的结合减少1000倍而降低全身毒性。制备sea-缀合物的方案可以在专利申请cn102114239a,cn1629194a和cn101829322a中找到。
除共刺激分子b7.1外,其他共刺激分子也可用作细胞灭活分子,例如选自其他b7家族成员的那些,包括b7.2(cd86),b7-h1(pd-l1),b7-h2(b7rp-1或icos-l或b7h或gl-50),b7-h3(b7rp-2),b7-h4(b7x或b7s1),b7-dc(pd-l2)等,以及它们的具有与天然和人造变体超过70%同一性的氨基酸序列的蛋白质。共刺激分子b7.1(cd80)或其他共刺激分子的作用是刺激机体的免疫反应。此外,除了b7家族成员外,其他分子也可以刺激t细胞,也可以用作本发明的细胞灭活分子。专利申请cn102391377a(cn201110338886)中描述的方案可以容易地用于本发明。例如,cn102391377a中融合蛋白的细胞因子可以用自身抗原替换,以产生本申请的缀合物,以灭活抗原特异性b细胞和/或t细胞。
b7是在活化的抗原呈递细胞(apc)上发现的一种外周膜蛋白,当与t细胞上的cd28或cd152(ctla-4)表面蛋白配对时,可产生共刺激信号或共抑制信号以增强或者降低apc和t细胞之间的mhc-tcr信号的活性。某些b7蛋白可以增强t细胞的活性(例如b7.1,b7.2),其中一些可以抑制b/t细胞的活性(b7.dc/pd-l2,b7.h1/pd-l1)。当t细胞激活b7与抗原偶联缀合时,它将募集/激活其他t细胞或细胞毒性免疫细胞以抑制/杀死(类似于目前的双特异性抗体杀死癌细胞,不同之处是使用自身抗原代替癌细胞抗体)可以与抗原结合的靶b/t细胞(优选靶t细胞的抗原是由其tcr识别的mhc-肽复合物)。当b/t细胞抑制b7用于缀合物时,它将与靶b/t细胞上的相应受体结合,以杀死/灭活可与抗原结合的靶b/t细胞。
像b7一样,其他可以激活免疫细胞上的抑制性免疫检查点受体的配体,如a2ar,b7-h3,b7-h4,btl,ido,kir,lag3,pd-1,tim-3和vista,或可阻断免疫细胞如cd27,cd28,cd40,cd122,cd137,ox40,gitr,cd52和icos上的活化检查点分子的配体(例如抗体或其片段),也可用作细胞灭活分子。例如,细胞灭活分子可以是pd-l1或其衍生物/片段或模拟物或其他结合pd-1以防止b或t细胞活化配体,pd-l2或其衍生物/片段或模拟物或其他结合pd-1以防止b或t细胞活化的配体等。
当靶细胞是b细胞时,也可以使用bcr抗原-tcr抗原缀合物。可以在这些功能组之间添加可选的链接子。在缀合物中,b细胞抗原与靶b细胞结合,t细胞抗原(mhc-抗原肽复合物,其可以共价连接在一起)与效应t细胞结合。b细胞和t细胞的抗原可以不同。原理是募集现有的效应t细胞以杀死/灭活靶b细胞。t细胞抗原也可以是能够与mhc结合形成mhc-肽复合物或其衍生物的肽,而不是完整的mhc-肽复合物型t细胞抗原,在这种情况下,肽将由apc处理然后在体内形成mhc-肽复合物以诱导免疫耐受。
当上述和图4中描述的缀合物中的抗原被癌细胞的亲和配体替换时(例如,针对癌细胞的抗体或对下文段落中描述的对癌细胞具有亲和力的细胞因子/肽/蛋白),它可用于治疗癌症(例如图5所示,vegf可以是vegf拮抗剂,例如vegf165b,vegf也可以用抗癌细胞的抗体或其片段代替)。本发明还公开了治疗癌症和杀死癌细胞的方法和试剂。cn101829322a(pct/cn2010/078854)公开了细胞因子-超抗原融合蛋白在制备抗癌/肿瘤药物中的用途,其中细胞因子是表皮生长因子或血管内皮细胞生长因子,超抗原是超抗原金黄色葡萄球菌肠毒素a.可以用于治疗癌症的sea-缀合物也在专利申请cn102114239a,cn1629194a和cn101829322a中公开。用于抗癌疗法的超抗原融合蛋白和制备方法也公开于cn1629194a。专利申请cn102391377a,us10/571,836。cn102391377a公开了一种可诱导和激活癌靶向t细胞的融合蛋白及制备方法及用途,该蛋白质包含具有与癌细胞作用的肽和共刺激分子b7.1,所述与癌细胞作用的肽选自转化生长因子-α、表皮生长因子、血管内皮细胞生长因子、促性腺激素释放激素或促胃液素释放肽,该发明的融合蛋白具有癌靶向作用,一方面可分别与vegfr、egfr、gnrh-r、或grp-r作用,另一方面又与t细胞上表达的相应受体cd28和ctla-4相互作用,这样就将t细胞靶向性定位到大量表达vegfr、egfr、gnrh-r、或grp-r的癌细胞周围,实验证明该发明的融合蛋白能够抑制肿瘤生长和引起癌细胞的凋亡。上面列出的专利利用b7.1或超级抗原与可与癌细胞结合的细胞因子或肽或蛋白质缀合。
本发明还公开了通过将上述专利中使用的细胞因子或肽或蛋白质(其与b7或超级抗原缀合)与可与免疫细胞结合的αgal或抗体偶联来治疗癌症和杀死癌细胞的方法和试剂。(例如用于癌症治疗的双特异性抗体中使用的那些抗体,例如针对t淋巴细胞抗原如cd3的抗体)。向患者施用所得的缀合物可用于治疗癌症。缀合物的几个实例是:αgal-连接子(任选的)-egf,αgal-连接子(任选的)-vegf,αgal-连接子(任选的)-tgf-α,αgal-gnrh。优选地,所得的缀合物不具有egfr/vegfr激动剂活性。当使用天然egf或vegfr时,缀合物可能仍具有激动剂活性。优选的亲和配体,其可以与egfr或vegfr结合而不激活它们,例如采用egfr或vegf拮抗剂用于制备缀合物。例如,pct/ca2010/000275中披露的核心蛋白聚糖decorin,vegf165b,vegf拮抗剂可用于制备缀合物,而不是使用能够激活vegfr用于血管生成的天然vegf;它们还可以用于与毒素偶联缀和(例如mmae,mmaf和dm1)用于癌症治疗。这些细胞因子可以进一步修饰为对肽酶/蛋白酶稳定,以增加其体内半衰期,并且可以将半衰期修饰剂如fc或脂肪酸加入缀合物中以增加其半衰期。
αgal或l-鼠李糖与可与癌细胞结合的肽/蛋白质/小分子(例如叶酸,vegf或其衍生物/模拟物,例如vegf165b和先前公开的那些)的缀合物也可用于治疗癌症。它们的实例包括叶酸-任选的连接子-αgal,vegf165b-任选的连接子-αgal,vegf-任选的连接子-αgal,叶酸-任选的连接子-αl-鼠李糖,vegf165b-任选的连接子-αl-鼠李糖,vegf-任选的连接子-α-l-鼠李糖。
除了αgal之外,已经具有t细胞免疫活性或b细胞免疫活性的其他抗原也可用于替代所述缀合物中的αgal来灭活免疫细胞或癌细胞或病原体。它可以是内源的或通过使用所述抗原的疫苗接种诱导。内源性抗原的实例包括dnp(二硝基苯基)和l-鼠李糖(例如α-l-鼠李糖)。抗体或抗原特异性效应t细胞可以通过接种产生诱导。例如,大多数新生儿接受抗结核疫苗bcg,口服脊髓灰质炎病毒疫苗(opv)和抗乙型肝炎疫苗(hbvac)。他们对这些抗原具有b细胞或t细胞免疫力。可以使用来自opv或bcg或hbv的抗原来制备缀合物而不是使用αgal。可以首先测试患者的抗原反应性并选择具有强b细胞或t细胞免疫力的抗原以制备缀合物并将该个性化缀合物给予患者以治疗他的疾病(例如癌症或自身免疫疾病)。还可以给患者注射特殊抗原的疫苗(例如与klh缀合的非天然肽抗原,并给予增强剂),以使患者产生针对该抗原的t细胞免疫或b细胞免疫,然后使用该抗原制备本发明中描述的用于疾病治疗的缀合物。利用天然免疫的另一个例子是使用血型抗原代替α-gal来构建缀合物:abo抗原。例如,对于具有血型a组的患者,缀合物可以利用b抗原;对于具有血型b组的患者,缀合物可以利用a抗原;对于具有血型o组的患者,缀合物可以使用a或b抗原或它们的组合。在一个实例中,a抗原-双链dna的缀合物可用于治疗患有狼疮的b型血液患者;在另一个实例中,b抗原-vegf165b的缀合物可用于治疗患有癌症的a型血液患者。
当含有α-gal的缀合物用于治疗癌症或自身免疫性疾病或其他疾病时,可以给予患者可以诱导/增加抗α-gal抗体产生/功效的疫苗(例如αgal-klh缀合物与增强剂)和/或在治疗期间。这将增加抗αgal抗体的产生并增加抗体的亲和力/效力。该疫苗接种策略也可用于本发明的各种方法和的其他使用α-gal或l-鼠李糖或dnp的来募集内源性抗体以治疗疾病的已知治疗方法(例如αgal或l-鼠李糖或基于dnp的脂质对于癌症治疗,centauritherapeutics的αgal-aptamer缀合物用于癌症或病原体灭活的方法)通过给予患者α-gal或l-鼠李糖或基于dnp的疫苗以在治疗之前或期间增强其相应的抗体效力。centauritherapeutics使用αgal-aptamer结合物来治疗癌症或病原体。适体aptamer对癌细胞或病原体具有亲和力。centauritherapeutics的αgal-aptamer缀合物中的α-gal可以用dnp(二硝基苯基)或l-鼠李糖(例如αl-鼠李糖)代替,以灭活癌细胞或病原体。
涉及tcrs或cars的工程化t细胞疗法利用具有可与特定抗原结合的tcr或car的t细胞。患者在治疗期间和治疗后将在体内具有这些t细胞。可以给患者工程化t细胞(tcr或car型)然后使用这种特异性工程化t细胞攻击自身免疫t细胞或自身免疫b细胞来治疗他的自身免疫疾病,通过给患者提供缀合物:自身抗原-(可任选的连接子)-工程化t细胞的抗原。例如,可以识别fitc的嵌合抗原受体(car)工程化t细胞(car-ts)通过出版物j.am.chem.soc.2015,137(8),pp2832-2835中的描述制备。当该car-ts给予患者时,可以给患者施用fitc-b细胞自身抗原的缀合物或fitc-t细胞自身抗原(mhc-肽复合物)以治疗他的自身免疫疾病。缀合物的一个例示在图6中,通过灭活产生dna特异性自身抗体的b细胞来治疗狼疮。患有sle的患者将每周静脉内接受200mg~1g所述缀合物。注射治疗sle直至症状消失。
当针对癌细胞/自体免疫t/b细胞的亲和配体被针对细菌或病毒的亲和配体(例如针对细菌的抗体/适体)替换时,本发明的方法和试剂也可用于灭活病原体如病毒和细菌。
毒素/细胞抑制剂/灭活剂的实例包括但不限于能够杀死细胞或抑制细胞正常或特定功能的任何试剂(例如产生某些分子例如蛋白质(例如抗体),复制,分化,生长,发育成熟细胞或其他类型的细胞)。它们可以是放射性同位素,蛋白质,小分子,sirna,反义分子,酶等。它们的实例包括nk细胞毒因子,tnf如tnf-α和tnf-β(lt),穿孔素,颗粒酶,细胞凋亡诱导剂,自由基发生剂,细胞膜损伤剂,毒剂,化疗剂,sirna或反义核酸(用于细胞正常功能的核酸),细胞毒性剂等。有时它们可以制成前体型或非活性型,只有在它们与靶细胞结合或被靶细胞摄取后才变得有活性,例如前述抗原-道诺霉素缀合物。使用与细胞损伤试剂偶联的亲和分子广泛用于肿瘤的治疗。人们可以容易地采用它们的方法和原理用于本发明。如果细胞损伤试剂仅在细胞内有效,则通常涉及穿过细胞膜的机制,例如胞吞作用。
本发明还公开了通过将抗原和免疫抑制剂/药物的组合作为物理混合物或作为合成缀合物或作为纳米/微粒或脂质体应用于需要的对象/患者来治疗自身免疫疾病和过敏的方法和试剂。术语纳米/微米颗粒是指颗粒在纳米或微米范围内的尺寸(直径)。例如,纳米/微米颗粒的尺寸范围可以为50nm~50um。示例性免疫抑制药物的列表可以在维基百科的“免疫抑制药物”文章页面中找到。适用于本申请的免疫抑制剂/药物(免疫抑制剂)包括但不限于他汀类;mtor抑制剂,如雷帕霉素或雷帕霉素类似物;tgf-β信号传导因子;tgf-β受体激动剂;tlr(tolllikereceptor)抑制剂;模式识别受体抑制剂;nod样受体(nlr)抑制剂;rig-i样受体抑制剂;nod2抑制剂;组蛋白去乙酰化酶抑制剂,如曲古抑菌素a;糖皮质激素;线粒体功能的抑制剂,如鱼藤酮;p38抑制剂;nf-κβ抑制剂,如6bio,地塞米松,tcpa-1,ikkvii;腺苷受体激动剂;前列腺素e2激动剂(pge2),如米索前列醇;磷酸二酯酶抑制剂,如磷酸二酯酶4抑制剂(pde4),如咯利普兰;蛋白酶体抑制剂;激酶抑制剂;g蛋白偶联受体激动剂;g蛋白偶联受体拮抗剂;糖皮质激素;维甲酸;细胞因子抑制剂;细胞因子受体抑制剂;细胞因子受体激活剂;过氧化物酶体增殖物激活受体拮抗剂;过氧化物酶体增殖物激活受体激动剂;组蛋白去乙酰化酶抑制剂;钙调神经磷酸酶抑制剂;磷酸酶抑制剂;pi3kb抑制剂,如tgx-221;自噬抑制剂,如3-甲基腺嘌呤;芳烃受体抑制剂;蛋白酶体抑制剂i(psi);和氧化的atp,如p2x受体阻滞剂。免疫抑制剂还包括ido,维生素d3,环孢菌素,如环孢菌素a,芳烃受体抑制剂,白藜芦醇,硫唑嘌呤(aza),6-巯基嘌呤(6-mp),6-硫鸟嘌呤(6-tg),fk506,sanglifehrina,沙美特罗,霉酚酸酯(mmf),阿司匹林和其他cox抑制剂,尼氟酸,雌三醇和雷公藤内酯,siglec配体如唾液酸及其衍生物包括聚唾液酸唾液酸-脂质结合物。在实施方案中,免疫抑制剂可包含本文提供的任何药剂。免疫抑制剂可以是直接对apc提供免疫抑制(例如致耐受)作用的化合物,或者它可以是间接提供免疫抑制(例如致耐受)作用的化合物(即,在给药后通过某种方式被处理后)。因此,免疫抑制剂包括本文提供的任何化合物的前药形式。
免疫抑制剂还包括血红素氧合酶-1(ho-1)诱导剂,例如钴原卟啉(copp),含有三价铁离子的原卟啉ix(血红素b)和氯化物配体(hemin),血红素,铁原卟啉或血红素降解产物,以及pct/ep2015/074819中描述的那些。siglecs(唾液酸结合免疫球蛋白型凝集素)配体如唾液酸或其衍生物也是可用于本发明的另一类免疫抑制剂。pd-l1也是可用于本发明的另一类免疫抑制剂。pd-l1可有效抑制细胞毒性t细胞。也可以使用可以与pd-1结合的pd-l1的片段或模拟物或衍生物。其他可与抑制性检查点受体结合的抑制性配体(如a2ar,btla,ctla-4,kir,lag3,tim-3,vista等)如b7-h3,b7-h4也可用于代替pd-l1。可以促进t/breg扩增的分子(例如可以刺激t/breg扩增的细胞因子,例如il-2和tgf-β)也是另一种类型的免疫抑制剂。不同的免疫抑制剂可以作为混合物使用,并且可以在本发明中组合使用。
免疫抑制剂还包括编码本文中披露的肽,多肽或蛋白质的核酸,其导致免疫抑制(例如致耐受性)免疫应答。因此,在实施方案中,免疫抑制剂是编码导致免疫抑制(例如致耐受性)免疫应答的肽,多肽或蛋白质的核酸。核酸可以与合成纳米载体偶联。核酸可以是dna或rna,例如mrna。在实施方案中,本发明的组合物包含本文提供的任何核酸的互补物,例如全长互补物,或简并(由于遗传密码的简并性)。在实施方案中,核酸是表达载体,其可以在转染到细胞系中时转录。在实施方案中,表达载体可包含质粒,逆转录病毒或腺病毒等。可以使用标准分子生物学方法分离或合成核酸,例如通过使用聚合酶链反应产生核酸片段,然后将其纯化并克隆到表达载体中。
在一些实施方案中,本文提供的免疫抑制剂与合成纳米载体偶联。在优选的实施方案中,免疫抑制剂是除构成合成纳米载体结构的材料之外的元素。例如,在一个实施方案中,其中合成纳米载体由一种或多种聚合物组成,免疫抑制剂是另外并与一种或多种聚合物偶联的化合物。作为另一个实例,在一个实施方案中,其中合成纳米载体由一种或多种脂质组成,免疫抑制剂再次另外并与一种或多种脂质偶联。在实施方案中,例如合成纳米载体的材料也导致免疫抑制(例如,致耐受)效应的情况下,免疫抑制剂是除合成纳米载体的材料之外存在的元素,其导致免疫抑制(例如,致耐受)效应。
其他示例性免疫抑制剂包括但不限于小分子药物,天然产物,抗体(例如,抗cd20,cd3,cd4的抗体),基于生物制剂的药物,基于碳水化合物的药物,纳米颗粒,脂质体,rnai,反义核酸,适体,甲氨蝶呤,nsaids,芬戈莫德,那他珠单抗,阿仑单抗,抗cd16,抗cd3;他克莫司(fk506)等。其他免疫抑制剂是本领域技术人员已知的,并且本发明不限于此。另外适用的免疫抑制剂可以在专利和专利申请us13/880,778,us14/934,135,ca2910579,us13/084,662,us14/269,048,us8652487和selectabiosciences提交的其他专利申请中找到。
本发明公开了通过将抗原和免疫抑制剂的混合物局部施用于需要的对象/患者来治疗自身免疫疾病和过敏的方法和试剂。当抗原是药物(例如蛋白质药物)或其表位时,它还可用于抑制抗药物抗体的产生。它会诱导抗原的免疫耐受。适用于本申请的制剂的实例包括固体形式,例如粉末,凝胶,洗剂,软膏,溶液,喷雾剂,栓剂,锭剂,片剂和贴剂,其可局部施用于皮肤或粘膜。术语局部药物递送包括除注射之外的药物递送途径。它包括将药物应用于皮肤或粘膜。它包括鼻内给药,直肠给药,舌下给药和口腔粘膜给药。免疫抑制剂可以是活性药物形式,前药形式,微粒或纳米粒子形式或脂质体形式。抗原可以是b细胞抗原/表位或t细胞抗原/表位(例如mhc-肽复合物或其缀合物;或是可以与mhc结合的肽抗原)或它们的组合。该组合可以是b细胞抗原/表位与t细胞抗原/表位的组合;或几种不同b细胞抗原/表位和/或靶向相同疾病或不同疾病的几种不同t细胞抗原/表位的组合。使用非肽-mhc复合物形式的但是可与mhc结合然后在体内形成mhc-肽复合物(t细胞抗原)的肽抗原(t细胞表位),可以减小其大小和分子量,因此改善了透皮递送。它们的例子可以在当前的申请和相关出版物和专利申请中找到。
在一些实施方案中,该方法是使用含有抗原/过敏原和免疫抑制药物(上文列出的药物,例如雷帕霉素或福吉霉素或甲氨蝶呤或唾液酸或其衍生物或高亲和力siglec配体或它们的组合)的贴剂。唾液酸可以是游离唾液酸或唾液酸酯,唾液酸-脂质偶联物。例如,可以使用唾液酸的-cooh与胆固醇的-oh将唾液酸与胆固醇缀合以形成酯键。该缀合物将具有更好的透皮和细胞膜渗透能力。脂肪酸也可以与唾液酸的-oh偶联以形成缀合物。这些结合物在透皮递送后将作为免疫抑制药物起作用。高亲和力siglec配体的实例可以在专利us8357671中找到。
抗原和免疫抑制药物的透皮或透粘膜递送将通过皮肤中的dc细胞诱导免疫耐受。这对于食物过敏和自身免疫疾病治疗来说将是一种更方便的策略。皮肤可以是完整的或可以剥离以去除角质层以增加药物递送。微针系统也可用于皮肤。微针系统中的微针可以由生物可降解材料制成,例如应用plga包封抗原和免疫抑制剂。或者,也可以使用包封抗原和免疫抑制剂的生物可降解植入物。如果植入物是大颗粒,则植入物的尺寸可以大于10um直径,优选>100um。例如,用含有3mg雷帕霉素和1mg麦醇溶蛋白的plga制成的2mm(长度)×0.3mm(直径)的棒可用作皮下的植入物以治疗麸质过敏。也可以使用其他植入物形式,例如来自intarcia的medici药物递送系统或nanoprecisionmedical的nanoportalcapsule,只要它们可以同时递送抗原和免疫抑制剂。
dbvtechnologies和其他小组(例如,用于气过敏原和食物过敏的描述于doi:10.1007/s40521-013-0003-8,epicutaneousimmunotherapyforaeroallergenandfoodallergy中的那些)正在使用含有过敏原的皮肤贴剂通过诱导对抗原(过敏原)的耐受性来治疗过敏变态反应。这类表面局部贴剂或其他制剂可以很容易地转用于当前发明应用。例如,那些局部应用的制剂,例如us15/135,914,us6676961,us15/111,204,us8932562b2,us15/184,933a1和us8202533b2中描述的贴剂,以及那些商业来源的贴剂(例如viaskin®milk和viaskin®peanut),可以通过在其中添加额外的免疫抑制药物(例如0.1mg~20mg雷帕霉素或福吉霉素,或1mg~100mg甲氨蝶呤,或其衍生物或前药)而转用于本发明。除了贴剂含有免疫抑制剂外,其给药方法可以与现有技术基本相同。可以将附加的透皮促进剂(例如dmso,氮酮,脂肪酸,透明质酸等,这类物质以及它们的合适量可以在出版物中容易地找到)添加到贴剂中或在施用贴剂之前施用于皮肤。可加入透皮促进剂的实例包括dmso(例如10-300mg/贴剂),azone(例如总药物重量的1%~10%),表面活性剂,脂肪酸(例如1%~10%油酸)。皮肤也可以通过去角质处理或其他方式去除角质层以增强透皮递送。在一个实例中,贴剂含有500ug-10mg麸质蛋白(例如sigma#g5004,小麦麸质蛋白)和0.1mg~10mg雷帕霉素或1mg~50mg甲氨蝶呤,麸质蛋白和雷帕霉素和/或甲氨蝶呤可以是粉末形式或薄膜形式,可以简单地物理混合在一起或共同溶解,然后干燥,然后放入贴片中。在另一个实例中,贴剂含有5mg麸质蛋白(例如sigma#g5004,小麦麸质蛋白)和5mg雷帕霉素或50mg甲氨蝶呤和任选另外的30mg氮酮。在另一个实例中,贴剂含有5mg麸质蛋白(例如sigma#g5004,小麦麸质蛋白)和1g唾液酸或唾液酸-胆固醇缀合物,为粉末或脂质体形式的混合物。这可用于治疗麸质不耐症。麸质蛋白(谷蛋白)可以用麦醇溶蛋白代替。在实施方案中,贴剂可以每天施用共1-50周。在另一个实例中,抗原是花生抗原arah2200ug和2mg雷帕霉素一起在贴剂中以治疗花生过敏。在一个实施例中,将花生抗原arah2200ug,2mg雷帕霉素和50mg蔗糖溶解在水中,然后冻干,然后置于贴剂中。在一个实施例中,将花生抗原arah2200ug,2mg雷帕霉素,50mgsds和50mg蔗糖溶解在水中,然后冻干,然后置于贴剂中。在一个实施例中,将花生抗原arah2200ug,2mg雷帕霉素,100mgdmso和50mg蔗糖溶解在水中,然后冻干,然后置于贴剂中。在另一个实例中,抗原是前面图中用于治疗狼疮的双链dna(1mg~10mg),药物是3mg雷帕霉素或福吉霉素或替西罗莫司。在另一个实例中,鼻喷雾剂含有1mg麸质蛋白(例如来自sigma#g5004,小麦麸质蛋白)和1mg雷帕霉素或10mg甲氨蝶呤,采用相应合适的喷雾剂形式。在另一个实例中,舌下含片含有50mg麸质蛋白(例如来自sigma#g5004,小麦麸质蛋白)和1mg雷帕霉素或20mg甲氨蝶呤。在另一个实例中,凝胶剂为在每1ml凝胶中含有50mg麸质蛋白(例如来自sigma#g5004,小麦麸质蛋白)和2mg雷帕霉素或20mg甲氨蝶呤。免疫抑制药物或抗原或它们的组合可以是粉末或凝胶或半液体形式或脂质体形式(例如直径100nm~5μm)或纳米/微米颗粒(例如100nm~1um)或与树枝状聚合物或线性聚合物缀合(例如通过酯键偶联至聚丙烯酸或聚唾液酸以形成分子量=5,000~500,000道尔顿的基于聚合物的前药)。
其它药学上可接受量的抗原和免疫抑制剂也可以用于贴剂中,只要它可以产生令人满意的治疗(例如免疫耐受)效果,这可以通过用众所周知的方案和方法筛选和测试来实验确定。
抗原和免疫抑制药物透皮递送后被皮肤中抗原呈递细胞apc吞噬吸收,诱导/激活致耐受性树突细胞和treg/breg,抑制b细胞活化/抗体产生,生发中心形成和抗原特异性超敏反应,导致长期的抗原特异性免疫耐受。
皮肤贴剂(也称为透皮贴剂)是含有药物的粘性贴剂或有可附着性的贴剂,其置于皮肤上以通过皮肤递送特定剂量的药物并进入血流。现在有各种各样的药物以透皮贴剂形式提供。
有几种主要类型的皮肤/透皮贴剂。单层药物于粘合剂中类型是该给药系统的粘合剂层也含有药物。在这种类型的贴剂中,粘合剂层不仅用于将各个层与整个系统一起粘附到皮肤上,而且还负责药物的释放。粘合剂层由临时衬里和背衬围绕。多层药物于粘合剂类型类似于单层系统;但是其多层系统是不同的,因为它增加了另一层药物于粘合剂中,通常由膜隔开(但并非在所有情况下)。其中一层用于立即释放药物,而另一层用于控制药物从贮存器中释放。该贴片还具有临时衬垫层和永久背衬。由此释放的药物取决于膜渗透性和药物分子的扩散。储库类型不同于单层和多层药物于粘合剂系统,储库透皮系统具有单独的药物层。药物层可以是液体或凝胶或粉末隔室,其含有通过粘合剂层分离的药物溶液或悬浮液或粉末。此贴剂也有后背层支持。在这种类型的系统中,释放速率为零级。基质型具有固体或半固体基质的药物层,其含有药物溶液或悬浮液或固体层,例如粉末或薄膜。该贴剂中的粘合剂层围绕药物层,部分覆盖它。在一些实施方案中,储库类型和基质类型可用于本发明。
在一个实例中,通过使用溶剂浇铸方法制备负载了抗原和免疫抑制剂的基质型透皮贴剂。使用总面积为50cm2的培养皿。将抗原和免疫抑制剂溶解在5ml水/甲醇(1:1)溶液中并混合直至获得澄清溶液。使用200mg聚乙二醇400作为增塑剂,并使用任选的100mg丙二醇或油酸或吐温80作为渗透促进剂,将100mg蔗糖与抗原/免疫抑制剂溶液一起加入。将得到的均匀溶液浇铸在培养皿上,培养皿用甘油润滑并冻干或在室温下干燥24小时。然后将干燥的贴剂置于用作背衬膜的醋酸纤维素膜上。在另一个实施例中,将称好重量的pva(2.5%w/v)加入蒸馏水中,通过在60℃下持续搅拌和间歇加热几秒钟制成均匀溶液并倒入已经用铝箔在开口端周围包裹的玻璃模具中,并保持在60℃下干燥6小时,形成光滑,均匀和透明的背衬膜。背膜用作含有抗原和免疫抑制剂的基质的支持物。
在一些实施方案中,本发明方法中使用的皮肤贴剂装置优选包括背衬,所述背衬的周边适于与皮肤形成气密封闭的腔室。该背衬在腔室内的面向皮肤的一侧承载用于降低皮肤过敏反应性的组合物。优选地,背衬的周边具有粘合性并形成气密接合,以与皮肤形成密闭的腔室。
在一个具体实施方案中,过敏原和免疫抑制剂组合物通过静电和/或范德华力保持在背衬上。该实施方案特别适用于组合物过敏原为固体或干燥形式(例如颗粒)的情况,尽管它也可间接地用于过敏原为液体形式的情况。在本发明的上下文中,术语“静电力”通常表示涉及电荷的任何非共价力。术语范德瓦尔斯力表示在背衬表面和固体过敏原之间产生的非共价力,可以是三种类型:永久偶极子力,诱导偶极子力和伦敦范德华力。静电力和范德华力可以单独或一起起作用。在这方面,在优选实施例中,贴片装置包括静电背衬。如本文所用,表述“静电背衬”表示由能够累积静电荷和/或产生范德华力的材料制成的任何背衬,例如通过摩擦,加热或电离,以及保存这些电荷。静电背衬通常包括具有空间电荷的表面,其可以均匀地分散或不均匀地分散。取决于构成所述背衬的材料,以及用于产生电荷的方法,出现在背衬表面的一侧或另一侧上的电荷可以是正的或负的。在所有情况下,分布在背衬表面上的正电荷或负电荷在导电或非导电材料上引起吸引力,从而允许维持过敏原和免疫抑制剂。颗粒也可以被电离,从而在颗粒和背衬之间产生相同类型的静电吸引力。适于提供静电背衬的材料的实例是玻璃或选自包括纤维素塑料(ca,cp),聚乙烯(pe),聚对苯二甲酸乙二醇酯(pet),聚氯乙烯(pvc),聚丙烯,聚苯乙烯,聚碳酸酯,聚丙烯酸类的聚合物的聚合物。特别是聚(甲基丙烯酸甲酯)(pmma)和含氟聚合物(例如ptfe)。上述列表绝不是限制性的。
背衬的背面可以覆盖有签条,该签条可以在施用之前剥离。例如,当背衬至少部分半透明时,该签条使得可以将组合物过敏原储存在黑暗中。由于存在湿气导致的薄水膜,可以增强或降低表面和颗粒之间的力的强度。通常,贴剂制成并保存在干燥的地方。水分应足够低,以保持活性成分。可以调节水分率以获得最大的附着力。如上所述,在过敏原为干燥形式(例如颗粒形式)的情况下,使用静电背衬是特别有利的。此外,技术人员可以调节粒度以提高静电和/或范德华力的效率,以将颗粒保持在载体上。
在一个具体实施方案中,贴剂包含聚合物或金属或金属涂覆的聚合物背衬,并且组合物过敏原的颗粒基本上通过范德瓦尔斯力保持在背衬上。优选地,为了通过范德华力将颗粒保持在载体上,颗粒的平均尺寸小于60微米。在另一个实施方案中,通过背衬上的粘合剂涂层将过敏原保持在背衬上。背衬可以完全用粘合材料覆盖或仅部分覆盖。可以使用不同的闭合背衬,例如涂有铝的聚乙烯或pet薄膜,或具有粘合剂层(丙烯酸,硅树脂等)的pe,pvc或pet泡沫。用于本发明的贴剂装置的实例公开在专利申请us11/915,926或美国专利no.美国专利号7,635,488。
其他实例公开在us13/230,689中,其还公开了喷雾干燥方法,以将颗粒形式的物质加载到贴剂装置的背衬上。电喷雾装置使用高压将液体分散在细小气溶胶中。然后将溶解在溶剂中的过敏原和免疫抑制剂在贴剂背衬上粉碎,其中溶剂蒸发,留下颗粒形式的过敏原和免疫抑制剂。根据所需的蒸发时间,溶剂可以是例如水或乙醇。技术人员可以选择其他溶剂。这种在贴剂背衬上施加物质的方法允许纳米尺寸和单一尺寸的颗粒在背衬上具有规则且均匀的颗粒重新分配。该技术适用于任何类型的贴剂,例如具有背衬的贴剂,所述贴剂包括绝缘聚合物,掺杂的聚合物或有导电层的聚合物。优选地,背衬包括导电材料。
在另一个实施方案中,背衬的周边用干燥的亲水性聚合物覆盖,能够通过与湿润的皮肤接触形成粘合性水凝胶膜(如us12/680,893中所述)。在该实施方案中,在施用贴剂之前必须使皮肤保湿。当水凝胶与湿润的皮肤接触时,聚合物颗粒吸收液体并变成粘合剂,从而当贴剂施用于皮肤上时产生密闭的腔室。这种水凝胶的实例包括聚乙烯吡咯烷酮,聚丙烯酸酯钠,甲基乙烯基和马来酸酐共聚物醚。
在另一个具体实施方案中,过敏原和免疫抑制剂组合物液体在吸收材料储库中,保持在贴剂的支持物上。该组合物可以由过敏原+免疫抑制剂溶液组成,或者是混合物分散体中,例如在甘油中。吸附材料可以由例如乙酸纤维素制成。
背衬可以是刚性的或柔性的,可以是或不是亲水的,取决于组成材料,可以是半透明的或不是半透明的。在为玻璃的情况下,通过将一片塑料粘合到玻璃上,可以使支撑件具有抗破裂性。在一个实施方案中,贴剂的背衬含有透明区,允许直接观察和控制炎症反应,而不必去除贴剂。合适的透明材料包括聚乙烯薄膜,聚酯(聚对苯二甲酸乙二醇酯)薄膜,聚碳酸酯和各种透明或半透明的生物相容性薄膜或材料。
图7显示了与碳水化合物聚合物缀合以形成前药的例子。新型前药可以是碳水化合物(或其他聚合物)药物缀合物的形式,其中药物通过可裂解键连接到碳水化合物(或其他聚合物)上。可以将多于一种药物缀合到聚合物主链上。合适的碳水化合物包括含唾液酸的聚合物,透明质酸,硫酸软骨素,葡聚糖,羧基葡聚糖,纤维素,羧基纤维素及其衍生物。在一些实施方案中,优选地,碳水化合物选自含唾液酸的聚合物,透明质酸,淀粉,葡聚糖和硫酸软骨素。优选地,药物与聚合物骨架缀合,通过具有可生物降解的连接子或键,例如酯键或含有酯键的连接子。酯键的实例可以是在碳水化合物的-cooh基团和药物的-oh之间形成的酯键,或者如果药物含有-cooh基团,则在碳水化合物的-oh基团和药物的-cooh之间形成的酯键。例如,碳水化合物或其他聚合物载体的平均mw在1000~100,000道尔顿之间。碳水化合物是长链聚合物。结合后,它将携带多个药物分子。优选地,在每个碳水化合物分子或其他聚合物骨架上缀合的药物的数量>5。在一些实施方案中,在每个聚合物主链上缀合的药物的数量>10。
适用于本发明的含唾液酸的聚合物包括由与α2,3或α2,6或α2,8或α2,9键连接的唾液酸单体或它们的组合形成的聚唾液酸。它还包括接枝聚合物或含有唾液酸的支化聚合物。它也可以是线性聚合物主链骨架(例如葡聚糖或合成聚合物,例如pva,paa)。图8显示了与雷帕霉素缀合的聚唾液酸通过酯键形成前药的实例。r也可以用脂质类型分子代替,以用于纳米/微粒包封或如上所述用于脂质体。还可以在药物和聚合物主链之间添加连接子。图9显示连接子是甘氨酸的实例。图9中的药物r可以是雷帕霉素或其他免疫抑制药物。图10显示了基于透明质酸的甲氨蝶呤前药的实例。
此外,免疫抑制药物也可以直接与抗原缀合或通过连接子或载体与抗原缀合,并用于贴剂中。载体可以是聚合物。例如,图8中的聚唾液酸-雷帕霉素可用于通过edc偶联的蛋白质赖氨酸结合(例如麸质蛋白或抗体药物或麦醇溶蛋白或花生抗原蛋白arah2)并用于贴剂中(例如100ug~15mg)代替抗原和药物的混合物。图11显示了含有抗原和雷帕霉素的缀合物结构的实例。
其他化学手段如马来酰亚胺-sh偶联也可用于将药物与抗原偶联(通过连接子或聚合物载体)。缀合物的通用结构是抗原-药物或抗原-连接子-药物或抗原-载体-药物。可以将多于一种药物分子与每个抗原缀合。如果使用聚合物载体,则所得的缀合物可含有多种抗原和多种药物分子。在一些实施方案中,如果抗原是b细胞抗原,则每个聚合物中抗原分子的数目小于6以避免补体活化。图12显示了3种不同形式的抗原-药物缀合物的实例。
当使用脂质体时,可以将药物包封在脂质体中或抗原和免疫抑制药物两者都包封在脂质体中。
皮肤中树突状细胞丰富,在贴片中加入dc调节药物和抗原/过敏原可有效诱导耐受。
除局部施用外,还可以注射或口服混合物或缀合物以诱导免疫耐受并治疗自身免疫疾病/过敏。
局部制剂或植入物可含有抗原+药物或抗原-药物缀合物或包封的抗原/药物(例如在微球或脂质体中)或它们的组合。抗原可以是粗抗原(例如花生提取物,麸质蛋白)或纯化抗原(例如花生抗原蛋白arah2,麦醇溶蛋白)或抗原-药物缀合物或包封抗原(例如微球或脂质体)或它们的混合物的形式。
在另一种形式中,如图13所示,表位(抗原)-富含唾液酸聚合物的缀合物或表位(抗原)-富含siglec配体的聚合物的缀合物可用于治疗自身免疫性疾病或过敏或诱导免疫耐受,可以是注射或植入(封装在植入物内)或局部施用。可以使用药学上可接受量的缀合物,只要它可以产生令人满意的治疗(例如免疫耐受)效果,其可以通过用众所周知的方案筛选和测试来实验确定。
术语“富含唾液酸的聚合物”是指具有与其主链骨架缀合的多个唾液酸或siglec配体的聚合物。骨架可以是支链或线性聚合物或树枝状聚合物,例如合成聚合物pva,paa,多胺,或天然聚合物,例如聚唾液酸,碳水化合物。唾液酸或含有唾液酸的片段或siglec配体与聚合物骨架缀合。唾液酸聚合物含有可以与siglec结合的α2,3或α2,6或α2,8唾液酸苷或唾液酸或其衍生物(例如jimmunol.2006sep1;177(5):2994-3003,专利申请us9522183和专利us8357671中描述的那些)。具有α2,8连接骨架的寡/聚唾液酸本身也是富含唾液酸的聚合物。富含唾液酸的聚合物还可在其骨架上含有不同的唾液酸苷,唾液酸和/或其衍生物的混合物。在其表面上附着有唾液酸或唾液酸苷的脂质体也可以被认为是富含唾液酸的聚合物(例如在专利申请us9522183中描述的那些)。
有许多适用于本申请的富含唾液酸/siglec配体的聚合物可以容易地在文献中找到,例如描述于jimmunol.2006sep1;177(5):2994-3003,natchembiol.2014jan;10(1):69-75,jamchemsoc.2013dec11;135(49):18280-18283,jimmunol.2014nov1;193(9):4312-21,jallergyclinimmunol.2017jan;139(1):366-369.e2,angewchemintedengl.2015dec21;54(52):15782-8,procnatlacadsciusa.2009feb24;106(8):2500-5,jexpmed.2010jan18;207(1):173-87,jimmunol.2013aug15;191(4):1724-31,procnatlacadsciusa.2016sep13;113(37):10304-9,jclininvest.2013jul;123(7):3074-83,procnatlacadsciusa.2016mar22;113(12):3329-34,专利申请us9180182和美国专利us9552183中的。这些富含唾液酸/siglec配体的聚合物可以容易地转用于本发明。在一些实施方案中,当使用b细胞抗原时,每种聚合物与少于6个拷贝的抗原缀合以降低补体活化的风险,在一些实施方案中,每种聚合物仅与一种抗原缀合。在一些实施方案中,每种聚合物与超过10个拷贝的抗原缀合。
使用表位(抗原)-富含唾液酸聚合物的缀合物,抗原将与自身免疫t细胞或b细胞克隆结合,这将引导富含共轭唾液酸的聚合物选择性地灭活这些抗原特异性自身免疫t细胞或b细胞克隆。
图14显示了适用于本发明的含有唾液酸/siglec配体的缀合物的例子。可以在抗原和聚合物之间和/或在siglec配体和聚合物之间添加任选的连接子。
当使用表达抗原和siglec配体的脂质体时(例如本发明中描述的那些和jclininvest.2013jul;123(7):3074-83,jimmunol.2013aug15;191(4):1724-31和美国专利us9552183中描述的那些),脂质体可以进一步包封免疫抑制药物如雷帕霉素。例如,每个脂质体颗粒可含有药物有效量的雷帕霉素(例如雷帕霉素为1%~50%脂质体重量)。这将进一步提高诱导免疫耐受和治疗自身免疫疾病/过敏的功效。
适用于当前应用的另一种形式是使用微球。术语微球包括从纳米尺寸到微米(例如直径50nm~5um)的颗粒。优选地,微球是生物可降解的(例如由可生物降解的聚合物如聚丙交酯乙交酯共聚物(plga)制成),微球可以进一步包封免疫抑制药物,例如雷帕霉素(其含量例如微球的1%~80%重量)。
图15显示了用于诱导免疫耐受和治疗自身免疫疾病/过敏的基于微球的药剂的结构的示意性例子。例如,微球可以是可生物降解的合成聚合物,例如plga。免疫抑制药物如雷帕霉素(例如以微球的1%~80%重量)被包封。微球的尺寸为3μm或300nm。富含唾液酸的聚合物或其他siglec配体直接或通过连接子与微球表面缀合,抗原也直接或通过连接子与微球表面缀合。或者,富含唾液酸的聚合物直接或通过连接子与微球表面缀合,并且抗原与富含唾液酸的聚合物缀合。抗原也可以包封在微球体中。或者,药物(免疫抑制剂)可以与微球体的表面缀合或与富含唾液酸的聚合物缀合而不是被包封。适用于本申请的微球的实例可以容易地从诸如专利申请us13/880,778,us14/934,135,ca2910579,us13/084,662和专利us8652487以及由selectabiosciences提交的其他专利申请中的那些出版物中的公开内容得到转用。它可用于治疗自身免疫疾病或过敏或诱导免疫耐受,其可以注射或植入(封装在植入物内)或局部施用于患者。可以使用这些类型的缀合物的药学上可接受的量,只要它可以产生令人满意的治疗(例如免疫耐受)效果,这可以通过用众所周知的方案筛选和测试来实验确定。
适用于本申请的另一种形式是使用与抗原,siglec配体和/或其他免疫抑制剂缀合的聚合物载体,如图16所示。或者,siglec配体和其他免疫抑制剂都可以与抗原缀合。图16显示了适用于本发明的不同形式。与多抗原(例如1-100),多个siglec配体(例如5~500个拷贝)和多拷贝的其他免疫抑制剂缀合的聚合物基本上是先前描述的与抗原和siglec配体缀合的聚合物,并其进一步与多个免疫抑制剂分子缀合(例如5~500个分子)。或者,与多个免疫抑制剂分子和多个siglec配体缀合的聚合物可以与一个抗原分子缀合。或者,多个免疫抑制剂分子和多个siglec配体可以直接或通过连接子与一个抗原分子缀合但不含聚合物载体。或者,可以将一个或多个与多个免疫抑制剂分子缀合的聚合物和一个或多个与siglec配体缀合的多个聚合物缀合到一个抗原分子上。或者,可以将一个或多个与多个免疫抑制剂分子缀合的聚合物和一个或多个与siglec配体缀合的聚合物缀合在一起,然后与一种抗原分子缀合。
它们可用于治疗自身免疫疾病或过敏或诱导由用于构建这些缀合物的抗原引起的免疫耐受,其可以注射或植入(被包封在植入物内)或局部施用于需要的受试者。可以使用在药学上可接受的制剂中的药学上可接受的量的缀合物,只要它可以产生令人满意的治疗(例如免疫耐受)效果,其可以通过用众所周知的方案筛选和测试来实验确定。该方法可用于治疗抗原特异性自身免疫疾病或过敏。
用于系统性红斑狼疮(sle)的富含唾液酸的聚合物-抗原缀合物的示例显示在图17中。用于sle治疗的唾液酸聚合物-抗原缀合物具有dna-连接子-唾液酸聚合物的结构。在一个实例中,患有sle的患者将每周静脉内接受200mg~1g所述缀合物,注射治疗sle。
使用抗原和免疫抑制剂组合的上述透皮递送系统用于过敏,自身免疫疾病和抗药物抗体治疗。当用免疫增强剂(例如疫苗佐剂如tlr激动剂)代替上述实施例和方法中的免疫抑制剂并且抗原是病原体抗原时,透皮递送系统就成为病原体抗原的疫苗或疫苗加强剂。例如,透皮递送系统是皮肤贴剂,其含有免疫增强剂以及病原体抗原,任选的透皮递送促进剂(例如,azone,脂肪酸,透明质酸),配伍在viaskin®贴片或类似的皮肤贴片样结构中。它也可以是乳液,凝胶,液体,喷雾剂,薄膜或适于局部施用于皮肤或膜的其他剂型。疫苗佐剂型分子如tlr激动剂可用于本发明,例如mpla,cpgodn,咪喹莫特,聚ic,瑞喹莫德,加地喹莫德,r848和3m-052。抗原的实例可以是合成的或纯化的,或者是由病原体制成的混合物。例如,它可以是hivgp-120,它可以是流感神经氨酸酶,它可以是流感病毒裂解物,它可以是hbv表面抗原,它可以是肿瘤细胞裂解物。使用这些抗原将产生针对病原体的免疫应答而作为疫苗或疫苗加强剂。
在一些实施方案中,局部制剂在每个贴剂中含有0.1~100mg抗原,0.1~50mgtlr激动剂或0.1~100mg抗原,0.1~50mgtlr激动剂于每ml凝胶/洗剂/液体。也可以向其中加入透皮增强剂,例如dmso,azone(例如1%~10%),表面活性剂,脂肪酸(例如1%~10%油酸)。在一个实例中,制剂含有10mg/ml流感病毒裂解物,5mg/ml咪喹莫特,20mg/mlsds于1xpbs和5%蔗糖中,然后冻干。冻干粉末可用于制备皮肤贴剂并以10~500mg粉末/贴剂附着于皮肤。在另一个实例中,将10~100mghbv表面抗原,5-50mg咪喹莫特混合在一起并加入到类似viaskin的皮肤贴片结构中。它可以每周两次施用于皮肤,持续2周,每次作为疫苗接种2天,然后在1个月和3个月后作为加强剂施用2天以产生针对hbv的免疫力。在另一个实例中,将100mg病原体抗原,20mg聚ic,20mg咪喹莫特和100mgdmso混合在一起并加入皮肤贴剂中。它可以每周两次施用于皮肤,持续2周,每次作为疫苗接种2天,然后在1个月和3个月后作为加强剂施用2天以产生针对所述病原体的免疫力。病原体抗原可以是可以与mhc结合形成mhc-肽复合物的抗原肽。使用抗原肽代替mhc-肽复合物可以促进透皮给药。
本文描述的化合物可以作为与药学上可接受的载体一起配制的药物或药品施用。因此,该化合物可用于制备药物或药物组合物。本发明的药物组合物可以配制成用于肠胃外给药的溶液或冻干粉末。粉末可以在使用前通过加入合适的稀释剂或其它药学上可接受的载体来重构。液体制剂可以是缓冲的,等渗的水溶液。粉末也可以以干燥形式喷雾。合适的稀释剂的实例是正常的等渗盐水溶液,标准的5%葡萄糖水溶液,或缓冲的乙酸钠或乙酸铵溶液。此类制剂特别适用于肠胃外给药,但也可用于口服给药或包含在计量剂量吸入器或雾化器中用于吹入。化合物可配制以包括其他医学上有用的药物或生物制剂。所述化合物还可以与对本发明化合物所针对的疾病或病症有用的其他药物或生物制剂联合给药。
如本文所用,短语“有效量”是指足以提供足够高的浓度以对其接受者产生有益效果的剂量。任何特定受试者的特定治疗有效剂量水平将取决于多种因素,包括所治疗的病症,病症的严重程度,特定化合物的活性,给药途径,化合物的清除率,治疗持续时间,与化合物组合或同时使用的药物,受试者的年龄,体重,性别,饮食和一般健康状况,以及医学领域和科学中众所周知的相似因素。在确定“治疗有效量”时考虑的各种一般考虑因素是本领域技术人员已知的并且已有描述。剂量水平通常落在约0.001至100mg/kg/天的范围内;通常适用的水平范围为约0.05至10mg/kg/天。化合物可以肠胃外给药,例如血管内,静脉内,动脉内,肌肉内,皮下等。给药还可以通过气溶胶口服,经鼻,直肠,透皮或吸入给药。化合物可以推注给药,或缓慢输注。最初可以通过从细胞培养测定ic50测定估计治疗有效剂量。然后可以在动物模型中配制剂量以达到血药浓度范围,血药浓度范围包括在细胞培养中测定的ic50。这些信息可用于更准确地确定人体中有用的初始剂量。血浆中的药物水平可以例如通过hplc测量。确切的配方,给药途径和剂量可以由个体医生根据患者的病情选择。
在当前的申请中,“/”标记表示“和”和“或”。除非另外定义,否则本文使用的所有技术和科学术语具有与本发明所属领域的普通技术人员通常理解的含义相同的含义。本说明书中提及的所有专利和出版物表示本发明所属领域的技术人员的水平。所有专利和出版物在此引入作为参考,其程度如同每个单独的出版物被具体和单独地指出通过引用并入。上述发明涉及许多众所周知的化学,仪器,方法和技能。技术人员可以容易地从诸如化学教科书,科学期刊论文和其他众所周知的参考源之类的教科书中找到相关知识。
sequencelisting
<110>王,天欣
<120>一种治疗自身免疫性疾病和过敏的方法和试剂
<130>1
<160>2
<170>patentinversion3.5
<210>1
<211>20
<212>dna
<213>人工合成
<400>1
gtgtgtgtgtgtgtgtgtgt20
<210>2
<211>20
<212>dna
<213>人工合成
<400>2
cacacacacacacacacaca20
- 还没有人留言评论。精彩留言会获得点赞!