用于治疗痤疮的局部组合物的制作方法
本发明涉及局部配方,包含植物提取物与附加成分的不同混合物。本发明还涉及该配方在治疗痤疮中的用途。
背景技术:
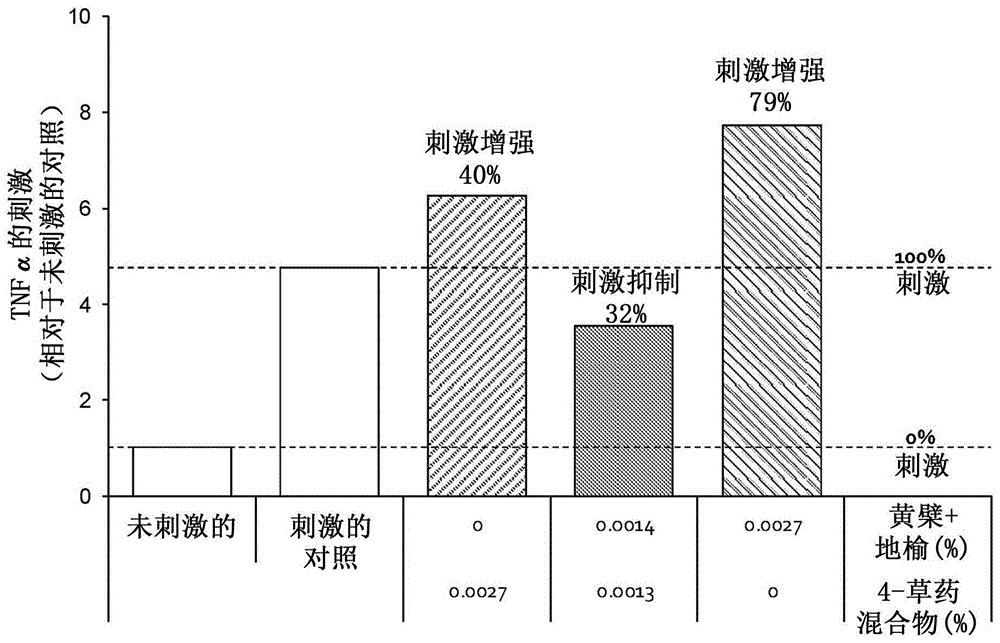
:寻常痤疮(囊肿性痤疮或“痤疮”)是一种常见的人类皮肤病,其以具有发红、粉刺(黑头和白头)、丘疹(针头)、脓疱(丘疹)、结节(大丘疹)和可能的疤痕的皮肤区域为特征。痤疮主要影响具有最密集的皮脂腺毛囊群的皮肤;这些区域包括面部、胸部上部和背部。严重的痤疮是炎症性的,但痤疮也可以以非炎症形式出现。病变是由毛囊皮脂腺单位(由毛囊及其相关皮脂腺组成的皮肤结构)的变化、需要雄激素刺激的变化引起的。痤疮最常见于青春期,并且通常持续到成年期。鉴于已知的痤疮治疗的缺点,需要一种包含草药的局部组合物用于治疗痤疮。技术实现要素:根据本发明的一些实施方式,提供了一种局部配方,其包含马齿苋(portulacaoleracea)提取物、掌叶大黄(rheumpalmatum)根提取物、野菊(chrysanthemumindicum)花提取物、黄芩(scutellariabaicalensis)根提取物、黄檗(phellodendronamurense)树皮提取物和地榆(sanguisorbaofficinalis)根提取物或它们的活性分子。根据本发明的一些实施方式,所述局部配方用于治疗或预防痤疮。根据本发明的一些实施方式,所述配方进一步包含锡兰肉桂(cinnamomumzeylanicum)树皮提取物、欧洲云杉(piceaabies)提取物、甘油或它们的任何组合。根据本发明的一些实施方式,所述配方包含水杨酸,水杨酸可以在0.1-5.0%w/w的范围内。根据本发明的一些实施方式,所述配方是凝胶的形式。根据本发明的一些实施方式,提供了一种治疗痤疮的方法,包括将本发明的组合物局部施用于需要的受试者的步骤。本发明的实施方式涉及一种局部配方,包含草药提取物马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根提取物、黄檗树皮提取物和地榆根提取物或它们的活性分子。进一步的实施方式涉及如本文详述的这种配方在治疗或预防痤疮中的用途。根据一些实施方式,所述局部配方包括抗炎化合物、抗微生物剂、益生元成分、皮肤水合增强成分、镇痛剂、抗氧化剂、皮脂调节剂、角质层分离剂或它们的任何组合。根据一些实施方式,所述局部配方进一步包含锡兰肉桂树皮提取物、欧洲云杉提取物、甘油或它们的任何组合。根据一些实施方式,所述局部配方进一步包含水杨酸。根据一些实施方式,所述水杨酸在所述局部配方中的量在0.1-5.0%w/w的范围内。根据一些实施方式,所述局部配方是凝胶。根据一些实施方式,所述局部配方的ph在4.0-5.5的范围内。根据一些实施方式,所述草药提取物在所述局部配方中的组合浓度为至少1%w/w。根据一些实施方式,所述局部配方包含总计约5.5%w/w的野菊花、马齿苋、掌叶大黄根和黄芩根的提取物;约3%w/w的地榆根和约3%w/w的黄檗树皮。根据一些实施方式,所述局部配方包含约1.5%w/w野菊花提取物、约1.5%w/w马齿苋提取物、约1.5%w/w掌叶大黄根提取物和约1.0%w/w黄芩根提取物。进一步的实施方式涉及一种治疗痤疮的方法,包含局部施用本文公开的局部组合物的步骤。进一步的实施方式涉及一种局部配方,包含马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根提取物和黄檗树皮提取物或它们的活性分子。附图说明图1显示了各种组合物对用egf/lps(表皮生长因子/脂多糖)刺激的角质形成细胞分泌tnf-α的结果;图2显示了使用各种组合物获得的关于用lps刺激的人皮肤释放il-8的结果;图3显示了使用各种组合物获得的关于用佛波醇12-肉豆蔻酸酯13-乙酸酯(pma)刺激的人造皮肤分泌il-8的结果;图4显示了使用各种组合物获得的关于用pma刺激的人造皮肤分泌il-1α的结果;图5显示了琼脂平板病原体抑制实验的结果;图6和图9显示了不同处理下表皮葡萄球菌的生长情况,显示了草药提取物的益生元特征;图7和图8分别显示了各种草药提取物在促进或抑制表皮葡萄球菌或头状葡萄球菌的生长中的活性;图10、11和12显示了受试者炎性病变的红斑(图10),高度(图11)和整体印象(图12);和图13显示了治疗前(a)和治疗后(b)的痤疮丘疹的外观。具体实施方式本发明的一个实施方式是一种局部配方,包含马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根提取物、黄檗树皮提取物和地榆根提取物或它们的活性成分,如下详述用于治疗痤疮。根据一些实施方式,所述局部配方进一步包含水杨酸、锡兰肉桂树皮提取物、欧洲云杉提取物、甘油或它们的任何组合。提取物中几种活性成分的列举草药标记物黄芩黄芩苷野菊蒙花苷地榆没食子酸马齿苋黄酮类化合物掌叶大黄大黄酸黄檗小檗碱根据一些实施方式,所述局部配方包括抗炎成分、皮脂调节成分、抗微生物成分、益生元成分、皮肤水合增强成分、镇痛剂、角质层分离成分、抗氧化剂及其任何组合中的一种或多种。根据一些实施方式,本文所述的局部配方中的活性成分提供治疗痤疮的协同效应。根据进一步的实施方式,所述配方中掌叶大黄根提取物、马齿苋提取物、野菊花提取物、黄芩根提取物、黄檗树皮提取物和地榆根提取物或其有效成分中的至少两种或更多种的组合提供治疗痤疮的协同效应。所述协同/互补效应可以通过增强抗炎活性、通过益生元作用、通过抗菌作用、通过增强活性成分向皮肤中的渗透、通过降低皮肤刺激或者它们的任何组合来治疗病症。掌叶大黄根提取物、黄芩根提取物、黄檗树皮提取物、地榆根提取物或它们的活性物以及锡兰肉桂树皮提取物可以通过表现出抗菌(尤其是抗痤疮丙酸杆菌(anti-p.acne))活性来起作用,其对治疗痤疮瑕疵有益。野菊花提取物和掌叶大黄根提取物或其活性成分可通过展示益生元活性(尤其是亲表皮葡萄球菌活性)而协同地起作用,这有利于平衡皮肤的天然微生物群,并因此有利于治疗痤疮瑕疵。在青春期期间,过量的睾酮会增加皮脂的产生。游离睾酮(雄激素)穿透皮脂腺细胞,并转化为5α还原酶介导的二氢睾酮(dth)。黄芩和掌叶大黄降低雄激素受体的表达,因此可用于减少雄激素介导的皮脂腺活动刺激,导致皮脂产生减少。锡兰肉桂树皮提取物通过抗-5α-还原酶作用调节皮脂生产。因此,掌叶大黄和黄芩根提取物或它们的活性成分与锡兰肉桂树皮提取物(sepicontrola5)或任何其它等效成分的组合,可能协同地减少皮脂分泌和从皮肤吸收油。水杨酸是一种广泛用于局部痤疮制剂的角质层分离剂。其可能增强其它草药活性成分的渗透。掌叶大黄根提取物、黄芩根提取物、黄檗树皮提取物、地榆根提取物以及锡兰肉桂树皮提取物和欧洲云杉提取物具有抗氧化特性。因此,其组合或者任何其它等效成分的组合可能协同地增强草药提取物的抗氧化活性,因此减轻痤疮严重程度和症状。根据进一步的实施方式,所述局部配方包含水杨酸。根据进一步的实施方式,所述局部配方包含至少0.1%w/w的水杨酸。根据进一步的实施方式,所述局部配方包含至少1.0%w/w的水杨酸。根据进一步的实施方式,所述局部配方包含至少1.5%w/w的水杨酸。根据进一步的实施方式,所述局部配方包含0.1-5.0%w/w的水杨酸。根据进一步的实施方式,所述局部配方包含1-3%w/w的水杨酸。根据进一步的实施方式,所述局部配方包含1.5-2.5%w/w的水杨酸。根据进一步的实施方式,所述局部配方包含约2%的水杨酸。根据一些实施方式,所述局部配方的ph介于约3.0-6.0。根据进一步的实施方式,所述局部配方的ph介于约3.5-5.0。根据进一步的实施方式,所述局部配方的ph介于约4.5-5.0。根据一些实施方式,所述配方中草药提取物的组合浓度为至少1%。根据一些实施方式,所述配方中草药提取物的组合浓度为至少2.5%。根据一些实施方式,所述配方中草药提取物的组合浓度为至少5%。根据一些实施方式,所述配方中草药提取物的组合浓度为至少7.5%。根据一些实施方式,所述配方中草药提取物的组合浓度为10-12.5%。根据一些实施方式,所述配方中草药提取物的组合浓度为11.5%。使用常规方法,根据预期用途,可将本发明的配方配制成各种制剂。这些制剂包括但不限于医用局部皮肤组合物和局部皮肤化妆品组合物。作为医用局部皮肤组合物和局部皮肤化妆品组合物,可以使用许多形式的凝胶、软膏、肥皂、乳膏和洗剂。所述配方可以任何合适的方式施用,即通过手、刮刀、喷雾或垫施用。本发明的配方可以是乳膏的形式。本发明的配方可以施用于受痤疮影响的整个皮肤区域或局部施用于每个疮。当应用于人体皮肤时,本发明的配方显示出高的皮肤相容性和低刺激性。根据一些实施方式,将所述配方施用于身体并随后例如通过用水洗涤从身体上除去。当本发明的局部组合物用作化妆品组合物时,化妆品或皮肤病学可接受的成分可任选地按需要以任意组合掺入并根据本领域技术人员确定。根据一些实施方式,该组合物可包括油、脂肪、蜡、洗涤剂、调理剂、ph调节剂、防腐剂、溶剂、粘度调节剂、着色剂、香料、染料等。所述组合物可以是以下形式:水包油、油包水、水包油包水和硅酮包水包油乳液,乳膏,软膏,水溶液,洗剂,肥皂,糊剂,泡沫,乳液,凝胶,油膏,油,洗液,调理剂或气溶胶。根据本发明的一个实施方式,本发明的组合物每天施用一次。根据其它实施方式,所述组合物每天施用两次、每天施用三次或更多次。根据本发明的一些实施方式,所述组合物施用约1天,10天或更长,20天,30天,60天,90天,120天或更长时间。在本发明的一些实施方式中,所述组合物还含有清洁剂或洗涤剂,它们通常是阴离子、阳离子、非离子或两性表面活性剂。典型的阴离子表面活性剂是羧酸盐、磺酸盐、硫酸盐或磷酸盐,例如脂肪酸皂、十二烷基硫酸盐和月桂基醚硫酸盐。阳离子表面活性剂的实例是衍生自脂肪和松香酸的脂族单-、二-和多-胺,胺氧化物,乙氧基化烷基胺和咪唑啉类。非离子表面活性剂的实例是聚氧乙烯表面活性剂、烷基酚乙氧基化物、羧酸酯,例如甘油单酯和甘油二酯、聚氧乙烯酯和脂肪酸二乙醇胺缩合物。两性表面活性剂是含有上述阴离子和阳离子基团的组合的那些,特别是含有酸性羧基和碱性氮基团的那些。典型的两性表面活性剂是咪唑啉类和甜菜碱类,例如月桂酸和肉豆蔻酸咪唑啉类和甜菜碱类,以及酰胺丙基甜菜碱类。所述局部药物组合物还可包含合适的乳化剂,其是指增强或促进混合和悬浮水包油或油包水的试剂。本文使用的乳化剂可以由单一乳化剂组成,或者可以是非离子、阴离子、阳离子或两性表面活性剂或者两种或更多种此类表面活性剂的共混物;优选用于本文的是非离子或阴离子乳化剂。此类表面活性剂描述于mccutcheondivision,mcpublishingcompany,175rockroad,glenrock,n.j.07452,usa于1980年年度出版的"mccutcheon'sdetergentandemulsifiers"北美版中。ctfa化妆品成分手册(ctfacosmeticingredienthandbook)第二版(1992)描述了皮肤护理工业中常用的各种非限制性化妆品成分,它们适用于本发明的组合物。这些成分类的例子包括:研磨剂,吸收剂,美学组分如香料、颜料、染色剂/着色剂、精油、皮肤感觉剂、收敛剂等(例如丁香油、薄荷醇、樟脑、桉叶油、丁子香酚、乳酸薄荷酯、金缕梅馏分),抗痤疮剂,抗结块剂,消泡剂,抗菌剂(例如丁基氨基甲酸碘丙酯),抗氧化剂,粘合剂,生物添加剂,缓冲剂,膨松剂,螯合剂,化学添加剂,着色剂,化妆品收敛剂,化妆品杀菌剂,变性剂,药物收敛剂,外用镇痛药,成膜剂或用于辅助组合物的成膜性和亲和力的材料如聚合物(例如二十碳烯和乙烯基吡咯烷酮的共聚物),遮光剂,ph调节剂,推进剂,还原剂,多价螯合剂,皮肤调理剂(例如湿润剂,包括杂项和闭塞),皮肤舒缓和/或愈合剂(例如泛醇和衍生物(例如乙基泛醇)、芦荟、泛酸及其衍生物、尿囊素、红没药醇和甘草酸二钾),皮肤处理剂,增稠剂和维生素及它们的衍生物。可以通过所述配方的实施方式治疗或预防的其它皮肤病学疾病例如是但不限于毛囊炎和油性皮肤病症。术语“约”是指±10%。术语“%w/w”是指特定成分的重量占整个配方重量的百分比。本文所用的表述“皮肤病学可接受的载体”是指与皮肤、头皮、毛发,指甲等相容的载体。术语“预防”是指防止在受试者中发生疾病、病症或病情。在某些情况下,受试者可能有发展疾病的风险,但尚未被诊断为患有该疾病。在一些情况下,术语“预防”是指防止疾病的下一个循环发生。本文使用的术语“益生元”是指选择性地增加皮肤菌群的有益微生物(例如表皮葡萄球菌)的生长和存活的物质,被归类为“益生元”。尽管已知各种类型的益生元,但是仍然需要可以以协同方式起作用的更具活性的替代物或添加剂。本文使用的植物提取物可以通过使用极性溶剂诸如乙醇(乙醇)、丁醇(丁醇)、甲醇、水或丙醇、丙二醇、丁二醇、甘油纯化(即极性提取物)。本发明的极性提取物可包含任何百分比的极性溶剂。或者,所述植物提取物可以通过使用非极性溶剂(即非极性提取物)诸如但不限于异辛烷纯化。本发明的非极性提取物可包含任何百分比的非极性溶剂。通常,疏水性分子倾向于是非极性的,因此使用非极性溶剂。亲水性分子倾向于是极性的并且被水和/或其它极性物质溶解。可以通过色谱法等将活性成分浓缩在提取物中。通常,本发明的植物提取物是含水提取物。为了获得纯化的植物提取物(例如植物提取物中有机盐和/或重金属和/或淀粉含量降低),通常通过色谱法进一步纯化含水植物提取物。可以将甘油或丙二醇加入到水提取物中以提高提取物的溶解度、提高进入皮肤的穿透能力并且进一步保存提取物。提取物可还含有防腐剂体系。因此,根据另一实施方式,提供了一种制备包含浓缩草药提取物的组合物的方法,该组合物用于治疗和/或预防痤疮,该方法包括:(a)使植物处于x1-10体积的水中以产生该植物的提取物;和(b)使用大孔树脂减少植物提取物中有机盐和/或重金属和/或淀粉的量,这导致植物提取物中存在的活性成分含量升高。根据一些实施方式,所述配方包含任何附加成分,包括溶剂、润肤剂、保湿剂、调理剂、增粘剂(viscositybuilder)、皮肤镇静剂、乳化剂、ph调节剂、防腐剂、抗氧化剂、增粘剂(viscosityincreasingagent)、香料、湿润剂、抗痤疮剂、稳定剂和洗涤剂。本发明的一些实施方式涉及马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根提取物与黄檗树皮和地榆根提取物的混合物之间抑制il-8的协同生物活性。本发明的一些实施方式涉及马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根提取物和黄檗树皮提取物之间抑制il-1α的协同生物活性。本发明的一些实施方式涉及马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根和黄檗树皮提取物之间显示的协同效应。因此,根据一些实施方式,所述组合物包含马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根、黄檗树皮和地榆根提取物。根据一些实施方式,所述组合物包含马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根和黄檗树皮提取物。一些实施方式涉及抗痤疮丙酸杆菌有效的抗微生物组合物,其中该组合物包含马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根提取物、黄檗树皮提取物和地榆根提取物或它们的任何组合中的任一种。一些实施方式涉及益生元和/或抗生素组合物,其包含本文公开的草药提取物例如掌叶大黄根、马齿苋、野菊花、黄芩根、黄檗树皮和/或地榆根提取物的任意组合。本发明的一些实施方式涉及黄檗树皮提取物和野菊花提取物之间显示的协同/互补效应。根据一些实施方式,所述局部配方包含总计约5.5%的野菊花、马齿苋、掌叶大黄根和黄芩根的提取物。根据一些实施方式,所述局部配方包含总计约5.5%的野菊花、马齿苋、掌叶大黄根和黄芩根的提取物以及约3%w/w的地榆根提取物和约3%w/w的黄檗树皮提取物。根据一些实施方式,所述局部配方包含约1.5%w/w的野菊花提取物、约1.5%w/w的马齿苋提取物、约1.5%w/w的掌叶大黄根提取物和约1.0%w/w的黄芩根提取物,可能还有约3%w/w的地榆根提取物和约3%w/w的黄檗树皮提取物。实施例实施例1评价草药提取物在角质形成细胞中和在天然及人工人皮肤模型中的协同抗炎作用痤疮病变的特征为高含量的促炎细胞因子诸如肿瘤坏死因子α(tnf-α)、白细胞介素-8(il-8)和白细胞介素-1(il-1)。它们的活性增加先于炎症性痤疮中滤泡的角化过度。本文涉及的痤疮斑点治疗包括使用含有以下四种草药提取物的产品(kamedis):马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根提取物。上述混合物或四种提取物与另外两种草药提取物(即黄檗树皮提取物和/或地榆根提取物)之间的协同效应已经如下进行了检查,其结果如下所示。材料与实验程序细胞培养模型已通过用mtt(3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四唑溴化物)进行活体染色,预先确定了草药提取物对人角质形成细胞系hacat刺激的egf(表皮生长因子)和lps(脂多糖)的毒性水平。将70%汇合的hacat细胞暴露于egf/lps刺激下,并以无毒剂量测试物品24小时。将地塞米松用作阳性对照。通过商业elisa(酶联免疫吸附测定)试剂盒确定来自刺激细胞的tnf-α分泌。皮肤模型将人体天然皮肤的样品(来自接受整形手术的健康患者)或人工3d人体重构皮肤(epidermtmsystem;mattek)分别暴露于lps或佛波醇12-肉豆蔻酸酯13-乙酸酯(pma)的刺激。在软膏基质中应用草药提取物的组合,将其涂布在皮肤样品表面上并孵育48小时(人皮肤)或6小时(epidermtmsystem)。通过mtt测定法测量皮肤的活力。将地塞米松用作阳性对照。使用商业elisa试剂盒定量从刺激的细胞分泌的il-1α和il-8。结果计算(所有模型)细胞因子分泌值均计算为刺激比,即相对于未刺激对照的分泌值。根据等式1从刺激值计算“刺激的抑制”:等式1:结果人角质形成细胞模型图1显示了相对于刺激的未处理细胞(阴性对照),tnf-α释放的egf/lps刺激,其中阴性对照被定义为0%刺激的点。一种处理包括0.027%由稀释于生长培养基中的马齿苋、掌叶大黄根、野菊花和黄芩根提取物组成的4-草药混合物。第二处理包括0.027%的黄檗树皮和地榆根提取物。第三处理由全部六种草药提取物组成,浓度大约为前述浓度的一半。图1中重复之间的几何标准偏差为30%。如图1所示,使用所有六种草药提取物的混合物实现了抑制受刺激的角质形成细胞释放tnf-α。相比之下,通过仅由一些提取物组成的部分混合物实际上增加了tnf-α释放(负抑制)。因此,当组合六种提取物时,高度可取的协同效应是明显的。值得注意的是,所测试的模型与痤疮有关。天然人体皮肤模型图2显示了用lps刺激人体皮肤所获得的结果。特别地,图2显示了天然皮肤中il-8的分泌,其中高于85%的抑制被认为在α=0.05水平上具有统计学意义(tukeyhsd)。如图2所示,lps诱导il-8从皮肤到测定培养基中的分泌增加了2.2倍。在使用四-草药混合物(马齿苋、掌叶大黄根、野菊花、黄芩根的提取物)和含有6%黄檗树皮提取物或6%地榆根提取物的配方处理的lps-激活的样品中,没有观察到il-8分泌的抑制。然而,含有所有六种草药提取物的配方完全抑制了il-8分泌的刺激。因此,黄檗和地榆提取物之间的协同效应是明显的。值得注意的是,此处测试的模型与痤疮有关。人工人体皮肤(epidermtmsystem)模型在测量人工皮肤中il-1α和il-8分泌的实验中,在将两种细胞因子释放到测定培养基中,pma分别诱导了2.9倍和2.6倍的刺激。特别地,人工皮肤中il-8分泌的结果如图3所示,说明应用四种草药提取物的组合物[野菊花(1.5%)、马齿苋(1.5%)、掌叶大黄根(1.5%)和黄芩根(1%),在图3中称为“4-草药混合物”]当分别与提取物3%地榆根或3%黄檗树皮一起施用时提供了60%或53%的刺激抑制。此外,当所有六种提取物一起施用时,刺激的抑制增加至75%,这是统计学上显著的结果,表明了组合物的六种组分之间的协同作用。值得注意的是,测试模型与痤疮有关。人工皮肤模型中il-1α分泌的结果如图4所示,其中所获得的值相对于未刺激的对照显示。在该实验中,在a=0.05水平下,大于44%的抑制被认为是显著的(tukeyhsd)。如图4所示,只有五种草药提取物[野菊花(1.5%)、马齿苋(1.5%)、掌叶大黄根(1.5%)和黄芩根(1%)]与3%黄檗树皮的一种组合提供了显著抑制。四种草药提取物的混合物[野菊花(1.5%)、马齿苋(1.5%)、掌叶大黄根(1.5%)和黄芩根(1%)]没有显示出对il-1α分泌的任何抑制活性的迹象。施用黄檗树皮提取物也没有明显的效果。因此,使用上述五种草药提取物观察到的il-1α分泌的显著抑制似乎表明,前四种(或前四种的至少一部分)与黄檗树皮提取物之间存在协同作用。总结在四种草药提取物(马齿苋提取物、掌叶大黄根提取物、野菊花提取物、黄芩根提取物)与黄檗树皮和地榆根提取物的混合物之间(总共六种草药提取物)观察到了抑制il-8的协同生物活性,而对于抑制il-1α,上述四种草药提取物与黄檗(总共五种草药提取物)之间显示出了协同效应。实施例2草药提取物的益生元和抗生效果的评估背景人体皮肤是由人类细胞和多种微生物群落组成的活组织,所述微生物群落包括真菌、细菌和病毒。虽然这些微生物中的一些是有害的,但是许多其它微生物可能有益于它们的宿主,例如通过提供防止更有害生物入侵的保护。可以相信的是,破坏皮肤微生物群体中的平衡可能导致紊乱或感染。微生物参与涉及许多常见的皮肤病。皮肤细菌痤疮丙酸杆菌与常见的人类皮肤病寻常痤疮(囊性痤疮或“痤疮”)有关,并且发现头状葡萄球菌在痤疮的进展中起作用。另一方面,表皮葡萄球菌是一种常见的皮肤微生物,被认为是有益的。选择性地增加皮肤菌群的有益微生物(例如表皮葡萄球菌)的生长和存活的物质被归类为“益生元”。尽管已知各种类型的益生元,但是仍然需要可以以协同方式起作用的更具活性的替代物或添加剂。材料与实验程序琼脂扩散测定这是一种定性分析,旨在确定提取物抑制病原体生长的能力。将痤疮丙酸杆菌的培养物稀释在新鲜培养基中(1:1,000)并涂布在软琼脂平板上,并在每个平板上放置3个滤纸盘。将100μl每种提取物的等分试样施加到滤纸盘上。将平板温育5天。样品扩散到孔周围的琼脂中,并测定产生抑制区域的能力。记录区域的直径,包括孔的直径。微孔板稀释测定这是一种定量分析,旨在确定每种提取物针对生长培养基中每种病原体的抑制浓度。将每种植物提取物稀释(一系列1:2稀释)在适合的生长培养基中并且将100μl的等分试样分配在96孔板的10个孔中。将过夜生长的培养物以1:1000稀释在新鲜培养基中,并将100μl加入到每个孔中,使得提取物的最终浓度在25%和~0.05%之间。对照组是没有病原体(用于寻找污染物)的提取物或者没有植物提取物的新鲜生长培养基中的病原体(最大生长)。将平板温育5天并且确定未观察到生长的最小浓度。将该浓度定义为mic(最小抑制浓度)。细菌生长将表皮葡萄球菌或头状葡萄球菌接种在营养肉汤(nb)琼脂平板上。将过夜的细菌菌落悬浮至在600nm下光密度为0.1,然后在无菌盐水中以1:100稀释。在96孔板中制备两倍连续稀释的植物提取物。对照是1)具有nb培养基但没有细菌的孔,2)具有提取物但没有nb培养基的孔和3)具有nb培养基和提取物但没有细菌的孔。细菌生长之后是在37℃温育24小时期间每5分钟测量600nm吸光度。在所有实验中,进行了两到四个独立重复。结果草药提取物的抗痤疮丙酸杆菌效果使用琼脂扩散(图5)和微孔板稀释测定法测量草药提取物对抗痤疮丙酸杆菌的抗生活性。六种草药中的四种在两种测定中的至少一种中表现出不同水平的抗生活性。值得注意的是,如表1所示,这两种测定的结果并不完全相关;这是符合预期的,因为抗生素物质只有在具有足够高的扩散系数以使它们能够以足够的速率渗入琼脂时,才能在琼脂扩散测定中有效。表1.草药提取物对痤疮丙酸杆菌的抗生素效应草药提取物的益生元活性图6示出了草药提取物中的五种对表皮葡萄球菌具有显著的益生元活性,即由于草药提取物的施用而促进了表皮葡萄球菌的生长。图6中显示的相对生长速率是由18小时内600nm吸光度(δa600)的增加计算的,其相对于对照显示的增加进行归一化(平均对照δα600=0.35,一式三份组的合并stdev=0.05)。相同草药提取物剂量的益生元和抗生素效果图7总结了实验结果,其中将五种草药提取物以相同浓度添加到表皮葡萄球菌和头状葡萄球菌的培养物中。图7中所示的所有草药提取物剂量都减少了病原体头状葡萄球菌的生长并促进了表皮葡萄球菌的生长。因此,当用于皮肤治疗时,该五种草药提取物被提议为具有双重活性(益生元和抗生素),从而提供双重益处。图8进一步示出了提取物之一(即掌叶大黄)对两种细菌生长动态的对比效果,其中使用相同剂量的提取物(0.05%掌叶大黄根提取物)。如图8所示,0.05%掌叶大黄根提取物抑制头状葡萄球菌的生长(左图),同时促进表皮葡萄球菌的生长(右图)。某些草药提取物的益生元效果在某些情况下可能是互补的或甚至是协同的。图9中的直方图显示了由于23小时内细菌生长导致的600nm吸光度的增加,表明虽然黄檗和野菊的提取物都显示出对表皮葡萄球菌的益生元活性,但是组合使用两种提取物可以实现更优异的生长促进。总结本发明中描述的草药提取物对以下痤疮病原体具有突出的抗生素活性:痤疮丙酸杆菌和头状葡萄球菌。在五种提取物中观察到促进表皮葡萄球菌生长的益生元活性。这些发现总结在下表中。新发现:对于六种测试提取物中的五种,发现剂量在促进有益细菌的生长的同时抑制病原菌的生长。至少两种提取物显示出互补或协同的益生元活性。实施例3表2.用于治疗痤疮(凝胶)的配方实施例4植物性痤疮斑点治疗的随机对照研究目的:该研究评估了新提出的痤疮治疗的耐受性和疗效。产品是otc外用凝胶,包含2%水杨酸(sa),其中还富含已被证明具有抗炎特性的植物性成分。设计:该研究被设计为单点,随机,研究者-盲法,分面10天研究。设置:招入的受试者尽可能最大程度地在面部两侧的对称位置具有至少2个炎性丘疹性痤疮病变和2个非炎性开放或闭合性粉刺的受试者。随机选择每个受试者面部的一侧以接收研究治疗产品。参与者:25名受试者,15名女性和10名男性,年龄12至43岁,患有轻度至中度痤疮。测量:研究持续时间为10天,研究访问发生在基线(第0天)、第1天、第2天、第3天、第7天和第10天。在每个访问日,受试者接受皮肤科医生的调查员面部评价和病变评估。对于炎性病变,评估的参数是红斑、高度、硬结和整体印象。评估的非炎症参数是高度和整体印象。结果:观察到的治疗组和对照组之间的差异在第1天和第2天之间增加,并且达到平均15%至20%的参数之间的小变化,并且在剩余的访问中保持相似。所有炎症和非炎症测试参数均达到了统计学显著性(p<0.005)。结论:进行本研究以确定植物性痤疮治疗凝胶在减少炎症性痤疮病变红斑、高度和硬结方面的安全性、有效性和易用性。红斑和高度是炎症性病变中最有影响的参数,应用2天后注意到改善。方法招募25名受试者,15名女性和10名男性,年龄12至43岁,患有轻度至中度痤疮并且符合研究资格。该研究被设计为单点,研究者-盲法,分面10天研究(dermatologyconsultingservices,pllc,highpoint,northcarolina,usa)。该研究在机构审查委员会(concordiairb,beachhaven,nj,usa)下进行,在进行任何研究程序之前,从每位受试者获得签署的知情同意书和照片发布表。根据入选标准招入的受试者尽可能最大程度地在面部两侧的对称位置具有最少2个炎性丘疹性痤疮病变和2个非炎性开放或闭合性粉刺。受试者在研究开始前2周内未使用任何局部痤疮治疗,在研究开始前4周内未服用任何口服痤疮药物,并且在研究开始前2周内未使用任何局部痤疮药物。在该研究中,随机选择每位受试者面部的一侧以接受研究治疗产品-kamedis痤疮斑点治疗。在治疗前通过dove敏感性皮肤无香味皂条洗涤面部的治疗选择侧,并且通过kamedis斑点治疗进行治疗。要求受试者根据指示,在早晨、中午和晚上使用dove条洗涤面部后施用治疗产品,每日三次。与治疗侧相同,使用dove条洗涤非治疗面部侧或对照侧每日三次,但是不使用局部产品进行治疗。研究持续时间为10天,研究访问发生在基线(第0天)、第1天、第2天、第3天、第7天和第10天。在每个访问日,受试者接受皮肤科医生的调查员面部评价和病变评估。在第0天、第1天、第2天、第3天和第10天拍摄面部的数码照片。使用带有intelliflash系统的canfield3点式头部安装的尼康d-90相机拍摄90度、+45度和-45度的图像,并在所有时间点都具有一致的光圈值(f-stop)以实现再现性。调查员在每个访问日0、1、2、3、7和10分别评估面部两侧的每个炎症和非炎症病变的多个参数。对于炎症性病变,评估的参数是红斑、高度、硬结和整体印象。对于非炎症,评估的参数是高度和整体印象。每个参数,使用以下分级标度:0=无,1=最小,2=温和,3=中等,4=严重。在治疗之后,在第10天,受试者完成了发起人提供的营销调查问卷,并且还提供了他们对整个体验的评论。统计分析采用双因素方差分析(anova),以访问和治疗/对照为主要因素和它们之间的相互作用。显著的相互作用意味着治疗和对照之间的差异在访问间不相似。p值小于0.05的因素被认为统计学显著。对于每个参数,通过计算相对于每位患者在基线(第0天)的分数测量的增加分数百分比,将原始分数转换为改善百分比。结果在招入的25名受试者中,24名受试者完成了该研究。一位受试者由于与测试产品无关的个人原因未完成该研究。在试验过程中没有发生任何不良经历或事件。示出了受试者的人口统计学特征(见下表3)。在基线访视(第0天)中,在随机选择的治疗组和对照病变组之间的特征方面没有观察到显著的统计学差异。表3受试者人口统计学特征调查员在每次访问时评估受试者炎症选择病变的红斑(图10)、高度(图11)、硬结和整体印象(图12)以及非炎症性病变的高度和整体印象。一般而言,可以看出,kamedis痤疮斑点治疗表现出随时间推移相对于对照组的持续改善。治疗一天后观察到相对于对照组的改善,并在第二天(第2天)后继续扩大。kamedis痤疮斑点治疗在随后的访问直至第10天的期间保持了其优势。观察到的治疗组和对照组之间的差异在第1天和第2天之间增加,并且达到平均15%至20%的参数之间的小变化,并且在剩余的访问中保持相似。所有炎症和非炎症测试参数均达到了统计学显著性(p<0.005)。在炎症病变上测量的红斑改善在2天后在测试产品和对照之间达到约20%的差异,并且在第3天达到最大差异24%。在10个治疗日后,测试产品的红斑改善幅度达到50%,在测试产品和对照之间保持了相似的差异(图10)。在炎性病变上测量的高度改善在第一天仅达到18%的改善,这也是与对照相比的差异,因为对照值在第一天显示为0%。在第二天,差异超过20%并且直到第10天保持相似或增加。在第10天,测试产品的高度改善幅度达到63%(图11)。与前两个参数相比,炎性病变的硬结改善显示出较小的差异。在第2天,测试产品和对照之间的差异达到10%并且在第3天增加至20%,在研究的其余时段保持相似。到第10天,测试产品的硬结改善程度达到52%。到第10天,测试产品的炎性病变的总体印象达到66%,从第2天和第3天开始保持比对照改善20%(图12)。与炎性病变相比,在非炎性病变上测试的测试产品的高度改善到第10天显示出较小的改善(31%)。测试产品与对照之间的差异也较小,从第2天的5%开始并且在第7天和第10天增加到13%。非炎性病变的总体改善与高度结果非常相似,从第2天测试产品和对照之间的7%差异开始,在第10天达到13%的差异,到第10天测试产品的最终改善为31%。除了测量参数之外,早在第2天或第5天应用治疗产品时,视觉上就有明显改善(图13a和13b)。讨论本研究评估了一种新的基于植物的痤疮治疗,其具有抗炎活性。发现该产品在改善痤疮症状方面是有效的且耐受良好。对照侧包括用肥皂进行的一般洗涤,但不包括对炎性和非炎性痤疮病变的局部治疗。选择合适的对照是痤疮研究中的挑战,因为在没有干预的情况下会发生愈合。在炎症性病变中,痤疮研究植物产品随着时间的推移提供了更好的结果,通常在两天后,但高度在治疗一天后即具有明显的显著改善。在非炎症性病变中,痤疮研究植物产品相对于对照也是有益的,尽管程度小于炎症性病变。痤疮研究调查了一种产品,该产品基于11.5%具有抗炎和抗菌活性的草药植物成分,诸如掌叶大黄、马齿苋、野菊、黄芩、黄檗和地榆。掌叶大黄和黄芩还显示出抗氧化活性以及减少皮脂分泌,这可能有助于改善和缓解痤疮病变的严重程度。选择所述植物药是因为它们的抗炎特性。基于整个文献综述,随后在角质形成细胞细胞系和皮肤模型上进行体外研究,从众多草药中选出了它们。体外试验通过抑制tnf-α释放研究了植物药的抗炎活性,并在上述草药的组合中产生了有前景的结果。与掌叶大黄的抗炎活性相关的化学活性分子包括大黄素和芦荟大黄素。两者均由掌叶大黄产生,作为酶11β-hsd1的抑制剂有效且具有选择性,所述酶11β-hsd1催化应激激素皮质醇转化为无活性代谢物可的松。此外,最近的科学证据支持大黄素在医学中的应用,以通过调节炎性小体激活来治疗各种炎症性疾病,其中大黄素显示出减弱nlrp3炎症小体的活化,导致裂解的il-1β分泌减少,并阻断炎性小体诱导的细胞凋亡。这项研究是一项初步研究,介绍了这种基于植物的原始产品,因此只包括少量样本。总结进行本研究以确定植物性痤疮治疗凝胶在减轻炎症性痤疮病变红斑、高度和硬结方面的安全性、有效性和易用性。红斑和高度是影响最大的炎症病变参数,在应用2天后注意到改善。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1